Tolérance aux biothérapies
Objectifs pédagogiques
- Connaître les mesures à prendre avant de débuter un traitement
- Connaître les réactions au traitement
- Connaître les complications infectieuses et la gestion du traitement en cas de survenue
- Connaître les complications cutanées, rhumatologiques, neurologiques
- Prescription des anti-TNF et risque tumoral
Introduction
Au cours de la dernière décennie, la prise en charge des patients atteints de maladie inflammatoire chronique de l’intestin (MICI), dont les deux entités principales sont la maladie de Crohn (MC) et la rectocolite hémorragique (RCH), a été bouleversée par l’avènement des biothérapies. En 2012, nous disposons dans notre pays de deux anticorps monoclonaux ciblant le Tumor Necrosis Factor alpha (TNF-a) : l’infliximab (IFX) et l’adalimumab (ADA). Bien que ces molécules soient récentes, leur prescription s’est rapidement étendue, notamment dans la MC. Ainsi, selon les données du registre aquitain des MICI recueillies en 2008-2009, 34 % des malades atteints de MC avaient déjà reçu au moins un anti-TNF et 10 % de ceux atteints de RCH [1]. à l’inverse, plusieurs facteurs paraissent limiter une prescription encore plus large des anti-TNF au cours des MICI : leur prix, la durée du traitement qui demeure inconnue, mais surtout les effets indésirables potentiels qui sont redoutés par les malades et parfois même par leur gastroentérologue. Les anti-TNF ont donc fait l’objet d’une surveillance étroite et nous disposons d’un recul de plus de 10 ans. Il faut enfin rappeler en préambule que la mortalité des MICI avoisine celle de la population générale. Nous verrons successivement dans cette revue les mesures à prendre avant de débuter un anti-TNF puis les différents effets indésirables potentiels de ces molécules.
Quelles mesures prendre avant de débuter un traitement anti-TNF ?
Outre les examens qui permettront de s’assurer la pertinence de l’indication du traitement par un anti-TNF, certaines mesures doivent être systématiques avant de débuter le traitement (pour la pratique, une checklist avant de débuter un traitement anti-TNF au cours d’une MICI est disponible sur les sites de la SNFGE – http://www.snfge.asso.fr/ – et du GETAID – http://www.getaid.org/) (Figure 1) :
Figure 1. Checklist avant de débuter un traitement anti-TNF au cours d’une MICI (disponible en intégralité sur les sites de la SNFGE et du GETAID)
Éliminer une infection aiguë non contrôlée (contre-indication absolue)
Il peut tout d’abord s’agir d’une suppuration intra-abdominale ou ano-périnéale en rapport avec la MC. Un examen clinique orienté et une imagerie de coupe permettront de lever cette hypothèque.
Ensuite, toute infection bactérienne évolutive doit être dépistée par un examen clinique complet, un hémogramme, un dosage de la CRP voire un ECBU, et traitée avant de débuter le traitement anti-TNF.
Éliminer une infection chronique à risque de réactivation grave (contre-indication absolue)
Une infection chronique latente peut être réactivée à la faveur d’un traitement anti-TNF. A l’extrême, il peut s’agir d’une infection mortelle comme cela a été décrit avec la tuberculose ou l’hépatite virale B [2,3].
Le dépistage de la tuberculose est indispensable avant d’instaurer un traitement anti-TNF. Il repose sur :
- un interrogatoire à la recherche d’un contage (antécédent de tuberculose active ou latente chez le patient et dans son entourage proche, séjour en zone d’endémie) ;
- un test antituberculeux spécifique : intradermoréaction (IDR) à la tuberculine (Tubertest 5 U®) considérée comme positive si l’induration est ≥ 5 mm, ou test sérique basé sur le relargage d’interféron-g par les lymphocytes T au contact d’antigènes mycobactériens (QuantiFERON TB Gold® ou T-SPOT TB®). Bien qu’il existe quelques discordances, la réalisation d’un seul de ces deux tests suffit généralement, excepté lorsque le test sérique est indéterminé (test ni positif ni négatif) où une IDR sera nécessaire. à ce jour, aucun des tests sériques n’est remboursé par la sécurité sociale (prix d’environ 85 e).
- une radiographie pulmonaire.
En cas de tuberculose active, l’anti-TNF ne pourra être débuté qu’à la guérison ou après un délai minimum de deux mois de traitement. En cas de tuberculose latente, un traitement antibiotique sera également nécessaire et l’anti-TNF pourra être administré trois semaines plus tard (recommandations AFSSAPS).
La réactivation virale de l’HBV est l’autre infection chronique à dépister systématiquement avant la mise sous anti-TNF [4]. Une sérologie B complète, incluant l’antigène HBs, les anticorps anti-Hbs et anti-HBc et l’ADN viral en cas de positivité de l’antigène HBs, est alors requise. Chez un malade non immunisé, la vaccination est recommandée. Quand l’antigène HBs est positif, un traitement préemptif par analogues nucléosidiques doit être débuté au moins deux semaines avant l’anti-TNF afin d’éviter une réactivation grave voire mortelle [5].
Éliminer une affection chronique à risque d’aggravation sous anti-TNF
Un traitement anti-TNF est susceptible de décompenser plusieurs affections chroniques qui doivent être préalablement recherchées :
- infection VIH,
- maladie démyélinisante,
- insuffisance cardiaque,
- cancer (une tumeur solide dans les cinq dernières années constitue une contre-indication aux anti-TNF, à l’exception des carcinomes baso-cellulaires et des cancers in situ du col utérin).
Quand il existe une indication majeure aux anti-TNF, il s’agit de situations qui doivent être discutées au cas par cas avec le spécialiste correspondant et surtout avec le malade.
Autres précautions
Les affections suivantes ne constituent pas une contre-indication aux anti-TNF, si bien que leur dépistage à l’occasion du bilan pré-thérapeutique est optionnel et recommandé dans certaines conditions [5] :
- hépatite virale C,
- infection à CMV (contre-indication temporaire en cas de localisation viscérale notamment colique),
- infection à EBV et à HSV,
- infection à VZV (sérologie conseillée en l’absence d’antécédent connu),
- infection à HPV (examen gynécologique avec frottis cervical),
- pneumocystose pulmonaire (chémo-prévention conseillée chez les malades recevant trois immunomodulateurs simultanément),
- tumeurs cutanées (examen dermatologique annuel conseillé).
Réaction au traitement
Deux facteurs ont un rôle prépondérant dans la survenue de réactions induites par les anticorps monoclonaux anti-TNFa :
- la voie d’administration, intraveineuse pour l’infliximab et sous-cutanée pour l’adalimumab,
- l’immunogénicité qui est liée en grande partie au degré d’humanisation de l’anticorps (l’infliximab est un anticorps chimérique humanisé à 75 % et l’adalimumab est humanisé à 100 %).
Il convient donc de distinguer les réactions induites selon l’anti-TNF administré.
Réactions à l’infliximab
Il existe deux types de réactions à l’infliximab selon leur délai de survenue par rapport à la perfusion : les réactions immédiates survenant pendant ou au décours de la perfusion et les réactions retardées qui arbitrairement apparaissent au moins 24-48 heures après.
Les réactions d’hypersensibilité immédiate surviennent habituellement dès les premières minutes de perfusion. Dans l’expérience incomparable de l’équipe belge de Louvain (n = 682), 17 % des malades ont développé une réaction d’hypersensibilité immédiate, en médiane après deux perfusions [6]. Les symptômes étaient généralement modérés (seuls deux malades ont être hospitalisés) et résolutifs sous corticoïdes et anti-anti-histaminiques, si bien que dans la plupart des cas la perfusion a pu être réalisée en en réduisant le débit. En définitive, l’infliximab n’a été abandonné que chez 16 % des 115 malades ayant eu une réaction à la perfusion. Les résultats de ce centre pionnier dans les biothérapies ont été confirmés en population. Ainsi, dans une cohorte nationale ayant repris tous les malades ayant reçu de l’infliximab au Danemark entre 1999 et 2005 pour une MICI, 17 % des malades (4,4 % des perfusions) ont développé une réaction d’hypersensibilité immédiate conduisant à l’interruption du traitement chez 16 % d’entre eux [7]. La prise concomitante d’un immunosuppresseur et l’administration régulière d’infliximab réduisent ce risque de réaction aiguë. à l’inverse, un traitement en épisodique et la reprise de l’infliximab après une pause de plus de 50 semaines sont à risque de réaction d’intolérance, ce d’autant que l’infliximab est réadministré par trois perfusions aux semaines 0-2-6 [8].
Les réactions d’hypersensibilité retardée surviennent dans un délai 1 à 14 jours après la perfusion. Les symptômes sont ceux d’une maladie sérique et associent de la fièvre, des arthralgies, des myalgies et parfois un rash. Dans la série de Louvain, elles ont été observées chez 7 % des malades, plus souvent chez des femmes et quand l’infliximab était perfusé à la demande [6]. à la différence des réactions aiguës, 92 % des malades ayant développé une réaction retardée ont dû interrompre l’infliximab, en raison d’une intolérance confirmée et/ou d’une perte de réponse.
Réaction à l’adalimumab
Des réactions locales au point d’injection sont observées chez 5 % des malades traités par adalimumab [9]. Il s’agit le plus souvent d’une douleur au site de l’injection, parfois d’une rougeur. Ces manifestations sont de courte durée et ne nécessitent pas l’interruption du traitement.
Les réactions allergiques systémiques à l’adalimumab semblent exceptionnelles et aucun cas grave n’a été signalé à ce jour.
Nature et prise en charge des infections survenant sous anti-TNF
Les MICI constituent en soi une situation d’immunodépression. En effet, selon le Center for Disease Control (CDC) d’Atlanta, les MICI correspondent à une immunodépression de catégorie 1 de la même manière que les hémopathies aiguës et chroniques ou les cancers [5]. Cette immunodépression est non seulement la conséquence des traitements, a fortiori quand plusieurs immunomodulateurs sont associés, mais est aussi liée à la maladie elle-même et au terrain du patient (comorbidités, âge).
Dans une revue Cochrane ayant récemment repris tous les essais menés avec les traitements biologiques, la fréquence des infections quelle que soit la biothérapie était identique à celle sous placebo [10]. Si les infections ne sont pas plus fréquentes avec les anti-TNF, elles peuvent être plus sévères. Selon la nature de l’agent infectieux on distingue les infections banales des infections opportunistes.
Une infection banale chez un malade immunodéprimé
Lorsque l’on évalue le risque infectieux sous anti-TNF, la métaanalyse compilant les 21 premiers essais randomisés et contrôlés dans les MICI n’identifie pas plus d’infection sous traitement que sous placebo (2,09 % et 2,13 %, respectivement) [11]. Mais, il faut rappeler que les malades recrutés dans ces études ont été à la fois très sélectionnés et très surveillés.
Les données observationnelles provenant de centres experts ou d’études en population sont moins rassurantes. Ainsi, selon l’expérience initiale des 500 premiers malades traités par infliximab à la Mayo Clinic, 41 d’entre eux ont développé une infection liée au traitement [12]. Dans 34 (83 %) cas, il s’agissait d’infections bactériennes non opportunistes : pneumopathie, septicémie, abcès intra-abdominal ou ano-périnéal, cellulite, infection urinaire… Il faut alors souligner toute la gravité de ces infections puisque quatre de ces malades sont morts. Parmi eux, une femme de 35 ans qui avait reçu de l’infliximab après avoir été drainée radiologiquement d’un abcès intra-abdominal a développé une suppuration intra-abdominale mortelle. De la même manière, parmi les 217 malades traités par infliximab dans la cohorte de Stockholm, 11 cas d’infections sévères ont été rapportés, dont 2 cas mortels [13]. Ces deux décès, consécutifs à une septicémie et à une bronchite sont survenus chez des malades de 67 et 75 ans.
Un âge supérieur à 65 ans est en effet un facteur de risque indépendant d’infection sévère et de décès sous anti-TNF comme l’a montré une étude cas-témoin italienne récemment publiée (Figure 2) [14].
Dans l’ensemble, les malades recevant un anti-TNF ne font pas plus d’infection que les autres, mais des infections qui sont plus graves, ce d’autant qu’ils sont âgés. En pratique et comme le recommande ECCO, une infection non contrôlée est une contre-indication absolue à l’administration d’un anti-TNF [15]. En corolaire, toute suspicion d’infection bactérienne chez un malade sous anti-TNF justifie un avis médical rapide et la suspension du traitement.
Figure 2. Risques d’infection sévère, de cancer et de décès sous anti-TNF en fonction de l’âge [14]
Infections opportunistes (IO)
Une IO est occasionnée par un micro-organisme qui n’a pas ou peu d’effet pathogène en situation normale, mais qui est responsable d’une infection grave à la faveur d’une autre affection ou de son traitement [16]. Comme toujours, l’âge élevé, la dénutrition, les comorbidités et la sévérité de la pathologie constituent des facteurs de risque indépendants et cumulatifs d’IO. Encore faut-il rappeler que les MICI les plus sévères et les plus graves sont de facto celles qui justifient les traitements les plus lourds.
Le risque d’IO n’est pas l’apanage des anti-TNF. Il existe quelque soit l’immunomodulateur – corticoïde, immunosuppresseur ou anti-TNF – avec un odds ratio entre 3,3 et 4,4 selon les molécules. Plus que la nature du traitement administré, ce sont les associations thérapeutiques qui démultiplient le risque d’IO. Ainsi, comme cela a été observé dans une étude cas-témoin de la Mayo Clinic, lorsque trois immunomodulateurs sont prescrits simultanément, le risque d’IO devient maximal avec un odds ratio qui tend vers l’infini [17].
La nature de ces IO est très variable. L’observatoire national français RATIO a colligé entre 2004 et 2007 tous les cas d’infections observées quelle que soit l’indication et le type d’anti-TNF, ce qui a permis de lister les micro-organismes responsables d’IO dans notre pays (Figure 3) [18]. La tuberculose représentait de très loin la première cause d’IO. Comme cela a été observé depuis le début des années 2000, il est probable que la systématisation du dépistage selon les modalités citées plus haut ait peu à peu réduit le nombre de cas déclarés de tuberculose. Parmi les autres IO recensées, il faut souligner la fréquence des infections virales par les virus du groupe herpes (HSV, VZV, EBV et CMV), qui sont heureusement plus souvent des réactivations que des primo-infections qui peuvent alors être très sévères. Enfin, plusieurs micro-organismes occasionnant des pneumopathies parfois graves ont été détectés chez des malades sous anti-TNF, au premier rang desquels figure Legionella pneumophila.
Figure 3. Détail des 134 cas d’infection opportuniste observés sous anti-TNF et déclarés dans l’observatoire français RATIO entre 2004 et 2007 [18]
BK : bacille de Koch ; VZV : varicella zoster virus ; CMV : cytomégalovirus ; MAC : Mycobacterium avium complex
Complications dermatologiques, articulaires et neurologiques des anti-TNF
L’administration d’un traitement anti-TNF est susceptible de générer des manifestations inflammatoires extra-digestives, que ce soient des atteintes dermatologiques, rhumatismales ou neurologiques. Leur description est récente et leur physiopathologie demeure mal connue.
Manifestations dermatologiques paradoxales
Selon l’expérience de Louvain, 20 % des malades développent des lésions dermatologiques sous anti-TNF. Celles-ci ont un retentissement significatif pour le patient et requièrent un avis spécialisé dans 42 % des cas [6]. Outre des infections cutanées opportunistes (candidose, réactivation HSV ou VZV, etc., …) et des vascularites, des éruptions psoriasiformes et/ou eczématiformes ont été observées. Ces dernières constituent une nouvelle entité nosologique et sont regroupées sous la terminologie de manifestations dermatologiques paradoxales dans la mesure où les anti-TNF ont démontré leur efficacité dans le traitement du psoriasis sévère ou réfractaire.
Une récente revue de la littérature sur le sujet a dénombré 127 cas de psoriasis induits ou réactivés sous anti-TNF entre 1990 et septembre 2007 [19]. La prévalence de ces dermatoses paradoxales, toutes affections et anti-TNF confondus était de 0,6-5,3 %. Elles ont été observées avec tous les anti-TNF (infliximab, etanercept, adalimumab et certolizumab pegol) et semblent être un effet secondaire de cette classe thérapeutique.
Plusieurs arguments sont en faveur de l’imputabilité des anti-TNF dans le déclenchement de ces dermatoses paradoxales :
- apparition de la dermatose après le début du traitement,
- existence d’un nombre élevé de cas publiés,
- guérison à l’arrêt du traitement,
- rechute de la dermatose lors de la reprise d’un autre anti-TNF.
La physiopathologie de ces manifestations paradoxales demeure non élucidée. Plusieurs pistes ont été évoquées et mettent en jeu un déséquilibre de la balance cytokinique au niveau cutané secondaire à l’activité accrue des cellules dendritiques plasmocytoïdes dermiques et à une production d’IL-17 [20].
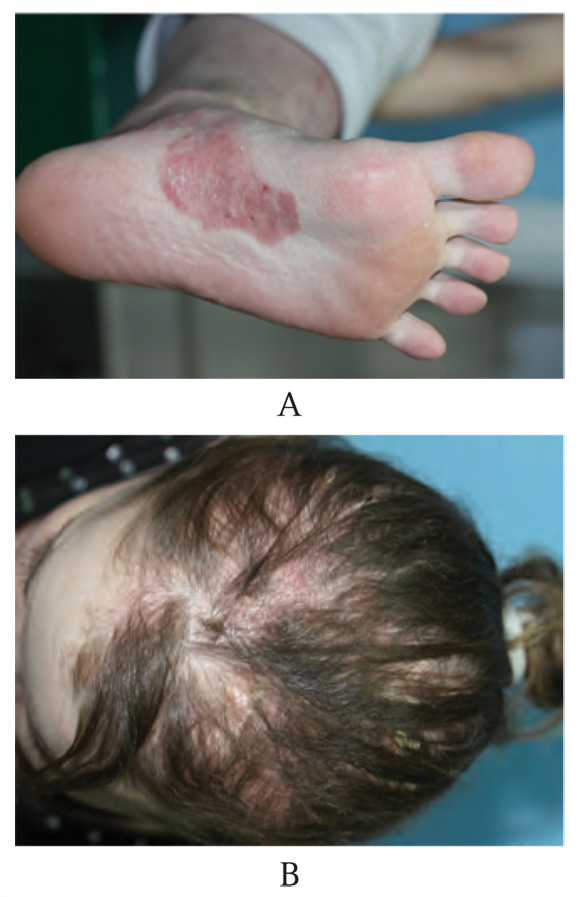
Le GETAID a colligé une série de 85 malades atteints de MICI (69 MC) ayant développé des dermatoses paradoxales sévères induites par les anti-TNF. Le diagnostic était à chaque fois certifié par un dermatologue [5]. Il s’agissait majoritairement de femmes (73 %) et un antécédent personnel ou familial de dermatose inflammatoire était présent dans 46 % des cas. Deux types de manifestations dermatologiques paradoxales étaient identifiés. Les éruptions psoriasiformes qui étaient les plus fréquentes avaient des caractéristiques sémiologiques particulières puisqu’elles étaient localisées au scalp, aux régions palmo-plantaires et aux plis (Figure 4). Les lésions eczématiformes, plus rares, n’avaient pas de localisation particulière.
La prise en charge de ces manifestations est difficile et reste assez empirique quand les lésions sont étendues et les traitements locaux inefficaces. Dans les formes les plus sévères, un arrêt du traitement anti-TNF est parfois nécessaire et doit alors être décidé en concertation avec le dermatologue et le malade.
Figure 4. Manifestations dermatologiques induites par les anti-TNF : lésions érythémato-squameuses plantaires (A) ; lésions érythémato-squameuses alopéciantes du cuir chevelu (B)
Manifestations articulaires paradoxales
à l’image des lésions dermatologiques induites, des cas de rhumatismes paradoxaux ont été récemment décrits sous anti-TNF. à l’inverse des rhumatismes inflammatoires associés aux MICI qui répondent favorablement aux anti-TNF, il s’agit ici de manifestations qui apparaissent sous traitement.
Dans la série de Louvain (1 300 patients traités par infliximab et adalimumab pour une MICI), 21 (1,6 %) patients (17 avec une MC et 4 une RCH) ont développé une symptomatologie rhumatismale, généralement à type de polyarthralgies périphériques. Il existait une légère prépondérance féminine (62 %) [21]. Des anticorps antinoyau élevés, au-delà de 1/640e, étaient détectés chez 15 de ces malades et 17 avaient des anticorps anti-DNA. Lors de l’apparition des symptômes articulaires, l’infliximabémie résiduelle était quantifiable, avec une médiane de 6,32 µg/mL et il n’y avait pas de corrélation avec la présence d’anticorps anti-infliximab. Plusieurs études ont déjà montré par le passé que les malades traités par anti-TNF développaient des auto-anticorps, en particulier des anticorps antinoyau et des anti-DNA, faisant craindre la survenue de manifestations lupiques induites [22,23]. Toutefois, cette série est la première à décrire ces manifestations articulaires paradoxales à l’instar des effets dermatologiques observés. La prise en charge thérapeutique de ces rhumatismes induits n’est pas codifiée à ce jour.
Manifestations neurologiques
Plusieurs cas d’aggravation ou d’apparition de maladies démyélinisantes, au premier rang desquelles la sclérose en plaques, ont été signalés chez des malades recevant des anti-TNF [24]. Lorsque de telles manifestations surviennent sous anti-TNF, le traitement est habituellement interrompu par principe de précaution.
Anti-TNF et cancer
La mortalité des MICI étant voisine de celle de la population générale, le risque d’induire une affection maligne par les anti-TNF constitue une crainte majeure. De nombreux travaux se sont penchés sur cette question essayant d’y répondre soit par des études de cohorte et soit par des études cas-témoin.
Essais contrôlés randomisés
Selon la métaanalyse de Peyrin-Biroulet et coll. qui a repris les données de 21 essais conduits avec les anti-TNF ayant recruté un total de 5 356 malades atteints de MICI, il n’était pas identifié plus d’affections malignes sous traitement que sous placebo [11].
Les métaanalyses des essais cliniques menés chez des malades traités pour polyarthrite rhumatoïde ou psoriasis arrivaient aux mêmes conclusions.
Études de cohorte
Les données provenant des études cohortes sont également rassurantes. Ainsi, dans les deux plus grandes séries disponibles déjà mentionnées précédemment, peu de cas de cancers ont été observés : 23 à Louvain et 4 au Danemark [6,7]. Bien qu’il s’agisse d’études de cohorte, les auteurs de ces études ont tenté de préciser le risque de développer de cancer sous anti-TNF. Tenant compte de réserves méthodologiques quant à la comparaison avec un groupe témoin non apparié et recruté sur des critères différents, il ne semblait pas exister un risque accru de cancer chez les malades traités par anti-TNF.
Parmi les cancers observés, il existait toutefois une proportion importante de cancers cutanés non mélanocytaires. Les carcinomes baso- et spino-cellulaires constituaient ainsi plus du tiers des cancers dans la série belge.
Études cas-témoin
Les études cas-témoin sont le meilleur moyen de caractériser le risque néoplasique sous anti-TNF. Cependant, il faut souligner que de telles études doivent avoir une taille suffisante et une durée d’observation longue pour détecter un risque faible à modéré. Ainsi, il a fallu recruter près de 20 000 patients atteints de MICI suivis pendant presque trois ans dans l’étude CESAME pour identifier un risque global accru de lymphome sous thiopurines et surtout pour caractériser le sous-groupe de malades ayant le risque le plus élevé [25].
à la demande des agences américaine et européenne, les laboratoires commercialisant les anti-TNF ont dû conduire de grandes études observationnelles de phase IV. à ce jour, une seule a été publiée dans une revue à comité de lecture [26]. Il s’agit de la cohorte TREAT qui a recruté entre 1999 et 2004 en Amérique du Nord 6 290 patients, dont 3 179 traités par infliximab. Les taux de cancer et de lymphome n’étaient pas différents entre les malades traités et les témoins (Tableau 1).
Des études indépendantes ont également tenté de préciser quel était le risque de cancer sous anti-TNF. Une étude multicentrique cas-témoin italienne a recruté entre 1999 et 2004 plus de 400 malades ayant une MC traitée par infliximab appariés à un groupe témoin sur le sexe, l’âge, la durée et la localisation anatomique de la maladie et la prise associée d’immunosuppresseurs [27]. Avec un recul médian de 6 ans, les taux de cancers observés étaient voisins : 3,9 % dans le groupe traité et 4,2 % chez les témoins (P = 0,95) (Figure 5). De plus, aucun type de cancer n’était plus fréquemment observé dans le groupe traité par l’infliximab. Pour mémoire, étant donné la faible proportion de malades sous infliximab dans la cohorte nationale CESAME, il n’était pas possible de déterminer s’il existait un risque de cancer lié aux anti-TNF dans cette étude française.
à ce jour, avec un recul de près de 10 ans, il ne semble donc pas exister de surcroît de cancers chez les malades traités par les anti-TNF. Cependant, comme cela a été observé avec les immunosuppresseurs dans CESAME, on ne peut exclure l’existence d’un sous-groupe de malades à risque plus élevé ou la survenue de cancers spécifiquement associés aux anti-TNF (cf. cancers cutanés non mélanocytaires sous immunosuppresseurs) [11].
| Avec Infliximab | Sans Infliximab | Risque relatif (IC95) | |
|---|---|---|---|
| Nombre de patients/années | 3 272 | 3 001 | |
| Mortalité pour 100 patients/années | 0,472 | 0,472 | 1,00 (0,64-0,56) |
| Cancers | 0,582 | 0,532 | 1,10 (0,71-1,63) |
| Lymphomes | 0,062 | 0,052 | 1,30 (0,36-5,03) |
Tableau 1. Risque de cancer et de lymphome sous infliximab au cours de la maladie de Crohn : registre TREAT [26]
Figure 5. Courbe de survie sans cancer selon une étude cas-témoin évaluant le risque de cancer sous anti-TNF [27]
Conclusion
Les anti-TNF sont devenus un traitement essentiel des MICI, à la fois dans l’obtention de la rémission sans corticoïde que dans son maintien. Leur prescription justifie un bilan préalable rigoureux et idéalement une prescription concertée, à l’instar des chimiothérapies anti-cancéreuses, dans la mesure où l’on engage des patients souvent jeunes sur des traitements au long cours. Globalement, le taux d’effet indésirable sous anti-TNF semble proche de celui des corticoïdes et des immunosuppresseurs. Selon l’expérience danoise, 47 % des malades traités par infliximab ont développé au moins un effet indésirable qui était considéré comme sévère dans 15 % des cas [7]. Il peut alors s’agir d’infections graves ou de manifestations paradoxales qu’il faut savoir reconnaître bien qu’elles dépassent le domaine de la gastroentérologie.
Références
- Laharie D, Leveque AM, Barberis C, Capdepont M, Beyssac R, Zerbib F. Impact of medical treatments on the clinical course of inflammatory bowel diseases (IBD): data from a French regional survey. Gastroenterology 2010;138:S1203.
- Keane J, Gershon S, Wise RP, Mirabile-Levens E, Kasznica J, Schwieterman WD, Siegel JN, Braun MM. Tuberculosis associated with infliximab, a tumor necrosis factor alpha-neutralizing agent. N Engl J Med. 2001;345:1098-104.
- Esteve M, Saro C, Gonzalez-Huix F, Suarez F, Forne M, Viver JM. Chronic hepatitis B reactivation following infliximab therapy in Crohn’s disease patients: need for primary prophylaxis. Gut 2004;53:1363-5.
- Mindikoglu AL, Regev A, Schiff ER. Hepatitis B virus reactivation after cytotoxic chemotherapy: the disease and its prevention. Clin Gastroenterol Hepatol 2006;4:1076-81.
- Rahier JF, Ben-Horin S, Chowers Y, Conlon C, De Munter P, D’Haens G, Domenech E, Eliakim R, Eser A, Frater J, Gassul M, Giladi M, Kaser A, Lemann M, Moreels T, Moschen A, Pollok R, Reinisch W, Schunter M, Stange EF, Tilg H, Van Assche G, Viget N, Vucelic B, Walsh A, Weiss G, Yazdanpanah Y, Zabana Y, Travis S, Colombel JF. European evidence-based Consensus on the prevention, diagnosis and management of opportunistic infections in inflammatory bowel disease J Crohn Colitis 2009;3:47-91.
- Fidder HH, Schnitzler F, Ferrante M, Noman M, Katsanos K, Segaert S, Van Assche G, Vermeire S, Rutgeerts P. Long-Term Safety of Infliximab for the treatment of Inflammatory Bowel Disease: A Single Center Cohort Study. Gut 2008.
- Caspersen S, Elkjaer M, Riis L, Pedersen N, Mortensen C, Jess T, Sarto P, Hansen TS, Wewer V, Bendtsen F, Moesgaard F, Munkholm P. Infliximab for inflammatory bowel disease in Denmark 1999-2005: clinical outcome and follow-up evaluation of malignancy and mortality. Clin Gastroenterol Hepatol 2008;6:1212-7; quiz 1176.
- Laharie D, Chanteloup E, Chabrun E, Subtil C, Kowo M, El Hanafi K, V DEL. The tolerance and efficacy of a postponed retreatment with infliximab in Crohn’s disease primary responders. Aliment Pharmacol Ther 2009;29:1240-8.
- Baumgart DC, Grittner U, Steingraber A, Azzaro M, Philipp S. Frequency, phenotype, outcome, and therapeutic impact of skin reactions following initiation of adalimumab therapy: Experience from a consecutive cohort of inflammatory bowel disease patients. Inflamm Bowel Dis 2011.
- Singh JA, Wells GA, Christensen R, Tanjong Ghogomu E, Maxwell L, Macdonald JK, Filippini G, Skoetz N, Francis D, Lopes LC, Guyatt GH, Schmitt J, La Mantia L, Weberschock T, Roos JF, Siebert H, Hershan S, Lunn MP, Tugwell P, Buchbinder R. Adverse effects of biologics: a network meta-analysis and Cochrane overview. Cochrane Database Syst Rev 2011:CD008794.
- Peyrin-Biroulet L, Deltenre P, de Suray N, Branche J, Sandborn WJ, Colombel JF. Efficacy and safety of tumor necrosis factor antagonists in Crohn’s disease: meta-analysis of placebo-controlled trials. Clin Gastroenterol Hepatol 2008;6:644-53.
- Colombel JF, Loftus EV, Jr., Tremaine WJ, Egan LJ, Harmsen WS, Schleck CD, Zinsmeister AR, Sandborn WJ. The safety profile of infliximab in patients with Crohn’s disease: the Mayo clinic experience in 500 patients. Gastroenterology. 2004;126:19-31.
- Ljung T, Karlen P, Schmidt D, Hellstrom PM, Lapidus A, Janczewska I, Sjoqvist U, Lofberg R. Infliximab in inflammatory bowel disease: clinical outcome in a population based cohort from Stockholm County. Gut 2004;53:849-53.
- Cottone M, Kohn A, Daperno M, Armuzzi A, Guidi L, D’Inca R, Bossa F, Angelucci E, Biancone L, Gionchetti P, Ardizzone S, Papi C, Fries W, Danese S, Riegler G, Cappello M, Castiglione F, Annese V, Orlando A. Advanced age is an independent risk factor for severe infections and mortality in patients given anti-tumor necrosis factor therapy for inflammatory bowel disease. Clin Gastroenterol Hepatol 2011;9:30-5.
- Dignass A, Van Assche G, Lindsay JO, Lemann M, Soderholm J, Colombel JF, Danese S, D’Hoore A, Gassul M, Gomollon F, Hommes D, Michetti P, O’Morain C, Oresland T, Windsor AC, Stange EF, Travis S. The second European evidence-based consensus on the diagnosis and management of Crohn’s disease: current management. J Crohn Colitis 2010;4:28-62.
- Symmers WS. Opportunistic Infections. The Concept of “Opportunistic Infections”. Proc R Soc Med 1965;58:341–6.
- Toruner M, Loftus EV, Jr., Harmsen WS, Zinsmeister AR, Orenstein R, Sandborn WJ, Colombel JF, Egan LJ. Risk factors for opportunistic infections in patients with inflammatory bowel disease. Gastroenterology 2008;134:929-36.
- Salmon-Ceron D, Tubach F, Lortholary O, Chosidow O, Bretagne S, Nicolas N, Cuillerier E, Fautrel B, Michelet C, Morel J, Puechal X, Wendling D, Lemann M, Ravaud P, Mariette X. Drug-specific risk of non-tuberculosis opportunistic infections in patients receiving anti-TNF therapy reported to the 3-year prospective French RATIO registry. Ann Rheum Dis 2011;70:616-23.
- Ko JM, Gottlieb AB, Kerbleski JF. Induction and exacerbation of psoriasis with TNF-blockade therapy: a review and analysis of 127 cases. J Dermatolog Treat 2009;20:100-8.
- Seneschal J, Milpied B, Vergier B, Lepreux S, Schaeverbeke T, Taieb A. Cytokine imbalance with increased production of interferon-alpha in psoriasiform eruptions associated with antitumour necrosis factor-alpha treatments. Br J Dermatol 2009;161:1081-8.
- Van Moerkercke W, Ackaert C, Kasran A, Ballet V, Gils A, Van Assche G, Rutgeerts P, Lories R, De Vlam K, Vermeire S. Severe auto-immune driven arthralgia as a new side effect in anti-TNF treated IBD patients? J Crohn Colitis 2010;4:S11.
- Vermeire S, Noman M, Van Assche G, Baert F, Van Steen K, Esters N, Joossens S, Bossuyt X, Rutgeerts P. Autoimmunity associated with anti-tumor necrosis factor alpha treatment in Crohn’s disease: a prospective cohort study. Gastroenterology 2003;125:32-9.
- Beigel F, Schnitzler F, Paul Laubender R, Pfennig S, Weidinger M, Goke B, Seiderer J, Ochsenkuhn T, Brand S. Formation of antinuclear and double-strand DNA antibodies and frequency of lupus-like syndrome in anti-TNF-alpha antibody-treated patients with inflammatory bowel disease. Inflamm Bowel Dis 2011;17:91-8.
- Felekis T, Katsanos K, Christodoulou D, Asproudis I, Tsianos EV. Reversible bilateral optic neuritis after Infliximab discontinuation in a patient with Crohn’s disease. J Crohns Colitis 2009;3:212-4.
- Beaugerie L, Brousse N, Bouvier AM, Colombel JF, Lemann M, Cosnes J, Hebuterne X, Cortot A, Bouhnik Y, Gendre JP, Simon T, Maynadie M, Hermine O, Faivre J, Carrat F. Lymphoproliferative disorders in patients receiving thiopurines for inflammatory bowel disease: a prospective observational cohort study. Lancet 2009;374:1617-25.
- Lichtenstein GR, Feagan BG, Cohen RD, Salzberg BA, Diamond RH, Chen DM, Pritchard ML, Sandborn WJ. Serious infections and mortality in association with therapies for Crohn’s disease: TREAT registry. Clin Gastroenterol Hepatol 2006;4:621-30.
- Biancone L, Petruzziello C, Orlando A, Kohn A, Ardizzone S, Daperno M, Angelucci E, Castiglione F, D’Inca R, Zorzi F, Papi C, Meucci G, Riegler G, Sica G, Rizzello F, Mocciaro F, Onali S, Calabrese E, Cottone M, Pallone F. Cancer in Crohn’s Disease patients treated with infliximab: a long-term multicenter matched pair study. Inflamm Bowel Dis 2011;17:758-66.
Les 5 points forts
- Un bilan systématique infectieux et cardio-vasculaire est indispensable avant de débuter un anti-TNF.
- Les anti-TNF n’augmentent pas la fréquence des infections chez les sujets de moins de 65 ans, mais leur sévérité.
- La mortalité et la sévérité des infections augmentent chez les sujets âgés (+ de 65 ans).
- Les manifestations paradoxales, qu’elles soient dermatologiques ou rhumatismales, constituent un effet indésirable nouvellement décrit avec les anti-TNF.
- Avec un recul de plus de 10 ans, les anti-TNF ne semblent pas augmenter le risque de cancer.
FMC HGE : Organisme certifié Qualiopi pour la catégorie ACTIONS DE FORMATION
FMC HGE : Organisme certifié Qualiopi pour la catégorie ACTIONS DE FORMATION