Encéphalopathie hépatique au cours de la cirrhose
Objectifs pédagogiques
- Connaître la symptomatologie de l’encéphalopathie hépatique et sa signification
- Connaître les moyens diagnostiques
- Savoir comment prévenir et traiter l’encéphalopathie hépatique
Introduction
L’encéphalopathie hépatique est un syndrome neuropsychiatrique complexe qui survient le plus souvent dans un contexte de dysfonction hépatique aiguë ou chronique. Les manifestations cliniques de l’encéphalopathie hépatique couvrent un large spectre : de troubles mineurs des fonctions supérieures jusqu’au coma. On distingue 2 entités : l’encéphalopathie hépatique minime (EHM) et l’encéphalopathie hépatique clinique (EHC). On admet que l’EHC est la continuité de l’EHM et que leur physiopathologie est commune. Les mécanismes physiopathologiques sont encore incomplètement élucidés. Deux phénomènes participent à la survenue de l’encéphalopathie associée à la cirrhose : l’insuffisance hépatocellulaire et la présence de shunts porto-systémiques. L’hyperammoniémie et l’inflammation jouent un rôle majeur. Ces 2 facteurs provoquent un œdème des cellules gliales, lui-même à l’origine de dysfonction neuronale prédominant au niveau des noyaux gris centraux et des cortex frontaux, pariétaux et occipitaux.
Définitions
La classification actuelle de l’encéphalopathie hépatique a été proposée au cours d’une conférence de consensus en 1998 [1]. Elle tient compte de l’étiologie et de la présentation clinique de l’encéphalopathie hépatique et distingue 3 types (Tableau I).
Tableau I : Classification de l’encéphalopathie hépatique selon Ferenci et al. [1]
| Type | Description | Catégorie | Sous-catégorie |
|---|---|---|---|
| A | Encéphalopathie hépatique associée à l’insuffisance hépatique aiguë sans cirrhose | – | – |
| B | Encéphalopathie hépatique associée à la présence de shunts porto-systémiques sans cirrhose | – | – |
| C | Encéphalopathie hépatique associée à la cirrhose | Épisodique |
Précipitée Spontanée Récurrente |
| Persistante |
Modérée Sévère Traitement– dépendante |
||
| Minimale | – |
L’encéphalopathie hépatique de type C associée à la cirrhose se divise en 3 catégories :
-
épisodique : on observe un retour à un état neurologique normal entre les épisodes. Elle peut être qualifiée d’encéphalopathie hépatique :
- précipitée : existence d’un facteur déclenchant (infections, hémorragie digestive, troubles hydro-électrolytiques, prise de médicaments, constipation…),
- spontanée : aucun facteur déclenchant n’est objectivé,
- récidivante : au moins 2 épisodes d’EHC en 1 an ;
- persistante: on n’observe pas de retour à un état neurologique normal ;
- minimale.
Présentation et signification
La prévalence de l’EHM et de l’EHC est respectivement de 20 à 60 % et de 30 à 45 % selon les séries de patients hospitalisés.
L’EHM se définit par la présence d’anomalies neuropsychologiques détectables par la réalisation de tests -psychométriques alors que l’examen clinique est normal. Les fonctions supérieures atteintes sont l’attention, les fonctions exécutives (capacité d’anticipation, d’organisation, d’inhibition, d’alternance de tâches, de détection d’erreurs) et les fonctions psychomotrices [2]. La mémoire et les capacités verbales sont peu altérées. M. Groeneweg et al. ont montré que l’EHM était responsable d’une altération de la qualité de vie indépendamment de la sévérité et de l’étiologie de la cirrhose [3]. Les capacités de communication étaient préservées chez les patients avec EHM tandis que le sommeil, le travail, la vie domestique, les loisirs, la vie sociale étaient particulièrement perturbés. Plusieurs travaux ont montré que les patients avec EHM avaient une baisse des facultés de conduite automobile avec une augmentation du risque d’accidents de la route et également montré une augmentation du risque de chutes et de traumatismes [4, 5]. Enfin, la présence d’une EHM est prédictive de la survenue d’une EHC [6].
Les signes cliniques de l’EHC habituellement recherchés en pratique sont une inversion du cycle nycthéméral, des troubles de la vigilance, allant d’une simple obnubilation avec désorientation temporo-spatiale jusqu’au coma. Des signes neurologiques objectifs peuvent s’y ajouter : l’astérixis, l’hypertonie extra-pyramidale, l’hyperréfléxie ostéotendineuse, des signes frontaux. Ces signes cliniques sont habituellement retrouvés lorsque le stade de l’encéphalopathie hépatique est supérieur ou égal à 2 selon la classification de la gravité de West-Haven. En 2010, une nouvelle classification (Tableau II), plus simple d’utilisation pour la pratique courante ou les essais cliniques, a été proposée [7]. Ainsi, l’existence d’un astérixis ou d’une désorientation temporo-spatiale définit l’EHC. L’existence de perturbations des tests psychométriques sans astérixis ni désorientation temporo-spatiale définit l’EHM.
Tableau II : Les différents stades d’encéphalopathie adaptés de Bajaj et al. [3]
| Normal | EH minimale | EH clinique | |
|---|---|---|---|
| Conscience | Non altérée | Non altérée | De la désorientation au coma |
| Tests psychométriques | Non altérés | Pertubés | Inutiles |
| Asterixis et autres signes neurologiques | Absents | Absents | Présents |
La survenue d’un épisode d’encéphalopathie hépatique clinique est un élément pronostique majeur à prendre en compte dans l’histoire naturelle de la cirrhose. En effet, les taux de mortalité à 1 et 5 ans étaient de 64 % et 85 % respectivement dans une série prospective scandinave et la complication la plus grave de la cirrhose [8].
Moyens diagnostiques
Encéphalopathie hépatique minime
Tests psychométriques
Une batterie de 5 tests psychométriques pour le diagnostic de l’EHM a été mise au point : le Psychométric Hepatic Encephalopathy Sum-Score (PHES) [9]. Ces 5 tests évaluent le ralentissement psychomoteur, le déficit attentionnel et l’atteinte des fonctions exécutives (Fig. 1). Les résultats sont dépendants de l’âge et du niveau d’éducation. Le résultat du PHES est exprimé en nombre de déviation-standard (DS) par rapport à une population appariée sur l’âge et le niveau d’éducation. Un seuil £ –4DS définit l’EHM selon les recommandations actuelles. Les normes espagnoles sont disponibles (redeh.org) en attendant la mise au point de normes françaises. Néanmoins, la réalisation de ces tests est consommatrice de temps (30 à 40 minutes) difficilement applicable en pratique de routine. Pour ces raisons, d’autres tests plus simples ont été évalués, pour exemples : le Critical Flicker Frequency (CFF) et l’Inhibitory Control Test (ICT).

Figure 1 : Les 5 tests psychométriques du PHES (Number Connection Test A et B, Line Tracing Test, Digit Symbol Test, Serial Dotting Test)
Tests automatisés
Le CFF ou fréquence critique de clignotement explore les capacités attentionnelles. Il est basé sur une stimulation visuelle par une diode lumineuse de fréquence décroissante à partir de 60 Hz. La fréquence à laquelle le patient perçoit le passage d’une lumière continue au clignotement (ou plutôt scintillement) correspond à la fréquence critique de clignotement. On considère que le CFF est perturbé dans l’encéphalopathie hépatique, en raison d’une rétinopathie hépatique liée à la présence d’un œdème intracellulaire des cellules gliales intra-rétiniennes. Selon les études, ce test apparaît comme un moyen simple, reproductible, non influencé par le niveau d’éducation et peu influencé par l’âge. Un seuil < 39 Hz serait corrélé aux résultats des tests psychométriques et associé au risque de développé une EHC [6, 10].
L’ICT est un test numérisé également simple et rapide. Ce test explore les capacités attentionnelles et la capacité d’inhibition (fonction exécutive). Son principe est le suivant : une séquence de lettres apparaît toutes les 500 ms. Le patient doit appuyer sur un curseur lorsque la séquence « XY » ou « YX » (cibles) apparaît. Cette tâche a pour but d’évaluer les capacités attentionnelles. Lorsque les séquences « XX » ou « YY » (leurres) apparaissent, on demande au patient de ne pas appuyer. Cette tâche évalue les capacités d’inhibition. Ce test a surtout été validé aux USA [11]. La même équipe a développé un test automatisé utilisable sur un smartphone [12].
Autres explorations
EEG
Différents types d’anomalies ont été décrites au cours de nombreuses études. Aucune anomalie n’est cependant spécifique de l’encéphalopathie hépatique. Une réduction du rythme alpha, entrecoupé d’ondes thêta, a pu être observée. Plus rarement, on retrouve des ondes thêta diffuses ou des ondes triphasiques.
Les potentiels évoqués
La mesure des potentiels évoqués est une méthode d’exploration de la transmission des messages nerveux après une stimulation donnée. Seule la mesure des potentiels évoqués endogènes présente un intérêt dans le diagnostic de l’EHM. Elle consiste à enregistrer les ondes générées au niveau du cortex frontal lors de la réalisation de tâches cognitives simples. On mesure l’amplitude de l’onde P300 qui reflète les capacités attentionnelles liées à une tâche. L’onde P300 est altérée dès lors qu’il existe des anomalies à l’EEG et aux tests psychométriques. Les potentiels évoqués endogènes et l’EEG avec analyse spectrale sont les meilleures explorations neurophysiologiques pour l’étude de l’EHM.
L’IRM encéphalique avec séquences de diffusion et la spectroscopie par résonnance magnétique sont deux techniques prometteuses. Toutefois le coût et le manque de disponibilité de ces techniques ne permettent pas de les utiliser en pratique clinique.
Actuellement, il est donc recommandé d’utiliser une batterie de tests psychométriques : PHES pour le diagnostic d’EHM [13]. Pour les raisons évoquées plus haut, cela est difficile à réaliser en pratique clinique chez tous les patients avec cirrhose. Quand les résultats des tests automatiques seront parfaitement validés, alors tous les patients devraient être explorés.
EHC
Bien que l’encéphalopathie hépatique soit une cause fréquente d’altération de la vigilance chez les patients cirrhotiques, d’autres causes peuvent être responsables d’une même symptomatologie. De plus, aucun symptôme n’est spécifique de l’encéphalopathie hépatique. Le diagnostic d’EHC reste un diagnostic d’exclusion. L’examen clinique s’appuie sur une évaluation neuro-psychiatrique approfondie. L’entretien avec le patient et sa famille doit faire rechercher toutes modifications apparues dans la vie quotidienne : perte d’énergie, perturbation du cycle veille-sommeil, troubles cognitifs, troubles de la conscience ou de la fonction motrice. L’examen clinique cherche à détecter des troubles de l’état de vigilance : niveau de conscience, attention, capacité à interagir avec le clinicien, vitesse d’expression. Les troubles neuro-musculaires sont aussi explorés. L’astérixis ou flapping tremor a une bonne valeur d’orientation pour le diagnostic. Il est conseillé lors du premier épisode d’EHC d’effectuer une imagerie cérébrale (tomodensitométrie ou IRM cérébrale) afin d’éliminer d’autres causes aux troubles neurologiques. Lorsque le patient est dans un état de coma aréactif, il est utile d’effectuer un EEG pour éliminer le rare état de mal épileptique non convulsivant. Néanmoins, le tracé est le plus souvent celui d’une souffrance diffuse comme pour toutes les « encéphalopathies métaboliques ». Une analyse quantitative spectrale permettrait d’améliorer la reproductibilité de la lecture simple.
Le dosage de l’ammoniémie (aspécifique et absence de valeur pronostique) a peu d’intérêt en pratique clinique, normale elle doit remettre en cause le diagnostic d’encéphalopathie hépatique.
Traitements
Les mesures thérapeutiques ont au moins 3 objectifs : traiter un éventuel facteur déclenchant, améliorer la qualité de vie et prévenir la récidive.
Le traitement de l’EHC passe par la recherche d’un facteur précipitant et sa prise en charge (Fig. 1 et Fig. 2). Les facteurs précipitants sont les infections, les médicaments (benzodiazépines, morphiniques, psychotropes en général), l’hémorragie digestive, la déshydratation et les troubles hydro-électrolytiques éventuellement favorisés par un traitement diurétique, la constipation, l’aggravation de l’hépatopathie chronique… Il est donc primordial d’effectuer une enquête étiologique complète. Une antibiothérapie probabiliste peut être proposée une fois les prélèvements effectués et lorsqu’aucune autre cause n’est retrouvée. Les médicaments psychotropes doivent être stoppés.

Figure 2 : Proposition d’algorithme pour la prise en charge de l’EHM
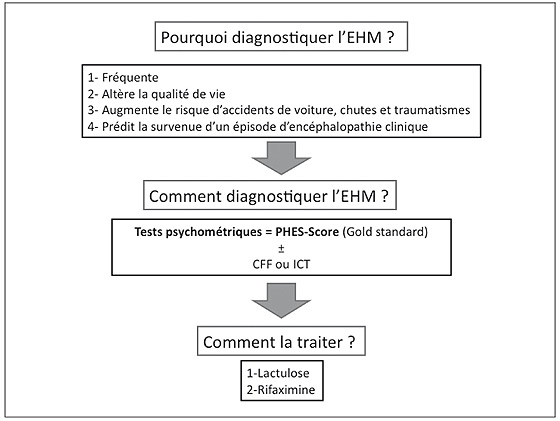
Figure 3 : Proposition d’algorithme pour la prise en charge de l’EHC
Un régime nutritionnel équilibré est recommandé sans restriction protidique, qui conduit à un risque de dénutrition, elle-même associée à un risque d’encéphalopathie.
La survenue d’une EHC est un facteur de mauvais pronostic à court terme. Il est important d’évaluer la faisabilité d’une transplantation hépatique. En cas d’encéphalopathie hépatique récidivante nécessitant des hospitalisations prolongées ou répétées, il existe une exception au score de MELD pour améliorer l’accessibilité à la transplantation de ces patients.
Disaccharides non absorbables : lactulose, lactitol
Le lactulose est un disaccharide synthétique introduit en 1966 et composé de deux monosaccharides : le fructose et le galactose. Il est métabolisé par les bactéries de la flore intestinale en acide acétique et acide lactique. Il en résulte une diminution du pH intraluminal qui inhibe la croissance des bactéries productrices d’ammoniac et favorise la conversion de l’ammoniac NH3 en ion ammonium NH4+ (qui diffuse moins facilement à travers la muqueuse intestinale). Enfin, par ses propriétés laxatives, le lactulose diminue l’absorption d’ammoniac. La posologie recommandée est de 30 à 60 mL par jour pour un objectif de 2 à 3 selles par jour. Le traitement par lactulose n’entraîne pas d’effets indésirables sévères. On observe néanmoins une mauvaise tolérance digestive chez environ un tiers des patients : douleurs abdominales, ballonnements, nausées et vomissements. Il constitue le traitement de première ligne de l’encéphalopathie hépatique depuis les années 1980. Cependant, très peu d’essais randomisés contrôlés ont été réalisés contre placebo.
Le lactitol (béta-galactosido-sorbitol) est apparu en 1982. Il était présenté comme une alternative avec une meilleure tolérance. En 2004, une revue systématique de la littérature a analysé 44 essais cliniques ; certains d’entre eux concluaient à l’efficacité du lactulose ou du lactitol dans le traitement de l’EHC, épisodique ou persistante. Le critère de jugement principal retenu était le nombre de patient ne présentant pas d’amélioration de l’encéphalopathie hépatique. Cette analyse concluait à l’absence d’arguments suffisants pour affirmer ou infirmer l’effet bénéfique de ces deux disaccharides dans le traitement curatif de l’encéphalopathie hépatique.
Depuis, d’autres études ont été conduites, principalement pour prévenir l’apparition ou la récidive de l’encéphalopathie hépatique. Pour exemples, BC Sharma et al. ont montré l’efficacité du lactulose en prophylaxie primaire et secondaire de l’EHC [15, 16]. Dans la première étude, 120 patients atteints d’une cirrhose sans antécédent d’EHC ont été inclus. Les patients étaient randomisés en ouvert soit dans le groupe placebo, soit dans le groupe lactulose et traités pendant 12 mois. Dans le groupe lactulose, 11 % des patients ont développé un épisode d’EHC au cours du suivi contre 19 % dans le groupe placebo (p = 0,02). Dans la seconde, 140 patients avec un antécédent d’EHC ont été inclus et randomisés en ouvert dans les groupes placebo ou lactulose. Dans le groupe lactulose, 19,6 % des patients ont développé un épisode d’EHC contre 46,8 % dans le groupe placebo (p = 0,001). L’absence de double aveugle fragilise les résultats de ces 2 études. Le lactulose reste néanmoins le traitement de première intention pour la prévention de la récidive.
Concernant l’EHM, une méta-analyse de 5 travaux portant sur le traitement de l’EHM par le lactulose conclut à un effet bénéfique de ce traitement [17].
Antibiotiques
La rifaximine (C43H51N3O11) est un antibiotique semi-synthétique, faiblement absorbé, appartenant à la famille des rifamycines. Il agit par fixation à la sous-unité bêta de l’ARN polymérase bactérienne, inhibant ainsi la synthèse d’ARN bactérien. In vitro, la rifaximine possède une activité antibactérienne de large spectre, à la fois vis-à-vis de bactéries gram positif, gram négatif, aéro- et anaérobies. Elle diminue la flore productrice d’ammoniac. Elle pourrait ainsi limiter la production intestinale d’ammoniac mais aussi diminuer la translocation bactérienne qui participe à l’inflammation au cours de l’encéphalopathie hépatique. Il a été suggéré que la décontamination intestinale par la rifaximine pouvait améliorer l’hémodynamique systémique chez les patients cirrhotiques. Après administration orale, l’activité spécifique de la rifaximine vis-à-vis de -l’intestin résulte d’une très faible absorption systémique. La tolérance de cette molécule est excellente. Dans les essais pour l’encéphalopathie hépatique, le taux de survenue d’effets indésirables n’était pas différent par -rapport au groupe placebo et la tolérance était meilleure que celle observée dans les groupes disaccharides [18]. Le risque de sélection de mutants résistants apparaît faible avec la rifaximine.
La rifaximine est actuellement approuvée dans 33 pays pour des indications variées dans le domaine de l’hépato-gastro-entérologie, dont 11 pays pour le traitement de l’encéphalopathie hépatique. En France, ce médicament n’est pas encore commercialisé, mais est disponible via une autorisation temporaire d’utilisation (ATU) nominative de la spécialité NORMIX®, comprimés dosés à 200 mg. La posologie majoritairement utilisée dans les essais cliniques est de 550 mg deux fois par jour. En France, du fait du dosage -disponible, la posologie quotidienne usuelle est de 1 000 mg à 1 200 mg répartis en 2 prises. Cette autorisation repose sur une étude de NM Bass et al. [19]. Il s’agit d’une étude prospective, de phase III, randomisée en double aveugle contre placebo. Les patients inclus (n = 299) étaient en rémission d’une EHC épisodique récurrente (survenue d’au moins 2 épisodes d’EHC spontanés de stade supérieur ou égal à 2 selon les critères de West-Haven dans les 6 mois précédant l’inclusion). À l’inclusion, les patients présentaient un score de MELD inférieur ou égal à 25 pour la majorité d’entre eux. La durée de traitement était de 6 mois. La majorité des patients ont poursuivi un traitement par lactulose durant l’étude (91 %). Il a été montré une diminution significative du risque de récidive de 58 % chez les patients traités par rifaximine (22,1 % contre 45,9 % dans le groupe placebo ; p < 0,001) ainsi qu’une diminution significative du risque d’hospitalisation pour encéphalopathie hépatique de 50 % (13,6 % contre 22,6 % dans le groupe placebo ; p = 0,01). Une partie des patients de cette étude (n = 219) a été inclue dans une seconde étude, dont le but était d’évaluer l’impact d’un traitement par rifaximine sur la qualité de vie. Une amélioration significative a été obtenue dans le groupe rifaximine en comparaison au groupe placebo [20].
J.S. Bajaj et al. ont évalué l’efficacité de la rifaximine dans le traitement de l’EHM [21]. Quarante-deux patients présentant une EHM ont été inclus, puis randomisés en double aveugle, dans le groupe placebo ou rifaximine 1 100 mg par jour. Le suivi était de 8 semaines. Des tests psychométriques, une épreuve de conduite en simulateur et une évaluation de la qualité de vie ont été réalisés à l’inclusion et après 8 semaines de traitement. Il existait une amélioration des erreurs de conduite chez 76 % des patients du groupe rifaximine contre 33 % des patients du groupe placebo. Les performances aux tests psychométriques étaient améliorées chez 91 % des patients traités par rifaximine contre 61 % des patients traités par placebo. On notait également une amélioration du SIP-score, échelle de qualité de vie, pour sa composante psycho-sociale, dans le groupe rifaximine. Des résultats comparables étaient retrouvés dans une seconde étude randomisée, contrôlée, en double aveugle [22]. Quatre-vingt-quatorze patients avec une EHM étaient randomisés dans un groupe placebo ou rifaximine 1 200 mg par jour. Les tests psychométriques et le SIP-score étaient réalisés à l’inclusion, après 2 semaines et 8 semaines de traitement. Le nombre de patients avec normalisation des tests psychométriques était significativement plus élevé dans le groupe rifaximine, à 2 semaines (57,1 % contre 17,8 % ; p < 0,0001) et à 8 semaines (75,5 % contre 20 % ; p < 0,0001) comparé à celui du groupe placebo. On retrouvait également une amélioration significative des résultats de l’échelle de qualité de vie dans le groupe rifaximine en comparaison au groupe placebo après 8 semaines de traitement (variation du SIP-score entre 0 et 8 semaines : 4,61 contre 0,88 ; p < 0,001).
La rifaximine est actuellement proposée en prévention secondaire aux patients en échec de traitement par le lactulose. Elle n’est actuellement pas encore disponible en France pour le traitement de l’EHM.
Enfin, une étude récente a suggéré que, pour le traitement curatif de l’encéphalopathie hépatique, l’association rifaxime + lactulose était supérieure au lactulose seul [23]. Ces résultats n’ont pas été observés dans notre travail qui a montré que la rifaximine permettait de diminuer le risque de récidive mais n’améliorait pas l’encéphalopathie persistante [24].
En cas d’encéphalopathie hépatique récidivante sans facteur déclenchant identifiable, réfractaires aux traitements habituels et de contre-indication à la transplantation hépatique, l’oblitération de gros shunts porto-systémiques peut être tentée [25].
Références
- Ferenci P, Lockwood A, Mullen K, Tarter R, Weissenborn K, Blei AT. Hepatic encephalopathy – -definition, nomenclature, diagnosis, and quantification: final report of the working party at the 11th World Congresses of Gastroenterology, Vienna, 1998. Hepatology 2002;35:716-21.
- Schomerus H, Hamster W. Neuro-psychological aspects of portal-systemic encephalopathy. Metab Brain Dis 1998;13:361-77.
- Groeneweg M, Quero JC, De Bruijn I, Hartmann IJ, Essink-bot ML, Hop WC, Schalm SW. Subclinical hepatic encephalopathy impairs daily functioning. Hepatology 1998;28(1):45-9.
- Bajaj JS, Saeian K, Schubert CM, Hafeezullah M, Franco J, Varma RR, et al. Minimal hepatic encephalopathy is associated with motor vehicle crashes: the reality beyond the driving test. Hepatology 2009;50:1175-83.
- Roman E, Cordoba J, Torrens M, Torras X, Villanueva C, Vargas V, Guarner C, Soriano G. Minimal hepatic encephalopathy is associated with falls. Am J Gastroenterol 2011;106: 476-82.
- Romero-Gomez M, Cordoba J, Jover R, del Olmo JA, Ramirez M, Rey R, et al. Value of the critical flicker frequency in patients with minimal hepatic encephalopathy. Hepatology 2007;45:879-85.
- Bajaj JS, Cordoba J, Mullen KD, Amodio P, Shawcross DL, Butterworth RF, et al. Review article: the design of clinical trials in hepatic encephalopathy – an International Society for Hepatic Encephalopathy and Nitrogen Metabolism (ISHEN) consensus statement. Aliment Pharmacol Ther 2011;33:739-47.
- Jepsen P, Ott P, Andersen PK, Sorensen HT, Vilstrup H. Clinical course of alcoholic liver cirrhosis: a Danish population-based cohort study. Hepatology 2010;51:1675-82.
- Weissenborn K, Ennen JC, Schomerus H, Ruckert N, Hecker H. Neuropsychological characterization of hepatic encephalopathy. J Hepatol 2001;34:768-73.
- Kircheis G, Wettstein M, Timmermann L, Schnitzler A, Haussinger D. Critical flicker frequency for quantification of low-grade hepatic encephalopathy. Hepatology 2002; 35:357-66.
- Bajaj JS, Saeian K, Verber MD, Hischke D, Hoffmann RG, Franco J, Varma RR, Rao SM. Inhibitory control test is a simple method to diagnose minimal hepatic encephalopathy and predict development of overt hepatic encephalopathy. Am J Gastroenterol 2007; 102:754-60.
- Bajaj JS, Thacker LR, Heuman DM, Fuchs M, Sterling RK, Sanyal AJ, et al. The Stroop smartphone application is a short and valid method to screen for minimal hepatic encephalopathy. Hepatology 2013;58:1122-32.
- Randolph C, Hilsabeck R, Kato A, Kharbanda P, Li YY, Mapelli D, Ravdin LD, Romero-Gomez M, Stracciari A, Weissenborn K. Neuropsychological assessment of hepatic encephalopathy: ISHEN practice guidelines. Liver Int 2009;29:629-35.
- Als-Nielsen BE, Gluud LL, Gluud CN. Nonabsorbable disaccharides for the treatment of hepatic encephalopathy – a systemic review of randomized clinical trials – a secondary publication. Ugeskr Laeger 2004; 167:179-82.
- Sharma P, Sharma BC, Agrawal A, Sarin SK. Primary prophylaxis of overt hepatic encephalopathy in patients with cirrhosis: an open labelled randomized controlled trial of lactulose versus no lactulose. J Gastroenterol Hepatol 2012;27:1329-35.
- Sharma BC, Sharma P, Agrawal A, Sarin SK. Secondary prophylaxis of hepatic encephalopathy: an open-label randomized controlled trial of lactulose versus placebo. Gastroenterology 2009;137:885-91.
- Shukla S, Shukla A, Mehboob S, Guha S. Meta-analysis: the effects of gut flora modulation using prebiotics, probiotics and synbiotics on minimal hepatic encephalopathy. Aliment Pharmacol Ther 2011;33:662-71.
- Wu D, Wu SM, Lu J, Zhou YQ, Xu L, Guo CY. Rifaximin versus Nonabsorbable Disaccharides for the Treatment of Hepatic Encephalopathy: A Meta-Analysis. Gastroenterol Res Pract 2013;2013:236963. doi: 10.1155/2013/236963
- Bass NM, Mullen KD, Sanyal A, Poordad F, Neff G, Leevy CB, et al. Rifaximin treatment in hepatic encephalopathy. N Engl J Med 2010;362:1071-81.
- Sanyal A, Younossi ZM, Bass NM, Mullen KD, Poordad F, Brown RS, et al. Randomised clinical trial: rifaximin improves health-related quality of life in cirrhotic patients with hepatic encephalopathy – a double-blind placebo-controlled study. Aliment Pharmacol Ther 2011;34:853-61.
- Bajaj JS, Heuman DM, Wade JB, Gibson DP, Saeian K, Wegelin JA, et al. Rifaximin improves driving simulator performance in a randomized trial of patients with minimal hepatic encephalopathy. Gastroenterology 2011;140:478-87 e1.
- Sidhu SS, Goyal O, Mishra BP, Sood A, Chhina RS, Soni RK. Rifaximin improves psychometric performance and health-related quality of life in patients with minimal hepatic -encephalopathy (the RIME Trial). Am J Gastroenterol 2011;106:307-16.
- Sharma BC, Sharma P, Lunia MK, Srivastava S, Goyal R, Sarin SK. A randomized, double-blind, controlled trial comparing rifaximin plus lactulose with lactulose alone in treatment of overt hepatic encephalopathy. Am J Gastroenterol 2013;108:1458-63.
- Chautant F , Duhalde V , Berlioux P, Robic MA, Christol C, Péron JM, et al. Rifaximine et encéphalopathie hépatique : premier retour d’expérience française dans le cadre de l’ATU. A52 p49 AFEF 2013
- Laleman W, Maleux G, Cordoba J, Nevens F. Embolisation of large spontaneous portosystemic shunts in the treatment of refractory hepatic encephalopathy: A technique for the few but not the many. Hepatology 2013 Jun 14. doi: 10.1002/hep.26574.
Les Cinq points forts
-
L’encéphalopathie hépatique minime se définit par un déficit attentionnel, une atteinte des fonctions exécutives et un ralentissement psychomoteur. Son diagnostic nécessite la réalisation de tests psychométriques.
-
L’encéphalopathie hépatique minime est à l’origine d’une altération de la qualité de vie et des facultés de conduite et augmente le risque de chutes. Elle est prédictive de la survenue d’une encéphalopathie hépatique clinique.
-
Le lactulose ou la rifaximine peuvent être proposés pour traiter l’encéphalopathie hépatique minime.
-
La prévention de l’encéphalopathie hépatique clinique passe par l’éviction des facteurs favorisants : médicaments psychotropes, infections, déshydratation… Le traitement de l’encéphalopathie hépatique clinique est la recherche puis la prise en charge des facteurs précipitants. Le lactulose et/ou la rifaximine peuvent être proposés en prévention secondaire.
-
La survenue d’une encéphalopathie hépatique clinique est de mauvais pronostic et doit faire envisager la transplantation hépatique.
FMC HGE : Organisme certifié Qualiopi pour la catégorie ACTIONS DE FORMATION