Objectifs pédagogiques
- Connaître les principaux diagnostics et leur histoire naturelle
- Connaitre les critères d’un diagnostic étiologique
- Connaître les modalités de surveillance
- Connaître les principes thérapeutiques et leurs indications
Boston Scientific, Creo Médical
Kyste pancréatique, TIPMP, Echoendoscopie
ACE : Antigène Carcino-Embryonnaire
CS : Canaux Secondaires
CPP : Canal Pancréatique Principal
EE : ÉchoEndoscopie
IRM : Imagerie par Résonance Magnétique
LKP : Lésions Kystiques Pancréatiques
LST : Lateral Spreading Tumor
MCA : cystadénome mucineux
PanIN : Pancreatic Intraepithelial Neoplasia
SCA : cystadénome séreux
TIPMP : Tumeur Intracanalaire Papillaire et Mucineuse du Pancréas
TKP : Tumeurs Kystiques du Pancréas
TNE : Tumeur NeuroEndocrine
TSPP : Tumeur Solide et Pseudo Papillaire
Les LKP sont très fréquentes en population générale et leur prévalence augmente avec l’âge. Elles sont dans la grande majorité des cas asymptomatiques, découvertes fortuitement à l’occasion d’une imagerie abdominale. Leur prévalence varie de 2,5 % à 5 % de la population entre 50 et 60 ans, de 5 % à 10 % entre 60 et 70 ans, de 10 % à 20 % entre 70 et 80 ans et atteint 30 % après 85 ans. 80 % des LKP sont des tumeurs kystiques du pancréas (TKP). Les 20 % restants sont des lésions inflammatoires survenant après une pancréatite aiguë ou dans le cadre d’une pancréatite chronique.
D’un point de vue histopathologique, on distingue les TKP vraies, les plus fréquentes, qui sont des proliférations tumorales avec un éventuel potentiel de dégénérescence, et les TKP non proliférantes beaucoup plus rares, dystrophiques ou malformatives. On distinguera, à part, les cystadénocarcinomes conventionnels et les cystadénocarcinomes à cellules acinaires.
Le but de la prise en charge de ces lésions est de faire un diagnostic précis de leur nature histologique, de déterminer leur risque de dégénérescence, pour décider de les surveiller ou de les opérer si nécessaire.
Par ordre décroissant de prévalence sont observées :
Les tumeurs intracanalaires papillaires et mucineuses du pancréas (TIPMP) sont des lésions précancéreuses canalaires intraépithéliales développées aux dépens des canaux pancréatiques (principal ou/et secondaires). La TIPMP présente un épithélium de type mucineux avec production de mucus. Au cours du processus d’oncogenèse, des papilles commencent à se former et 4 phénotypes cellulaires distincts ont été décrits :
La TIPMP présente une séquence évolutive comparable à celle des adénomes coliques avec une progression depuis la dysplasie de bas grade vers la dysplasie de haut grade, puis vers l’adénocarcinome micro invasif et enfin l’adénocarcinome invasif.
La TIPMP est extrêmement fréquente dans la population après 60 ans. Le sexe ratio est de 1. On distingue l’atteinte localisée aux canaux secondaires (CS) de l’atteinte du canal pancréatique principal (CPP). L’atteinte des canaux secondaires est la plus fréquente (75 % des cas) et son risque de dégénérescence est 3,3 %, 6,6 % et 15 % respectivement à 5, 10 et 15 ans (1). L’atteinte isolée du canal pancréatique principal est rare (5 % des cas), mais de 20 % lorsqu’associée à l’atteinte des CS (on parle alors de TIPMP mixte). Son risque de dégénérescence est élevé à court et moyen terme.
Lorsque la dilatation du CPP dépasse 10 mm, et surtout 15 mm, le risque de cancérisation est de 40 % après 5 ans d’évolution, 80 % après 10 ans et est proche de 100 % après 15 ans (2).
Cette évolution est le plus souvent assez lente et le pronostic de l’adénocarcinome invasif développé sur un kyste connu, découvert au cours de la surveillance, est meilleur que celui de l’adénocarcinome ductulaire classique, à taille et stade T comparable. Néanmoins, 50 % des cancers qui vont survenir au cours du suivi d’une TIPMP CS ne correspondent pas à la dégénérescence d’un kyste de TIPMP CS, mais à la survenue d’un adénocarcinome à distance du kyste que l’on qualifie d’adénocarcinome ductulaire concomitant à la TIPMP (1). L’explication est qu’une partie des patients qui sont porteurs d’une TIPMP CS sont également porteurs d’un autre type de lésion pré-cancéreuse quasiment indétectable en imagerie : la PanIN (pancreatic intraepithelial neoplasia) qui peut elle aussi évoluer de la PanIN 1 à la PanIN 3 (équivalent de la DHG) et enfin à l’adénocarcinome ductulaire.
Cette particularité évolutive complique bien sûr la surveillance des TIPMP CS, car l’adénocarcinome ductulaire concomitant évolue rapidement comme un adénocarcinome ductulaire classique, si bien qu’un intervalle supérieur à un an, entre deux examens de surveillance, peut être responsable de la découverte d’un cancer localement avancé ou métastatique. La connaissance de ce phénomène justifie des intervalles de surveillance rapprochés où l’EE, examen plus invasif que l’imagerie en coupe, garde toute sa place en alternance avec elle, car c’est le seul examen d’imagerie susceptible de détecter les adénocarcinomes ductulaires concomitants de petite taille (3).
Il s’agit d’une prolifération de l’épithélium canalaire qui réalise des papilles centrées par un axe vasculaire sécrétant du mucus, qui s’écoule difficilement, s’accumule donc dans le CS, entraînant la création d’une dilatation kystique du CS. Le canal jonctionnel qui relie le CS kystisé et le CPP n’est pas toujours visible en imagerie canalaire de type IRM ou EE.
Lorsque le CS est assez volumineux (supérieur à 2 cm) et posé sur le CPP, il est souvent difficile de mettre en évidence, la communication avec le CPP.
Les principaux éléments du diagnostic positif de TIPMP CS sont :
La TIPMP est souvent faite de kystes uniloculaires, mais parfois le kyste est bilobé ou trifolié.
Plus rarement la TIPMP CS est faite de multiples cavités communiquant les unes avec les autres, réalisant un aspect en grappe de raisin. Encore plus rarement, on peut visualiser un aspect en nid d’abeille, qui pose un difficile problème de diagnostic différentiel avec le SCA.
L’évolution naturelle de la TIPMP CS est le plus souvent l’augmentation lente en taille des formations kystiques. Parfois la taille des kystes reste longtemps stable, ce qui ne préjuge pas du caractère définitif de cette stabilité. Rarement leur volume décroît. Parfois un ou plusieurs kystes disparaissent lors des contrôles ultérieurs. Les gouttelettes de mucus peuvent se calcifier.
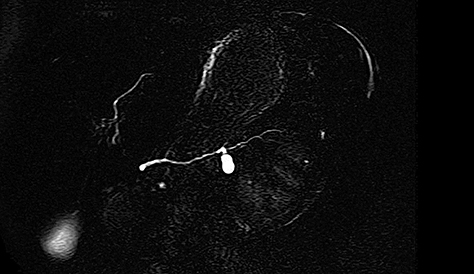
TIPMP CS unique avec raccordement bien visible au canal pancréatique principal en CP-IRM

TIPMP CS avec gouttelette de mucus intrakystique en EE
Dans sa forme isolée (sans dilatation des CS), elle est rare et de diagnostique aisé. On distingue 4 formes :
Sur la pièce d’exérèse est habituellement observé une TIPMP pancréatobiliaire en DHG.

TIPMP CPP « historique » avec dilatation jusqu’au duodénum en CP-IRM
Il s’agit le plus souvent de multiples lésions de TIPMP CS plus ou moins volumineuses, communicantes pour certaines d’entre elles à plein canal avec le CPP qui est dilaté à plus de 6 mm. Lorsque la dilatation du CPP dépasse 8 mm, le diagnostic de TIPMP mixte doit être considéré comme acquis. En dessous, il est difficile d’écarter une dilatation passive en aval de la communication.
Plusieurs aspects observés d’emblée ou au cours du suivi sont prédictifs d’une évolution péjorative. On parle de facteurs de risque élevés de dégénérescence et de facteurs de risques relatif de dégénérescence dans la recommandation européenne de 2018 (4) (à la place des « worrisome features » et des « high risk stigmata » du consensus international de 2012) (5).
Il est fréquent, découvert le plus souvent chez une femme de plus de 60 ans, également réparti dans la glande, dégénère exceptionnellement, et se présente sous 4 formes morphologiques différentes.
Dans une série multicentrique ayant colligé 2516 SCA (6), 61 % ont été opérés (52 % dans l’année), en raison d’un doute diagnostique avec une TKP mucineuse, principalement une TIPMP CS. Plusieurs raisons expliquent ce pourcentage de chirurgie mutilante et potentiellement morbide pour une TKP dont le risque dégénérescence est quasi nul :
Pour toutes ces situations, la réalisation d’un prélèvement EE-guidé est nécessaire et permet de redresser le diagnostic.

Cystadénome séreux typique avec calcification centrale en scanner
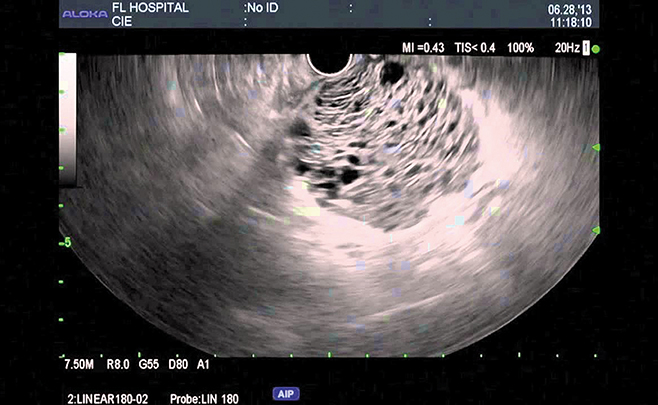
Cystadénome séreux microkystique avec aspect feuilleté en EE
C’est une TKP qui est nettement moins fréquent que le SCA, retrouvée dans 90 % des cas chez une femme. Le MCA est corporéocaudal dans la quasi-totalité des cas, et mesure entre 2 cm et 10 cm de diamètre au moment du diagnostic.
Histologiquement il s’agit d’une TKP dont le revêtement épithélial interne est sécrétant, mucineux, et le contenu mucoïde. La paroi du kyste est collagène et exprime des récepteurs hormonaux aux œstrogènes et à la progestérone. On parle de stroma ovarien qui est indispensable au diagnostic histologique lors de l’examen anatomopathologique. Il s’agit probablement d’un reliquat d’origine embryologique développé le plus souvent au niveau de la capsule postéro-inférieure de la jonction corporéocaudale féminine. Par analogie avec le pancréas aberrant qui est un reliquat embryonnaire développé le plus souvent au niveau de la grande courbure antrale horizontale, mais qui peut beaucoup plus rarement être développé dans le duodénum ou le fundus, le MCA peut être plus rarement caudal distal, ou isthmo-corporéale, et exceptionnellement céphalique ou masculin. L’épithélium mucineux interne est très souvent abrasé, et ne subsiste que par plage, ce qui explique que certaines techniques de caractérisation microscopique (endomicroscopie confocale ou microbiopsies endokystiques) soient prises en défaut, car n’accédant pas à une portion d’épithélium viable.
Presque toujours bénin lorsqu’il mesure moins de 4 cm de diamètre (7), il est toujours au moins en DHG au-delà de 8 cm de diamètre.
Le risque évolutif de dégénérescence est évalué à 30 % à 5 ans, mais il est en réalité mal connu, car nous ne disposons pas de séries de suivi conséquentes, puisque la majorité des patientes sont opérées. Le fait que de nombreuses observations de cystadénocarcinomes diagnostiqués 10 à 15 ans après une perte de vue aient été rapportées, et que le pic de survenue du cystadénocarcinome survienne entre 65 et 75 ans, suggère qu’il est préférable de convaincre les patientes porteuses d’un MCA de se faire opérer dès qu’une taille est supérieure à 40 mm, car le risque évolutif au long cours pourrait être comparable à la TIPMP du CPP.
En imagerie et en EE, il s’agit d’une tumeur le plus souvent uniloculaire, ronde, ayant une paroi propre de 1 à 3 mm, qui prend modérément le contraste en imagerie et en EE de contraste. En EE de contraste, la prise de contraste est brève, dure le plus souvent moins de 20 secondes. Il existe souvent plusieurs septas plus épais que dans le cas du SCA macrokystique. Le contenu est souvent épaissi avec parfois un sédiment déclive. Dans 20 % des cas, on observe des calcifications de la paroi en coquille d’œuf qui témoignent de l’ancienneté du processus tumoral et sont un argument supplémentaire pour proposer une exérèse.
Le principal diagnostic différentiel du MCA est le SCA macrokystique uniloculaire ou pauci loculaire. Le prélèvement EE-guidé aidé si besoin des techniques ancillaires intra kystiques (cf. infra) redresse facilement le diagnostic.

Cystadénome mucineux avec nodule mural en EE
Elle est rare, le plus souvent bénigne et de bas grade. Elle doit être distinguée de la volumineuse TNE solide qui contient des petites images kystiques.
Il en existe 2 formes morphologiques :
Le diagnostic est facilement confirmé par une ponction EE-guidée utilisant une aiguille coupante de 22G qui ramène un liquide fluide, eau de roche ou discrètement hématique, ayant les mêmes caractéristiques que le SCA macrokystique mais riche en Chromogranine A. Une fois la seringue de liquide retirée, et le kyste complètement collabé, la ponction de la portion charnue permet d’obtenir le plus souvent le diagnostic de certitude histologique et le grade de prolifération.

Tumeur neuroendocrine kystique en EE
C’est une tumeur rare, potentiellement maligne si elle évolue longtemps, dont la présentation en imagerie est très polymorphe. Classiquement, elle touche la femme jeune de moins de 30 ans, siège avant tout dans la région corporéocaudale, est souvent volumineuse (> 4 cm) au moment du diagnostic. Elle peut aussi toucher l’enfant ou l’adolescent, plus souvent un garçon, et siège alors électivement dans la tête (tumeur de Frantz des pédiatres).
La TSPP est le plus souvent une tumeur solide, bien limitée, encapsulée, hypoéchogène, assez richement vascularisée en mode contraste, d’autant plus qu’elle est petite (< 2 cm, aspect pseudo endocrine). Elle possède souvent des plages liquidiennes plutôt périphériques mal limitées, évocatrices du diagnostic, parfois de multiples et parfois de volumineuses calcifications. Plus rarement, elle se présente comme une tumeur kystique de plusieurs centimètres de diamètre, à paroi épaisse (> 3 mm), mais une composante solide satellite est le plus souvent présente. Parfois il s’agit d’une tumeur apparemment solide mais avec des zones d’échostructure variable (échogène, hypoéchogène, mixte), avec en contraste des zones riches en contraste, d’autres pauvres en contraste et d’autres avasculaires. À titre exceptionnel, elle peut avoir une architecture microkystique mimant un SCA.
Le diagnostic en imagerie en coupe est souvent proposé par l’association TDM et IRM dans la forme classique caudale de la femme de moins de 40 ans, et il n’y a pas d’indication de prélèvement sous EE. Lorsque ce n’est pas le cas, et notamment lorsque la tumeur est céphalique, le diagnostic est facilement obtenu par le prélèvement EE-guidé (22G coupante), avec une immunohistochimie positive à la béta-caténine. L’effraction capsulaire spontanée, traumatique ou lors de l’acte chirurgical est source de récidive abdominale et de métastases hépatiques. Par analogie, il n’est pas recommandé de réaliser des prélèvements EE-guidés à visée diagnostique, par voie trans gastrique (risque d’essaimage), si le diagnostic est suspecté ou possible, et que la taille de la lésion est en soit une indication opératoire.
Elles sont rares et il en existe plusieurs types : par ordre de fréquence décroissant :
Il est la conséquence d’une pancréatite aiguë nécrosante ou d’une pancréatite chronique calcifiante. Sa découverte fortuite est rare, raison pour laquelle il ne sera pas traité spécifiquement dans cette mise au point.
De manière générale, en l’absence de technique ancillaire intra kystique, le prélèvement du liquide kystique est réalisé à l’aide d’une aiguille de 22G standard.
Une antibioprophylaxie est recommandée.
En cas de liquide visqueux c’est-à-dire lorsque le « string-sign » est positif, il est spécifique d’une TKP mucineuse. Le « string-sign » consiste en l’étirement entre l’index et le pouce du liquide kystique. Si le liquide est étiré sous la forme d’une corde de plus de 1 cm de long pendant plus de 1 seconde, le « string-sign » est positif (8).
En cas de liquide laiteux, il est très spécifique d’un lymphangiome kystique. En cas de liquide brun, c’est évocateur d’un pseudokyste post-nécrotique.

« String-sign » positif dans une TIPMP des canaux secondaires

Aspect laiteux du liquide kystique dans un lymphangiome kystique
En cas de liquide citrin fluide, l’aspect est compatible avec un SCA, mais dans certaines TIPMP CS, TNE kystique, certains MCA et certains pseudokystes rétentionnels, l’aspect peut être comparable.
En l’absence de nodule mural ou de paroi épaisse qui peut être biopsiée après avoir évacué le liquide, l’étude cytologique est globalement décevante avec une sensibilité de 50-60 % (9).
La réalisation de micro-biopsies de la paroi interne d’une TKP est devenue possible à travers une aiguille de 19G. Sous réserve de réaliser 3 biopsies avec à chaque fois 2 ou 3 prises biopsiques, le succès technique est de 98 %, le succès histologique est de 88 %, et la rentabilité diagnostique de 66 %. En comparaison du diagnostic histologique effectué sur la pièce d’exérèse, la concordance histologique est de 100 % (12). Cette rentabilité qui est donc imparfaite est en partie au moins en rapport avec l’abrasion de l’épithélium intra kystique qui est très fréquent. 2 limites doivent être mentionnées : le coût important, et le taux de complication bien plus élevé que la ponction habituelle (11,6 %) (hémorragie : 6,3 % et pancréatite aiguë : 5,3 %).
Elle consiste à appliquer contre la paroi interne d’une LKP une fibre laser prémontée à l’intérieur d’une aiguille de 19G, et à délivrer le rayonnement laser à la longueur d’onde de la fluorescéine préalablement injectée par voie veineuse, afin de visualiser les structures épithéliales éclairées par leur vascularisation spécifique. La résolution est de 3,5 microns, le champ d’exploration est de 325 microns et la profondeur analysable est de 40-70 microns. 5 lésions élémentaires ont été décrites :
L’endomicroscopie confocale est conclusive dans 85 % des cas, très efficace dans la distinction entre SCA macrokystique ou mixte et lésion mucineuse sans communication décelable. Elle est également très efficace en cas de TIPMP CS minikystique qui peut en imposer pour un SCA. Le taux de complication (à condition de ne pas dépasser 6 minutes d’examen, d’utiliser une antibioprophylaxie, et de vidanger si cela est possible le kyste en fin de procédure) est comparable à celui d’un prélèvement EE-guidé de LKP (2-3 %).
Ses performances sont excellentes pour le diagnostic de SCA (se : 95 %, spé : 100 %), de TIPMP CS (se : 92 %, spé : 95 %), pour le diagnostic de lésions kystiques mucineuses versus non mucineuse (se : 95 %, spé : 95 %), et pour celui de TNE kystique (se : 100 %, spé : 90 %). Elles sont moins bonnes dans le MCA (se : 65 %, spé : 95 %), en raison de l’importance de l’abrasion spontanée de l’épithélium propre à cette lésion (13).
Dans une étude prospective ayant évalué en aveugle, auprès d’experts pancréatologues, l’apport de la nCLE, en comparaison du prélèvement EE-guidé dans 209 LKP non communicantes chez des patients indemnes de pancréatite chronique ou d’ATCD de pancréatite aiguë, la nCLE améliorait de 27 % le diagnostic et changeait la prise en charge dans 28 % des cas (14). La limite principale est comme pour les biopsies intrakystiques le coût de la procédure.
L‘étude des marqueurs moléculaires dans le liquide des LKP, utilisant les plateformes de séquençages moléculaires les plus récentes, portant sur plus de 600 patients, ayant une LKP a démontré (15) :
Les limites à son utilisation en routine sont son coût et la nécessité de recours à des plateformes de séquençages.
Après un TDM pancréatique injecté triphasique en coupes fines et une IRM pancréatique avec CPIRM. Il y a 3 possibilités :
Certaines LKP ne nécessitent aucune surveillance ni traitement :
Certaines LKP nécessitent de discuter d’une chirurgie d’emblée :
Pour les TIPMP, c’est l’algorithme de prise en charge de la TIPMP basé sur les recommandations européennes qui doit être utilisé (cf. ci-dessous).
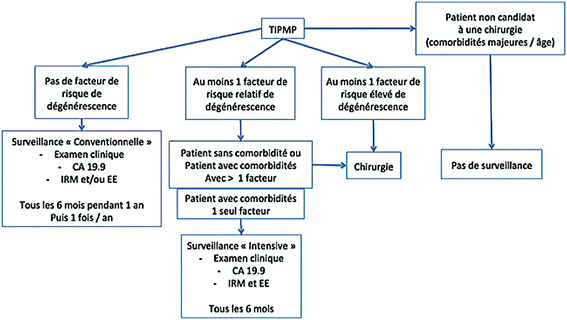
Algorithme de prise en charge des TIPMP selon les recommandations européennes
| Facteurs de risque relatif de dégénérescence de la TIPMP |
| 1. Atteinte du CPP avec dilatation comprise entre 5 mm et 10 mm |
| 2. Diamètre d’un CS supérieur à 40 mm |
| 3. Augmentation de diamètre d’un CS de plus de 5 mm en un an. |
| 4. Existence d’un nodule mural de moins de 5 mm, authentifié par une prise de contraste en imagerie en coupe ou lors de l’EE de contraste |
| 5. Pancréatite aiguë |
| 6. Découverte d’un diabète de novo |
| 7. Élévation du CA-19-9 sérique |
| Facteurs de risque élevé de dégénérescence de la TIPMP |
| 1. Atteinte du CPP avec dilatation supérieure à 10 mm |
| 2. Présence d’une masse tissulaire parenchymateuse |
| 3. Existence d’un nodule mural de plus de 5 mm, authentifié par une prise de contraste en imagerie en coupe ou lors de l’EE de contraste |
| 4. Ictère en rapport avec la compression biliaire par la lésion |
| 5. Cytologie positive (DHG/Cancer) lors du prélèvement EE-guidé |
Toute reproduction ou réécriture, totale ou partielle, sans l’accord préalable écrit de la FMC HGE est interdite.
FMC HGE : Organisme certifié Qualiopi pour la catégorie ACTIONS DE FORMATION.