La place de la radiothérapie dans les cancers digestifs : discutons-en en RCP ! – Partie 3
Les points forts
LIENS D’INTÉRÊT
Abbvie ; Amgen ; BMS ; GSK ; Incyte ; Leo Pharma ; Merck Serono ; MSD ; Novocure ; Nutricia ; Servier ; Takeda ; Viatris.
MOTS-CLÉS
Cancer du pancréas ; Radiothérapie ; Néoadjuvant ; Induction ; Clôture.
ABRÉVIATIONS
A-RT : radiothérapie ablative à haute dose ; CRT : chimioradiothérapie ; GEMCAP : gemcitabine + capécitabine ; GEMNAB : gemcitabine + nab-paclitaxel ; 5FU : 5-fluorouracil ; SBRT : radiothérapie stéréotaxique ; SG : survie globale ; SSM : survie sans maladie ; SSP : survie sans progression ; SSR : survie sans récidive ; ypCR : taux de réponse pathologique complète.
Introduction
L’incidence des adénocarcinomes du pancréas augmente régulièrement en France depuis plusieurs années avec près de 16 000 nouveaux cas en 2025. De nombreux essais cliniques récents ont investigué de nouvelles stratégies thérapeutiques pour les cancers du pancréas localisés. En situation métastatique, la prise en charge thérapeutique repose sur des lignes de chimiothérapie successives mais les traitements locorégionaux conservent une place dans des indications particulières.
Au diagnostic et selon le bilan d’extension, les cancers du pancréas sont classés en 4 groupes (1) :
- les cancers résécables d’emblée, sans contact vasculaire ou avec un contact veineux< 180° et sans déformation de la veine,
- les cancers de résécabilité limite ou « borderline », avec un contact veineux≥ 180° et/ou une déformation veineuse mais reconstructible, et/ ou un contact artériel< 180°,
- les cancers localement avancés non résécables, avec une atteinte veineuse non reconstructible, un cavernome porte ou un contact artériel> 180°,
- les cancers métastatiques.
Ces seuls critères anatomiques ne suffisent néanmoins pas à déterminer au mieux la stratégie thérapeutique et certaines tumeurs résécables peuvent être considérées comme « borderline » en raison de critères cliniques (dénutrition, altération de l’état général, pancréatite…) ou biologiques (seuil de CA19-9> 200 ou 500 UI/ml selon les équipes) (2). Le rôle des réunions de concertation pluridisciplinaire est ici majeur pour discuter du bénéfice/ risque des différentes options et orienter au mieux le choix thérapeutique.
L’objectif de cet article est de faire un point sur les indications actuelles de la radiothérapie pour les cancers du pancréas.
Traitement adjuvant des cancers résécables
L’essai de phase 3 ESPAC-1 a comparé une chimioradiothérapie (CRT) à une chimiothérapie à base de 5-Fluorouracil (5FU) bolus en adjuvant chez les patients opérés d’un adénocarcinome du pancréas. La CRT était associée à un effet délétère avec un taux de survie globale (SG) à 5 ans significativement plus faible par rapport au bras chimiothérapie (10 % vs. 20 % ; p= 0,05). La chimiothérapie adjuvante était associée à un bénéfice significatif de survie (taux de SG à 5 ans de 21 % vs. 8 % sans chimiothérapie ; p= 0,009) (3). Bien que les modalités de la radiothérapie administrée dans cet essai soient discutables (radiothérapie conventionnelle en 2 dimensions en split course pour une dose totale de 40 Gy à 60 Gy), la CRT adjuvante n’est actuellement plus indiquée chez les patients opérés d’un adénocarcinome du pancréas.
La prise en charge actuelle des cancers du pancréas résécables repose sur une chirurgie première suivie d’une chimiothérapie adjuvante. Le standard en adjuvant a longtemps été une monochimiothérapie à base de gemcitabine ou 5-fluorouracile (5FU) pour une durée de 6 mois (4,5).
Les combinaisons gemcitabine plus capécitabine (GEMCAP, essai ESPAC4) et gemcitabine plus nab-paclitaxel (GEMNAB, essai APACT) étaient associées à une augmentation significative mais limitée de la survie globale (SG) et il n’existait pas ou peu de différence pour la survie sans maladie (SSM) (6,7) Depuis 2018, le FOLFIRINOX modifié est le standard en adjuvant (8). Chez les patients non éligibles au FOLFIRINOX, les alternatives les mieux tolérées sont la gemcitabine ou le 5FU en monothérapie mais le protocole GEMCAP reste une option.
L’intérêt d’une CRT après chimiothérapie adjuvante a été évaluée dans l’essai de phase 3 NRG/RTOG 0848 (9). En l’absence de progression après 5 mois de gemcitabine, les patients étaient randomisés entre un cycle supplémentaire de gemcitabine ou un cycle de gemcitabine suivi d’une CRT (50,4 Gy en 28 fractions avec capécitabine). L’étude est négative car la CRT n’améliorait pas la SG mais apportait un bénéfice significatif en termes de SSM (taux de SSM à 5 ans : 21,4 % versus 15,2 %, p= 0,045), sans majoration de la toxicité. En analyse exploratoire, le bénéfice de la CRT semblait plus important dans le sous-groupe des patients pN0 (taux de SG à 5 ans : 48 % versus 29 %, p= 0,04). Ces résultats posent la question du bénéfice de la CRT dans certains sous-groupes de patients mais des études complémentaires sont nécessaires avant toute conclusion.
Traitement néoadjuvant / d’induction
Pour les cancers résécables, les résultats de la séquence chirurgie – chimiothérapie adjuvante sont peu satisfaisants. Près de 40 % des patients ne peuvent recevoir de chimiothérapie adjuvante à cause de la morbi-mortalité chirurgicale et les résultats oncologiques restent médiocres : taux de résection R1 (marge> 1 mm) de 60 % à 70 %, taux de pN+ de 70 % à 80 % et taux de SSM à 5 ans inférieur à 30 % (6-8). Dans ce contexte, l’administration d’un traitement néoadjuvant pourrait permettre d’optimiser la stratégie thérapeutique et d’améliorer les résultats oncologiques en sélectionnant mieux les patients à opérer.
Pour les cancers borderline et localement avancés, un traitement d’induction est un standard thérapeutique depuis de nombreuses années en raison de l’absence de résection à visée curative possible en 1re intention. La confirmation définitive de l’intérêt d’un traitement d’induction a été apportée par l’étude ESPAC-5 (n= 86) qui a comparé 3 bras de traitement d’induction à la chirurgie d’emblée chez les patients avec un cancer borderline (10). Les 3 bras d’induction comportaient une CRT (CRT 50,4 Gy avec capécitabine), une chimiothérapie par GEMCAP ou par FOLFIRINOX. Le taux de SG à 1 an était significativement plus élevé dans les bras induction (tous confondus) par rapport au bras chirurgie [76 % vs. 39 % ; HR= 0,29 (IC 95 % : 0,14-0,60) ; p= 0,0052)].
Plusieurs essais récents ont évalué différentes modalités de traitement néoadjuvant/ d’induction. Parmi ceux-ci, les essais de phase 3 PREOPANC-1 et PREOPANC-2 ont évalué une CRT à base de gemcitabine (GEM-CRT) : 1000 mg/m2 à J1 et J8 puis CRT (15 x 2,4 Gy avec gemcitabine 1000 mg/ m2 à J1, J8 et J15) puis un cycle avec 1000 mg/m2 à J1 et J8 avant chirurgie (11,12). [Ces deux essais ont inclus des tumeurs résécables et borderline (≈50 % dans PREOPANC-1 et ≈33 % dans PREOPANC-2).
L’étude PREOPANC-1 a démontré l’intérêt de cette GEM-CRT avec une augmentation significative de la SG par rapport à une chirurgie d’emblée (HR= 0,73 ; IC 95 % : 0,56-0,96) (11). Bien que l’effet de ce traitement pré-opératoire semblait plus important dans le sous-groupe des tumeurs borderline, le test d’interaction avec le stade initial (résécable ou borderline) était négatif, ne permettant pas de conclure à une différence d’effet selon le stade (figure 1). La GEM-CRT en induction était associée à une augmentation significative du taux de résection R0 (72 % vs. 43 % ; p< 0,001), de la survie sans récidive (SSR) (HR= 0,69 ; IC 95 % : 0,53-0,91 ; p= 0,009), de la SSR locorégionale (HR= 0,57 ; IC 95 % : 0,39-0,83 ; p= 0,004) et une augmentation de la survie sans métastase (HR= 0,74 ; IC 95 % : 0,54-1,03 ; p= 0,070).
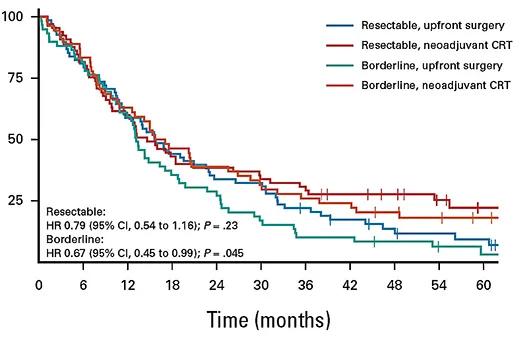
À la suite de cette 1re étude, les auteurs ont conduit l’étude PREOPANC-2 qui a comparé la GEM-CRT à 8 cycles de FOLFIRINOX (12). À la différence des patients du bras GEM-CRT, ceux du bras FOLFIRINOX n’ont pas reçu de chimiothérapie adjuvante. Après une médiane de suivi de 41,7 mois, les médianes de SG étaient identiques, de 21,3 mois dans le bras GEM-CRT et de 21,9 mois dans le bras FOLFIRINOX (HR= 0,87 ; IC 95 % : 0,68-1,12 ; p= 0,28).
Une autre étude de phase 3 japonaise, l’essai Prep-02/JSAP05, a démontré la supériorité d’une chimiothérapie néoadjuvante (gemcitabine+ S1) par rapport à la chirurgie d’emblée chez des patients avec un cancer résécable ou borderline veineux (20 %) (13). La SG était significativement allongée dans le bras néoadjuvant (médianes de 37,0 vs. 26,6 mois ; HR= 0,73 ; IC 95 % : 0,56-0,95 ; p= 0,018). Plusieurs autres études de phase 2 ont démontré la faisabilité et le potentiel intérêt d’une chimiothérapie néoadjuvante en cas de cancer résécable : SWOG 1505, NEONAX, NORPACT-1 et PANACH01 (14-17). La faisabilité est clairement démontrée avec des taux d’administration complète de la chimiothérapie néoadjuvante de ≥ 90 % dans la majorité des études, une morbi-mortalité chirurgicale comparable à une chirurgie d’emblée, des taux de résection R0 et de tumeurs (y) pN0 supérieurs dans les bras néoadjuvants et l’absence d’impact sur l’administration d’une chimiothérapie adjuvante.
Le bénéfice d’une chimiothérapie néoadjuvante doit néanmoins toujours être démontré dans des essais prospectifs. Les essais de phase 3 en cours évaluent une chimiothérapie néoadjuvante sans CRT : PREOPANC-3, Alliance AO21806 et PANACH02. Le schéma GEM-CRT n’est a priori pas utilisé en France.
Radiothérapie en consolidation après chimiothérapie d’induction
La prise en charge des cancers du pancréas borderline et localement avancés repose d’abord sur une chimiothérapie d’induction. La différence majeure entre ces deux stades concerne le taux de résection secondaire qui peut atteindre près de deux tiers en cas de cancer borderline mais reste inférieur à 10 % en cas de cancer localement avancé. Ces deux groupes de cancers se caractérisent par la fréquence des contacts artériels et veineux et la difficulté de réaliser une résection R0 d’emblée. Il existe un fort rationnel pour combiner un traitement systémique et un traitement locorégional avant chirurgie, afin de maximiser l’effet thérapeutique locorégional. Dans cette optique, l’intérêt d’une radiothérapie de consolidation (après chimiothérapie et avant chirurgie) ou de clôture (en l’absence de chirurgie) a été évaluée dans plusieurs essais.
Cancer borderline
L’essai de phase 2 randomisé ALLIANCE A021501 a comparé une chimiothérapie d’induction par 8 cycles de mFOLFIRINOX à 7 cycles de mFOLFIRINOX suivis d’une radiothérapie stéréotaxique (SBRT) (18). Le bras avec SBRT a été fermé prématurément en raison d’un taux de résection R0 inférieur au seuil fixé de 36 %. Le taux de survie à 18 mois était plus faible dans le bras SBRT (47 % vs. 67 %). Ces mauvais résultats pourraient être expliqués par une évaluation trop précoce après SBRT (conclusion à tort d’une progression du fait de la réaction inflammatoire) et/ ou une qualité médiocre de la radiothérapie (82 % de SBRT à dose modérée (33 Gy avec boost de 40 Gy intégré, en 5 fractions, dose biologique équivalente 55 Gy) et 18 % de radiothérapie 5×5 Gy) avec une couverture du volume-cible suboptimale de 60 % (19).
L’essai de phase 2 randomisé PRODIGE 44-PANDAS a randomisé les patients avec une maladie contrôlée après 4 cycles de mFOLFIRINOX entre un bras avec deux cycles supplémentaires et un bras avec deux cycles suivis d’une CRT (50,4 Gy en 28 fractions avec capécitabine) avant chirurgie et chimiothérapie adjuvante. Les résultats préliminaires présentés à l’ESMO en 2024 n’ont pas mis en évidence de différence significative en termes de taux de résection R0 ou de SG chez les patients opérés (n= 80) (20). Néanmoins, parmi les patients ayant eu la résection pancréatique (n= 68), la CRT était associée à un SG plus longue (médianes 47,9 mois vs. 35,7 mois) et le taux de réponse histologique complète (ypCR) était très supérieur dans le bras CRT (29 % versus 8 %). Les résultats définitifs de cette étude sont attendus avec impatience.
L’essai de phase 2 randomisé STEREOPAC (NCT05083247) en cours vise à évaluer l’efficacité d’une SBRT à haut niveau de dose après une chimiothérapie d’induction par mFOLFIRINOX et avant chirurgie. La SBRT présente plusieurs avantages par rapport à une CRT : s’affranchir de la chimiothérapie concomitante, permettre une escalade de dose et un temps de traitement court amenant à une interruption limitée du traitement systémique.
Cancer localement avancé
Après chimiothérapie d’induction, la place de la CRT de « consolidation » ou de « clôture » a été évaluée dans deux essais de phase 3, LAP07 (après 4 mois de gemcitabine) et CONKO-07 (après 3 mois de FOLFIRINOX dans≥ 80 % des cas) (21,22). La CRT n’était pas associée à une augmentation de la SG et ne peut donc constituer un standard thérapeutique. Néanmoins, la CRT était associée à un allongement de la SSP (médianes 9,9 vs. 8,4 ; p= 0,06), du temps sans traitement (6,1 vs. 3,7 mois ; p= 0,02) et à moins de progression locorégionale (32 % vs. 46 % ; p= 0,035) dans LAP07 et à une augmentation significative du taux de résection R0 dans CONKO-007 (marge>1 mm, 17 % vs. 9 % ; p= 0,035) (21,22). Ces résultats témoignent d’un effet thérapeutique certain de la CRT. En sus d’un éventuel meilleur contrôle locorégional, la CRT pourrait permettre d’optimiser la sélection des « bons candidats » à la chirurgie secondaire, en s’assurant de l’absence de progression à distance pendant les 3 mois de la CRT. Elle permet également de « fermer » une 1re séquence thérapeutique chez les patients restants non opérables avec un cancer localement avancé et de proposer une pause thérapeutique. La CRT est actuellement proposée comme une option thérapeutique dans le TNCD. Son indication doit être discutée en RCP avec les différentes spécialités impliquées dans la prise en charge de ces patients.
Plus récemment, les innovations en matière de techniques d’irradiation ont ouvert de nouvelles perspectives pour les tumeurs localement avancées permettant une escalade de dose jusqu’à un équivalent biologique de 100 Gy. Ainsi, la radiothérapie stéréotaxique adaptative guidée par IRM (SMART) se base sur l’utilisation d’un accélérateur linéaire couplé à une IRM (IRM-Linac) avec une planification adaptative (nouvelle définition des volumes-cibles à chaque fraction avec un recalcul des doses). L’essai de phase 2 SMART a rapporté des résultats prometteurs d’une dose de 50 Gy en 5 fractions délivrée après ≥ 3 mois de chimiothérapie d’induction (23). Le taux de SG à 2 ans était de 54 % avec une médiane de survie ≥ 22 mois. La radiothérapie ablative à haute dose (A-RT) délivre des doses élevées de manière hypofractionnée (75 Gy en 25 fractions ou 67,5 Gy en 15 fractions) et est réalisable sur des accélérateurs linéaires conventionnels avec IGRT. L’A-RT administrée après chimiothérapie d’induction était associée à taux de SG à 2 ans de 38 % et une bonne tolérance (24). En dehors de ces nouvelles modalités de radiothérapie, de nouveaux radiosensibilisants sont en cours d’étude tels que des nanoparticules (essai Nano-SMART), des inhibiteurs de checkpoints ou des mimétiques sélectifs de la dismutase.
En France, l’essai de phase 2 GABRINOX ART en cours évalue une chimiothérapie séquentielle avec alternance mensuelle de GEMNAB et FOLFIRINOX pendant 4 mois suivie d’une SBRT par IRM Linac pour les cancers localement avancés.
Cas particuliers
Patients inopérables
Une étude rétrospective monocentrique a rapporté des résultats intéressants d’une radiothérapie hypofractionnée avec escalade de dose dite ablative (A-RT) administrée après une chimiothérapie d’induction chez des patients avec un cancer résécable mais inopérable (24). Parmi les 25 patients inclus, le taux de SG à 2 ans était de 44 % avec un taux de contrôle local à 2 ans de 79 %. Ces résultats prometteurs restent à confirmer sur un plus grand nombre de patients de manière prospective.
Douleurs du plexus cœliaque
La radiothérapie a montré depuis des décennies son efficacité à visée antalgique pour de très nombreux cancers métastatiques avancés en situation palliative. Pour les cancers du pancréas, l’innervation par le plexus cœliaque et l’invasion locale destructrice sont sources de douleurs épigastriques transfixiantes très intenses et invalidantes, souvent résistantes aux approches médicamenteuses. L’essai de phase 2 non randomisé PAINPAC a évalué chez des patients atteints de douleurs pancréatiques réfractaires une irradiation de la tumeur pancréatique à la dose de 24 Gy en 3 fractions hebdomadaires (25). Une réduction des douleurs était rapportée par 80 % des patients, avec, pour plus de la moitié, une réduction des morphiniques prescrits. Il existait également un bénéfice cliniquement significatif sur la qualité de vie. Une irradiation stéréotaxique du plexus cœliaque en une fraction de 25 Gy permet également une réduction au moins partielle de la douleur à 3 semaines chez 53 % des patients (26). La SBRT cœliaque est une approche à privilégier car moins invasive que les techniques classiques par infiltration ou anesthésiques locaux, voire la neurolyse par phénolisation. Cependant, il n’existe pas à ce jour de comparaison entre ces différentes approches.
Récidive locorégionale et maladie oligométastatique
En cas de rechute locorégionale isolée et à l’instar des cancers localement avancés, la radiothérapie de clôture peut être discutée comme une option thérapeutique après une 1re étape de chimiothérapie systémique. La SBRT est particulièrement adaptée dans cette situation permettant d’obtenir un taux de contrôle local élevé.
En cas de maladie oligométastatique (cinq métastases maximum), la SBRT des métastases pourrait allonger la survie des patients. Dans l’essai de phase II randomisé EXTEND, les patients ayant eu une SBRT de leurs métastases en plus du traitement systémique avaient une médiane de survie sans progression allongée par rapport à ceux n’ayant reçu que le traitement systémique (10,3 mois versus 2,5 mois p= 0,03) (27). L’essai de phase III EXPAND est en cours d’ouverture pour confirmer ces résultats sur de plus larges effectifs.
Conclusion
La radiothérapie garde une place importante dans la prise en charge des adénocarcinomes du pancréas. Si son bénéfice en consolidation lors de la séquence d’induction reste en cours d’investigation, les résultats des essais LAP07 et CONKO-07 soutiennent son intérêt et en font une option thérapeutique chez les patients avec un cancer localement avancé. La radiothérapie est également une option intéressante chez les patients non opérables avec une tumeur résécable, en cas de récidive locorégionale isolée ou de maladie oligométastatique. En situation adjuvante, en attendant de nouvelles données, il n’existe pas d’indication.
Références
- Tempero MA, Malafa MP, Chiorean EG, et al. Pancreatic Adenocarcinoma, Version 1.2019. J Natl Compr Canc Netw 2019;17(3):202-210.
- Schwarz L, Katz MHG. Diagnosis and Management of Borderline Resectable Pancreatic Adenocarcinoma. Hematol Oncol Clin North Am 2015;29(4):727-40.
- Neoptolemos JP, Stocken DD, Helmut Friess H, et al. A Randomized Trial of Chemoradiotherapy and Chemotherapy after Resection of Pancreatic Cancer. N Engl J Med 2004;350:1200-1210.
- Oettle H, Neuhaus P, Hochhaus A, et al. Adjuvant chemotherapy with gemcitabine and long-term outcomes among patients with resected pancreatic cancer: the CONKO-001 randomized trial. JAMA 2013;310(14):1473-81.
- Neoptolemos JP, Stocken DD, Bassi C, et al. Adjuvant chemotherapy with fluorouracil plus folinic acid vs. gemcitabine following pancreatic cancer resection: a randomized controlled trial. JAMA 2010 ;304(10):1073-81.
- Neoptolemos JP, Palmer DH, Ghaneh P, et al. Comparison of adjuvant gemcitabine and capecitabine with gemcitabine monotherapy in patients with resected pancreatic cancer (ESPAC-4): a multicentre, open-label, randomised, phase 3 trial. Lancet 2017;389(10073):1011-1024.
- Tempero MA, Pelzer U, O’Reilly EM, et al. Adjuvant nab-Paclitaxel + Gemcitabine in Resected Pancreatic Ductal Adenocarcinoma: Results From a Randomized, Open-Label, Phase III Trial. J Clin Oncol 2023 Apr 10;41(11):2007-2019.
- Conroy T, Castan F, Lopez A, et al. Five-Year Outcomes of FOLFIRINOX vs. Gemcitabine as Adjuvant Therapy for Pancreatic Cancer: A Randomized Clinical Trial. JAMA Oncol 2022;8(11):1571-1578.
- Abrams RA, Winter KA, Safran H, et al. Results of the NRG Oncology/RTOG 0848 Adjuvant Chemotherapy Question-Erlotinib+Gemcitabine for Resected Cancer of the Pancreatic Head: A Phase II Randomized Clinical Trial. J Clin Oncol 2020;43:173-179.
- Ghaneh P, Palmer D, Cicconi S, et al. Immediate surgery compared with short-course neoadjuvant gemcitabine plus capecitabine, FOLFIRINOX, or chemoradiotherapy in patients with borderline resectable pancreatic cancer (ESPAC5): a four-arm, multicentre, randomised, phase 2 trial. Lancet Gastroenterol Hepatol 2023;8(2):157-168.
- Versteijne E, van Dam JL, Suker M, et al. Neoadjuvant Chemoradiotherapy Versus Upfront Surgery for Resectable and Borderline Resectable Pancreatic Cancer: Long-Term Results of the Dutch Randomized PREOPANC Trial. J Clin Oncol 2022;40(11):1220-1230.
- Janssen QP, van Dam JL, van Bekkum ML, et al. Neoadjuvant FOLFIRINOX versus neoadjuvant gemcitabine-based chemoradiotherapy in resectable and borderline resectable pancreatic cancer (PREOPANC-2): a multicentre, open-label, phase 3 randomised trial. Lancet Oncol 2025;26(10):1346-1356.
- Unno M, Motoi F, Matsuyama Y, et al. Neoadjuvant chemotherapy with gemcitabine and S-1 versus upfront surgery for resectable pancreatic cancer: Results of the randomized phase II/III Prep-02/JSAP05 trial. Ann Surg 2025 (sous presse).
- Sohal DPS, Duong M, Ahmad SA, et al. Efficacy of Perioperative Chemotherapy for Resectable Pancreatic Adenocarcinoma: A Phase 2 Randomized Clinical Trial. JAMA Oncol 2021;7(3):421-427.
- Seufferlein T, Uhl W, Kornmann M, et al. Perioperative or only adjuvant gemcitabine plus nab-paclitaxel for resectable pancreatic cancer (NEONAX)-a randomized phase II trial of the AIO pancreatic cancer group. Ann Oncol 2023;34(1):91-100.
- Schwarz L, Bachet JB, Meurisse A, et al. Neoadjuvant FOLF(IRIN)OX Chemotherapy for Resectable Pancreatic Adenocarcinoma: A Multicenter Randomized Noncomparative Phase II Trial (PANACHE01 FRENCH08 PRODIGE48 study). J Clin Oncol 2025;43(17):1984-1996.
- Labori KJ, Bratlie SO, Andersson B, et al. Neoadjuvant FOLFIRINOX versus upfront surgery for resectable pancreatic head cancer (NORPACT-1): a multicentre, randomised, phase 2 trial. Lancet Gastroenterol Hepatol 2024;9(3):205-217.
- Katz MHG, Shi Q, Meyers J, et al. Efficacy of Preoperative mFOLFIRINOX vs. mFOLFIRINOX Plus Hypofractionated Radiotherapy for Borderline Resectable Adenocarcinoma of the Pancreas: The A021501 Phase 2 Randomized Clinical Trial. JAMA Oncol 2022;8:1263-1270.
- Tchelebi LT, Segovia D, Smith K, et al. Radiation Therapy Quality Assurance Analysis of Alliance A021501: Preoperative mFOLFIRINOX or mFOLFIRINOX Plus Hypofractionated Radiation Therapy for Borderline Resectable Adenocarcinoma of the Pancreas. Int J Radiat Oncol Biol Phys 2024;120:111-119.
- Lambert A, Bouche O, Ayav A, et al. LBA62 Preoperative modified FOLFIRINOX (mFOLFIRINOX) with or without chemoradiation (CRT) in borderline resectable pancreatic cancer (BRPC): Results from the randomized phase II trial PANDAS/PRODIGE 44. Ann Oncol 2024;35:S1252.
- Hammel P, Huguet F, van Laethem JL, et al. Effect of Chemoradiotherapy vs. Chemotherapy on Survival in Patients With Locally Advanced Pancreatic Cancer Controlled After 4 Months of Gemcitabine With or Without Erlotinib: The LAP07 Randomized Clinical Trial. JAMA 2016;315(17):1844-53.
- Fietkau R, Ghadimi M, Grützmann R, et al. Randomized phase III trial of induction chemotherapy followed by chemoradiotherapy or chemotherapy alone for nonresectable locally advanced pancreatic cancer: First results of the CONKO-007 trial. J Clin Oncol 2022;40,16_ suppl:4008.
- Chuong MD, Lee P, Low DA, et al. Stereotactic MR-guided on-table adaptive radiation therapy (SMART) for borderline resectable and locally advanced pancreatic cancer: A multi-center, open-label phase 2 study. Radiother Oncol 2024;191:110064.
- Reyngold M, Schoenfeld JD, O’Reilly EM, et al. Nonoperative Management of Technically Resectable Pancreatic Cancer With Ablative Radiation Therapy. JAMA Oncol 2025;11:609-616.
- Tello Valverde CP, Ebrahimi G, Sprangers MA, et al. Impact of Short-Course Palliative Radiation Therapy on Pancreatic Cancer-Related Pain: Prospective Phase 2 Nonrandomized PAINPANC Trial. Int J Radiat Oncol Biol Phys 2024;118:352-361.
- Lawrence YR, Miszczyk M, Dawson LA, et al. Celiac plexus radiosurgery for pain management in advanced cancer: a multicentre, single-arm, phase 2 trial. Lancet Oncol 2024;25:1070-9.
- Ludmir EB, Sherry AD, Fellman BM, et al. Addition of Metastasis-Directed Therapy to Systemic Therapy for Oligometastatic Pancreatic Ductal Adenocarcinoma (EXTEND): A Multicenter, Randomized Phase II Trial. J Clin Oncol 2024;42:3795-3805.
Toute reproduction ou réécriture, totale ou partielle, sans l’accord préalable écrit de la FMC HGE est interdite.
