Lien d’intérêt
L’auteure ne déclare aucun lien d’intérêt en relation avec sa présentation
Mots-clés
Chirurgie bariatrique ; obésité ; micronutriments
Abréviations
Non communiquées
Introduction
L’obésité est un enjeu de santé publique majeur et en pleine expansion : lors de la dernière enquête épidémiologique de 2020, sa prévalence était estimée à 17 % de la population générale (1) et une augmentation rapide de l’incidence était notée, surtout dans les groupes d’âge les plus jeunes et pour l’obésité morbide, dont la prévalence a été multipliée par 7 entre 1997 et 2020.
Au vu des résultats décevants des approches diétético-comportementales et médicamenteuses (avant l’avènement des incrétinomimétiques comme les analogues du GLP-1), la chirurgie bariatrique s’est imposée comme l’alternative proposant les meilleurs résultats en termes de perte de poids maintenue sur le long terme. Cette dernière a connu une forte progression durant ces dernières décennies, le nombre d’actes ayant été multiplié par 20 entre 1997 et 2017, portée par la prise en charge de l’Assurance Maladie.
D’après les recommandations HAS de 2009 (2) la chirurgie bariatrique est recommandée en 2e intention après échec des règles hygiéno-diététiques, pour des patients ayant un IMC≥ 40 kg/m2, ou ≥ à 35 kg/m2 associé à une comorbidité. Peu importe le type de procédure, les effets bénéfiques attendus sont une perte de poids soutenue dans le temps, une amélioration des comorbidités associées et une survie prolongée. En 2022, l’indication opératoire a été étendue aux patients diabétiques de type 2 en obésité modérée (IMC 30-35 kg/m2).
Les différents types de chirurgie bariatrique
De nombreuses techniques opératoires et montages chirurgicaux ont été décrits au fil des années, et plusieurs nouvelles techniques, y compris endoscopiques, sont en cours de développement. Actuellement, uniquement 4 techniques sont recommandées par la HAS :
- L’anneau gastrique ajustable ;
- La sleeve gastrectomie (SG) ;
- Le by-pass gastrique (BPG) (en version « classique en Y » ou en « omega ») ;
- La dérivation biliopancréatique avec diversion duodénale (DBP).
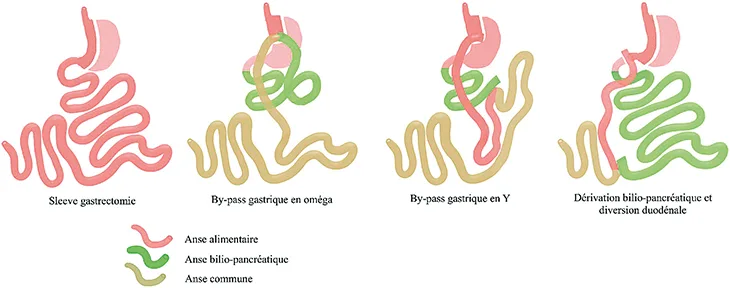
En France, la SG est l’intervention la plus pratiquée (env. 60 %), suivie du by-pass en Roux-en-Y (30 %). La dérivation biliopancréatique avec diversion duodénale, indiquée chez des patients avec patients avec IMC> 50 kg/m2 ou comorbidités métaboliques sévères, est la moins pratiquée (1 à 2 % des procédures) et limitée à quelques centres spécialisés (3). En raison de ses résultats moins convaincants et du taux de complications, l’AGA est de moins en moins pratiquée. La figure 1 schématise les différents montages chirurgicaux qui seront développés plus avant, en excluant l’AGA dont l’impact nutritionnel à long terme pose moins de problématiques que les 3 autres.

Figure 1 : Principaux montages chirurgicaux pratiqués en chirurgie bariatrique (avec l’aimable contribution du Dr Jérôme Danion, CHU Poitiers)
- La sleeve gastrectomie ou gastrectomie longitudinale consiste en l’ablation des 2/3 de l’estomac réduisant ainsi son volume à une capacité d’environ 150 ml contre>1 000 ml à l’état physiologique. Outre la réduction purement volumique, elle a également un effet de réduction de la compliance et de la capacité de relaxation gastrique et d’accélération de la vidange gastrique. Bien qu’elle n’implique aucune modification de l’anatomie grêlique, elle a des conséquences sur la production d’entéro-hormones et les capacités d’absorption Elle est considérée comme une chirurgie purement restrictive, mais ces modifications ont aussi pour effet d’induire des modifications dans l’absorption alimentaire.
- Le BPG par Roux-en-Y est antérieure à la SG mais sa relative plus grande complexité chirurgicale peut expliquer sa moindre diffusion. Elle consiste en une réduction du volume gastrique dont on ne laissera qu’une petite poche de 15-30 ml, combinée à une transposition d’une anse alimentaire d’environ 150 cm qui sera connectée à l’anse biliaire (d’env. 120 cm) via une anastomose jéjuno-jéjunale réalisée pour aboucher sur l’anse commune au milieu du jéjunum.
- Le BPG dit « en omega », à une seule anastomose, est une technique similaire à la BPG en Roux-en-Y. Il consiste en un by-pass direct, en anastomosant directement l’anse biliaire à la partie distale de l’estomac, sans création d‘une anastomose grêlo-grêlique supplémentaire. La longueur de l’anse biliaire by-passée conditionne l’importance de la malabsorption. La Société Française et Francophone de Chirurgie de l’Obesité et des Maladies Métaboliques recommande une anse biliaire maximale de 200 cm afin de limiter la survenue de complications.
- La dérivation bilio-pancréatique avec diversion duodénale consiste à créer un by-pass plus important au niveau grêlique. Une gastrectomie en manchon de type sleeve est réalisée, puis le duodénum est déconnecté de l’estomac et anastomosé à une anse L’anse biliaire restante, comprenant la majeure partie du jéjunum, est anastomosée à l’anse alimentaire très en distalité afin de ne laisser qu’une anse commune d’environ 100 cm jusqu’à la valvule iléocæcale. C’est la chirurgie la plus malabsorptive.
Effets de la chirurgie bariatrique sur la physiologie de la digestion
L’objectif principal de toute intervention bariatrique est la réduction de la quantité de nutriments absorbés et la création d’une balance énergétique déficitaire. L’anneau gastrique est la seule technique qui pourrait être qualifiée de purement restrictive, à savoir un effet uniquement par diminution de la quantité des ingesta. Les autres techniques sont à la fois restrictives et malabsorptives, avec un effet restrictif prédominant pour la SG et un effet malabsorptif prédominant pour le BPG et plus encore pour la DBP. Les conséquences physiologiques des chirurgies bariatriques découlent des modifications induites par l’altération de l’anatomie digestive.
Lors d’une SG, la résection gastrique entraîne, en sus de la réduction volumique, une accélération de la vidange gastrique, et une altération de la production acide avec modification significative du pH duodénal : cela a un impact sur l’activation des enzymes pancréatiques et biliaires. Lors d’un BPG ou d’une DBP, en plus des effets suscités, le court-circuit entéral induit une accélération mécanique du transit et une asynchronie entre enzymes bilio-pancréatiques et bol alimentaire. Ces 2 éléments induisent une malabsorption lipidique.
Après chirurgie bariatrique, on observe également une modification de l’expression de plusieurs entéro-hormones impliquées dans les processus de digestion et de régulation de l’appétit. La ghréline, principale hormone orexigène, est produite en majorité par les cellules fundiques avec une sensibilité à la présence de nutriments. Dans la plupart des études comparant la SG et la GBP, les taux de ghréline à jeun et en post prandial sont significativement plus bas chez les patients après SG, du fait de l’ablation définitive du fundus. Les résultats sont plus contrastés en ce qui concerne le BPG, avec une réduction rapide les premiers mois, suivie d’un rebond jusqu’aux taux préopératoires, suggérant un effet adaptatif du tube digestif (4). Dirksen et al. ont montré chez 33 patients, suivis pendant 1 an post GBP, que les meilleurs répondeurs étaient ceux chez qui la suppression de la ghréline avait été la plus prononcée (5). Les données concernant la DBP-DS sont plus rares, mais tendent à montrer un effet similaire au BPG (6).
D’autres entéro-hormones sont également affectées par la chirurgie bariatrique, notamment le GLP-1. Cette incrétine, produite par les cellules entéro- endocrines du grêle selon un gradient croissant cranio-caudal, a connu un intérêt considérable ces derniers années dans le traitement du diabète, puis de l’obésité. Après chirurgie bariatrique, la sécrétion postprandiale de GLP-1 est fortement augmentée, surtout en cas de BPG. Cet effet est probablement lié à une augmentation de la stimulation par les nutriments sur les cellules productrices du grêle distal. Des modifications similaires ont été constatées pour d’autres entéro-hormones comme la cholécystokinine, le peptide YY et le GIP. Le tableau 1 résume les principaux effets de la SG et du GBP sur les entéro-hormones digestives (7).
Tableau 1 : Modifications de la production et/ou de l’activité des principales entéro-hormones après sleeve et by-pass gastrique, adapté de Brown et al. (7).
| Effets physiologiques | modification après sleeve gastrectomie | Modification après by-pass gastrique |
| Ghréline | ↑ ↑ | appétit motilité | ↑ | ↑ puis ↑↑ à long terme |
| GLP-1 et GIP | ↑ ↑ ↑ | satiété vidange gastrique, motricité digestive production postprandiale d’insuline | ↑ | ↑ |
| Polypeptide pancréatique(pep- tide P) | ↑ ↑ ↑ | appétit vidange gastrique production pancréatique | Stable ou ↑ | Stable ou P |
| CCK | ↑ ↑ ↑ ↑ | satiété contraction vésiculaire production pancréatique exocrine motricité digestive | ↑ | ↑ |
| PYY | ↑ ↑ | satiété vidange gastrique, motricité digestive | ↑ | ↑ |
En dehors de l’effet direct sur les hormones secrétées par les cellules intestinales, la chirurgie bariatrique a également un effet sur la sécrétion pancréatique notamment sur l’insuline, ainsi que sur la sensibilité à la leptine, par des mécanismes non complètement élucidés, mais expliquant les effets sur le diabète et sur la perte pondérale (8). Le cycle entéro-hépatique est aussi impacté via une modulation de la production et de l’action des acides biliaires. La plupart des études de cohorte notent une augmentation des taux pré- et postprandiaux des acides biliaires, plus marqués après BPG qu’après SG, via une diminution de la recapture de ces derniers, ce qui contribue (effet souhaité) à la malabsorption lipidique (9).
Cette malabsorption est aggravée par l’insuffisance pancréatique fonctionnelle, secondaire à un asynchronisme entre la production d’enzymes pancréatiques et la progression du bol alimentaire, réduisant le temps de contact entre enzymes et nutriments.
De nombreux travaux ont aussi noté la modification rapide et durable du microbiote intestinal en postopératoire, même si leurs conclusions sont disparates quant à la nature des changements et à l’impact des différents types de chirurgie. Parmi les modifications les plus rapportées, on retrouve une relative surabondance en Protéobactéries et en Bacteroidetes, ainsi qu’une réduction en firmicutes et Bifidobactéries (10). Ces modifications de la composition du microbiote surviennent rapidement en postopératoire et se maintiennent à long terme. Leur impact sur la perte de poids et le mécanisme ne sont pas parfaitement élucidés (11). Toutefois, l’altération de la motilité, la modification du microbiote, la présence d’anses digestives borgnes peuvent favoriser l’apparition d’une pullulation bactérienne aggravant la malabsorption initiale.
Complications nutritionnelles de la chirurgie bariatrique et leur prise en charge
Déficit protéique et sarcopénie
Effet attendu et souhaité de la chirurgie bariatrique, la perte de poids peut dans certains cas être excessive et induire une malnutrition protéino- énergétique. La perte pondérale devrait idéalement se faire exclusivement aux dépens du tissu adipeux excédentaire, ce qui en réalité n’est pas le cas. Il a été estimé qu’à 1 an, environ 21 % du poids perdu en post-chirurgie bariatrique était de la masse maigre (12). Bien que les bénéfices de la perte pondérale surpassent les inconvénients de la perte musculaire, une diminution excessive de masse musculaire risque d’être préjudiciable à long terme. Si cette dernière n’est pas correctement prise en charge, elle conduit à la survenue d’une sarcopénie, facteur de risque majeur péjorant l’évolution de la plupart des maladies chroniques. Dans un travail portant sur 184 obèses opérés par SG, Voican et Nadeau (13) ont mis en évidence une prévalence de 32 % de sarcopénie tomodensitométrique à 1 an postopératoire. Parmi les facteurs prédictifs de la survenue d’une sarcopénie postopératoire figuraient le sexe masculin et l’existence d’une sarcopénie préopératoire (8 % de leur cohorte). La majeure partie de cette perte musculaire a lieu durant les 3 premiers mois postopératoires, en lien avec la faiblesse des apports alimentaires durant cette période, rendant difficile un apport protéique adéquat et renforçant une balance azotée négative. D’autres travaux ont aussi démontré que la perte de masse musculaire était corrélée au pourcentage de perte totale de poids, mais pas au type de chirurgie. De plus, un rebond pondéral s’accompagne souvent d’une reprise de masse grasse sans récupération de la masse musculaire. Dans une RCT de 2015, des patients ayant eu une SG ou un BPG, la prise d’un supplément protéique durant 6 mois en postopératoire a permis une perte plus importante de masse grasse et moins de perte de masse musculaire que les patients sous placebo (14).
Les recommandations récentes du consensus d’experts français suggèrent un apport protéique minimal de 60 g/jour dès les premiers jours postopératoires, pouvant être augmenté à 1,5 g/kg (de poids idéal), y compris via l’usage de compléments protéiques. Afin de renforcer l’action de la supplémentation protéique, il est également préconisé l’implémentation de 300 minutes d’activité physique hebdomadaire, dont un minimum de 150 min d’endurance, associées à 2 ou 3 séances de renforcement musculaire (15).
Déficit en micronutriments
La prévention de la survenue de carences en micronutriments est un des défis du suivi au long cours des patients post-bariatriques. Il est aisé de comprendre que plus une chirurgie sera malabsorptive, plus le risque carentiel sera important et plus l’observance et le suivi devront être nécessaires. Cependant, les patients ayant eu uniquement une SG ne sont pas sans risque et doivent être monitorés de la même façon que les patients ayant eu un BPG, du moins durant les premières années. D’ailleurs, la plupart des recommandations internationales ne distinguent pas spécifiquement les types de chirurgie bariatrique, mais rendent attentives au suivi plus rapproché en cas de chirurgie hautement malabsorptive.
Des déficits en micronutriments sont fréquemment rencontrés chez les patients obèses candidats à la chirurgie, en lien avec une alimentation souvent déséquilibrée et aggravés par les diètes restrictives préalables (16). Cela concerne surtout les vitamines A, B1, B9, B12, C et D, ainsi que le sélénium et le zinc. Dans une étude française portant sur 267 patients, 20 % d’entre eux présentaient au moins 2 carences. Une évaluation diététique, le dépistage des déficits et leur correction en préopératoire est systématiquement recommandée par l’ensemble des sociétés savantes.
En postopératoire, une prise en charge nutritionnelle par un professionnel de santé spécialisé est recommandée. Durant les premières semaines après la chirurgie, les apports oraux drastiquement réduits font que les patients couvrent moins de 50 % de leurs besoins journaliers en micronutriments. Une supplémentation par des combinaisons multivitaminiques est indispensable pour éviter les complications. À plus long terme, il est recommandé de poursuivre cette supplémentation à vie pour les chirurgies malabsorptives, et pendant 2 ans pour la SG, bien que des études aient montré que la prévalence de déficits en micronutriments restait élevée à distance (17). L’observance est la clé, mais rendue difficile par le caractère asymptomatique de la plupart des déficits, le coût financier des suppléments non pris en charge, la lassitude, l’absence de bénéfice clinique ressenti par le patient surtout après obtention du poids-cible. Environ 20 % de patients sont perdus de vue plus de 3 ans après la chirurgie, et beaucoup d’autres sont partiellement ou totalement inobservants 5 ans après une chirurgie (18). Il est à noter que certaines périodes, comme la grossesse, sont particulièrement à risque du fait de besoins accrus.
Nous allons ci-après développer les déficits les plus fréquents et leur prise en charge.
Fer
Elle est la principale carence post chirurgie bariatrique. Elle concernerait entre 10 et 50 % des patients après chirurgie bariatrique (19). Elle est causée par : la diminution de la consommation d’aliments riches en fer, l’hypochlorhydrie qui diminue la réduction du Fe3+en Fe2+ absorbable et la réduction de la surface d’absorption de ce dernier (principalement duodénojéjunale). Elle peut être aggravée par les saignements occultes sur ulcères anastomotiques ou par les règles chez la femme en âge de procréer. Après dérivation bilio-pancréatique, elle peut nécessiter une perfusion IV chez 40 % des patients et une transfusion sanguine chez 18 % d’entre eux (20). La supplémentation devra être préférentiellement par voie orale, mais celle-ci nécessite des apports prolongés, et a une tolérance digestive moyenne, ce qui accroît l’inobservance, surtout en cas de nécessité de cures répétées. Les suppléments multi-vitaminiques disponibles ne permettent pas une couverture optimale des besoins, notamment chez la femme jeune, un dépistage biologique doit être réalisé sans attendre la survenue de signes cliniques. Le dépistage doit être systématique, tous les 3-4 mois la 1re année, puis 1 à 2 fois/an, via un dosage de la NFS et de la ferritine, éventuellement complétées par le coefficient de saturation de la transferrine. L’utilisation du fer injectable est recommandée en cas d’anémie< 10 g/L ou de non-tolérance de la voie orale.
Vitamine B12
Du fait de réserves élevées, la survenue de la carence en B12 est souvent tardive. Elle est principalement liée à la diminution de production du facteur intrinsèque via la réduction gastrique. Elle est donc systématique après GBP et DBP, mais reste fréquente après SG. Les manifestations cliniques sont surtout hématologiques et neurologiques mais elle peut se révéler par une glossite ou une dysgueusie. C’est le seul micronutriment pour lequel les modalités de supplémentation diffèrent en fonction du type de chirurgie. Le consensus d’experts français recommande une supplémentation systématique après BPG et DBP, et une surveillance après SG (15). En cas de BPG et de DBP, la supplémentation est systématique et doit être poursuivie à vie. Elle peut être effectuée par voie orale, car une fraction peut être absorbée de façon passive dans l’intestin grêle sans recours au facteur intrinsèque, par une voie non saturable. Comme pour la carence martiale, les produits multi-vitaminiques disponibles sont insuffisants pour éviter une carence. Une dose entre 350 et 1 000 µg par jour serait suffisante en prévention, soit 1 à 2 ampoules de 1 000 µg/semaine. Cela ne dispense pas d’un contrôle régulier puisqu’uniquement 5 % de la B12 administrée est absorbée par voie passive, et que d’autres éléments peuvent perturber cette absorption, comme une pullulation bactérienne. Le recours à une supplémentation intramusculaire sera nécessaire en cas de déficit sévère, de non-observance ou d’inefficacité de la voie orale.
Vitamine B1
La thiamine est une vitamine hydrosoluble essentielle pour le métabolisme énergétique des glucides. Ses réserves dans l’organisme sont limitées et dépendent principalement des apports alimentaires. De nombreuses situations cliniques peuvent conduire à un déficit en thiamine, comme une perte pondérale rapide, un éthylisme chronique ou des vomissements répétés. La prévalence est variable dans la littérature, avec une prépondérance en cas de chirurgie hautement malabsorptive comme la DBP (21). De nombreux cas d’encéphalopathie de Gayet-Wernicke ont été décrits chez des patients après chirurgie bariatrique, y compris après SG (22). Au vu de sa gravité clinique et du délai d’obtention des résultats du dosage, une supplémentation systématique avant toute perfusion de sérum glucosé doit être effectuée chez tout patient à risque (éthylisme, dénutrition, perte de poids rapide) et en présence de signes digestifs, neurologiques ou psychiatriques. Elle repose sur une perfusion IV de minimum 100 mg en prévention bien que des doses plus élevées soient utilisées en pratique clinique sans risque, et ce sans attendre les résultats de dosage. En cas de suspicion de Gayet-Wernicke, la posologie est à majorer à 500 mg IV 3x/j pendant 3 jours, suivie d’un relais oral. Ne pas oublier l’adjonction de magnésium pour son rôle de cofacteur de la thiamine pyrophosphokinase.
Calcium et vitamine D
L’absorption du calcium se fait principalement dans le duodénum et le jéjunum proximal et celle de la vitamine D, liposoluble, dans le jéjunum et l’iléon. La carence en vitamine D est extrêmement fréquente en préopératoire, allant jusqu’à 90 % de la population en attente de chirurgie bariatrique (23). En post chirurgie, les produits laitiers peuvent être mal tolérés et les apports calciques recommandés par l’ANSES de 950 mg/jour seront alors difficiles à atteindre. Une supplémentation systématique est préconisée au long cours, aussi bien après DBP et BPG qu’après SG. Elle varie entre 500 et 1 000 mg/j en fonction des apports alimentaires. Il est prescrit en doses de 500 mg réparties sur la journée pour une meilleure absorption. Le calcium sous forme citrate serait mieux absorbé en l’absence d’acidité gastrique, mais les principales préparations pharmaceutiques disponibles sont sous forme de carbonate. Les substitutions de fer et de calcium ne doivent pas être prises ensemble (intervalle minimum de 2 heures) (24). Une substitution suffisante en calcium prise aux repas a également pour effet bénéfique de réduire le risque de formation de calculs rénaux d’oxalate de calcium après chirurgie malabsorptive.
En raison de la malabsorption lipidique et des besoins importants, les apports en vitamines D sont également rarement atteints par l’alimentation seule. Les formulations combinées calcium et vitamine D sont intéressantes et permettent de limiter le déficit mais sont en général insuffisantes pour éviter une carence en vitamine D qui doit toujours être dépistée. Un complément par apport ponctuel ou régulier de doses élevées sera souvent nécessaire afin d’atteindre le taux sanguin recommandé> 30 ug/L (75 nmol/l). La substitution par voie intramusculaire peut aussi être proposée en cas de difficultés à maintenir ce seuil malgré la supplémentation orale.
Les déficits en calcium et vitamine D peuvent être précocement détectés via une élévation de la parathormone (PTH), la calcémie corrigée restant souvent dans les valeurs normales pendant longtemps. La mesure de la calciurie des 24 h permet aussi de s’assurer que les apports sont suffisants. La principale complication en cas d’apports insuffisants et de déséquilibre phosphocalcique est la survenue d’une ostéoporose accélérée. Le risque fracturaire est significativement augmenté 2 ans après chirurgie bariatrique, les montages hautement malabsorptifs étant les plus à risque (25).
Autres vitamines
Hormis la vitamine A en cas de DBP, un déficit, voire une carence, en vitamines liposolubles reste relativement rare. L’ESPEN recommande (26), en présence d’un déficit en vitamines liposolubles, de rechercher la présence d’une insuffisance pancréatique exocrine fonctionnelle, voire de mettre en place des extraits pancréatiques en cas de persistance malgré la supplémentation, y compris si l’élastase n’est pas significativement abaissée.
Bien que rares, des déficits en vitamine C ont été retrouvés chez des patients post-bariatriques, en lien avec la malabsorption et une alimentation déséquilibrée. Les signes cliniques étant multiples, principalement cutanés, il ne faut pas hésiter à débuter une supplémentation en cas de suspicion clinique, dans l’attente des résultats du dosage spécifique. Il est à noter que le dosage de la vitamine C n’est pas remboursé, mais que la supplémentation est relativement abordable et doit être réalisée sans nécessité de dosage préalable en cas de suspicion clinique d’après les recommandations HAS de 2018 sur le sujet.
Éléments-trace
Le zinc, le cuivre et le sélénium sont abondants dans l’alimentation et relativement bien absorbés au niveau du jéjunum. Il faut penser à une carence en cuivre en cas d’anémie inexpliquée, et au zinc en cas d’anomalies cutanées, de dysgueusie ou de troubles de la cicatrisation. Les formes sévères sont toutefois rares. Dans une cohorte de 110 patients ayant subi une chirurgie bariatrique de type SG modifiée, le taux de zinc a significativement chuté malgré une supplémentation par multi-vitamines, mais la correction a pu être obtenue via une supplémentation orale (27). L’absorption du cuivre et du zinc étant compétitives au niveau intestinal (le 2e diminuant l’absorption du premier), une supplémentation en zinc peut révéler ou aggraver un déficit en cuivre. En cas de supplémentation combinée, il faudra veiller à espacer les prises de chaque élément d’environ 4 heures. Enfin, les taux de sélénium doivent aussi être monitorés car un déficit chronique peut être à l’origine de dysfonction cardiaque ou de troubles du métabolisme osseux.
Le tableau 2 résume les principaux déficits en micronutriments et leur surveillance en fonction de la chirurgie réalisée.
Tableau 2 : Suivi clinique et biologique selon le type de chirurgie
| Sleeve gastrectomie | By-pass gastrique | Dérivation biliopancréatique |
| Clinique* | x | x | x |
| Bilan biologique minimal ** | x | x | x |
| Ferritine *** | x | x | x |
| Vitamine B9 | x | x | x |
| Vitamine B12 | x | x | x |
| PTH | x | x | x |
| 25-OH vitamine D | x | x | x |
| Vitamine B1 | selon contexte | x | x |
| Zinc/Cuivre | optionnel | x | x |
| Sélénium | si symptômes | optionnel | x |
| Vitamine A | si symptômes | si symptômes | x |
| Vitamine E/K | si symptômes | si symptômes | si symptômes |
| Bilan urinaire des 24h (oxalates,calcium) | optionnel | optionnel | x |
| Ostéodensitométrie | À 2 ans, puis selon résultats |
*Clinique : Poids, % âge de perte de poids, activité physique, présence de symptômes
**Bilan biologique minimal : NFS, glycémie ionogramme sanguin, urée, créatininémie, albumine, bilan hépatique, Ca, Mg
***Ferritine : à compléter par un fer sérique et coefficient de saturation de la transferrine si besoin
Autres complications nutritionnelles
Hypoglycémie-hyper-insulinique
Après by-pass gastrique, il existe une amélioration significative, voire une résolution du diabète. Cela résulte de la modification de la sécrétion des entéro-hormones gastro-intestinales, de la diminution de la résistance à l’insuline, +/- associée à une majoration de sa sécrétion. Le corollaire est la survenue de phénomènes d’hypoglycémies-hyper-insuliniques, communément appelés « dumping tardif ». Il touche entre 1 et 10 % des patients opérés, selon la méthode diagnostique (28, 29). Elle est plus rare mais également plus sévère que le dumping précoce, lié à l’afflux précoce du bol alimentaire hyperosmolaire au niveau du jéjunum. Elle survient en général 90-120 min après le repas, mais peut être encore plus tardive. Son diagnostic peut être fait par différentes méthodes (monitoring du glucose en continu, test de provocation orale, mixed meal test…). Sa prise en charge est multimodale mais repose sur les conseils diététiques en 1re intention. En cas d’efficacité incomplète, des options thérapeutiques existent comme l’acarbose, le diazoxide ou les analogues de la somatostatine mais avec des effets secondaires non négligeables et une efficacité variable (30). Dans les cas réfractaires, avec un impact très significatif dans la vie quotidienne et/ou une mise en danger, une chirurgie de révision peut être discutée.
Hyperoxalurie entérique
La lithiase oxalique est la complication rénale principale après chirurgie bariatrique. Sa fréquence de survenue est augmentée en cas d’antécédent lithiasique, d’âge élevé, et en fonction du type de chirurgie (les procédures les plus malabsorptives étant, comme toujours les plus à risque) (31). À l’état physiologique, une grande partie des oxalates ingérés via l’alimentation est chélatée par le calcium alimentaire, conduisant à la formation de complexes insolubles éliminés dans les selles. En cas de malabsorption chronique, l’afflux d’acides gras au niveau colique va augmenter la séquestration du calcium via un mécanisme de saponification, laissant libre une grande quantité de sels d’oxalates très solubles et facilement absorbés à travers la muqueuse. Cet afflux d’oxalates au niveau sanguin va entraîner une augmentation de leur excrétion urinaire, et donc la formation de cristaux d’oxalates de calcium au niveau tubulaire. D’autres phénomènes peuvent aggraver cette surconcentration urinaire en oxalates, comme une baisse de la diurèse (secondaire aux diarrhées), une hypocitraturie ou une hypomagnésémie.
L’hyperoxalurie doit être prise en charge pour éviter la survenue au long cours d’une insuffisance rénale chronique (souvent secondaire à des épisodes lithiasiques répétés, mais aussi plus rarement à une néphropathie à l’oxalate, fruit d’une toxicité directe). Sa prise en charge repose sur des conseils diététiques via la limitation des aliments riches en oxalates et une augmentation des apports calciques, une hydratation abondante avec un objectif de diurèse d’au moins 2l/j. En cas de besoin, une supplémentation calcique pouvant aller jusqu’à 3 000 mg/j peut être prescrite, à prendre au moment des repas pour plus d’efficacité.
Suivi et supplémentations
Le suivi après chirurgie bariatrique doit être multidisciplinaire, incluant chirurgiens, endocrinologues, diététiciens et gastroentérologues, et devrait être poursuivi durant toute la vie, de préférence en centre spécialisé pour les chirurgies très malabsorptives. Cependant, étant donné le nombre élevé de patients perdus de vue au fil des ans, et l’augmentation notable du nombre de patients opérés, tout médecin de premier recours devrait connaître les principes généraux de surveillance ainsi que les complications tardives après chirurgie bariatrique.
Les recommandations de l’HAS de 2009 préconisaient une supplémentation systématique uniquement après chirurgie hautement malabsorptive (BPG et DBP) mais toutes les guidelines plus récentes l’incluent aussi après SG, au moins pendant la 1re année, voire de façon plus prolongée au vu de la présence de déficit à distance de l’intervention, surtout si l’alimentation reste déséquilibrée. Celles des sociétés américaines datant de 2019 (32) françaises de 2021 (15) et européennes de 2023 (26) ont été synthétisées dans le tableau 2 ci-contre.
Après intervention, il est admis qu’un suivi clinique et biologique rapproché doit être mené à 3,6 et 12 mois post-opératoires, puis annuellement (ou biannuel pour la DBP). Bien que leur carence puisse survenir après tout type de chirurgie, le dosage systématique de certains micronutriments (tels le zinc et le cuivre) est réservé au suivi post BPG et DBP.
Conclusion
Les chirurgies à visée de réduction pondérale sont des traitements efficaces de l’obésité et des complications métaboliques associées. Cependant, la modification définitive de l’anatomie digestive qu’elles entraînent induit des modifications physiologiques à long terme et imposent un suivi à vie. Plus la chirurgie est malabsorptive, plus le risque de complications nutritionnelles et de déficits en micronutriments est élevé. Au vu de l’augmentation du nombre de patients opérés, il est important que le plus de praticiens possible soient sensibilisés et formés au dépistage et au suivi de ces complications nutritionnelles.
Bibliographie
- Fontbonne A, Currie A, Tounian P, Picot MC, Foulatier O, Nedelcu M, et Prevalence of Overweight and Obesity in France: The 2020 Obepi-Roche Study by the « Ligue Contre l’Obésité ». J Clin Med. 25 janv 2023;12(3):925.
- Obésite – prise en charge chirurgicale chez l’adulte – 2009;
- Lazzati Épidémiologie de la prise en charge chirurgicale de l’obésité. J Chir Viscérale. 1 avr 2023;160(2, Supplement):S3-7.
- Xu HC, Pang YC, Chen JW, Cao JY, Sheng Z, Yuan JH, et Systematic Review and Meta-analysis of the Change in Ghrelin Levels After Roux-en-Y Gastric Bypass. Obes Surg. avr 2019;29(4):1343-51.
- Dirksen C, Jørgensen NB, Bojsen-Møller KN, Kielgast U, Jacobsen SH, Clausen TR, et al. Gut hormones, early dumping and resting energy expenditure in patients with good and poor weight loss response after Roux-en-Y gastric bypass. Int J Obes 2005. nov 2013;37(11):1452-9.
- Elias K, Webb DL, Diaz Tartera HO, Hellström PM, Sundbom M. Impact of biliopancreatic diversion with duodenal switch on glucose homeostasis and gut hormones and their correlations with Surg Obes Relat Dis Off J Am Soc Bariatr Surg. déc 2022;18(12):1392-8.
- Brown RM, Guerrero-Hreins E, Brown WA, le Roux CW, Sumithran Potential gut–brain mechanisms behind adverse mental health outcomes of bariatric surgery. Nat Rev Endocrinol. sept 2021;17(9):549-59.
- Meek CL, Lewis HB, Reimann F, Gribble FM, Park The effect of bariatric surgery on gastrointestinal and pancreatic peptide hormones. Peptides. mars 2016;77:28-37.
- Kohli R, Bradley D, Setchell KD, Eagon JC, Abumrad N, Klein Weight Loss Induced by Roux-en-Y Gastric Bypass But Not Laparoscopic Adjustable Gastric Banding Increases Circulating Bile Acids. J Clin Endocrinol Metab. avr 2013;98(4):E708-12.
- Aron-Wisnewsky J, Doré J, Clement Modifications de la flore intestinale après chirurgie bariatrique : état des connaissances et mécanismes impliqués. 2012;
- Tremaroli V, Karlsson F, Werling M, Ståhlman M, Kovatcheva-Datchary P, Olbers T, et Roux-en-Y Gastric Bypass and Vertical Banded Gastroplasty Induce Long-Term Changes on the Human Gut Microbiome Contributing to Fat Mass Regulation. Cell Metab. 4 août 2015;22(2):228-38.
- Nuijten MAH, Eijsvogels TMH, Monpellier VM, Janssen IMC, Hazebroek EJ, Hopman The magnitude and progress of lean body mass, fat-free mass, and skeletal muscle mass loss following bariatric surgery: A systematic review and meta-analysis. Obes Rev. 2022;23(1):e13370.
- Voican CS, Lebrun A, Maitre S, Lainas P, Lamouri K, Njike-Nakseu M, et al. Predictive score of sarcopenia occurrence one year after bariatric surgery in severely obese patients. PLOS ONE. 14 mai 2018;13(5):e0197248.
- Schollenberger AE, Karschin J, Meile T, Küper MA, Königsrainer A, Bischoff Impact of protein supplementation after bariatric surgery: A randomized controlled double-blind pilot study. Nutr Burbank Los Angel Cty Calif. févr 2016;32(2):186-92.
- Quilliot D, Coupaye M, Ciangura C, Czernichow S, Sallé A, Gaborit B, et Recommendations for nutritional care after bariatric surgery: Recommendations for best practice and SOFFCO-MM/AFERO/SFNCM/expert consensus. J Visc Surg. févr 2021;158(1):51-61.
- Roust LR, DiBaise Nutrient deficiencies prior to bariatric surgery. Curr Opin Clin Nutr Metab Care. mars 2017;20(2):138.
- Kikkas EM, Sillakivi T, Suumann J, Kirsimägi Ü, Tikk T, Värk Five-Year Outcome of Laparoscopic Sleeve Gastrectomy, Resolution of Comorbidities, and Risk for Cumulative Nutritional Deficiencies. Scand J Surg. 1 mars 2019;108(1):10-6.
- Puzziferri N, Roshek TB III, Mayo HG, Gallagher R, Belle SH, Livingston Long-term Follow-up After Bariatric Surgery: A Systematic Review. JAMA. 3 sept 2014;312(9):934-42.
- Steenackers N, Schueren BV der, Mertens A, Lannoo M, Grauwet T, Augustijns P, et Iron deficiency after bariatric surgery: what is the real problem? Proc Nutr Soc. nov 2018;77(4):445-55.
- Risstad H, Søvik TT, Engström M, Aasheim ET, Fagerland MW, Olsén MF, et al. Five-year outcomes after laparoscopic gastric bypass and laparoscopic duodenal switch in patients with body mass index of 50 to 60: a randomized clinical trial. JAMA avr 2015;150(4):352-61.
- Aasheim Wernicke encephalopathy after bariatric surgery: a systematic review. Ann Surg. nov 2008;248(5):714-20.
- Kröll D, Laimer M, Borbély YM, Laederach K, Candinas D, Nett Wernicke Encephalopathy: a Future Problem Even After Sleeve Gastrectomy? A Systematic Literature Review. Obes Surg. janv 2016;26(1):205-12.
- Giustina A, di Filippo L, Facciorusso A, Adler RA, Binkley N, Bollerslev J, et Vitamin D status and supplementation before and after Bariatric Surgery: Recommendations based on a systematic review and meta-analysis. Rev Endocr Metab Disord. 4 sept 2023.
- Favre L, Ferrario C, Mantziari S, Suter Recommandations de suivi des carences nutritionnelles après chirurgie bariatrique. Rev Med Suisse. 20 mars 2019;643:626-30.
- Lu CW, Chang YK, Chang HH, Kuo CS, Huang CT, Hsu CC, et al. Fracture Risk After Bariatric Surgery: A 12-Year Nationwide Cohort Medicine (Baltimore). déc 2015;94(48):e2087.
- Bischoff SC, Ockenga J, Eshraghian A, Barazzoni R, Busetto L, Campmans-Kuijpers M, et Practical guideline on obesity care in patients with gastrointestinal and liver diseases – Joint ESPEN/UEG guideline. Clin Nutr. juin 2023;42(6):987-1024.
- Hassn A, Luhmann A, Rahmani S, Morris-Stiff Medium-Term Results of Combined Laparoscopic Sleeve Gastrectomy and Modified Jejuno-Ileal Bypass in Bariatric Surgery. Obes Surg. oct 2016;26(10):2316-23.
- Raverdy V, Baud G, Pigeyre M, Verkindt H, Torres F, Preda C, et Incidence and Predictive Factors of Postprandial Hyperinsulinemic Hypoglycemia After Roux-en-Y Gastric Bypass: A Five year Longitudinal Study. Ann Surg. nov 2016;264(5):878-85.
- Favre L, Giusti Gestion des hypoglycémies après le bypass gastrique. Rev Med Suisse. 30 mars 2011;288:706-10.
- Øhrstrøm CC, Worm D, Hansen Postprandial hyperinsulinemic hypoglycemia after Roux-en-Y gastric bypass: an update. Surg Obes Relat Dis. 1 févr 2017;13(2):345-51.
- Bhatti UH, Duffy AJ, Roberts KE, Shariff Nephrolithiasis after bariatric surgery: A review of pathophysiologic mechanisms and procedural risk. Int J Surg. 1 déc 2016;36:618-23.
- Mechanick JI, Apovian C, Brethauer S, Garvey WT, Joffe AM, Kim J, et Clinical Practice Guidelines For The Perioperative Nutrition, Metabolic, and Nonsurgical Support of Patients Undergoing Bariatric Procedures – 2019 Update.Endocr Pract. 1 déc 2019;25:1-75.