Liens d’intérêt
Abbvie, Astellas, Gilead, Sandoz
Mots-clés
Transplantation hépatique ; Hépatite fulminante ; Cirrhose
Introduction
Les indications de la transplantation hépatique (TH) ont considérablement évolué en quelques années (1). Poser l’indication d’une TH est souvent complexe puisque deux aspects entrent en ligne de compte au moment de la décision. Le premier aspect est le bénéfice individuel pour le patient, en termes de survie globale mais également de qualité de vie. Cet aspect respecte une logique habituelle aux décisions médicales. Le deuxième aspect est sociétal, particulier à l’univers de la TH puisque, compte tenu de la pénurie d’organes, seul un patient dont la survie globale à 5 ans est estimée entre 60 % et 70 % est candidat à la TH.
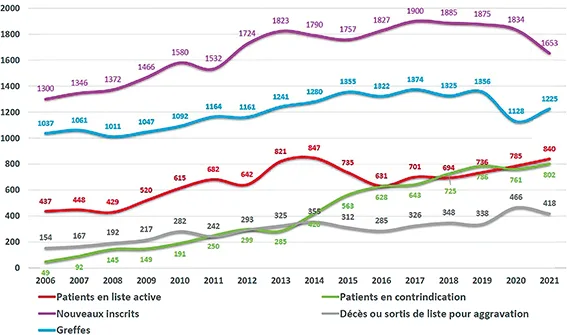
En France, un peu plus de 1 200 TH ont été réalisées en 2021, chiffre en diminution depuis la pandémie de Sars-CoV-2 (figure 1). On estime qu’il y a un seul donneur pour plus de deux receveurs. Face à ce constat, la sélection des candidats à la TH obéit à une obligation de résultats.

Figure 1 : Évolution de l’activité de transplantation hépatique en France de 2006 à 2021
Source : Rapport annuel du groupe technique Foie de l’Agence de Biomédecine
Si les deux indications les plus fréquentes sont le carcinome hépato-cellulaire et la cirrhose grave décompensée, il existe de nombreuses autres indications que l’hépato-gastro-entérologue doit connaître.
Chaque centre de TH valide l’indication et l’absence de contre-indication et est responsable de l’inscription d’un patient. L’accès à la TH se fait en fonction du score national Foie qui détermine la position sur la liste, tenue par l’Agence de Biomédecine (ABM) qui encadre l’activité nationale de prélèvement et de transplantation.
Quand adresser un patient ayant une cirrhose ?
Une TH doit être envisagée pour tous patients dont le pronostic vital est engagé dans l’année sans transplantation, ou s’il existe une atteinte majeure de sa qualité de vie. Une indication de TH peut être posée en cas d’insuffisance hépatocellulaire sévère ou en cas de complications graves malgré une prise en charge adaptée et maximale.
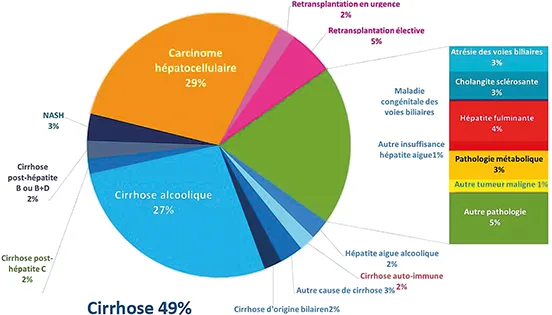
Quelle que soit la cause de la cirrhose, la TH n’est envisagée que si les complications de l’insuffisance hépato-cellulaire et/ ou de l’hypertension portale ne peuvent être contrôlées par d’autres traitements. La cirrhose grave ou décompensée représente 49 % des indications de TH en 2021 (figure 2).

Figure 2 : Indications de transplantation hépatique en France en 2021
Source: Rapport annuel du groupe technique Foie de l’Agence de Biomédecine
Établir le pronostic de la cirrhose et poser l’indication de TH
Si certaines indications comme l’ascite réfractaire sont bien connues, il est parfois difficile pour le clinicien de poser l’indication en cas d’insuffisance hépatique. Cependant, l’apparition et la persistance d’un ictère, la baisse du taux de prothrombine en dessous de 50 % (ou un INR (International Normalized Ratio) > 1,5) à distance de toute décompensation infectieuse ou hémorragique doivent faire considérer la TH. La cinétique de l’évolution est une information importante dans la prise de décision. Si l’aggravation est rapide sans espoir de réversibilité après traitement de la cause, les patients doivent être adressés sans délai à un centre de TH.
Le score de Child-Pugh est un score largement validé et simple d’utilisation. Bien que comprenant deux variables subjectives, c’est un score souvent utilisé pour prédire la survie des patients cirrhotiques. Un patient ayant une cirrhose classée Child-Pugh C est un candidat potentiel à la TH.
Depuis plus de quinze ans, ce score est supplanté par le score de MELD (Model for End Stage Liver Disease) pour poser l’indication de TH et définir l’accès à la TH. C’est un score composite comprenant des variables objectives : la créatinine, la bilirubine et l’INR. Le score de MELD a été développé initialement pour déterminer le pronostic à court terme des patients candidats à un TIPS (shunt intrahépatique porto-systémique par voie transjugulaire) (2,3). Il s’est avéré être un score pronostique puissant de la mortalité à court terme. Les patients ayant un score de MELD ≤ 14 ont une mortalité liée à la TH supérieure à la mortalité liée à leur cirrhose à un an (4) Par conséquent, seuls les patients ayant un score de MELD supérieur ou égal à 15 sont candidats à la TH. Les variables utilisées dans ce score composite peuvent être soumises à variation interindividuelle ou modifiées par des traitements, notamment la créatininémie par les diurétiques et l’INR par la prise d’anticoagulants. Aussi, le MELD est un outil moins performant pour prédire la mortalité à moyen et long terme. Pour pallier cette limite, plusieurs scores dérivés ont été proposés dans la littérature en prenant en compte par exemple la natrémie (MELD-Na) ou encore l’albuminémie (MELD 3.0) (5,6). Un rapport récent de la base de données américaines UNOS (United Network for Organ Sharing) qui comprenait 44 388 patients inscrits sur liste de TH a révélé une augmentation de 30 % des taux de mortalité ou de retrait de liste pour aggravation chez les femmes par rapport aux hommes, après la mise en place du score de MELD (7). Ce déséquilibre entre les sexes pourrait s’expliquer par des concentrations sériques de créatinine plus faibles chez les femmes que chez les hommes, qui ne reflètent pas leur véritable fonction rénale. Une publication récente propose un nouveau score, le modèle d’équité entre les sexes pour l’allocation hépatique dit GEMA, en remplaçant la créatinine sérique par une estimation du débit de filtration glomérulaire développé pour
le cirrhotique dans les équations du MELD et du MELD-Na, et en réajustant leurs composantes. Dans cette étude, 12 à 15 % des patients seraient priorisés différemment, principalement des femmes (8).
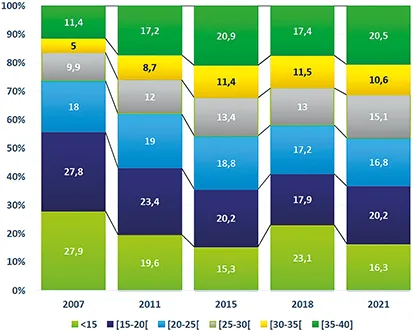
Jusqu’en 2007, la position du patient sur liste d’attente de TH dépendait du temps d’attente. Actuellement, l’attribution des greffons se fait grâce à au score de MELD et sans tenir compte du temps d’attente sur liste pour les patients ayant une cirrhose isolée. Son utilisation a conduit pour la première fois dans l’histoire de la TH à une réduction de la mortalité sur liste d’attente en priorisant les patients les plus graves. Plus le score de MELD est élevé (capé à 40), plus l’accès à la transplantation est rapide car le MELD est le principal composant du score national Foie. Mais le système d’allocation actuel, basé sur le MELD s’essouffle et il devient difficile de transplanter des patients ayant des scores de MELD entre 20 et 30, bien que l’indication de TH soit formelle. En effet, les patients ayant un score de MELD ≥ 30 représentaient 16,4 % des inscrits en 2007 contre 31,1 % en 2021 (figure 3). Une réflexion sur l’évolution de notre système d’allocation devrait être menée dans les prochains mois.

Figure 3 : Évolution du score de MELD à l’inscription des patients
ayant une cirrhose isolée
Source : Rapport annuel du groupe technique Foie de l’Agence de Biomédecine
Les exceptions au MELD
Si le score de MELD est un bon prédicteur de la mortalité à court terme, il ne prend pas en compte certaines complications de la maladie hépatique qui menacent le pronostic vital des patients comme l’hémorragie digestive, l’ascite ou l’hydrothorax réfractaire ou incontrôlée, le syndrome hépatopulmonaire ou encore l’angiocholite à répétition (9). Or, ces complications, communément qualifiées d’exception au MELD, peuvent survenir alors même que le score de MELD est bas, voire inférieur à 15 (tableau 1). L’indication à la TH repose sur l’absence d’autre possibilitéthérapeutique, médicamenteuse ou TIPS pour certaines.
L’accès à la transplantation se fait grâce à l’attribution de points supplémentaires après acceptation de deux experts auprès de l’ABM, pour faire concurrence au MELD élevé. En 2021, 62 % et 84 % des patients ayant une indication de TH via cette composante avaient un MELD < 15 ou < 20, respectivement. Les experts déterminent en fonction de l’indication et du cas présenté, le nombre de points attribués, 650 ou 800 points sur les 1 000 maximum du score national Foie et le délai pour obtenir ces points, immédiatement (appelé J0), à 3 mois ou 6 mois. Une réévaluation des critères permettant d’obtenir cette composante a été menée en 2022 sous l’égide des sociétés savantes AFEF et ACHBT et en cours de finalisation. En effet, le nombre de demande d’expertise est en augmentation constante, témoignant de l’insuffisance du seul MELD pour permettre l’accès à la TH et représente environ un tiers des candidats.
| Indications | Conditions | Délais accordés |
|---|
| Ascite réfractaire | MELD < 15
Et Natrémie < 130 mmol/L et/ou âge > 60 ans et/ou TIPS
contre-indiqué et/ou infection du liquide d’ascite | 6 mois |
| Hydrothorax hypoxémiant | 3 mois |
| Encéphalopathie hépatique | MELD < 15
Et au moins un épisode de grade 3 ou 4 et hospitalisation
prolongée ou répétée | 6 mois |
| Signes focaux ou syndrome extra-pyramidal | 3 mois |
| Hémorragies digestives récidivantes | MELD < 15
Et échec des autres traitements | Avis d’expert au cas par cas |
| Hypertension porto-pulmonaire | | Avis d’expert au cas par cas |
| Syndrome hépato-pulmonaire | PaO2<60mmHg | 3 mois |
| Prurit réfractaire | Echec des traitements médicamenteux (anti-histaminiques,
rifampicine, sertraline) et/ou épuration extra-hépatique | Avis d’expert au cas par cas |
| Angiocholites récidivantes | Atteinte biliaire non accessible à un traitement conservateur
et au moins 2 épisodes de bactériémies documentées en 6
mois et/ou un épisode de sepsis sévère (abcès, endocardite,
ostéomyélite, méningite) | 6 mois |
Episode de choc septique, infection à germes multirésistants
ou retransplantation | 0 mois |
| Carcinome hépatocellulaire | MELD < 15, score AFP ≤ 2
Plus d’un nodule ou tumeur > 2cm avec traitement d’attente
contre-indiqué | 9 mois |
| Cholangiocarcinome hilaire | Après traitement néoadjuvant et laparotomie éliminant une
tumeur résiduelle | 0 mois |
| Hémangioendothéliome épithélioïde | | Avis d’expert au cas par cas |
Métastases hépatiques de tumeur
endocrine | | Avis d’expert au cas par cas |
| Polykystose hépatique | Ascite et/ou restriction alimentaire sans dénutrition objective | 6 mois |
| Dénutrition objective | 3 mois | |
| Maladie de rendu-Osler | Insuffisance cardiaque droite à haut débit (augmentation
des pressions de remplissage et/ou Pcap>15mmHg et
PAPd>25mmHg) | 3 mois |
Lésions biliaires ischémiques diffuses responsables
d’angiocholites ou d’abcès hépatiques | 0 mois |
| Neuropathie amyloïde | Atteinte sensitive isolée | 12 mois |
| Atteinte motrice et/ou dysautonomie associée | 6 mois |
Atteinte motrice d’évolution rapide (marche avec une canne)
et/ou atteinte digestive avec dénutrition et altération de l’état
général | 3 mois |
Tableau 1 : Exceptions au score MELD
MELD élevé et ACLF
L’attribution prioritaires des greffons selon le score MELD a conduit à la TH de patients ayant des maladies de plus en plus sévères. La proportion de candidats ayant un MELD au-delà de 35, est passée de 11 % en 2007 à 20 % en 2021 en France (figure 3). Les patients qui ont les scores MELD les plus élevés sont ceux qui tirent le plus grand bénéfice de la TH et cette stratégie a permis de diminuer le risque de décès en attente de TH, sans pour autant altérer les résultats de la TH. Cependant, le bénéfice est moins certains pour les scores MELD les plus élevés (au-delà de 40) ou lorsqu’il existe d’autres défaillances d’organes. L’ACLF (Acute-on-Chronic Liver Failure) est une entité définie par une dégradation très brutale de la fonction hépatique ne s’accompagnant pas obligatoirement d’une augmentation du score MELD et associée à une défaillance multiviscérale. Elle est classée en trois stades de sévérité croissante selon le nombre et le type de défaillance d’organes calculés par le CLIF-SOFA, variante du score pronostique SOFA dont les variables habituelles ont été remplacées pour tenir compte de l’atteinte hépatique. Cette nouvelle nomenclature a permis de mieux définir le pronostic de ces classes qui étaient avant cela regroupées dans les études. L’influence de l’ACLF sur les résultats de la TH est de plus en plus étudiée, en particulier pour les patients les plus graves ayant une ACLF de grade 3. Même si les données sont contrastées, un certain nombre de patients transplantés au stade d’une ACLF 3 ont un pronostic similaire aux patients transplantés sans ACLF (10). Cela nécessite une prise en charge experte et de bien établir la fenêtre de transplantabilité de ces patients, en particulier bien évaluer l’atteinte pulmonaire et le risque infectieux (11).
Malgré ces résultats, l’accès à la TH pour ces patients, le plus souvent en réanimation, est inégal (12). Plusieurs études s’intéressent à la sélection des candidats en ACLF 3 sans qu’un consensus soit clairement établi.
Indications selon la cause
L’indication de TH est à poser au moment le plus propice afin de limiter les greffes en excès lorsqu’une amélioration est possible tout en limitant le risque de décès sans TH. L’histoire naturelle des hépatopathies chroniques est différente selon chaque étiologie. Ainsi, lorsqu’un patient est admis pour une première décompensation, l’attitude sera de proposer d’emblée une TH ou d’attendre selon la possibilité de contrôle de la cause.
Les indications selon la cause de l’hépatopathie chronique évoluent dans le temps. Si la cirrhose liée à l’alcool demeure la première cause de TH en France (27 % des indications en 2021), certaines indications sont en net recul comme les hépatites virales, en particulier l’hépatite virale C grâce aux traitement antiviraux directs, et d’autres émergent comme l’hépatite alcoolique (HA) ou la stéatohépatite métabolique.
Alcool
Les patients ayant une maladie du foie liée à l’alcool et candidats à la TH ont souvent accès à la TH grâce à un score MELD élevé. L’arrêt durable de la consommation d’alcool est indispensable, mais reste un sujet de controverse. L’argument médical est de loin le plus robuste : l’abstinence permet une amélioration des fonctions hépatiques, qui se produit principalement dans les 3 premiers mois. À la fameuse mais controversée « règle des six mois », on préfère dorénavant une évaluation psycho-sociale, adossée à une évaluation addictologique. En effet, le niveau de preuve de cette règle des six mois comme seul critère prédictif de la rechute est faible (13). Cette évaluation vise à écarter les rechuteurs massifs qui, dans les études récentes, ont une mortalité augmentée, par maladies cardio-vasculaires, néoplasies ou pathologies du greffon.
Un cas particulier est celui de l’HA. Les travaux français, menés par l’équipe de Lille, ont permis de définir une catégorie de patients à haut risque de mortalité précoce et de positionner la TH dans leur prise en charge (14). Ainsi, les patients ayant un échec au traitement médical dont les corticoïdes (défini par un score de Lille ≤ 0,45) doivent être évalués selon les critères suivants : consensus du personnel paramédical et médical et notamment des addictologues en faveur du projet de transplantation, absence de comorbidité, intégration sociale et soutien familial. Si le bénéfice en termes de survie est indiscutable, une étude récente comparative entre les patients transplantés dans cette indication et des patients cirrhotiques sevrés depuis plus de 6 mois a montré un risque de rechute massive plus importante dans le groupe HA à deux ans (15).
Malgré cela, il existe encore une opinion publique plutôt défavorable à prioriser ces patients ayant une maladie auto-infligée, qui engendre une réticence à ce programme y compris parmi les soignants. Finalement, le nombre de patients transplantés pour HA reste faible même s’il augmente, passant de 20 (1,1 %) en 2018 à 41 (2,5 %) en 2021. Le renforcement du suivi addictologique pré et post transplantation est une clef de la réussite chez ces patients.
Virus
Les hépatites virales B ou C représentent chacune 2 % de l’activité de TH en 2021. Il faut rappeler qu’avant les antiviraux directs traitant
l’hépatite C, cette indication représentait près de 20 % des indications en France. En cas d’hépatite B ou C chronique, l’indication doit être posée si des critères de TH existent alors que le candidat est contrôlé sur le plan virologique par antiviral B ou guéri de l’hépatite C.
Il est parfois difficile de poser l’indication du traitement antiviral lorsque l’infection est découverte au stade de cirrhose grave. Un traitement antiviral B doit toujours être prescrit quelle que soit la gravité de la cirrhose et permet une amélioration de certains patients et aussi de diminuer la charge virale avant la TH pour limiter le risque de récidive (16). Le traitement de l’hépatite C doit être décidé en réunion de concertation
pluridisciplinaire et avec le centre de TH. Chez les patients ayant un score de MELD > 20, le bénéfice du traitement avant TH est incertain compte tenu d’améliorations partielles qui desservent les patients en termes d’accès à la TH, d’effets indésirables rares mais graves, plus fréquents dans cette population. À l’exception de ces patients, la tendance actuelle est de traiter et guérir l’hépatite C avant la TH pour éviter la récidive sur le greffon (16).
L’accès à la TH de ces patients peut être facilité par l’acceptation de greffons dérogatoires avec des résultats similaires aux autres greffons. Les donneurs ayant une sérologie anti-HBc+ peuvent être attribués à tout receveur mais ceux ayant un antigène HBs positif avant la greffe sont à privilégier puisqu’ils devront recevoir un traitement préventif de la récidive virale B. Les greffons de donneurs ayant une sérologie positive pour l’hépatite C ne peuvent être attribués qu’aux receveurs ayant une sérologie également positive et qui ont consenti. Certains pays acceptent que ces greffons soient attribués à tout receveur mais la loi en France l’interdit même si un groupe de réflexion à l’ABM va émettre des recommandations pour faire évoluer cette réglementation.
Maladies auto-immunes
Les maladies auto-immunes représentent un groupe d’indications rares de TH. En 2021, la cholangite sclérosante primitive, l’hépatite auto-immune
(HAI) et la cholangite biliaire primitive représentaient respectivement 3 %, 2 % et 1 % de l’activité de TH.
Pour les maladies cholestatiques, des critères propres existent et la majorité des patients sont transplantés pour des exceptions au MELD (angiocholites, prurit réfractaire). Une bilirubine ≥ 100 µmol/L est un critère de TH mais tout patient ne répondant pas au traitement médical devrait être adressé au centre de TH pour évaluation.
Pour l’HAI parvenue aux stades de cirrhose, il n’y a pas de critère spécifique si le traitement immunosuppresseur est un échec. Il doit cependant être tenté. Seules les formes aiguës ou subaiguës constituent une exception. Les corticoïdes sont controversés dans les formes les plus sévères, d’emblée fulminante. Dans un travail multicentrique français, SURFASA, un score a été établi pour prédire la réponse des patients ayant une forme d’emblée sévère traités par corticoïdes tenant compte de l’INR, de la bilirubine et de l’évolution sous traitement (17). Ce score devrait être validé prochainement dans un travail prospectif multicentrique français.
Stéatohépatite métabolique
La stéatohépatite métabolique isolée est une indication très minoritaire en France, contrairement à d’autres pays occidentaux comme les États- Unis. Cette indication est enregistrée dans le thésaurus de l’ABM depuis 2018. En 2021, elle représentait seulement 3,3 % de l’activité de TH. En revanche, 25 % des inscrits ont une stéatohépatite métabolique, associée à une autre maladie hépatique (carcinome hépatocellulaire, cirrhose liée à l’alcool). Ce chiffre est en augmentation et 13 % des inscrits en 2021 avaient une stéatohépatite métabolique.
Il n’y a pas de particularité pour poser l’indication de transplantation dans cette indication mais les possibilités thérapeutiques pour améliorer la maladie en attente de TH sont quasi-nulles, au stade de cirrhose grave. La chirurgie bariatrique doit être proposée lorsqu’elle est indiquée et possible mais l’hypertension portale et/ ou l’insuffisance hépato-cellulaire la contre-indique le plus souvent en attente de TH (18). Cependant, elle doit être proposée après TH, pour éviter la récidive de la maladie initiale sur le greffon.
Quand adresser un patient ayant une tumeur hépatique ?
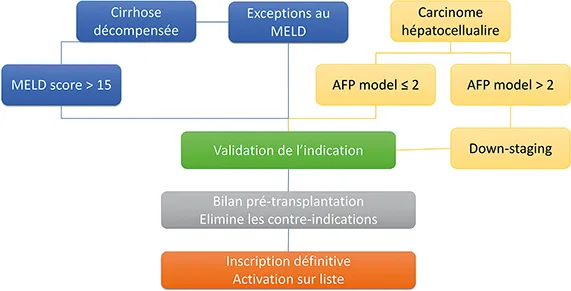
Le carcinome hépatocellulaire
La TH demeure un traitement de choix du CHC puisqu’elle permet une prise en charge curative sur le plan oncologique mais également concernant la cirrhose sous-jacente. Si un candidat peut bénéficier en première intention d’un traitement curatif autre que la TH (résection ou thermo-ablation), celui-ci doit être privilégié pour réaffecter des greffons à d’autres indications plus prioritaires. Ainsi, un nodule unique de moins de 1 cm ne constitue pas à lui une indication de TH.
Il existe cependant des limites liées au risque de récidive sur le greffon. C’est pourquoi, les règles de transplantabilité en cas de CHC sont guidées par la nécessité d’obtenir une survie à 5 ans identique aux patients transplantés pour d’autres indications ainsi qu’un taux de récidive inférieur à 15 %.
Plusieurs critères de transplantation pour CHC ont été établis au cours du temps, dont les critères de Milan qui restent les critères les plus utilisés dans le monde. En France, depuis 2013, la sélection des patients est faite grâce au score alphafœtoprotéine (AFP) qui regroupe le nombre de nodule, leur taille et le taux d’alphafœtoprotéine (tableau 2). Les patients ayant un score AFP ≤ 2 sont à faible risque de récidive de CHC associée à une survie de 70 % à 5 ans de la TH. En revanche, les patients ayant un score supérieur à 2 ont un risque de récidive de 51 % à 5 ans associée à une survie globale d’environ 48 % à 5 ans (19) C’est pourquoi seuls les patients atteints d’un CHC avec un score AFP ≤ 2 peuvent être candidats à une TH. Le score AFP a été validé dans une cohorte sud-américaine et une cohorte italienne de plus de 500 patients (20,21).
Les patients ayant initialement un score AFP > 2 peuvent devenir éligibles à une TH en cas d’efficacité d’un traitement d’attente (down-staging en anglais) qui permettrait un score AFP ≤ 2 après traitement et maintenu pendant 3 mois.
L’accès à la TH des patients inscrits pour CHC a été revu en 2015 afin de prioriser les patients les plus malades dans les bonnes indications et de retarder l’accès à la TH des patients qui ont des tumeurs contrôlées par un traitement à visée curative. Ainsi, pour un CHC traité par un traitement curatif et sans récidive, l’accès à la TH est conditionné par le score MELD. En cas de récidive (à plus de six mois) toujours dans le score AFP, il a été proposé un accès accéléré à la transplantation en 6 mois à partir de la date de la récidive. Pour les patients qui ne sont pas dans ces critères de sélection, on reste sur un traitement d’attente dans la composante score national Foie CHC, c’est-à-dire que le candidat gagnera des points sur liste en fonction du temps. Si le traitement d’attente est impossible et si le patient a un MELD inférieur à 15, il existe une « composante expert » spécifique pour un accès à la TH en neuf mois.
Le carcinome hépato-cellulaire (CHC) est devenu la première indication de TH en 2014. Cette indication concerne 32 % des inscrits en 2021. Depuis 2018, on observe cependant une diminution de cette indication, probablement liée au progrès extraordinaire observée dans le traitement du CHC. Il est probable que les indications de la TH pour CHC vont être complètement modifiées dans les années futures avec l’essor des traitements médicaux (immunothérapie) et radiologiques (radio-embolisation) qui seuls ou combinés permettent d’obtenir une rémission chez certains patients. La place de la TH dans ce groupe de malades reste à définir. En attendant ces données, la TH doit être réalisée chez des patients ayant les critères du score AFP et traités par immunothérapie malgré un surrisque de rejet induit par ces traitements, qui pourrait concerner jusqu’à un tiers des patients (22,23). Un délai compris entre 1 à 6 mois après l’arrêt de l’immunothérapie pour réaliser la TH est aujourd’hui proposé, sans faire le consensus et sans niveau de preuve, en fonction du degré d’urgence de la TH.
| Points |
|---|
Diamètre (cm)
≤ 3
3-6
> 6 | 0
1
4 |
Nombre de nodules
1-3
≥ 4 | 0
2 |
AFP (μg/l)
≤ 100
100-1000
> 1000 | 0
2
3 |
Tableau 2 : Score AFP pour allocation du carcinome hépatocellulaire
Le cholangiocarcinome
Deux types de cholangiocarcinome constituent des indications potentielles de TH : cholangiocarcinome intrahépatique (CCI) et péri-hilaire (CPH). Il s’agit d’indications rares représentant moins de 1 % de l’activité de TH (24).
Le CCI est le cancer du foie le plus fréquent après le CHC avec une incidence en constante augmentation. Selon les dernières recommandations européennes, la TH pour le CCI n’est actuellement pas recommandée devant une survie globale à 5 ans inférieure à celle obtenue dans les autres indications de transplantation. Cependant les données disponibles sont très discordantes. Une sélection stricte des candidats à la transplantation pourrait permettre d’obtenir un taux de survie à 5 ans satisfaisant. Une étude récente a montré qu’en cas de CCI de petite taille (< 5 cm) non résécable sur cirrhose, la TH pouvait être une stratégie curative avec une survie globale allant jusqu’à 69 % à 5 ans de la transplantation (25,26). Concernant le CPH, la résection est le traitement de référence. Chez des patients jeunes (< 50 ans) atteints d’un CPH non résécable, la TH peut être discutée après mise en place d’un traitement néoadjuvant. L’étude menée par l’équipe de la Mayo Clinic a montré qu’une sélection rigoureuse des patients permettait d’obtenir après TH un taux de survie à 5 ans de 73 %. Une étude plus récente reprenant les cas au niveau international montre une survie sans récidive de 62 % à 5 ans (27). En France, la TH est actuellement validée dans le traitement du CPH non résécable dans le cadre du protocole de la Mayo Clinic. Ces patients font l’objet d’une priorisation sur liste d’attente après avis d’expert lorsqu’ils remplissent les critères.
Les autres tumeurs
L’ensemble des tumeurs malignes hors CHC et cholangiocarcinome représente 1,3 % de l’activité de TH en France. Les indications sont donc exceptionnelles et la transplantabilité repose sur un avis expert entre l’oncologue et l’équipe de TH. Dans de rares cas, la TH peut être indiquée en cas de métastases hépatiques non résécables de tumeurs d’évolution lente. C’est par exemple le cas pour les métastases hépatiques des tumeurs neuroendocrines ou de tumeurs vasculaires comme l’hémangiopéricytome ou l’hémangiome endothélial épithélioïde (28).
Certaines séries rapportent l’intérêt de la TH pour des patients très sélectionnés ayant des métastases de cancer colorectal non résécables et dont la maladie résiduelle n’est qu’hépatique (29,30). Une étude randomisée multicentrique française (TRANSMET) est en cours, dont les inclusions sont terminées, pour valider cette indication.
Enfin, certaines tumeurs bénignes peuvent conduire à la TH lorsqu’elles menacent le pronostic vital ou provoquent une gêne qui altère considérablement la qualité de vie et qu’un autre traitement n’est pas envisageable (par exemple, hémangiome géant, polyadénomatose). La décision doit se faire au cas par cas.
Quand adresser un patient ayant une hépatite aiguë ?
L’hépatique aiguë est une maladie du foie conduisant à la destruction des hépatocytes dont la principale complication est l’insuffisance hépatite aiguë caractérisée par une altération brutale des fonctions hépatiques. Elle survient sur un foie antérieurement sain. L’évolution peut être marquée par une aggravation et l’apparition d’une encéphalopathie hépatique, désignée sous le terme d’insuffisance hépatique aiguë grave ou « acute liver failure » en anglais. Le pronostic vital est alors engagé à court terme en raison, d’une part, de la survenue d’un œdème cérébral avec une hypertension intracrânienne et, d’autre part, du développement d’une défaillance multiviscérale associant une défaillance circulatoire, une insuffisance rénale aiguë et parfois une défaillance respiratoire. Cependant, quel que soit le stade de gravité, l’évolution spontanément favorable est possible grâce à la régénération hépatique et le foie peut guérir ad integrum. Les causes sont nombreuses. L’objectif de la prise en charge est d’identifier les patients dont les chances d’amélioration spontanée sont faibles et qui doivent être adressés sans délai vers un centre de TH. Des recommandations, communes à la SFAR et l’AFEF, sur la prise en charge en soins critiques de l’insuffisance hépatique aiguë ont été publiés en 2018 (31).
Les critères de gravité d’une hépatite aiguë
Les facteurs pronostiques d’une hépatite aiguë sont bien identifiés (32). Ils comprennent :
- le degré d’altération des fonctions hépatiques, principalement évalué par les facteurs de la coagulation et/ ou l’INR ;
- la cause (tableau 3) ;
- la présence d’une maladie hépatique sous-jacente ou de comorbidités ;
- la rapidité d’installation de la maladie : plus l’installation est lente, moins bon est le
Ainsi, les insuffisances hépatiques aiguës liées au paracétamol sont associées à une diminution brutale des facteurs de coagulation, quelques jours après l’intoxication et il s’agit d’une des causes pour laquelle le risque d’être transplanté est le plus faible. Au contraire, pour les causes dont l’évolution est subaiguë lorsque l’intervalle entre l’apparition de l’ictère et l’apparition de l’encéphalopathie est de plus de deux semaines (hépatites médicamenteuses immuno-allergiques et de cause indéterminée), le pronostic est moins bon.
| CAUSES D’IHA | DIAGNOSTIC |
|---|
| Causes fréquentes | 1e
intention |
| Virus | |
| Virus de l’hépatite A (VHA) | IgM VHA |
| Virus de l’hépatite B (VHB) | AgHBs, IgM anti-HBc puis PCR VHB en 2e
intention |
| Paracétamol | Anamnèse, Paracétamolémie |
| Toxiques/Autres médicaments | Anamnèse, Dosage |
| Indéterminée | |
| Causes rares | 2e
intention |
| Virus | |
| Virus de l’hépatite E (VHE) | IgM anti-VHE, PCR VHE |
| Virus du groupe Herpès (HSV, VZV, CMV, EBV) | PCR |
| Parvovirus B19 | PCR Parvovirus B19 |
| Leptospirose | Test de microagglutination |
| Maladie de Wilson | Cuprémie, cuprurie, céruloplasmine, cuivre
échangeable |
| Hépatite auto-immune | Hypergammaglobulinémie, Auto-anticorps
(FAN, antimuscles lisses, anti-LKM1), infiltrat
plasmocytaire à l’histologie |
| Hépatite hypoxique | Anamnèse, cytolyse importante (ASAT>>ALAT),
recherche d’une cause cardiaque ou
hémodynamique |
| Coup de chaleur | Anamnèse |
| Intoxication aux champignons | Anamnèse, recherche de la toxine pour l’amanite
phalloïde |
| Budd-Chiari aigu | Thrombose des veines sus-hépatiques, ascite, à
l’échographie-doppler ou tomodensitométrie |
| HELLP syndrome | Thrombopénie, cytolyse, hémolyse, CIVD,
insuffisance rénale |
| Stéatose aiguë gravidique | 3e trimestre de la grossessr |
| Syndrome de Reye | Stéatose microvésiculaire à l’histologie |
| Infiltration néoplasique | Infiltration néoplasique à l’histologie |
Tableau 3 : Causes d’insuffisance hépato-cellulaire aiguë et outils diagnostiques

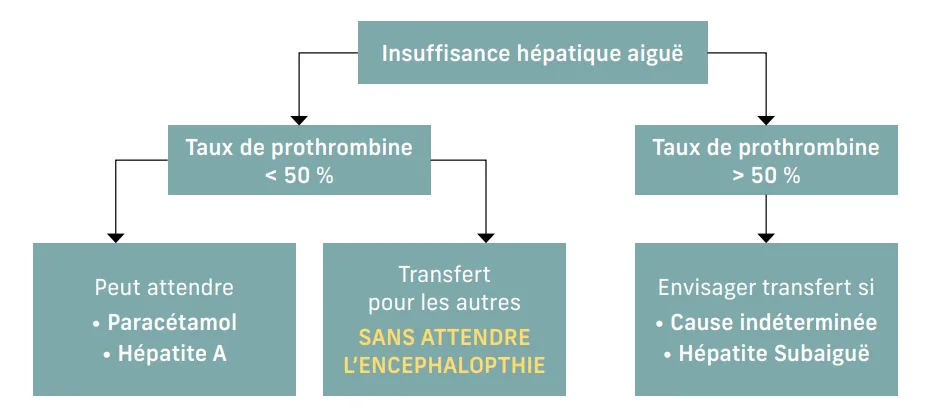
Figure 4 : Quand adresser le patient au centre de transplantation ?
Quand transférer un patient dans un centre de TH
Il ne faut pas attendre que la TH soit requise pour transférer les patients. Le délai nécessaire pour l’évaluation accélérée par le centre de TH ainsi que l’obtention d’un donneur compatible peut être long et aléatoire. Cependant, les patients ayant une hépatite aiguë sévère ont un accès prioritaire au niveau national, dit super-urgence. Lorsque l’indication est validée et en l’absence de contre-indication, le centre va demander l’accord d’un expert de l’ABM. Le receveur sera alors placé tout en haut de la liste correspondant à son groupe sanguin. La probabilité pour qu’un receveur inscrit en super-urgence reçoive un greffon dans les premières 48 heures est supérieure à 80 %. Malgré cela, le transfert d’un candidat potentiel doit être anticipé, le seul risque étant celui d’un transfert superflu pour un patient qui finalement s’améliorerait après le transfert.
Il est généralement recommandé de transférer un patient atteint d’insuffisance hépatique aiguë sévère lorsque le taux de prothrombine et/ ou le facteur V sont inférieurs à 50 %. Cependant, ceci n’est pas un dogme et le moment de transfert idéal peut varier selon les facteurs pronostiques cités dans le paragraphe 4.1. Le transfert peut être différé pour les causes associées à un bon pronostic comme l’intoxication par le paracétamol ou l’hépatite aiguë A à condition d’une surveillance étroite. À l’inverse, le transfert peut être anticipé s’il s’agit d’une cause associée à un mauvais pronostic comme les hépatites subaiguës et sans attendre bien sûr l’apparition de l’encéphalopathie. Dans tous les cas, il faut anticiper et prendre contact avec le centre de TH pour décider conjointement du moment optimal pour le transfert.
Critères de TH pour hépatite aiguë
La TH est la seule option chez les patients dont l’insuffisance hépatique ne s’améliore pas spontanément et qui développent des complications extrahépatiques (œdème cérébral et/ ou défaillance multiviscérale) menaçant le pronostic vital à très court terme. En 2021, cela représentait 4,9 % des nouveaux inscrits en TH.
Les critères de TH ont été développés pour déterminer le meilleur compromis entre transplanter sans délai pour corriger l’insuffisance hépatique et ne pas transplanter par excès des patients qui seraient améliorés afin d’éviter les TH inutiles.
Les critères les plus utilisés sont les critères de Clichy-Villejuif et les critères du King’s College Hospital (33). Malgré la large utilisation de ces critères, on estime qu’entre 10 et 20 % des patients sont peut-être transplantés alors qu’ils auraient pu s’améliorer (33). Les critères de Clichy- Villejuif tiennent compte de l’âge, du facteur V et l’encéphalopathie hépatique. Développés à partir d’une cohorte d’hépatite B fulminante, ils ne sont pas adaptés pour certaines causes comme les hépatites subaiguës. Les critères du King’s College Hospital dépendent de la cause avec des critères spécifiques pour le paracétamol, logique aux vues du meilleur pronostic. Il s’agit de scores plus complexes prenant en compte les autres défaillances que celle du foie.
D’autres critères ont été établis dans la littérature, spécifiques d’une cause comme pour l’hépatite A ou encore l’intoxication aiguë aux champignons (34,35). (34, 35.
Les indications particulières
Liées à une maladie génétique
Certaines maladies génétiques représentent une indication de TH sans hépatopathie chronique.
La neuropathie amyloïde familiale est une maladie héréditaire autosomique dominante caractérisée par la production hépatique d’une protéine modifiée : la transthyrétine. Cette mutation va conduire à des dépôts amyloïdes au niveau du système nerveux, du cœur ou encore du rein. Cette accumulation conduit à une altération fonctionnelle et menace le pronostic vital des patients. La prise en charge thérapeutique a grandement évolué ces dernières années avec l’apparition de nouvelles thérapeutiques telles que le tafamidis ou le patisiran (acide ribonucléique interférent) (36). En cas d’échec, la TH doit être envisagée pour arrêter la progression de la maladie. L’accès à la transplantation se fait sur avis d’expert.
La polykystose rénale dominante s’accompagne le plus souvent d’une polykystose hépatique. Cette polykystose hépatique est à l’origine d’une hépatomégalie pouvant conduire à une gêne fonctionnelle par compression allant jusqu’à la dénutrition. Une TH peut être indiquée en cas de gêne majeure ou de dénutrition ou de forme symptomatique en cas de greffe rénale indiquée (37).
La maladie de Rendu-Osler est liée à une dérégulation de l’angiogenèse conduisant à des dilatations artérioveineuses qui se traduisent par des épistaxis à répétition, des télangiectasies cutanées ou muqueuses et des malformations artérioveineuses viscérales (MAV) systémiques. Les MAV hépatiques peuvent être responsables de d’ischémie biliaire, d’encéphalopathie mais aussi d’un hyper-débit cardiaque conduisant à une insuffisance cardiaque pouvant faire indiquer une TH. Le bevacizumab a montré son efficacité dans la diminution du débit cardiaque dans une étude de phase II (38). Néanmoins, la durée de l’effet de ce traitement et la possibilité de le renouveler restent indéterminées. L’indication d’une TH doit être posée le plus précocement possible et le bevacizumab ne doit être proposé qu’en traitement d’attente (39). D’autres maladies génétiques peuvent conduire à une indication de TH qui sera discutée au cas par cas.
Liées à une maladie vasculaire
Le syndrome de Budd-Chiari est lié à la thrombose des veines sus-hépatiques. Dans sa forme suraiguë, il conduit à une cytolyse majeure et une insuffisance hépato-cellulaire. Dans sa forme chronique, les symptômes peuvent mimer une cirrhose. Une anticoagulation efficace est proposée de même qu’un traitement de la maladie thromboembolique sous-jacente. En cas d’échec, un TIPS ou une anastomose porto-cave chirurgicale doivent être envisagés. En l’absence d’amélioration des symptômes ou en cas de contre-indication, la TH est la seule option thérapeutique (40).
De nombreuses autres maladies vasculaires du foie peuvent conduire à la TH, le plus souvent pour une hypertension portale non contrôlée par les traitements médicaux et/ ou radiologiques.
La retransplantation
Les principales indications de re-TH en France sont représentées par les thromboses de l’artère hépatique, la non-fonction primaire du greffon et la récidive de la maladie initiale sur le greffon. Un quart des re-TH ont lieu durant les deux premières semaines et la moitié dans les 6 premiers mois. La re-TH urgente représente 2 % tandis que la re-TH élective concerne 5 % des nouveaux inscrits de 2021, stable dans le temps et ce, malgré une diminution des indications de re-TH pour récidive de l’hépatite C sur le greffon. L’indication doit être posée par une équipe experte car le score MELD a une moins bonne prédiction de la mortalité dans cette indication et les résultats sont moins bons que pour une première greffe avec une réduction de 20 % de la survie (41). Cependant, il existe une priorisation de l’accès à la TH pour ces patients.
Comment évaluer un patient candidat à la transplantation ?
L’évaluation d’un candidat à la TH consiste à valider l’indication de TH et éliminer les contre-indications. En dehors de la super-urgence, cette évaluation peut être longue et prendre plusieurs semaines. Aussi, en cas d’indication à une TH, il faut anticiper le transfert du candidat potentiel ou prendre contact avec le centre de TH de façon à débuter cette évaluation conjointement et sans délai.
Bilan pré-transplantation
Il n’y a pas aujourd’hui de recommandation précise ni de standardisation pour réaliser cette évaluation, appelée bilan pré-transplantation. Cependant, il convient d’évaluer tous les autres organes que le foie, de rechercher une contre-indication opératoire mais aussi à la prise au long cours des traitements immunosuppresseurs comme les pathologies psychiatriques, les maladies infectieuses ou des cancer extrahépatiques. Le tableau 4 précise à titre indicatif, le bilan réalisé au Centre Hépato-Biliaire.
| Examens systématiques | Consultations spécialisées | Selon contexte |
|---|
| Cardiologique | Electrocardiogramme
Echographie cardiaque
transthoracique | Oui | Epreuve d’effort
Coronarographie |
| Vasculaire | Doppler veineux et artériels
des membres inférieurs et des
troncs supra-aortiques | Artériographie |
| Pneumologique | Examens fonctionnels
respiratoires
Scanner thoracique | Oui | Epreuve de contraste
Cathétérisme droit |
| Rénale | Echographie rénale
Ionogramme urinaire,
protéinurie
Créatininémie | Selon contexte | Mesure du débit de filtration
glomérulaire
Biopsie rénale |
| Neurologique | Examen clinique | Selon contexte (systématique
en cas de maladie du foie liée
à l’alcool) | Scanner ou IRM cérébrale |
Dépistage des infections
et des cancers | Fibroscopie et coloscopie
après 50 ans
Mammographie et frottis
cervicale
PSA | Oui : gynécologique, ORL et
stomatologique | |
| Addictologie et psychiatrie | Consultations | Selon contexte | |
| Consultation d’anesthésie (à l’inscription puis tous les 6 mois sur liste) |
Tableau 4 : Bilan pré-transplantation au Centre Hépato-Biliaire en dehors du contexte de super-urgence
Au terme de ce bilan, une fois la partie administrative faite auprès de l’ABM, le patient sera inscrit et considéré comme «actif» sur une liste de TH correspondant à son groupe sanguin. Le temps d’attente est variable en fonction du nombre de points qu’à le receveur, entre 0 et 1 000 dans le score national Foie. La figure 5 reprend le processus d’évaluation du receveur.

Une fois le patient inscrit, une réévaluation clinique et paraclinique est nécessaire tous les 3 mois et les données actualisées saisies dans la base de l’ABM pour que le patient reste actif sur liste.
Contre-indications absolues et relatives
Depuis plusieurs décennies maintenant, les chirurgiens, anesthésistes réanimateurs et médecins spécialisés en TH n’ont cessé de repousser les limites de la TH. Ainsi, il y a finalement très peu de contre-indications absolues. La seule vraie est l’impossibilité d’implantation du système porte en cas de thrombose complète du système porte et mésentérique.
Toutes les autres contre-indications sont relatives et le renoncement à la TH est une décision d’équipe qui tient compte de la balance bénéfice- risque pour le receveur mais aussi pour le système, actuellement contraint en raison de la pénurie des greffons, priorisant ainsi les receveurs ayant les meilleures chances de survie sur le moyen et long terme. Il faut donc préciser d’emblée que le chapitre présent détaille des limites en 2023 mais qui seront peut-être différentes dans une décennie et fonction du nombre d’organes disponibles. À titre d’exemple, l’infection par le virus de l’immunodéficience humaine était une contre-indication jusqu’à l’arrivée des antirétroviraux (42). De la même façon, l’hypertension porto- pulmonaire était une contre-indication absolue alors qu’aujourd’hui les patients contrôlés sous traitement peuvent être transplantés pour cette indication. Une forme sévère avec une pression artérielle pulmonaire moyenne de plus de 50 mmHg malgré le traitement est en revanche toujours une contre-indication (43).
Existe-t-il un âge limite ?
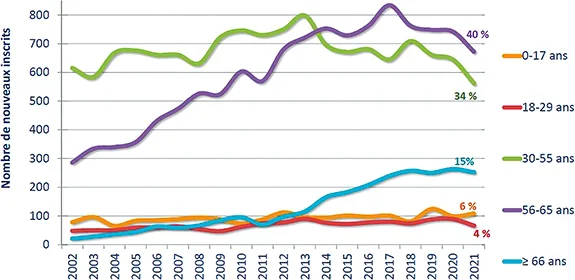
Cette question est un sujet de controverse. Le risque de décès et les comorbidités pouvant grever le pronostic des receveurs augmentent incontestablement avec l’âge. Cependant, plusieurs études démontrent la faisabilité de la transplantation à un âge supérieur à 65 voire 70 ans (44,45). Certains défendent donc un âge civil limite au-delà duquel la TH serait contre-indiquée. Si cette approche est raisonnable pour la meilleure utilisation possible des greffons, d’autres opposent l’équité d’accès et proposent de limiter l’accès à la TH en fonction de l’âge physiologique. Ce d’autant que les progrès dans la prise en charge des patients ayant une maladie terminale du foie repoussent sans cesse l’âge auquel les patients ont une indication de TH (figure 5). Une réflexion est actuellement menée pour intégrer des échelles de fragilité pour sélectionner les candidats.

Figure 6 : Évolution de l’âge du receveur à l’inscription
Source : Rapport annuel du groupe technique Foie de l’Agence de Biomédecine
Les autres points d’attention
Comorbidités métaboliques et obésité
Les comorbidités associées au syndrome métabolique doivent être évaluées de façon exhaustive avant inscription sur liste. L’évaluation cardiologique, vasculaire et pulmonaire doit, en particulier, être adaptée. Par exemple, une épreuve d’effort doit être systématique et certains recommandent une coronarographie de principe, bien que cela soit encore controversé (46).
L’obésité est un facteur indépendant d’aggravation d’une éventuelle hépatopathie chronique, un facteur de décompensation d’une cirrhose ou d’apparition d’un CHC. Cependant, même si les données de la littérature sont discordantes, le poids seul n’apparaît pas comme un facteur d’échec de transplantation (47). En revanche, l’obésité augmente le risque de sortie de liste pour décès ou aggravation (48). Il n’en demeure pas moins qu’il faut évaluer ces patients avec des équipes spécialisées et envisager dès que possible une chirurgie bariatrique avant, pendant ou plus sûrement après TH (49). À ce jour, il n’y a pas de recommandation pour limiter un patient sur son seul poids même si une vigilance et prise en charge particulière doivent être faites.
Comorbidités oncologiques
Les innovations thérapeutiques en oncologie de la dernière décennie ont été majeures et ont complètement bouleversé certains dogmes. Si le cancer extra-hépatique non traité demeure le plus souvent une contre-indication à la TH, cela peut dépendre des perspectives thérapeutiques, avec ou sans TH et du pronostic à court et moyen terme. Le même raisonnement peut s’appliquer à un cancer extra-hépatique récemment traité : dans ce cas, c’est le risque de récidive qui doit être pris en compte. Le dogme des 5 ans de délai entre cancer et TH doit être remis en cause. Une évaluation individuelle du rapport bénéfice/ risque en réunion de concertation pluridisciplinaire paraît la meilleure stratégie.
Une problématique nouvelle a également émergé ces dernières années pour les patients traités par immunothérapie. En effet, un surrisque de rejet existe (22,23). L’intervalle libre entre arrêt de l’immunothérapie et TH est donc sujet à débat. Si là aussi, une discussion au cas par cas est nécessaire pour les patients dont le pronostic vital est engagé sans une TH urgente, pour les autres, un délai allant de 3 à 6 mois est préconisé sans que les données aujourd’hui ne soient solides.
Comorbidités rénales
Une insuffisance rénale avant la TH a une influence sur la survie après TH. L’évaluation de la fonction rénale est donc capitale pour limiter son aggravation avec en particulier l’utilisation d’agents néphrotoxiques, anticiper le protocole d’immunosuppression et parfois poser l’indication d’une greffe combinée lorsque le débit de filtration glomérulaire est ≤ 30 mL/min et/ ou s’il existe une glomérulosclérose > 30 % et/ ou une fibrose interstitielle > 30 % à la biopsie rénale (11).
Évaluation nutritionnelle
La dénutrition et la sarcopénie sont des facteurs indépendants de mortalité avant et après TH. Leur évaluation, cependant, n’est pas standardisée. Les biomarqueurs habituels de dénutrition ne peuvent s’appliquer aux patients cirrhotiques comme l’albumine (50). De façon récente, une mesure plus globale de la fragilité du patient émerge, mesurée par le Liver Frailty Index, également facteur indépendant de mortalité avant et après TH (51).
Il s’agit de mesurer l’aptitude des patients à accomplir cinq exercices sollicitant leur tonus musculaire. En tout cas, une évaluation des besoins nutritionnels chez les patients en attente de TH est absolument nécessaire et la correction de la dénutrition doit systématiquement être envisagée (52). Conclusion
Après plusieurs décennies de succès et progrès médicaux et chirurgicaux, la TH a atteint un âge de maturité. Les innovations médicales ou chirurgicales sont rendues plus difficiles compte tenu des résultats excellents sur le court, moyen et long terme. En revanche, les indications ne cessent d’évoluer en fonction des progrès de la prise en charge des maladies hépatiques. Certaines indications sont en net recul comme la cirrhose virale C alors que d’autres indications sont en augmentation comme la stéatohépatite métabolique ou certaines tumeurs. Ces évolutions contraignent les systèmes d’allocation des organes, en particulier le système français, à s’adapter rapidement pour maintenir l’équité d’accès en fonction des indications pourtant très variées.
Références
- European Association for the Study of the Electronic address eee. EASL Clinical Practice Guidelines: Liver transplantation. J Hepatol. 2016;64(2):433-85.
- Wiesner R, Edwards E, Freeman R, Harper A, Kim R, Kamath P, et al. Model for end-stage liver disease (MELD) and allocation of donor livers. Gastroenterology. 2003;124(1):91-6.
- Malinchoc M, Kamath PS, Gordon FD, Peine CJ, Rank J, ter Borg A model to predict poor survival in patients undergoing transjugular intrahepatic portosystemic shunts. Hepatology. 2000;31(4):864-71.
- Merion RM, Schaubel DE, Dykstra DM, Freeman RB, Port FK, Wolfe The survival benefit of liver transplantation. Am J Transplant. 2005;5(2):307-13.
- Polyak A, Kuo A, Sundaram Evolution of liver transplant organ allocation policy: Current limitations and future directions. World J Hepatol. 2021;13(8):830-9.
- Kim WR, Mannalithara A, Heimbach JK, Kamath PS, Asrani SK, Biggins SW, et MELD 3.0: The Model for End-Stage Liver Disease Updated for the Modern Era. Gastroenterology. 2021;161(6):1887-95 e4.
- Bernards S, Lee E, Leung N, Akan M, Gan K, Zhao H, et Awarding additional MELD points to the shortest waitlist candidates improves sex disparity in access to liver transplant in the United States. Am J Transplant. 2022;22(12):2912-20.
- Rodriguez-Peralvarez ML, Gomez-Orellana AM, Majumdar A, Bailey M, McCaughan GW, Gow P, et al. Development and validation of the Gender-Equity Model for Liver Allocation (GEMA) to prioritise candidates for liver transplantation: a cohort Lancet Gastroenterol Hepatol. 2022.
- Francoz C, Belghiti J, Castaing D, Chazouilleres O, Duclos-Vallee JC, Duvoux C, et Model for end-stage liver disease exceptions in the context of the French model for end-stage liver disease score-based liver allocation system. Liver Transpl. 2011;17(10):1137-51.
- Artru F, Louvet A, Ruiz I, Levesque E, Labreuche J, Ursic-Bedoya J, et al. Liver transplantation in the most severely ill cirrhotic patients: A multicenter study in acute-on-chronic liver failure grade 3. J Hepatol. 2017;67(4):708-15.
- AFEF Indications de la transplantation hépatique chez l’adulte et l’enfant. 2018.
- Belli LS, Duvoux C, Artzner T, Bernal W, Conti S, Cortesi PA, et Liver transplantation for patients with acute-on-chronic liver failure (ACLF) in Europe: Results of the ELITA/EF-CLIF collaborative study (ECLIS). J Hepatol. 2021;75(3):610-22.
- Lucey MR, Schaubel DE, Guidinger MK, Tome S, Merion Effect of alcoholic liver disease and hepatitis C infection on waiting list and posttransplant mortality and transplant survival benefit. Hepatology. 2009;50(2):400-6.
- Mathurin P, Moreno C, Samuel D, Dumortier J, Salleron J, Durand F, et Early liver transplantation for severe alcoholic hepatitis. N Engl J Med. 2011;365(19):1790-800.
- Louvet A, Labreuche J, Moreno C, Vanlemmens C, Moirand R, Feray C, et al. Early liver transplantation for severe alcohol-related hepatitis not responding to medical treatment: a prospective controlled study. Lancet Gastroenterol Hepatol. 2022;7(5):416-25.
- SDC. Indications de transplantation hépatique pour hépatites virales. Hépato-Gastro et Oncologie Digestive 2020;27:5-10.
- De Martin E, Coilly A, Chazouilleres O, Roux O, Peron JM, Houssel-Debry P, et Early liver transplantation for corticosteroid non-responders with acute severe autoimmune hepatitis: The SURFASA score. J Hepatol. 2021;74(6):1325-34.
- Lazzati A, Iannelli A, Schneck AS, Nelson AC, Katsahian S, Gugenheim J, et Bariatric surgery and liver transplantation: a systematic review a new frontier for bariatric surgery. Obes Surg. 2015;25(1):134-42.
- Duvoux C, Roudot-Thoraval F, Decaens T, Pessione F, Badran H, Piardi T, et al. Liver transplantation for hepatocellular carcinoma: a model including alpha-fetoprotein improves the performance of Milan criteria. Gastroenterology. 2012;143(4):986-94 e3; quiz e14-5.
- Notarpaolo A, Layese R, Magistri P, Gambato M, Colledan M, Magini G, et al. Validation of the AFP model as a predictor of HCC recurrence in patients with viral hepatitis-related cirrhosis who had received a liver transplant for HCC. J Hepatol. 2017;66(3):552-9.
- Pinero F, Tisi Bana M, de Ataide EC, Hoyos Duque S, Marciano S, Varon A, et Liver transplantation for hepatocellular carcinoma: evaluation of the alpha-fetoprotein model in a multicenter cohort from Latin America. Liver Int. 2016;36(11):1657-67.
- d’Izarny-Gargas T, Durrbach A, Zaidan Efficacy and tolerance of immune checkpoint inhibitors in transplant patients with cancer: A systematic review. Am J Transplant. 2020;20(9):2457-65.
- Abdel-Wahab N, Safa H, Abudayyeh A, Johnson DH, Trinh VA, Zobniw CM, et Checkpoint inhibitor therapy for cancer in solid organ transplantation recipients: an institutional experience and a systematic review of the literature. J Immunother Cancer. 2019;7(1):106.
- Gringeri E, Gambato M, Sapisochin G, Ivanics T, Lynch EN, Mescoli C, et al. Cholangiocarcinoma as an Indication for Liver Transplantation in the Era of Transplant Oncology. J Clin Med. 2020;9(5).
- De Martin E, Rayar M, Golse N, Dupeux M, Gelli M, Gnemmi V, et al. Analysis of Liver Resection Versus Liver Transplantation on Outcome of Small Intrahepatic Cholangiocarcinoma and Combined Hepatocellular-Cholangiocarcinoma in the Setting of Liver Transpl. 2020;26(6):785-98.
- Sapisochin G, Rodriguez de Lope C, Gastaca M, Ortiz de Urbina J, Suarez MA, Santoyo J, et “Very early” intrahepatic cholangiocarcinoma in cirrhotic patients: should liver transplantation be reconsidered in these patients? Am J Transplant. 2014;14(3):660-7.
- Breuer E, Mueller M, Doyle MB, Yang L, Darwish Murad S, Anwar IJ, et al. Liver Transplantation as a New Standard of Care in Patients With Perihilar Cholangiocarcinoma? Results From an International Benchmark Study. Ann Surg. 2022;276(5):846-53.
- Grossman EJ, Millis Liver transplantation for non-hepatocellular carcinoma malignancy: Indications, limitations, and analysis of the current literature. Liver Transpl. 2010;16(8):930-42.
- Hagness M, Foss A, Line PD, Scholz T, Jorgensen PF, Fosby B, et Liver transplantation for nonresectable liver metastases from colorectal cancer. Ann Surg. 2013;257(5):800-6.
- Solheim JM, Dueland S, Line PD, Hagness Transplantation for Nonresectable Colorectal Liver Metastases – Long Term follow- up of the First Prospective Pilot Study. Ann Surg. 2022.
- AFEF Insuffisance hépatique aiguë en soins critiques. 2018.
- Stravitz RT, Lee Acute liver failure. Lancet. 2019;394(10201):869-81.
- Bernal W, Williams Beyond KCH selection and options in acute liver failure. Hepatol Int. 2018;12(3):204-13.
- Escudie L, Francoz C, Vinel JP, Moucari R, Cournot M, Paradis V, et Amanita phalloides poisoning: reassessment of prognostic factors and indications for emergency liver transplantation. J Hepatol. 2007;46(3):466-73.
- Taylor RM, Davern T, Munoz S, Han SH, McGuire B, Larson AM, et Fulminant hepatitis A virus infection in the United States: Incidence, prognosis, and outcomes. Hepatology. 2006;44(6):1589-97.
- Carroll A, Dyck PJ, de Carvalho M, Kennerson M, Reilly MM, Kiernan MC, et al. Novel approaches to diagnosis and management of hereditary transthyretin amyloidosis. J Neurol Neurosurg Psychiatry. 2022;93(6):668-78.
- Olaizola P, Rodrigues PM, Caballero-Camino FJ, Izquierdo-Sanchez L, Aspichueta P, Bujanda L, et Genetics, pathobiology and therapeutic opportunities of polycystic liver disease. Nat Rev Gastroenterol Hepatol. 2022;19(9):585-604.
- Dupuis-Girod S, Ginon I, Saurin JC, Marion D, Guillot E, Decullier E, et Bevacizumab in patients with hereditary hemorrhagic telangiectasia and severe hepatic vascular malformations and high cardiac output. JAMA. 2012;307(9):948-55.
- Dupuis CC, Quelle place pour la transplantation hépatique dans la maladie de Rendu-Osler? La lettre de l’hépato-gastroentérologue. 2022;N°3.
- Coilly A, Potier P, Broue P, Kounis I, Valla D, Hillaire S, et Budd-Chiari syndrome. Clin Res Hepatol Gastroenterol. 2020;44(4):420-5.
- Memeo R, Laurenzi A, Pittau G, Sanchez-Cabus S, Vibert E, Adam R, et Repeat liver retransplantation: rationale and outcomes. Clin Transplant. 2016;30(3):312-9.
- Campos-Varela I, Dodge JL, Berenguer M, Adam R, Samuel D, Di Benedetto F, et Temporal Trends and Outcomes in Liver Transplantation for Recipients With HIV Infection in Europe and United States. Transplantation. 2020;104(10):2078-86.
- Savale L, Guimas M, Ebstein N, Fertin M, Jevnikar M, Renard S, et Portopulmonary hypertension in the current era of pulmonary hypertension management. J Hepatol. 2020;73(1):130-9.
- Durand F, Levitsky J, Cauchy F, Gilgenkrantz H, Soubrane O, Francoz Age and liver transplantation. J Hepatol. 2019;70(4):745-58.
- Germani G, Zeni N, Zanetto A, Adam R, Karam V, Belli LS, et Influence of donor and recipient gender on liver transplantation outcomes in Europe. Liver Int. 2020;40(8):1961-71.
- Tsochatzis E, Coilly A, Nadalin S, Levistky J, Tokat Y, Ghobrial M, et al. International Liver Transplantation Consensus Statement on End-stage Liver Disease Due to Nonalcoholic Steatohepatitis and Liver Transplantation. Transplantation. 2019;103(1):45-56.
- Ayloo S, Armstrong J, Hurton S, Molinari Obesity and liver transplantation. World J Transplant. 2015;5(3):95-101.
- Delacote C, Favre M, El Amrani M, Ningarhari M, Lemaitre E, Ntandja-Wandji LC, et al. Morbid obesity increases death and dropout from the liver transplantation waiting list: A prospective cohort study. United European Gastroenterol J. 2022;10(4):396-408.
- Diwan TS, Rice TC, Heimbach JK, Schauer Liver Transplantation and Bariatric Surgery: Timing and Outcomes. Liver Transpl. 2018;24(9):1280-7.
- Buchard B, Boirie Y, Cassagnes L, Lamblin G, Coilly A, Abergel Assessment of Malnutrition, Sarcopenia and Frailty in Patients with Cirrhosis: Which Tools Should We Use in Clinical Practice? Nutrients. 2020;12(1).
- Lai JC, Covinsky KE, Dodge JL, Boscardin WJ, Segev DL, Roberts JP, et Development of a novel frailty index to predict mortality in patients with end-stage liver disease. Hepatology. 2017;66(2):564-74.
- European Association for the Study of the Electronic address eee, European Association for the Study of the L. EASL Clinical Practice Guidelines on nutrition in chronic liver disease. J Hepatol. 2019;70(1):172-93.
ABRÉVIATIONS
ABM : Agence de Biomédecine
ACLF : Acute on Chronic Liver Failure
CCI : CholangioCarcinome Intrahépatique
CHC : Carcinome Hépato-Cellulaire
CPH : Cholangiocarcinome Péri-Hilaire
HA : Hépatite Alcoolique
HAI : Hépatite Auto-Immune
MELD : Model for End Stage Liver Disease
TH : Transplantation Hépatique
TIPS : Shunt Intrahépatique Porto-systémique par voie Transjugulaire