Abréviations
CDA : Coefficient de diffusion apparent
GETAID : Groupe d’étude thérapeutique des affections inflammatoires du tube digestif
MC : Maladie de Crohn
MICI : Maladies inflammatoires chroniques de l’intestin
PACS : Picture archiving and communication system
PEG : Polyéthylène Glycol
RCH : Rectocolite hémorragique
RPO : Récidive post-opératoire
RX : Rayons X
VCE : Vidéo-capsule endoscopique
Introduction
Chaque patient atteint de Maladie de Crohn (MC) a un profil spécifique, nécessitant une prise en charge thérapeutique et un suivi adapté. La stratégie d’optimisation des examens d’imagerie est indispensable afin d’éviter la lourdeur du parcours de ces malades atteints de maladie chronique. La pertinence dans l’indication des examens doit être une priorité pour le demandeur ainsi que pour le médecin radiologue. Par conséquent le gastro-entérologue doit connaître le panel des examens possibles, leurs techniques de réalisation avec les bénéfices attendus à chaque étape de la MC, mais aussi les éventuels risques de ces différentes techniques d’imagerie. Le choix des examens varie à chaque phase spécifique de la maladie mais doit, dans tous les cas, privilégier l’absence de Rayons X (RX).
Techniques d’imagerie utiles dans la maladie de Crohn
Échographie
L’échographie permet un examen direct de la paroi digestive et de l’atmosphère péri-digestive par voie transpariétale, et plus rarement endocavitaire. Il s’agit d’un examen simple, facile d’accès, bien toléré par le malade et dépourvu d’exposition aux rayons X.
Le patient doit être à jeun 4 à 6 heures avant la réalisation de l’examen. Aucune préparation spécifique n’est nécessaire par ailleurs.
L’examen commence toujours par un balayage de la cavité abdominale par une sonde curviligne basse fréquence, qui permet de rechercher des anomalies profondes (atteinte digestive profonde, abcès), de repérer la position du la valvule iléo-caecale (le cæcum présente parfois une position atypique liée à un défaut d’accolement) et enfin de rechercher des anomalies pouvant être associées à une MC (cholangite, abcès hépatique, thrombose porte).
L’examen échographique se poursuit ensuite obligatoirement par un examen avec une sonde de haute fréquence linéaire ou curviligne, avec un balayage de tout l’abdomen et du pelvis en réalisant une compression dosée (1) ; celle-ci permettra d’écarter les gaz s’interposant entre la sonde et le tube digestif pathologique et de diminuer l’espace entre la zone à analyser et le transducteur. Elle comporte aussi une étude en mode doppler couleur et/ou énergie, analysant la vascularisation pariétale. La technique échographique d’analyse micro-vasculaire récente paraît prometteuse. L’échographie de contraste peut être utilisée à des fins qualitatives ou quantitatives, mais le Sonovue® n’a pas l’AMM dans cette indication (2). La quantification des paramètres vasculaires paraît intéressante pour un suivi longitudinal des données de l’inflammation, mais elle reste peu reproductible à ce jour.
Entéro-IRM
L’entéro-IRM nécessite une préparation spécifique dans le service d’imagerie. Elle consiste à distendre les anses grêles afin de limiter les faux positifs dus à des pseudo-épaississements d’un tube digestif collabé au moment de la réalisation des images. À cet effet, on utilise préférentiellement une solution iso- osmotique (PEG) à raison d’1 à 1,2 litres qu’on fera absorber au patient de façon régulière dans la demi- heure avant l’examen. Il n’y a pas de préparation au domicile du patient, hormis la période de jeûne de 4 à 6 heures avant l’examen. L’IRM étant extrêmement sensible aux artéfacts de mouvements, on injecte un antipéristaltique lorsque le patient entre dans l’aimant, en privilégiant le glucagon, extrêmement efficace pour sidérer le mouvement des anses dans les secondes suivant l’injection et ceci pendant 10 à 15 minutes. À 1,5 ou 3 Tesla, le protocole d’examen comporte systématiquement des coupes pondérées en T2, en diffusion et en T1 avec injection de gadolinium et saturation graisseuse. Les coupes pondérées en T2 permettent une analyse morphologique facile des signes pariétaux et extra-muraux. Les coupes pondérées en diffusion, moins anatomiques, ont pour objectif une analyse fonctionnelle. Un hypersignal sur l’analyse des images réalisées avec un gradient de diffusion élevé (b800) est souvent associé à des signes inflammatoires. Les paramètres des images acquises en diffusion permettent aussi le calcul du coefficient de diffusion apparent (CDA) utilisé pour réaliser des mesures, évaluant la capacité de mouvement cellulaire au sein du tissu. Le CDA est utilisé dans le score inflammatoire de Clermont (3) mais l’utilisation du CDA reste assez complexe du fait de l’hétérogénéité des paramètres des séquences de diffusion utilisés en pratique courante. Une injection IV de gadolinium est nécessaire afin d’étudier le rehaussement du signal en pondération T1 à la phase parenchymateuse (80-100 secondes) après le début de l’injection puis à la phase tardive (7-8 minutes environ). Suite aux observations récentes sur les accumulations de certains produits de contraste gadolinés dans les noyaux gris centraux, on injecte des produits macrocycliques en priorité (4). Les images sont acquises dans plusieurs plans de l’espace en privilégiant les plans frontaux et axiaux ; cependant des acquisitions obliques mettant en exergue les zones de sténoses pourront permettre une étude optimisée. La lecture des images nécessite des écrans multiples, permettant une analyse simultanée des différentes pondérations pour une même zone d’étude.
L’utilisation d’un PACS permet de faciliter la comparaison de plusieurs examens successifs dans le temps. La lecture des images d’entéro-IRM nécessite une longue courbe d’apprentissage. L’efficacité dans la lecture des images augmente de 66 à 75 % après la lecture de 100 cas, avec une sous-estimation des lésions passant de 15 à 7 % et une surestimation stable dans 20 % des cas (5).
Scanner abdomino-pelvien
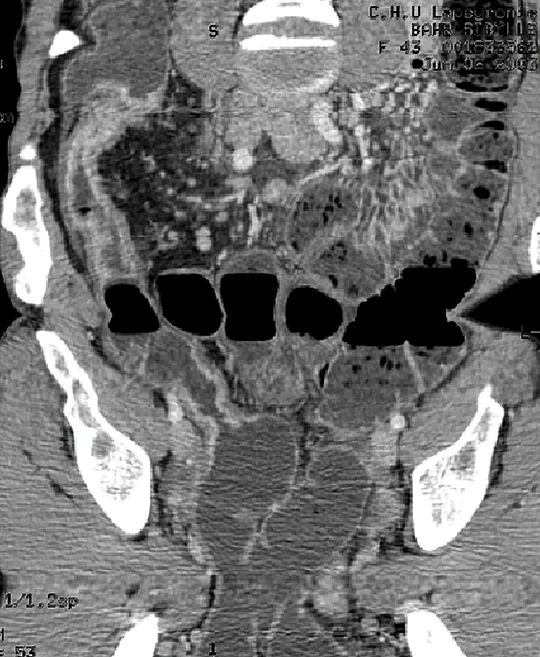
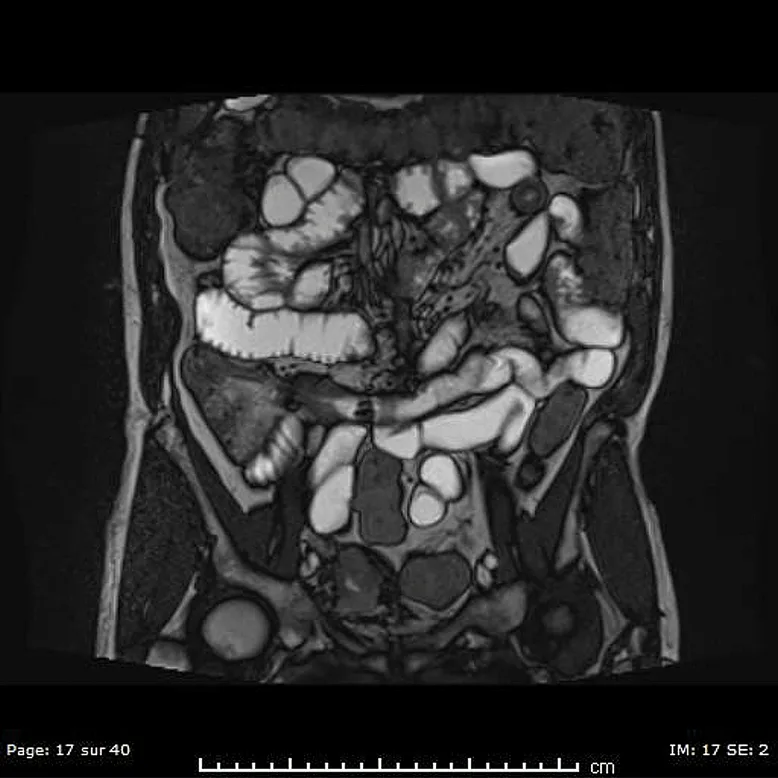
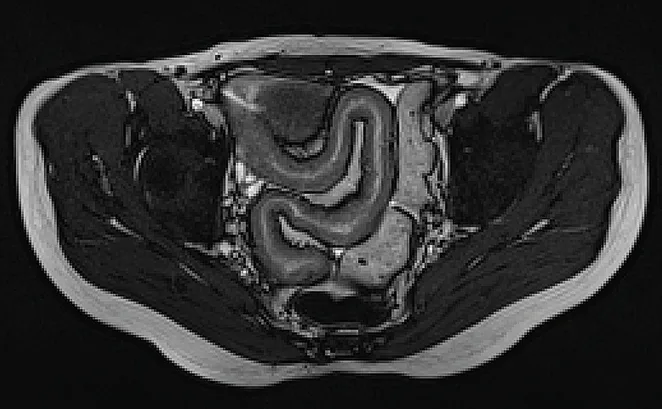
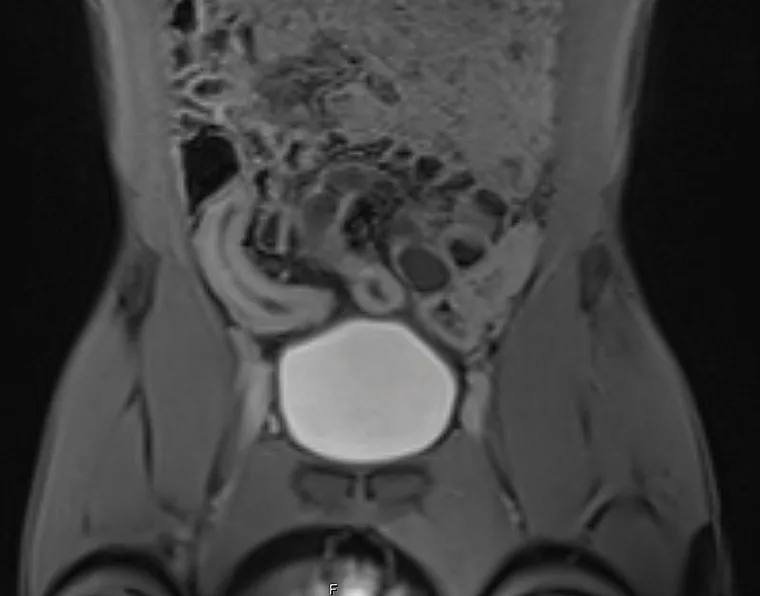
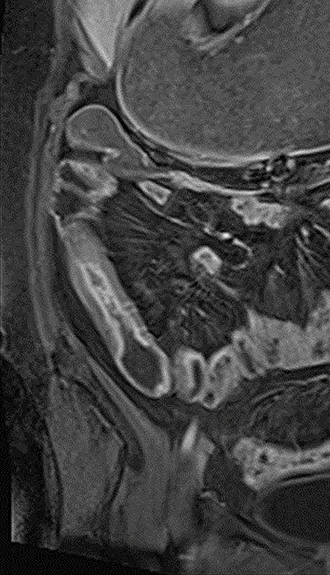
Bien que la résolution en contraste soit moins importante que celle de l’IRM, le scanner présente l’avantage de son excellente résolution temporelle, permettant une acquisition en moins de 10 secondes pour l’ensemble de la cavité abdominale et pelvienne. Ainsi cet examen est peu sensible aux artéfacts de mouvements des anses digestives et/ou respiratoires. Dans un souci de limitation des doses d’exposition aux RX, un seul passage au temps portal doit être réalisé (à 70 secondes du début de l’injection). L’acquisition des images le plus souvent infra- millimétriques permettra des reconstructions multiplanaires de grande qualité dans tous les plans de l’espace souhaités (image 1) (6). Malgré son excellente sensibilité et spécificité dans la recherche de complications (7), la réalisation d’un scanner dans la maladie de Crohn (MC) doit être limitée, en raison de l’exposition au RX. Une surexposition aux RX (de plus de 50 mSv) était observée chez 20 % de patients atteints de MC dans une cohorte de 243 malades entre 2011 et 2013, en raison de la réalisation de scanners et d’entéro-scanners (8). Les facteurs de risque connus de surexposition aux RX sont les antécédents de chirurgie, l’utilisation de corticoïdes, le jeune âge au diagnostic (17 ans), l’atteinte du haut appareil digestif, les maladies pénétrantes et l’utilisation d’infliximab (9,10,11). L’utilisation du scanner doit se limiter – si possible – aux urgences (occlusion, suspicion d’abcès profonds) avec un intérêt particulier pour la recherche d’une perforation digestive (image 2). L’IRM est en effet peu performante pour repérer avec fiabilité des bulles d’air extra-digestives en cas de perforation digestive. En cas d’indisponibilité de l’IRM en urgence ou semi-urgence, les performances du scanner sont excellentes pour faire le bilan d’occlusion, de sténoses ou de complications abcédées profondes (7). Une étude menée sur 10 années entre 2006 et 2015 montre la stabilité de l’utilisation du scanner dans la prise en charge de la MC, mais la diminution de 60 % des doses de RX administrés (2006 : 16,9 ± 7,1 mGy ; 2015 : 6,87 ± 4,62 mGy, P < 0,001) (12), témoignant de l’effort des constructeurs et des radiologues dans la réduction de doses de RX.

Image 1. Scanner abdomino-pelvien au temps portal ; apport des reconstructions curvilignes dans la mesure et l’étude des sténoses

Image 2. Apport du scanner injecté pour la recherche de bulles d’air extra-digestives
Entéro-scanner
Comme pour l’entéro-IRM, l’entéro-scanner nécessite la distension des anses grêles, afin de ne pas confondre un épaississement pathologique des parois de l’intestin grêle et une anse digestive simplement collabée. Un agent de contraste oral neutre est préconisé. Deux techniques de distension sont possibles : la première consiste en l’ingestion de PEG (comme pour l’entéro-IRM). L’ingestion d’eau ne permet pas de distendre le grêle terminal comme un produit iso-osmotique, car elle est absorbée progressivement par le grêle lors de son ingestion lente par le patient. La seconde technique de distension nécessite le placement d’une sonde d’entéroclyse sous scopie dans l’angle de Treitz, puis le remplissage de l’intestin par 1,5 à 2 litres d’eau manuellement ou par un entéroclyseur. La qualité de la distension est plus fiable avec cette seconde technique, mais elle est plus complexe dans sa mise en œuvre tant pour l’opérateur que pour le patient. L’acquisition des images tomodensitométriques doit suivre de peu la distension du tube digestif. L’administration d’agents de contraste oraux positifs n’est pas recommandée. Comme pour le scanner, la limitation de l’exposition au RX est souhaitable, avec un seul passage au temps portal de l’injection intra- veineuse d’iode.
ASP
L’ASP est un examen très peu contributif dans la MC. L’HAS n’autorise plus son utilisation qu’en cas de recherche de colectasie, dans les colites aiguës graves.
Transit du grêle
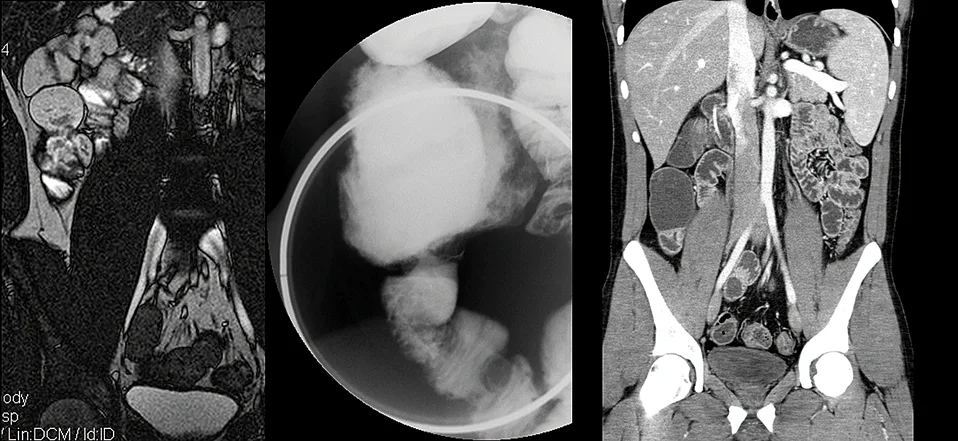
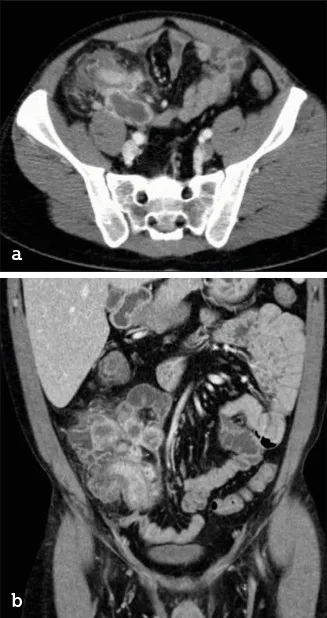
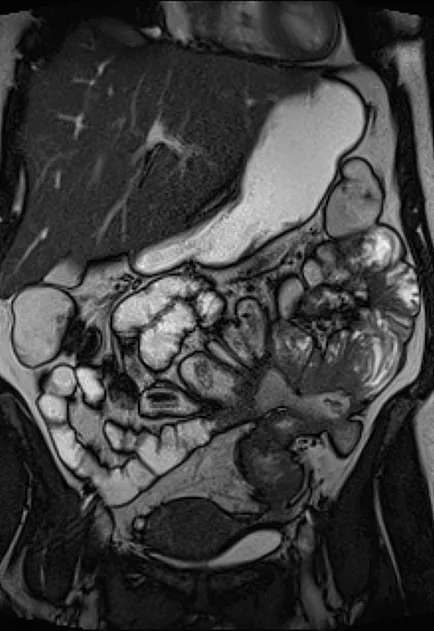
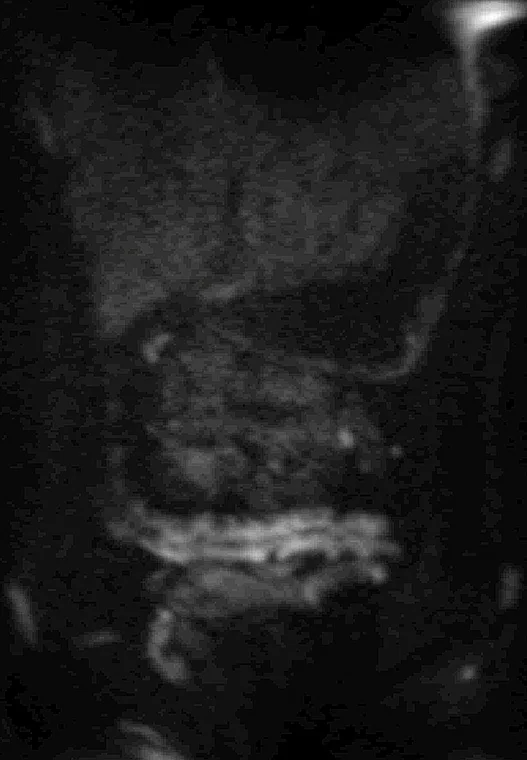
Le transit du grêle longtemps utilisé dans le bilan morphologique des lésions de l’intestin grêle n’a plus d’indication car il est moins sensible, plus fastidieux à réaliser, plus difficile à accepter par les patients, et surtout n’apporte pas d’information sur l’activité inflammatoire et les lésions péri-digestives, à l’inverse de l’imagerie en coupe (image 3).

Image 3. Comparaison d’une sténose intestinale avec le transit du grêle, l’entéroscanner et l’entéro-IRM
Stratégie d’exploration en imagerie dans la maladie de Crohn
Diagnostic
Les données cliniques, biologiques et endoscopiques sont incontournables, mais les examens d’imagerie réalisés à la phase initiale du diagnostic peuvent aider à orienter vers le diagnostic de MC.
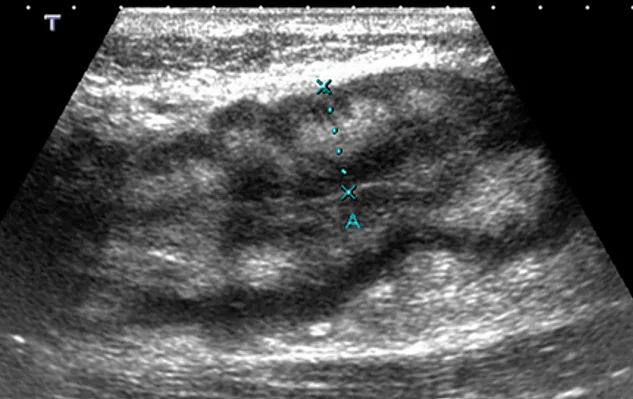
L’échographie est souvent le premier examen d’imagerie demandé en cas de douleurs abdominales ou de troubles du transit dans les suites de l’examen clinique. Elle a pour objectif de différencier au mieux les troubles fonctionnels intestinaux (TFI) d’une autre pathologie dont la MC. La découverte d’un épaississement digestif circonférentiel et symétrique en échographie pourra orienter vers une MC, d’autant qu’elle s’associe à des signes plus spécifiques, tels que des anomalies multifocales discontinues, des anomalies transmurales pénétrantes et/ou des anomalies extra-murales. Ainsi la découverte d’ulcérations profondes, de fistules borgnes, de fistules internes, de sclérolipomatose, d’hyperhémie mésentérique pourront argumenter une MC, d’autant qu’elles sont centrées sur le carrefour iléo-cæcal (images 4, 5, 6a, 6b). Une méta-analyse de 5 études de cohorte prospectives et 2 études cas-témoins ayant évalué l’échographie dans le diagnostic de MC en présence de douleurs et/ou de diarrhée, a prouvé son excellente spécificité et sa bonne sensibilité, variant selon un seuil d’épaisseur de paroi fixé à 3 ou 4 mm et selon la localisation colique ou iléale (13).

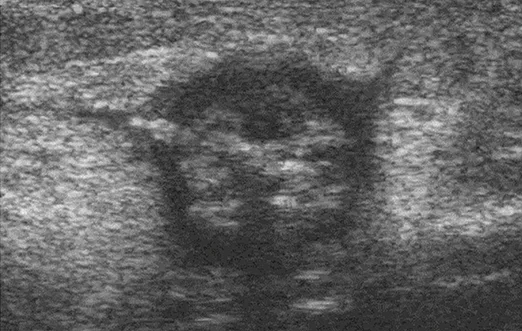
Image 4. Atteinte transmurale de la paroi digestive en échographie lors d’une poussée

Image 5. Ulcération de paroi et fistule borgne en échographie

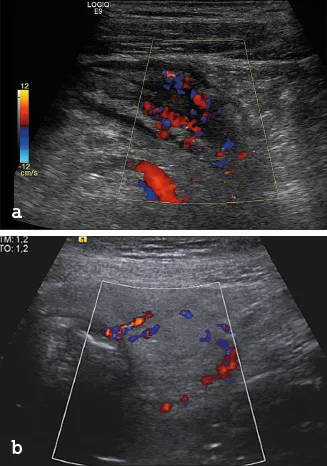
Image 6. Hyperhémie pariétale (a) et mésentérique (b) en échographie
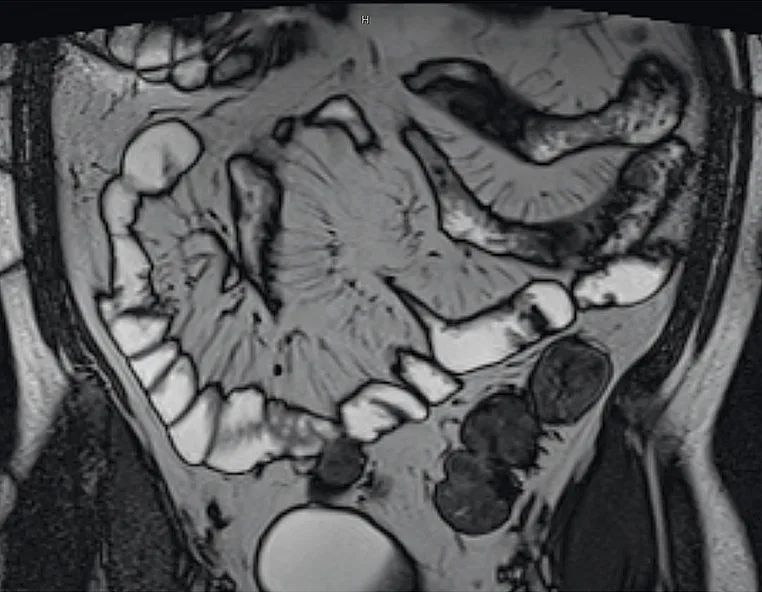
L’entéro-IRM peut être utile à la phase diagnostique de la MC. En l’absence d’arguments endoscopiques, la réalisation d’une entéro-IRM recherche des atteintes gréliques évocatrices. Sa négativité n’exclut pas le diagnostic. Cependant, elle aura pu éliminer des sténoses qui contre-indiqueraient la réalisation d’une vidéo-capsule endoscopique (VCE). Si elle est positive, l’entéro-IRM permettra alors de préciser l’extension précise de la maladie, d’évaluer son phénotype sténosant, pénétrant, ou non sténosant – non pénétrant selon la classification de Montréal (14, 15, 16) (images 7, 8, 9). L’extension et la sévérité initiale des lésions de la MC est ainsi effectué, associant les informations cliniques, biologiques, endoscopiques et d’imagerie (cartographie lésionnelle).

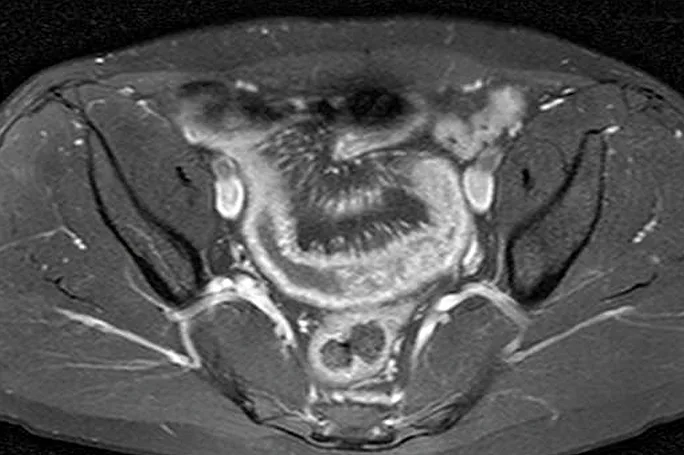
Image 7. Phénotype non sténosant non pénétrant de MC en Entéro-IRM ; aspect inflammatoire de la paroi et de la graisse péri-digestive d’aspect peignée (comb-sign)

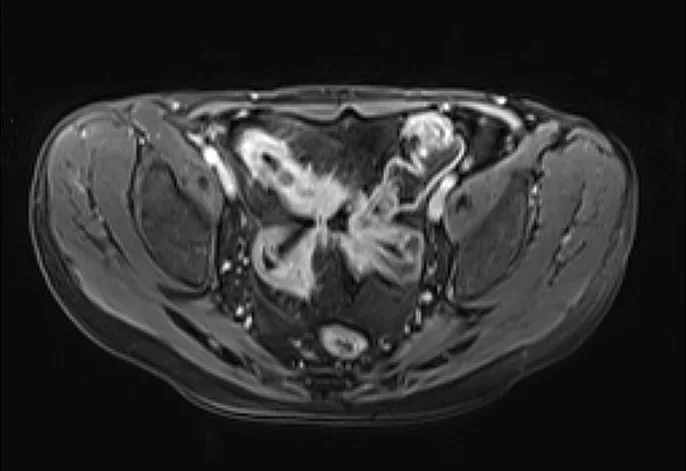
Image 8. Phénotype pénétrant de MC en Entéro-IRM ; fistule iléo-iléale (coupes pondérées en T1 après injection de Gadolinium)

Image 9. Phénotype sténosant de MC en Entéro-IRM ; sténose courte de l’iléon terminal avec distension du grêle d’amont (coupes pondérées en T2)
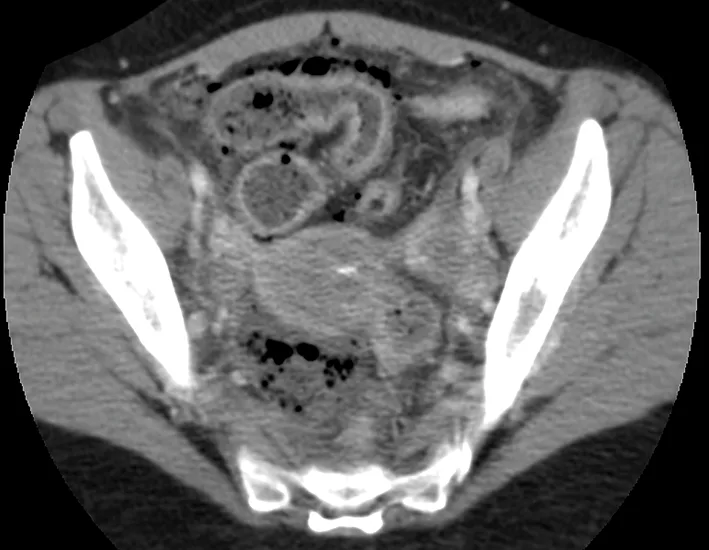
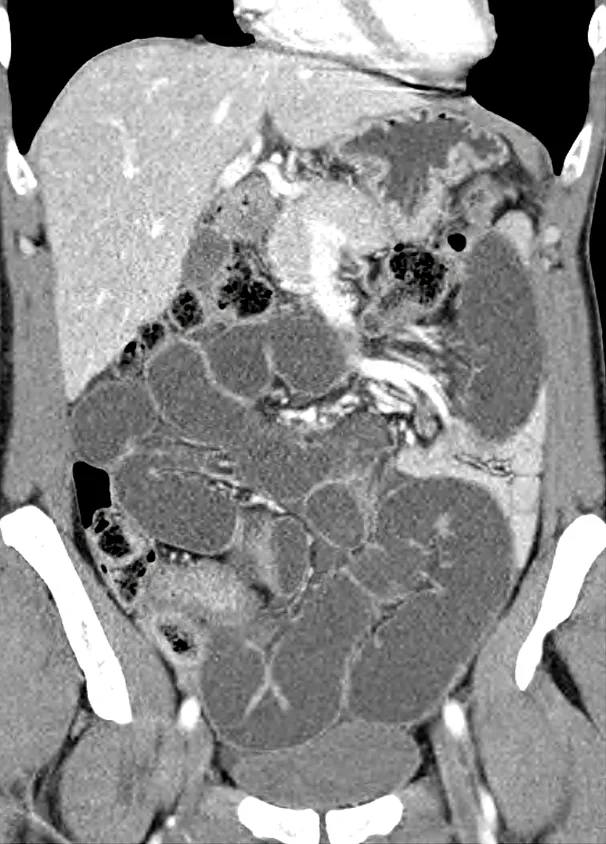
Le scanner abdomino-pelvien injecté peut être à l’origine de la découverte d’une MC, dans le contexte d’exploration d’un ventre « chirurgical », inaugurant parfois la pathologie. La découverte d’une occlusion mécanique du grêle en rapport avec un épaississement long circonférentiel de l’intestin grêle oriente vers la MC (image 10). En cas de syndrome appendiculaire avec signes de défense, la réalisation systématique d’un scanner donne parfois l’opportunité de diagnostiquer une MC mimant une appendicite aiguë (image 11a,b).

Image 10. Occlusion mécanique du grêle sur sténose longue dans un contexte de MC (scanner abdomino- pelvien injecté)

Image 11. Scanner abdomino-pelvien pour suspicion d’appendicite aigue révélant une iléite de MC avec abcès (a) abcès rétro-iléal, (b) logettes abcédées multiples peri-iléales
Une méta-analyse de 33 articles comparant les performances de l’échographie, du scanner et de l’IRM pour le diagnostic de la MC a montré des sensibilités et spécificités par segment moindres pour le scanner par rapport à l’échographie et à l’IRM, mais similaires pour les sensibilités et spécificités par patient. Les sensibilités par patient étaient respectivement pour l’échographie, l’IRM et le scanner de 90 %, 93 % et 84 % et les spécificités de 96 %, 93 % et 95 % (17). Cependant au vu de l’exposition aux RX lors d’acquisitions scanographiques, l’échographie et l’IRM sont à privilégier en priorité à la phase diagnostique.
Bilan d’une poussée
Le suivi de la maladie nécessite l’utilisation des examens les moins invasifs possibles. En effet, il n’est pas légitime de proposer des examens d’imagerie irradiants lors du bilan de simples poussées pour lesquelles le suivi clinico-biologique est souvent suffisant. À ce stade, l’imagerie permet éventuellement de réaliser un bilan d’extension de la poussée et d’éliminer une complication.
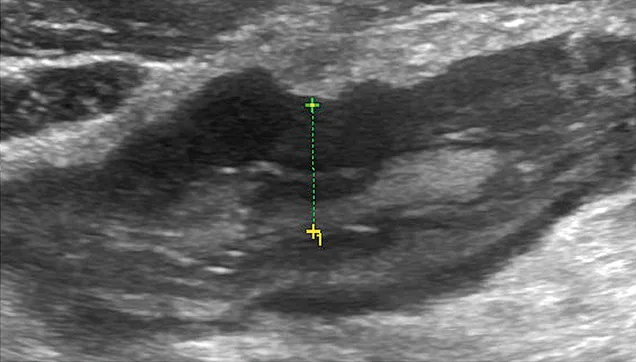
L’échographie est l’examen le plus facile à mettre en œuvre, eu égard à son accessibilité, son faible coût et sa bonne acceptabilité par les patients (18). Son intérêt chez les enfants est indiscutable. Sa sensibilité poolée sur 8 études est de 86 % (95 % CI 83 – 88 %) et sa spécificité de 94 % (95 % CI 93 – 95) pour la localisation de la maladie en comparaison à d’autres techniques d’imagerie et/ou la chirurgie et/ou l’endoscopie (19). En cas de poussée, l’échographie démontre un épaississement pariétal de plus de 4 mm au niveau du grêle, l’enjeu étant de réaliser correctement cette mesure depuis la séreuse jusqu’à la lumière digestive, ce qui nécessite une courbe d’apprentissage. La pathologie située au niveau du carrefour iléo- caecal sera la plus simple à analyser. En effet, la sensibilité de détection des anomalies en échographie est supérieure au niveau du côlon ascendant et de l’iléon terminal. Selon la gravité du dommage pariétal, la paroi pourra être plus ou bien différenciée (image 12). Contrairement à la rectocolite hémorragique ne touchant que la superficie de la paroi intestinale, l’atteinte peut être transmurale en échographie s’accompagnant parfois d’ulcère(s) ou de fistule(s) borgne(s). La présence d’une hyperhémie ou d’un aspect en verre dépoli de la graisse péri-digestive est fréquente en cas de poussée inflammatoire (image 6b).

Image 12. Image échographique de dédifférenciation pariétale
L’échographie peut cependant être limitée par les localisations profondes ou proximales de la maladie et sa difficulté à quantifier précisément l’extension lors des atteintes longues (19). L’expérience des opérateurs est hétérogène, souvent sans relecture rétrospective possible.
L’entéro-IRM a d’excellents résultats dans l’analyse de l’extension de la MC avec des résultats supérieurs pour les localisations jéjunales par rapport à l’échographie et en cas d’atteinte longue de la maladie (images 13, 14) (19). Dans une méta-analyse datant de 2011, la sensibilité de l’IRM pour faire le bilan d’extension de la MC était de 74 % (95 % CI 68 – 80) et sa spécificité de 91 % (95 % CI 86 – 95). La tolérance de l’échographie par les patients est cependant supérieure à celle de l’entéro-IRM (18) et les difficultés d’accès aux plateaux techniques d’IRM au moment des poussées de façon rapide, orientent plutôt vers l’échographie à cette phase de la maladie.

Image 13. Intérêt de l’entéro-IRM dans le bilan d’extension lors d’atteinte grêlique longue ; coupes axiales pondérées en T2

Image 14. Intérêt de l’entéro-IRM dans la détection des anomalies proximales (jéjunum)
L’entéroscanner et l’entéro-IRM ont une efficacité comparable pour réaliser le bilan d’extension et le bilan topographique de la maladie dans une étude prospective menée chez 44 patients (20). Cependant, au vu des performances démontrées de l’échographie et de l’entéro-IRM pour faire le bilan d’extension de la maladie, il faudra éviter de réaliser des scanners lors des poussées de la MC en raison de l’exposition répétée aux RX.
Évaluation de l’inflammation dans la MC sous traitement
L’évaluation de la cicatrisation muqueuse est l’objectif ultime des traitements. L’imagerie pourrait être une alternative non invasive et mieux acceptée par les patients que les examens endoscopiques pour objectiver l’état pariétal. L’entéro-IRM est l’examen de choix pour étudier l’inflammation dans la MC tant par son étude morphologique « classique » que pour son analyse en tant que « biomarqueur » de l’inflammation.
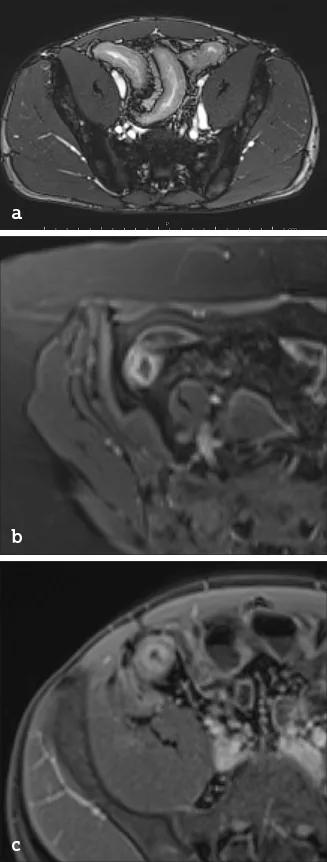
Les signes morphologiques corrélés à l’inflammation sont l’épaisseur pariétale, l’hypersignal en T2 relatif de la paroi, l’intensité de la prise de contraste à la phase tardive, le type de prise de contraste (en cocarde à la phase parenchymateuse), le signe du peigne (« comb sign »), la présence d’ulcères pariétaux et/ou d’abcès (images 15a, b) (22). L’étude du signal sur les coupes pondérées en diffusion et les mesures quantitatives sur la cartographie ADC sont intéressantes dans l’étude de l’inflammation (23).

Images 15a, 15b, 15c. Signes inflammatoires de MC en Entéro-IRM (a) Hypersignal T2 relatif de la paroi par rapport au muscle adjacent (b) Prise de contraste stratifiée en cocarde de la paroi (c). Ulcération pariétale en pondération T1 avec injection de Gadolinium
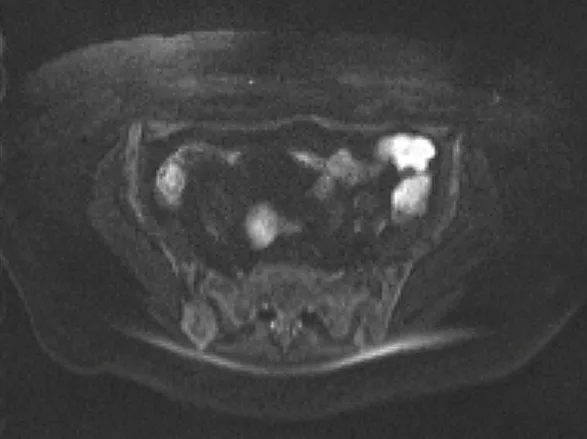
L’hypersignal en diffusion est corrélé à l’activité de la maladie (24, 25) (image 16). Le seuil de valeur de coefficient de diffusion apparent (CDA) de 1,6 10-3 mm2/sec distinguerait les anses inflammatoires de celles qui ne sont pas avec une sensibilité de 84,2 % et une spécificité de 100 % (25). Cependant, trop de chevauchements persistent à ce jour pour « trier » formellement les anses pathologiques et non pathologiques et une standardisation des gradients de diffusion utilisés pour réaliser des mesures de CDA reproductibles est nécessaire.

Image 16. Entéro-IRM montrant un hypersignal de la paroi iléale sur les coupes pondérées en Diffusion (b800)
Outre l’analyse sémiologique morphologique « classique », plusieurs scores ont été développés afin de quantifier de façon la plus reproductible possible l’inflammation au cours de la MC : le Magnetic Resonnance Index of Activity ou score MaRIA (Barcelone) (26), le score de Clermont (prenant en compte la diffusion et MaRIA) (25), le score CDAS (Londres) (27), le score MICD (Belgique) (28), le score CDMRIS (GETAID). L’objectif de standardisation des suivis par des scores IRM est nécessaire afin de fiabiliser les lectures, mais ces scores nécessitent d’importantes séries de validation. Le score MaRIA comparé au standard coloscopique prend en compte de façon exclusive le côlon et l’iléon terminal et nécessite un lavement au cours de l’IRM, complexe pour le patient dans la machine. Le CDMRIS repose sur une construction statistique pure et reprend l’exploration de tout le tube par segment de 20 cm. Les caractéristiques de chacun de ces scores sont résumées dans le tableau 1.
| MaRia | Rimola | Gut 2009 | MaRIA (segmentaire) = 1,5*épaisseur paroi (mm) + 0,02*RRP + 5*oedème + 10*ulcération MaRIA (global) = Σ maria (rectum + sigmoïde + descendant + transverse + ascendant + iléon) |
| Clermont | Buisson | Alim Pharamco Ther 2013 | 1.646*épaisseur paroi + 1.321*ADC + 5.613*oedème + 8.306*ulcérations + 5.039 |
| MICD | Van Assche | J Crohns colitis 2013 | pondération de 0 à 3 attribuée à chaque signe signes étudiés = épaisseur pariétale, signes extra-digestifs, intensité de réhaussement |
| CDAS | Steward | Eur J Radiol 2012 | 1.79 + 1.34 épaisseur paroi + 0.94 score signal T2 paroi |
| CDMRIS | Bouhnik GETAID | ECCO 2013 | 2*n(lm) + 3*n(s) + n(up) + n(p) + 3*n(f) + 4*n(a) avec n = nombre de segments de 20 cm lm = Intensité du Réhaussement légère à modérée en T1 ; s = intensité de réhaussement sévère en T1 up = ulcération profonde sans fistule ; f = fistule ; p = signe du peigne ; a = abcès |
Tableau 1. Résumé des scores d’évaluation de l’inflammation en IRM
Une méta-analyse publiée en 2015 montre une efficacité similaire du scanner et de l’entéro-IRM dans l’évaluation de l’activité dans la MC (86 et 84 % par patient, respectivement) (21). Mais les patients ne peuvent pas faire l’objet d’un suivi régulier par scanner et/ou par entéroscanner pendant le suivi sous traitement, dans un souci de limitation de leur exposition aux RX de façon répétée.
L’échographie est intéressante dans le monitoring simple des patients sous traitement, dans le prolongement de l’examen clinique, en complément des analyses biologiques. Peu coûteuse et non irradiante, elle permettra d’écarter rapidement lors du suivi une complication de la MC et de réaliser un bilan d’extension. La reproductibilité de l’examen est facilitée par l’étude d’un même segment et par un même opérateur, au mieux à l’aide du réseau d’archivage numérique (PACS) avec l’enregistrement de boucles vidéo. L’échographie reste cependant limitée par la variabilité de l’efficacité inter-opérateur, par les patients peu échogènes et enfin par les localisations proximales ou profondes de la MC. Il est difficile de l’utiliser dans les études cliniques devant ses difficultés de standardisation.
Recherche et bilan des complications (fistules, abcès, sténoses)
Bilan des sténoses
Une cohorte de 306 patients qui présentait un phénotype non sténosant non pénétrant au diagnostic dans 81 % des cas, évoluait dans 51 % des cas vers un phénotype plus agressif à 20 ans selon la classification de Montréal (29). Le phénotype sténosant est observé dans 15 % des cas au diagnostic et dans 43 % des cas après 10 ans d’évolution (30, 31). L’imagerie a un rôle majeur dans l’étude des sténoses dans la MC. Ses objectifs sont multiples : (i) descriptif (dénombrer les sténoses ; localiser la(les) sténose(s) ; caractériser les sténoses – longueur, caractéristiques inflammatoire et/ou fibreuse -), (ii) de réaliser une cartographie pré-opératoire, (iii) de rechercher des signes associés de maladie pénétrante, et (iv) de prédire la réponse au traitement par anticorps anti-TNF-a (32). Une étude menée chez 97 patients a en effet identifié des facteurs pronostiques de l’efficacité de l’adalimumab chez des patients de MC porteurs de sténoses symptomatiques à 24 semaines, en associant des critères cliniques et IRM. Une sténose mesurant moins de 12 cm, l’absence de fistule, une distension du grêle en amont de la sténose mesurée entre 18 et 29 mm et une prise de contraste marquée au temps tardif de la paroi étaient les items IRM prédictifs d’une réponse favorable aux anticorps anti-TNF-a sur le long terme (32). En entéro-IRM, une sténose se caractérise par une distension grêlique en amont de la zone d’épaississement (32). Les caractéristiques inflammatoires associent préférentiellement un épaississement pariétal du grêle de plus de 6 mm, un hypersignal en pondération T2, une prise de contraste intense et stratifiée au temps parenchymateux en pondération post-injection, un hypersignal en pondération de diffusion (à l’étude des coupes réalisées avec le facteur b élevé). La présence d’ulcérations pariétales profondes et d’une hyperhémie mésentérique sont également évocateurs d’une sténose inflammatoire (33, 34). Mais la prise de contraste au temps tardif est possible en cas d’inflammation (32) (image 17). Dans une étude menée chez 53 malades, l’inflammation était corrélée au score de fibrose (r = 0,63) (22) et il est parfois complexe de différencier formellement les sténoses inflammatoires des sténoses fibreuses car les deux composantes sont souvent associées.

Image 17. Prise de contraste homogène et intense au temps tardif de l’injection en Entéro-IRM
Il est possible de détecter une sténose en échographie dans des mains entraînées, avec une sensibilité de détection accrue après ingestion de produit de contraste oral (majoration de la sensibilité de 74 à 89 %) (35). Dans trois études poolées ayant pour référence standard la chirurgie, la sensibilité de l’échographie était de 79 % et sa spécificité de 92 %.
L’entéro-scanner présente également une excellente sensibilité dans la détection des sténoses (images 18 et 3). C’est un très bon examen pour réaliser un bilan d’extension de la MC notamment pour les cartographies pré-opératoires. Dans une étude menée chez 158 malades atteints de 78 sténoses, la spécificité du scanner était légèrement supérieure à celle de l’IRM (99 vs. 94 %) (7). La sensibilité et la spécificité du scanner et de l’entéro-IRM pour le diagnostic de sténose était similaire dans une étude prospective réalisée chez 44 patients (sensibilité : 85 vs. 92 % ; spécificité : 100 vs. 90 %) (20).

Image 18. Sténose inflammatoire iléale en scanner avec injection d’iode au temps portal
Au total scanner et entéro-IRM sont d’excellents outils dans la détection des sténoses avec des arguments plus en faveur de l’utilisation de l’IRM non irradiante et dont la résolution en contraste permet de mieux étudier les composantes fibreuses et inflammatoires des sténoses (image 19).

Image 19. Sténose iléale terminale d’aspect inflammatoire en pondération T1 post-injection de Gadolinium en Entéro-IRM
Bilan des fistules, abcès et phlegmons
Les fistules se développent surtout dans les atteintes iléales de la MC, le plus souvent iléo-iléales mais aussi entéro-cutanées, entéro-vésicales, compliquant une inflammation pariétale transmurale suivie d’une perforation péri-digestive (36). Ces fistules peuvent se compliquer d’abcès ou de phlegmons (suppurations péritonéales mal limitées). Au diagnostic, 15,5 % des patients présentent un phénotype pénétrant de la maladie. Échographie, scanner injecté et entéro-IRM ont une grande efficacité pour le diagnostic des complications pénétrantes. L’échographie et le scanner peuvent permettre de réaliser des drainages d’abcès. L’IRM et le scanner sont plus sensibles pour le diagnostic de trajets fistuleux profonds (images 20 et 21). La sensibilité poolée de plusieurs études dans le diagnostic de fistule en IRM était de 76 % pour une spécificité de 96 % (19). Les résultats de l’échographie dans l’étude des fistules sont bons, mais le scanner et l’IRM lui seront préférés s’ils sont disponibles (37). Devant une suspicion d’abcès, l’échographie et le scanner permettent une meilleure rapidité d’accès au diagnostic qu’en IRM au vu de la modeste disponibilité des machines en urgence. Le scanner permet un meilleur bilan d’extension en profondeur en cas d’abcès complexe (image 11).

Image 20. Abcès inter-anse associé à une confluence d’anses jéjunales et iléales fistulisées entre elles en Entéro-IRM

Image 21. Fistule iléo-colique en pondération T1 après injection de Gadolinium en Entéro-IRM
Recherche de récidive post-opératoire
La recherche de signes de récidive post-opératoire (RPO) est un objectif majeur. Elle permet de traiter précocement les malades par anticorps anti-TNF-a. Le taux de récidive anastomotique et dans l’iléon après la chirurgie est en effet élevé (au moins 60 % à un an et 80 % à trois ans). Le score endoscopique de Rutgeerts a pour but de prédire le risque de récidive clinique après une résection iléo-colique droite et reste le seul validé aujourd’hui (38). Les recommandations actuelles chez les patients opérés sont la réalisation d’une endoscopie de surveillance 6 à 12 mois après la chirurgie afin d’établir le score de Rutgeerts, puis tous les 2 ans. Cependant la recherche de techniques non invasives permettant de prouver une RPO, sans réalisation d’endoscopies systématiques dont l’acceptabilité est réduite, constitue un défi pour la surveillance de ces malades. Une étude chez 58 malades atteints de MC compliquée ont bénéficié 6 à 12 mois après une iléo-colectomie droite, d’une échographie sans et avec injection de produit de contraste et d’une iléoscopie. Les patients dont l’épaisseur pariétale était inférieure à 3,5 mm avaient moins de 1 % de risque de présenter un score de Rutgeerts ≥ à i2 (39). L’entéro-IRM a été évaluée dans deux études comparées à l’endoscopie, avec d’excellentes performances en termes de sensibilité de détection de la récidive. Une entéro-IRM et une endoscopie (score de Rutgeerts) ont été réalisées chez 30 patients suspects de récidive de la MC après résection iléocolique, afin de comparer leur efficacité. Un score IRM classait les patients en 4 niveaux : MR0 (aucune caractéristique anormale), MR1 (modifications muqueuses minimes), MR2 (iléite aphtoïde diffuse, récidive modérée) et MR3 (récidive grave avec modifications transmurales et extramurales). En comparant les scores IRM et de Rutgeerts, l’accord moyen des observateurs pour le score total était de 77,8 %. En comparant uniquement les scores inférieurs ou supérieurs à MR2 (seuil indiquant la nécessité d’un traitement médical), il existait un accord de 95,1 % (40). Une étude de faisabilité de l’IRM colique sans préparation orale ni rectale et avec séquence de diffusion a étudié la corrélation entre les scores endoscopiques et des scores IRM chez 96 patients atteints de MICI. L’hypersignal en diffusion était prédictif de la récidive inflammatoire endoscopique dans la RCH et la MC [Odds ratio (OR) respectifs de 13,26 et 2,67] (41) (image 22).

Image 22. Hypersignal en Diffusion du colon transverse en Colo-IRM (coupe frontale)
Conclusion
L’imagerie joue un rôle très important dans la prise en charge des patients atteints de MC. La recherche permanente de réduction de l’exposition des patients aux RX doit faire réserver le scanner à l’analyse de complications aiguës, alors que l’entéro-IRM et l’échographie permettront un suivi régulier de la maladie. L’entéro-IRM apparaît comme la technique la plus reproductible pour effectuer le bilan d’extension de la maladie, le suivi de l’inflammation sous traitement et pour le bilan des sténoses. L’évolution du nombre d’installations de machines d’IRM devrait permettre de substituer le maximum de scanner ou entéro- scanner réalisés dans la MC, dans un souci de pertinence et de sécurité des patients.
Références
- Puylaert JB. Mesenteric adenitis and acute terminal ileitis: US evaluation using graded compression. Radiology. 1986; 161(3):691-5.
- Serafin Z, Białecki M, Białecka A, Sconfienza LM, Kłopocka M. Contrast-enhanced ultrasound for detection of Crohn’s disease activity: systematic review and meta-analysis. J Crohns Colitis. 2016;10:354-62.
- Buisson A, Hordonneau C, Goutte M, Boyer L, Pereira B, Bommelaer G. Diffusion-weighted magnetic resonance imaging is effective to detect ileocolonic ulcerations in Crohn’s disease. Aliment Pharmacol Ther. 2015;42:452-60.
- Recommandations ANSM janvier 2018 « Produits de contraste à base de gadolinium et rétention de gadolinium dans le cerveau et dans d’autres tissus : suspension des AMM de l’acide gadopentétique et du gadodiamide utilisés en intraveineux, restriction de l’AMM de l’acide gadobénique à l’imagerie du foie et modification de l’information des autres spécialités maintenues – Lettre aux professionnels de santé ».
- Tielbeek JA, Bipat S, Boellaard TN, Nio CY, Stoker J. Training readers to improve their accuracy in grading Crohn’s disease activity on MRI. Eur Radiol. 2014;24:1059-67.
- Aufort S, Charra L, Lesnik A, Bruel JM, Taourel P. Multidetector CT of bowel obstruction: value of post-processing. Eur Radiol. 2005;15:2323-9.
- Panés J, Bouzas R, Chaparro M, et al. Systematic review: the use of ultrasonography, computed tomography and magnetic resonance imaging for the diagnosis, assessment of activity and abdominal complications of Crohn’s disease. Aliment Pharmacol Ther. 2011;34:125-45.
- Estay C, Simian D, Lubascher J, Figueroa C, O’Brien A, Quera R. Ionizing radiation exposure in patients with inflammatory bowel disease: are we overexposing our patients? J Dig Dis. 2015;16:83-9.
- Desmond AN, O’Regan K, Curran C et al. Crohn’s disease: factors associated with exposure to high levels of diagnostic radiation. Gut. 2008;57:1524-9.
- Chatu S, Subramanian V, Pollok RC. Meta-analysis: diagnostic medical radiation exposure in inflammatory bowel disease. Aliment Pharmacol Ther. 201;35:529-39.
- Levi Z, Fraser E, Krongrad R, et al. Factors associated with radiation exposure in patients with inflammatory bowel disease. Aliment Pharmacol Ther. 2009;30:1128-36.
- Kordbacheh H, Baliyan V, Serrao J, et al. Imaging in Patients with Crohn’s Disease: Trends in Abdominal CT/MRI Utilization and Radiation Exposure Considerations over a 10-Year Period. Inflamm Bowel Dis. 2017;23:1025-33.
- Fraquelli M, Colli A, Casazza G, et al. Role of US in detection of Crohn disease: meta-analysis. Radiology. 2005;236:95-101.
- Louis E, Collard A, Oger AF, et al. Behaviour of Crohn’s disease according to the Vienna classification: changing pattern over the course of the disease. Gut. 2001;49:777-82.
- Silverberg MS, Satsangi J, Ahmad T, et al. Toward an integrated clinical, molecular and serological classifi cation of inflammatory bowel disease: Report of a Working Party of the 2005 Montreal World Congress of Gastroenterology. Can J Gastroenterol. 2005;19 (suppl A):5–36.
- Satsangi J, Silverberg MS, Vermeire S, et al. The Montreal classification of inflammatory bowel disease: controversies, consensus, and implications Gut. 2006;55:749–53.
- Horsthuis K, Bipat S, Bennink RJ, Stoker J. Inflammatory bowel disease diagnosed with US, MR, scintigraphy, and CT: meta-analysis of prospective studies. Radiology 2008;247:64–79.
- Comparative acceptability and perceived clinical utility of monitoring tools: a nationwide survey of patients with inflammatory bowel disease. Buisson A, Gonzalez F, Poullenot F, et al. Inflamm Bowel Dis. 2017;23(8):1425-1433.
- Panes J, Bouzas R, Chaparro M, et al. Systematic review: the use of ultrasonography, computed tomography and magnetic resonance imaging for the diagnosis, assessment of activity and abdominal complications of Crohn’s disease. Aliment Pharmacol Ther. 2011;34:125–45.
- Fiorino G, Bonifacio C, Peyrin-Biroulet L, et al. Prospective comparison of computed tomography enterography and magnetic resonance enterography for assessment of disease activity and complications in ileocolonic Crohn’s disease. Inflamm Bowel Dis. 2011;17:1073–80.
- Puylaert CAJ, Tielbeek JA, Bipat S, Stoker J. Grading of Crohn’s disease activity using CT, MRI, US and scintigraphy: a meta-analysis Eur Radiol. 2015;25:3295–313.
- Zappa M, Stefanescu C, Cazals-Hatem D, et al. Which magnetic resonance imaging findings accurately evaluate inflammation in small bowel Crohn’s disease? A retrospective comparison with surgical pathologic analysis. Inflamm Bowel Dis. 2011;17:984-93.
- Tielbeek JA, Ziech ML, Li Z, et al. Evaluation of conventional, dynamic contrast enhanced and diffusion weighted MRI for quantitative Crohn’s disease assessment with histopathology of surgical specimens. Eur Radiol. 2014;24:619-29.
- Puylaert CAJ, Tielbeek JAW, Schüffler PJ et al. Comparison of contrast-enhanced and diffusion- weighted MRI in assessment of the terminal ileum in Crohn’s disease patients. Abdom Radiol. 2018. Epub ahead of print.
- Buisson A, Joubert A, Montoriol PF, et al. Diffusion-weighted magnetic resonance imaging for detecting and assessing ileal inflammation in Crohn’s disease. Aliment Pharmacol Ther. 2013;37:537-45.
- Rimola J, Rodriguez S, García-Bosch O, et al. Magnetic resonance for assessment of disease activity and severity in ileocolonic Crohn’s disease. Gut. 2009;58:1113-20.
- Steward MJ, Punwani S, Proctor I, et al. Non-perforating small bowel Crohn’s disease assessed by MRI enterography: derivation and histopathological validation of an MR-based activity index. Eur J Radiol. 2012;81:2080-8.
- Van Assche G, Herrmann KA, Louis E, et al. Effects of infliximab therapy on transmural lesions as assessed by magnetic resonance enteroclysis in patients with ileal Crohn’s disease. J Crohns Colitis. 2013;7:950-7.
- Thia KT, Sandborn WJ, Harmsen WS, Zinsmeister AR, Loftus EV Jr. Risk factors associated with progression to intestinal complications of Crohn’s disease in a population-based cohort. Gastroenterology. 2010;139:1147–55.
- Pariente B, Peyrin-Biroulet L, Cohen L, Zagdanski AM, Colombel JF. Gastroenterology review and perspective: the role of cross-sectional imaging in evaluating bowel damage in Crohn disease. AJR Am J Roentgenol. 2011;197:42-9.
- Cosnes J, Cattan S, Blain A, et al. Long-term evolution of disease behavior of Crohn’s disease. Inflamm Bowel Dis. 2002;8:244–50.
- Bouhnik Y, Carbonnel F, Laharie D, et al. For the GETAID CREOLE Study Group. Efficacy of adalimumab in patients with Crohn’s disease and symptomatic small bowel stricture: a multicentre, prospective, observational cohort (CREOLE) study. Gut. 2018; 67:53–60.
- Zappa M, Stefanescu C, Cazals-Hatem D, et al. Which magnetic resonance imaging findings accurately evaluate inflammation in small bowel Crohn’s disease? A retrospective comparison with surgical pathologic analysis. Inflamm Bowel Dis. 2011;17:984-93.
- Punwani S, Rodriguez-Justo M, Bainbridge A, et al. Mural inflammation in Crohn disease: locationmatched histologic validation of MR imaging features. Radiology. 2009;252:712-20.
- Parente F, Maconi G, Bollani S, et al. Bowel ultrasound in assessment of Crohn’s disease and detection of related small bowel strictures: a prospective comparative study versus X ray and intraoperative findings. Gut. 2002;50:490-5.
- Pariente B, Cosnes J, Danese S, et al. Development of the Crohn’s disease digestive damage score, the Lémann score. Inflamm Bowel Dis. 2011;17:1415-22.
- Van Assche G, Dignass A, Reinisch W, et al; European Crohn’s and Colitis Organisation (ECCO). The second European evidence-based Consensus on the diagnosis and management of Crohn’s disease: Special situations. J Crohns Colitis. 2010;4:63-101.
- Rutgeerts P, Geboes K, Vantrappeng G, et al. Predictabiliy of the post-operative course of Crohn’s disease. Gastroenterology. 1990;99:956-63.
- Pallotta N, Giovannone M, Pezzotti P, et al. Ultrasonographic detection and assessment of the severity of Crohn’s disease recurrence after ileal resection. BMC Gastroenterol. 2010;10:69.
- Sailer J, Peloschek P, Reinisch W, Vogelsang H, Turetschek K, Schima W. Anastomotic recurrence of Crohn’s disease after ileocolic resection: comparison of MR enteroclysis with endoscopy. Eur Radiol. 2008;18:2512-21.
- Oussalah A, Laurent V, Bruot O, et al. Diffusion-weighted magnetic resonance without bowel preparation for detecting colonic inflammation in inflammatory bowel disease. Gut. 2010;59:1056-65.