Objectifs pédagogiques
- Connaître l’épidémiologie des arthropathies liées aux MICI
- Connaître la démarche diagnostique des spondylarthropathies et atteintes périhériques
- Connaître les effets secondaires rhumatologiques des traitements
ASAS : Assessment of spondyloarthritis international society
Les maladies inflammatoires chroniques de l’intestin (MICI), maladie de Crohn (MdC) et rectocolite hémorragique (RCH), s’accompagnent souvent de manifestations extra-digestives ; en effet, elles vont concerner environ 50 % des patients atteints de MICI à un moment ou l’autre de leur vie. Au sein de ces manifestations extra-digestives, les manifestations ostéo-articulaires (MOA) constituent les plus fréquentes.
Les MOA des MICI comprennent surtout des manifestations articulaires périphériques et des manifestations axiales, mais il existe également des enthésites périphériques et des dactylites. Ces manifestations font partie des spondyloarthrites (SpA) (1 et tableau 1), vérifiant ou ne vérifiant pas les critères de classification proposés comme ceux de l’ASAS (2 et tableaux 2 et 3). Enfin, on n’oubliera pas le retentissement osseux de la maladie et de son traitement corticoïde, domaine que l’on n’abordera pas ici.
Tableau 1. Terminologie permettant de décrire le phénotype clinique d’un patient atteint de spondyloarthrite (1)

Globalement les manifestations articulaires périphériques affectent 10 à 20 % des patients avec une MdC et 5 à 10 % des patients avec une RCH. Elles sont plus fréquentes chez les femmes. L’atteinte colique, ainsi que les atteintes péri-anales, sont associées à une plus grande fréquence de ces manifestations articulaires périphériques dans les MICI. D’autres facteurs ont été retrouvés comme associés, tels que l’érythème noueux, les aphtes, le pyoderma gangrenosum et les uvéites.
La plus grande partie de ces atteintes est constituée par les arthralgies inflammatoires. Les arthrites vraies, beaucoup moins fréquentes, répondent aux critères de classification des SpA périphériques de l’ASAS (2).
Depuis le travail empirique d’Orchard publié en 1998, les arthralgies/arthrites périphériques associées aux MICI sont décrites sous deux formes dominantes : le type 1, pauci-articulaire et le type 2, poly- articulaire (5). La prévalence des atteintes de type 1 est de 29 % dans la MdC et 35 % dans la RCH. Les arthralgies/arthrites touchent moins de cinq articulations, particulièrement les chevilles, les genoux, les hanches, les poignets, les coudes et les épaules. L’atteinte est souvent aiguë, asymétrique et migratrice. On peut considérer que 20-40 % des patients avec une MICI auront au moins un épisode d’arthralgies ou arthrite. Ces arthralgies/arthrites de type 1 sont en général corrélées à l’activité de la MICI. Elles cèdent spontanément en général dans les dix semaines. Elles peuvent être plus rapidement contrôlées encore si la rémission de la MICI est obtenue par une intervention thérapeutique. Concernant les arthralgies/arthrites de type 2, leur prévalence est de 20 % dans la MdC et de 24 % dans la RCH. Le seul facteur retrouvé comme associé à cette atteinte de type 2 est l’uvéite. Il s’agit d’une atteinte poly-articulaire touchant au moins cinq articulations et prédominant sur les petites articulations, tout particulièrement les MCP. Elle peut être symétrique dans sa répartition. Son évolution est plutôt chronique, la poussée persistant souvent de nombreux mois, voire plusieurs années. Enfin, il n’y a pas de parallélisme entre le développement ou la persistance de ces atteintes et l’activité de la MICI. Notons qu’alors que l’ensemble de ces manifestations articulaires périphériques ne s’accompagne pas de lésion radiographique (pincement, érosion), il peut y avoir, de temps à autre, des formes érosives dans ce type 2 (5).
Une étude génétique est venue augmenter la robustesse de cette séparation entre ces deux types, puisque les antigènes HLA B27, B35 et DR103 ont été retrouvés comme associés au type 1 alors que c’est l’antigène HLA B44 qui a été retrouvé comme associé au type 2 (6). Néanmoins, cette classification en 2 types n’a pas été reproduite sur des populations de plus large taille.
Tableau 2. Critères ASAS des spondyloarthrites axiales (2)
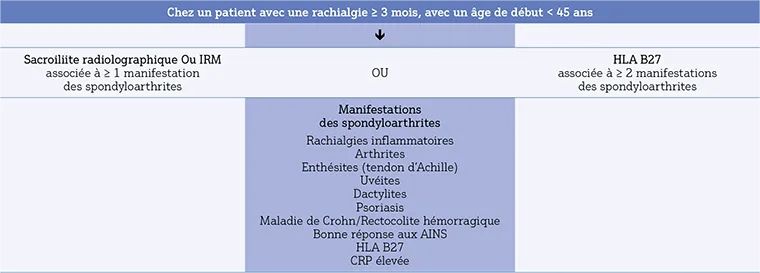
Tableau 3. Critères ASAS des spondyloarthrites périphériques (2)

L’atteinte axiale symptomatique (rachis, sacroiliaques, paroi thoracique antérieure) paraît moins fréquente que l’atteinte articulaire périphérique, de l’ordre de 3 à 5 % des patients avec MICI ; il faut cependant noter que ces valeurs sont variables dans la littérature et que des fréquences de 25 % ont été rapportées.
Les hommes sont plus fréquemment concernés que les femmes. L’atteinte axiale est en général indépendante de l’activité de la MICI. L’atteinte radiographique des sacro-iliaques (sacroiliite) est, elle, fréquente, retrouvée chez 20 à 50 % des patients et donc souvent asymptomatique, du moins au moment où est pratiquée la radiographie. Mais, dans la majorité des cas, elle n’est pas associée à l’antigène HLA B27, et n’évolue pas vers un enraidissement rachidien de spondylarthrite ankylosante (SA).
L’atteinte symptomatique et avec enraidissement axial (syndesmophytose) de SA est observée chez 1 à 10 % des patients.
L’enthésite constitue la lésion anatomique caractéristique des SpA, comme l’est la synovite pour la polyarthrite rhumatoïde. Elle est constituée d’une atteinte inflammatoire douloureuse de l’enthèse, c’est- à-dire l’insertion dans l’os des tendons, ligaments et capsules. Cette inflammation évolue assez souvent vers une « cicatrisation » anormale, ossifiante, qui explique la production osseuse constatée dans la spondyloarthrite (syndesmophyte au rachis, « épine calcanéene » par exemple, au talon). La dactylite est un épisode de gonflement douloureux et global d’un doigt ou d’un orteil, souvent appelé « doigt ou orteil en saucisse ». Elles ont été globalement peu étudiées dans le cadre des MICI. Elles semblent globalement moins fréquentes que dans le cadre des autres SpA, leur fréquence étant augmentée en cas d’association au psoriasis (effet surtout du « terrain » psoriasique ?) (7). Cependant, des analyses en échographie- doppler des enthèses de patients atteints de MICI suggèrent des anomalies plus fréquentes que ce qui est rapporté cliniquement, sans que l’on connaisse encore l’intérêt réel de ces anomalies ultrasonores (8).
Une étude néerlandaise, recherchant de façon standardisée des symptômes évocateurs de SpA chez 350 patients atteints de MICI, en a retrouvé au moins un chez 129 (36,9 %) d’entre eux. Seuls 66 (51,2 %) de ces derniers avaient déjà vu un rhumatologue, le diagnostic de SpA ayant été posé chez 38 (58 %) d’entre eux (18 SpA axiale et 20 SpA périphérique). Ainsi les symptômes de type SpA seraient présents chez au moins 1/3 des patients avec MICI, mais ne conduiraient à la consultation rhumatologique que dans un cas sur deux, consultation qui pourtant retient le diagnostic de SpA dans plus d’un cas sur 2 (9).
Notons enfin qu’il est fréquent que la symptomatologie ne soit pas purement axiale ou périphérique chez un patient donné, mais mixte, soit de façon concomitante, soit au cours du temps.
Comme pour l’ensemble de la sphère des SpA, le diagnostic repose le plus souvent sur un faisceau d’arguments, puisqu’il n’y a pas de gold standard de référence du diagnostic. Les cas où le diagnostic est rapide et sans grand doute est celui de l’arthrite vraie périphérique, stérile et sans auto-anticorps chez un patient ayant une MICI, ou celui, rare, de la dactylite évidente. La radiographie de bassin de face à la recherche d’une sacroiliite garde un petit intérêt, limité par la variabilité d’interprétation des images et par ses faibles sensibilité et spécificité. Le scanner des sacroiliaques peut parfois aider à affirmer une atteinte structurale de SpA, surtout chez un sujet jeune (les lésions perdant en spécificité avec l’âge).
Parfois l’IRM peut assoir le diagnostic devant une symptomatologie axiale isolée lorsqu’elle montre une inflammation sacro-iliaque suffisamment nette et de bonne localisation pour conférer une bonne spécificité. Plus rarement encore, c’est l’IRM du rachis qui apporte une « certitude ». La scintigraphie osseuse n’a quasiment plus aucune place dans ce domaine. Dans les autres cas, c’est l’association de symptômes de l’appareil locomoteur d’horaire inflammatoire à l’existence d’une MICI amènera le clinicien au diagnostic de SpA, mais avec un niveau de preuve moins élevé.
Dans tous les cas, l’échange entre le gastroentérologue et le rhumatologue est indispensable.
Pour les formes axiales pures ou très prédominantes, s’il est acceptable d’un point de vue gastroentérologique de recourir aux AINS, ceux-ci restent le traitement de première intention. En cas d’échec, ou d’intolérance ou de déséquilibre de la MICI, on recourra à un traitement anti-TNFa.
Pour les formes articulaires périphériques, on peut essayer un traitement de fond synthétique conventionnel, sulfasalazine ou méthotrexate, si besoin l’un après l’autre, en y ajoutant les gestes locaux (infiltrations) si adaptés. En cas d’échec, on recourra là encore à un traitement anti-TNFa.
En cas d’échec d’un anti-TNFa, on préfèrera en général l’essai d’un deuxième anti-TNFa plutôt que celui d’un anti-Il17 (secukinumab, ixékizumab), de peur de déséquilibrer la MICI. L’ustékinumab n’a pas montré son efficacité dans la spondyloarthrite axiale et n’a une AMM rhumatologique que pour le rhumatisme psoriasique (avec des études pivots qui ont inclus des patients ayant des arthrites périphériques).
Il faut aborder le problème des manifestations rhumatologiques inflammatoires apparaissant sous traitement anti-TNFa donné pour la MICI, avec une MICI bien contrôlée. Deux hypothèses dominent : le rare lupus induit, qu’il conviendra d’éliminer de principe (Ac anti DNA natifs de type IgG), et les fréquentes « manifestations paradoxales ». Celles-ci peuvent prendre à peu près toutes les présentations topographiques. Si les traitements symptomatiques peuvent être utilisés avec succès et bonne tolérance, la situation est favorable et l’on continue ainsi. Dans le cas contraire, si le retentissement fonctionnel est important, on peut être amené à changer de biomédicament en espérant ne pas retrouver les mêmes douleurs rhumatologiques.
Toute reproduction ou réécriture, totale ou partielle, sans l’accord préalable écrit de la FMC HGE est interdite.
FMC HGE : Organisme certifié Qualiopi pour la catégorie ACTIONS DE FORMATION.