Lien d’intérêt
Formateur pour Olympus, Cook, Pentax, Boston
Co-inventeur de CONECCT app, ATRACT et IPEFIX
Mots-clés
caractérisation, chromoendoscopie, stratégie thérapeutique
Abréviations
CONECCT : colorectal neoplasia classification to choose the treatment ; NBI : narrow band imaging ; BLI : Blue laser imaging ; FTRD : full thickness resection device ; HEH : Hopital Edouard Herriot
Introduction
Une fois détectées, les lésions colorectales doivent être caractérisées afin de prédire l’histologie en temps réel au cours de l’endoscopie et choisir la meilleure option thérapeutique pour chaque lésion.
Le meilleur moyen de prédire l’histologie d’une lésion colorectale n’est pas la biopsie car elle n’analyse qu’une partie infime de la lésion et ne détecte pas forcément l’histologie la plus péjorative contenue dans la tumeur. Paradoxalement, elle génère une fibrose sous-muqueuse parfois intense compromettant ou gênant la résection endoscopique ultérieure. L’intelligence artificielle dont on attend beaucoup n’est pas encore suffisamment performante pour prédire les différentes histologies et n’est pour l’instant qu’une aide pour différencier polypes hyperplasiques et lésions néoplasiques. Elle doit encore beaucoup évoluer et pour l’instant c’est à l’expertise humaine qu’il faut se fier. Néanmoins cette dernière ne s’acquiert qu’après une importante formation.
Classification conecct
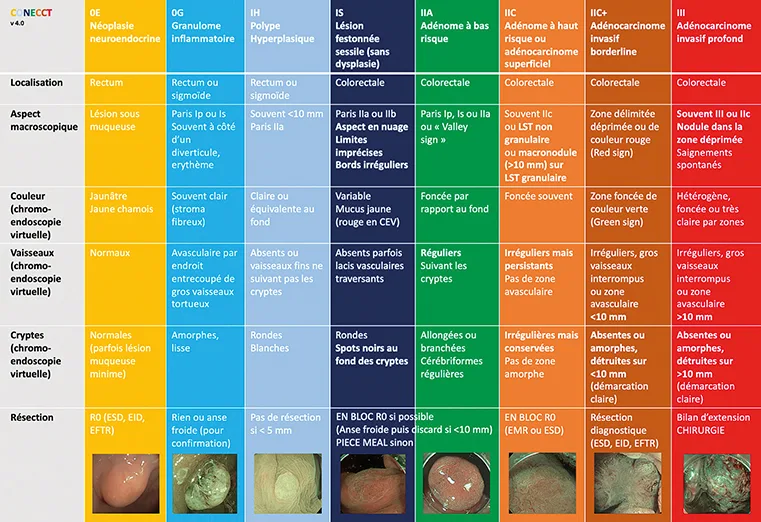
En simplifiant, il existe 7 types de lésions colorectales fréquentes et qui peuvent être différenciées par la caractérisation endoscopique avec chromoendoscopie (détaillées ci-après).

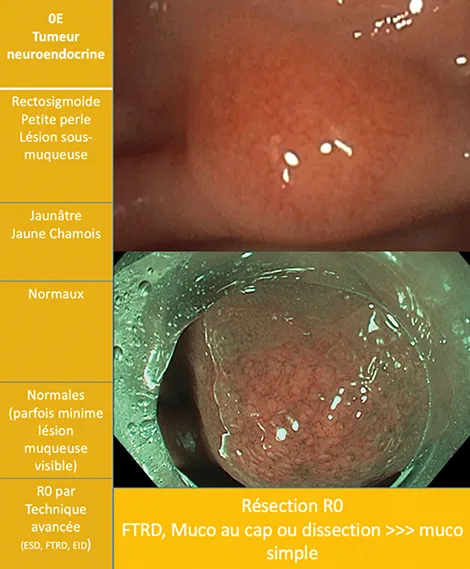
1) Les tumeurs neuroendocrines rectales (CONECCT OE) sont un type rare de lésion, plus difficile à caractériser que les autres car si le point de départ de ces lésions est muqueux par néoplasie des cellules neuroendocrines de la muqueuse, son développement est majoritairement sous-muqueux avec de ce fait une sur-élévation de la paroi couverte d’une muqueuse majoritairement normale. De ce fait, l’aspect est celui d’une lésion sous- muqueuse rectale, souvent jaunâtre, assez dure à la palpation par un outil endoscopique et qui présente parfois une toute petite zone d’altération du pattern muqueux ou vasculaire à son sommet. Il est très important de les reconnaître afin de proposer une résection R0 par une technique avancée (1,2). Les techniques les plus efficaces pour atteindre le R0 sont la résection FTRD et la dissection sous-muqueuse (et peut-être la dissection intermusculaire dans le futur). La mucosectomie standard donne de mauvais résultats de R0 et si la mucosectomie est la seule option disponible, elle doit être associée avec une ligature élastique préalable ou une succion dans un capuchon de mucosectomie. En cas de résection non R0, une révision de la cicatrice par dissection ou FTRD est justifiée car plus de 40 % des cicatrices contiennent encore du tissu neuroendocrine résiduel (3).

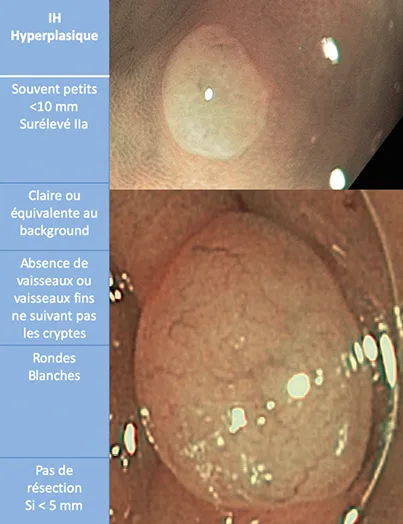
2) Les polypes hyperplasiques simples (CONECCT IH) du rectosigmoïde, qui n’ont aucun potentiel néoplasique sont le plus souvent nombreux, petits < 5 mm et dépassent exceptionnellement 10 Ils apparaissent plus clairs [NICE I (4)] que la muqueuse environnante en chromoendoscopie virtuelle (NBI, BLI, iscan EO), sous forme de petite perle surélevée [Paris IIA (5)]. Ils ne sont jamais déprimés ou ulcérés, mais peuvent rarement avoir une petite ombilication centrale. Les cryptes muqueuses sont rondes ou étoilées et à fond clair en chromoendoscopie [Kudo I ou II (6)]. Les vaisseaux profonds sont visibles au travers de la muqueuse de surface et l’on voit ainsi des lacis vasculaires sombres traversant la lésion et s’affinant progressivement jusqu’à un capillaire trop fin pour être vu. Ces vaisseaux ressemblent à l’extrémité d’une racine de carotte qui s’affine progressivement. À très gros niveau de zoom (> 100), on commence aussi à voir des capillaires vasculaires qui entourent les cryptes rondes mais qui ne sont pas visibles en vision non magnifiée (Sano I). L’ensemble de ces caractéristiques est regroupé sous la colonne IH de la classification CONECCT. Lorsqu’ils sont typiques et < 5 mm, ils ne doivent pas être réséqués, car ils n’ont aucun potentiel néoplasique. Il faut en revanche tous les regarder pour ne pas méconnaître un adénome parmi ces nombreux polypes similaires. En cas de doute, ils peuvent être réséqués. Si l’histologie potentielle ne modifie pas la prise en charge, ils peuvent être jetés. Si l’histologie peut changer l’intervalle de la future coloscopie, il faut les envoyer pour analyse.

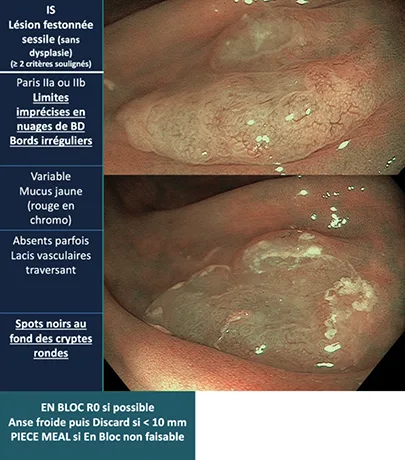
3) Les lésions festonnées sessiles (CONECCT IS) sont, comme les polypes hyperplasiques des lésions festonnées (glandes dentelées au microscope) mais dont le potentiel de dégénérescence est réel classiquement via la voie Ces lésions sécrètent beaucoup de mucus et de ce fait sont souvent cachées dans un nuage de mucus, leur donnant un aspect flou, aux contours mal délimités, comme un nuage de bande dessinée. La couleur de ces lésions varie souvent plus claire que la muqueuse environnante mais pouvant aussi être équivalente ou plus foncée. Une fois le mucus lavé, leurs contours deviennent nets, avec dans les formes non dysplasiques, un relief muqueux d’allure hyperplasique avec des cryptes rondes ou étoilées mais dont le fond de crypte est foncé (point noir au fond de la crypte). Ce sous-type de muqueuse est décrit sous le type IIO de la classification de Kudo. Pour les vaisseaux, on retrouve souvent des lacis vasculaires traversant la lésion comme pour les polypes hyperplasiques simples (CONECCT IH). Les critères des lésions festonnées sont regroupés dans une classification spécifique appelée WASP (7). Pour les lésions festonnées non dysplasiques, une résection complète est nécessaire en visant si possible le caractère En bloc mais de manière non indispensable car le taux de dégénérescence des formes typiques est extrêmement faible (< 1 %). Les lésions diminutives ou < 1 cm doivent être réséquées à l’anse froide et les plus importantes par technique de mucosectomie En bloc (sous-marine +++) ou fragmentée (à l’anse froide ou en mucosectomie chaude). Les récidives festonnées semblent plus difficiles à détecter et de ce fait une attention très particulière doit être portée au contrôle à 6 mois après une résection fragmentée. Attention, ces lésions festonnées sessiles peuvent aussi être dysplasiques arborant alors des zones de pattern typique de festonnée CONECCT IS ainsi que des zones adénomateuses (CONECCT IIA) ou des zones de dégénérescence (CONECCT IC ou plus). Dans ce cas, la stratégie thérapeutique dépend du contingent le plus à droite dans la classification CONECCT, avec une résection endoscopique complète sans viser le R0 si CONECCT IIA, en visant le R0 pour les IIC et IIC+ et en confiant le malade pour bilan d’extension puis chirurgie pour les CONECCT III.

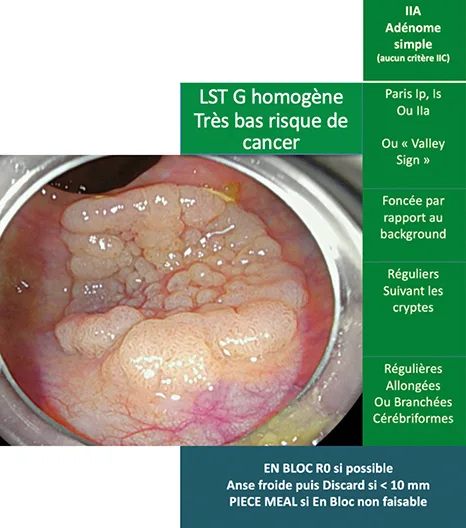
4) Les adénomes simples à bas risque de lésion dégénérée (CONECCT IIA) sont un groupe de lésions dont le risque de contenir un cancer T1 ne dépasse pas 1 %. Il comprend les lésions de moins de 10 mm et les tumeurs à extension latérale (LST) granulaire homogène (sans nodule) présentant un pit pattern régulier (Kudo III ou IV) ainsi qu’un vascular pattern régulier (Sano II). Ces lésions ne présentent aucun facteur de risque de cancer T1 de la sous classification CONECCT IIC ci-dessous. Ces lésions doivent comme les lésions festonnées sessiles être réséquées complètement en choisissant la technique la moins risquée c’est-à-dire l’anse froide pour les lésions de moins de 10 mm, la mucosectomie En Bloc si possible [sous-marine ou avec ancrage (8,9)] ou bien fragmentée si le En Bloc est impossible. En cas de résection fragmentée, une destruction minutieuse des berges de la lésion avec du courant de coagulation est recommandée (pointe d’anse) (10) et un contrôle à 6 mois pour détecter la récidive reste nécessaire. En France actuellement, 20,2 % des polypes de plus de 20 mm pouvant être guéris par une résection endoscopique sont envoyés aux chirurgiens pour colectomie avec une mortalité évitable de 0,5 % et une morbidité évitable de 24,3 % (11). Il est indispensable de prendre conscience que la taille n’est plus un critère de choix pour décider de la stratégie, et toute lésion même volumineuse doit être réévaluée par un endoscopiste interventionnel habitué aux larges résections.

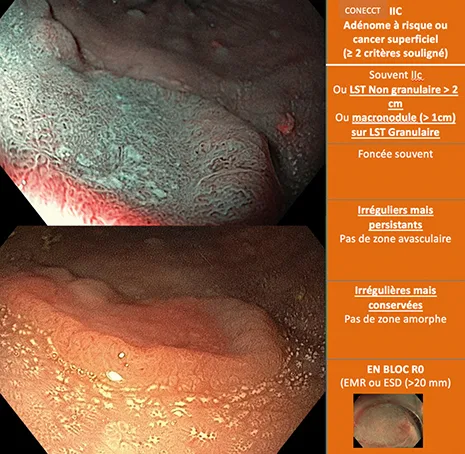
5) Les adénomes à haut risque et les carcinomes superficiels (CONECCT IIC) sont un sous-groupe de lésions dont le risque de cancer T1 est supérieur à 5 %. Ce sous-groupe comprend deux concepts différents : les lésions à risque de cancer T1 sans qu’aucune zone dégénérée ne soit réellement visible et les lésions présentant une zone démarquée de dégénérescence Dans le premier cas, c’est l’aspect macroscopique de la lésion dans la classification de Paris qui permet de déterminer le risque de cancer T1 même lorsqu’aucune zone de pattern irrégulier n’est détectée. Ainsi les LST granulaires avec macronodule ont un risque de cancer T1 de 8 % lorsque ce nodule fait moins de 1 cm et 18 % lorsque le nodule est supérieur à 1 cm. Les LST non granulaires sont à risque plus élevé puisque les formes surélévées ont jusqu’à 20 % de cancer T1 et les pseudodéprimées jusqu’à 47 % (12). Si un nodule apparaît au milieu d’une NG pseudodéprimée, le risque de cancer T1 est alors de 90 %. En parallèle de cela, la classification CONECCT IIC comprend également les lésions arborant une zone de pattern irrégulier, que ce soit sur le plan muqueux (Kudo Vi) ou vasculaire (Sano IIIa). Dans ce cas, la zone de dégénérescence est bien visible mais elle reste superficielle en l’absence de pattern amorphe ou avasculaire (CONECCT IIC+ et III). Ces lésions CONECCT IIC, dégénérées ou à haut risque de dégénérescence, doivent être réséquées complètement et en répondant aux exigences de qualité carcinologique. Pour obtenir une analyse histologique de qualité, il est indispensable d’avoir pour ces lésions une résection complète en un seul morceau (En Bloc) avec des marges de sécurité latérales et profondes (R0). En effet, seule une analyse histologique de qualité permettra de détecter des critères de mauvais pronostic (invasion profonde focale, emboles lymphatiques, budding). Ces derniers critères sont associés au risque de récidive ganglionnaire et leur reconnaissance fait proposer un traitement complémentaire par chirurgie avec curage ganglionnaire. Pour obtenir des marges de sécurité suffisantes, la mucosectomie reste acceptable jusqu’à 20 mm mais la technique de dissection sous-muqueuse est la référence au-delà. Ces résections endoscopiques de qualité permettent d’éviter une chirurgie colique dont la morbidité est bien plus importante pour un résultat carcinologique équivalent lorsqu’il s’agit de lésions superficielles.

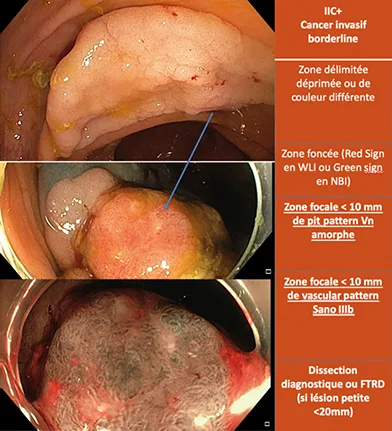
6) Ensuite, il existe une sous-classification entre les cancers superficiels (CONECCT IIC) et les cancers profonds (CONECCT III) avec une zone grise dans laquelle une prise en charge endoscopique peut éviter un certain nombre de chirurgies inutiles. Nous avons appelé cette zone grise « borderline » CONECCT IIC+, car ces lésions présentent des critères de cancer profond (relief muqueux amorphe et avasculaire) mais sur une zone focale très limitée de moins de 10 mm. Lorsque ces lésions sont réséquées endoscopiquement par dissection sous-muqueuse, FTRD ou dissection intermusculaire, au moins 40 % (13) d’entre elles sont en réalité des cancers superficiels, guéris par la résection endoscopique si la résection est R0. Environ 15 % de lésions seront à risque moyen de récidive ganglionnaire (< 5 %), et dans cette situation une surveillance pourra être proposée au lieu d’une chirurgie complémentaire, en particularité chez les patients avec comorbidités. Il y a donc une place pour une dissection diagnostique, en centre expert pour ces lésions limites avec zone invasive de moins de 10 mm. L’expertise en résection est alors indispensable pour minimiser au maximum le risque de perforation pour une lésion dégénérée, car une telle perforation laisse ensuite planer le doute sur un ensemencement potentiel de l’orifice de perforation ou du péritoine. Pour limiter ce risque perforatif, la technique de FTRD est une bonne option pour les petites lésions de moins de 15 mm mais au-delà, le risque de ne pas être R0 augmente et l’option à privilégier est alors la dissection sous-muqueuse dans le côlon et la dissection intermusculaire dans le rectum pour augmenter les chances d’être R0 profond.

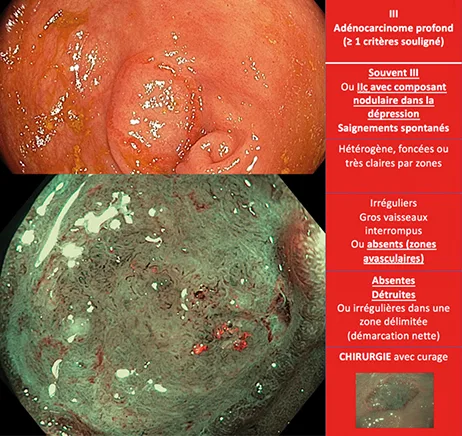
7) Les adénocarcinomes profondément invasifs (CONECCT III) sont une classe très large de lésions qui comprend l’ensemble des cancers colorectaux pour lesquels une résection endoscopique n’apportera pas de guérison au patient car la maladie est déjà à haut risque d’être au moins régionale (métastatique ganglionnaire) ou générale (métastatique à distance). Ces lésions présentent soit des critères évidents d’invasion profonde comme un caractère ulcéré (Paris III), un caractère bourgeonnant ou sténosant, ou bien des critères moins évidents comme la présence d’une zone de relief muqueux amorphe et avasculaire dépassant 10 L’élément commun à ces lésions est la nécessité d’évaluer l’extension régionale et/ou générale afin d’adapter la thérapeutique. Pour ces lésions, l’endoscopiste doit réaliser des biopsies (au moins 6 selon les recommandations), ciblées dans les zones amorphes ou avasculaires et non sur la couronne inflammatoire périphérique ou dans les zones de nécrose ulcérée (risque de biopsie faussement négative).

8) Les lésions plus rares
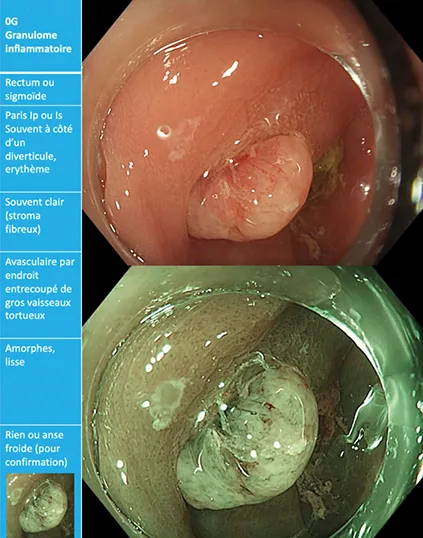
Les granulomes inflammatoires paradiverticulaires sont des lésions bénignes, cicatricielles d’une diverticulite et se présentent sous la forme d’une lésion polypoïde sessile au contact immédiat d’un diverticule inflammatoire. S’agissant d’un granulome fibro inflammatoire, il n’y a pas de pattern organisé de muqueuse digestive mais un stroma fibreux dans lequel se « promènent » de larges vaisseaux isolés au sein de zones avasculaires et amorphes sans aucun pattern muqueux (lisse).

Conclusion
Cette mini revue qui accompagnera la présentation FMC de caractérisation des polypes visait à vous présenter les lésions colorectales les plus fréquentes sous la forme d’une brève fiche d’identité.
Si vous souhaitez en savoir plus, n’hésitez pas à télécharger les podcasts réalisés par Pierre Lafeuille dans sa CONECCT-TV ou à rejoindre la page facebook HEH endoscopie pour voir des lésions caractérisées tous les jours.
Pour s’autoévaluer, un certain nombre d’atlas existe en ligne et nous travaillons actuellement à une application smartphone pour réaliser des tests de caractérisation en ligne et ainsi tester vos compétences.
Lien vers les podcasts de la CONECCT TV de Pierre Lafeuille

Références
- Fine C, Roquin G, Terrebonne E, et al. Endoscopic management of 345 small rectal neuroendocrine tumours: A national study from the French group of endocrine tumours (GTE). United European Gastroenterol J 2019; 7: 1102–1112. doi:10.1177/2050640619861883
- Veyre F, Lambin T, Fine C, et Endoscopic characterization of rectal neuroendocrine tumors with virtual chromoendoscopy: differences between benign and malignant lesions. Endoscopy 2020; doi:10.1055/a-1244-9526
- Cheminel L, Lupu A, Wallenhorst T, et Systematic Resection of the Visible Scar After Incomplete Endoscopic Resection of Rectal Neuroendocrine Tumors. Am J Gastroenterol 2023; doi:10.14309/ajg.0000000000002516
- Hayashi N, Tanaka S, Hewett DG, et Endoscopic prediction of deep submucosal invasive carcinoma: validation of the narrow-band imaging international colorectal endoscopic (NICE) classification. Gastrointest Endosc 2013; 78: 625–632. doi:10.1016/j.gie.2013.04.185
- The Paris endoscopic classification of superficial neoplastic lesions: esophagus, stomach, and colon: November 30 to December 1, Gastrointest Endosc 2003; 58: S3-43
- Kudo S, Rubio CA, Teixeira CR, et Pit pattern in colorectal neoplasia: endoscopic magnifying view. Endoscopy 2001; 33: 367–373. doi:10.1055/s-2004-826104
- IJspeert JEG, Bastiaansen BAJ, van Leerdam ME, et Development and validation of the WASP classification system for optical diagnosis of adenomas, hyperplastic polyps and sessile serrated adenomas/polyps. Gut 2016; 65: 963–970. doi:10.1136/gutjnl-2014-308411
- Yamashina T, Uedo N, Akasaka T, et Comparison of Underwater vs Conventional Endoscopic Mucosal Resection of Intermediate-Size Colorectal Polyps. Gastroenterology 2019; 157: 451-461.e2. doi:10.1053/j.gastro.2019.04.005
- Pioche M, Wallenhorst T, Lepetit H, et Endoscopic mucosal resection with anchoring of the snare tip: multicenter retrospective evaluation of effectiveness and safety. Endosc Int Open 2019; 7: E1496–E1502. doi:10.1055/a-0990-9068
- Sidhu M, Shahidi N, Gupta S, et Outcomes of Thermal Ablation of the Mucosal Defect Margin After Endoscopic Mucosal Resection: A Prospective, International, Multicenter Trial of 1000 Large Nonpedunculated Colorectal Polyps. Gastroenterology 2021; 161: 163-170.e3. doi:10.1053/j.gastro.2021.03.044
- Le Roy F, Manfredi S, Hamonic S, et Frequency of and risk factors for the surgical resection of nonmalignant colorectal polyps: a population-based study. Endoscopy 2015; doi:10.1055/s-0034-1392976
- Yamada M, Saito Y, Sakamoto T, et Endoscopic predictors of deep submucosal invasion in colorectal laterally spreading tumors. Endoscopy 2016; 48: 456–464. doi:10.1055/s-0042-100453
- Patenotte A, Yzet C, Wallenhorst T, et Diagnostic endoscopic submucosal dissection for colorectal lesions with suspected deep invasion. Endoscopy 2023; 55: 192–197. doi:10.1055/a-1866-8080