LIENS D’INTÉRÊT
Aucun
MOTS-CLÉS
Gastrite auto-immune, gastrite lymphocytaire, gastropathie à gros plis
Introduction
Les 2 principales causes de gastrite chronique sont l’infection à Helicobacter pylori (H. Pylori), de loin la plus fréquente même si sa prévalence a fortement diminué dans les pays occidentaux, et la gastrite auto-immune (maladie de Biermer) (tableau 1). Du fait de leur grande fréquence, ces 2 causes doivent être éliminées avant d’en envisager une autre. Pour le gastroentérologue, la discussion diagnostique doit aussi porter sur les autres formes de gastrite, notamment la gastropathie réactionnelle (anciennement chimique) et les gastropathies/gastrites hypertrophiques.
| Gastrites chroniques | Gastrite à H. pylori Gastrite auto-immune Gastrite liée aux MICI Gastrite lymphocytaire Gastrite collagène |
| Autres formes de gastrites/ gastropathies | Gastropathie réactionnelle (« chimique ») Gastrites granulomateuses Gastrites à éosinophiles Gastropathies hypertrophiques/hyperplasiques Gastropathies vasculaires Mastocytose, amylose… |
Tableau 1 : Principales causes des gastrites « non-aiguës »
Le risque évolutif des 2 formes les plus fréquentes de gastrite chronique est le développement d’une atrophie glandulaire (gastrite chronique atrophique) et d’une métaplasie intestinale avec un risque de tumeurs gastriques dont les types peuvent être différents selon la cause de la gastrite chronique. Une surveillance de la muqueuse gastrique peut donc être nécessaire.
Quelle est la définition de la gastrite chronique ?
La gastrite chronique est définie histologiquement par la présence d’un infiltrat anormalement dense de cellules inflammatoires, essentiellement mononucléées, dans le chorion de la muqueuse gastrique (1). Des polynucléaires éosinophiles (PNE) et plus rarement neutrophiles (PNN) peuvent être présents au sein de l’infiltrat. Le diagnostic est assez subjectif car, en dehors de la classification de Sydney (2) qui ne concerne que l’infection à H. pylori, il n’y a pas de définition précise du caractère anormalement dense de l’infiltrat. La gastrite chronique est le plus souvent asymptomatique.
Que sait-on de l’épidémiologie de la gastrite non liée à H. pylori ?
Il y a peu de données épidémiologiques sur la prévalence de la gastrite non liée à H. pylori. Il est probable que les chiffres soient très variables d’une population à une autre, dépendant notamment de la prévalence de l’infection à H. pylori dans la population générale. Une étude Nord-américaine méthodologiquement bien faite car, pour déclarer l’absence d’infection à H. pylori 4 critères étaient nécessaires (dont la sérologie mais pas la PCR), a évalué la prévalence de la gastrite non liée à H. pylori à 21 % des sujets ayant une gastrite (3). À partir d’une large base de données anatomopathologiques nord-américaine (près de 900 000 patients), il a été montré que la gastrite n’était pas liée à H. pylori chez environ 10 % des sujets avec gastrite (4). On peut conclure de ces 2 études qu’en cas de gastrite chronique, la cause n’est pas H. pylori dans 10 à 20 % des cas.
Première étape de la démarche diagnostique devant une gastrite chronique : éliminer une infection à H. pylori
La prise en charge de l’infection à H. pylori a récemment été précisée lors d’une précédente session de la FMC-HGE par JD de Korwin(5) et dans la cinquième version de la conférence de consensus de Maastricht (6). En dehors des manifestations cliniques évocatrices liées à H. pylori, notamment ulcéreuses, le diagnostic de l’infection à H. pylori est suspecté sur les anomalies anatomopathologiques de la muqueuse gastrique et confirmé par la mise en évidence du germe, quelle que soit la méthode. En cas d’infection à H. pylori, même s’il existe des formes antrales-prédominantes, fundiques-prédominantes ou pangastriques, les muqueuses antrale et fundique sont toujours anormales (figure 1).

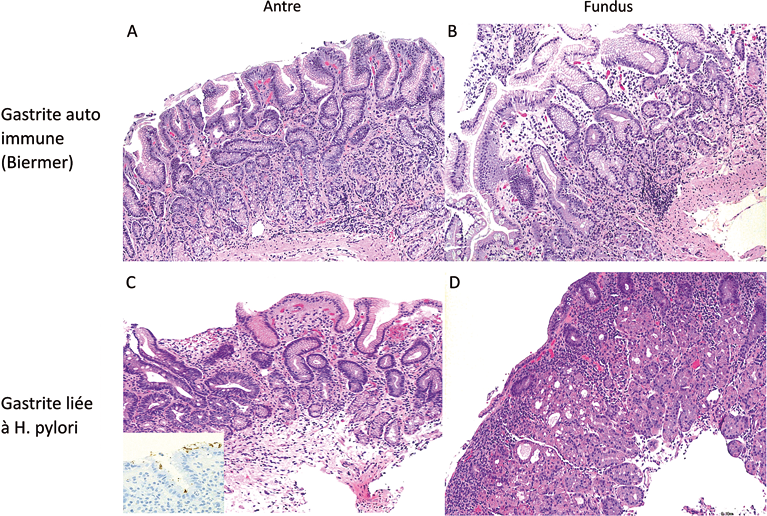
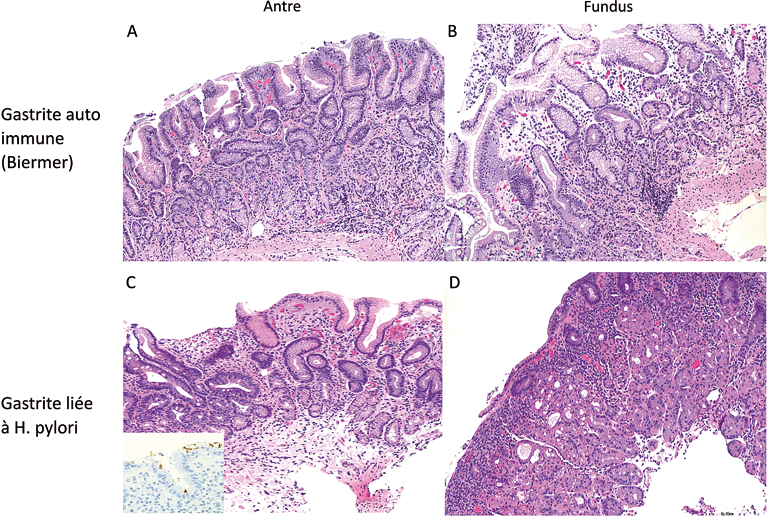
Figure 1 : A et B : Maladie de Biermer. C et D : Gastrite liée à Helicobacter pylori
(A) Muqueuse antrale histologiquement dans les limites de la normale. (B) Muqueuse fundique siège de lésions de gastrite
marquée avec atrophie glandulaire et foyer de métaplasie intestinale. (C) Gastrite antrale marquée avec atrophie et métaplasie intestinale. Mise en évidence de colonies d’H. Pylori en immunohistochimie (vignette en bas de l’image). (D) Gastrite fundique modérée, superficielle, sans atrophie. HES x 100.
Aux stades initiaux, l’infiltrat inflammatoire, essentiellement mononucléé, est confiné à la muqueuse superficielle (1). La lympho-plasmocytose sous- épithéliale s’étend par la suite, plus ou moins en profondeur, dans les glandes. Avec le temps, l’inflammation peut confluer jusqu’à occuper toute l’épaisseur de la muqueuse. Des PNN, PNE, macrophages, monocytes, mastocytes peuvent également infiltrer la muqueuse. La présence de PNN témoigne de l’activité histologique. Il peut exister des agrégats lymphocytaires avec centre germinatif. L’évolution peut se faire vers le développement d’une atrophie glandulaire (disparition des glandes) dans l’antre et dans le fundus, remplacée par une fibrose ou une métaplasie intestinale ou pseudo-pylorique. Le plus souvent, H. pylori est mis en évidence histologiquement soit avec les colorations standards soit avec des colorations spéciales (Giemsa…). Les germes se situent dans le mucus adhérent à l’épithélium. Une coloration immunohistochimique est nécessaire en cas de négativité de la recherche standard ou après coloration spéciale. Ceci a été recommandé lors de la dernière conférence de consensus de Maastricht (6). Exceptionnellement, le germe responsable est Helicobacter heilmannii. En pratique courante, en cas de gastrite chronique, si la recherche anatomopathologique et immunohistochimique d’H. pylori est négative, une sérologie H. pylori doit être faite pour s’assurer de l’absence de contact avec la bactérie, la sensibilité et la spécificité de la sérologie étant d’environ 90 % et probablement un peu moindre en cas d’atrophie (7). Les causes de faux négatifs de l’examen direct sont la prise d’antibiotiques ou d’inhibiteur de la pompe à protons (IPP), une métaplasie intestinale étendue, un nombre insuffisant de biopsies ou le site et les modalités des biopsies. Une étude a montré que les biopsies dirigées par les anomalies constatées en Narrow Band Imaging (NBI) étaient plus rentables pour la recherche de la bactérie mais aussi des lésions prénéoplasiques que les biopsies faites selon Sydney (8). Une étude évaluant la recherche de l’ADN d’Helicobacter par PCR sur biopsies a montré qu’H. pylori ou d’autres espèces d’Helicobacter étaient finalement présentes dans 49 % des cas de gastrite chronique sans mise en évidence histologique d’H. pylori (9). Le test respiratoire à l’urée C13 n’est pas indiqué en cas de gastrite chronique atrophique en raison des risques de faux négatifs et probablement aussi de faux positifs (7). En effet, la réduction de la sécrétion gastrique acide réduit la population d’H. pylori et peut ainsi rendre faussement négatif le test respiratoire. À l’inverse, elle peut induire une pullulation d’autres bactéries qui peut faussement positiver le test respiratoire.
Après l’infection à H. pylori, la cause la plus fréquente de gastrite chronique est la gastrite auto-immune (maladie de Biermer)
La maladie de Biermer est une gastrite chronique auto-immune du fundus conduisant progressivement au remplacement des glandes fundiques par de l’atrophie et de la métaplasie intestinale, pseudopylorique ou pancréatique (10-11). Elle ne touche pas l’antre, à l’inverse de la gastrite chronique liée à H. pylori (figure 1). L’infiltrat inflammatoire du chorion est fait de cellules lymphoplasmocytaires avec parfois présence de PNE et de mastocytes. Il prédomine à la partie profonde de la muqueuse.
Les lymphocytes peuvent « grignoter » les glandes (lésions lympho-épithéliales et destructrices des glandes). À un stade plus tardif, l’atrophie devient plus importante ainsi que la métaplasie (intestinale, pseudopylorique, pancréatique) qui peut devenir prédominante. Dans ce cas, la normalité de la muqueuse antrale est quasi pathognomonique, d’où l’importance de bien séparer dans des pots différents les biopsies faites dans l’antre et dans le fundus. Il existe de façon quasi constante une hyperplasie des cellules endocrines du fundus qui est liée à l’effet de la gastrine qui favorise la prolifération cellulaire, notamment sous la forme d’une hyperplasie nodulaire. Celle-ci est également liée à la concentration de cellules endocrines dans les glandes atrophiques. Tous les aspects de l’hyperplasie de ces cellules sont visibles : simple, linéaire, micronodulaire, adénomatoïde pouvant conduire à la dysplasie endocrine et aux tumeurs neuroendocrines (TNE) du fundus de type 1 (ECLomes) (10-12). Il s’agit de surélévations muqueuses du fundus, souvent érythémateuses, presque toujours multiples et qui mesurent moins de 1 cm dans 80 % des cas. Elles sont pratiquement toujours de grade 1 et bénignes (10). En cas de TNE de moins de 1 cm, les explorations complémentaires sont inutiles. Les lésions de cette taille peuvent être détruites endoscopiquement chez les sujets en bon état général (10-12). Au-delà de 1 cm, l’échoendoscopie est nécessaire pour décider du traitement après discussion en RCP RENATEN (www.tncd.org).
La gastrite auto-immune est associée dans au moins la moitié des cas à une ou plusieurs maladies auto-immunes, principalement les thyroïdites auto-immunes et le diabète de type 1 (13) (tableau 2). La présence d’anticorps anti-cellules pariétales est quasi constante (sensibilité 90 % mais spécificité faible de 60 %), alors que celle d’anticorps anti-facteur intrinsèque est moins fréquente (60 %) mais est quasi pathognomonique (spécificité 90 %) (10). L’hypergastrinémie est quasi constante. Elle est réactionnelle à l’hypochlorhydrie induite par la réduction de la masse cellulaire pariétale (atrophie glandulaire). C’est dans la maladie de Biermer qu’on constate les niveaux les plus élevés d’hypergastrinémie, souvent très supérieurs à ceux du syndrome de Zollinger-Ellison (SZE). La recherche d’H. pylori est indispensable sur les biopsies et par sérologie si cette recherche est négative (6). En effet, certaines études suggèrent un lien avec l’infection à H. pylori qui serait le déclencheur du phénomène auto-immun (11). D’autre part, il n’y a pas de raison que les patients atteints d’une maladie de Biermer authentique ne puissent pas être infectés par H. pylori. Dans ce cas, il peut exister des anomalies histologiques antrales liées à l’infection, jusque chez 20 % des patients.
| Maladies auto-immunes | n (%) |
| Basedow | 12 (16,2 %) |
| Hashimoto | 45 (60,8 %) |
| Diabète | 23 (31,1 %) |
| Vitiligo | 9 (12,2 %) |
| Gougerot-Sjögren | 7 (9,5 %) |
| Syndrome des anti-phospholipides | 5 (6,8 %) |
| Hépatite auto-immune | 1 (1,35 %) |
| Addison | 5 (6,8 %) |
| Myasthénie | 2 (2,7 %) |
| Lupus systémique | 1 (1,35 %) |
| Anémie hémolytique auto-immune | 2 (2,7 %) |
Tableau 2 : Répartition des maladies auto-immunes chez 74 patients ayant une maladie de Biermer et au moins une autre maladie auto-immune (tableau extrait de la référence 13)
Sur le plan clinique, le diagnostic de la maladie peut être fortuit, ou bien fait lors de l’exploration d’une carence en vitamine B12 ou en fer, avec ou sans anémie. Parfois l’anémie est profonde. Environ 20 % des anémies ferriprives inexpliquées seraient liées à une maladie de Biermer. La carence en fer, liée en partie à l’hypochlorhydrie, touche plutôt les femmes jeunes ; elle est plus fréquente que la carence en vitamine B12 qui est tardive et qui touche les sujets plus âgés (10). La maladie peut aussi être révélée par des manifestations systémiques de la maladie de Biermer en rapport avec la carence en vitamine B12 (neurologiques, psychiatriques, cutanéo-muqueuses…). La maladie peut aussi être détectée lors de l’exploration d’une autre maladie auto-immune ou par la présence d’anticorps anti-cellules pariétales. Sur le plan endoscopique, il n’y a pas d’aspect pathognomonique de la maladie de Biermer, c’est le cas notamment de l’aspect en fond d’œil de la muqueuse gastrique qui n’a pas de réelle signification (figure 2). À l’inverse la muqueuse fundique peut être polypoïde (figure 2) en raison du caractère irrégulier, en plages, de l’atrophie, les « polypes » correspondant à de la muqueuse moins atrophique pouvant prendre l’aspect d’une gastrite pseudopolypoïde (figure 3). Ceci est une raison supplémentaire de toujours biopsier la muqueuse gastrique non polypoïde en cas de polypes gastriques. Enfin les polypes hyperplasiques sont très fréquents et il existe un risque de développement d’adénomes et d’adénocarcinome, ce qui justifie la surveillance endoscopique chez les sujets jeunes.

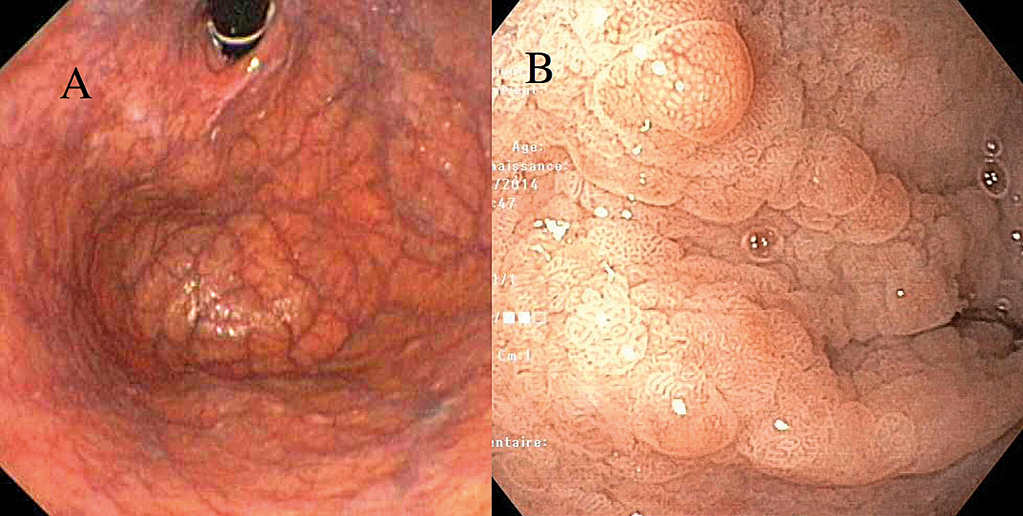
Figure 2 : Deux aspects endoscopiques de muqueuse fundique en cas de maladie de Biermer
(A) muqueuse fundique en fond d’œil (B) muqueuse pseudopolypoïde.

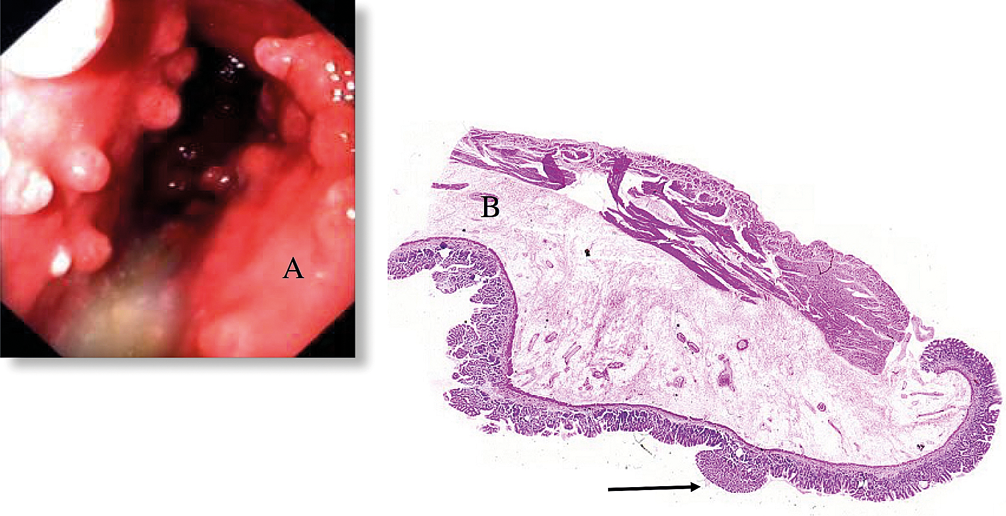
Figure 3 : Gastrite pseudopolypoïde en cas de maladie de Biermer
(A) Aspect endoscopique et (B) lame montée montrant que les formations polypoïdes correspondent à de la muqueuse
fundique moins atrophique (flèche noire) (Courtesy : Pr. MD Diebold, Reims).
Modalités de réalisation de l’endoscopie en cas de gastrite chronique
Une question non résolue concerne les modalités de l’exploration endoscopique de l’estomac des patients atteints d’une gastrite auto-immune. Il est évident que les 5 biopsies habituelles nécessaires à l’établissement de la classification de Sydney ne sont pas suffisantes. Il a d’ailleurs été montré dans la gastrite liée à H. pylori que des biopsies ciblées sur les anomalies détectées en NBI détectaient plus d’anomalies histologiques prénéoplasiques que les biopsies classiques (8). Il en est de même en augmentant le nombre de biopsies (14). Dans la maladie de Biermer, nous n’avons pas connaissance d’une étude évaluant le nombre minimal de biopsies ou si une coloration (virtuelle ou vitale) permettant de cibler les biopsies, doit être utilisée ou pas. Cependant les récentes recommandations de la Société britannique de gastroentérologie (BSG) (15), venant après celles de l’ESGE de 2012 (16), indiquent, en cas d’atrophie gastrique ou de métaplasie intestinale (quelle qu’en soit la cause), de faire une endoscopie selon la technique publiée par les Japonais (17) comprenant des étapes systématisées, documentées par des photographies systématiques, avec un examen par coloration virtuelle permettant de caractériser d’éventuelles lésions et de cibler les biopsies. Pour plus d’information, cette technique a été présentée lors du symposium de la SFED des JFHOD 2016 par Sarah Leblanc (18). À notre connaissance, un tel protocole n’est malheureusement pas (ou peu ?) appliqué en France. De ce fait, par défaut, nous recommandons, lors des explorations endoscopiques de la gastrite auto-immune, de faire systématiquement au minimum une dizaine de biopsies étagées dans le fundus et, initialement, les biopsies antrales habituelles, en plus des biopsies ciblées sur d’éventuelles anomalies macroscopiques qui seraient alors au mieux caractérisées par coloration virtuelle.
Sur le plan anatomopathologique, le niveau de risque de cancer dans la gastrite liée à H. pylori a été évalué par les scores OLGA et OLGIM qui reposent respectivement sur la sévérité et la topographie des lésions de gastrite chronique atrophique et de métaplasie intestinale (19-20). Cette classification est utile pour déterminer le rythme de surveillance.
La classification OLGA n’a été que très peu appliquée à la gastrite auto-immune (21). Seules les formes évoluées OLGA III et IV étaient à risque de néoplasie épithéliale dans la seule étude sur le sujet (21). La classification OLGIM n’est pas appropriée à ce type de gastrite.
Quelles sont les causes rares de gastrite chronique ?
Les autres causes de gastrite chronique que nous pouvons rencontrer non exceptionnellement sont celles liées aux MICI et la gastrite lymphocytaire. La gastrite collagène est exceptionnelle. Les autres formes de gastrite, qui sont par ailleurs très rares voire exceptionnelles, ne sont pas considérées comme des gastrites chroniques (tableau 1).
Gastrites liées aux MICI
La maladie de Crohn peut induire les mêmes lésions macroscopiques et anatomopathologiques dans l’estomac que dans le reste du tube digestif. L’atteinte serait plus fréquente chez les enfants. Classiquement, il s’agit d’une gastrite focale, définie par une inflammation très localisée constituée d’éléments lymphocytaires et histiocytaires entourant des glandes avec ou sans polynucléaires et plasmocytes. En périphérie, la muqueuse gastrique est normale, sans signe d’inflammation (figure 4). Cet aspect n’est cependant pas spécifique de la maladie de Crohn comme cela avait été initialement suggéré ; elle est aussi observée chez les enfants atteints de RCH (22). Elle peut toucher l’antre et/ou le fundus jusqu’à 40 % des patients atteints de maladie de Crohn (23) et plus de 50 % des enfants (22). Au total, des anomalies histologiques gastriques sont présentes chez 68 % des patients atteints de maladie de Crohn (24). En dehors de la gastrite focale, il s’agit d’une gastrite chronique active, d’une gastrite lymphocytaire ou de granulomes (24). Dans la RCH, l’atteinte gastrite est rare, le plus souvent sous forme de gastrite focale.

Figure 4 : Biopsie gastrique chez un patient atteint d’une maladie de Crohn :
(A) Muqueuse gastrique antro-fundique siège d’une inflammation focale (dans la zone encadrée). En périphérie de cette zone, la muqueuse est normale, non inflammatoire (HES x 40).
(B) À plus fort grossissement, l’infiltrat inflammatoire, composé d’éléments lympho-plasmocytaires et de polynucléaires
neutrophiles, apparaît dense, entourant les cryptes (HES x 200).
Gastrite lymphocytaire
La gastrite lymphocytaire est définie par la présence d’au moins 25 lymphocytes (CD3+ CD8+) pour 100 cellules épithéliales (1). Habituellement, l’infiltrat est intense. Elle peut être associée à l’infection à H. pylori et à la maladie cœliaque, avec, pour cette dernière, une prévalence très variable selon les études (3 à 38 %) (25-26). L’aspect macroscopique typique est la gastrite varioliforme, définie par des surélévations muqueuses déprimées (27). Elle se voit également en l’absence d’anomalie macroscopique, en cas d’érosions gastriques ou de gros plis avec, dans ce cas, le diagnostic différentiel avec la gastropathie à gros plis de Ménétrier dont nous parlerons plus loin. Le plus souvent, elle touche préférentiellement le corps ou tout l’estomac. H. pylori, s’il est présent, doit être éradiqué. Dans ce cas, la plupart du temps la gastrite disparaît (1). Une maladie cœliaque doit être recherchée. Il existe d’exceptionnelles observations de gastrite lymphocytaire induite par des médicaments (olmesartan, pembrolizumab). En dehors des symptômes liés à l’éventuelle cause, la gastrite lymphocytaire n’est pas responsable de symptôme et il n’y a pas de traitement spécifique.
Gastrite collagène
Elle est définie par un épaississement de la bande collagène sous-épithéliale > 10 µm avec un infiltrat lympho-plasmocytaire du chorion (1). Dans une revue publiée en 2014, 60 cas seulement avaient été publiés (28). Il existe 2 formes principales : une forme limitée à l’estomac qui survient chez les enfants ou les adultes jeunes et une forme associée à la colite collagène avec diarrhée chronique (1, 28). Il peut exister des maladies auto-immunes associées (Sjögren, gastrite ou colite lymphocytaire, RCH). Il n’y a pas de lien avec H. pylori. Sur le plan endoscopique, un aspect nodulaire de la muqueuse est décrit dans environ 50 % des cas. Parfois, il s’agit d’œdème, d’érythème ou d’érosions ou bien la muqueuse est normale (10 %). Sur le plan clinique, il a été décrit des douleurs abdominales et une anémie dans la forme de l’enfant/adulte jeune. L’évolution est très mal connue. L’inflammation mais pas l’épaississement de la bande collagène pourrait être améliorée par les traitements (IPP) qui peuvent aussi être des corticoïdes, voire même la nutrition parentérale.
Les autres formes de gastrites
Le nombre de causes de gastrite est élevé mais chacune est rare sauf la gastrite/gastropathie réactionnelle (tableau 1).
La gastropathie réactionnelle
Appelée autrefois la gastrite chimique, c’est la plus fréquente des gastrites après la gastrite à H. pylori. Ce n’est pas une gastrite chronique, mais une réaction gastrique aux sels biliaires (notamment après chirurgie gastrique) ou à certains médicaments (AINS) (1). Il existe une hyperplasie fovéolaire (hyperplasie des cryptes) et une extension des fibres musculaires entre les cryptes. Il y a peu d’inflammation sauf s’il existe des érosions.
Les granulomatoses gastriques
Les causes des granulomes gastriques épithélioïdes et giganto-cellulaires sont très nombreuses (tableau 3). La conduite à tenir est finalement simple sur le plan pratique. Soit la cause est évidente en raison du contexte ou des données anatomopathologiques, soit elle ne l’est pas (dyspepsie, découverte fortuite). Dans ce cas, après avoir réalisé une nouvelle série de biopsies et évoqué la maladie de Crohn (figure 5) et la sarcoïdose, la cause n’est habituellement pas trouvée et il est inutile de la chercher. Le temps permettra éventuellement de faire le diagnostic ultérieurement.
| Maladie de Crohn |
| Sarcoïdose |
| Tuberculose et autres mycobactéries |
| Maladie de Whipple |
| Histoplasmose |
| Anisakiase |
| Lymphome |
| Corps étrangers (aliments, sutures…) |
| Idiopathique |
Tableau 3 : Principales causes de granulomatoses gastriques

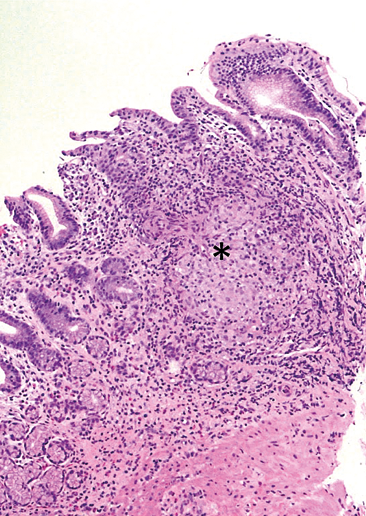
Figure 5 : Gastrite antrale granulomateuse chez un patient atteint d’une maladie de Crohn :
présence d’un volumineux granulome (*) composé de cellules épithélioïdes, sans nécrose. (HES x 100).
La gastrite à éosinophiles
Elle est définie par un infiltrat à PNE dans le chorion (1). Celui-ci peut atteindre la surface épithéliale et les PNE peuvent être éliminés dans la lumière ou infiltrer l’épithélium glandulaire. Des cristaux de Charcot-Leyden peuvent être présents au sein de l’infiltrat. Il peut exister une hyperplasie de la musculaire muqueuse. Le nombre minimal de PNE nécessaire au diagnostic n’est pas fixé formellement. Une proposition est : plus de 30 PNE par champ à fort grossissement (x 400) ou 127 PNE par mm2 comptés dans au moins 5 grands champs (29). L’infection à H. pylori et la maladie de Crohn doivent être éliminées mais elles ne sont habituellement pas associées à des taux aussi élevés de PNE. Il peut s’agir d’une gastroentérite à éosinophiles dont la preuve est portée par l’existence d’un infiltrat à PNE dans le reste du tube digestif. Les autres causes sont très nombreuses, notamment parasitaires ou hématologiques (tableau 4).
| Gastroentérite à éosinophiles |
| Syndrome hyperéosinophilique |
| Infections parasitaires |
| Maladie de Crohn |
| H. pylori |
| Médicaments |
| Allergie |
| Idiopathique |
Tableau 4 : Principales causes des gastrites à éosinophiles
Les gastropathies hypertrophiques/hyperplasiques
L’estomac est considéré hypertrophique si l’épaisseur de la muqueuse dépasse 1,5 mm (1). Sur le plan endoscopique, la gastropathie hypertrophique se manifeste par des gros plis parfois cérébriformes ne s’effaçant pas à l’insufflation. Les gros plis peuvent être diffus ou localisés. Il existe principalement 2 types bien définis de gastropathies hypertrophiques : la maladie de Ménétrier qui peut induire une exsudation de protéines d’origine gastrique avec hypoalbuminémie majeure et hypochlorhydrie et le SZE avec hypersécrétion gastrique acide. La gastrite lymphocytaire et l’infection à H. pylori peuvent aussi se présenter comme une gastrite hypertrophique. Le principal diagnostic différentiel est l’infiltration par des cellules tumorales (adénocarcinome à cellules indépendantes ou lymphome), de loin la première cause de gros plis gastriques. La muqueuse gastrique comporte 2 compartiments, la zone des cryptes et, au-dessous, le compartiment glandulaire. L’hyperplasie peut concerner 1 ou les 2 compartiments. Quand un compartiment est hyperplasique, l’autre peut être normal, hyperplasique ou atrophique. Dans la maladie de Ménétrier, il existe une hyperplasie des cryptes et une atrophie glandulaire (ou des glandes normales). Il peut exister des pseudokystes correspondant à l’invagination des cryptes dans la sous-muqueuse, circonscrites par des fibres musculaires lisses (gastritis cystica profunda). Dans le SZE, les cryptes sont normales et le compartiment glandulaire est hyperplasique dans le fundus. L’antre est normal. On constate une hyperplasie des cellules pariétales même proches de la surface muqueuse et une hyperplasie des cellules neuroendocrines fundiques. Enfin, il existe des variantes de gastropathies hypertrophiques, notamment en cas de gastrite lymphocytaire hypertrophique.
Le diagnostic anatomopathologique peut être difficile car les biopsies sont souvent trop superficielles. Des macrobiopsies peuvent être nécessaires. Cependant le diagnostic du SZE ne repose jamais sur l’analyse de la muqueuse, mais sur les symptômes (ulcères duodénaux, œsophagite, amaigrissement…), la biologie (hypergastrinémie en l’absence de prise d’IPP, hyperchlorhydrie) et la mise en évidence de(s) tumeur(s) (30). Chez l’enfant, il existe une forme particulière de Ménétrier liée à une infection à CMV (1). L’échoendoscopie peut être d’une grande aide dans le diagnostic des gastropathies à gros plis, une épaisseur de la paroi gastrique > 9,8 mm et un épaississement de la musculeuse étant des critères prédictifs de malignité (31). Un épaississement de plus de 5 mm de la seconde couche est évocateur de la maladie de Ménétrier (32).
Traitement et surveillance des gastrites chroniques
Traitement
Le traitement est celui de la cause, notamment l’éradication d’H. pylori, sur lequel nous ne reviendrons pas. Il n’y a pas de traitement spécifique de la gastrite auto-immune ni des autres types de gastrite sauf de la maladie de Ménétrier, mais celui-ci ne sera pas abordé ici.
En cas de gastrite chronique responsable d’une hypochlorhydrie, essentiellement en cas de gastrite auto-immune, il existe un risque de carence en vitamine B12 et de carence en fer qu’il faut régulièrement chercher (1 fois par an) et le cas échéant corriger (10). Une supplémentation préventive par vitamine B12 est nécessaire une fois qu’une carence en vitamine B12 a été constatée. L’administration orale de la vitamine B12 est une alternative à la voie parentérale (IM ou SC). Cette voie est aussi efficace, mais nécessite des apports quotidiens ou beaucoup plus fréquents que par voie parentérale (33). Per os, la dose est de 1 mg/j jusqu’à normalisation des taux, à poursuivre en traitement d’entretien. Chez les sujets ayant une carence limitée, après correction initiale des taux, nous proposons souvent des cures mensuelles per os de vitamine B12 quotidienne tous les 2 à 3 mois en surveillant les taux 1 fois par an. En ce qui concerne l’administration parentérale, la posologie recommandée est d’une injection IM de 1 mg de vitamine B12 par jour pendant 1 semaine, puis 1 injection par semaine pendant 1 mois puis 1 injection par mois (33). Les taux de vitamine B12 doivent être contrôlés après le traitement d’attaque, puis une surveillance annuelle est nécessaire.
Surveillance des gastrites chroniques
En raison du risque néoplasique, une surveillance des gastrites responsables d’une atrophie et/ou d’une métaplasie intestinale est préconisée. Les scores d’OLGA et d’OLGIM permettent de définir les intervalles de surveillance pour la gastrite à H. pylori (19-20). En ce qui concerne la gastrite auto-immune, la surveillance avec multiples biopsies fundiques et idéalement par la technique précédemment décrite préconisée par les Japonais est probablement nécessaire chez les sujets jeunes tous les 3 à 5 ans (10). L’objectif est de dépister des lésions néoplasiques ou prénéoplasiques : dysplasie épithéliale prédisposant à l’adénocarcinome, adénocarcinome à un stade précoce, TNE. En cas de dysplasie de bas ou de haut grade, un contrôle endoscopique précoce avec multiplication des biopsies, si possible avec la technique précédemment décrite, est nécessaire (20). En cas de persistance de la dysplasie de bas grade, un suivi annuel est indiqué et, en cas de dysplasie de haut grade (après relecture par un pathologiste expert), une gastrectomie totale doit être discutée. En cas de TNE fundiques associées à la maladie de Biermer, une endoscopie annuelle est conseillée les premières années de surveillance avec destruction des lésions.
Références
- Turner K, Genta The nonneoplastic stomach. In: Fenoglio-Preiser’s gastrointestinal pathology. Fourth edition. Amy Noffsinger ed. Wolters Kluwer, Philadelphia. 2017. pp 136-223.
- Dixon MF, Genta RM, Yardley JH, et al. Classification and grading of gastritis. The updated Sydney System. International Workshop on the Histopathology of Gastritis, Houston 1994. Am J Surg Pathol 1996;20:1161–81.
- Nordenstedt H, Graham DY, Kramer JR, et al. Helicobacter pylori-negative gastritis: prevalence and risk factors. Am J Gastroenterol. 2013;108:65-71.
- Genta RM, Sonnenberg A. Helicobacter-negative gastritis: a distinct entity unrelated to Helicobacter pylori Aliment Pharmacol Ther 2015;41:218-26.
- JD de Nouvelles recommandations sur la prise en charge des patients infectés par Helicobacter pylori. Post’U 2016.
- Malfertheiner P, Mégraud F, O’Morain CA, et Management of Helicobacter pylori infection – the Masstricht V/Florence conference consensus report. Gut 2017;66:6-30.
- Kokkola A, Rautelin H, Puolakkainen P, et al. Diagnosis of Helicobacter pylori infection in patients with atrophic gastritis: comparison of histology, 13C-urea breath test, and serology. Scand J Gastroenterol. 2000 Feb;35(2):138-41.
- Tongtawee T, Dechsukhum C, Leeanansaksiri W, et al. Improved detection of Helicobacter pylori infection and premalignant gastric mucosa using « site specific biopsy » : a randomised control clinical Asian Pac J Cancer Prev 2015:16(18):8487-90.
- Kiss S, Zsikla V, Frank A, et al. Helicobacter-negative gastritis: polymerase chain reaction for Helicobacter DNA is a valuable tool to elucidate the diagnosis. Aliment Pharmacol Ther 2016;43:924-32.
- de Mestier L, Diebold MD, Cadiot G. La maladie de Biermer. Hépato Gastro 2014;21:595-606.
- Varbanova M, Malfertheiner Chronic gastritis – an update. Best Pract Res Clin Gastroenterol 2014:28:1031-42.
- Scherübl H, Cadiot G, Jensen RT, Rösch T, Stölzel U, et al. Neuroendocrine tumors of the stomach (gastric carcinoids) are on the rise: small tumors, small problems? Endoscopy 2010;42:664-71.
- Zulfiqar AA, Andres Association pernicious anemia and autoimmune polyendocrinopathy: a retrospective study. J Med Life 2017;10:250-3.
- El-Zimaity HMT, Graham Evaluation of gastric mucosal biopsy site and number for identification of Helicobacter pylori or intestinal metaplasia: role of the Sydney system. Human Pathol 1999; 30:72-7.
- Banks M, Graham D, Jansen M, et al. British Society of Gastroenterology guidelines on the diagnosis and management of patients at risk of gastric adenocarcinoma. Gut 2019;68:1545-75.
- Dinis-Ribeiro M, Areia M, de Vries AC, et al. Management of precancerous conditions and lesions in the stomach (MAPS): guideline from the European Society of Gastrointestinal Endoscopy (ESGE), European Helicobacter Study Group (EHSG), European Society of Pathology (ESP), and the Sociedade Portuguesa de Endoscopia Digestiva (SPED). Endoscopy 2012;44:74–94.
- Yao The endoscopic diagnosis of early gastric cancer. Ann Gastroenterol 2013;26:11–22.
- http://mediatheque.sfed.org/mediatheque/media.aspx?mediaId=14794&playlistId=14814&channel=7360
- Rugge M, Fassan M, Pizzi M, et al. Operative link for gastritis assessment vs operative link on intestinal metaplasia assessment. World J Gastroenterol 2011;17:4596-601.
- den Hollander WJ, Holster IL, den Hoed CM, et al. Surveillance of premalignant gastric lesions: a multicenter prospective cohort study from low incidence regions. Gut 2019;68:585-93.
- Rugge M, Fassan M, Pizzi M, et Autoimmune gastritis: histology phenotype and OLGA staging. Aliment Pharmacol Ther 2012;35:1460-6.
- Roka K, Roma E, Stefanaki K, et al. The value of focally enhanced gastritis in the diagnosis of pediatric inflammatory bowel diseases. J Crohns Colitis 2013;7:797-802.
- Oberhuber G, Püspök A, Oesterreicher C, et Focally enhanced gastritis: a frequent type of gastritis in patients with Crohn’s disease. Gastroenterology 1997;112:698-706.
- Brown IS, Miller GC, Bettington ML, Rosty Histopathological findings of extra-ileal manifestations at initial diagnosis of Crohn’s disease-related ileitis. Virchows Arch 2016;469:515-522.
- Wu TT, Hamilton Lymphocytic gastritis: association with etiology and topology. Am J Surg Pathol 1999;23:153-8.
- Diamanti A, Maino C, Niveloni S, et al. Characterization of gastric mucosal lesions in patients with celiac disease: a prospective controlled Am J Gastroenterol 1999;94:1313-9.
- Haot J, Hamichi L, Wallez L, et al. Lymphocytic gastritis: a newly described entity: a retrospective endoscopic and histological study. Gut 1988;29:1258-64.
- Kamimura K, Kobayashi M, Sato Y, et al. Collagenous gastritis: Review. World J Gastrointest Endosc 2015;16;7:265-73.
- Lwin T, Melton SD, Genta RM. Eosinophilic gastritis: histopathological characterization and quantification of the normal gastric eosinophil content. Mod Pathol 2011;24:556-63.
- Metz DC, Cadiot G, Poitras P, et al. Diagnosis of Zollinger-Ellison syndrome in the era of PPIs, faulty gastrin assays, sensitive imaging and limited access to acid secretory testing. Int J Endocr Oncol 2017;4:167-185.
- Lim H, Lee GH, Na HK, et Use of Endoscopic Ultrasound to Evaluate Large Gastric Folds: Features Predictive of Malignancy. Ultrasound Med Biol 2015;41:2614-20.
- Hizawa K, Kawasaki M, Yao T, et al. Endoscopic ultrasound features of protein-losing gastropathy with hypertrophic gastric folds. Endoscopy 2000;32:394-7.
- Andrès E, Vogel T, Kaltenbach G. Vitamine B12 administrée par voie orale : indications et modalités pratiques d’utilisation. MT 2013;19:189-95.