LIENS D’INTÉRÊT
Ipsen, Kyowa Kirin, Mayoly Spindler, Biocodex, MSD, Norgine
MOTS-CLÉS
Gastroparésie, Vidange gastrique, Prokinétiques
Introduction
La gastroparésie est un trouble fonctionnel digestif défini par un ralentissement de la vidange gastrique en l’absence de tout obstacle mécanique organique (1). Les symptômes cardinaux sont la nausée, les vomissements, la plénitude post-prandiale et la satiété précoce. Un ballonnement et des douleurs abdominales peuvent être également notés, ces dernières étant associées à une altération plus marquée de la qualité de vie. Chez les patients souffrant d’une gastroparésie sévère, on retrouve un état anxio-dépressif plus important. Dans les formes les plus sévères, une altération de la qualité de vie, un retentissement nutritionnel marqué et une augmentation de la fréquence des hospitalisations peuvent être notés (2). Les symptômes sont chroniques avec des périodes d’exacerbation. Cette affection touche principalement les femmes jeunes.
Il existe un chevauchement avec la dyspepsie fonctionnelle, principalement chez les malades ayant des symptômes digestifs hauts sans cause organique et qui ne présentent ni nausée ni vomissement. Ainsi, 40 % des sujets dyspeptiques ont un ralentis- sement objectif de la vidange gastrique alors que ce dernier est noté chez 75 % des sujets ayant des nausées et/ou des vomisse- ments chroniques inexpliqués souffrant de gastroparésie (3, 4).
Jusqu’à récemment, la prévalence de la gastroparésie était mal connue et estimée à 2-3 % de la population générale (5). Une étude américaine récente menée en population générale a estimé la prévalence de la gastroparésie à 0,16 % (6). Les études de population montrent qu’1 à 5 % des patients diabétiques développent une gastroparésie (6, 7). Le risque de développer une gastroparésie est 4 fois plus fréquente dans le diabète de type 1 que le type 2. L’ancienneté du diabète ne semble pas jouer de rôle, par contre le sexe féminin, le déséquilibre du diabète et la présence d’une neuropathie périphérique sont des facteurs de risques reconnus (7).
Quand y penser ?
Les principaux symptômes de la gastroparésie sont la sensation de plénitude gastrique, la satiété précoce, la nausée et les vomissements, une douleur abdominale pouvant également être associée (8). La présence de nausées et vomissements doit conduire à une mesure de la vidange gastrique afin de distinguer une réelle gastroparésie d’une dyspepsie fonctionnelle.
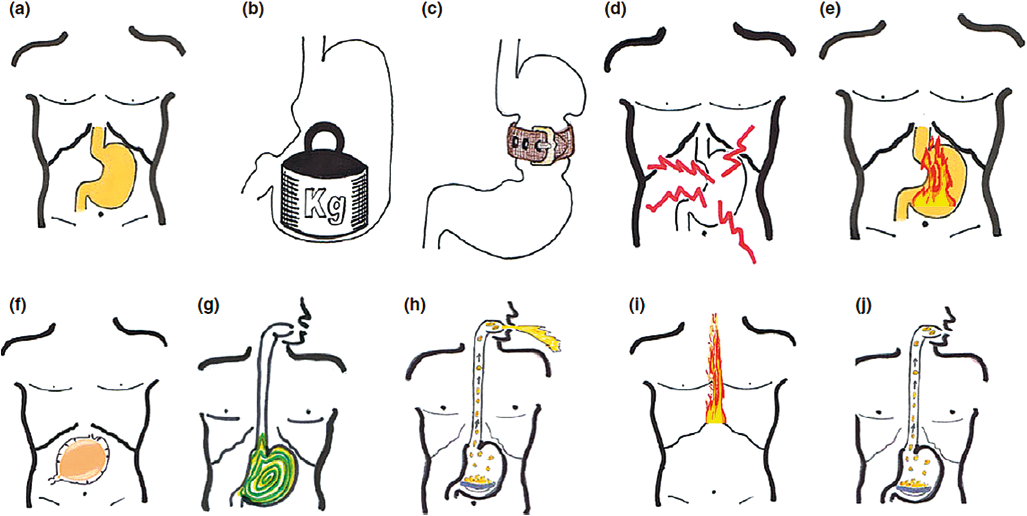
L’évaluation symptomatique peut être améliorée par l’utilisation d’un auto-questionnaire avec pictogrammes (figure 1) (9). Dans certains cas, les symptômes peuvent être absents ou au second plan. Chez les malades diabétiques, il faut savoir évoquer la gastroparésie devant une difficulté d’équilibration du diabète ou une altération de l’état général inexpliquée avec perte de poids.

Figure 1 : Pictogrammes indiquant a) la localisation de l’estomac, b) la pesanteur post-prandiale, c) la satiété précoce, d) la douleur, e) la brûlure épigastrique, f) le ballonnement épigastrique, g) la nausée, h) le vomissement, i) la brûlure d’estomac et j) la régurgitation (9)
Un reflux acide gastro-œsophagien mal équilibré par un traitement anti-sécrétoire bien suivi, la présence d’un bézoard gastrique, de résidus alimentaires abondants dans l’antre en endoscopie digestive malgré une nuit de jeûne doivent également faire évoquer une gastroparésie. Un examen permettant de mesurer objectivement la vidange gastrique est donc indispensable pour pouvoir poser le diagnostic.
Quelles sont les principales causes ?
Les 3 principales causes de gastroparésie sont le diabète, une chirurgie œso-gastrique et l’origine idiopathique. Il existe cepen- dant de nombreuses autres causes de gastroparésie (Tableau 1). Parmi les causes récemment soulignées, la prise d’opioïdes est fréquente, y compris chez les malades souffrant de gastroparésie diabétique ou idiopathique. La consommation d’opioïdes est associée à une plus grande sévérité des symptômes et à un allongement plus important de la vidange gastrique (10). Les autres causes médicamenteuses ne sont pas à négliger (Tableau 1).
| Gastroparésie par atteinte neurologique |
- Post-chirurgie (vagotomie)
- Diabète
- Médicaments (anticholinergique, opioïdes, antidépresseurs notamment tricycliques, phénothiazines, L-Dopa, anticalciques, hydroxyde d’alumine)
- Infections (virus Epstein-Barr, virus varicelle-zona, trypanosoma cruzi)
- Sclérose en plaques
- Accident vasculaire cérébral
|
| Gastroparésie par atteinte myogène |
- Sclérodermie
- Polymyosite
- Amylose
- Dystrophie musculaire progressive
|
| Autres |
- Syndrome de Zollinger Ellison
- Lésions radiques gastro-intestinales
- Anorexie mentale, dénutrition
- Hypothyroidie
|
| Gastroparésie idiopathique |
Tableau 1 : Causes de gastroparésie
Comment faire le diagnostic ?
Il existe 3 méthodes diagnostiques validées pour faire le diagnostic de gastroparésie (11). Ces tests sont indiqués après l’échec d’une première ligne de traitement et après la réalisation d’une fibroscopie œso-gastro-duodénale avec biopsies gastriques éliminant une infection par Helicobacter Pylori.
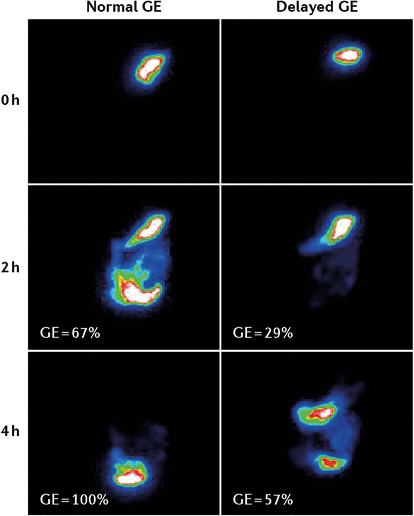
- La scintigraphie gastrique sur 4 heures (figure 2) est le test de référence (12, 13). Elle consiste à mesurer à l’aide d’une gamma-caméra la décroissance de la radioactivité dans l’aire gastrique après l’ingestion d’un repas isotopique standardisé (255 Kcal, pauvre en graisse avec un blanc d’œuf). La radioactivité mesurée dans l’aire gastrique est proportionnelle au volume du repas restant. Une mesure horaire sur une durée de 4 heures est recommandée (12, 13). L’évaluation à la première heure sert au diagnostic de vidange gastrique accélérée (dumping syndrome) et celles réalisées aux 2e et 4e heures servent au diagnostic de gastroparésie. Le marqueur le plus reproductible est le temps de rétention à 4 heures qui doit être inférieur à 10 %. Cette méthode est reproductible mais irradiante, et donc déconseillée chez les femmes enceintes ou à risque de grossesse. De même, une répétition des examens est difficile avec cette méthode.

Figure 2 : Exemples de vidanges gastriques évaluées par scintigraphie gastrique (14)
Nature Reviews | Gastroenterology & Hepatology
Keller, J. et al. (2018) Advances in the diagnosis and classification of gastric and intestinal motility disorders Nat. Rev. Gastroenterol. Hepatol. doi:10.1038/nrgastro.2018.7
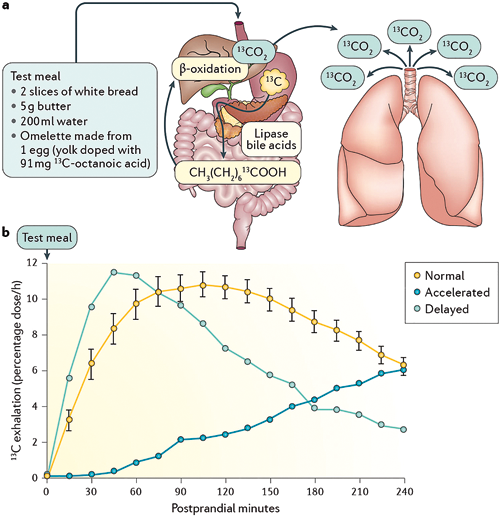
- La vidange gastrique par test respiratoire au carbone 13 (figure 3) est une alternative à la scintigraphie, non invasiveet validée (13). Elle utilise un repas marqué avec du carbone 13, isotope stable du carbone 12. Deux substrats comportant le C13 peuvent être utilisés, l’acide octanoïque et le spirulina platensis. Mélangés au jaune d’œuf, ils quittent l’estomac à la même vitesse que les solides. Après absorption dans le duodénum, ils sont finalement métabolisés et le C13 excrété dans l’air expiré sous forme de 13CO . Ce test est simple, sûr, peu coûteux et non irradiant. Des mesures répétées peuvent être réalisées sans risque. Ses résultats sont corrélés à ceux de la scintigraphie gastrique aux solides (15). Ses limites sont liées aux artefacts possibles en cas de malabsorption intestinale ou de maladies hépatiques et pulmonaires.

Figure 3 : Vidange gastrique par test respiratoire à l’acide octanoïque marqué au 13C (14)
Nature Reviews | Gastroenterology & Hepatology
Keller, J. et al. (2018) Advances in the diagnosis and classification of gastric and intestinal motility disorders Nat. Rev. Gastroenterol. Hepatol. doi:10.1038/nrgastro.2018.7
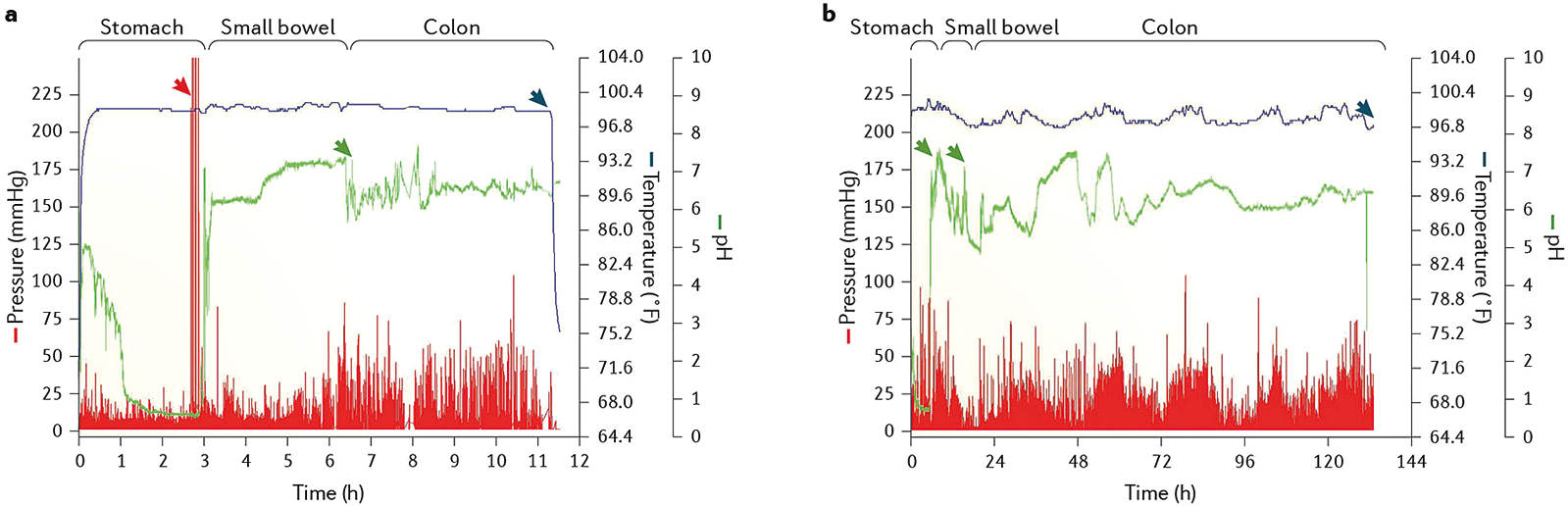
- La smartpill® (figure 4) peut également mesurer de manière non invasive la vidange gastrique. La smartpill® est une capsule à usage unique, non digestible qui est ingérée puis vidangée de l’estomac par les phases III antro-duodénales avec les particules indigestibles. Elle permet une mesure du pH, de la pression et de la température le long du tractus gastro-intestinal, les variations de pH servant à la détermination des temps de transit gastrique, grêlique et colique.

Figure 4 : Exemple d’enregistrement par Smartpill® (14)
Nature Reviews | Gastroenterology & Hepatology
Keller, J. et al. (2018) Advances in the diagnosis and classification of gastric and intestinal motility disorders Nat. Rev. Gastroenterol. Hepatol. doi:10.1038/nrgastro.2018.7
Le test aux marqueurs radio-opaques possède une fiabilité médiocre et ne doit être envisagé que lorsque les autres tests ne sont pas réalisables.
L’IRM et l’échographie peuvent également être utilisées en recherche clinique, mais il s’agit de techniques peu accessibles et il est parfois difficile de différencier au sein de la cavité gastrique le repas test des sécrétions gastriques.
Étude de la fonction pylorique
Désormais, il est également possible de réaliser des explorations reposant sur les mécanismes physiopathologiques en complé- ment de l’étude de la vidange gastrique. L’endoFLIP® récemment commercialisé permet de mesurer la pression et la disten- sibilité pylorique (16, 17). Une altération de la distensibilité pylorique est observée chez 1/3 des patients gastroparétiques.
Cette anomalie est corrélée au temps de vidange gastrique, aux symptômes et à la qualité de vie (16). De plus, la diminution de la distensibilité pylorique pourrait être prédictive de la réponse thérapeutique après injection intrapylorique de toxine botu- lique (18) et après pyloromyotomie (19). Cette technique reste encore difficilement accessible et n’est souvent disponible que dans certains centres experts.
Comment traiter ?
La gastroparésie est une pathologie difficile à traiter, seulement 1/3 des patients étant améliorés après 1 an de suivi (20). Les facteurs associés à une absence d’amélioration sont le surpoids et l’obésité, la présence de douleurs abdominales sévères, l’as- sociation à un RGO ou à une dépression (20).
Traitement de 1re intention
Le traitement de première ligne de la gastroparésie associe des règles hygiéno-diététiques et les prokinétiques. La prise en charge doit également tenir compte de la prescription associée de médicaments ralentissant la vidange gastrique (Tableau 1), notamment la prise d’opioïdes.
Le régime repose sur la réalisation de petits repas fréquents en favorisant les liquides aux solides. Les aliments hypercalo- riques, riches en graisses et en fibres sont déconseillés. Le niveau de preuve de ces mesures est cependant faible en raison de l’absence d’essai ayant prouvé son efficacité.
Le métoclopramide est un antagoniste du récepteur dopaminergique D2 et exerce des effets prokinétique et antiémétique. Le métoclopramide franchissant la barrière hémato-encéphalique, ses effets indésirables sont essentiellement centraux avec en particulier la survenue d’un syndrome extra-pyramidal pouvant aller jusqu’à la dyskinésie (21).
La dompéridone est un antagoniste périphérique du récepteur dopaminergique D2. Elle exerce ses effets antiémétiques sur le centre du vomissement situé sur le plancher du 4e ventricule qui est dépourvu de barrière hémato-encéphalique à ce niveau. Son principal effet secondaire est l’allongement du QT. Une vigilance supplémentaire est donc nécessaire en cas de prescrip- tion prolongée, compte tenu des effets secondaires à type d’arythmie cardiaque ou de mort subite. Il est recommandé de le donner à la dose minimale efficace pour une durée la plus courte possible. La réalisation préalable d’un ECG peut être néces- saire en cas d’administration concomitante de médicaments qui allongent le QT (antiarythmiques de classe Ia et III, certains neuroleptiques, les formes intraveineuses de l’érythromycine, la spiramycine et la vincamine ; certains antiparasitaires, les médicaments hypokaliémiants, en particulier les diurétiques). Il est contre indiqué en cas de maladies cardiaques sous-jacentes de type insuffisance cardiaque congestive, de troubles électrolytiques, d’allongement du QT connu, d’administration conco- mitante de médicaments qui allongent le QT ou d’inhibiteur puissant du CYP3A4. Une étude récente montre des résultats rassurant sur l’allongement du QT aux doses utilisées (22).
L’érythromycine est un antibiotique ayant la particularité d’être, à faible dose, un agoniste du récepteur à la motiline. L’érythromycine stimule l’apparition de phases III antro-duodénales, accélérant ainsi la vidange gastrique. L’érythromycine est plus efficace par voie intra-veineuse que par voie orale, et son utilisation au long cours se heurte à un phénomène de tachy- phylaxie. Par voie orale, la posologie est de 250 mg 2 à 4 fois par jour, par voie intra-veineuse de 200 mg sur une durée de 30 minutes. Un traitement intermittent, préférentiellement par voie veineuse, peut être une possibilité thérapeutique. À noter également que l’érythromycine augmente le tonus fundique et peut aggraver un trouble de l’accommodation déjà présent (23). L’érythromycine est un puissant inhibiteur du cytochrome P450 3A4 et peut être à l’origine de nombreuses interactions médicamenteuses avec risque d’allongement du QT et de torsade de pointe. La présence de troubles électrolytiques ou d’une cardiopathie sous-jacente favorise également ce risque cardiaque. Un ECG pré-thérapeutique peut être nécessaire et l’association avec les médicaments allongeant le QT doit être évitée. Les effets indésirables à type de douleur épigastrique, nausée et diarrhée sont fréquents.
Traitement médicamenteux de 2e intention
Le prucalopride est un agoniste des récepteurs sérotoninergiques de type 5-HT4 dont l’indication est la constipation chro- nique. Une étude de phase II a démontré son efficacité sur l’accélération de la vidange gastrique chez des patients gastroparé- tiques, s’accompagnant d’une amélioration symptomatique (24). Le principal problème de ce traitement est l’absence d’AMM et de remboursement en France en raison d’un faible niveau de preuve.
Traitement endoscopique et chirurgical
La stimulation électrique gastrique consiste à implanter 2 électrodes dans la paroi antrale de la grande courbure de l’estomac. Un boîtier de stimulation implanté dans la paroi abdominale permet de délivrer des stimulations le plus souvent à une fréquence de 12/min avec une durée d’impulsion de 330 µs et une amplitude de 5 mA. Les mécanismes de son efficacité ne sont pas connus, mais ne passent pas par une accélération de la vidange gastrique. Une étude randomisée, prospective, multicentrique française récente a prouvé l’efficacité de la stimulation gastrique chez des patients avec vomissements inex- pliqués, associés ou non à une gastroparésie. Elle permettait une amélioration symptomatique avec un rapport coût efficacité positif (25). Actuellement, ce traitement n’est disponible que dans des centres experts et n’est pas remboursé (coût du dispositif médical supérieur à 10 000 €).
L’injection de toxine botulique dans le pylore n’a pas montré son efficacité dans 2 études contrôlées de faible puissance et n’a donc pas l’AMM dans cette indication. Par contre, il a récemment été montré que la mesure de la distensibilité pylorique permettait de sélectionner les patients qui vont être répondeurs à 3 mois de l’injection de toxine botulique (18).
La pyloromyotomie par voie endoscopique (G-POEM) s’est développée au cours des dernières années. La technique consiste en une incision muqueuse en amont du pylore, puis à la réalisation d’un tunnel par dissection. Ce tunnel permet la réalisation d’une pyloromyotomie remontant sur la musculeuse antrale. Le tunnel est ensuite fermé par des clips. À l’heure actuelle, aucune étude contrôlée dans la gastroparésie n’est disponible. Néanmoins, les quelques études ouvertes avec recul à court terme rapportent une amélioration symptomatique de la qualité de vie et également de la vidange gastrique (26). Il existe respectivement 3,2 % et 2,1 % d’effets indésirables per et post procédure (26). Comme pour la toxine botulique, l’endoFLIP permettrait une meilleure sélection des patients répondeurs à cette thérapeutique (19).
Prise en charge nutritionnelle
La prise en charge nutritionnelle peut être une thérapeutique de dernier recours, après échec de l’ensemble des autres traitements, mais elle doit également s’envisager en cas de dénutrition associée. Elle doit être discutée dès lors que la perte de poids est supérieure à 5 % sur 1 mois, à 10 % sur 6 mois ou lorsque l’IMC est inférieur à 18 (27).
Compte tenu de sa moindre morbidité et de sa meilleure efficacité, la nutrition entérale est préférable à la nutrition parentérale. Une nutrition en site jéjunal est recommandée. Un apport par sonde naso-jéjunale est tenté avant de discuter d’une jéjunos- tomie d’alimentation. Elle peut soit permettre de passer un cap difficile, soit orienter vers une jéjunostomie d’alimentation si besoin (28). Il est recommandé de débuter la nutrition avec des solutions polymériques (1,0 à 1,5kcal.mL-1), avec une infusion lente (20-25 mL.h-1) avant d’augmenter le débit progressivement (60 mL.h-1 sur 12 à 15 heures par jour). La nutrition doit être réévaluée après une période de 4 à 6 semaines pour discuter de sa poursuite.
Conclusion
Les principales étiologies de la gastroparésie sont le diabète, la chirurgie œso-gastrique et l’origine idiopathique. Sa prévalence est de 0,16 %. Les principaux symptômes sont la nausée, les vomissements, la plénitude post-prandiale et la satiété précoce. Des douleurs abdominales et un ballonnement peuvent également être observés.
La dernière décennie a été un tournant dans la prise en charge de la gastroparésie, avec le développement d’une thérapeutique à la carte. Les traitements ciblés agissent soit sur la composante symptomatique (anti-émétiques, stimulation gastrique), soit sur les mécanismes sous-jacents comme la relaxation fundique ou la relaxation pylorique. Malgré ces progrès, la gastroparésie reste une pathologie difficile à traiter avec un fort impact sur la qualité de vie, voire parfois sur le statut nutritionnel.
Références
- Parkman HP, Hasler WL, Fisher American Gastroenterological Association medical position statement: diagnosis and treatment of gastroparesis. Gastroenterology. 2004 Nov;127(5):1589-91.
- Bharucha Epidemiology and natural history of gastroparesis. Gastroenterol Clin North Am. 2015 Mar;44(1):9-19.
- Pasricha PJ, Colvin R, Yates K, Hasler WL, Abell TL, et Characteristics of patients with chronic unexplained nausea and vomiting and normal gastric emptying. Clin Gastroenterol Hepatol. 2011 Jul;9(7):567-76 e1-4.
- Sarnelli G, Caenepeel P, Geypens B, Janssens J, Tack Symptoms associated with impaired gastric emptying of solids and liquids in functional dyspepsia. Am J Gastroenterol. 2003 Apr;98(4):783-8.
- Horowitz M, Su YC, Rayner CK, Jones Gastroparesis: prevalence, clinical significance and treatment. Can J Gastroen- terol. 2001 Dec;15(12):805-13.
- Syed AR, Wolfe MM, Calles-Escandon Epidemiology and Diagnosis of Gastroparesis in the United States: A Popula- tion-based Study. J Clin Gastroenterol. 2019 May 22.
- Choung RS, Locke GR, 3rd, Schleck CD, Zinsmeister AR, Melton LJ, 3rd, et Risk of gastroparesis in subjects with type 1 and 2 diabetes in the general population. Am J Gastroenterol. 2012 Jan;107(1):82-8.
- Parkman HP, Wilson LA, Hasler WL, McCallum RW, Sarosiek I, et al. Abdominal Pain in Patients with Gastroparesis: Associations with Gastroparesis Symptoms, Etiology of Gastroparesis, Gastric Emptying, Somatization, and Quality of Dig Dis Sci. 2019 Aug;64(8):2242-55.
- Tack J, Carbone F, Holvoet L, Vanheel H, Vanuytsel T, et al. The use of pictograms improves symptom evaluation by patients with functional dyspepsia. Aliment Pharmacol 2014 Sep;40(5):523-30.
- Hasler WL, Wilson LA, Nguyen LA, Snape WJ, Abell TL, et al. Opioid Use and Potency Are Associated With Clinical Features, Quality of Life, and Use of Resources in Patients With Clin Gastroenterol Hepatol. 2019 Jun;17(7):1285-94 e1.
- Fox MR, Kahrilas PJ, Roman S, Gyawali CP, Scott SM, et al. Clinical measurement of gastrointestinal motility and function: who, when and which test? Nat Rev Gastroenterol Hepatol. 2018 Sep;15(9):568-79.
- Abell TL, Camilleri M, Donohoe K, Hasler WL, Lin HC, et al. Consensus recommendations for gastric emptying scintigraphy: a joint report of the American Neurogastroenterology and Motility Society and the Society of Nuclear J Nucl Med Technol. 2008 Mar;36(1):44-54.
- Szarka LA, Camilleri M, Vella A, Burton D, Baxter K, et A stable isotope breath test with a standard meal for abnormal gastric emptying of solids in the clinic and in research. Clin Gastroenterol Hepatol. 2008 Jun;6(6):635-43 e1.
- Keller J, Bassotti G, Clarke J, Dinning P, Fox M, et Expert consensus document: Advances in the diagnosis and classifi- cation of gastric and intestinal motility disorders. Nat Rev Gastroenterol Hepatol. 2018 May;15(5):291-308.
- Chew CG, Bartholomeusz FD, Bellon M, Chatterton BE. Simultaneous 13C/14C dual isotope breath test measurement of gastric emptying of solid and liquid in normal subjects and patients: comparison with scintigraphy. Nucl Med Rev Cent East 2003;6(1):29-33.
- Gourcerol G, Tissier F, Melchior C, Touchais JY, Huet E, et al. Impaired fasting pyloric compliance in gastroparesis and the therapeutic response to pyloric dilatation. Aliment Pharmacol 2015 Feb;41(4):360-7.
- Malik Z, Sankineni A, Parkman Assessing pyloric sphincter pathophysiology using EndoFLIP in patients with gastro- paresis. Neurogastroenterol Motil. 2015 Apr;27(4):524-31.
- Desprez C, Melchior C, Wuestenberghs F, Zalar A, Jacques J, et Pyloric distensibility measurement predicts sympto- matic response to intrapyloric botulinum toxin injection. Gastrointest Endosc. 2019 Apr 25.
- Jacques J, Pagnon L, Hure F, Legros R, Crepin S, et al. Peroral endoscopic pyloromyotomy is efficacious and safe for refractory gastroparesis: prospective trial with assessment of pyloric function. Endoscopy. 2019 Jan;51(1):40-9.
- Pasricha PJ, Yates KP, Nguyen L, Clarke J, Abell TL, et Outcomes and Factors Associated With Reduced Symptoms in Patients With Gastroparesis. Gastroenterology. 2015 Dec;149(7):1762-74 e4.
- Al-Saffar A, Lennernas H, Hellstrom Gastroparesis, metoclopramide, and tardive dyskinesia: Risk revisited. Neuro- gastroenterol Motil. 2019 May 2:e13617.
- Field J, Wasilewski M, Bhuta R, Malik Z, Cooper J, et Effect of Chronic Domperidone Use on QT Interval: A Large Single Center Study. J Clin Gastroenterol. 2019 Oct;53(9):648-52.
- Yoon SB, Choi MG, Lim CH, Kim JS, Cho YK, et al. The effect of exenatide and erythromycin on postprandial symptoms and their relation to gastric functions. Digestion. 2012;85(3):211-8.
- Carbone F, Van den Houte K, Clevers E, Andrews CN, Papathanasopoulos A, et Prucalopride in Gastroparesis: A Randomized Placebo-Controlled Crossover Study. Am J Gastroenterol. 2019 Aug;114(8):1265-74.
- Ducrotte P, Coffin B, Bonaz B, Fontaine P, Des Varannes SB, et al. Gastric Electrical Stimulation Reduces Refractory Vomiting in a Randomized Cross-Over Trial. Gastroenterology. 2019 Oct
- Zhang H, Zhang J, Jiang A, Ni Gastric peroral endoscopic myotomy for gastroparesis: A systematic review of efficacy and safety. Gastroenterol Hepatol. 2019 Aug – Sep;42(7):413-22.
- Camilleri M, Parkman HP, Shafi MA, Abell TL, Gerson Clinical guideline: management of gastroparesis. Am J Gastroenterol. 2013 Jan;108(1):18-37; quiz 8.
- Abell TL, Bernstein RK, Cutts T, Farrugia G, Forster J, et al. Treatment of gastroparesis: a multidisciplinary clinical review. Neurogastroenterol Motil. 2006 Apr;18(4):263-83.