LIENS D’INTÉRÊT
Aucun
MOTS-CLÉS
Cirrhose, hypertension portale, transplantation hépatique.
ABRÉVIATIONS
TIPS shunt intra-hépatique porto-systémique transjugulaire ; MELD Model for End Stage Liver Diseases ; DCIP, dysfonction circulatoire induit par la paracentèse.
Introduction
L’ascite correspond à l’accumulation de liquide dans la cavité péritonéale. La cirrhose est la cause d’ascite la plus fréquente, responsable de près de 90 % des causes d’ascite. D’un autre côté, chez les malades atteints de cirrhose, l’ascite est la complication la plus fréquente. Une ascite est présente chez 40 % des malades au diagnostic de la cirrhose. Au cours du suivi, chez les malades atteints d’une cirrhose compensée, la probabilité de survenue d’ascite est d’environ 30 % à 5 ans (1). Alors que l’ascite peut être le plus souvent contrôlée par le traitement médical, dans environ 10 % des cas, l’ascite est dite réfractaire (2). Les malades atteints d’ascite réfractaire ont un mauvais pronostic à court terme, et doivent être référés à un centre expert pour envisager une prise en charge spécifique.
Cet article discutera la définition et la présentation clinique des malades atteints de cirrhose compliquée d’ascite réfractaire, la prise en charge médicale ainsi que les options thérapeutiques spécifiques de l’ascite réfractaire. Cet article s’appuie largement sur les recommandations de bonnes pratiques de la société européenne d’hépatologie (EASL) parues en 2018 (3).
Physiopathologie de l’ascite réfractaire chez les malades atteints de cirrhose
Pathogénie de l’ascite chez les malades atteints de cirrhose
L’ascite résulte d’une cascade d’évènements hémodynamiques, secondaires à l’hypertension portale, résumées dans la figure 1. L’ascite du cirrhotique est la conséquence de la vasodilatation artérielle splanchnique qui, simultanément, induirait d’une part un sous-remplissage artériolaire et d’autre part une augmentation de la pression dans les capillaires splanchniques (4). Le sous-remplissage artériel entraîne l’activation de mécanismes de rétention sodée (système rénine angiotensine aldostérone et système nerveux sympathique). L’hypertension portale et la diminution de la résistance vasculaire splanchnique sont à l’origine d’une augmentation de la production de lymphe, qui ne peut plus être compensée par l’augmentation du retour lymphatique dans la circulation systémique. La conséquence de ces deux anomalies est la fuite de liquide dans la cavité abdominale et la formation d’ascite.

Figure 1 : Physiopathologie de l’ascite chez les malades atteints de cirrhose
Facteurs contribuant à l’ascite réfractaire
Insuffisance rénale fonctionnelle
Lorsque la cirrhose et l’hypertension portale progressent, suite à la vasodilatation artérielle splanchnique et à l’hypovolémie qui en résulte, le maintien de la pression artérielle est médié par une vasoconstriction dans les territoires vasculaires extra- splanchniques incluant les reins. La vasoconstriction rénale (accompagnée par la chute de filtration glomérulaire consécutive) est un élément majeur dans la progression de l’ascite : l’insuffisance rénale entraîne une augmentation de la rétention de sodium (5). La réabsorption du sodium au niveau du tubule contourné proximal augmente et sa livraison aux segments distaux du néphron est réduite. Une quantité moindre de sel dans la partie distale du tubule (la portion « diluante » du néphron) entraîne une diminution franche de l’excrétion d’eau libre (6). La rétention rénale de sodium se produit dans le néphron proximal et donc en amont du site d’action des diurétiques que ce soient les anti-minéralocorticoïdes ou le furosémide. Suite aux altérations de perfusion rénale de ces patients, on constate donc un manque d’efficacité du traitement diurétique.
Déséquilibre entre formation et réabsorption
Le volume d’ascite accumulé dans la cavité péritonéale est la différence entre la production du liquide et sa résorption (7). La résorption de l’ascite semble être principalement assurée par les lymphatiques du péritoine diaphragmatique. Shear et al. ont montré que le taux de réabsorption de liquide de la cavité abdominale est lié à la pression intra-abdominale et que la capacité maximale de réabsorption à travers le péritoine chez les patients atteints de cirrhose alcoolique est inférieure à 500 ml/jour (8).
Rôle du diabète
La prévalence du diabète chez les malades atteints de cirrhose avec ascite réfractaire varie entre 20 et 30 % (9, 10). Chez les malades atteints d’ascite réfractaire, le diabète est plus fréquemment observé dans la classe de sévérité Child-Pugh B que dans la classe C (10). Cela suggère que la gravité de la maladie du foie d’une part, et le diabète d’autre part, peuvent être à l’origine du caractère réfractaire de l’ascite.
Définition de l’ascite réfractaire
Le terme « ascite réfractaire » correspond à une ascite qui ne peut pas être mobilisée (l’ascite persiste malgré les diurétiques) ou à une ascite dont la récidive précoce (dans les 4 semaines après mobilisation initiale) ne peut pas être empêchée par les moyens médicaux. L’ascite réfractaire peut être résistante ou intraitable par les diurétiques (tableau 1). En plus de l’ascite réfractaire, il existe une forme moins sévère d’ascite difficile à traiter, appelée ascite récidivante. Cette forme clinique correspond au stade précoce d’ascite réfractaire.
| Définition des formes cliniques d’ascite difficile à traiter |
| Ascite récidivante | Au moins 3 poussées d’ascite en 1 an, malgré un traitement médical bien conduit |
| Ascite résistante | Ascite qui ne peut pas être mobilisée ou dont la récidive précoce ne peut être empêchée en raison d’un manque de réponse à la restriction du sodium alimentaire (< 88 mmol par jour) et un traitement diurétique intensif (spironolactone 400 mg/jour et furosémide à 160 mg/jour) |
| Ascite intraitable | Ascite qui ne peut pas être mobilisée ou dont la récidive précoce ne peut être évitée en raison du développement de
complications qui empêchent l’utilisation d’une dose efficace de diurétique |
| Évaluation de la réponse aux diurétiques |
| Réponse | Sur une semaine de traitement diurétique maximal Perte de 0,8 kg par jour sur 4 jours ou diurèse sodée |
| Récidive précoce | Récidive d’ascite de grade 2 ou 3 moins de 4 semaines après la mobilisation |
| Complications induites par les diurétiques |
| Encéphalopathie | Apparition d’encéphalopathie en l’absence d’autre facteur favorisant |
| Insuffisance rénale | Augmentation de la créatinine sérique >100 % de la valeur initiale ou >177 mol/L, en l’absence d’autre cause |
| Hyponatrémie | Baisse de la natrémie <10 mmol/l ou <125 mmol/L |
| Hypo ou hyperkaliémie | Baisse de la kaliémie <3 mmol/l ou >6 mmol/l en l’absence d’autre cause |
| Crampes | Crampes invalidantes |
Tableau 1 : Définitions de l’International Ascites Club pour le diagnostic d’ascite réfractaire [d’après (11)]
Il est important de souligner que le diagnostic d’ascite récidivante comme celui d’ascite réfractaire ne peut être posé que chez un malade stable (à distance d’une complication comme une infection ou une hémorragie) et après une observation des malades pendant 4 semaines au minimum (3). Afin de limiter le caractère subjectif de ces termes, les définitions de l’ascite réfractaire, de la réponse aux diurétiques, et des complications induites par les diurétiques, ont été clarifiés lors la conférence de consensus du Club International de l’Ascite en 2003 (11). Celles-ci sont résumées dans le tableau 1.
Manifestations
Présentation clinique des malades atteints d’ascite réfractaire
L’ascite réfractaire est le témoin d’une maladie hépatique avancée, compliquée d’une hypertension portale sévère.
Ainsi, d’autres complications de l’hypertension portale doivent être recherchées. Des varices œsophagiennes à risque de saignement sont présentes chez 50 % des malades atteints d’ascite réfractaire, et doivent être recherchées par une endoscopie œso-gastroduodénale. Une encéphalopathie hépatique est également présente dans un tiers des cas (12).
Il est important de noter que malgré la sévérité de la maladie hépatique, seulement deux tiers des malades atteints de cirrhose compliquée d’ascite réfractaire ont une cirrhose classée Child-Pugh C (12,13). Les autres malades ont des paramètres de fonction hépatique (taux de prothrombine, bilirubine plasmatique) peu altérés, et ont une cirrhose classée Child-Pugh B, uniquement en raison de l’ascite importante. De même, dans une étude récente portant sur 151 malades atteints d’ascite réfractaire, le score MELD (Model for End Stage Liver Disease) médian était de 19 (12). Enfin, 30 % des malades avec ascite réfractaire présentent une sarcopénie (14). La sarcopénie est associée au décès sur la liste d’attente de transplantation hépatique (15).
Hydrothorax hépatique
L’hydrothorax hépatique correspond à un épanchement pleural abondant, chez un malade atteint de cirrhose, en l’absence de pathologie cardiaque, pleural ou pulmonaire. L’hydrothorax hépatique est lié à une accumulation du liquide d’ascite dans la cavité pleurale. La formation de l’hydrothorax est liée à un transfert unidirectionnel d’ascite de la cavité abdominale vers la cavité pleurale, du fait d’un gradient de pression hydrostatique, au travers de brèches diaphragmatiques. L’hydrothorax est localisé à droite dans 85 % des cas (figure 2). La concentration de protéines peut être plus élevée dans l’hydrothorax que dans l’ascite, toutefois la concentration de protéines dans l’hydrothorax est généralement inférieur à 25 grammes par litre.

Figure 2 : Radiographie thoracique d’un malade atteint de cirrhose compliquée d’hydrothorax hépatique, montrant un volumineux épanchement pleural droit
Les complications associées à l’hydrothorax hépatique sont les suivantes : (i) l’infection spontanée du liquide pleural, également appelée empyème spontané bactérien pleural, son incidence est de 20 % à 6 mois ; (ii) l’hémothorax et/ou le pneumothorax, complications iatrogènes secondaires aux thoracocentèses évacuatrices itératives. Au total, les malades atteints d’hydrothorax hépatique ont un mauvais pronostic à court terme. Dans une étude récente de 949 malades atteints de cirrhose compliquée d’hydrothorax hépatique, la mortalité à 6 mois était de 36 % (16).
Pronostic de l’ascite réfractaire
L’apparition d’ascite marque un tournant dans l’histoire de la maladie hépatique, avec le passage d’un stade de cirrhose compensée à un stade de cirrhose décompensée. Les malades atteints de cirrhose compensée ont une survie > 80 % à 5 ans, les malades avec ascite sensible aux diurétiques ont une survie de 70 % à 2 ans (17). En revanche, les malades atteints de cirrhose avec une ascite difficile à traiter ont une mortalité élevée à court terme. En effet, dans une étude française récente, ayant inclus 62 malades atteints de cirrhose compliquée une ascite récidivante, la survie sans transplantation était de 52 % à un an, chez les malades traités par paracentèse (18). Le pronostic le plus péjoratif est observé chez les malades atteints d’ascite réfractaire, avec une survie inférieure à 50 % à un an (12,19). Par conséquent, il est recommandé d’adresser rapidement les malades atteints d’ascite difficile à traiter dans un centre expert (3).
Prise en charge médicale de l’ascite difficile à traiter
Traitement étiologique de la cirrhose
Quelle que soit la cause de la cirrhose, la prise en charge du traitement du facteur causal est primordiale. En cas de cirrhose compensée, le traitement du facteur étiologique de la cirrhose est associé à une réduction de l’incidence des complications. En cas de cirrhose décompensée, le traitement du facteur étiologique peut également permettre, dans une moindre mesure, le retour à un stade de cirrhose compensée.
Chez les malades atteints de cirrhose alcoolique, le sevrage éthylique est associé à une régression de l’hypertension portale (20). Ainsi, chez des malades atteints d’ascite réfractaire, le sevrage éthylique permet le retour à un stade d’ascite sensible aux diurétiques, voire une disparition de l’ascite, dans 20 % des cas (13, 21). De façon importante, une observation prolongée des malades, pouvant aller jusqu’à deux ans, est parfois nécessaire.
De façon similaire, chez les malades atteints de cirrhose virale B décompensée, le traitement antiviral permet le retour à un stade de cirrhose compensée pour 2/3 des malades (22). Enfin, des résultats similaires ont été observés chez les malades atteints de cirrhose virale C : le traitement antiviral direct est associé à un retour à une cirrhose classée Child-Pugh A dans 80 % des cas (23).
Il est important de souligner que l’amélioration de la fonction hépatique et de l’hypertension portale en lien avec traitement du facteur étiologique de la cirrhose est inconstante. Les malades qui gardent une cirrhose décompensée ont une mortalité élevée à court terme. Par conséquent, le traitement du facteur causal de la cirrhose ne doit pas retarder la prise en charge dans un centre tertiaire et/ou de transplantation hépatique.
Arrêt des diurétiques
Chez les malades atteints de cirrhose résistante et/ou intraitable par les diurétiques, il est recommandé d’arrêter les diurétiques si la natriurèse est inférieure à 30 mmol/jour, en raison de l’absence de bénéfice (3).
Prévention de l’infection spontanée du liquide d’ascite
Chez les malades atteints de cirrhose avec ascite, l’administration prophylactique de fluoroquinolones au long cours permet de réduire l’incidence d’infection du liquide d’ascite (24, 25), mais au prix d’une augmentation des infections par des bactéries multi-résistantes.
La mortalité de l’infection spontanée du liquide d’ascite est élevée chez les malades ayant une cirrhose compliquée d’ascite pauvre en protéines (<15 grammes/litre) associée à une dysfonction hépatique (classée Child-Pugh C) ou une dysfonction rénale (élévation de la créatininémie ou de l’urée plasmatique). Chez ces malades, l’administration prophylactique de fluoroquinolones permettait de réduire la mortalité à 3 et 6 mois (24, 25).
Par conséquent, l’administration préventive d’antibiotiques est recommandée après un premier épisode d’infection du liquide d’ascite, ainsi que chez les malades ayant une cirrhose compliquée d’ascite pauvre en protéines (<15 grammes/litre) associée à une dysfonction hépatique, jusqu’à disparition de l’ascite ou transplantation hépatique. Dans les autres cas, l’antibiothérapie prophylactique n’est pas justifiée en raison de l’absence de bénéfice clair sur le pronostic à court terme (3).
Arrêt des béta-bloquants
Les béta-bloquants non cardio-sélectifs sont recommandés pour prévenir l’hémorragie digestive par rupture de varices œsophagiennes, après un 1er épisode hémorragique en association à l’éradication endoscopique des varices œsophagiennes (prophylaxie secondaire). Ils sont également recommandés chez les malades n’ayant jamais saigné (prophylaxie primaire), en cas de varices œsophagiennes de taille moyenne ou grande, et en cas de varices de petite taille si celles-ci présentent des signes rouges ou chez les malades ayant une cirrhose classée Child-Pugh C (26). Chez les malades atteints de cirrhose compliquée d’ascite réfractaire, les bétabloquants non cardio-sélectifs étaient associés à une sur-mortalité dans des études, et à une augmentation de la survie dans d’autres. Aucune de ces études n’était contrôlée (27). Les recommandations actuelles sont d’utiliser les bétabloquants avec prudence, voire d’envisager un arrêt transitoire des bétabloquants chez les malades atteints d’ascite réfractaire en cas (i) d’insuffisance rénale aiguë, (ii) de sepsis, ou (iii) d’hypotension artérielle (pression artérielle systolique < 90 mm Hg) (3, 26).
Perfusions d’albumine intra-veineuse au long cours
Chez les malades atteints de cirrhose avec ascite difficile à traiter (mais non réfractaire), une étude récente randomisée a montré que l’administration régulière d’albumine (40 grammes toutes les 2 semaines) permettait de réduire de façon significative le développement d’une ascite réfractaire, ainsi que des autres complications de la cirrhose, telles que l’encéphalopathie hépatique, le syndrome hépato-rénal ou l’infection spontanée du liquide d’ascite (28). Ces résultats étaient en faveur d’un effet bénéfique de l’albumine grâce à ses propriétés oncotiques, mais également anti- oxydantes et anti-inflammatoires.
Paracentèse évacuatrice de grand volume
Les paracentèses évacuatrices répétées sont le traitement de première intention le plus largement admis.
Principes
Les paracentèses de grand volume sont effectuées à la demande. Le rythme des paracentèses est guidé par la gêne fonctionnelle des patients. Chez les malades avec une ascite volumineuse, le volume évacué est habituellement supérieur à 5 litres. On parle alors de paracentèse de grand volume. La paracentèse totale raccourcit la durée d’hospitalisation et la procédure peut être réalisée en hospitalisation de jour.
Il est important de disposer d’une échographie contemporaine ou postérieure au diagnostic de la maladie du foie pour s’assurer qu’il n’y a pas de grosse anomalie anatomique dans la région de la fosse iliaque droite et notamment une énorme rate. De plus, en cas de hernie ombilicale, la réduction manuelle de la hernie permet de réduire le risque d’incarcération en lien avec l’évacuation rapide d’ascite.
La recherche d’une infection spontanée du liquide d’ascite, par une analyse cytologique (compte des polynucléaires neutrophiles) et bactériologique (examen direct et culture) est recommandée lors de toute ponction d’ascite, y compris chez un malade asymptomatique. L’utilisation de bandelettes réactives pourrait être une alternative à l’analyse cytologique et bactériologique standard (29).
Complications
La paracentèse est une procédure sûre. L’incidence de complications majeures liées à la procédure est d’environ 1 % (30). L’incidence d’un saignement cliniquement significatif au point de ponction, est très basse. Une étude rétrospective sur plus de 4 500 paracentèses a montré une hémorragie sévère dans seulement 0,5 % des procédures (31). Le recours à la ponction guidée par l’échographie (avec pour but principal de repérer les grosses veines collatérales abdominales pour les éviter) pourrait réduire le risque iatrogène, en particulier chez les malades recevant un traitement anticoagulant ou anti-aggrégant plaquettaire, chez les malades avec une insuffisance rénale ou une thrombopénie sévère (30). L’incidence des infections directement liées à la procédure est très faible, autour de 0,5 % (30).
Cependant, la procédure a de nom–breuses limitations : d’abord, elle induit une dysfonction circulatoire (cf. infra) et elle n’agit pas sur les mécanismes de la formation de l’ascite de sorte que l’épanchement se reproduit rapidement dans la cavité péritonéale. Ensuite, elle peut être source de pertes protéiques et ainsi contribuer à la dénutrition. De plus, les paracentèses peuvent être difficiles à réaliser en raison d’adhérences et/ou de cloisonnements. Enfin, les malades peuvent mal tolérer la répétition des paracentèses.
Les désordres circulatoires induits par la paracentèse
La paracentèse évacuatrice de grand volume, lorsqu’elle est faite seule (c’est-à-dire sans y associer un traitement compensateur) accentue l’hypovolémie efficace, pré-existante, conséquence de la cirrhose. L’ensemble de ces désordres a reçu le nom de dysfonction circulatoire induite par la paracentèse (DCIP) (32). En l’absence de remplissage, la fréquence de la DCIP est de 75 %, et est associée au volume d’ascite évacué : plus celui-ci est élevé, plus grand est le risque de développer un DCIP (33). La DCIP peut être associée à des évènements cliniques significatifs tels que la récidive précoce d’ascite, le développement d’une hyponatrémie de dilution ou d’un SHR. Enfin, le développement d’une DCIP est un indépendamment associé au décès (34). (Tableau 2).
| Altérations hémodynamiques |
Augmentation de la rénine plasmatique
Augmentation de la noradrénaline plasmatique
Augmentation du gradient de pression hépatique |
| Complications |
Hyponatrémie
Insuffisance rénale
Récidive précoce de l’ascite
Décès |
Tableau 2 : Dysfonction circulatoire induite par la paracentèse : anomalies hémodynamiques et complications cliniques
Le remplissage vasculaire au moment de la paracentèse permet de réduire l’incidence de DCIP (35). Plusieurs études ont montré que le remplissage vasculaire par albumine intraveineuse est plus efficace que les autres solutions de remplissage. Plus précisément, l’albumine est supérieure aux autres solutions quand le volume d’ascite évacué est supérieur ou égal à 5 litres, alors que cet avantage n’est plus observé pour les petits volumes de ponction (34, 36). De plus, le remplissage par albumine permet de réduire l’incidence des complications cliniquement significatives après paracentèse, en particulier l’hyponatrémie et la mortalité (35).
Par conséquent, l’utilisation de l’albumine intraveineuse est le traitement de choix pour prévenir la DCIP chez les malades avec une paracentèse ≥ 5 litres (3). La dose recommandée est de 8 g d’albumine à 20 % par litre d’ascite retiré. Il semble raisonnable de ne pas dépasser la dose de 100 g en raison du risque d’œdème pulmonaire.
Intérêt du shunt intra-hépatique porto-systémique transjugulaire (TIPS)
Principe
Le shunt intra-hépatique porto-systémique transjugulaire (TIPS) est une option thérapeutique de choix pour les malades atteints d’ascite réfractaire ou récidivante. Un TIPS efficace fonctionne comme un shunt porto-cave chirurgical et par conséquent, diminue la pression portale intra-hépatique. De plus, la mise en place d’un TIPS permet l’amélioration des désordres hémodynamiques et circulatoires associés à la cirrhose et responsables de l’ascite. En particulier, la mise en place d’un TIPS est associée à une baisse de la pression portale, une diminution de l’activité du système rénine-angiotensine aldostérone et du système nerveux sympathique, une augmentation du débit sanguin rénal et une augmentation de l’excrétion urinaire de sodium (37-39).
Complications
Faisabilité technique et dysfonction
Dans les études les plus récentes, la faisabilité du TIPS était excellente, supérieure à 95 % des cas (40, 41). De plus, la mise en place d’un TIPS est possible en cas de thrombose porte (42). Depuis la généralisation des prothèses couvertes, la dysfonction de TIPS est rare, survenant chez 16 % des malades (40). Celle-ci doit être suspectée en cas de ré-apparition de l’ascite. Il faut toutefois souligner que ces résultats proviennent d’études réalisées par des équipes expertes.
Encéphalopathie post TIPS
L’incidence de l’encéphalopathie hépatique ou son aggravation après la mise en place d’un TIPS est la complication la plus fréquente est de l’ordre de 20 à 30 % (43). Le meilleur traitement préventif de l’encéphalopathie post-TIPS repose sur une sélection adéquate des malades. L’âge et les antécédents d’encéphalopathie pré-TIPS sont des facteurs de risque d’apparition de l’encéphalopathie après cette procédure (44, 45). Le traitement de l’encéphaloapthie post-TIPS repose sur (i) l’éviction des psychotropes, (ii) le lactulose, et la rifaximine. En cas d’encéphalopathie réfractaire ou récidivante, on peut proposer une réduction du calibre du shunt, ou une transplantation hépatique (43).
Insuffisance hépatique
La détérioration de la fonction hépatique post TIPS se traduit par une augmentation de la bilirubine sérique. Les facteurs prédictifs d’une insuffisance hépatique post-TIPS sont un taux de bilirubine élevé avant la mise en place du TIPS, une cirrhose classée Child-Pugh ≥ C11 ou un score MELD > 18 (44, 46). Ce phénomène pourrait être lié à une ischémie hépatique juste après la mise en place du shunt puisque la plupart du volume sanguin portal est directement shunté par le TIPS vers la circulation systémique.
Insuffisance cardiaque
La mise en place du TIPS conduit à une augmentation brutale de la pré-charge avec une augmentation de la pression veineuse centrale. Ceci amène à une augmentation du débit cardiaque de près de 50 % (47). Par conséquent, la présence d’une insuffisance cardiaque et/ou d’une hypertension artérielle pulmonaire sont des contre-indications à la mise en place d’un TIPS et doivent être systématiquement recherchées.
Résultats du TIPS
L’intérêt du TIPS, comparé aux paracentèses répétées, a été étudié dans 7 études randomisées contrôlées. Elles ont montré des résultats discordants (tableau 3). Dans toutes les études, les critères de jugement étaient (i) le contrôle de l’ascite, (ii) la survie, et (iii) l’encéphalopathie hépatique. Le contrôle de l’ascite était plus fréquemment atteint chez les malades recevant un TIPS.
| Auteur, année | Proportion de malades avec ascite réfractaire/ récidivante (%) | Nombre de patients | Contrôle de l’ascite (%) | Encéphalopathie (%) | Survie (%) |
| TIPS | PA | TIPS | PA | TIPS | PA | TIPS | PA |
| Lebrec, 1996 (44) | 100/0 | 13 | 12 | 38 | 0* | 15 | 6 | 29 | 60 |
| Rossle, 2000 (45) | 55/45 | 29 | 31 | 84 | 43* | 23 | 13 | 58 | 32 |
| Ginés, 2002 (48) | 100/0 | 35 | 35 | 51 | 17* | 60 | 34 | 26 | 30 |
| Sanyal, 2003 (49) | 100/0 | 52 | 57 | 58 | 16* | 38 | 21 | 35 | 33 |
| Salerno, 2004 (46) | 68/32 | 33 | 33 | 79 | 42* | 61 | 39 | 59 | 29* |
| Narahar, 2011 (50) | 100/0 | 30 | 30 | 87* | 30 | 20 | 5 | 20 | 5* |
| Bureau, 2017 (18) | 0/100 | 29 | 33 | 52 | 0* | 35 | 35 | 93 | 52* |
Abréviations :TIPS, shunt intra-hépatique porto-systémique transjugulaire ; PA, paracentèse
*différence significative entre le groupe TIPS et paracentèse
Tableau 3 : Résumé des 7 études randomisées contrôlées ayant comparé le TIPS aux paracentèses de grand volume chez les malades atteints de cirrhose et d’ascite difficile à traiter
On note également que les résultats du TIPS étaient meilleurs pour les malades atteints d’une ascite récidivante, par rapport à ceux ayant une ascite réfractaire. En revanche, l’encéphalopathie hépatique survenait plus fréquemment chez les malades recevant un TIPS. Toutefois, il faut souligner que dans les études les plus récentes, ayant inclus des malades atteints de cirrhose avec ascite récidivante, et traités par TIPS couverts, le développement d’une encéphalopathie n’était pas augmenté pour les malades recevant un TIPS. Enfin, un bénéfice sur la survie n’a été observé que dans 3 études sur les 7, ayant inclus les malades les moins sévères. Dans certains cas, le TIPS était même délétère (44). De nombreux facteurs de bon pronostic et de mauvais pronostic après TIPS ont été identifiés (3) (tableau 4). Les résultats sont meilleurs dans les centres dans lesquels au moins 20 procédures sont effectuées chaque année. Ces résultats indiquent que les résultats du TIPS pour traiter l’ascite réfractaire dépendent largement d’une sélection rigoureuse des malades, ainsi que de l’expertise des centres.
| Facteurs de bon pronostic | Facteurs de mauvais pronostic | Contre-indications |
| Âge <70 ans Ascite récidivante Cirrhose Child-Pugh B MELD < 15 Plaquettes > 75 x 109/L + bilirubine < 50 mol/L Ascite riche en protides | Age > 70 ans Ascite réfractaire Cirrhose Child-Pugh C MELD > 15 Plaquettes < 75 x 109/L et/ou bilirubine >50
mol/L Sarcopénie Insuffisance rénale | Insuffisance cardiaque Hypertension artérielle pulmonaire Infection non contrôlée MELD > 18 Encéphalopathie hépatique |
Abréviations : MELD, Model for End Stage Liver Diseases
Tableau 4 : Facteurs de bon et de mauvais pronostic après mise en place d’un TIPS pour ascite réfractaire
Pompe péritonéo-vésicale : le système Alfapump
Le système ALFApump® de Sequana Medical a obtenu l’agrément de la Communauté Européenne (label CE) en juillet 2011, pour les malades atteints de cirrhose avec ascite réfractaire. Ce dispositif médical se compose d’une pompe rechargeable implantée dans l’espace sous-cutané, connectée d’une part à un cathéter placé dans la cavité abdominale, et d’autre part à un cathéter placé dans la vessie (figure 3). Le système recueille en continu l’ascite qui se forme, et le déplace vers la vessie, d’où elle est éliminée par les voies naturelles. L’ALFApump® est rechargée sans fil et peut être programmée selon les besoins de chaque patient. Ce dispositif, tout comme la paracentèse de grand volume, est uniquement symptomatique, et n’a pas d’effet sur la formation de l’ascite.

Figure 3 : Schéma représentant le principe du dispositif Alfapump®
Les principaux avantages de ce dispositif est sa mise en place facile, lors d’une brève intervention chirurgicale. Plusieurs études, dont une seule contrôlée, ont évalué montré que le dispositif Alfapump® permet un contrôle de l’ascite pour près de 60 % des malades (51, 52). De plus, dans une étude randomisée contrôlée, la qualité de vie était meilleure après la mise en place du dispositif Alfapump® (53).
Dans une méta-analyse ayant inclus 104 malades traités par ce dispositif, des complications techniques (dysfonction du cathéter vésical ou péritonéal, dysfonction de la pompe +/- nécessité de remplacement) étaient observées dans 77 % des cas. Surtout, les complications hépatiques étaient fréquentes. Les complications infectieuses sont au premier plan (infection du liquide d’ascite et urinaire dans 27 % et 20 % des cas, respectivement), malgré une antibioprophylaxie systématique. De plus, 30 % des malades présentaient une insuffisance rénale aiguë (51). Ces résultats suggèrent que malgré l’évacuation lente et continue de l’ascite (et un risque théorique de désordres circulatoires plus faible qu’en cas de paracentèse de grand volume), les perfusions d’albumine pourraient être nécessaires afin de prévenir les complications. Les contre-indications habituelles de l’Alfapump® sont présentées dans le tableau 5.
| Contre-indications |
| Troubles sévères de l’hémostase Thrombopénie sévère |
| Maladie urologique obstructive |
| Insuffisance rénale chronique |
| ATCD d’infection spontanée du liquide d’ascite |
| Ascite cloisonnée |
Tableau 5 : Contre-indications à l’implantation d’un dispositif Alfapump®
Enfin, la limitation actuelle de ce dispositif est son coût. Ce traitement n’est pas remboursé par la sécurité sociale. Une étude est actuellement en cours en France, afin d’évaluer l’éventuel bénéfice médico-économique de ce traitement.
Place de la transplantation hépatique pour ascite réfractaire
La transplantation hépatique se justifie pour plusieurs raisons chez les malades atteints de cirrhose compliquée d’ascite réfractaire. Tout d’abord, les malades atteints d’ascite réfractaire ont un mauvais pronostic à court terme. Ensuite, parmi les options thérapeutiques, les paracentèses et le dispositif Alfapump® sont des traitements symptomatiques, et ne modifient pas le pronostic. De plus, une importante proportion des malades présente des contre-indications à la mise en place d’un TIPS. Enfin, les résultats de la transplantation hépatique dans cette indication sont excellents, avec une survie > 50 % à 5 ans (54).
Les principales limitations de la transplantation hépatique chez les malades atteints de cirrhose compliquée d’ascite réfractaire sont un accès restreint à la transplantation hépatique En effet, les malades atteints de cirrhose ont le plus souvent un score MELD peu élevé, qui ne reflète pas la sévérité de la maladie du foie. Or en France, les greffons hépatiques sont attribués en priorité aux malades ayant les scores MELD les plus élevés.
Afin de pallier à cette limitation, une « composante expert » peut être accordée par les experts, permettant ainsi aux malades atteints d’ascite réfractaire et ayant une contre-indication au TIPS d’avoir un accès à la transplantation hépatique, dans un délai de 6 mois en général, voire 3 mois pour les malades les plus sévères (comme les malades atteints d’un hydrothorax réfractaire).
Conclusion
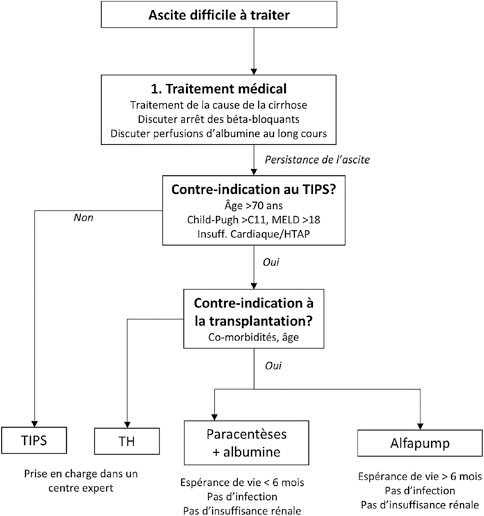
Le diagnostic d’ascite réfractaire est avant tout un diagnostic clinique. Il s’agit d’une complication sévère de la cirrhose. Le traitement de première ligne repose sur une optimisation médicale. Le choix du traitement spécifique repose sur une évaluation rigoureuse des malades, et doit être personnalisé (figure 4). Compte tenu d’un mauvais pronostic à court terme, une transplantation hépatique doit être envisagée, en l’absence de contre-indication, même si la fonction hépatique semble peu altérée.

Figure 4 : Proposition d’algorithme de prise en charge chez un malade atteint d’ascite difficile à traiter
Références
- Nilsson E, Anderson H, Sargenti K, Lindgren S et Prytz Clinical course and mortality by etiology of liver cirrhosis in Sweden: a population based, long-term follow-up study of 1317 patients. Aliment. Pharmacol. Ther. 2019;49:1421-1430.
- Planas R, Montoliu S, Ballesté B, Rivera M, Miquel M et al. Natural history of patients hospitalized for management of cirrhotic Clin. Gastroenterol. Hepatol. Off. Clin. Pract. J. Am. Gastroenterol. Assoc. 2006;4:1385-1394.
- European Association for the Study of the Electronic address: [email protected], European Association for the Study of the Liver. EASL Clinical Practice Guidelines for the management of patients with decompensated cirrhosis. J. Hepatol. 2018;69:406-460.
- Arroyo Pathogenesis, Diagnosis and Treatment of Ascites in Cirrhosis. In: The Textbook of Hepatology: from Basic Science to Clinical Practice, 3rd Edition. Wiley-Blackwell; 2007. p. 666-710.
- Arroyo V et Colmenero Ascites and hepatorenal syndrome in cirrhosis: pathophysiological basis of therapy and current management. J. Hepatol. 2003;38 Suppl 1:S69-89.
- Porcel A, Díaz F, Rendón P, Macías M, Martín-Herrera L et al. Dilutional hyponatremia in patients with cirrhosis and ascites. Arch. Intern. Med. 2002;162:323-328.
- Witte CL, Witte MH et Dumont Lymph imbalance in the genesis and perpetuation of the ascites syndrome in hepatic cirrhosis. Gastroenterology. 1980;78:1059-1068.
- Shear L, Ching S et Gabuzda Compartmentalization of Ascites and Edema in Patients with Hepatic Cirrhosis. N. Engl. J. Med. 1970;282:1391-1396.
- Sersté T, Melot C, Francoz C, Durand F, Rautou P-E et al. Deleterious effects of beta-blockers on survival in patients with cirrhosis and refractory ascites. Hepatol. Baltim. Md. 2010;52:1017-1022.
- Moreau R, Delègue P, Pessione F, Hillaire S, Durand F et al. Clinical characteristics and outcome of patients with cirrhosis and refractory ascites. Liver Int. Off. J. Int. Assoc. Study Liver. 2004;24:457-464.
- Moore KP, Wong F, Gines P, Bernardi M, Ochs A et al. The management of ascites in cirrhosis: report on the consensus conference of the International Ascites Club. Hepatol. Baltim. Md. 2003;38:258-266.
- Sersté T, Melot C, Francoz C, Durand F, Rautou P-E et al. Deleterious effects of beta-blockers on survival in patients with cirrhosis and refractory ascites. Hepatol. Baltim. Md. 2010;52:1017-1022.
- Moreau R, Delègue P, Pessione F, Hillaire S, Durand F et al. Clinical characteristics and outcome of patients with cirrhosis and refractory ascites. Liver Int. Off. J. Int. Assoc. Study Liver. 2004;24:457-464.
- Montano-Loza AJ, Duarte-Rojo A, Meza-Junco J, Baracos VE, Sawyer MB et Inclusion of Sarcopenia Within MELD (MELD-Sarcopenia) and the Prediction of Mortality in Patients With Cirrhosis. Clin. Transl. Gastroenterol. 2015;6:e102.
- Durand F, Buyse S, Francoz C, Laouénan C, Bruno O et al. Prognostic value of muscle atrophy in cirrhosis using psoas muscle thickness on computed tomography. J. Hepatol. 2014;60:1151-1157.
- Jindal A, Mukund A, Kumar G et Sarin Efficacy and safety of transjugular intrahepatic portosystemic shunt in difficult- to-manage hydrothorax in cirrhosis. Liver Int. Off. J. Int. Assoc. Study Liver. 2019;
- Bruno S, Saibeni S, Bagnardi V, Vandelli C, De Luca M et al. Mortality risk according to different clinical characteristics of first episode of liver decompensation in cirrhotic patients: a nationwide, prospective, 3-year follow-up study in Am. J. Gastroenterol. 2013;108:1112-1122.
- Bureau C, Thabut D, Oberti F, Dharancy S, Carbonell N et Transjugular Intrahepatic Portosystemic Shunts With Covered Stents Increase Transplant-Free Survival of Patients With Cirrhosis and Recurrent Ascites. Gastroenterology. 2017;152:157-163.
- Salerno F, Borroni G, Moser P, Badalamenti S, Cassarà L et al. Survival and prognostic factors of cirrhotic patients with ascites: a study of 134 outpatients. Am. J. Gastroenterol. 1993;88:514-519.
- Vorobioff J, Groszmann RJ, Picabea E, Gamen M, Villavicencio R et al. Prognostic value of hepatic venous pressure gradient measurements in alcoholic cirrhosis: a 10-year prospective Gastroenterology. 1996;111:701-709.
- Veldt BJ, Lainé F, Guillygomarc’h A, Lauvin L, Boudjema K et al. Indication of liver transplantation in severe alcoholic liver cirrhosis: quantitative evaluation and optimal timing. J. Hepatol. 2002;36:93-98.
- Liaw Y-F, Sheen I-S, Lee C-M, Akarca US, Papatheodoridis GV et Tenofovir disoproxil fumarate (TDF), emtricitabine/ TDF, and entecavir in patients with decompensated chronic hepatitis B liver disease. Hepatol. Baltim. Md. 2011;53:62-72.
- Manns M, Samuel D, Gane EJ, Mutimer D, McCaughan G et al. Ledipasvir and sofosbuvir plus ribavirin in patients with genotype 1 or 4 hepatitis C virus infection and advanced liver disease: a multicentre, open-label, randomised, phase 2 trial. Lancet Infect. Dis. 2016;16:685-697.
- Fernández J, Navasa M, Planas R, Montoliu S, Monfort D, Soriano G et al. Primary prophylaxis of spontaneous bacterial peritonitis delays hepatorenal syndrome and improves survival in cirrhosis. Gastroenterology. 2007;133:818-824.
- Moreau R, Elkrief L, Bureau C, Perarnau J-M, Thévenot T et al. Effects of Long-term Norfloxacin Therapy in Patients with Advanced Cirrhosis. Gastroenterology. 2018;
- de Franchis R et Baveno VI Expanding consensus in portal hypertension: Report of the Baveno VI Consensus Workshop: Stratifying risk and individualizing care for portal hypertension. J. Hepatol. 2015;63:743-752.
- Reiberger T et Mandorfer M. Beta adrenergic blockade and decompensated cirrhosis. J. Hepatol. 2017;66:849-859.
- Caraceni P, Riggio O, Angeli P, Alessandria C, Neri S et al. Long-term albumin administration in decompensated cirrhosis (ANSWER): an open-label randomised trial. Lancet Lond. Engl. 2018;391:2417-2429.
- Thévenot T, Briot C, Macé V, Lison H, Elkrief L et al. The Periscreen Strip Is Highly Efficient for the Exclusion of Spontaneous Bacterial Peritonitis in Cirrhotic Outpatients. Am. J. Gastroenterol. 2016;111:1402-1409.
- De Gottardi A, Thévenot T, Spahr L, Morard I, Bresson-Hadni S et al. Risk of complications after abdominal paracentesis in cirrhotic patients: a prospective Clin. Gastroenterol. Hepatol. Off. Clin. Pract. J. Am. Gastroenterol. Assoc. 2009;7:906-909.
- Pache I et Bilodeau M. Severe haemorrhage following abdominal paracentesis for ascites in patients with liver disease. Aliment. Pharmacol. 2005;21:525-529.
- Ruiz-del-Arbol L, Monescillo A, Jimenéz W, Garcia-Plaza A, Arroyo V et al. Paracentesis-induced circulatory dysfunction: mechanism and effect on hepatic hemodynamics in cirrhosis. Gastroenterology. 1997;113:579-586.
- Ginès P, Titó L, Arroyo V, Planas R, Panés J et al. Randomized comparative study of therapeutic paracentesis with and without intravenous albumin in cirrhosis. Gastroenterology. 1988;94:1493-1502.
- Ginès A, Fernández-Esparrach G, Monescillo A, Vila C, Domènech E et al. Randomized trial comparing albumin, dextran 70, and polygeline in cirrhotic patients with ascites treated by paracentesis. Gastroenterology. 1996;111:1002-1010.
- Bernardi M, Caraceni P, Navickis RJ, Wilkes MM et al. Albumin infusion in patients undergoing large-volume paracentesis: a meta-analysis of randomized trials. Hepatol. Baltim. Md. 2012;55:1172-1181.
- Sola-Vera J, Miñana J, Ricart E, Planella M, González B et al. Randomized trial comparing albumin and saline in the prevention of paracentesis-induced circulatory dysfunction in cirrhotic patients with ascites. Hepatol. Baltim. Md. 2003;37:1147-1153.
- Quiroga J, Sangro B, Núñez M, Bilbao I, Longo J et Transjugular intrahepatic portal-systemic shunt in the treatment of refractory ascites: effect on clinical, renal, humoral, and hemodynamic parameters. Hepatol. Baltim. Md. 1995;21:986-994.
- Gerbes AL, Gülberg V, Waggershauser T, Holl J et Reiser Renal effects of transjugular intrahepatic portosystemic shunt in cirrhosis: comparison of patients with ascites, with refractory ascites, or without ascites. Hepatol. Baltim. Md. 1998;28:683- 688.
- Lotterer E, Wengert A et Fleig Transjugular intrahepatic portosystemic shunt: short-term and long-term effects on hepatic and systemic hemodynamics in patients with cirrhosis. Hepatol. Baltim. Md. 1999;29:632-639.
- Wang Q, Lv Y, Bai M, Wang Z, Liu H et al. Eight millimetre covered TIPS does not compromise shunt function but reduces hepatic encephalopathy in preventing variceal rebleeding. J. Hepatol. 2017;67:508-516.
- Holster IL, Tjwa ETTL, Moelker A, Wils A, Hansen BE et Covered transjugular intrahepatic portosystemic shunt versus endoscopic therapy + β-blocker for prevention of variceal rebleeding. Hepatol. Baltim. Md. 2016;63:581-589.
- Rodrigues SG, Sixt S, Abraldes JG, De Gottardi A, Klinger C et Systematic review with meta-analysis: portal vein recanalisation and transjugular intrahepatic portosystemic shunt for portal vein thrombosis. Aliment. Pharmacol. Ther. 2019;49:20-30.
- Rössle M. TIPS: 25 years later. J. Hepatol. 2013;59:1081–1093.
- Lebrec D, Giuily N, Hadengue A, Vilgrain V, Moreau R et Transjugular intrahepatic portosystemic shunts: comparison with paracentesis in patients with cirrhosis and refractory ascites: a randomized trial. French Group of Clinicians and a Group of Biologists. J. Hepatol. 1996;25:135-144.
- Rössle M, Ochs A, Gülberg V, Siegerstetter V, Holl J et al. A comparison of paracentesis and transjugular intrahepatic portosystemic shunting in patients with ascites. N. Engl. J. Med. 2000;342:1701-1707.
- Salerno F, Merli M, Riggio O, Cazzaniga M, Valeriano V et al. Randomized controlled study of TIPS versus paracentesis plus albumin in cirrhosis with severe ascites. Hepatol. Baltim. Md. 2004;40:629-635.
- Huonker M, Schumacher YO, Ochs A, Sorichter S, Keul J et al. Cardiac function and haemodynamics in alcoholic cirrhosis and effects of the transjugular intrahepatic portosystemic stent shunt. Gut. 1999;44:743-748.
- Ginès P, Uriz J, Calahorra B, Garcia-Tsao G, Kamath PS et al. Transjugular intrahepatic portosystemic shunting versus paracentesis plus albumin for refractory ascites in cirrhosis. Gastroenterology. 2002;123:1839-1847.
- Sanyal AJ, Genning C, Reddy KR, Wong F, Kowdley KV et The North American Study for the Treatment of Refractory Ascites. Gastroenterology. 2003;124:634-641.
- Narahara Y, Kanazawa H, Fukuda T, Matsushita Y, Harimoto H et al. Transjugular intrahepatic portosystemic shunt versus paracentesis plus albumin in patients with refractory ascites who have good hepatic and renal function: a prospective randomized trial. J. Gastroenterol. 2011;46:78-85.
- Lepida A, Marot A, Trépo E, Degré D, Moreno C et Systematic review with meta-analysis: automated low-flow ascites pump therapy for refractory ascites. Aliment. Pharmacol. Ther. 2019;50:978-987.
- Bureau C, Adebayo D, Chalret de Rieu M, Elkrief L, Valla D et Alfapump® system vs. large volume paracentesis for refractory ascites: A multicenter randomized controlled study. J. Hepatol. 2017;67:940-949.
- Stepanova M, Nader F, Bureau C, Adebayo D, Elkrief L et al. Patients with refractory ascites treated with alfapump® system have better health-related quality of life as compared to those treated with large volume paracentesis: the results of a multicenter randomized controlled Qual. Life Res. Int. J. Qual. Life Asp. Treat. Care Rehabil. 2018;27:1513-1520.
- Silberhumer GR, Hetz H, Rasoul-Rockenschaub S, Peck-Radosavljevic M, Soliman T, Steininger R et al. Is MELD score sufficient to predict not only death on waiting list, but also post-transplant survival? Transpl. Int. 2006;19:275-281.