Objectifs pédagogiques
- Connaître les principales causes
- Savoir faire le diagnostic
- Connaître la stratégie étiologique en fonction du contexte
- Savoir proposer un traitement adapté
LIENS D’INTÉRÊTS
Amgen, Takeda, Sandoz, Pfizer, Janssen, Abbvie, Biogen, Arkopharma, UCB, Gilead, Tillots
MOTS-CLÉS
Carence martiale, anémie, ferritine
ABRÉVIATIONS
EPO (érythropoiétine), IPP (inhibiteur de la pompe à protons), MICI (maladie inflammatoire chronique de l’intestin), AINS (anti inflammatoire non stéroidien)
La carence martiale (CM) est la carence en nutriments la plus fréquente dans le monde (1) et la première cause d’anémie. La CM peut altérer la qualité de vie des patients même en l’absence d’anémie, entraîner entre autres, une diminution des performances physiques et cognitives, fatigue, céphalées, vertiges, dyspnée, syndrome des jambes sans repos, chute des cheveux, stomatite, glossite et baisse de la libido (2).
Le fer est un composant essentiel de l’hémoglobine dans les hématies et de la myoglobine dans les muscles. Le fer est indispensable aux fonctions cellulaires telles que les processus enzymatiques, la synthèse d’ADN et le métabolisme énergétique mitochondrial (3). La production et la matura- tion des précurseurs des érythrocytes dans la moelle osseuse mobilisent les deux tiers du fer de l’organisme. Chez l’homme, la majeure partie de ce fer provient du recyclage des globules rouges sénescents par les macrophages. Une partie du fer est également stockée dans les hépatocytes par la ferritine. Chez l’adulte, le fer se répartit de la façon suivante : 1 000 mg en réserve (ferritine), 2 500 mg sous forme de fer fonctionnel (hémoglobine) et 6 mg sous forme circulante (transferrine, coefficient de saturation). À l’état normal, les apports (1 à 4 mg/j) compensent les pertes (1 à 4 mg/j). En fonction des besoins, la régulation du fer se fait via son absorption intestinale et la gestion des réserves (foie/macrophages). L’hormone clé de la régulation est l’hepcidine, qui interagit avec le principal exportateur de fer cellulaire nommé ferroportine à la surface des entérocytes, des hépato- cytes et des macrophages. La synthèse hépatique d’hepcidine est contrôlée négativement en cas de CM (diminution de la ferritine) (Figure 1.a) et stimulée par les cytokines inflammatoires (IL 1, IL 6, TNFa) avec en conséquence, un défaut d’absorption intestinale du fer et une séquestration du fer dans les macrophages (augmentation de la ferritine) (Figure 1.b).

Figure 1.a : Carence martiale : baisse des réserves en fer (Ferritine) (A) puis diminution du fer de transport (coefficient de saturation, CS) (B) avec une biodisponibilité du fer insuffisante pour assurer une érythropoïèse normale et en conséquence une diminution de l’hémoglobine (C)
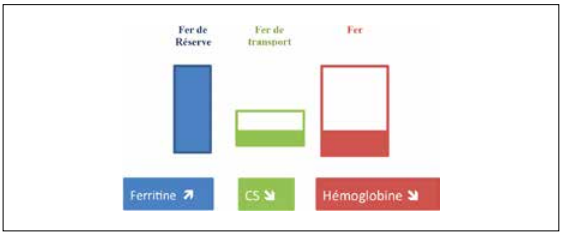
Figure 1.b : L’inflammation stimule la synthèse de l’hepcidine avec blocage de la ferroportine, blocage de l’absorption intestinale du fer et séquestration du fer dans les réserves aboutissant à une diminution de l’érythropoïèse
Une CM peut être favorisée par l’augmentation physiologique des besoins en fer chez l’enfant, l’adolescent, la femme jeune (menstruations) et pendant la grossesse. Les donneurs de sang réguliers sont aussi à risque de CM. Certains composants alimentaires affectent la biodisponibilité du fer. Le fer héminique (viandes et poissons) est mieux absorbé que le fer non héminique (végétaux et produits laitiers). Les phytates (céréales, végétaux) et polyphenols (thé, café, vin, et dans certains légumes, fruits et céréales) diminuent l’absorption du fer. Au contraire, l’acide ascorbique augmente son absorption. Plusieurs situations pathologiques peuvent entraîner une CM par pertes sanguines, le plus souvent digestives ou gynécologiques, ou par malabsorption intestinale (Tableau 1) (4).
| Augmentation des besoins | • Enfants, adolescents • Grossesse (2e et 3e trimestres) • Traitement par EPO |
| Diminution des apports | • Malnutrition • Végétariens, Vegans |
| Malabsorption | • Gastrectomie, bypass duodénal, chirurgie bariatrique • Maladie cœliaque • Gastrite auto-immune atrophique (Biermer) • Infection à Helicobacter Pylori • Traitement par IPP ou anti-H2 • Syndrome de Pica, pagophagie • Génétique : anémie ferriprive réfractaire au traitement martial (syndrome IRIDA) |
| Saignement chronique | • Saignement digestif : cancer colorectal, cancer gastrique, MICI, ulcères, angiodysplasies, parasitoses, traitement par aspirine ou AINS • Saignement gynécologique : ménorragies, métrorragies • Hématurie, épistaxis, hémoptysie • Dons de sang répétés |
| Causes multiples | • Maladies inflammatoires chroniques (MICI) • Insuffisance rénale chronique • Insuffisance cardiaque chronique • Cancers • Chirurgie |
Tableau 1 : Principales causes de carence martiale
Le dosage de la ferritine sérique permet d’estimer les réserves en fer de l’organisme et une ferritinémie < 30 ng/ml est le critère diagnostique de CM (2). En l’absence d’inflammation, la ferritinémie est le dosage le mieux corrélé avec le fer médullaire (coloration de Perls). La mesure du coeffi- cient de saturation n’est pas utile au diagnostic de CM. Le diagnostic de CM peut être difficile en cas d’inflammation qui augmente la ferritine. Des experts ont proposé d’augmenter les seuils diagnostiques de ferritine en cas d’inflammation. Toutefois, si l’élévation des seuils augmente la sensibi- lité diagnostique, c’est au prix d’une perte de spécificité avec probable surestimation diagnostique. Selon les recommandations de l’ECCO (5), une CM est « probable » en cas d’inflammation et de ferritinémie entre 30 et 100 mg/L. Ces mêmes seuils ont aussi été proposés chez les personnes âgées (2). Plusieurs paramètres biologiques ont été étudiés dans le but d’avoir un outil diagnostique de CM fiable et non modifié par l’inflammation. Le ratio calculé : récepteur soluble de la transferrine (sTfR) / log ferritine est un indicateur précis de CM vraie lorsqu’il est > 2 (6, 7). Pour des raisons de coût et de disponibilité, nous préconisons de ne l’utiliser qu’après un dosage initial de ferritine, en cas d’inflammation persistante avec ferritine normale (100 mg/L) (7).
L’interrogatoire oriente le bilan étiologique d’une CM (tableau 1). Il permet de connaître le contexte, les antécédents médicaux, les traitements en cours et les habitudes alimentaires. En raison de la fréquence des causes digestives et en l’absence d’autre cause évidente, une gastroscopie avec biopsies gastriques et duodénales, et une coloscopie sont demandées en première intention. Le bilan biologique est complété par la recherche d’un syndrome de malabsorption avec dosage des IgA anti-transglutaminase en s’assurant de l’absence de déficit en IgA. Une exploration de l’intestin grêle par vidéocapsule est indiquée en cas de bilan endoscopique conventionnel normal. Chez la femme, le bilan est complété par un examen gyné- cologique.
Le traitement étiologique doit être tenté dans tous les cas parallèlement à la supplémentation martiale. Les CM symptomatiques sans anémie doivent être traitées de la même façon qu’en présence d’anémie. L’objectif thérapeutique est de normaliser le taux d’hémoglobine et les réserves de fer (ferri- tine). En cas d’anémie sévère (hémoglobine < 7-8 g/dl) d’installation rapide, dans un contexte de saignement et/ou si mal tolérée, des transfusions sanguines sont indiquées. Le traitement martial peut être administré par voie orale ou par voie injectable. Le fer oral a l’avantage d’une adminis- tration facile et d’un faible coût. Toutefois, il est souvent mal toléré et mal absorbé surtout en cas d’inflammation. Son efficacité est lente puisqu’il faut plusieurs semaines pour augmenter l’hémoglobine, plusieurs mois pour la normaliser et environ 6 mois pour restaurer les réserves (8). Le fer intraveineux a l’avantage de sa rapidité d’action (9) et de sa bonne tolérance digestive. En France, il doit être administré par un personnel formé à surveiller et à prendre en charge une éventuelle réaction allergique dans un environnement disposant des moyens nécessaires pour assurer une réani- mation. Depuis la mise à disposition du fer injectable sous forme carboxymaltose, l’estimation des besoins en fer basée sur le poids et l’hémoglobine s’est simplifiée (2). L’administration d’une dose maximale de 1 000 mg par perfusion et par semaine est possible pour le fer carboxymaltose (10). La durée minimale de perfusion est de 15 minutes pour une dose de 1 000 mg suivie d’une surveillance de 30 minutes. L’administration intraveineuse de fer doit être privilégiée chez les patients ayant une inflammation chronique comme une MICI active, et chez les patients nécessitant un agent stimulant l’érythropoïèse.
Toute reproduction ou réécriture, totale ou partielle, sans l’accord préalable écrit de la FMC HGE est interdite.
FMC HGE : Organisme certifié Qualiopi pour la catégorie ACTIONS DE FORMATION.