LIEN D’INTÉRÊTS
Aucun
MOTS-CLÉS
Recommandations ; traitement ; hémorroïdes
ABRÉVIATIONS
SAI : sphinter anal interne, IST : infections sexuellement transmissibles, DGHAL : Ligature guidée par Doppler des artères hémorroïdaire, MICI : maladie inflammatoire chronique de l’intestin, AINS : anti inflammatoire non stéroidiens
Introduction
Jusqu’en 2019, les recommandations sur la prise en charge de la maladie hémorroïdaire avaient été publiées par la société américaine de chirurgie (1) et plusieurs sociétés scientifiques européennes, dont la SNFCP (2). Pour harmoniser nos pratiques au sein des états européens, la société européenne de colo-proctologie (ESCP) a mandaté un travail en ce sens. Le groupe de travail a réuni un méthodologiste, un médecin généraliste et des proctolo- gues chirurgicaux venant des Pays-Bas, Écosse, Danemark, Allemagne, Italie et France. L’objectif était de mener une réflexion commune à partir de données factuelles selon une méthodologie rigoureuse (GRADE) (3), et à défaut d’études ou de leur qualité médiocre, d’avis d’experts pour établir des recommandations européennes sur la prise en charge globale de la maladie hémorroïdaire. Des questions ont préalablement été retenues de manière consensuelle pour rechercher dans la littérature des réponses concernant le diagnostic de la maladie hémorroïdaire, son traitement (médical, instrumental et chirurgical) et certaines situations particulières. Les questions sur la thérapeutique étaient orientées sur les suites à attendre : rémis- sion des symptômes, satisfaction du patient, récidive, complications, qualité de vie, ré-intervention, retour à une activité normale, coût de l’interven- tion, sa durée et celle de l’hospitalisation. La recherche bibliographique a été réalisée sur MEDLINE, PubMeb, Embase et Cochrane Collaboration. Ce travail est destiné à tous les acteurs de la prise en charge de la maladie hémorroïdaire, les chirurgiens, gastro-entérologues, médecins généralistes, mais aussi les agents de santé et les patients.
Connaître les symptômes de la maladie hémorroïdaire
Rappels Physiologiques et physiopathologiques
Les hémorroïdes sont des formations vasculaires physiologiques de l’anus. On distingue les hémorroïdes externes situées en dessous de la ligne pectinée, sous la peau de la marge anale, provenant de l’artère rectale inférieure et les hémorroïdes internes situées dans la partie haute du canal anal, dépendantes essentiellement de l’artère rectale supérieure. Chaque plexus hémorroïdaire correspond à un lacis artério-veineux au sein d’un tissu conjonctif et de fibres musculaires lisses attachées au sphincter anal interne (SAI) par un épaississement de ces fibres. Elles participent pour 10 à 20 % de la pression de repos du canal anal. Lors d’efforts de poussée abdominale, en dehors de la défécation, elles participent à l’occlusion fine de l’anus et à la continence anale, empêchant la fuite de gaz et de selles liquides par l’afflux de sang en leur sein augmentant ainsi leur taille (4).
La pathogénie de la maladie hémorroïdaire n’est pas clairement définie. Elle fait intervenir des facteurs vasculaires (hyperplasie vasculaire respon- sable d’une distension des plexus) et mécaniques (destruction du tissu conjonctif et musculaire responsable d’une hyperlaxité du tissu conjonctif de soutien et d’un déséquilibre des flux vasculaires) qui vont expliquer les symptômes de la maladie hémorroïdaire. De ce fait, lorsque les hémorroïdes internes se prolabent en dessous de la ligne pectinée, elles ne jouent plus parfaitement leur rôle d’occlusion fine de l’anus et peuvent être respon- sables de saignements et de production de glaires expliquant le prurit fréquemment constaté (4).
Il est à noter que la dénomination « maladie hémorroïdaire externe » n’est reconnue que par les Français, celle-ci correspondant pour les autres experts européens à une symptomatologie en rapport avec des thromboses au sein de plexus veineux de la marge anale.
Éléments cliniques et classification
Les symptômes de la maladie hémorroïdaire interne sont les rectorragies, le prolapsus, la douleur et le prurit.
Les rectorragies sont typiquement faites de sang rouge éclaboussant la cuvette des toilettes immédiatement après le passage de la selle.
La douleur se traduit le plus souvent par une sensation de gonflement, de pesanteur intra canalaire non rythmée par la défécation, intermittente, avec à l’examen clinique un aspect normal de la marge anale et en anuscopie un aspect congestif des plexus hémorroïdaires internes. Ces « poussées fluxionnaires » peuvent notamment survenir en période pré menstruelle. Les douleurs intenses correspondent à des thromboses hémorroïdaires dues à la formation d’un ou plusieurs caillots de sang. Elles peuvent être non extériorisées avec une douleur permanente intra canalaire non rythmée par la défécation, perçues alors au toucher anal comme une petite masse arrondie douloureuse en « grain de plomb », apparaissant bleutées en anuscopie. Elles sont plus souvent extériorisées, localisées ou circulaires avec un prolapsus irréductible extrêmement douloureux. Il s’y associe un œdème réactionnel avec une coloration violacée, voire noirâtre. La douleur est alors très vive irradiant dans le périnée avec une sensation de prolapsus et un suintement séro-hémorragique fréquent. L’évolution peut se faire vers le sphacèle avec saignement spontané lors ou en dehors de la selle ou la régression avec formation de marisques séquellaires. Il n’y a aucun risque thromboembolique.
Le prurit s’accompagne parfois d’un suintement plus ou moins marqué, en rapport avec la production de glaires et une moindre occlusion anale. Le prolapsus hémorroïdaire est classé en tenant compte de l’interrogatoire et de l’examen clinique. La classification la plus communément retenue pour la maladie hémorroïdaire interne est celle de Goligher : le grade I correspond à une procidence des plexus hémorroïdaires au travers de l’anuscope, le grade II à une procidence lors d’un effort de défécation se réintégrant spontanément, le grade III lorsque cette procidence impose une réintégration manuelle et le grade IV à une procidence permanente non réductible.
Il est important de rechercher un trouble du transit associé, le plus souvent une constipation, plus rarement une diarrhée chronique. Les antécédents personnels de tumeur recto-colique, de maladie inflammatoire chronique de l’intestin, de chirurgie anale et les antécédents familiaux de cancer recto-coliques doivent être notés.
L’examen clinique doit être systématique pour poser le diagnostic et écarter les diagnostics différentiels. Il doit être préalablement expliqué au patient pour faciliter son acceptation. La position sera le plus souvent en genu pectoral ou en décubitus latéral gauche (position de Sims). Dans certaines circonstances, l’examen pourra être réalisé en position gynécologique ou de la taille. L’inspection de la marge anale est facilitée par le déplissement des plis radiés de l’anus. Le toucher anal débute toujours par une palpation de la marge anale préalablement lubrifiée (lubrifiant à base d’eau, pas de vaseline) suivi du toucher anal puis rectal.
Les symptômes de la maladie hémorroïdaire étant banals, il est primordial de toujours éliminer un diagnostic différentiel : le cancer recto-colique (5), les maladies inflammatoires de l’intestin, la fissure anale, le cancer de l’anus et les infections sexuellement transmissibles (IST).
Les recommandations étaient basées sur avis d’experts avec consensus du groupe de travail. Elles reprenaient les éléments développés précédemment.
Une maladie hémorroïdaire suspectée devant des symptômes évocateurs ne doit pas faire oublier de rechercher un autre diagnostic (MICI, cancer colo rectal).
L’examen clinique incluant inspection et examen physique de la région ano-rectale doit être réalisé pour éliminer une autre pathologie ano-rectale. L’examen par anuscopie ou rectoscopie doit visualiser le canal anal pour faire le diagnostic positif, apprécier l’importance du prolapsus et éliminer un autre diagnostic.
En cas d’éléments évocateurs dans les antécédents ou l’examen physique orientant vers un cancer colo rectal ou une MICI, les recommandations de chaque pays doivent être appliquées.
L’examen proctologique doit être réalisé dans une position adéquate pour faciliter le diagnostic. Si la plus confortable pour le patient est le décubitus latéral gauche, le genu pectorale reste une alternative souvent plus commode pour le proctologue.
En cas de diagnostic de maladie hémorroïdaire, le traitement médical de première intention doit être débuté (règles hygiéno-diététiques, laxatifs, topiques anesthésiants et phlébotoniques). En cas d’échec, ces patients doivent être référés à un proctologue. La classification de Goligher peut être utilisée pour guider la stratégie thérapeutique. |
Connaître le traitement médical, instrumental et chirurgical et leurs indications
Traitement médical
Le traitement de première intention de la maladie hémorroïdaire est toujours médical. Il a pour objectif de soulager des symptômes hémorroïdaires et prévenir leur récidive.
Les questions retenues par le groupe de travail étaient le rôle des règles d’hygiène, des laxatifs, des topiques et des phlébotoniques sur les symptômes de la maladie hémorroïdaire.
Il n’y a aucune donnée dans la littérature concernant les règles d’hygiène, les antalgiques, les AINS ou les dérivés de la cortisone. Les essais sur les laxatifs sont pour la plupart anciens et d’un faible niveau de preuve. Ils montrent qu’ils sont efficaces sur les rectorragies mais sans effet sur le prolapsus, sauf si associés à des ligatures élastiques (6). Seuls les topiques anesthésiants ont été évalués en post-opératoire dans des essais sans pouvoir démontrer un quelconque intérêt. Deux méta-analyses récentes se sont penchées sur l’intérêt des phlébotoniques. La première en 2006 montrait une efficacité significative sur les rectorragies et les douleurs ainsi qu’une diminution du risque de récidive symptomatique à court terme (7). La seconde en 2012 démontrait leur efficacité de façon significative sur le prurit, les saignements (y compris post hémorroïdectomie) et le « soiling » (8). Le niveau de preuves restait cependant faible du fait de biais, d’hétérogénéité statistique et d’imprécisions sur les doses et formula- tions utilisées.
Les recommandations sont donc basées sur des avis d’experts et des études de faible niveau de preuve.
Un apport suffisant en eau et fibres, et une activité physique régulière doivent être encouragés (avis d’experts avec consensus du groupe de travail). Une position facilitant l’évacuation des selles doit être conseillée et les efforts de défécation sont à éviter (avis d’experts avec consensus du groupe de travail).
Les laxatifs peuvent être proposés pour soulager les symptômes et diminuer les saignements (niveau de preuve faible). Les phlébotoniques peuvent contribuer à améliorer les symptômes (niveau de preuve faible).
Les AINS et les antalgiques non opioïdes peuvent être prescrits pour contrôler la douleur (avis d’expert). |
Traitement instrumental
En pratique courante, si la technique des injections sclérosantes est à présent quasi abandonnée, le proctologue français a recours à la photo- coagulation infrarouge et aux ligatures élastiques alors que dans les autres pays on retient essentiellement la ligature élastique.
Le traitement instrumental est réservé à l’échec du traitement médical d’une maladie hémorroïdaire de grades I, II et III non circulaire. En cas de grade III circulaire et grade IV, la chirurgie est à privilégier en l’absence de contre-indication ou refus du patient.
Les questions retenues par le groupe de travail étaient de déterminer l’efficacité et les complications des 3 techniques instrumentales comparées entre elles, et des ligatures élastiques comparées à la chirurgie : ligature guidée par doppler des artères hémorroïdaires (DGHAL), hémorroïdopexie agrafée circulaire et hémorroïdectomie pédiculaire.
Principes et complications
L’objectif des différentes techniques est de provoquer au sommet des plexus hémorroïdaires une destruction tissulaire ischémique avec comme conséquence une fibrose cicatricielle qui va détruire le réseau vasculaire hémorroïdaire sous muqueux et remonter le tissu hémorroïdaire prolabé en le fixant au plan profond. Ce dernier point est plus efficacement obtenu avec la ligature élastique. L’ensemble de ces techniques peuvent être répétées en plusieurs séances si nécessaire.
La ligature élastique
La ligature élastique nécessite un ligateur et un système d’aspiration. À travers un anuscope, un élastique est largué à la base d’un paquet hémorroïdaire aspiré. La ligature doit impérativement être réalisée à au moins un centimètre au-dessus de la ligne pectinée. Les tissus ligaturés se nécrosent rapidement et le sphacèle est éliminé en quelques jours, conduisant à la formation d’une escarre dont la cicatrisation se fait en 2 à 3 semaines.
Des effets indésirables mineurs sont très fréquents (douleurs et/ou rectorragies de faible abondance) (9). La survenue d’une douleur immédiate très intense peut être la conséquence d’une ligature posée trop près de la ligne pectinée imposant l’ablation de l’élastique. Des symptômes vagaux sont décrits jusqu’à 30 % des patients au décours de la procédure.
Des complications sont possibles (1 à 5 % des cas) : thrombose hémorroïdaire interne ou externe, dysurie ou plus rarement rétention aiguë d’urine, algies majeures, abcès péri anal. Une hémorragie sévère jusque 15 jours après la ligature est rare, nécessitant habituellement une hémostase chirurgi- cale. D’exceptionnelles complications infectieuses sévères ont été décrites, essentiellement des cellulites pelviennes (10).
La photocoagulation infrarouge
La photocoagulation infrarouge nécessite un photocoagulateur à rayons infrarouges qui transforme en chaleur le rayonnement émis par une ampoule de tungstène focalisé sur une tige en quartz au point d’application. Chaque point de photocoagulation dure environ 1 seconde et crée une brûlure circulaire de 6 mm de diamètre. La cicatrisation obtenue en 3 semaines induit une coagulation des capillaires et une fibrose cicatricielle.
Ses effets secondaires possibles sont rares et non graves à type de gêne transitoire, douleurs modérées, rectorragies minimes (9).
Les injections sclérosantes
Les injections sclérosantes utilisent du polidocanol ou du chlorhydrate double de quinine et d’urée qui est injecté en zone sus hémorroïdaire provoquant ainsi une nécrose tissulaire. Les injections peuvent être réalisées sur toute la circonférence (11). Plusieurs cas de complications infectieuses sévères ont été rapportés, à type d’abcès rétro péritonéal ou de cellulite périnéale à germes de la flore fécale (germes anaérobies et bacilles gram négatifs) (12). D’autres complications comme une épididymite, une cystite chronique, un abcès de prostate ou des vésicules séminales et des fistules vésico-périnéales ont été rapportées.
Évaluation des techniques instrumentales dans la littérature
L’analyse de la littérature montre que la cible des techniques instrumentales concerne essentiellement la maladie hémorroïdaire de grades I et II.
Une méta analyse ancienne (13) reprenant 18 essais randomisés et des études observationnelles de patients ayant une maladie hémorroïdaire de grade II-III concluait à la supériorité des ligatures élastiques sur les 2 autres techniques pour les grades I,II et III au prix de complications à type de douleurs plus fréquentes. La supériorité des ligatures élastiques était nette en cas de grade III localisé. Un essai randomisé récent montrait que la photocoagulation infrarouge avait une efficacité similaire aux ligatures élastiques en cas de grade I et II sur les symptômes, mais avec moins de saignements et douleurs (14). Gartel et al. concluaient enfin que la ligature élastique avait une efficacité supérieure aux injections sclérosantes en cas de grade II sur les symptômes au prix de plus d’effets indésirables mais moins de séances nécessaires (15).
La technique de ligature élastique a également été comparée à la chirurgie. Un important travail multicentrique a ainsi montré que la ligature arté- rielle guidée par doppler était plus efficace avec moins de récidives pour les prolapsus de grade II et surtout III (16). Plusieurs équipes dont celle de Shanmugam ont comparé les ligatures élastiques à l’hémorroïdopexie montrant que cette dernière était plus efficace avec moins de récidives pour les prolapsus de grade II mais au prix de douleurs plus fréquentes (17). La même équipe anglaise montrait dans une méta analyse comparant la ligature élastique à l’hémorroïdectomie pédiculaire une efficacité supérieure de la chirurgie pour les grades II-III et III au détriment de plus de complications post opératoires (18).
Les recommandations sont basées sur des études de niveaux de preuves faibles et moyens et des avis d’experts.
Le choix du traitement instrumental doit être décidé de façon conjointe avec le patient, informé loyalement des avantages et inconvénients des différentes techniques (avis d’experts avec consensus du groupe de travail).
La photocoagulation infrarouge peut être proposée en première intention en cas de rectorragies et de maladie hémorroïdaire de grade I (niveau de preuve faible). |
La ligature élastique est recommandée en cas de maladie hémorroïdaire de grades I, II et III. Les séances de ligatures peuvent être répétées si besoin (niveau de preuve moyen).
Les injections sclérosantes peuvent être proposées en cas de maladie hémorroïdaire de grades I et II (niveau de preuve faible).
Traitement chirurgical
Une chirurgie hémorroïdaire peut être proposée en cas d’échec du traitement médical et instrumental ou d’emblée en cas de maladie hémorroïdaire de grade III circulaire et IV. Les principales techniques étudiées sont la ligature des artères hémorroïdaires guidée par doppler (DGHAL) associée à une mucopexie, l’hémorroïdopexie agrafée circulaire (intervention de Longo) et l’hémorroïdectomie pédiculaire.
Les questions retenues par le groupe de travail étaient de déterminer l’intérêt de la DGHAL associée à une mucopexie comparé à la mucopexie seule, à l’hémorroïdopexie, à l’hémorroïdectomie pédiculaire et celui de l’hémorroïdopexie comparé à l’hémorroïdectomie pédiculaire.
Principes et complications
La ligature des artères hémorroidaires guidée par doppler (DGHAL) associée à une mucopexie est une technique qui a pris son essor au début des années 2000. La ligature artérielle a pour but de « désartérialiser » les hémorroïdes en diminuant de façon sélective le flux artériel des plexus hémorroïdaires grâce à un repérage doppler. Depuis quelques années, la technique s’est améliorée en associant au geste de ligature artérielle une mucopexie permettant de fixer le prolapsus hémorroïdaire au-dessus du canal anal. Au lieu d’exciser les hémorroïdes, le principe est donc de dimi- nuer leur taille (en ligaturant les artères les alimentant) et de restaurer les rapports anatomiques des plexus hémorroïdaires dans le canal anal avec la mucopexie.
La morbidité de la technique est faible, essentiellement des saignements et des douleurs. Plus rarement sont décrites des thromboses hémorroïdaires et fissures anales (19).
L’hémorroidopexie (ou anopexie) agrafée circulaire consiste à réséquer une collerette muqueuse circulaire au sommet des hémorroïdes internes, environ 4 centimètres au-dessus de la ligne pectinée, avec une pince mécanique introduite par voie trans-anale qui assure dans le même temps la résection et une suture muco-muqueuse par agrafage circulaire. Elle permet un repositionnement du canal anal avec suspension et dévascularisation partielle des plexus hémorroïdaires internes (grâce à une fixation cicatricielle à la musculeuse du bas rectum) tout en préservant l’anoderme cana- laire.
Les complications sont fréquentes, souvent mineures à type de douleurs, saignements, rétention urinaire et thromboses hémorroïdaires. Des compli- cations plus graves ont été décrites et doivent être connues des patients : hématome rétro rectal, cellulite pelvienne et perforation rectale avec périto- nite (20) voire même décès. Les autres complications (sténose, incontinence, douleurs recto-anales résiduelles parfois très invalidantes) n’étaient pas précisées dans ces recommandations.
L’hémorroïdectomie pédiculaire consiste à réséquer le tissu hémorroïdaire selon les 3 axes anatomiques artériels en préservant des ponts cuta- néo-muqueux entre les plaies opératoires.
De multiples variantes existent : hémorroïdectomie avec plaies fermées pour favoriser les suites post opératoires avec une cicatrisation plus rapide (intervention de Ferguson en 1959), avec plaies semi fermées en recouvrant partiellement les plaies par de l’anoderme (intervention de Parks en 1956) et avec plaies laissées ouvertes associées à une anoplastie postérieure pour diminuer le risque de rétrécissement (intervention de Bellan). Différents instruments sont classiquement utilisés pour la dissection : ciseaux, bistouri « froid », bistouri électrique. Il en existe d’autres comme les pinces de fusion tissulaire qui permettent de souder les vaisseaux (avant de les couper) en utilisant une énergie ultrasonique ou électrique : la thermofusion (Ligasure®) et le bistouri harmonique (Harmonic Scalpel®), ce dernier entraînant moins de lésions tissulaires du fait de son mode de fonctionnement (vibrations à haute fréquence).
Les complications de l’hémorroïdectomie sont fréquentes, souvent mineures à type de douleurs, saignements, rétention urinaire et thromboses hémorroïdaires. Les autres complications (sténose, incontinence, retard de cicatrisation) n’étaient pas précisées dans ces recommandations euro- péennes.
D’autres techniques sont en cours d’évaluation, comme le laser et la radiofréquence. Le laser, supposé diminuer les flux artériels hémorroïdaires, utilisé sous différentes modalités fait également partie de l’arsenal thérapeutique de la maladie hémorroïdaire essentiellement de grade II. Enfin, certaines équipes ont eu recours à des techniques de résections rectales dont le STARR® qui consiste en une double résection rectale trans-anale initialement développée pour corriger un trouble de la statique pelvi-rectale (rectocèle et intussusception recto-anale). La technique d’embolisation des branches de l’artère rectal supérieure (« emborrhoid ») n’a pas été évoquée dans ces recommandations européennes. La littérature est pauvre et sa place dans l’arsenal thérapeutique limitée : patients fragiles inopérables avec maladie de grade II sans prolapsus.
Évaluation des techniques chirurgicales dans la littérature
L’intérêt du repérage doppler a été mis en doute dans plusieurs essais contrôlés avec un taux de récidive équivalent, un essai rapportant même plus de complications en cas de guidage doppler (21-22). La DGHAL avec mucopexies est équivalente à l’hémorroïdopexie en terme de récidive et com- plications post opératoires (23-24) et équivalente à l’hémorroïdectomie en terme de récidive avec un retour plus rapide à une reprise d’activité (25). L’hémorroïdopexie a fait l’objet de nombreuses revues de la littérature (26-27) et méta-analyses d’essais contrôlés (28-29) la comparant à l’hémor- roïdectomie pédiculaire chez des patients opérés pour une maladie hémorroïdaire de grades II, III et IV. Il en ressort que l’hémorroïdopexie a des suites immédiates moins douloureuses avec retour plus rapide à une activité normale au prix de récidives des symptômes initiaux plus fréquentes ; de même, il est noté une récidive plus fréquente du prolapsus en cas d’hémorroïdopexie avec un risque à un an 2,6 fois supérieur qu’après hémorroïdectomie, principalement en cas de grade IV (29). La technique d’hémorroïdectomie ouverte a été comparée à celle fermée, plus usitée outre-Atlantique, dans une méta analyse récente reprenant 11 essais randomisés de patients ayant une maladie hémorroïdaire de grades II à IV. Il n’y avait pas de diffé- rence significative de récidive mais la technique fermée permettait moins de douleurs et saignements post opératoires ainsi qu’une cicatrisation plus rapide (30). Une autre méta-analyse incluant 8 essais de patients avec maladie hémorroïdaire de grades II à IV a comparé le bistouri harmonique à une hémorroïdectomie classique. L’utilisation de la fusion tissulaire aux ultrasons permettait d’avoir moins de douleurs post opératoires et une reprise plus rapide d’activité (31). La technique utilisant la thermofusion (Ligasure®) a été comparée à l’hémorroïdectomie fermée dans une méta-analyse incluant 5 essais randomisés. Elle concluait à un taux significativement moindre de saignements per opératoires, de douleurs et rétentions urinaires post opératoires (32). Une technique utilisant le laser pour obturer les artères hémorroïdaires guidée par doppler (HeLP) selon le même principe que la DGHAL a fait l’objet d’un essai randomisé la comparant à l’hémorroïdectomie selon Milligan Morgan chez des patients avec un grade II. Les saignements per opératoires, le temps d’intervention, et les douleurs post opératoires étaient significativement diminuées dans le groupe HeLP, les taux de patients asymptomatiques à un an étant comparables (33). L’équipe de Maloku et al. a comparé l’utilisation du laser sans guidage doppler à l’hémorroïdectomie pédiculaire chez des patients avec maladie hémorroïdaire de grades III et IV montrant également une durée d’intervention plus courte et des douleurs post opératoires significativement diminuées en cas d’utilisation du laser (34). Pour finir la procédure STARR® a été évaluée dans la maladie hémorroïdaire dans plusieurs essais transalpins. Son efficacité similaire à l’hemorroïdopexie au prix d’un temps d’intervention plus long et de risques de séquelles plus importants (douleurs ano-rectales et pelviennes, incontinence anale aux gaz, perforation rectales, fistules recto vaginales, rétro pneumo péritoine) (35-36).
Les recommandations se basent sur des avis d’experts et des études de niveaux de preuves faibles et moyens.
Le choix de la technique se fait de façon concertée avec le patient après information claire et loyale en tenant compte des attentes du patient, de la disponibilité des procédures et aptitudes aux procédures chirurgicales (avis d’experts avec consensus du groupe de travail).
La DGHAL associée à la mucopexie peut être proposée en cas de maladie hémorroïdaire de grades II et III et/ou en cas d’échec des traitements instrumentaux (niveau de preuve faible). L’intérêt du doppler étant cependant actuellement remis en cause, la mucopexie seule peut être envisagée (niveau de preuve très faible et avis d’experts avec consensus du groupe de travail).
L’hémorroïdopexie agrafée circulaire peut être proposée en cas de maladie hémorroïdaire de grades II et III et/ou en cas d’échec destraitements instrumentaux (niveau de preuve faible).
L’hémorroïdectomie peut être proposée en cas de maladie hémorroïdaire grades II et III et doit être proposée en cas d’échec du traitement instrumen- tal (niveau de preuve moyen) et de maladie hémorroïdaire grade IV (niveau de preuve moyen).
La technique ouverte comme fermée d’hémorroïdectomie peut être réalisée (niveau de preuve faible). L’hémorroïdectomie fermée permet cependant moins de douleurs et de saignements (niveau de preuve faible).
Les techniques utilisant le Harmonic Scalpel® et le Ligasure® peuvent être utilisées (niveau de preuve faible). Les techniques alternatives comme le laser et la radiofréquence peuvent proposées (niveau de preuve faible).
La résection rectale à l’aide d’une agrafeuse (dont STARR®) ne doit pas être utilisée dans la maladie hémorroïdaire (niveau de preuve faible). |
Situations cliniques particulières : grossesse, MICI, troubles de la coagulation
Grossesse
Les deux manifestations hémorroïdaires les plus fréquentes chez la parturiente sont la thrombose hémorroïdaire externe et la fissure anale. On estime l’incidence de la première à 8 % au dernier trimestre de grossesse et 20 % en post partum immédiat et de la deuxième à 9 % (37). L’objectif du traitement est de soulager cet épisode « aigu » qui le plus souvent est contrôlé médicalement. Peu d’essais ont concerné cette population montrant un intérêt des phlébotoniques en cure de courte durée pour l’amélioration des symptômes (38), des topiques associant dermocorticoïdes et anesthésiques locaux (39) et des bains de siège tièdes salés associés à une régulation du transit (40). L’hémorroïdectomie, évaluée dans un seul travail, n’était pas responsable de complications fœtales (41).
Les recommandations se basent sur des avis d’experts avec consensus du groupe de travail.
| Chez la parturiente et en post-partum il doit être proposé en première intention un traitement médical (associant laxatifs, topiques, phlébotoniques et antalgiques) ; en cas de thrombose hémorroïdaire ne répondant pas au traitement médical, une chirurgie peut être proposée. |
Maladies inflammatoires chroniques de l’intestin (MICI)
La maladie hémorroïdaire semble rare en cas de MICI (42) mais est certainement sous-estimée du fait de l’attention portée par les patients à leur maladie inflammatoire. Un travail ancien concluait à la contre-indication de tout geste chirurgical en cas de maladie de Crohn (43). Dans 2 publi- cations ultérieures, les complications post opératoires étaient fréquentes avec des taux de 41 % (hémorragie, fissure, abcès) (44) et 17 %, celles-ci nécessitant une proctectomie chez 10 % des patients opérés (45). Tous les auteurs s’accordaient sur l’extrême prudence à s’imposer avant d’envisager tout geste instrumental ou chirurgical en cas de MICI, notamment de maladie de Crohn, de colite indéterminée et de RCH en phase active.
Les recommandations se basent sur des avis d’experts avec consensus du groupe de travail.
| En cas de MICI, le traitement instrumental et/ou chirurgical peut être envisagé uniquement en l’absence de signe d’activité de la maladie inflamma- toire. |
Troubles de la coagulation
En cas de troubles de la coagulation, le traitement médical doit être proposé en première intention. Le risque hémorragique a été évalué en cas de ligatures élastiques réalisées chez des patients sous anti thrombotiques sans constater davantage de complications hémorragiques, en dehors du clopi- dogrel, responsable d’un sur-risque significatif de saignements (46). Un autre travail évaluant la DGHAL sous anti thrombotiques n’a pas montré plus de complications hémorragiques en post opératoire tout en permettant un meilleur contrôle de la maladie hémorroïdaire comparé aux patients sans anti thrombotique (47).
Les recommandations se basent sur un niveau de preuve très faible et des avis d’experts avec consensus du groupe de travail.
| En cas de nécessité de traitement instrumental et/ou chirurgical, une interruption du traitement anticoagulant doit être réalisée selon les recommanda- tions des sociétés savantes de chaque pays. |
Conclusion
Les recommandations européennes sur la prise en charge de la maladie hémorroïdaire tentent d’uniformiser les points de vue des experts européens. Elles se basent sur une méthodologie robuste avec une analyse de la littérature selon la classification GRADE et à défaut sur un consensus issu de l’expertise des membres du groupe de travail.
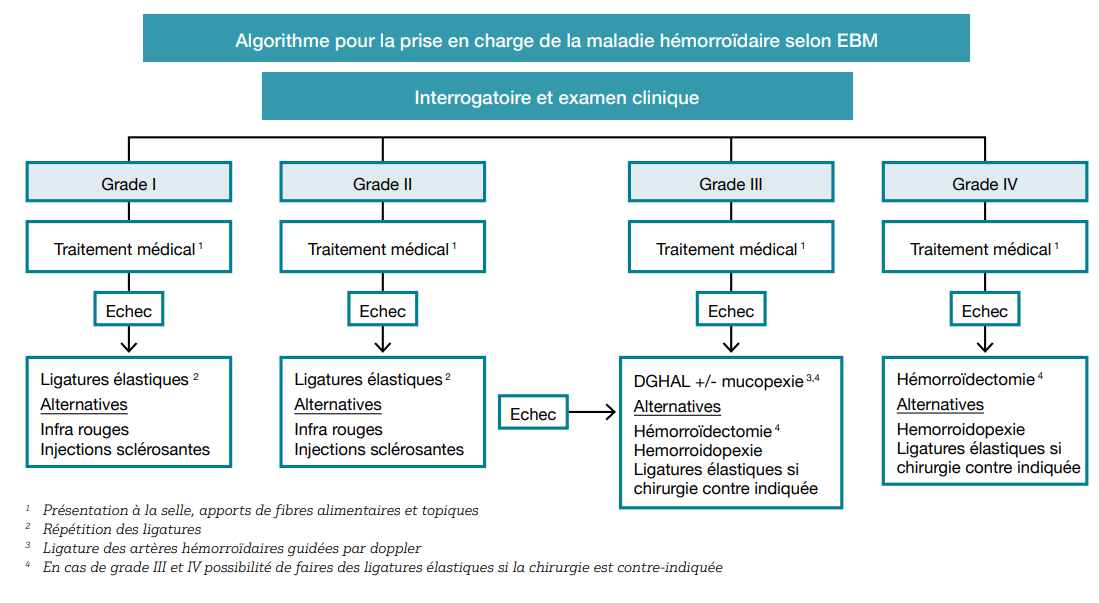
Il en ressort 34 recommandations et un algorithme de prise en charge. L’importance du traitement médical et instrumental, le caractère personnalisé de la technique (instrumentale ou opératoire) retenue basée sur le prolapsus et les attentes du patient sont clairement mis en avant.

Références
- Davis BR, Lee-Kong SA, Migaly J, Feingold DL, Steele SR. The American Society of Colon and Rectal Surgeons clinical practice guidelines for the management of hemorrhoids. Dis Colon Rectum 2018; 61: 284–92.
- Higuero T, Abramowitz L, Castinel A, et al. Guidelines for the treatment of hemorrhoids (short report). J Visc Surg 2016; 153: 213–8.
- van Tol RR, Kleijnen J, Watson AJM, Jongen J, Altomare DF, Qvist N, et al. European Society of ColoProctology (ESCP) Guideline for Haemor- rhoidal Colorectal Disease 2020. Jun ;22(6) :650-662.
- Nikolaos Pathophysiology of internal hemorrhoids. Ann Gastroenterol 2019; 32 (3): 264-72.
- Vogel JD, Eskicioglu C, Weiser MR, Feingold DL, Steele SR. The American Society of Colon and Rectal Surgeons Clinical Practice Guidelines for the Treatment of Colon Cancer. Dis Colon Rectum 2017. 60(10): p. 999-1017.
- Alonso-Coello P, Guyatt G, Heels-Ansdell D, Johanson JF, Lopez-Yarto M, Mills E, et al. Laxatives for the treatment of Cochrane Database Syst Rev 2005(4): p. CD004649
- Alonso-Coello P, Zhou Q, Martinez-Zapata MJ, Mills E, Heels-Ansdell D, Johanson JF, et Meta-analysis of flavonoids for the treatment of haemorrhoids. Br J Surg 2006. 93(8): p 909-20.
- Perera N, Liolitsa D, Iype S, Croxford A, Yassin M, Lang P, et al. Phlebotonics for haemorrhoids. Cochrane Database Syst Rev 2012; (8): p.
- Cocorullo G, Tutino R, Falco N, Licari L, Orlando G, Fontana T, et al. The non-surgical management for hemorrhoidal disease. A systematic G Chir 2017; 38(1): p 5-14.
- Sim HL, Tan KY, Poon PL, Cheng A, Mak K. Life-threatening perineal sepsis after rubber band ligation of haemorrhoids. Tech Coloproctol 2009; 13(2): p. 161-4.
- Yuksel BC, Armagan H, Berkem H, Yildiz Y, Ozel H, Hengirmen S. Conservative management of hemorrhoids: a comparison of venotonic flavonoid micronized purified flavonoid fraction (MPFF) and Surg Today 2008; 38(2): p 123-9.
- Kaman L, Aggarwal S, Kumar R, Behera A, Katariya RN. Necrotizing fascitis after injection sclerotherapy for hemorrhoids: report of a case. Dis Colon Rectum 1999; 42(3): p 419-20.
- MacRae HM, McLeod Comparison of hemorrhoidal treatments: a meta-analysis. Can J Surg 1997; 40(1): p 14-7.
- Marques CF, Nahas SC, Nahas CSR, Sobrado Jr CW, Habr-Gama A, Kiss Early results of the treatment of internal hemorrhoid disease by infrared coagulation and elastic banding: a prospective randomized cross-over trial. Tech Coloproctol 2006; 10(4): p 312-7.
- Gartell PC, Sheridan RJ, McGinn Out-patient treatment of haemorrhoids: a randomized clinical trial to compare rubber band ligation with phenol injection. Br J Surg 1985; 72(6): p 478-9.
- Brown SR, Tiernan JP, Watson AJM, Biggs K, Shephard N, Wailoo AJ, et al. Haemorrhoidal artery ligation versus rubber band ligation for the management of symptomatic second-degree and third-degree haemorrhoids (HubBLe): a multicentre, open-label, randomised controlled trial. Lancet 2016; 388(10042): p 356-64.
- Shanmugam V, Muthukumarasamy G, Cook JA, Vale L, Watson AJM, Loudon MA. Randomized controlled trial comparing rubber band ligation with stapled haemorrhoidopexy for Grade II circumferential haemorrhoids: long-term Colorectal Dis, 2010. 12(6): p. 579-86
- Shanmugam V, Thaha MA, Rabindranath KS, Campbell KL, Steele RJC, Loudon Systematic review of randomized trials comparing rubber band ligation with excisional haemorrhoidectomy. Br J Surg, 2005. 92(12): p. 1481-7
- Pucher PH, Sodergren MH, Lord AC, Darzi D, Ziprin P. Clinical outcome following Doppler-guided haemorrhoidal artery ligation: a systematic Colorectal Dis, 2013. 15(6): p. e284-94
- Faucheron JL, Voirin D, Abba J. Rectal perforation with life-threatening peritonitis following stapled haemorrhoidopexy. Br J Surg 2012; 99(6): p. 746-53.
- Gupta PJ, Kalaskar S, Taori T, Heda Doppler-guided hemorrhoidal artery ligation does not offer any advantage over suture ligation of grade 3 symptomatic hemorrhoids. Tech Coloproctol, 2011. 15(4): p. 439-44.
- Schuurman JP, BorelRinkes IH, Go Hemorrhoidal artery ligation procedure with or without Doppler transducer in grade II and III hemor- rhoidal disease: a blinded randomized clinical trial. Ann Surg 2012; 255(5): p. 840-5.
- Giordano P, Nastro P, Davies A, Gravante G. Prospective evaluation of stapled haemorrhoidopexy versus transanal haemorrhoidal dearteriali- sation for stage II and III haemorrhoids: three-year outcomes. Tech Coloproctol, 2011. 15(1): p. 67-73.
- Sajid MS, Parampalli U, Whitehouse P, Sains P, McFall MR, Baig A systematic review comparing transanal haemorrhoidal de-arteriali- sation to stapled haemorrhoidopexy in the management of haemorrhoidal disease. Tech Coloproctol, 2012. 16(1): p. 1-8.
- Bursics A, Morvay K, Kupcsulik P, Flautner L. Comparison of early and 1-year follow-up results of conventional hemorrhoidectomy and hemorrhoid artery ligation: a randomized Int J Colorectal Dis, 2004. 19(2): p. 176-80.
- Jayaraman S, Colquhoun PH, Malthaner Stapled versus conventional surgery for hemorrhoids. Cochrane Database Syst Rev 2006(4); p. CD005393
- Burch J, Epstein D, Sari AB, Weatherly H, Jayne D, Fox D, et Stapled haemorrhoidopexy for the treatment of haemorrhoids: a systematic review. Colorectal Dis, 2009. 11(3): p. 233-43.
- Yang J, Pei-Jing C, Hua-Zhong H, Da-Nian Meta-analysis of stapled hemorrhoidopexy vs LigaSure hemorrhoidectomy. World J Gastroen- terol, 2013. 19(29): p. 4799-807.
- Watson AJ, Hudson J, Wood J, Kilonzo M, Brown SR, McDonald A, et al. Comparison of stapled haemorrhoidopexy with traditional excisional surgery for haemorrhoidal disease (eTHoS): a pragmatic, multicentre, randomised controlled Lancet, 2016. 388(10058): p. 2375-2385.
- Bhatti MI, Sajid MS, Baig MK. Milligan-Morgan (Open) Versus Ferguson Haemorrhoidectomy (Closed): A Systematic Review and Meta-Analysis of Published Randomized, Controlled World J Surg 2016; 40(6): p. 1509-19.
- Mushaya CD, Caleo PJ, Bartlett L, Buettner PG, Ho Harmonic scalpel compared with conventional excisional haemorrhoidectomy: a meta-analysis of randomized controlled trials. Tech Coloproctol, 2014. 18(11): p. 1009-16.
- Xu L, Honglei C, Guoqiang L, Qiongxiang Ligasure versus Ferguson hemorrhoidectomy in the treatment of hemorrhoids: a meta-analysis of randomized control trials. Surg Laparosc Endosc Percutan Tech, 2015. 25(2): p. 106-10.
- Naderan M, Saeed Shoar S, Nazari M, Elsayed A, Mahmoodzadeh H, Khorgami A Randomized Controlled Trial Comparing Laser Intra-Hemorrhoidal Coagulation and Milligan-Morgan Hemorrhoidectomy. J Invest Surg, 2017. 30(5): p. 325-331.
- Maloku H, Gashi Z, Lazovic R, Islami H, Juniku-Shkololli A. Laser Hemorrhoidoplasty Procedure vs Open Surgical Hemorrhoidectomy: a Trial Comparing 2 Treatments for Hemorrhoids of Third and Fourth Acta Inform Med, 2014. 22(6): p. 365-7.
- Boccasanta P, Venturi M, Roviaro Stapled transanal rectal resection versus stapled anopexy in the cure of hemorrhoids associated with rectal prolapse. A randomized controlled trial. Int J Colorectal Dis 2007; 22(3): p. 245-51.
- Gagliardi G, Pescatori M, Altomare DF, Binda GA, Bottini C, Dodi G, et al. Results, outcome predictors, and complications after stapled transanal rectal resection for obstructed defecation. Dis Colon Rectum, 2008. 51(2): p. 186-95; discussion 195.
- Abramowitz Management of hemorrhoid disease in the pregnant woman. Gastroenterol Clin Biol 2008; 32(5 Pt 2): p. S210-4.
- Quijano CE, Abalos Conservative management of symptomatic and/or complicated haemorrhoids in pregnancy and the puerperium. Cochrane Database Syst Rev, 2005(3): p. CD004077.
- Vohra S, Akoury H, Bernstein P, Einarson TR, Pairaudeau N, Taddio A, et al. The effectiveness of Proctofoam-HC for treatment of hemorrhoids in late pregnancy. J ObstetGynaecol Can, 31(7): p. 654-9.
- Shirah BH, Shirah HA, Fallata AH, Alobidy SN, Al Hawsawi Hemorrhoids during pregnancy: Sitz bath vs. ano-rectal cream: A comparactive prospective study of two conservative treatment protocols. Women Birth, 2018 Aug;31(4):e272-e277
- Saleeby RG Jr, Rosen L, Stasik JJ, Riether RD, Sheets J, Khubchandani Hemorrhoidectomy during pregnancy: risk or relief? Dis Colon Rectum 1991; 34(3): p 260-1.
- Lewis RT, Maron DJ. Anorectal Crohn’s disease. Surg Clin North Am 2010; 90(1): p. 83-97.
- Jeffery PJ, Parks AG, Ritchie JK. Treatment of haemorrhoids in patients with inflammatory bowel disease. Lancet 1977; 1(8021): p. 1084-5.
- D’Ugo S, Franceschilli L, Cadeddu F, Leccesi L, Del Vecchio Blanco G, Calabrese E, et al. Medical and surgical treatment of haemorrhoids and anal fissure in Crohn’s disease: a critical appraisal. BMC Gastroenterol, 2013. 13: p. 47.
- Cracco N, Zinicola Is haemorrhoidectomy in inflammatory bowel disease harmful? An old dogma re-examined. Colorectal Dis 2014; 16(7): p. 516-9.
- Nelson RS, Thorson Risk of bleeding following hemorrhoidal banding in patients on antithrombotic therapy. Gastroenterol Clin Biol 2009; 33(6-7): p. 463-5.
- Atallah S, Maharaja GK, Martin-Perez B, Burke JP, Albert MR, Larach SW. Transanal hemorrhoidal dearterialization (THD): a safe procedure for the anticoagulated patient? Tech Coloproctol, 2016. 20(7): p. 461-6.