Objectifs pédagogiques
- Connaître les antibiothérapies en cas d’iléo-colites infectieuses en fonction de leur cause
- Connaître les antibiothérapies en cas de diverticulite
- Connaître les antibiothérapies en cas d’appendicite
LIEN D’INTÉRÊTS
Aucun
MOTS-CLÉS
Iléocolites infectieuses, appendicite, diverticulite
ABRÉVIATIONS
AZM : azitromycine ; AMOX/ Ac. CLAV : amoxicilline/ acide clavulanique ; C3G : céphalosporine de 3e génération ; CIP : ciprofloxacine ; FQ : fluoroquinolones ; GENTA : gentamicine MZD : métronidazole
Comme pour tout traitement anti-infectieux, une antibiothérapie probabiliste à visée digestive doit :
L’épidémiologie des iléo-colites infectieuses bactériennes d’origine alimentaire susceptibles de bénéficier d’un traitement antibiotique est dominée par 5 espèces (citées par ordre de prévalence) : Campylobacter spp, Salmonella enterica non typhi, Yersinia spp, E.coli producteur de SHIGA-toxine et Shigella spp (1). Le suivi des profils de résistance aux antibiotiques de ces différentes espèces est réalisé en France par leurs centres nationaux de référence respectifs.
Le tableau 1 résume leur prévalence ainsi que leur profil de sensibilité selon les derniers rapports disponibles de ces différents centres et leurs résistances naturelles connues (1,2,3,4). L’avènement de Campylobacter spp comme première cause de colite infectieuse (liée notamment à l’ingestion de poulet contaminé), associée à l’émergence d’une résistance aux fluoroquinolones de près de 60 % des souches, justifie de proscrire l’utilisation de cette famille d’antibiotiques en première intention.
Se : Sensibilité ; FQ : fluoroquinolones ; AZM : azitromycine ; MZD : métronidazole ; C3G : céphalosporine de 3e génération ; AMOX/ Ac. CLAV : amoxicilline/acide clavulanique ; CIP : ciprofloxacine. Source : (1,2,3,4).
| Bactéries | % TIAC symptomatique | Se FQ | Se AZM | Se MZD | Se C3G | Proposition de traitement probabiliste |
|---|---|---|---|---|---|---|
| Campylobacter spp | 26,1 | 41 % | 98,8 % | Résistance Naturelle | Résistance naturelle | AZM 500mg/jour – 3 jours / Signe de gravité ou bactériémie : AMOX/Ac. CLAV (<1 % de résistance) |
| Salmonella enterica non typhi | 12,2 | 75 %C | 99,4 % | Résistance Naturelle | 98,6 % | AZM 500 mg/jour – 3 jours |
| Yersinia spp | 1,4 | 99,9 % | Résistance Naturelle | Résistance Naturelle | 100 % | Ofloxacine 200 mg/12h – 7 jours Alternative Doxycycline 100 mg/12 h – 7 jours |
| E. coli productrice de Shiga-Toxine | 1,2 | 81,1- 100 % | 100 % | Résistance Naturelle | 99 % | Indication discutée- Possibilité de traiter par AZM 500 mg/ jour – 3 jours |
| Shigella | 0,2 | 77 % | 76 % | Résistance Naturelle | 94 % | Selon Antibiogramme ++ Ceftriaxone 2 g/j- 5 jours – Alternative possible AZM 500 mg/jour – 3 jours/ CIP 500 mg/12 h 3-5 j |
En cas d’iléite isolée, Yersinia spp est le germe le plus fréquemment en cause (environ 40 % des iléites aiguës infectieuses) a fortiori dans un contexte d’ingestion de viande de porc insuffisamment cuite (5). Le profil de sensibilité spécifique de Yersinia spp avec une résistance naturelle aux macrolides justifie l’utilisation des fluoroquinolones dans le traitement probabiliste de cette forme clinique (iléite sans atteinte colique avérée). À noter que Campylobacter spp est la deuxième cause d’iléite aiguë infectieuse (25 % environ) (5). En cas d’évolution défavorable et/ou d’identification de Campylobacter spp, un changement de traitement antibiotique pour couvrir une souche résistante aux fluoroquinolones devra être envisagée (traitement par azithromycine ou l’association amoxicilline/acide clavulanique en cas d’éléments de sévérité).
À noter que seulement 50 % des prélèvements infectieux réalisés dans un contexte d’iléo-colite aiguë permettront l’identification d’un agent pathogène. Ce chiffre pourrait toutefois évoluer avec la diffusion des techniques diagnostiques moléculaires par PCR dans les selles (y compris à partir d’écouvillon rectal). Par ailleurs, les coprocultures standards nécessitent au moins 5 jours d’incubation. Ainsi, dans un grand nombre de cas, l’évolution pourra être cliniquement favorable avec un traitement antibiotique probabiliste sans que l’on n’obtienne de diagnostic précis. La réalisation de sérologies Yersinia spp, Campylobacter spp et Anisakis simplex (nématode parasite associé à l’ingestion de poisson cru non congelé) entre 4 et 8 semaines après l’épisode clinique peut permettre un diagnostic rétrospectif.
En cas de prise récente d’antibiotiques (<1 mois), a fortiori en contexte nosocomial, la première cause de colite aiguë infectieuse est une infection à C. difficile toxinogène (6). Son diagnostic repose sur l’identification d’une souche de C. difficile productrice de toxine par méthode immuno- enzymatique ou PCR. L’identification seule de la présence de C. difficile sans toxine ne permet pas d’affirmer le diagnostic. En effet, près de 3 % de la population générale sont porteurs asymptomatiques de C. difficile non toxinogène. À noter que dans 30 % des cas de colite à C. difficile communautaire aucun facteur de risque ou de prise d’antibiotique n’est identifié (7). Il convient donc de rechercher ce germe systématiquement devant tout tableau de colite aiguë y compris en situation communautaire.
Une fois le diagnostic posé, le traitement repose sur une antibiothérapie par fidaxomicine ou vancomycine per os. Les dernières recommandations publiées en 2021 des sociétés savantes de maladies infectieuses américaine et européenne ont positionné la fidaxomicine en première intention du fait d’un risque diminué de récidive entre 10 et 15 % et d’une efficacité identique à la vancomycine, voire possiblement supérieure chez les patients avec un cancer (8,9). Malgré son coût élevé (1 300 € la cure complète), la fidaxomicine est donc à privilégier en première intention, surtout en cas de facteurs de risque de récidive (âge ≥ 65 ans, ICD nosocomiale, hospitalisation de moins de 3 mois, poursuite d’une antibiothérapie concomitante ou d’un traitement par inhibiteur de la pompe à proton).
La vancomycine per os à la dose de 125 mg 4 fois par jour pendant 10 jours est également une alternative en traitement de première intention. Ce traitement comme la fidaxomicine nécessite une prescription et une délivrance hospitalières. Toutefois la vancomycine présente pour principal inconvénient de nécessiter la reconstitution du produit par le patient à partir des flacons destinés au traitement intraveineux. Du fait des difficultés d’accès possible et du coût de la fidaxomine, on peut envisager en cas de suspicion diagnostique de débuter initialemment un traitement probabiliste par métronidazole 500 mg/8 h, actif également sur C. difficile bien que d’efficacité moindre et qui sera à modifier en cas d’infection confirmée (10) (figure 1).
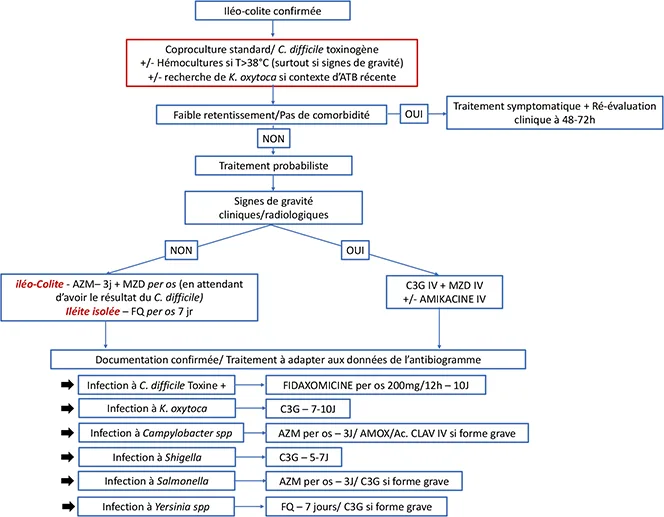
Figure 1 : Proposition d’algorithme décisionnel pour le choix d’une antibiothérapie dans un contexte d’iléite ou d’iléocolite aiguë présumée infectieuse
ATB : antibiothérapie ; AZM : AZITHROMYCINE ; MZD : METRONIDAZOLE ; C3G : Céphalosporines de 3e génération ; FQ : fluoroquinolones ;AMOX : AMOXICILLINE ; Ac. CLAV : Acide CLAVULANIQUE ; À partir de : www.ePOPI.fr
Klebsiella oxytoca, une bactérie commensale du côlon est le deuxième germe responsable de colite associée aux antibiotiques. En effet, certaines souches de K oxytoca productrices d’une toxine inhibant la synthèse de l’ADN sont à l’origine d’une colite classiquement décrite hémorragique et de localisation droite mais pouvant être également étendue (11). Elle est particulièrement à suspecter chez des patients exposés aux pénicillines ou à la pristinamycine. K. oxytoca serait à l’origine de 50 à 80 % des cas de colites hémorragiques C. difficile négatives après antibiotiques (12). À noter que la recherche de K. oxytoca sur les coprocultures standards n’est pas systématiquement réalisée par les laboratoires et que la demande doit donc être précisée spécifiquement au moment de l’envoi du prélèvement. Le traitement de K. oxytoca repose en première intention sur l’arrêt de l’antibiothérapie responsable permettant le plus souvent la résolution des symptômes. En cas de persistance ou de signe de gravité, le traitement doit être orienté suivant les résultats de l’antibiogramme et repose sur l’utilisation des céphalosporines de 3e génération en première intention. L’exposition aux antibiotiques peut également favoriser la colonisation et l’infection par les bactéries pathogènes classiquement associées aux Toxi-Infections Alimentaires Collectives (TIAC) et celles-ci doivent donc être systématiquement recherchées et prises en compte dans la stratégie thérapeutique initiale.
Les éléments anamnestiques suivants doivent être recherchés systématiquement pour orienter le choix d’une antibiothérapie initiale :
Lorsque disponible et pour les formes de colite avec atteinte distale, la réalisation d’une recto-sigmoïdoscopie précoce notamment en cas d’évolution de plus de 7 jours de la symptomatologie digestive permet de réaliser des biopsies coliques et iléales ainsi que des prélèvements infectieux (liquide d’aspiration avec lavage de la muqueuse avec quelques mL de sérum physiologique pour envoi en bactériologie pour coprocultures et recherche de C. difficile). L’examen anatomo-pathologique des biopsies permettra notamment d’orienter vers un diagnostic différentiel comme une MICI avec la recherche d’éléments en faveur d’une chronicité de l’inflammation digestive (distorsions architecturales des cryptes, infiltrat lympho-plasmocytaire, granulome épithélioïde sans nécrose caséeuse) ou la recherche d’éléments évocateurs d’une tuberculose intestinale (granulome avec une nécrose caséeuse classiquement dans 40 % des cas), plus rare en France. Le tableau 2 présente les principaux germes suspectés en fonction du tableau clinique initial et l’antibiothérapie probabiliste proposée.
| Contexte clinique | Principaux germes impliqués | Traitement recommandé (forme non grave) |
|---|---|---|
| Iléo-colite aiguë | – Campylobacter spp – Salmonella enterica non typhi – Shigella – E. coli productrice de SHIGA-toxine (contexte de SHU+++) – C. difficile – K. oxytoca (si ATB <1 mois) | – Azithromycine – Alternative Fluoroquinolones (ofloxacine/ ciprofloxacine) – Pas de traitement ou Azithromycine – Fidaxomicine ou Vancomycine per os – Arrêt ATB causale +/- C3G |
| Iléite aiguë | – Yersinia spp – Campylobacter spp – Salmonella – Anisakis simplex (ingestion poisson cru) | – Fluoroquinolones (alternative doxycyclines) – Azithromycine – Idem – Pas de traitement |
| Retour de voyage en pays tropicales | – Entamoeba histolytica – Bactéries multi-résistantes (Entérobactéries BLSE ou EPC) – Bactéries communautaires | – Métronidazole + Amoebicide de contact – Traitement en fonction de l’antibiogramme – Idem |
| Rectite aiguë | – Chlamydia trachomatis – Neisseria gonorrhoeae – Treponema pallidum – Herpes virus – Entamoeba histolytica | – Doxycycline – C3G monodose – Benzathine benzylpénicilline (Extencilline) IM – Valaciclovir – Métronidazole + Amoebicide de contact |
| Immunodépression | – Bactéries communautaires – CMV – Cryptosporidies/ microsporidies | – C3G IV (hors C. difficile ou Campylobacter spp) – Ganciclovir IV – Correction de l’immunodépression/ nitazoxanide en ATU |
En pratique, au service d’accueil des Urgences ou en consultation, il est licite en cas de forme fortement symptomatique de débuter un traitement antibiotique probabiliste immédiatement après réalisation des prélèvements microbiologiques associés à une réévaluation clinique rapide.
Ainsi au vu de l’épidémiologie actuelle, un traitement probabiliste par azithromycine (modalités de prescription décrites dans le tableau 3) pour couvrir les principaux pathogènes d’origine alimentaire associé à un traitement par métronidazole per os pour couvrir une possible infection à C. difficile permet de cibler les causes majoritaires d’iléo-colite infectieuse non grave. En cas de négativité de la recherche de C. difficile toxinogène (résultats normalement disponibles en moins de 24 h), le traitement par métronidazole pourra être interrompu. De même, en cas de recherche de C. difficile toxinogène positive, le traitement par azithromycine devra être interrompu et le métronidazole relayé par de la fidaxomicine per os (la vancomycine per os est également une alternative avec les limites listées ci-dessus).
| Antibiotiques/classe | Voie d’administration | Posologie usuelle | Précautions d’emploi et principaux effets indésirables | Adaptation à la fonction rénale |
|---|---|---|---|---|
| AZITHROMYCINE | Per os | 500 mg/jour – 3 jours | – Risque d’allongement du QT – Interactions médicamenteuses (antivitamines K, statines, digoxine, amiodarone, ciclosporine, tacrolimus…) – Contre-indication en association avec la colchicine/ Dérivés de l’ergot de seigle – Contre-indication en cas d’insuffisance hépatiquesévère | NON |
Fluoroquinolones :
| Per os ou IV | 200 mg/12 h | – Photosensibilisation – Risque de tendinopathie – Confusion en particulier chez le sujet âgé – En cas de grossesse préférer la ciprofloxacine possible quel que soit le terme | OUI |
Céphalosporines de 3ème génération :
| IV ou IM IV | 1 g/24 h | Réaction immuno-allergique (cutanée/ hépatique/ hématologique) | NON OUI |
| AMOXICILLINE/ ACIDE CLAVULANIQUE | Per os ou IV | 1 g/8 h | – Réaction immuno-allergique (cutanée/ hépatique/ hématologique) – Diarrhées motrices sous traitement | OUI (<30 ml/min) |
| DOXYCYCLINE | Per os – (prendre assis ou debout avec un grand verre d’eau) | 100 mg/12 h | – Ulcérations œsophagiennes – Photosensibilisation – Contre-indication < 8ans | NON |
| METRONIDAZOLE | Per os ou IV | – Neuropathie dose-dépendante – Effet antabuse vis-à-vis de l’alcool – Dysgueusie | NON | |
| VANCOMYCINE | Per os | 125 mg/6 h | NON (pas/peu d’absorption systémique en prise per os) | |
| FIDAXOMICINE | Per os | 200 mg/12 h | NON (pas/peu d’absorption systémique) |
L’utilisation de l’azithromycine doit toutefois être considérée avec prudence chez les patients avec un risque d’allongement du QT (co-prescription de traitement allongeant le QT, syndrome de QT long connu, insuffisance cardiaque sévère, bradycardie sévère, trouble ionique avec retentissement sur l’intervalle QT -hypokaliémie, hypomagnésémie). En effet, un sur-risque de torsade de pointe a été identifié chez les patients à haut risque cardiovasculaire au sein d’un registre américain (13). Ce sur-risque n’a toutefois pas été identifié chez les sujets de moins de 65 ans au sein d’une cohorte nationale danoise (14). De même, l’azithromycine interagit avec de nombreux autres médicaments, et il conviendra de vérifier l’absence d’association dangereuse au moment de la prescription (contre-indication absolue en association avec la colchicine, dérivés de l’ergot de seigle, augmentation de l’exposition aux antivitamines K, digoxine, ciclosporine,…). En cas de contre-indication aux macrolides, un traitement par fluoroquinolones (ofloxacine, ciprofloxacine, levofloxacine) en association avec le métronidazole est une alternative possible, même s’il expose à un risque plus élevé d’échec en cas d’infection à Campylobacter spp.
En l’absence de réponse clinique après un traitement initial de l’iléo-colite, une endoscopie digestive diagnostique devra être réalisée pour l’obtention de biopsies à la recherche d’éléments en faveur d’un diagnostic différentiel comme une MICI ou une cause ischémique.
En cas d’éléments de gravité clinique (sepsis avec un score qSOFA ≥ 2), ou radiologiques (péritonite, pneumatose pariétale, aéroportie, perforation), le bilan microbiologique initial sera étendu à la réalisation d’hémocultures et un traitement probabiliste à large spectre permettant de couvrir les pathogènes digestifs pourra être débuté par une céphalosporine de 3e génération qui couvrira les principales entérobactéries et streptocoques digestifs (ceftriaxone 1 g/24 h IV ou cefotaxime 1 g/8 h) associée au métronidazole (500 mg/8 h per os ou IV) qui ciblera les bactéries anaérobies. L’objectif principal de ce traitement antibiotique probabiliste sera le traitement d’une éventuelle translocation bactérienne tout en cherchant à contrôler l’infection intestinale, ce qui justifie le spectre large d’emblée recherché par cette stratégie thérapeutique. En cas d’infection à Campylobacter spp documentée, espèce naturellement résistante aux céphalosporines de 3e génération, le traitement à privilégier dans un second temps sera l’association amoxicilline/acide clavulanique (< 1 % de résistance décrite).
La figure 1 fait la synthèse des différents traitements recommandés et présente une proposition d’algorithme décisionnel dans le choix de l’antibiothérapie probabiliste en contexte d’iléo-colite infectieuse aiguë en fonction du contexte clinique.
En pratique, les tableaux cliniques d’iléo-colites chroniques purement infectieuses sont rares. L’étiologie principale est la tuberculose intestinale dont le traitement repose autant que possible sur l’identification et l’antibiogramme de Mycobacterium tuberculosis (plus rarement Mycobacterium bovis) au niveau de la muqueuse, d’un liquide d’ascite ou d’un prélèvement respiratoire et l’utilisation d’une quadrithérapie antituberculeuse standard de 6 mois dans la plupart des cas pour M. tuberculosis (M. bovis étant naturellement résistant au pyrazinamide, une trithérapie de 9 mois est le plus souvent utilisée). Dans certains contextes d’immunodépressions on peut toutefois rencontrer des tableaux d’iléo-colites chroniques liées aux germes classiquement impliqués dans les iléo-colites aiguës (yersiniose chronique chez les patients avec une hémochromatose, colites récidivantes à Campylobacter spp chez les patients très immunodéprimés en particulier avec hypo-gammaglobulinémie, colites virales chez les transplantés…) mais dont la prise en charge ne peut se concevoir qu’en lien avec une équipe d’infectiologie au cas par cas.
La prise en charge chirurgicale reste le traitement de première intention de l’appendicite aiguë en France en 2021. Malgré 7 essais contrôlés randomisés évaluant la possibilité d’un traitement uniquement médical des formes non compliquées, cette approche n’a pas fait la preuve de sa pertinence clinique sur le long terme (15). En effet, dans ces différents essais, le traitement uniquement médical était associé à un taux de récidive de l’appendicite de près de 30 % dans l’année suivante ainsi qu’un plus grand nombre de complications en particulier en cas de stercolithe appendiculaire (16,17). Aucun protocole d’antibiothérapie spécifique n’a pu démontrer une supériorité par rapport aux autres.
Le choix de l’antibiothérapie, son indication et sa durée dépendent des constatations per opératoires (18) :
En cas de forme compliquée la durée de traitement est de 1 à 5 jours.
Une diverticulite non compliquée (stade Hinchey ≤ Ia= inflammation diverticulaire ou phlegmon péricolique) est définie par l’absence d’abcès péricolique ou pelvien ou de péritonite. Plusieurs essais contrôlés randomisés ont montré que l’absence de traitement antibiotique chez ces patients n’était pas associée à un sur-risque de complication ou de récidive dans l’année. L’abstention thérapeutique en dehors d’un traitement symptomatique est aujourd’hui la règle [recommandations Grade A, HAS 2017 ; (19)]. Toutefois en cas de non réponse au traitement symptomatique seul, une antibiothérapie par voie orale est alors recommandée associant amoxicilline + acide clavulanique 1 g/8 h, ou en cas d’allergie, une fluoroquinolone (levofloxacine 500 mg/24 h ou ciprofloxacine 500 mg/12 h) associée au métronidazole 500 mg/8 h. Ce traitement antibiotique ne doit pas dépasser 7 jours (19).
Les éléments suivants doivent faire débuter un traitement antibiotique par voie intra-veineuse sans délai :
Il est alors recommandé de débuter un traitement antibiotique par voie intra-veineuse par amoxicilline-acide clavulanique 1 g/8 h + gentamicine 3 à 6 mg/kg, OU cefotaxime 1 g/8 h + métronidazole 500 mg/8 h, OU ceftriaxone 1 g/24 h + métronidazole 500 mg/8 h. En cas d’allergie prouvée, une association levofloxacine 500 mg/24 h + gentamicine 3 à 6 mg/kg + métronidazole 500mg/8h est possible. La durée du traitement n’est pas codifiée, mais une durée de 10 jours est habituellement décrite. Un drainage radiologique est recommandé en cas d’abcès diverticulaire ≥ 3 cm lorsque celui-ci est possible. L’indication à une chirurgie en urgence est à réserver aux patients en échec de la prise en charge médicale +/- radiologique initiale ou en cas de signe péritonite clinique ou d’instabilité hémodynamique (19). La stratégie thérapeutique pour le choix et les modalités de l’antibiothérapie est résumée figure 2.
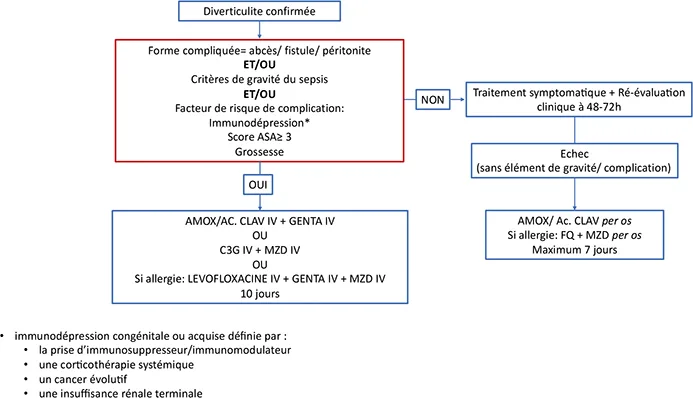
Figure 2 : Algorithme décisionnel pour l’indication et le choix de l’antibiothérapie dans la diverticulite aiguë
AMOX/ Ac/ CLAV : amoxicilline/ acide clavulanique ; C3G : Céphalosporines de 3e génération ; GENTA : gentamicine ; MZD : métronidazole ; FQ : fluoroquinolones ; Source : (19).
Le tableau 3 résume les posologies et mode d’administration des principaux antibiotiques utilisées dans les infections digestives.
Toute reproduction ou réécriture, totale ou partielle, sans l’accord préalable écrit de la FMC HGE est interdite.
FMC HGE : Organisme certifié Qualiopi pour la catégorie ACTIONS DE FORMATION.