LIEN D’INTÉRÊTS
Aucun en lien avec cet article
MOTS-CLÉS
Échographie ; non invasif ; fiable ; réponse transmurale
Introduction
L’échographie digestive s’impose de plus en plus comme un outil accessible et efficace de diagnostic et de suivi des MICI. Cette évolution est liée à une amélioration spectaculaire de la qualité des images et de l’ergonomie des appareils, facilitant l’apprentissage et l’utilisation mais également liée à l’accumulation récente de données de la littérature. Parallèlement, le coût des appareils a diminué d’un facteur 3 en 20 ans autorisant aujourd’hui l’acquisition d’un appareil de qualité aux alentours de 30 000 €. Les publications scientifiques validant l’échographie par rapport aux examens actuels (l’endoscopie, l’I.R.M. ou la calprotectine) sont en nombre croissant. L’échographie a des qualités intrinsèques : disponibilité immédiate, innocuité, faible coût, acceptabilité par le patient, lui permettant de s’intégrer parfaitement dans le concept du « suivi serré ».
Conditions techniques de la réalisation de l’examen
Le premier point fort de l’échographie est qu’aucune préparation n’est recommandée et que sa disponibilité immédiate avec un praticien formé permet un examen en temps réel (« point of care »). Un jeune de 6 h n’est nécessaire que si le praticien désire effectuer une échographie abdominale complète, qui n’est pas systématique. À noter que le jeun diminue les mouvements péristaltiques qui sont une aide au diagnostic des lésions intestinales. Il est possible d’ajouter la prise de 250 à 500 cc de PEG 30 minutes avant l’examen pour améliorer la visualisation du grêle proximal, mais cela diminue l’acceptabilité de l’examen et reste pour l’instant limité à quelques centres experts. Il faut compter 20 à 30 minutes pour un examen initial diagnostic avec cartographie complète du tube digestif, l’examen de surveillance peut-être plus rapide, entre 10 et 15 minutes. L’obésité est une limite classique de cet examen en diminuant l’échogénicité.
La première étape est la formation du praticien qui repose aujourd’hui sur le diplôme universitaire d’échographie abdominale. Cette formation non obligatoire, d’une durée d’un an, ne comprend qu’une faible partie théorique et pratique d’échographie digestive. La création d’une formation en France dédiée à l’échographie digestive serait souhaitable [QS Formation européenne IBUS (1)]. Une étude française est en cours pour évaluer le nombre d’examens permettant de former un gastro-entérologue ; les premiers résultats sont en faveur d’une formation relativement rapide (30 à 40 examens tutorés) pour obtenir une efficacité diagnostique acceptable et une bonne fiabilité dans la surveillance des lésions identifiées.
La 2e étape est l’acquisition d’un appareil. L’échographie digestive nécessite des images de haute définition avec une résolution de l’ordre du millimètre, disponible uniquement à partir d’appareils récents de moyenne gamme. L’équipement devra comprendre une sonde convexe basse fréquence de 3 à 6-8 MHz pour l’exploration profonde et une sonde plane haute fréquence de 6 à 12 MHz pour l’étude de la paroi intestinale. Il n’existe aucune sonde haute fréquence dédiée au digestif, elles ont été conçues pour le vasculaire ou le musculosquelettique, plus superficiel que le tube digestif (situé entre 3 et 6 cm). Le meilleur conseil est de se rapprocher de praticiens déjà formés, et de tester systématiquement le matériel proposé par le constructeur en insistant sur l’optimisation des préréglages de la machine lors de l’installation et par la suite.
Connaître la sémiologie échographique de l’atteinte intestinale
Le second point fort de l’échographie est une sémiologie échographique relativement simple. Le plus compliqué est d’identifier une zone normale puisque la paroi du côlon ou de l’iléon normal est de l’ordre du millimètre, noyée par les gaz digestifs.
La sémiologie de l’atteinte intestinale comprend 4 paramètres :
- l’épaisseur de la paroi,
- la différenciation de la paroi,
- la présence d’un effet Doppler,
- l’aspect de l’espace péri digestif (inflammation, sclérose, adénopathies).
Il s’y ajoute une sémiologie des complications : sténose, fistule, abcès.
Les zones constamment identifiées comprennent le sigmoïde, le côlon gauche, le côlon transverse (au moins dans ces 2 extrémités), le côlon droit, et l’iléon. Le rectum est plus difficile, à visualiser par voie transpariétale, mais il se développe aujourd’hui une échographie trans-anale permettant une meilleure visualisation (application de la sonde sur la zone anale). Le grêle proximal reste d’accès limité en raison de superposition gazeuse, mais l’expérience permet une exploration partielle à l’aide de manœuvres de compression et de mobilité du patient.
L’épaisseur de la paroi est le critère le plus important : le consensus est de considérer comme anormale une paroi digestive supérieure à 3 mm pour le côlon et le grêle (4 mm pour le rectum). Cette mesure doit être faite à la fois en coupe longitudinale et transversale, et répétée en deux points des segments étudiés. Cette donnée simple a la meilleure sensibilité, spécificité, et reproductibilité que ce soit dans la maladie de Crohn comme dans la rectocolite hémorragique. (Sensibilité 89,7 %, spécificité 95,6 %, corrélation inter-observateurs (95 % CI) : ICC = 0,96 (0,94-0,98), p < 0,001) (2,6,30).
Les autres paramètres sont aujourd’hui plus subjectifs et plus difficile à standardiser.
La différenciation de la paroi repose sur l’examen en haute fréquence permettant de distinguer les différentes couches muqueuses, sous muqueuse, musculeuse et séreuse. La muqueuse est hypo-échogène, la sous muqueuse hyperéchogène, la musculeuse hypo-échogène et la séreuse est un fin liseré hyperéchogène en périphérie (Cf. figures 1 et 2).

Figure 1

Figure 2
On repère la couche la plus anormale et l’aspect différencié ou dédifférencié des différentes couches (plutôt maladie Crohn).
Le Doppler nécessite des sondes de grande qualité et un réglage fin de l’acquisition (réglage du gain et de la PRF au minimum sans parasite). Il s’évalue par l’indice de Limberg de 0 à 3 suivant l’intensité perçu (QS image 2), une activité Doppler > 1 était corrélée avec la présence d’ulcérations en coloscopie avec une sensibilité de 67 %, une spécificité de 92 % et une forte valeur prédictive positive à 97 % (3). Des outils quantitatifs sont en cours d’étude chez les constructeurs avec le développement d’un doppler dit tissulaire.
L’examen de l’espace péri digestif comprend l’examen de la graisse qui est d’autant plus hyperéchogène qu’elle est inflammatoire et la recherche d’adénopathie inflammatoire de formes ovalaires hypo-échogènes. En cas de doute avec un vaisseau, le doppler est utile (QS figure 3).

Figure 3
La sémiologie des complications comprend la visualisation de fistule hypoéchogène, contrastant avec le caractère hyperéchogène de la graisse inflammatoire environnante. Elle part de la paroi digestive, et fuse dans la graisse péri-digestive. L’abcès est une zone mal limitée au contenu hypoéchogène voir hétérogène au sein d’une graisse hyperéchogène inflammatoire, relié le plus souvent par une fistule à la paroi de l’anse (QS figure 4).

Figure 4 : Comparaison du même malade en scanner et échographie basse fréquence
La sténose est un épaississement localisé avec diminution ou disparition de la lumière (< 1 cm), distension d’amont gazeux ou liquidien (> 2 cm) et parfois augmentation du péristaltisme (QS figure 5).

Figure 5
Les résultats de la littérature, sur des effectifs peu nombreux, montrent pour les sténoses, fistules et abcès, une sensibilité d’environ 80 % et une spécificité de l’ordre de 90 %. La limite est essentiellement la localisation des lésions ; les lésions profondes notamment pelviennes, sont parfois difficiles d’accès en échographie. Les méta-analyses ne montrent pas de différence de sensibilité entre l’échographie, le scanner et l’IRM (4).
Les techniques complémentaires comprennent l’échographie de contraste, le doppler tissulaire et l’élastométrie. Ces techniques sont toujours en cours de validation et ne sont pas recommandées pour l’instant. L’échographie de contraste la mieux connue, permet d’augmenter la sensibilité de dépistage de l’inflammation, et des abcès, mais l’utilisation IV du produit est limitée en France par la nécessité de prescription par un anesthésiste réanimateur ou un radiologue, comme en échoendoscopie. Dans la maladie de Crohn, l’adjonction d’injection de produit de contraste améliore la sensibilité de la détection de la présence d’ulcérations pour des valeurs du doppler basse, Limberg 0 et 1 (2).
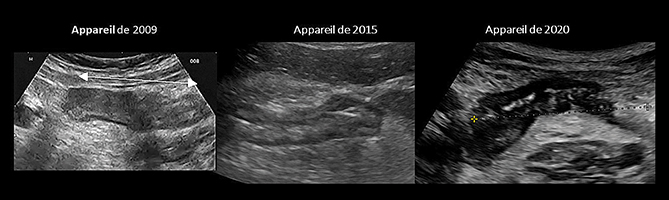
Il faut souligner que l’amélioration spectaculaire des images sur les appareils récents aide beaucoup à l’apprentissage, la détection et la caractérisation de ces lésions. (figure 6)

Figure 6 : Colon pathologique: Colon pathologique
Connaître les indications et les limites de l’échographie dans la surveillance
L’utilisation de l’échographie pour la surveillance des maladies inflammatoires est recommandée pour l’évaluation de la maladie iléale, la recherche de complications (abcès, fistules, sténoses) et la récidive post opératoire de la MC iléocolique. Elle est suggérée pour le suivi de patients asymptomatiques (ECCO 2018) (5). Elle répond pourtant aux nécessités du «suivi serré» comme seul examen morphologique non invasif, complémentaire du couple CRPCalprotectine, d’efficacité proche de celle des examens invasifs. Les seules limites de l’échographie sont les lésions non accessibles, habituellement le grêle proximal, les lésions pelviennes profondes, et le rectum (par voie transpariétale mais accessible en trans- anal). Les données récentes et le développement de scores échographiques devraient valider définitivement son utilisation dans les recommandations à venir (QS figure 7) (6).

Figure 7 : ECCO 2018
Il est admis que le l’évolution des symptômes n’est pas corrélée avec l’activité de la maladie avec un risque de sous- ou de surtraitement au cours du suivi (7). Les autres marqueurs non invasifs d’activité, la C-reactive protein [CRP], insuffisamment sensible, et la calprotectine fécale souvent mal acceptée par les patients, ne donnent aucune indication sur l’étendue des lésions ou la présence de complications. L’échographie a donc toute sa place dans la surveillance des maladies inflammatoires. Elle est non invasive, disponible, peu coûteuse, et parfaitement acceptée par les patients. Elle répond aux objectifs de surveillance décrits dans le consensus STRIDE 2 visant à la cicatrisation des lésions. L’échographie est également le seul moyen de surveillance morphologique recommandé chez les femmes enceintes et les enfants.
Le dernier consensus ECCO (de 2018) recommande l’usage de l’échographie pour le diagnostic des maladies inflammatoires et suggère son utilisation pour le suivi (5). Plusieurs travaux récents ont depuis conforté son efficacité dans la surveillance sur des effectifs plus significatifs.
Trois caractéristiques sont essentielles pour que l’échographie soit un parfait outil de surveillance des MICI : le repérage efficace des lésions et des complications, la corrélation avec l’activité de la maladie, sa disponibilité et l’acceptabilité par le patient
Repérage des lésions
L’échographie est efficace dans plus de 90 % cas pour déterminer la localisation des lésions ; L’étude Metric (8) dans le Crohn et une méta
analyse (9) dans la RCH montre une excellente corrélation entre les données de l’échographie et celle de l’endoscopie ou de l’IRM, exception faite des lésions du grêle proximal ou l’IRM reste plus performante, et de la localisation rectale versus l’endoscopie. La surveillance de l’extension ou de la régression des lésions de l’ensemble du côlon et de l’iléon sera donc parfaitement efficace. À noter que les études récentes ne montrent pas d’écart inter-centre et une bonne corrélation inter-observateur avec l’item le plus sensible et le plus spécifique : « taille de la paroi » (2).
Corrélation échographie/activité de la maladie
La corrélation entre les données de l’échographie et l’activité de la MICI s’appuie aujourd’hui sur de nombreuses études. La variation de la taille de la paroi reste le critère le plus sensible de l’activité de la maladie.
Dans la RCH
L’étude de référence pour la rectocolite hémorragique vient de l’équipe de Milan qui sur un travail prospectif de 53 malades compare la coloscopie à l’échographie. La présence d’une paroi colique supérieure à 3 mm a une sensibilité et une spécificité pour le diagnostic d’activité endoscopique Mayo ≥ 2 de 89 et 87 % (10).
Plus récemment, une étude prospective sur 60 patients confirmait qu’une paroi inférieure à 2,1 mm permettait de prédire un sous score endoscopique Mayo 0 avec une sensibilité et une spécificité de 82 et 93 %. À 3,2 mm, on différenciait un sous score Mayo 0-1 versus 2-3 avec une sensibilité et une spécificité aux alentours de 90 % (11) (Figure 7).

Figure 7
Des scores cumulant l’épaisseur de la paroi et l’effet Doppler sont en cours de validation pour améliorer l’efficacité diagnostique (11-10).
Une limite de l’échographie par voie abdominale est l’étude du rectum qui n’est concluante que dans 15 à 50 % des cas. L’échographie trans-anale (application de la sonde sur la zone anale) récemment développée a montré une bonne corrélation entre la taille de la paroi rectale < 4 mm et la cicatrisation endoscopique et histologique (12).
L’échographie est la seule technique non invasive permettant de diagnostiquer l’extension de la maladie sur le plan colique. L’évaluation de l’extension de la rectocolite hors rectum en échographie est corrélé à l’endoscopie avec une sensibilité et une spécificité de 95 et 97 % (9). Il y a donc également une utilité dans la surveillance des rectites dont l’extension vers le côlon gauche survient dans 1/3 des cas dans les 5 ans (Registre ECCO- epicom).
Dans la maladie de Crohn
Plusieurs revues ont comparé la sensibilité des différentes techniques pour le diagnostic de l’activité de la maladie Crohn. L’échographie a montré une sensibilité spécificité comparable à celle du scanner ou de l’IRM couplé à l’endoscopie (85 % : 91 %) (13,14,15).
L’étude prospective la plus importante pour le diagnostic de l’activité de la maladie de Crohn (MC) a été conduit sur 249 patients. Les patients ont été explorés par iléo-coloscopie, échographie et entéro IRM, en aveugle. 120 avaient une maladie de Crohn du grêle active, l’échographie avait une sensibilité et une spécificité pour ce diagnostic de 94 et 97 %. Aucune différence significative avec l’IRM n’a été retrouvée (11).
L’autre étude est une étude multicentrique menée en Angleterre avec des radiologues hospitaliers non experts sur 248 malades. Elle compare les résultats de l’IRM à celle de l’échographie. On retrouve une différence significative pour l’IRM en faveur du diagnostic et de l’extension de l’atteinte du grêle, alors que l’échographie semble plus efficace pour le diagnostic de l’atteinte colique. La différence est faible et ces résultats plaident en tout cas pour l’efficacité de l’échographie dans la surveillance de l’activité de la maladie (12).
La récidive post opératoire de la maladie de Crohn est la circonstance ou la surveillance par échographie est la mieux établie. Une méta-analyse sur plus de 500 patients donne une sensibilité, spécificité, de 94 et 84 % pour une paroi du grêle ≥ 3 mm. Une paroi ≥ 5,5 est corrélée avec une récidive Rutgeerts ≥ 3 (Sensibilité, spécificité : 83,8 %, 97,7 %) (16). (figure 8)

Figure 8
Récemment un groupe d’expert internationaux ont proposé un nouveau score (International Bowel Ultrasound Segmental Activity, Score – IBUS- SAS) à partir de 4 éléments sémiologiques ayant une bonne corrélation inter-observateur qui pourra être utilisé au cours de la maladie de Crohn afin de suivre l’activité de la maladie (17).
À l’inverse le diagnostic de rémission endoscopique de maladie de Crohn en échographie (patients SES CD 0 en endoscopie) a été évalué avec une sensibilité et spécificité de 92 et 86 % supérieure à celle de la calprotectine (18).
Détection des complications
On retrouve également une bonne sensibilité de la détection des complications entre 80 et 90 %. L’injection de produit de contraste améliore la sensibilité mais elle n’est pas de pratique courante. Il est à noter que la sensibilité augmente avec le caractère récent de l’étude, ce qui traduit probablement l’effet de l’augmentation la qualité des images (4,19 [QS Figure 6]).
L’acceptabilité de l’échographie est un argument majeur pour son utilisation dans la surveillance des maladies inflammatoires. Si le prélèvement sanguin est bien accepté, la CRP est insuffisante comme outil de surveillance, et la calprotectine est nettement moins bien tolérée. Plus de la moitié des calprotectines prescrites ne sont jamais faites, et cet examen n’est toujours pas remboursé en France. L’étude de Clermont-Ferrand place l’échographie en tête des examens bien tolérés par les patients et la pratique montre qu’elle est un outil important d’éducation thérapeutique et d’adhésion au traitement (20). Elle améliore la compréhension de la maladie, l’observance du malade, et double l’optimisation thérapeutique au décours de la consultation par le praticien (21). (figure 9)

Figure 9
Conclusion
L’échographie a donc toute sa place dans la surveillance des maladies inflammatoires dans sa localisation colique ou grêle que ce soit pour l’extension, l’activité, où la survenue de complications au cours du suivi. Elle semble pouvoir même évaluer la rémission endoscopique ou transmurale, de la maladie Crohn. L’item principal « taille de la paroi », le plus facile à acquérir, est également le plus efficace et reproductible, ce qui rend l’utilisation de l’échographie accessible à tous. L’acceptabilité est un argument majeur, intégrée à la consultation avec un résultat et une possibilité d’optimisation immédiate. Les limites de l’échographie sont les lésions inaccessibles à l’examen. Cette situation, rare, concerne le grêle proximal et les lésions pelviennes profondes. La vraie limite est le manque de formation des gastroentérologues et la disponibilité des appareils pour cet examen qui a longtemps été réservé à l’usage exclusif des radiologues en France. Les Allemands ont réussi avoir plus de 42 centres d’échographie digestive par une formation de compagnonnage. L’accumulation des données scientifiques et la nécessité de suivi serré des patients avec un objectif de cicatrisation devrait motiver prochainement les centres universitaires français à s’approprier la technique et à former la jeune génération de gastro-entérologues.
Connaître les indications et les limites de l’échographie dans l’évaluation de la réponse au traitement
L’utilisation de l’échographie pour l’évaluation de la réponse au traitement est pour l’instant suggérée dans les recommandations. Elle est considérée comme efficace pour la recherche de la récidive postopératoire et la détermination d’une cicatrisation transmurale dans la maladie de Crohn. Elle est mentionnée comme une alternative à l’endoscopie dans l’évaluation de la réponse au traitement des rectocolites hémorragiques dépassant le rectum. La rapidité de la réponse échographique, sa corrélation avec la réponse à un an, et la valeur donnée à la cicatrisation transmurale devraient valider rapidement son utilisation dans l’évaluation de la réponse au traitement.
La littérature a comparé l’échographie aux outils actuels d’évaluation de la réponse au traitement à 3 niveaux : corrélation avec la clinique, les examens biologiques ou morphologiques de référence, et valeur prédictive du recours aux corticoïdes, hospitalisation ou chirurgie.
Dans la RCH
La première étude prospective multicentrique de suivi de la réponse thérapeutique dans la rectocolite hémorragique a été conduite en Allemagne incluant 224 patients (50 % colite gauche, 50 % pancolite). Le résultat principal est que la normalisation de la paroi en échographie était fortement corrélée à la réponse clinique à la 12e semaine. Le point particulier est que cette réponse était obtenue dès la 2e semaine en échographie, plus tôt que la normalisation de la calprotectine. Il n’y a pas eu d’évaluation endoscopique systématique mais un sous-groupe de 63 patients a eu une coloscopie au cours du suivi avec une excellente corrélation entre l’échographie et l’endoscopie. Il n’y a pas eu de différence inter-centre (22).
Sur un modèle de suivi à court terme, 32 patients hospitalisés pour colite aiguë grave sous corticothérapie IV ont été évalués en échographie à J0 et J10. On notait une variation significative de la paroi des différents segments dans le groupe répondeur à la corticothérapie (p < 0,001) versus aucune variation dans le groupe non répondeur (23).
L’équipe de Milan a publié en abstract à l’ECCO en 2021 leur résultat sur 87 RCH suivis un an. Elle montre que le score échographique élevé initial prédit le risque de recours à la corticothérapie, l’hospitalisation, voire la chirurgie à un an de façon comparable à l’endoscopie (24). (figure 10)

Figure 10
Il manque encore des données pour valider définitivement l’intérêt de l’échographie dans l’évaluation de la réponse aux traitements dans la RCH mais ces premiers résultats sont prometteurs.
La littérature est plus riche dans la maladie de Crohn
La première étude prospective multicentrique comprenait 47 centres en Allemagne avec 234 patients entre 2010 et 2014. L’objectif de l’étude était de corréler la réponse échographique à la CRP, marqueur non invasif de référence à l’époque, à 3, 6 et 12 mois. Les résultats montraient une bonne corrélation entre la CRP et l’amélioration de la paroi iléale ou sigmoïdienne, Il n’y a pas eu de corrélation endoscopique (25).
Une étude italienne plus récente regroupait 218 malades traités depuis au moins 2 ans par anti-TNF et suivi au moins un an en échographie tous les 3 mois. Les patients étaient classés en maladies actives, rémission endoscopique, et rémission transmurale en échographie. Le suivi à un an montre que la rémission transmurale échographique initiale diminuait de façon significative le risque de recours aux corticoïdes, à l’hospitalisation, au risque de changement de traitement ou à l’intervention chirurgicale par rapport aux deux autres groupes (26). (figure 11)

Figure 11/p>
Une étude avec échographie de contraste et ingestion de PEG sur 80 malades avant et 18 mois après l’introduction d’une biothérapie confirme ces données. L’obtention d’une rémission échographique complète à 18 mois entraînait une diminution très significative du recours à la corticothérapie et à la chirurgie sur un suivi d’au moins 12 mois (27). (figure 12)

Figure 12/p>
Depuis, l’échographie de contraste, plus contraignante, a été évaluée comme rarement discriminante. Elle n’est donc pas recommandée (28).
À plus long terme, des résultats préliminaires ont été présentés cette année sur 202 patients suivis à l’hôpital de Melbourne entre 2017 et 2020. La présence d’une rémission échographique entraînait une différence significative en termes d’absence de corticothérapie, de recours à l’hospitalisation, de modification thérapeutique, et de traitement chirurgical à 3 ans. Ces résultats sont actuellement en attente de publication (29).
Une large étude multicentrique américaine (Stardust) a évalué a réponse thérapeutique sous ustekinumab de la maladie de Crohn en échec d’une première ligne de biothérapie (30). Les patients avaient une évaluation par une échographie à la 4e, 8e et 16e semaines : 34 % étaient en réponse thérapeutique à 4 mois et 11 % en rémission. Le point important de ce travail est que la réponse échographique semble débuter tôt dès la 4e semaine. Il manque les données à 6 et 12 mois.
Le développement de scores devrait aider à définir la réponse échographique. L’équipe de Milan a présenté en abstract ses résultats de suivi à un an de 224 maladies de Crohn. La valeur prédictive la plus significative d’une évolution péjorative à un an (recours à la corticothérapie, hospitalisation voire chirurgie) était le score échographique initial élevé (BUSS > 3,54) (31).
Enfin, de nombreuse études IRM confirme l’intérêt de la rémission transmurale dans la maladie de Crohn, prédictive d’une meilleure évolution. Celle-ci semble pouvoir être évaluée également en échographie (29,33,34). Sur 40 patients sous Anti-TNF pendant 2 ans la corrélation entre l’échographie et l’IRM pour l’évaluation de la rémission transmurale était bonne (35). Une étude montre également une bonne concordance entre l’échographie et l’IRM pour l’évaluation de la destruction pariétale évaluée par l’index de Lemann (32).
En conclusion
Les données s’accumulent pour valider la valeur de l’échographie dans l’évaluation de la réponse thérapeutique, avec les premières données montrant la corrélation de la réponse échographique avec la diminution du recours aux corticoïdes, à l’hospitalisation, voire à la chirurgie. Dans la maladie de Crohn, l’échographie est le seul outil non invasif permettant d’évaluer la rémission endoscopique, voire transmurale, objectif thérapeutique optimal. Il manque encore des données prospectives, avec des scores échographiques reproductibles pour valider définitivement la réponse échographique versus la réponse IRM ou endoscopique, mais plusieurs études sont en cours. La rapidité de la réponse en échographie (dès 4 semaines) pourrait accélérer l’optimisation thérapeutique (36) en espérant des études prochaines d’impact sur l’efficacité thérapeutique à long terme. On peut penser que les prochaines recommandations ECCO seront plus favorables à cette technique, les principaux experts européens de l’échographie digestive participant désormais à leur rédaction.
Un exemple de proposition de surveillance proposé dans la maladie de Crohn. (figure 13)

Figure 13 : Proposition d’algorithme de surveillance /p>
Références
- International Bowel Ultrasound Group: https://ibus-group.org/
- Expert consensus on optimal acquisition and development of the International Bowel Ultrasound Segmental Activity Score (IBUS-SAS): a reliability and inter-rater variability study on intestinal ultrasonography in Crohn’s Disease Kerri L Novak : Journal of Crohn’s and Colitis, 2021, 609-16.
- The Role of Intravenous Contrast Agent in the Sonographic Assessment of Crohn’s Disease Activity: Is Contrast Agent Injection Necessary? Tomás Ripollés: Journal of Crohn’s and Colitis, Volume 13, Issue 5, May 2019, Pages 585-92.
- Systematic review: the use of ultrasonography, computed tomography and magnetic resonance imaging for the diagnosis, assessment of activity and abdominal complications of Crohn’s disease. Panes J, Aliment Pharmacol Ther. 2011;34(2):125-45.
- European Crohn’s and Colitis Organisation [ECCO] and the European Society of Gastrointestinal and Abdominal Radiology [ESGAR]. ECCO-ESGAR Guideline for Diagnostic Assessment in IBD. Part 1: Initial diagnosis, monitoring of known IBD, detection of complications. Maaser C, Sturm A, Vavricka SR, et J Crohns Colitis 2019;13:144–64. ECCO-ESGAR Guideline for Diagnostic Assessment in IBD Part 2: ECCO-ESGAR Guideline for Diagnostic Assessment in IBD Part 2: ECCO-ESGAR Guideline for Diagnostic general principles and technical aspects IBD scores and general principles and technical aspects. Journal of Crohn’s and Colitis, 2018, 273-90. Statement 5.3.2.1 à 5.
- Is Intestinal Ultrasound Ready to be Used as Standard Monitoring Tool in Daily practice and as Endpoint in Clinical Trials? Christian Journal of Crohn’s and Colitis, 2021, 1-2.
- Clinical disease activity, C-reactive protein normalisation and mucosal healing in Crohn’s disease in the SONIC trial.: Peyrin-Biroulet L, Reinisch W, Colombel JF et al. Gut 2014; 63: 88-95.
- Diagnostic accuracy of magnetic resonance enterography and small bowel ultrasound for the extent and activity of newly diagnosed and relapsed Crohn’s disease (METRIC): a multicentre trial. Taylor:. Lancet Gastroenterol Hepatol 2018; 3: 548-58.
- Systematic Review: Clinical Utility of Gastrointestinal Ultrasound in the Diagnosis, Assessment and Management of Patients With Ulcerative Rebecca L. Smith: Journal of Crohn’s and Colitis, 2020, 465-79.
- Accuracy of Humanitas Ultrasound Criteria in Assessing Disease Activity and Severity in Ulcerative Colitis: A Prospective Study. Mariangela Allocca :Journal of Crohn’s and Colitis, 2018, 1385-91.
- Intestinal Ultrasound to Assess Disease Activity in Ulcerative Colitis: Development of a novel UC-Ultrasound Index. Steven Bots, Journal of Crohn’s and Colitis, 2021, 1264-71.
- Transperineal ultrasound predicts endoscopic and histological healing in ulcerative colitis Shintaro Sagami APT Volume51, Issue12,June 2020,Pages 1373-83.
- Calabrese E, Maaser C, Zorzi F, et al. Bowel ultrasonography in the management of Crohn’s disease. a review with recommendations of an international panel of Inflamm Bowel Dis 2016;22:1168-83.
- Comparative Accuracy of Bowel Ultrasound Versus Magnetic Resonance Enterography in Combination With Colonoscopy in Assessing Crohn’s Disease and Guiding Clinical Decision-making . Mariangela Allocca. Journal of Crohn’s and Colitis, 2018, 1280-87.
- Puylaert CA, Tielbeek JA, Bipat S, Stoker J. Grading of Crohn’s diseaseactivity using CT, MRI, US and scintigraphy: a meta-analysis. Eur Radiol 2015;25:3295-313.
- Diagnostic Accuracy of Ultrasonography in the Detection of Postsurgical Recurrence in Crohn’s Disease: A Systematic Review with Meta-analysis. Antonio Rispo : Inflamm Bowel Dis Volume 24, Number 5, May.
- Expert Consensus on optimal Acquisition and Development of the International Bowel Ultrasound Segmental Activity Score [IBUS-SAS]: A Reliability and Inter-rater Variability Study on Intestinal Ultrasonography in Crohn’s Disease Kerri L Novak J Crohns Colitis . 2021 ;15(4):609-16.
- Gastrointestinal Ultrasound Can Predict Endoscopic Activity in Crohn’s Disease Fredrik Sævik 1 Ultraschall Med . 2020 Apr 24. -1149-9092.
- Ultrasound vs Endoscopy, Surgery, or Pathology for the Diagnosis of Small Bowel Crohn’s Disease and its Complications Natasha Bollegala Inflamm Bowel Dis Volume 25, Number 8, August 2019.
- Comparative Acceptability and Perceived Clinical Utility of Monitoring Tools: A Nationwide Survey of Patients with Inflammatory Bowel Anthony Buisson: Inflamm Bowel Dis 2017;23:1425-33.
- Effect of point-of-care gastrointestinal ultrasound on decision-making and management in inflammatory bowel disease , Antony B Aliment Pharmacol Ther . 2021 Sep;54(5):652-66.
- Intestinal ultrasound for monitoring therapeutic response in patients with ulcerative colitis: results from the TRUST&UC study Maaser C, et al. Gut 2020;69:1629-36.
- Arienti V, Campieri M, Boriani L, et al. Management of severe ulcerativecolitis with the help of high resolution ultrasonography. Am J Gastroenterol 1996;91:2163-9.
- Predictive value of Milan Ultrasound Criteria in Ulcerative Colitis: A prospective observational cohort study. Présentation orale ECCO 2021: Allocca, M.(1); Dell’Avalle, C.(2); Furfaro, F.(2); Craviotto, V.(2); Zilli, A.(2); D’Amico, F.(2); Peyrin-Biroulet, L.(3); Fiorino, G.(1); Danese, S.(1).
- Use of Intestinal Ultrasound to Monitor Crohn’s Disease Activity. Torsten Kucharzik and the TRUST study group. Clinical Gastroenterology and Hepatology 2017;15:535-42.
- One-year clinical outcomes with biologics in Crohn’s disease:transmural healing compared with mucosal or no healing. Fabiana Castiglione: Aliment Pharmacol Ther. 2019;1-14.
- Response Assessed by Ultrasonography as Target of Biological Treatment for Crohn’s Disease Zorzi et al. Clinical Gastroenterology and Hepatology 2020;18:2030-7.
- The Role of Intravenous Contrast Agent in the Sonographic Assessment of Crohn’s Disease Activity: Is Contrast Agent Injection Necessary? Tomás Ripollésa. Journal of Crohn’s and Colitis, 2019, 585-92.
- Sonographic healing is associated with sustained clinical remission in patients with Crohn disease. R Vaughan; Presentation IBUS 2021. Royal Melbourne Hospital.
- Intestinal ultrasound response and transmural healing after ustekinumab induction in Crohn’s disease, Week 16 interim analysis of the STARDUST trial substudy. Torsten Kucharzik Journal of Crohn’s and Colitis, Volume 14, Issue Supplement_1, January 2020, Pages S046-S048.
- Predictive Value of Bowel Ultrasound in Crohn’s Disease: A 12-Month Prospective Study , Mariangela Allocca. Clin Gastroenterol 2021 Apr 22;S1542-1565.
- Rispo A, Imperatore N, Testa A, et al. Bowel damage in Crohn’s disease: direct comparison of ultrasonography-based and magnetic resonance based lemann Inflamm Bowel Dis 2017;23:143-51.
- Noninvasive Diagnosis of Small Bowel Crohn’s Disease: Direct Comparison of Bowel Sonography and Magnetic Resonance Enterography Fabiana Castiglione : Inflamm Bowel Dis Volume 19, Number 5, April 2013.
- Comparative Accuracy of Bowel Ultrasound Versus Magnetic Resonance Enterography in Combination With Colonoscopy in Assessing Crohn’s Disease and Guiding Clinical Decision-making. Mariangela Allocca. Journal of Crohn’s and Colitis, 2018, 1280-7.
- One-year clinical outcomes with biologics in Crohn’s disease: transmural healing compared with mucosal or no healing.Castiglione F Aliment Pharmacol Ther. 2019;1-14.
- Clinic-based Point of Care Transabdominal Ultrasound for Monitoring Crohn’s Disease: Impact on Clinical Decision Making. Kerri Novak,a Journal of Crohn’s and Colitis, Volume 9, Issue 9, September 2015, Pages 795-801.