Lien d’intérêts
Pas de lien d’intérêt à déclarer.
Mots-clés
Carcinome hépatocellulaire, Radiofréquence, Chimioembolisation, Electroporation, Radioembolisation.
Abréviations
- CHC : carcinome hépatocellulaire
- RF : radiofréquence
- MO : micro-onde
- RLR : récidive loco régionale
- CE : chimioembolisation
- mCE : chimioembolisation aux microparticules chargées
- RE : radioembolisation
Introduction
Le carcinome hépatocellulaire (CHC) est un cancer fréquent touchant désormais plus de 10 000 nouveaux patients annuellement. Il survient le plus souvent sur un foie de cirrhose, rarement sur un foie non cirrhotique notamment en cas d’hépatite virale B ou de contexte dysmétabolique et exceptionnellement sur un foie sain.
La décision thérapeutique dépendra de plusieurs facteurs indispensables à déterminer en pré-thérapeutique qui sont :
- Des critères liés à la tumeur : taille, nombre des nodules, envahissement vasculaire portal et son extension (segmentaire, tronculaire…), présence de localisations métastatiques extra hépatiques. Une tumeur unique de moins de 5 cm ou 3 tumeurs de moins de 3 cm sont dites « dans les critères de Milan ».
- Des critères liés à l’hépatopathie : la fonction hépatique (TP, INR, albuminémie, bilirubinémie, ascite, encéphalopathie) avec détermination du score de Child Pugh, la présence d’une hypertension portale avec la recherche scanographique et endoscopique de voies de dérivations.
- Des critères généraux : l’état nutritionnel et général est important à déterminer. La tolérance des traitements anti tumoraux en cas de cirrhose est médiocre en cas d’altération de l’état général et on estime qu’un grade OMS <2 est nécessaire pour envisager une thérapie anti cancéreuse pour CHC
- Par conséquent, le patient aura en pré thérapeutique un bilan minimal comportant :
- TDM thoracique et hépatique avec temps artériel portal et tardif hépatique
- Si possible une IRM hépatique avec les mêmes temps d’injection et des séquences de diffusion
- Une endoscopie digestive haute
- Un bilan biologique complet comportant une numération formule sanguine, un ionogramme sanguin, un bilan hépatique et un taux d’alfafoetoprotéine
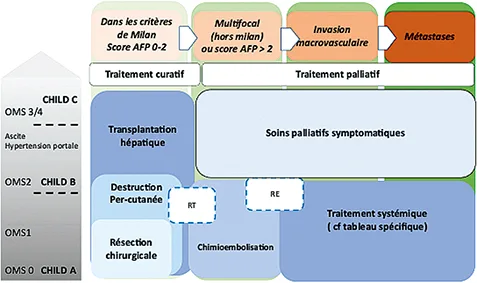
L’algorithme décisionnel thérapeutique le plus souvent utilisé est la classification espagnole BCLC (dite de Barcelone). Un algorithme simplifié a été proposé en 2021 sur le thésaurus national de cancérologie selon les critères tumoraux, hépatologiques et généraux précités (figure 1). L’accès à la transplantation hépatique dépend notamment en France du score alfafoetoprotéine (tableau 1).
Les traitements radiologiques ont une place importante dans l’arsenal thérapeutique et sont l’objet de cette présentation.
Carcinome hépato-cellulaire et traitement par thermoablation
La thermoablation est, avec la transplantation hépatique et la résection chirurgicale, l’un des traitements curatifs du carcinome hépato-cellulaire (CHC). Ses progrès, avec le développement de plusieurs modalités de thermablation, l’augmentation en taille des zones d’ablation, l’amélioration du repérage de la lésion à traiter au cours de la procédure, et une meilleure connaissance de ses indications et de ses limites, permettent à un plus grand nombre de patients de bénéficier de ce traitement curatif.
Plusieurs techniques d’ablation per-cutanée sont actuellement de pratique courante, qui sont toutes des techniques dites « thermiques » : la radiofréquence, méthode au sein de laquelle il faudra distinguer la radiofréquence (RF) monopolaire et multibipolaire, de réalisation un peu différente, avec des résultats parfois éloignés selon leur mise en pratique, et la technique de micro-onde. Le but recherché est d’exposer les cellules tumorales à une température supérieure à 70°C, qui provoque quasi immédiatement une dénaturation cellulaire irréversible par nécrose de coagulation, les cellules tumorales n’étant pas plus résistantes à la chaleur que les hépatocytes.
Ces techniques peuvent être réalisées seules avec un abord per-cutané ou en combinaison avec une résection hépatique par une approche laparoscopique ou lors d’une chirurgie ouverte.

Figure 1 : Stratégie thérapeutique dans le carcinome hépatocellulaire selon le Thésaurus National de Cancérologie Digestive, TNCD juin 2021
Tableau 1 : Score alfa fœtoprotéine selon Duvoux et Roudot-Thoraval 2012| Score Alpha-fœtoprotéine |
|---|
| Paramètre | Classe | Score |
|---|
| Taille | ≤ 3cm
3-6cm
> 6cm | 0
1
4 |
|---|
| Nombre de nodules | ≤ 3
> 4 | 0
2 |
|---|
| AFP (ng/ml) | ≤ 100 100-1 000 > 1 000 | 0
2
3 |
|---|
Principes et réalisation d’une thermoablation
Le premier temps du traitement est la mise en place la plus précise possible de la ou des électrodes, par guidage échographique, ou scanographique en fonction de la localisation de la lésion et de l’expertise de l’équipe réalisant le geste.
La destruction doit porter sur la tumeur en totalité mais aussi sur une marge d’ablation périphérique, voisine du centimètre, d’autant plus importante que la lésion est volumineuse et que le risque d’emboles tumoraux vasculaires et de nodules satellites est élevé.
De la précision de la ponction dépend l’efficacité du traitement. L’opérateur peut s’aider des progrès de l’échographie et des possibilités de réaliser une fusion de l’image échographique avec une imagerie en coupes, de l’utilisation en échographie de produit de contraste Sonovue pour repérer le nodule à traiter. Le repérage au scanner est souvent limité par le caractère fugace du réhaussement du CHC après injection, un tatouage lipiodolé préalable peut être nécessaire par la réalisation concomittante ou préalable d’une angiographie lipiodolée. Le scanner (ou maintenant les acquisitions cone beamCT) avec vérification en temps réel du positionnement des aiguilles apporte une sécurité à la technique dans les cas difficiles.
Sur le plan pratique, on distingue (1) :
- La technique de radiofréquence monopolaire mono-aiguille, permettant une ablation radiaire centrifuge, dont on peut augmenter le volume grâce à l’utilisation d’aiguilles à baleines, ou au positionnement de plusieurs aiguilles avec une superposition de zones de traitement indépendantes. La technique monopolaire est la plus répandue dans le monde, le plus gros volume de la littérature concerne cette modalité d’ablation. Afin d’augmenter la zone de traitement, plusieurs aiguilles peuvent être positionnées pour une thermoablation simultanée, mais avec la nécessité d’obtenir un chevauchement complet de ces différentes zones de destruction indépendantes.
- La technique de radiofréquence multibipolaire, multi-aiguilles, permettant une ablation centripète avec diffusion convergente d’une électrode à l’autre de l’énergie délivrée. La continuité de la zone de traitement entre les aiguilles est ainsi assurée. La mise en place de 3 aiguilles (jusqu’à 6 aiguilles), même si elle est plus complexe, permet de circonscrire la tumeur et d’obtenir une cicatrice sphérique de grande taille. La mise en place extra-tumorale des aiguilles assure une double sécurité : elle limite les risques de dissémination tumorale, particulièrement en cas de repositionnement des aiguilles, et d’autre part permet de déterminer l’épaisseur des marges d’ablation qui conditionnent la réussite du traitement en limitant le risque de récidive loco-régionale, et de s’adapter à la forme de la lésion.
Cette approche est particulièrement intéressante pour le traitement des nodules sous-capsulaires, pour lesquels une ponction directe est contre- indiquée en raison d’un possible ensemencement (2,3).
La mise en place de ces aiguilles selon cette technique est certes plus complexe, au prix d’une courbe d’apprentissage, mais le choix des marges de traitement et de la taille de la cicatrice, les possibilités de traiter des lésions jusqu’à 5 cm de diamètre sans repositionnement multiple des aiguilles, est un avantage, qui se traduit par une diminution des récidives loco-régionales (4).
– La technique de micro-onde (MO), qui, comme la RF monopolaire, est à l’origine d’une destruction centrifuge dont le point de départ est l’antenne droite mise en place au centre du nodule à traiter. L’utilisation d’une seule aiguille, plus simple qu’une technique multi-aiguilles, a permis à de nombreuses équipes de débuter une activité de thermoablation. L’augmentation de la zone d’ablation au-delà de 30 mm de diamètre, nécessite alors le repositionnement, pas toujours très simple, de l’antenne. Cependant, les progrès de certaines antennes de dernière génération permettent d’augmenter la taille d’ablation au-delà de 3 cm. La montée en température plus rapide et plus élevée qu’avec la radiofréquence, l’absence d’interruption du transfert d’énergie à partir de 100° (à l’origine d’une carbonisation avec la RF), permettent des temps de traitements courts.
Quelle que soit la technique utilisée, le but de l’opérateur est de minimiser au maximum le risque de récidive loco-régionale (RLR), en créant une zone d’ablation idéale. Cette récidive locale est un facteur indépendant de survie globale (5), il s’agit du seul facteur sur lequel on peut influer, et est directement lié à la technique d’ablation. Lorsque les marges de traitement sont inférieures à 4-5 mm (marges de traitement admises en cas de résection), le risque est pris de constater une repousse tumorale locale (6,7).
Le volume et la forme d’une zone d’ablation vont dépendre de la quantité d’énergie déposée, des caractéristiques du tissu cible et de la déperdition de chaleur engendrée par la perfusion cellulaire. Ainsi les gros vaisseaux sanguins vont agir comme un système de refroidissement tissulaire : il s’agit du « Heat Sink Effect » (8,9). Les tumeurs de grande taille nécessitent des ablations plus importantes, avec sur leurs berges une dispersion de la chaleur et un heat sink effect plus marqué si l’on choisit une technique de destruction de type centrifuge. Le mode monopolaire en raison de sa capacité moindre à coaguler les vaisseaux à distance de l’aiguille, là où la température décroît, induit la formation de zones de coagulation irrégulières (« zone transitionnelle ») qui s’ajoutent aux irrégularités des structures vasculaires et qui peuvent contenir en histologie après ablation des cellules vivaces même si cette zone est dévascularisée. Cette zone transitionnelle n’est pas retrouvée sur les berges d’une cicatrice de micro- onde, avec l’absence totale d’hépatocytes viables à la jonction entre le foie ablaté et non ablaté (8).
La technique de micro-onde est donc moins sensible que la radiofréquence monopolaire au heat sink effect (10,11), et dans certaines études entraine moins de RLR que la RF monopolaire, avec à 3 ans, 29 % de récidives loco-régionales avec les aiguilles monopolaires à baleine et 11 % avec le micro-onde (12). Cette différence de résultats n’est plus aussi évidente dès lors que l’on privilégie une technique de RF « multi-aiguilles » : pas de différence de RLR, de complications, de temps moyen à progression et de survie globale dans une série randomisée comparant MO et RF monopolaire multi-aiguille (14). RF monopolaire multi-aiguille et MO ont finalement des résultats assez voisins.
L’interêt d’une technique à aiguilles multiples est de mieux contrôler ses marges de traitement. Ainsi l’étude de Lee (128 patients traités par RF monopolaire multiaiguille pour des CHC de moins de 2,5 cm) montre que le positionnement extra-tumoral des aiguilles permet de limiter le taux de récidive locale de 1,6 % à 2 ans dans cette étude (15).
L’avantage de la technique de RF multibipolaire est de combiner l’intérêt d’un positionnement multiple des aiguilles et d’un travail à haute énergie permettant d’obtenir facilement des cicatrices de grande taille. Ainsi la comparaison chez 362 patients cirrhotiques de la RF monopolaire et RF multibipolaire (16) a montré un risque significativement inférieur de récidive loco-régionale pour cette dernière technique, inférieure à 10 % à 5 ans, comparativement à 36,7 % pour la RF monopolaire dans le traitement des CHC de 2 à 5 cm de diamètre. Même pour des lésions de petite taille, de moins de 20 mm, le risque de RLR restait supérieur pour la RF monopolaire.
Enfin dans cette étude la proximité de la lésion avec un gros vaisseau était un facteur indépendant de progression tumorale locale uniquement chez les patients traités par RF monopolaire.
En résumé, les techniques de micro-onde et la RF mono-polaire multi-aiguille ont des résultats assez voisins, les techniques multi-aiguilles permettent de choisir les marges de traitement et de limiter les risques de dissémination. Enfin la RF multibipolaire est une technique particulièrement intéressante pour son faible taux de récidive loco-régionale, lié à la taille des cicatrices obtenues, et d’un effet limité du heat sink effect.
Indications et résultats
La thermo-ablation est considérée comme le meilleur choix thérapeutique chez les patients présentant un CHC de stade précoce non accessible à un traitement chirurgical, c’est-à-dire une seule tumeur de moins de 5 cm ou trois nodules de moins de 3 cm chacun (critères dits de Milan), sans invasion vasculaire, ni propagation extra-hépatique (17). C’est une indication non discutée chez le patient non transplantable en raison de son âge, non opérable en raison de ses comorbidités, d’une hypertension portale (HTP) ou de fonctions hépatiques trop limites, mais restant Child A, voire jusqu’à B7.
Les études randomisées comparant chirurgie et thermoablation sont peu nombreuses (18,19,20,21), il n’y a pas de série prospective non asiatique avec suffisamment de puissance ou suffisamment homogène pour permettre cette comparaison (études discutables mélangeant patients cirrhotiques et non cirrhotiques, ou avec un suivi insuffisant…). Parmi ces études, celle ayant inclus le plus grand nombre de patients (18), pour des lésions dans les critères de Milan, comparant chirurgie et RF monopolaire mono-aiguille, montre une meilleure survie globale et moins de récidives loco-régionales dans le groupe de patients opérés.
Par contre, plusieurs études rétrospectives ont montré que la RF était aussi efficace que la chirurgie pour les CHC solitaires de moins de 2 à 3 cm. De plus, elle est associée à une moindre morbidité liée à l’intervention, avec un meilleur rapport coût-efficacité et une meilleure qualité de vie (22,23). Parmi les études plus favorables à la chirurgie, Kolarich et al (24) montrent que le bénéfice en termes de survie de la résection est corrélé à la taille de la tumeur, et à l’importance de la fibrose hépatique (moins le foie est cirrhotique, plus le patient bénéficie de l’avantage de la chirurgie par rapport à l’ablation) alors que Lee et al (25) dans leur analyse de cohorte montrent une meilleure survie globale dans le groupe de patients opérés, quelle que soit la taille de la tumeur et le degré de fibrose. Le type de thermoablation n’est pas détaillé dans cette étude.
Le mode opératoire intervient aussi dans ces comparaisons : ainsi une étude rétrospective comparant RF monopolaire multi-aiguille et résection chirurgicale non anatomique (simple tumorectomie) a montré que l’efficacité thérapeutique à long terme de ces 2 traitements était similaire comme traitement de première intention des petits CHC de moins de 3 cm (26).
Certaines localisations anatomiques de la tumeur sont moins favorables à une prise en charge chirurgicale : Pan et al. (27) ont montré une survie sans récidive identique pour les lésions entre 3 et 5 cm de topographie centrale en raison d’une morbidité moindre de la RF. Alors que des localisations plus périphériques (segments VI, II et III) sont plus accessibles à un contrôle chirurgical de la maladie. La difficulté technique prévisible du geste chirurgical et le volume de foie non tumoral réséqué doivent donc être pris en compte dans le choix entre ces 2 méthodes.
La comparaison de la technique de RF multibipolaire et de la chirurgie pour les CHC de taille intermédiaire (entre 2 et 5 cm) (28), confirme l’intérêt de cette technique, montrant un taux de récidive locale non statistiquement significatif (à 1 et 3 ans, respectivement de 5,5 % et 10 % pour la RF multibipolaire et de 1,9 et 1,9 % pour la chirurgie) mais, avec par contre un taux de récidive intra-segmentaire plus élevé dans le groupe RF (7,4 % vs. 1,9 % à 1 an, 27,8 % vs. 3,3 % à 3 ans, p = 0,008). L’avantage de la résection, si elle est bien anatomique, est d’emporter les possibles micro-métastases diffusées par voie portale dans la périphérie proche de la tumeur, même pour les lésions solitaires de petite taille. Dans cette série, les taux de survie globale (86,7 % après RF multibipolaire, 91,4 % après chirurgie à 3 ans) et sans récidive identiques s’expliquent par la prise en charge possible par RF itérative des récidives loco-régionales et à distance, toujours dans une intention curative.
En pratique, le choix du traitement entre la chirurgie et la RF (tableau 2) va dépendre d’une part de la mortalité péri-opératoire prévisible des patients, et d’autre part du taux prévisible de récidive locale du mode de thermoablation choisie, dont on a vu qu’il est influencé par de nombreux facteurs (localisation et taille de la lésion, choix de la technique de thermoablation…).
Autres indications et procédures
Down-staging avant transplantation hépatique
Les patients en attente de transplantation hépatique peuvent en bénéficier, soit pour stabiliser la maladie dans l’attente de la greffe et limiter le nombre de sorties de liste, soit pour réduire la masse tumorale et leur permettre d’accéder aux critères de greffe (29,17). L’avantage de la RF est de limiter les adhérences en perspective d’une transplantation.
L’absence de CHC viable dans le foie natif sur l’examen histologique de la pièce d’hépatectomie totale est un facteur pronostic par rapport à la récidive du CHC après la transplantation (30,31), le contrôle de la maladie tumorale améliorant la survie globale après la transplantation, en particulier lorsque la période sur la liste d’attente dépasse 6-12 mois (32).
Combinaison chimioembolisation (CE) et RF
La réduction de la taille de la tumeur améliore l’efficacité de la RF, et la CE, le plus souvent première, en réduisant le flux artériel et veineux hépatique, crée une ischémie et une nécrose tumorale, augmentant la sensibilité des cellules tumorales à l’hyperthermie, avec une potentialisation de ces 2 méthodes.
Cette association peut être intéressante justement dans le down-staging des patients en attente de greffe : pour exemple la comparaison de 2 groupes de patients en attente de transplantation hépatique, porteurs de CHC dans les critères de Milan et en dehors des critères, qui ont été traités par RF pour le 1er groupe et par CE puis RF dans le 2e groupe. Les séances de chimio-embolisation ont été répétées jusqu’à retrouver les critères de Milan, la RF était réalisée en moyenne 1 à 2 mois après le geste intra-artériel. Les courbes de survie globale et sans récidive après avoir appliqué des scores de propension sont comparables, avec un taux de complications comparables (33).
Mais le bénéfice clinique est souvent difficile à évaluer et l’avantage de combiner RF et CE reste à confirmer. Pour le traitement de CHC solitaires de 3 à 5 cm non opérables, la vaste cohorte de Chu et al. (plus de 500 patients) (34) a comporté une analyse rétrospective à 3 bras comparant d’une part la CE associée 15 jours plus tard à l’ablation par RF et d’autre part les groupes de CE et de RF monopolaire en monothérapie, avec durée médiane de suivi longue de près de 4 ans. Les taux de survie globale sont restés significativement plus élevés dans le groupe CE-ablation par RF que dans chaque groupe de monothérapie. Cinq, dix et quinze ans après le traitement, les taux de survie globale étaient respectivement de 57,8 %, 41,8 % et 30,9 % dans le groupe CE -ablation par RF, de 47,2 %, 28,4 % et 19,2 % dans le groupe CE et de 35,2 %, 11,9 % et 11,9 % dans le groupe ablation par RF. On reste interrogatif sur les résultats de la RF (applications répétées d’une aiguille monopolaire unique, ou utilisation de cluster) comparativement à ceux de la CE. La combinaison de ces 2 traitements permettrait ainsi de compenser les résultats insuffisants de la RF, dans la modalité utilisée.
Suivi du traitement
Une imagerie en coupes (scanner ou IRM) est réalisée précocement après le geste (environ 1 mois après, lorsque les phénomènes inflammatoires, à l’origine de prises de contraste difficiles à interpréter, ont bien diminué). Cet examen a pour but de s’assurer que le ciblage du traitement a été correct et qu’il n’y a pas de reliquat tumoral qui nécessiterait un traitement complémentaire rapide. Cet examen permet aussi de juger des marges d’ablation. Par la suite la surveillance se fait par scanner, ou de préférence par IRM tous les 3 mois pendant les 2 premières années, pour juger d’une récidive loco-régionale ou à distance dans le foie.
La cicatrice de thermoablation se présente sous forme d’une image nodulaire avasculaire, spontanément hyper intense T1 avant injection, en rapport avec la nécrose de coagulation (figure 2).
Une récidivé loco-régionale se présente sous forme de prise de contraste nodulaire sur les berges de cette cicatrice. Les séquences en pondération T2 ou en diffusion pour diagnostiquer la récidive sont plus difficiles à interpréter car il persiste longtemps après le geste une hyper intensité T2 au sein ou au pourtour de la cicatrice.
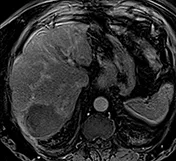
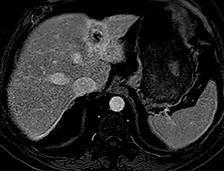
Figure 2 a |  |
| Carcinome hépato-cellulaire de 45 mm de diamètre, typique en IRM chez un patient de 75 ans, porteur d’une cirrhose éthylique et dysmétabolique incomplètement sevrée, Child A avec une alfafoetoprotéine normale. La clairance au vert d’indocyanine très pathologique à 34% à 15 min (Nle <15) a fait contre-indiquer un traitement chirurgical. |
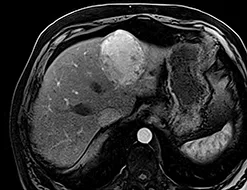
Figure 2 b |  |
| Contrôle en IRM après radiofréquence multibipolaire : la cicatrice de thermoablation apporte des marges centimétriques, est totalement avasculaire aux différents temps de l’injection (artériel et portal). |
Complications
Un certain nombre de patients présentant un CHC accessible à un traitement curatif par RF sont détournés de ce traitement curatif en raison de leur localisation « à risque » (position dans le dôme sous-diaphragmatique, sous-capsulaire proche du colon ou de l’estomac…). Alors qu’il existe de nombreux artifices permettant de s’affranchir de complications pour ces zones « à risque » : hydrodissection pour protéger le diaphragme
et améliorer la visibilité d’une lésion haut située, limiter le retentissement sus-diaphragmatique (épanchements pleuraux et pneumopathies), hydrodissection ou carbodissection pour protéger le tube digestif (angle colique droit pour les lésions de la pointe du foie droit, et estomac pour les lésions lobaires gauches), ponction « no touch » pour les lésions sous-capsulaires, guidage cœlio-assisté pour traiter une lésion en position sous- capsulaire en présence d’adhérences avec le tube digestif…
L’ablation par RF pour le CHC est considérée comme une procédure sûre et peu invasive, avec dans l’étude japonaise de Maeda et al. un taux de mortalité de 0,064 % (6/9 411 patients), et un taux de complications de 2,92 % (330 complications/11 298 procédures) (35). Le taux de complications majeures est < 4-5 % dans la plupart des études (4).
RF et micro-ondes ne montrent pas de différence statistiquement significative en termes de mortalité ou de taux de complications majeures ou mineures. Le micro-onde a un taux de mortalité compris entre 0 % et 0,36 % (36,37,38).
Pour réduire l’incidence des complications majeures, la sélection des patients et le choix de l’approche percutanée sont essentiels ; les patients à haut risque d’infection, de troubles de la coagulation et de chirurgie abdominale antérieure doivent être évalués pour établir le bénéfice de la méthode d’ablation. Le score de Child-Pugh doit être pris en compte avant de réaliser des ablations multiples ou de grande taille exposant à une insuffisance hépatique. Il ne faut pas hésiter dans ces cas précis à recourir à un traitement séquentiel.
Le syndrome post-ablation comporte des douleurs et de la fièvre pendant 24-48 h, et est facilement contrôlé par un traitement symptomatique. Les complications les plus fréquentes sont l’hémorragie et l’abcédation, parfois graves chez ces patients fragiles. Les complications hémorragiques, comme l’ensemencement sur le trajet de ponction, sont limitées par la cautérisation soigneuse au retrait de l’aiguille. L’ensemencement tumoral est observé dans 0,5 à 3 % des RF (39), il est favorisé par la ponction directe du CHC sous-capsulaire, la ponction multi-aiguille extra-tumorale doit permettre d’éviter ce genre de complications.
Tableau 2 : Critères de choix entre destruction percutanée et résection chirurgicale en cas de petit CHC | Thermoablation | Chirurgie |
|---|
| État général | Présence de co-morbidités | Peu ou pas de co-morbidités |
| Foie sous-jacent | Cirrhose | Foie peu fibreux |
| Fonctions hépatiques | Child A < B7 | Child A VIC* normal |
| Hypertension portale | oui | absente |
| Nodule unique | Plutôt si < 3cm
Possible jusquà 5 cm de diam.
(RF multibipolaire, RF + chimioembol.) | Plutôt si > 3 cm |
| Nombre de nodules | 2 à 3 lésions dans des segments éloignés | 2 à 3 lésions dans le même segment |
| Projet de transplantation | oui | non |
| AFP élevée | non | oui |
| Situation anatomique | Centrale | Périphérique |
(VIC* = test au vert d’indocyanine)
Les contre-indications (tableau 3)
Pour limiter les complications, on rappelle que la cirrhose doit être compensée Child A jusquà B7 sans ascite, et que les éventuels troubles de coagulation doivent être compensés ou contre-indiquent le geste si les plaquettes sont < à 50 000/mm3 et le TP < à 50 %. Le geste est possible sous aspirine, et nécessite une cautérisation soigneuse du trajet de ponction, il est contre –indiqué sous décoagulation efficace ou sous clopidrogel.
La présence d’un pace-maker n’est pas une contre-indication pour le micro-onde et la technique multi-bipolaire. En cas de RF monopolaire, la mise en place par l’anesthésiste d’un aimant sur le boîtier du pace-maker, remettant temporairement le rythme cardiaque en mode asynchrone est à discuter au cas par cas, en fonction de la proximité des sondes ventriculaires et de la zone de traitement, et de la dépendance ou non du patient au pace-maker.
Les contre-indications les plus formelles restent les rapports avec les voies biliaires proximales, avec dans ces cas-là, le choix d’une autre modalité de traitement (électroporation, CE…).
La présence d’une anastomose bilio-digestive ou d’antécédents de sphinctérotomie, (et donc d’une contamination de la bile par les germes du tube digestif), augmentent significativement le risque d’abcédation (40). Il faut opter pour une autre thérapeutique, ou envisager le geste sous couverture antibiotique ; on peut proposer une antibiothérapie contre les bacilles gram négatifs et les anaérobies, débutée la veille du geste et maintenue après le geste pour une durée de minimum sept jours.
Les procédures d’ablation thermique sont la meilleure option de traitement curatif pour les patients atteints de CHC qui ne peuvent pas bénéficier de résection chirurgicale ou de transplantation hépatique, en raison de leur contrôle tumoral local élevé et de leur nature peu invasive. Lorsque l’on discute chirurgie ou thermoablation, le choix entre ces 2 traitements est posé après analyse des co-morbidités, des fonctions hépatiques, de la localisation et de la taille de la lésion, du projet thérapeutique (transplantation hépatique) et de la technique de thermoablation utilisée. Enfin il faut connaître les différentes techniques de thermo-ablation, leurs risques respectifs de récidive loco-régionale, et leur sensibilité variable au heat sink effect.
Tableau 3 : Contre-indications des thermoablations| THERMOABLATIONS | Contre-indications absolues | Contre-indications relatives |
|---|
| Pace maker | non | Aimant sur le boitier pendant la procédure si RF monopolaire |
| Fonctions hépatiques et de coagulation | Score Child Pugh > B7 Ascite clinique | Compensation d’une thrombopénie pour le geste |
| Proximité avec les voies biliaires proximale | oui | |
| Voies biliaires dilatées | oui | |
| Anastomose bilio-digestive, ou large sphincterotomie | Oui si cicatrice prévisible de grande taille | A discuter si pas d’autre alternative et sous traitement antibiotique |
| Proximité avec le tube digestif | Oui si adhérences chirurgicales | Non si hydrodissection ou carbodissection possible |
| Localisation sous-capsulaire | | Non si méthode de traitement multiaiguille no touch |
Carcinome hépato-cellulaire et traitement par électroporation
L’électroporation irréversible est une technique d’ablation non thermique qui préserve les structures vasculaires, les voies biliaires et le tissu conjonctif, et n’est pas sujette au heat sink effect. C’est une technique sûre et efficace pour les tumeurs hépatiques qui présentent des contre- indications à la thermoablation, en particulier en raison de leur proximité avec les voies biliaires proximales. C’est donc un traitement à visée curative.
L’administration de multiples et brèves impulsions électriques à haut voltage et intensité élevée, provoque l’apoptose cellulaire par modification de l’équilibre ionique des membranes cellulaires avec ouverture irréversibles des pores membranaires. L’analyse histologique de pièces d’hépatectomie montre que les zones de traitement contiennent des branches portales et des canaux biliaires intacts (41).
Le geste est techniquement plus difficile qu’une thermoablation avec une mise en place strictement parallèle des aiguilles qui ne doivent pas être espacées de plus de 25 mm.
La procédure est réalisée sous anesthésie générale, avec curarisation profonde et synchronisation cardiaque.
Les contre-indications sont essentiellement d’origine cardiaque, arythmies qui ne permettent pas d’obtenir la synchronisation cardiaque ou présence d’un stimulateur cardiaque.
La sécurité et l’efficacité de cette technique ont maintenant été démontrées dans de nombreuses études, avec en particulier, sur le long terme, la préservation des structures biliaires (42,43,44). Les taux de récidive locale ne diffèrent pas significativement entre les lésions qui sont ou non proches des vaisseaux sanguins. En outre, l’ablation est complète jusqu’au contact des vaisseaux.
Les tumeurs de grande taille (> 4 cm) nécessitent un plus grand nombre d’aiguilles (toutes orientées dans une direction parallèle), et si les distances entre les extrémités des aiguilles sont trop grandes, l’ablation risque d’être incomplète. À l’inverse, si les distances entre les pointes des aiguilles sont trop courtes, des lésions thermiques de la zone cible peuvent résulter du courant élevé entre les pointes des sondes d’électroporation. Ainsi des lésions de plus de 4 cm de diamètre sont sans doute plus difficiles à traiter avec cette technique (43).
Les douleurs sont moins présentes qu’après une RF, et l’impact sur les fonctions hépatiques est moins marqué, avec peut-être un élargissement des indications chez des patients fragiles, présentant des fonctions hépatiques limites.
Suite au traitement, le processus de réparation est précoce en raison d’une augmentation rapide des facteurs d’inhibition des macrophages et entraîne une diminution rapide de la taille de la zone d’ablation avec une régénération rapide des tissus, beaucoup plus rapidement qu’avec une RF, puisque la zone de traitement peut avoir disparu à 1 an du traitement (45).
Peu d’études ont rapporté leur expérience uniquement avec le CHC : dans ce type d’indication, une ablation complète est observée dans plus de 90 % des cas (46,47), avec une survie sans progression tumorale locale de 83,6 % à un an dans la première étude et de 70 % dans la seconde qui a porté sur des lésions disparates, nodulaires mais aussi infiltrantes et des plus grands diamètres jusqu’à 50 mm.
L’électroporation est une option de traitement sûr et efficace pour le CHC non résécable, avec de très bons taux de réponse complète et de survie sans progression tumorale, pour des lésions qui auraient bénéficié de traitements loco-régionaux moins performants (CE) en raison de leur situation anatomique contre-indiquant la thermoablation.
Carcinome hépato-cellulaire et traitement par chimio-embolisation
Selon les recommandations BCLC, la chimio-embolisation intra-artérielle (CE) est le traitement de première ligne du carcinome hépatocellulaire (CHC) dans sa forme « intermédiaire », qui concerne les patients en bon état général (OMS < 2) présentant des lésions multi-nodulaires limitées et non résécables, sans invasion vasculaire ni propagation extra-hépatique et dont la fonction hépatique est bien préservée. L’obtention d’une réponse objective élevée et la préservation de la fonction hépatique sont tout aussi importantes, l’objectif est de prolonger la survie tout en maintenant une bonne qualité de vie.
Principe et techniques
Il existe deux techniques de chimio-embolisation, la chimio-embolisation conventionnelle (CE), qui utilise du Lipiodol, et la chimio-embolisation avec des microparticules chargées de chimiothérapie (mCE).
La chimiothérapie conventionnelle (CE)
Il s’agit de l’injection intra-artérielle la plus sélective possible dans les artères nourricières du processus tumoral d’un médicament cytotoxique (doxorubicine, épirubicine, idarubicine, mitomycine C ou cisplatine), émulsionné avec un agent huileux, le Lipiodol (Lipiodol® Ultra-Fluid, Guerbet), très radio-opaque, qui sert de vecteur aux antimitotiques par fixation au sein des vaisseaux intratumoraux. Le lipiodol circule au-delà des artères d’alimentation de la tumeur dans les branches portales distales par le plexus capillaire péribiliaire, les vasa vasorum de la veine porte et les branches portales de drainage de la tumeur (48). Il s’agit donc d’une embolisation à la fois artérielle et portale, certains auteurs ayant montré une relation entre l’absence de récidive tumorale et le degré d’opacification lipiodolée des petites branches veineuses périportales tumorales pendant la procédure (49).
Cette injection de chimiothérapie est suivie d’une embolisation artérielle, par gélatine résorbable (en 1 à 2 semaines) ou par microparticules (embolisation définitive). La fixation lipiodolée de la tumeur est le témoin de la nécrose tumorale et sert de biomarqueur de la réponse tumorale avec une nécrose proportionnelle à la fraction du volume tumoral tatoué par le lipiodol, elle permet de prédire la survie globale (50). L’absence de fixation ou une fixation partielle suggère que des artères nourricières de la tumeur n’ont pas été cathétérisées ou que la fixation de Lipiodol dans la tumeur était faible.
La CE sélective est définie comme le traitement intra-artériel au sein de l’artère hépatique segmentaire, et la CE supersélective est définie comme le traitement à l’étage sous-segmentaire au sein des pédicules artériels tumoraux. Cette dernière est considérée comme curative, avec une survie globale significativement meilleure que la CE non supersélective (51). Une CE non sélective, pratiquée en cas de charge tumorale élevée, expose le parenchyme hépatique normal à une ischémie étendue avec des lésions possiblement irréversibles.
La chimio-embolisation aux microparticules chargées (mCE)
L’utilisation de microsphères calibrées et chargées d’agents cytotoxiques entraîne une occlusion durable des vaisseaux intra-tumoraux à l’étage segmentaire et sous-segmentaire, ces microbilles sont un vecteur de libération lente permettant un relargage progressif de la chimiothérapie, augmentant sa concentration locale et diminuant le relargage systémique. La taille recommandée des microparticules calibrées, est de 100-300 μ afin d’assurer une occlusion distale avec préservation des artères segmentaires d’alimentation. Ce calibrage permet l’embolisation des vaisseaux tumoraux dont le calibre est inférieur à 100 μ, avec une densité plus élevée de billes et donc de chimiothérapie dans la tumeur (52).
Il a été montré que l’utilisation de microbilles était associée à une augmentation de la toxicité locale hépatique par rapport à la CE, avec un plus grand nombre de lésions biliaires et de bilomes intrahépatiques, tout particulièrement chez les patients présentant une cirrhose moins avancée (53), en raison de leurs plexus vasculaires péri-biliaires (shunts artério-veineux) moins développés, exposant à un plus grand risque d’ischémie biliaire. La CE aux microparticules chargées est donc à éviter chez les patients avec un foie sub-normal.
Quelle que soit la technique utilisée, la doxorubicine est l’agent chimio-toxique le plus couramment utilisé dans le monde pour le traitement intra- artériel du CHC, mais la justification de son utilisation repose sur des études anciennes, et n’est probablement pas le médicament le plus cytotoxique pour le CHC. Une étude française récente de phase II (54) a montré l’intérêt de l’utilisation de l’idarubicine chargée sur des microbilles 100-300 μ, avec un taux de réponse objective élevé, de 52 % à 6 mois, un temps moyen jusqu’à progression prometteur de 9,5 mois, bien supportée sur le plan de sa toxicité.
L’adjonction de chimiothérapie à l’embolisation a montré sa supériorité comparativement à l’embolisation seule : une différence significative a été constatée entre l’embolisation simple et la mCE, avec un taux de nécrose histologique des tumeurs analysées sur foies explantés de 77 % dans le groupe de traitement combiné versus 27,2 % dans le groupe embolisation seule (55). Des études randomisées (56,57) ont montré une meilleure réponse locale, moins de récidives et un temps à progression plus long si on associe embolisation et chimiothérapie intra-artérielle comparativement à l’embolisation seule. Enfin une chimiothérapie intra-artérielle seule s’accompagne d’une survie globale moins bonne que si elle s’accompagne d’une embolisation (58).
Le facteur le plus important pour améliorer le pronostic des patients est le contrôle local tumoral. Une réponse soutenue d’une durée de 6 mois ou plus est associée à une meilleure survie globale (59).
Ce contrôle local a bénéficié des progrès techniques, avec des efforts pour standardiser la méthode :
- Avec l’utilisation systématique de micro-cathéters permettant une navigation plus distale du cathéter et donc une administration hypersélective du traitement, plus récemment par l’introduction de microcathéters avec ballon d’occlusion, avec une diminution du nombre de séances de CE dans les 6 premiers mois (60). Ce cathétérisme sélectif et hypersélectif des vaisseaux tumoraux, permet aussi d’épargner au maximum le parenchyme hépatique non tumoral, et donc les effets secondaires.
- La généralisation de l’utilisation d’une angiographie 3D avec cone beam CT permet, comparativement à l’artériographie 2D, une détection plus exhaustive des pédicules vasculaires tumoraux, cette détection est maintenant facilitée par le traçage automatique des artères nourricières à l’aide de logiciels embarqués. Enfin, il est possible de vérifier en fin de procédure le tatouage suffisant et complet de la tumeur par le lipiodol (61,62).
Indications
Les CHC intermédiaires, multiples, non opérables, relèvent du traitement par CE, mais cette population est hétérogène, et tous les patients ne vont pas tirer bénéfice de ce traitement. Les indications classiquement retenues (17) sont en train d’évoluer (63) puisque nous avons à disposition d’autres modalités de traitement efficaces :
- les patients asymptomatiques (statut ECOG > 2),
- les fonctions hépatiques préservées (Child Pugh A, < B8 sans ascite),
- l’absence de localisation extra-hépatique,
- le volume tumoral limité : la stratégie thérapeutique repose maintenant sur une évaluation plus précise de la charge tumorale, qui peut annuler le bénéfice en termes de survie apporté par la CE. Il faut tenir compte de la taille de la lésion la plus volumineuse et du nombre total de lésions. Yamakado et al. (64) ont démontré que les formes avec 4 tumeurs mesurant 7 cm ou moins avaient un pronostic plus favorable. Les patients répondant aux critères « up-to-7 » (somme du nombre de lésions et de la taille de la plus volumineuse) ont la plus grande probabilité de réponse complète, tandis que les patients au-delà des critères « up-to-11 » ont la plus faible probabilité de réponse complète et la plus grande chance de réévoluer (65). Mais si l’on prend comme critère la classification « up to 7 » dans l’étude de Hung, 70 % des patients auraient été classés avec une charge tumorale élevée et donc inaptes à la CE.
Lors de la décision thérapeutique, il faut mettre en balance d’une part les traitements systémiques, et d’autre part la radioembolisation sélective interne. Il sera plus difficile après échec de la CE de revenir à une radio-embolisation, en raison du risque de vascularite, de thrombose artérielle induites par la CE, compromettant alors une nouvelle thérapie intra-artérielle. Le capital vasculaire est un élément à préserver et à prendre en compte dans le choix thérapeutique. Enfin des CE répétées induisent le développement d’une vascularisation tumorale à point de départ extra-hépatique (artères diaphragmatiques, capsulaires…) qui vont rendre plus difficile, voire compromettre la réalisation d’une radio-embolisation.
En pratique, en cas d’atteinte bi-lobaire, il faut opter pour un traitement séquentiel, afin de diminuer le risque de complications de la CE.
Les éléments décisionnels sont :
- la taille et le nombre de lésions qui déterminent le nombre de traitements,
- la localisation intra-hépatique des lésions : ainsi des lésions périphériques, avec des pédicules nourriciers peu nombreux bénéficieront mieux du traitement intra-artériel que des lésions centrales,
- la qualité de la vascularisation tumorale : des lésions hypovasculaires, avec une composante infiltrante sont de mauvais candidats à la chimioembolisation. Lorsque l’on dispose d’une histologie, les formes mal différenciées sont de mauvais candidats à la CE,
- de même les lésions compliquées d’une invasion segmentaire ou sous-segmentaire de la veine porte (qui n’est pas une contre-indication absolue à condition de ne pas réaliser d’embolisation complémentaire dans du parenchyme hépatique privé du flux veineux portal et de ne réaliser l’embolisation que dans les artères vascularisant exclusivement le processus tumoral), bénéficient maintenant d’une autre prise en charge. Ces cas particuliers, que l’on a pu traiter à une époque, quand il n’y avait pas d’autre proposition thérapeutique, relèvent maintenant soit d’une radio- embolisation sélective interne, soit de traitements généraux (immunothérapie),
- l’évaluation soigneuse des fonctions hépatiques : son aggravation après une CE est un risque à évaluer, en particulier chez les patients présentant une charge tumorale élevée. On peut s’aider de l’utilisation de scores, avant le 1er traitement : par exemple le score HAP (66) basé sur 4 paramètres (albumine, bilirubine, AFP et taille de la tumeur), ou le score ALBI, mis en avant par la dernière conférence de consensus Asie-Pacifique (63), calculé assez simplement à partir du taux d’albumine et de bilirubine. Un score ALBI 2 est un facteur de mauvais pronostic pour la survie après une CE. L’étude de sa variation en fonction de la charge tumorale a montré que la présence de localisations de CHC au-delà du critère « up-to-seven » est un facteur de risque pour présenter une décompensation hépatique au décours immédiat du traitement dans 24 % des cas, et que l’atteinte bi-lobaire au-delà du « up-to-11 » augmente le risque de garder sur le long terme des perturbations du bilan hépatique (67).
Après une première séance, faut-il retraiter et quand faut-il retraiter ?
La CE ne doit pas être répétée lorsqu’il y a une progression ou une altération de la fonction hépatique, une aggravation de l’état de performance (PS), l’apparition d’une thrombose tumorale de la veine porte ou de métastases extra-hépatiques (17,68).
Les patients qui présentent une réponse complète dans les suites de leur 1re CE ont une survie globale significativement plus longue, ce qui suggère l’importance d’obtenir une réponse complète dès la première séance de traitement. Mais faut-il persévérer après un premier échec de CE ? Des études ont montré que 40 à 50 % des patients qui n’avaient pas répondu à la chimio-embolisation initiale pouvaient répondre à une deuxième procédure, avec à la fois une réponse et une meilleure survie globale que les non-répondeurs (69,70). Par la suite les séances réalisées « à la demande » augmente l’efficacité et la tolérance du traitement (71), en ciblant les tumeurs actives résiduelles, chez des patients avec une fonction hépatique stable. Mais avec le risque, lorsque les lésions deviennent réfractaires, que 20 à 30 % des patients aient évolué vers les classes Child-Pugh B ou C, ne permettant plus de poursuivre avec un traitement systémique (63).
Résultats
Depuis 2002, des essais contrôlés randomisés et des méta-analyses ont démontré la supériorité de la CE sur les soins de support pour le CHC de stade intermédiaire : Llovet et al. ont rapporté que la survie moyenne était significativement plus longue avec la CE (28,6 mois) qu’avec les soins de support (17,9 mois ; P = 0,009) (72), avec une évolution moins fréquente vers la thrombose portale tumorale. Cette augmentation du taux de survie est directement liée à l’importance de la fixation lipiodolée par les lésions tumorales, inversement proportionnelle au volume tumoral et au stade selon la classification Child-Pugh (50).
Dans l’étude SPACE (73), plus récente, la très bonne sélection des patients, et l’amélioration de la technique ont permis d’obtenir une amélioration de la survie à 2 ans à plus de 50 % (29 % dans l’étude Llovet de 2002).
La survie globale dépend étroitement de la réponse complète, et de la charge tumorale donc de la sélection des patients : Kim et al. (74) ont rapporté une survie globale médiane de 43,6 mois et un taux de réponse complète de 59,2 % chez des patients dont la charge tumorale était conforme aux critères up-to-7.
Choix entre CE classique et aux microparticules :
Le choix entre les 2 techniques alimente encore de nombreux débats entre radiologues.
La CE aux billes marquées devrait être la technique de choix en raison d’une meilleure standardisation de la technique, et d’études pharmacocinétiques plus favorables avec une plus faible absorption systémique de la doxorubicine et une concentration intra-tumorale plus importante, mais le bénéfice en termes de survie et de taux de réponse reste à prouver :
L’efficacité et la toxicité des 2 types de traitement intra-artériel ont été évaluées dans le cadre de l’essai européen randomisé de phase II Precision V (75) comparant mCE et CE chez 212 patients présentant principalement un CHC de stade intermédiaire. Mais ni le critère principal d’efficacité (réponse à 6 mois, p = 0,11) ni le critère principal de toxicité (incidence des évènements indésirables graves dans les 30 jours suivant la procédure, p = 0,86) n’ont été atteints dans cette étude. La mCE a montré quelques avantages dans les sous-groupes fragiles, tels que les patients Child-Pugh B, ainsi qu’une alopécie moins fréquente.
La seconde étude randomisée (76) n’a pas non plus montré de différence significative dans la réponse tumorale, le critère d’évaluation principal, qui était la supériorité de la mCE pour la survie à deux ans, n’a pas été vérifié. Il n’y a pas eu de différence significative dans l’incidence des événements indésirables. Seule la douleur post-procédure était plus fréquente et plus sévère dans le groupe CE.
Enfin une méta-analyse de 2016 (1 449 patients), a confirmé la non-supériorité de la mCE par rapport à la CE en termes de réponse tumorale et de survie (77).
Les preuves sont insuffisantes pour recommander une technique de CE plutôt qu’une autre et le choix est laissé à l’opérateur (17). Le coût supérieur de la mCE est un élément qui est aussi à prendre en compte (78).
CE en dehors des stades BCLCB
- Les patients en attente de transplantation hépatique peuvent en bénéficier, soit pour stabiliser la maladie dans l’attente de la greffe, soit pour réduire la charge tumorale et leur permettre d’accéder aux critères de greffe (29,17).
On rappelle que l’absence de CHC viable dans le foie natif sur l’examen histologique de la pièce d’hépatectomie totale est un facteur pronostic par rapport à la récurrence du CHC après la transplantation. Le contrôle de la maladie tumorale améliore la survie globale après la transplantation, en particulier lorsque la période sur la liste d’attente dépasse 6-12 mois (32). - Combinaison de la CE et de la thermoablation : voir le chapitre sur la thermoablation
- Combinaison de la CE et du traitement systémique. Deux études de phase II/phase III, l’essai SPACE (73) et l’essai CE 2 (79) ont comparé l’association CE – sorafénib à la CE seule. Deux autres études randomisées ont comparé la CE à la combinaison chimio-embolisation et médicaments antiangiogéniques : le brivanib dans l’étude BRISK-TA (80) et l’orantinib dans l’étude ORIENTAL (81). Malheureusement, ces quatre essais n’ont pas réussi à démontrer un quelconque bénéfice clinique du traitement combiné.
Tous les espoirs sont maintenant placés dans l’association CE et immunothérapie. Les thérapies locales induisant la libération d’antigènes et de cytokines pro-inflammatoires, leur association avec les inhibiteurs de VEGF et de tyrosine kinase renforçant l’immunité sont à l’étude, nous sommes dans l’attente des essais en cours.
Complications
Le taux de mortalité globale est faible (0,6 % sur un total de 34 137 patients ayant subi 50 953 séances dans la méta-analyse de Lencioni et al.), la cause la plus fréquente de décès étant l’insuffisance hépatique menant à une défaillance hépatique ou à une encéphalopathie avec coma, ce qui montre qu’une sélection précise des patients est un facteur clé pour réduire le retentissement hépatique (82).
Le syndrome post-chimio-embolisation est la complication la plus fréquente (douleurs abdominales, nausées, hyperthermie et cytolyse) et est la conséquence de la nécrose tumorale, elle est responsable d’une prolongation de l’hospitalisation.
Il n’a pas été montré d’association robuste entre ce syndrome et la réponse tumorale, ce n’est donc pas le témoin d’un pronostic plus favorable (83). Les autres complications graves (hémorragie digestive, dissection artérielle, bilomes, abcès hépatiques, cholécystite ischémique…) surviennent dans moins de 10 % des cas. La cholécystite ischémique est rarement grave mais peut expliquer un certain nombre de phénomènes douloureux dans les suites du geste et est la conséquence de la migration de matériel d’embolisation dans l’artère cystique.
La survenue d’une surinfection de la nécrose tumorale est favorisée par la présence d’une anastomose bilio-digestive ou d’une prothèse biliaire, qui contamine chroniquement les voies biliaires intra-hépatiques par des germes d’origine digestive (84). Une couverture antibiotique large est préconisée mais le risque de complications infectieuses reste malgré tout élevé. L’abcédation de la nécrose tumorale, elle-même compliquée de rupture ou de fistulisation trans-diaphragmatique, est une complication redoutée en présence de lésion de grande taille (> 10 cm de diamètre). Contre-indications (tableau 4)
On rappelle qu’un Child > B8, un état général altéré (OMS > 2) sont des contre-indications absolues, de même qu’un envahissement tumoral portal tronculaire, une rupture récente de varices œsophagiennes, une extension tumorale extra-hépatique, un shunt artério-veineux circulant. Une anastomose bilio-digestive ou un antécédent de sphinctérotomie expose à un risque infectieux important nécessitant une couverture antibiotique selon les mêmes modalités que celles évoquées pour la thermoablation. Les troubles de l’hémostase sont des contre-indications relatives, l’anti agrégation plaquettaire par aspirine peut être maintenue, le clopidogrel doit être de préférence arrêté de même que l’anticoagulation pour le geste.
Mais si le geste doit être réalisé dans des conditions défavorables sur le plan de l’hémostase, il faudra discuter soit un abord par voie radiale, soit une fermeture du point de ponction fémoral (Femoseal®, Angioseal®, etc.).
La CE artérielle reste la norme de soins pour les lésions intermédiaires (maladie multi-nodulaire chez des patients asymptomatiques et avec une fonction hépatique conservée). Cependant, on fera dorénavant une étude plus attentive de la charge tumorale hépatique, en ne réservant ce type de traitement qu’à des lésions nodulaires hypervasculaires peu nombreuses et peu volumineuses, afin d’assurer au mieux le contrôle local et préserver sur le long terme les fonctions hépatiques de ces patients.
Tableau 4 : Contre-indications de la chimio-embolisation intra-artérielle| CHIMIOEMBOLISATIONS | Contre-indications absolues | Contre-indications relatives |
|---|
| Fonctions hépatiques | Child B7
Ascite clinique | |
| Troubles de la coagulation | | Thrombopénie (transfusion possible avant le geste)
Traitement anticoagulant qui ne peut être arrêté : intérêt de la voie radiale |
| Extension vasculaire de la maladie tumorale | Thrombose tumorale VP3 et 4* | Thrombose tumorale VP1 et 2* |
| Volume tumoral | - Métastases extra-hépatique
- Atteinte hépatique bi lobaire de grande taille
- Lésions infiltrantes hypo vasculaires
| |
| Anastomose bilio-digestive, ou large sphinctérotomie | | Nécessité d’une antibiothérapie de couverture pendant et dans les suites du geste |
| HTP | Rupture récente de varices œsophagiennes | Varices non traitées |
*Thrombose VP1 Thrombose distale n’atteignant pas une branche portale de second ordre VP2 thrombose dans une branche portale de second ordre VP3 : thrombose dans la branche portale droite ou gauche VP4 thrombose dans le tronc porte
Carcinome hépato-cellulaire et traitement par radioembolisation
La radioembolisation transartérielle (RE) à l’yttrium 90 (90Y) permet d’administrer de manière ciblée des radiations bêta à forte dose aux tumeurs hépatiques et de limiter l’exposition aux radiations du parenchyme hépatique normal. Le terme de radiothérapie sélective interne est plus adapté car le traitement repose sur l’irradiation, l’effet emboligène des sphères utilisées est peu marqué.
Technique
La procédure se déroule en 2 temps, avec une 1re angiographie hépatique « de simulation » ou work-up, qui détermine le ou les points d’injection avec au préalable si nécessaire l’embolisation des artères à destinée digestive, susceptibles d’être concernées par l’irradiation (par reflux). Aux points d’injection ainsi choisis, on réalise l’injection intra-artérielle d’albumine humaine macroagrégée au technétium 99m (99mTc). Cette artériographie est suivie d’une scintigraphie de perfusion hépatique afin d’évaluer le risque d’exposition extra-hépatique aux radiations, de mesurer le shunt hépato- pulmonaire, de détecter d’éventuels shunts digestifs qui n’auraient pas été dépistés et embolisés lors de cette première artériographie, et enfin de quantifier la dose de radiation absorbée par la tumeur et donc de calculer l’activité à administrer. Au terme de ce work-up, on peut décider de ne pas administrer le traitement si la dose prévisible à la tumeur n’est atteinte pour traiter correctement la lésion, ou si la dose prévisionnelle d’irradiation au poumon est supérieure à 25 Gy (soit un shunt pulmonaire d’environ 30 %). Le rôle déterminant de ce work–up et de cette scintigraphie a été montré (85), c’est un outil prédictif précis de la réponse tumorale et de la survie globale, il peut être considéré comme une sorte de biomarqueur pour la meilleure sélection des patients.
La 2e artériographie, réalisée entre 7 et 15 jours plus tard, correspond au traitement, avec l’injection des microsphères marquées à l’Yttrium 90, le point d’injection étant nécessairement identique à celui de la 1re artériographie. Deux types de microbilles marquées sont à disposition : les microsphères de verre (TheraSphere®, Boston), et de résine (SIR- Spheres®, Sirtex), dont l’activité diffère, celle des billes de verre est 50 fois supérieure à celle de résine, avec par conséquent un nombre de billes injectées différent, un effet emboligène différent, et une dosimétrie qui n’est pas comparable.
L’Yttrium n’irradiant pas au-delà de 1 cm de chaque sphère, il n’y a pas de mesure de radioprotection particulière et le traitement peut être organisé en ambulatoire, tout particulièrement si l’abord artériel est radial.
L’organisation de ce type de geste nécessite une bonne coopération entre les différents intervenants, qui sont nombreux : radiologues, médecins nucléaires, radio-pharmaciens, radio-physiciens et hépatologues, dont le dialogue est nécessaire, non seulement pour la gestion pratique de ces 2 temps de traitement, mais surtout pour la définition des indications avant le geste et entre les 2 temps artériographiques, la décision de traiter ou non reposant sur le calcul de la dose effective prévue à la tumeur et de l’irradiation du foie non tumoral (avec les risques que cela peut comporter chez ces patients cirrhotiques).
Indications et résultats
La radiothérapie sélective interne se positionne dans le traitement des CHC « intermédiaires ».
Préalablement aux essais randomisés, des études, le plus souvent rétrospectives, ont permis de comparer cette modalité de traitement à la CE, et ont montré une bonne qualité de vie, une augmentation du temps à progression, avec donc un meilleur contrôle tumoral local (86,87,88). Mais ce meilleur contrôle local ne se traduit pas par une augmentation de la survie globale. Ces études ont permis de mieux définir les patients auxquels s’adresse ce type de traitement : absence de maladie extra-hépatique, un ECOG < 2, de bonnes fonctions hépatiques avec Child Pugh < 7, l’absence d’ascite, un envahissement hépatique < 25 % du foie total, l’absence d’envahissement portal tronculaire.
Trois essais contrôlés randomisés de phase III, comparant RE et le sorafénib (étude française SARAH) (89), SIRveNIB (étude asiatique) (Chow et al.) et SORAMIC (90) ont montré des réponses tumorales, une tolérance au traitement et une qualité de vie significativement meilleures avec la radioembolisation qu’avec le sorafénib, mais sans amélioration de la survie globale.
Sans doute ces différentes études, au design ancien, ont inclus des patients trop graves, avec des volumes tumoraux trop importants, et avec une randomisation des patients avant le work-up, qui explique que près d’un quart des patients n’ont pas accédé au traitement. Enfin et surtout l’absence de dosimétrie personnalisée n’a pas permis de préciser si le seuil tumoricide avait été atteint sur les lésions cibles.
On a donc commencé à s’intéresser à la dose à la tumeur avec une étude ancillaire de Sarah (91) qui a évalué pour la première fois la relation entre la dose à la tumeur et la survie, et a montré que la dose d’irradiation calculée à partir du TEP Scanner au technétium 99m était un facteur indépendant d’allongement de la survie et était aussi positivement associée au taux de contrôle de la maladie. Une dose à la tumeur supérieure ou égale à 100 Gy (billes de résine) était le meilleur facteur indépendant de survie prolongée et de contrôle de la maladie, de même qu’une concordance optimale entre la TEP/TDM du work-up et celle réalisée en post traitement.
Le concept de dosimétrie personnalisée, c’est-à-dire avec un objectif de dose à la tumeur de plus de 205 Gy (billes de verre) a été à l’origine de l’étude multicentrique randomisée DOSISPHERE (92) comparant l’efficacité de la dosimétrie standard par rapport à cette approche personnalisée de RE avec des microsphères de verre chargées en 90Y.
Dans cette étude, la survie globale médiane dans le groupe dosimétrie personnalisée était de 26,6 mois, (ce qui est long si l’on considère que ces patients présentaient des lésions de grande taille supérieure à 7 cm et qu’il y avait une proportion élevée de patients présentant une thrombose de la veine porte), contre seulement 7,1 mois chez ceux ayant reçu une dose tumorale inférieure à 205 Gy. Les évaluations dosimétriques prospectives ont montré que sur les 30 patients ayant reçu une dose tumorale de 205 Gy ou plus, 23 (77 %) ont eu une réponse objective sur leurs lésions cibles comparativement à ceux ayant reçu moins de 205 Gy. Cette étude souligne la nécessité de bien sélectionner des patients avec une bonne fonction hépatique et une maladie hépatique limitée, avec la possibilité d’épargner au moins 30 % du foie de la radiation.
Dans certains cas bien particuliers se dessinent ainsi les indications de la RE :
- Chez les patients présentant une thrombose veineuse portale tumorale. Ces patients, bien souvent exclus des études thérapeutiques, sont de très mauvais candidats à la CE, en raison de l’effet défavorable sur les fonctions hépatiques de la privation de flux artériel. Dans ce sous-groupe particulier, tant que leurs fonctions hépatiques sont préservées, la RE peut être une proposition de traitement efficace (93) : ainsi la survie globale dans le groupe des patients Child-Pugh A de cette étude est de 13,3 mois.
- Chez les patients présentant une tumeur unique de grande taille, et qui ne sont pas candidats à une résection chirurgicale en raison de leurs co-morbidités ou de leurs fonctions hépatiques, qui ne peuvent accéder à une transplantation hépatique sans down staging préalable. C’est dans ce type d’indication, pour les lésions solitaires de moins de 8 cm de diamètre, que la RE fait son apparition pour la 1re fois dans l’algorithme décisionnel BCLC.
Un traitement segmentaire avec des doses d’irradiation plus élevées qui peuvent être délivrées en toute sécurité avec une épargne du parenchyme non tumoral, se traduit par des taux de réponse robustes et constants, dans ces cas, on peut parler de « segmentectomie radiologique ». Dans l’étude LEGACY, avec des patients sélectionnés (tumeurs de moins de 8 cm, Child Pugh A), et avec une stratégie consistant à administrer de fortes doses à la tumeur (la dose médiane dans le volume hépatique traité était de 410 Gy), le contrôle local élevé des lésions s’est accompagné d’un bénéfice clinique prolongé avec une survie sans progression de plus de 93 % à 2 ans, ce qui a permis à une cinquantaine de patients d’accéder secondairement à la chirurgie ou à la transplantation (94).
- Chez les patients porteurs de tumeurs nécessitant un traitement d’attente ou un down staging pour accéder à la transplantation. Dans l’étude rétrospective de Salem et al. (95) (cohorte de 291 patients), 47 % des patients présentant des tumeurs ≥ T2 ont pu réintégrer les critères de Milan, Le taux de survie à long terme n’a pas été différent, que l’Yttrium ait été réalisé comme traitement d’attente ou comme downstaging.
- Comme traitement néoadjuvant avant chirurgie hépatique : outre l’intérêt du contrôle tumoral, on constate une hypertrophie du foie controlatéral chez ces patients cirrhotiques, avec une augmentation du volume du futur foie jugée comme équivalente à une embolisation portale (96). Les dommages fonctionnels causés par les radiations sont susceptibles d’évoluer dans le temps, et il a été montré dans un groupe de patients cirrhotiques, après une RE unilobaire, que l’augmentation en volume du foie et la fonction hépatique, étudiée par scintigraphies hépato-biliaires répétées à la mébrofénine n’évoluent pas parallèlement (97) : on constate tout d’abord une perte des fonctions du foie non traité dans les 15 premiers jours, avec une récupération jusqu’au 3e mois, puis une poursuite ultérieure de cette augmentation fonctionnelle qui peut atteindre 59 % à 6 mois. Une attente de 6 mois avant résection chirurgicale de ces pathologies tumorales évoluées, permet à la fois de sélectionner les patients ne présentant pas d’évolution dans le foie contro-latéral et de bénéficier d’un gain fonctionnel optimal pour le futur foie restant.
Imagerie de surveillance (figure 3)
La nécrose tumorale est visible lorsque la dose d’irradiation est élevée avec une destruction de la vascularisation tumorale. Mais la distribution inhomogène du traitement dans des lésions de grand volume rend l’interprétation radiologique difficile.
Tout d’abord une augmentation paradoxale de la taille de la tumeur peut être observée dans la phase initiale en raison de la nécrose et de l’œdème, elle est observée jusqu’à 36 % des lésions durant le 1er mois. Par conséquent, l’évaluation de la réponse tumorale doit être effectuée après 3 mois (98). La décroissance en taille de la lésion est très lente, avec une réponse complète et des critères d’amélioration qui augmentent avec le temps : dans l’étude de Lee et al., la réduction de la taille de la tumeur est de 2 % à 1 mois, 14 % à 3 mois, et 28 % à 6 mois (99). Bien que la diminution de la taille de la tumeur soit rassurante, l’absence d’augmentation dans le temps est un signe positif, et peut être considéré comme le reflet d’une réponse clinique, car l’histoire naturelle de la tumeur est la poursuite de la croissance tumorale…
Il est préférable d’utiliser les critères mRecist pour juger de l’efficacité du traitement (100), mais les variations du réhaussement tumoral, la diminution de l’hypervascularisation peuvent se faire attendre. Les données de Lee et al. montrent une amélioration selon mRecist dans 31 % des cas à 1 mois, 50 % à 3 mois et 59 % à 6 mois. Par conséquent, il faut attendre jusqu’à 3-6 mois avant de prendre la décision de retraiter, le meilleur signe de progression étant l’apparition de nouvelles lésions péritumorales ou à distance dans le foie.
La confrontation de l’analyse histologique d’explants après RE a montré que les 49 % de patients pour lesquels l’imagerie avait conclu à une réponse partielle présentaient en fait une nécrose complète histologique dans 78 % des cas, ce qui montre bien la difficulté de l’interprétation radiologique de l’imagerie de surveillance (101). Toujours dans cette étude, la présence d’un réhaussement annulaire périphérique, correspondant au tissu de granulation entourant la nécrose, était un signe de réponse positive puisque 93 % de ces lésions avec réhaussement annulaire présentaient une nécrose complète.
Perspectives
Des essais de combinaison de la RE avec l’immunothérapie administrée de façon séquentielle après la RE sont en cours d’élaboration mais ne sont pas encore activés.
La RE offre des possibilités de traitement pour des patients présentant des CHC évolués et agressifs, qui peuvent être de grande taille, ou avec une thrombose veineuse portale. Il faudra attendre des études complémentaires pour définir plus précisément ses indications, en particulier par rapport aux traitements par immunothérapie. D’ores et déjà, une étude au cas par cas en RCP spécialisée doit sélectionner des patients présentant des fonctions hépatiques conservées, des tumeurs laissant un volume de foie non tumoral suffisant (au moins 30 %) et surtout l’utilisation systématique de la dosimétrie personnalisée pour permettre de juger objectivement du traitement réalisé.
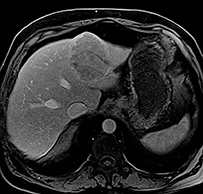
Figure 3 a |  |
| Acquisition en IRM à la phase artérielle et portale de l’injection d’un carcinome hépa- to-cellulaire de 8 cm de diamètre sur hépatopathie dysmétabolique chez un patient de 63 ans présentant une contre-indication formelle à la chirurgie en raison d’une myocardiopathie ischémique avec dysfonction ventriculaire contre-indiquant une prise en charge chirurgicale. |
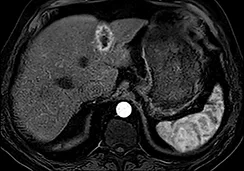
Figure 3 b |  |
| Contrôle par IRM (acquisition en pondération T1 à la phase artérielle et portale) à 1 an du traitement par radiothérapie sélective interne par Therasphères dans l’artère hépatique gauche avec une dose à la tumeur de 370Gy. A noter la prise de contraste annulaire périphérique séquellaire de la lésion involuée. |
Conclusion
La discussion du traitement d’un carcinome hépato-cellulaire doit être collégiale, en présence d’un radiologue interventionnel car les traitements radiologiques ont une spécificité et une place à tous les stades d’avancement de la maladie. Pour chaque modalité de traitement, une évaluation précise de la pathologie hépatique sous-jacente est indispensable.
Les différentes techniques de thermoablation peuvent prétendre à des survies prolongées, et se discutent maintenant en alternative à la chirurgie dans un grand nombre de cas en présence de lésions de moins de 5 cm de diamètre. L’électroporation est une technique curative intéressante en alternative à la radiofréquence en présence de lésions adossées aux voies biliaires proximales, cette situation restant la principale contre-indication des thermo-ablations.
La chimio-embolisation est toujours le traitement à proposer pour les atteintes multi-nodulaires chez des patients asymptomatiques et avec une fonction hépatique conservée, mais les résultats des nouveaux traitements systémiques rendent plus exigeants pour porter des indications en présence de localisations multiples avec un volume tumoral important.
Enfin, même si des études complémentaires sont encore nécessaires, la radiothérapie sélective interne a des indications particulières pour des lésions évoluées de mauvais pronostic, sa place par rapport à l’immunothérapie est encore à débattre dans ce type d’indication.
Bilbliographie
- Seror O. Ablative therapies: Advantages and disadvantages of radiofrequency, cryotherapy, microwave and electroporation methods, or how to choose the right method for an individual patient? Diagn Interv Imaging. 2015;96(6):617–624. doi: 10.1016/j.diii.2015.04.007.
- Jaskolka JD, Asch MR, Kachura JR, et al. Needle tract seeding after radiofrequency ablation of hepatic tumors. J Vasc Interv Radiol JVIR. 2005;16(4):485–491. doi: 10.1097/01.RVI.0000151141.09597.5F.
- Petit A, Hocquelet A, N’kontchou G, et al. No-Touch Multi-bipolar Radiofrequency Ablation for the Treatment of Subcapsular Hepatocellular Carcinoma ≤ 5 cm Not Puncturable via the Non-tumorous Liver Parenchyma. Cardiovasc Intervent Radiol. 2020;43(2):273–283. doi: 10.1007/ s00270-019-02357-9.
- Nault J-C, Sutter O, Nahon P, Ganne-Carrié N, Séror O. Percutaneous treatment of hepatocellular carcinoma: State of the art and innovations. J Hepatol. 2018;68(4):783–797. doi: 10.1016/j.jhep.2017.10.004.
- Lee MW, Kang D, Lim HK, et al. Updated 10-year outcomes of percutaneous radiofrequency ablation as first-line therapy for single hepatocellular carcinoma < 3 cm: emphasis on association of local tumor progression and overall survival. Eur Radiol. 2020;30(4):2391–2400. doi: 10.1007/s00330-019-06575-0.
- Kim Y-S, Lee WJ, Rhim H, Lim HK, Choi D, Lee JY. The minimal ablative margin of radiofrequency ablation of hepatocellular carcinoma (> 2 and < 5 cm) needed to prevent local tumor progression: 3D quantitative assessment using CT image fusion. AJR Am J Roentgenol. 2010;195(3):758–765. doi: 10.2214/AJR.09.2954.
- Liu C-H, Arellano RS, Uppot RN, Samir AE, Gervais DA, Mueller PR. Radiofrequency ablation of hepatic tumours: effect of post-ablation margin on local tumour progression. Eur Radiol. 2010;20(4):877–885. doi: 10.1007/s00330-009-1610-4.
- Bhardwaj N, Strickland AD, Ahmad F, Atanesyan L, West K, Lloyd DM. A comparative histological evaluation of the ablations produced by microwave, cryotherapy and radiofrequency in the liver. Pathology (Phila). 2009;41(2):168–172. doi: 10.1080/00313020802579292.
- Tong Y, Yang H, Xu X, et al. Effect of a hypoxic microenvironment after radiofrequency ablation on residual hepatocellular cell migration and invasion. Cancer Sci. 2017;108(4):753–762. doi: 10.1111/cas.13191.
- Huang S, Yu J, Liang P, et al. Percutaneous microwave ablation for hepatocellular carcinoma adjacent to large vessels: a long-term follow-up. Eur J Radiol. 2014;83(3):552–558. doi: 10.1016/j.ejrad.2013.12.015.
- An C, Li W-Z, Huang Z-M, et al. Small single perivascular hepatocellular carcinoma: comparisons of radiofrequency ablation and microwave ablation by using propensity score analysis. Eur Radiol. 2021;31(7):4764–4773. doi: 10.1007/s00330-020-07571-5.
- Bouda D, Barrau V, Raynaud L, et al. Factors Associated with Tumor Progression After Percutaneous Ablation of Hepatocellular Carcinoma: Comparison Between Monopolar Radiofrequency and Microwaves. Results of a Propensity Score Matching Analysis. Cardiovasc Intervent Radiol. 2020;43(11):1608–1618. doi: 10.1007/s00270-020-02549-8.
- Suwa K, Seki T, Aoi K, et al. Efficacy of microwave ablation versus radiofrequency ablation for hepatocellular carcinoma: a propensity score analysis. Abdom Radiol N Y. 2021;46(8):3790–3797. doi: 10.1007/s00261-021-03008-9.
- Vietti Violi N, Duran R, Guiu B, et al. Efficacy of microwave ablation versus radiofrequency ablation for the treatment of hepatocellular carcinoma in patients with chronic liver disease: a randomised controlled phase 2 trial. Lancet Gastroenterol Hepatol. 2018;3(5):317–325. doi: 10.1016/S2468-1253(18)30029-3.
- Lee DH, Lee MW, Kim PN, Lee YJ, Park HS, Lee JM. Outcome of No-Touch Radiofrequency Ablation for Small Hepatocellular Carcinoma: A Multicenter Clinical Trial. Radiology. 2021;301(1):229–236. doi: 10.1148/radiol.2021210309.
- Hocquelet A, Aubé C, Rode A, et al. Comparison of no-touch multi-bipolar vs. monopolar radiofrequency ablation for small HCC. J Hepatol. Elsevier; 2017;66(1):67–74. doi: 10.1016/j.jhep.2016.07.010.
- Galle PR, Forner A, Llovet JM, et al. EASL Clinical Practice Guidelines: Management of hepatocellular carcinoma. J Hepatol. Elsevier; 2018;69(1):182–236. doi: 10.1016/j.jhep.2018.03.019.
- Huang J, Yan L, Cheng Z, et al. A randomized trial comparing radiofrequency ablation and surgical resection for HCC conforming to the Milan criteria. Ann Surg. 2010;252(6):903–912. doi: 10.1097/SLA.0b013e3181efc656.
- Chen M-S, Li J-Q, Zheng Y, et al. A prospective randomized trial comparing percutaneous local ablative therapy and partial hepatectomy for small hepatocellular carcinoma. Ann Surg. 2006;243(3):321–328. doi: 10.1097/01.sla.0000201480.65519.b8.
- Feng K, Yan J, Li X, et al. A randomized controlled trial of radiofrequency ablation and surgical resection in the treatment of small hepatocellular carcinoma. J Hepatol. 2012;57(4):794–802. doi: 10.1016/j.jhep.2012.05.007.
- Lee HW, Lee JM, Yoon J-H, et al. A prospective randomized study comparing radiofrequency ablation and hepatic resection for hepatocellular carcinoma. Ann Surg Treat Res. 2018;94(2):74–82. doi: 10.4174/astr.2018.94.2.74.
- Peng Z-W, Lin X-J, Zhang Y-J, et al. Radiofrequency ablation versus hepatic resection for the treatment of hepatocellular carcinomas 2 cm or smaller: a retrospective comparative study. Radiology. 2012;262(3):1022–1033. doi: 10.1148/radiol.11110817.
- Uhlig J, Sellers CM, Stein SM, Kim HS. Radiofrequency ablation versus surgical resection of hepatocellular carcinoma: contemporary treatment trends and outcomes from the United States National Cancer Database. Eur Radiol. 2019;29(5):2679–2689. doi: 10.1007/s00330-018- 5902-4.
- Kolarich AR, Cabrera R, Hughes SJ, George TJ, Geller BS, Grajo JR. Thermal ablation versus wedge or segmental resection in patients with early stage hepatocellular carcinoma: a population survival analysis. HPB. 2019;21(2):249–257. doi: 10.1016/j.hpb.2018.07.004.
- Lee GC, Ferrone CR, Vagefi PA, et al. Surgical resection versus ablation for early-stage hepatocellular carcinoma: A retrospective cohort analysis. Am J Surg. 2019;218(1):157–163. doi: 10.1016/j.amjsurg.2018.12.067.
- Kang TW, Kim JM, Rhim H, et al. Small Hepatocellular Carcinoma: Radiofrequency Ablation versus Nonanatomic Resection–Propensity Score Analyses of Long-term Outcomes. Radiology. 2015;275(3):908–919. doi: 10.1148/radiol.15141483.
- Pan Y-X, Long Q, Yi M-J, et al. Radiofrequency ablation versus laparoscopic hepatectomy for hepatocellular carcinoma: A real world single center study. Eur J Surg Oncol J Eur Soc Surg Oncol Br Assoc Surg Oncol. 2020;46(4 Pt A):548–559. doi: 10.1016/j.ejso.2019.10.026.
- Mohkam K, Dumont P-N, Manichon A-F, et al. No-touch multibipolar radiofrequency ablation vs. surgical resection for solitary hepatocellular carcinoma ranging from 2 to 5 cm. J Hepatol. 2018;68(6):1172–1180. doi: 10.1016/j.jhep.2018.01.014.
- Pompili M, Francica G, Ponziani FR, Iezzi R, Avolio AW. Bridging and downstaging treatments for hepatocellular carcinoma in patients on the waiting list for liver transplantation. World J Gastroenterol. 2013;19(43):7515–7530. doi: 10.3748/wjg.v19.i43.7515.
- Agopian VG, Morshedi MM, McWilliams J, et al. Complete pathologic response to pretransplant locoregional therapy for hepatocellular carcinoma defines cancer cure after liver transplantation: analysis of 501 consecutively treated patients. Ann Surg. 2015;262(3):536–545; discussion 543-545. doi: 10.1097/SLA.0000000000001384.
- Habibollahi P, Shamchi SP, Choi JM, et al. Association of Complete Radiologic and Pathologic Response following Locoregional Therapy before Liver Transplantation with Long-Term Outcomes of Hepatocellular Carcinoma: A Retrospective Study. J Vasc Interv Radiol JVIR. 2019;30(3):323–329. doi: 10.1016/j.jvir.2018.11.037.
- Montalti R, Mimmo A, Rompianesi G, et al. Absence of viable HCC in the native liver is an independent protective factor of tumor recurrence after liver transplantation. Transplantation. 2014;97(2):220–226. doi: 10.1097/TP.0b013e3182a8607e.
- Shi F, Wu M, Lian S-S, et al. Radiofrequency Ablation Following Downstaging of Hepatocellular Carcinoma by Using Transarterial Chemoembolization: Long-term Outcomes. Radiology. 2019;293(3):707–715. doi: 10.1148/radiol.2019181991.
- Chu HH, Kim JH, Yoon H-K, et al. Chemoembolization Combined with Radiofrequency Ablation for Medium-Sized Hepatocellular Carcinoma: A Propensity-Score Analysis. J Vasc Interv Radiol JVIR. 2019;30(10):1533–1543. doi: 10.1016/j.jvir.2019.06.006.
- Maeda M, Saeki I, Sakaida I, et al. Complications after Radiofrequency Ablation for Hepatocellular Carcinoma: A Multicenter Study Involving 9,411 Japanese Patients. Liver Cancer. 2020;9(1):50–62. doi: 10.1159/000502744.
- Bertot LC, Sato M, Tateishi R, Yoshida H, Koike K. Mortality and complication rates of percutaneous ablative techniques for the treatment of liver tumors: a systematic review. Eur Radiol. 2011;21(12):2584–2596. doi: 10.1007/s00330-011-2222-3.
- Livraghi T, Meloni F, Solbiati L, Zanus G, Collaborative Italian Group using AMICA system. Complications of microwave ablation for liver tumors: results of a multicenter study. Cardiovasc Intervent Radiol. 2012;35(4):868–874. doi: 10.1007/s00270-011-0241-8.
- Liang P, Wang Y, Yu X, Dong B. Malignant liver tumors: treatment with percutaneous microwave ablation–complications among cohort of 1136 patients. Radiology. 2009;251(3):933–940. doi: 10.1148/radiol.2513081740.
- Nakagomi R, Tateishi R, Shiina S, et al. Drastically reduced neoplastic seeding related to radiofrequency ablation for hepatocellular carcinoma. Am J Gastroenterol. 2014;109(5):774–776. doi: 10.1038/ajg.2014.42.
- Choi D, Lim HK, Kim MJ, et al. Liver abscess after percutaneous radiofrequency ablation for hepatocellular carcinomas: frequency and risk factors. AJR Am J Roentgenol. 2005;184(6):1860–1867. doi: 10.2214/ajr.184.6.01841860.
- Cheng RG, Bhattacharya R, Yeh MM, Padia SA. Irreversible Electroporation Can Effectively Ablate Hepatocellular Carcinoma to Complete Pathologic Necrosis. J Vasc Interv Radiol JVIR. 2015;26(8):1184–1188. doi: 10.1016/j.jvir.2015.05.014.
- Lee EW, Thai S, Kee ST. Irreversible electroporation: a novel image-guided cancer therapy. Gut Liver. 2010;4 Suppl 1:S99–S104. doi: 10.5009/gnl.2010.4.S1.S99.
- Niessen C, Igl J, Pregler B, et al. Factors associated with short-term local recurrence of liver cancer after percutaneous ablation using irreversible electroporation: a prospective single-center study. J Vasc Interv Radiol JVIR. 2015;26(5):694–702. doi: 10.1016/j.jvir.2015.02.001.
- Gupta P, Maralakunte M, Sagar S, et al. Efficacy and safety of irreversible electroporation for malignant liver tumors: a systematic review and meta-analysis. Eur Radiol. 2021;31(9):6511–6521. doi: 10.1007/s00330-021-07742-y.`
- Sugimoto K, Kakimi K, Takeuchi H, et al. Irreversible Electroporation versus Radiofrequency Ablation: Comparison of Systemic Immune Responses in Patients with Hepatocellular Carcinoma. J Vasc Interv Radiol JVIR. 2019;30(6):845-853.e6. doi: 10.1016/j.jvir.2019.03.002.
- Freeman E, Cheung W, Kavnoudias H, Majeed A, Kemp W, Roberts SK. Irreversible Electroporation For Hepatocellular Carcinoma: Longer-Term Outcomes At A Single Centre. Cardiovasc Intervent Radiol. 2021;44(2):247–253. doi: 10.1007/s00270-020-02666-4.
- Sutter O, Calvo J, N’Kontchou G, et al. Safety and Efficacy of Irreversible Electroporation for the Treatment of Hepatocellular Carcinoma Not Amenable to Thermal Ablation Techniques: A Retrospective Single-Center Case Series. Radiology. 2017;284(3):877–886. doi: 10.1148/ radiol.2017161413.
- Terayama N, Matsui O, Gabata T, et al. Accumulation of iodized oil within the nonneoplastic liver adjacent to hepatocellular carcinoma via the drainage routes of the tumor after transcatheter arterial embolization. Cardiovasc Intervent Radiol. 2001;24(6):383–387. doi: 10.1007/s00270-001- 0070-2.
- Miyayama S, Matsui O, Yamashiro M, et al. Ultraselective Transcatheter Arterial Chemoembolization with a 2-F Tip Microcatheter for Small Hepatocellular Carcinomas: Relationship Between Local Tumor Recurrence and Visualization of the Portal Vein with Iodized Oil. J Vasc Interv Radiol. Elsevier; 2007;18(3):365–376. doi: 10.1016/j.jvir.2006.12.004.
- Kim DY, Ryu HJ, Choi JY, et al. Radiological response predicts survival following transarterial chemoembolisation in patients with unresectable hepatocellular carcinoma. Aliment Pharmacol Ther. 2012;35(11):1343–1350. doi: 10.1111/j.1365-2036.2012.05089.x.
- Yamakado K, Miyayama S, Hirota S, et al. Hepatic arterial embolization for unresectable hepatocellular carcinomas: do technical factors affect prognosis? Jpn J Radiol. 2012;30(7):560–566. doi: 10.1007/s11604-012-0088-1.
- Lee K-H, Liapi E, Vossen JA, et al. Distribution of iron oxide-containing Embosphere particles after transcatheter arterial embolization in an animal model of liver cancer: evaluation with MR imaging and implication for therapy. J Vasc Interv Radiol JVIR. 2008;19(10):1490–1496. doi: 10.1016/j.jvir.2008.06.008.
- Monier A, Guiu B, Duran R, et al. Liver and biliary damages following transarterial chemoembolization of hepatocellular carcinoma: comparison between drug-eluting beads and lipiodol emulsion. Eur Radiol. 2017;27(4):1431–1439. doi: 10.1007/s00330-016-4488-y.
- Guiu B, Chevallier P, Assenat E, et al. Idarubicin-loaded Beads for Chemoembolization of Hepatocellular Carcinoma: The IDASPHERE II Single-Arm Phase II Trial. Radiology. Radiological Society of North America; 2019;291(3):801–808. doi: 10.1148/radiol.2019182399.
- Nicolini A, Martinetti L, Crespi S, Maggioni M, Sangiovanni A. Transarterial chemoembolization with epirubicin-eluting beads versus transarterial embolization before liver transplantation for hepatocellular carcinoma. J Vasc Interv Radiol JVIR. 2010;21(3):327–332. doi: 10.1016/j. jvir.2009.10.038.
- Malagari K, Pomoni M, Kelekis A, et al. Prospective randomized comparison of chemoembolization with doxorubicin-eluting beads and bland embolization with BeadBlock for hepatocellular carcinoma. Cardiovasc Intervent Radiol. 2010;33(3):541–551. doi: 10.1007/s00270-009-9750-0.
- Meyer T, Kirkwood A, Roughton M, et al. A randomised phase II/III trial of 3-weekly cisplatin-based sequential transarterial chemoembolisation vs embolisation alone for hepatocellular carcinoma. Br J Cancer. 2013;108(6):1252–1259. doi: 10.1038/bjc.2013.85.
- Takayasu K, Arii S, Ikai I, et al. Overall survival after transarterial lipiodol infusion chemotherapy with or without embolization for unresectable hepatocellular carcinoma: propensity score analysis. AJR Am J Roentgenol. 2010;194(3):830–837. doi: 10.2214/AJR.09.3308.
- Zhang Y, Zhang M, Chen M, et al. Association of Sustained Response Duration With Survival After Conventional Transarterial Chemoembolization in Patients With Hepatocellular Carcinoma. JAMA Netw Open. 2018;1(6):e183213. doi: 10.1001/jamanetworkopen.2018.3213.
- Golfieri R, Bezzi M, Verset G, et al. Retrospective European Multicentric Evaluation of Selective Transarterial Chemoembolisation with and without Balloon-Occlusion in Patients with Hepatocellular Carcinoma: A Propensity Score Matched Analysis. Cardiovasc Intervent Radiol. 2021;44(7):1048–1059. doi: 10.1007/s00270-021-02805-5.
- Deschamps F, Solomon SB, Thornton RH, et al. Computed analysis of three-dimensional cone-beam computed tomography angiography for determination of tumor-feeding vessels during chemoembolization of liver tumor: a pilot study. Cardiovasc Intervent Radiol. 2010;33(6):1235–1242. doi: 10.1007/s00270-010-9846-6.
- Miyayama S, Yamashiro M, Hashimoto M, et al. Comparison of local control in transcatheter arterial chemoembolization of hepatocellular carcinoma ≤6 cm with or without intraprocedural monitoring of the embolized area using cone-beam computed tomography. Cardiovasc Intervent Radiol. 2014;37(2):388–395. doi: 10.1007/s00270-013-0667-2.
- Kudo M, Han K-H, Ye S-L, et al. A Changing Paradigm for the Treatment of Intermediate-Stage Hepatocellular Carcinoma: Asia-Pacific Primary Liver Cancer Expert Consensus Statements. Liver Cancer. 2020;9(3):245–260. doi: 10.1159/000507370.
- Yamakado K, Miyayama S, Hirota S, et al. Subgrouping of intermediate-stage (BCLC stage B) hepatocellular carcinoma based on tumor number and size and Child-Pugh grade correlated with prognosis after transarterial chemoembolization. Jpn J Radiol. 2014;32(5):260–265. doi: 10.1007/s11604-014-0298-9.
- Hung Y-W, Lee I-C, Chi C-T, et al. Redefining Tumor Burden in Patients with Intermediate-Stage Hepatocellular Carcinoma: The Seven-Eleven Criteria. Liver Cancer. 2021;1–12. doi: 10.1159/000517393.
- Kadalayil L, Benini R, Pallan L, et al. A simple prognostic scoring system for patients receiving transarterial embolisation for hepatocellular cancer. Ann Oncol Off J Eur Soc Med Oncol. 2013;24(10):2565–2570. doi: 10.1093/annonc/mdt247.
- Chi C-T, Lee I-C, Lee R-C, et al. Effect of Transarterial Chemoembolization on ALBI Grade in Intermediate-Stage Hepatocellular Carcinoma: Criteria for Unsuitable Cases Selection. Cancers. 2021;13(17):4325. doi: 10.3390/cancers13174325.
- Raoul J-L, Forner A, Bolondi L, Cheung TT, Kloeckner R, de Baere T. Updated use of TACE for hepatocellular carcinoma treatment: How and when to use it based on clinical evidence. Cancer Treat Rev. 2019;72:28–36. doi: 10.1016/j.ctrv.2018.11.002.
- Park C, Chu HH, Kim JH, et al. Clinical Significance of the Initial and Best Responses after Chemoembolization in the Treatment of Intermediate-Stage Hepatocellular Carcinoma with Preserved Liver Function. J Vasc Interv Radiol JVIR. 2020;31(12):1998-2006.e1. doi: 10.1016/j. jvir.2020.04.017.
- Georgiades C, Geschwind J-F, Harrison N, et al. Lack of response after initial chemoembolization for hepatocellular carcinoma: does it predict failure of subsequent treatment? Radiology. 2012;265(1):115–123. doi: 10.1148/radiol.12112264.
- Ernst O, Sergent G, Mizrahi D, Delemazure O, Paris JC, L’Herminé C. Treatment of hepatocellular carcinoma by transcatheter arterial chemoembolization: comparison of planned periodic chemoembolization and chemoembolization based on tumor response. AJR Am J Roentgenol. 1999;172(1):59–64. doi: 10.2214/ajr.172.1.9888740.
- Llovet JM, Real MI, Montaña X, et al. Arterial embolisation or chemoembolisation versus symptomatic treatment in patients with unresectable hepatocellular carcinoma: a randomised controlled trial. Lancet Lond Engl. 2002;359(9319):1734–1739. doi: 10.1016/S0140-6736(02)08649-X.
- Lencioni R, Llovet JM, Han G, et al. Sorafenib or placebo plus TACE with doxorubicin-eluting beads for intermediate stage HCC: The SPACE trial. J Hepatol. 2016;64(5):1090–1098. doi: 10.1016/j.jhep.2016.01.012.
- Kim BK, Kim SU, Kim KA, et al. Complete response at first chemoembolization is still the most robust predictor for favorable outcome in hepatocellular carcinoma. J Hepatol. 2015;62(6):1304–1310. doi: 10.1016/j.jhep.2015.01.022.
- Lammer J, Malagari K, Vogl T, et al. Prospective Randomized Study of Doxorubicin-Eluting-Bead Embolization in the Treatment of Hepatocellular Carcinoma: Results of the PRECISION V Study. Cardiovasc Intervent Radiol. 2010;33(1):41–52. doi: 10.1007/s00270-009-9711-7.
- Golfieri R, Giampalma E, Renzulli M, et al. Randomised controlled trial of doxorubicin-eluting beads vs conventional chemoembolisation for hepatocellular carcinoma. Br J Cancer. 2014;111(2):255–264. doi: 10.1038/bjc.2014.199.
- Facciorusso A, Di Maso M, Muscatiello N. Drug-eluting beads versus conventional chemoembolization for the treatment of unresectable hepatocellular carcinoma: A meta-analysis. Dig Liver Dis Off J Ital Soc Gastroenterol Ital Assoc Study Liver. 2016;48(6):571–577. doi: 10.1016/j. dld.2016.02.005.
- Wu X, Chapiro J, Malhotra A, Kothary N. Comparison of Drug-Eluting Embolics versus Conventional Transarterial Chemoembolization for the Treatment of Patients with Unresectable Hepatocellular Carcinoma: A Cost-Effectiveness Analysis. J Vasc Interv Radiol JVIR. 2021;32(1):2-12.e1. doi: 10.1016/j.jvir.2020.09.022.
- Meyer T, Fox R, Ma YT, et al. Sorafenib in combination with transarterial chemoembolisation in patients with unresectable hepatocellular carcinoma (TACE 2): a randomised placebo-controlled, double-blind, phase 3 trial. Lancet Gastroenterol Hepatol. 2017;2(8):565–575. doi: 10.1016/ S2468-1253(17)30156-5.
- Kudo M, Han G, Finn RS, et al. Brivanib as adjuvant therapy to transarterial chemoembolization in patients with hepatocellular carcinoma: A randomized phase III trial. Hepatol Baltim Md. 2014;60(5):1697–1707. doi: 10.1002/hep.27290.
- Kudo M, Cheng A-L, Park J-W, et al. Orantinib versus placebo combined with transcatheter arterial chemoembolisation in patients with unresectable hepatocellular carcinoma (ORIENTAL): a randomised, double-blind, placebo-controlled, multicentre, phase 3 study. Lancet Gastroenterol Hepatol. 2018;3(1):37–46. doi: 10.1016/S2468-1253(17)30290-X.
- Lencioni R, de Baere T, Soulen MC, Rilling WS, Geschwind J-FH. Lipiodol transarterial chemoembolization for hepatocellular carcinoma: A systematic review of efficacy and safety data. Hepatol Baltim Md. 2016;64(1):106–116. doi: 10.1002/hep.28453.
- Shim JH, Park J-W, Choi J-I, Kim H-B, Lee WJ, Kim C-M. Does postembolization fever after chemoembolization have prognostic significance for survival in patients with unresectable hepatocellular carcinoma? J Vasc Interv Radiol JVIR. 2009;20(2):209–216. doi: 10.1016/j.jvir.2008.10.021.
- Song SY, Chung JW, Han JK, et al. Liver abscess after transcatheter oily chemoembolization for hepatic tumors: incidence, predisposing factors, and clinical outcome. J Vasc Interv Radiol JVIR. 2001;12(3):313–320. doi: 10.1016/s1051-0443(07)61910-1.
- Garin E, Rolland Y, Pracht M, et al. High impact of macroaggregated albumin-based tumour dose on response and overall survival in hepatocellular carcinoma patients treated with 90 Y-loaded glass microsphere radioembolization. Liver Int Off J Int Assoc Study Liver. 2017;37(1):101–110. doi: 10.1111/liv.13220.
- Salem R, Lewandowski RJ, Kulik L, et al. Radioembolization results in longer time-to-progression and reduced toxicity compared with chemoembolization in patients with hepatocellular carcinoma. Gastroenterology. 2011;140(2):497-507.e2. doi: 10.1053/j.gastro.2010.10.049.
- Salem R, Gordon AC, Mouli S, et al. Y90 Radioembolization Significantly Prolongs Time to Progression Compared With Chemoembolization in Patients With Hepatocellular Carcinoma. Gastroenterology. 2016;151(6):1155-1163.e2. doi: 10.1053/j.gastro.2016.08.029.
- Sangro B, Carpanese L, Cianni R, et al. Survival after yttrium-90 resin microsphere radioembolization of hepatocellular carcinoma across Barcelona clinic liver cancer stages: A European evaluation. Hepatology. 2011;54(3):868–878. doi: 10.1002/hep.24451.
- Vilgrain V, Pereira H, Assenat E, et al. Efficacy and safety of selective internal radiotherapy with yttrium-90 resin microspheres compared with sorafenib in locally advanced and inoperable hepatocellular carcinoma (SARAH): an open-label randomised controlled phase 3 trial. Lancet Oncol. 2017;18(12):1624–1636. doi: 10.1016/S1470-2045(17)30683-6.
- Ricke J, Klümpen HJ, Amthauer H, et al. Impact of combined selective internal radiation therapy and sorafenib on survival in advanced hepatocellular carcinoma. J Hepatol. 2019;71(6):1164–1174. doi: 10.1016/j.jhep.2019.08.006.
- Hermann A-L, Dieudonné A, Ronot M, et al. Relationship of Tumor Radiation-absorbed Dose to Survival and Response in Hepatocellular Carcinoma Treated with Transarterial Radioembolization with 90Y in the SARAH Study. Radiology. 2020;296(3):673–684. doi: 10.1148/ radiol.2020191606.
- Garin E, Tselikas L, Guiu B, et al. Personalised versus standard dosimetry approach of selective internal radiation therapy in patients with locally advanced hepatocellular carcinoma (DOSISPHERE-01): a randomised, multicentre, open-label phase 2 trial. Lancet Gastroenterol Hepatol. 2021;6(1):17–29. doi: 10.1016/S2468-1253(20)30290-9.
- Abouchaleh N, Gabr A, Ali R, et al. 90Y Radioembolization for Locally Advanced Hepatocellular Carcinoma with Portal Vein Thrombosis: Long-Term Outcomes in a 185-Patient Cohort. J Nucl Med Off Publ Soc Nucl Med. 2018;59(7):1042–1048. doi: 10.2967/jnumed.117.199752.
- Salem R, Johnson GE, Kim E, et al. Yttrium-90 Radioembolization for the Treatment of Solitary, Unresectable HCC: The LEGACY Study. Hepatol Baltim Md. 2021;74(5):2342–2352. doi: 10.1002/hep.31819.
- Gabr A, Kulik L, Mouli S, et al. Liver Transplantation Following Yttrium-90 Radioembolization: 15-Year Experience in 207-Patient Cohort. Hepatology. John Wiley & Sons, Ltd; 2021;73(3):998–1010. doi: 10.1002/hep.31318.
- Edeline J, Lenoir L, Boudjema K, et al. Volumetric Changes after 90Y Radioembolization for Hepatocellular Carcinoma in Cirrhosis: An Option to Portal Vein Embolization in a Preoperative Setting? Ann Surg Oncol. 2013;20(8):2518–2525. doi: 10.1245/s10434-013-2906-9.
- Allimant C, Deshayes E, Kafrouni M, et al. Hepatobiliary Scintigraphy and Glass 90Y Radioembolization with Personalized Dosimetry: Dynamic Changes in Treated and Nontreated Liver. Diagn Basel Switz. 2021;11(6):931. doi: 10.3390/diagnostics11060931.
- Alem Z, Murray TE, Egri C, et al. Treatment response assessment following transarterial radioembolization for hepatocellular carcinoma. Abdom Radiol N Y. 2021;46(8):3596–3614. doi: 10.1007/s00261-021-03095-8.
- Lee JS, Choi HJ, Kim BK, et al. The Modified Response Evaluation Criteria in Solid Tumors (RECIST) Yield a More Accurate Prognoses Than the RECIST 1.1 in Hepatocellular Carcinoma Treated with Transarterial Radioembolization. Gut Liver. 2020;14(6):765–774. doi: 10.5009/ gnl19197.
- Seyal AR, Gonzalez-Guindalini FD, Arslanoglu A, et al. Reproducibility of mRECIST in assessing response to transarterial radioembolization therapy in hepatocellular carcinoma. Hepatol Baltim Md. 2015;62(4):1111–1121. doi: 10.1002/hep.27915.
- Riaz A, Kulik L, Lewandowski RJ, et al. Radiologic-pathologic correlation of hepatocellular carcinoma treated with internal radiation using yttrium-90 microspheres. Hepatol Baltim Md. 2009;49(4):1185–1193. doi: 10.1002/hep.22747.