Liens d’intérêts
Aucun
Mots-clés
Coloscopie, cancer colorectal, polypes coliques, polypectomie, surveillance
Abréviations
- FIT : test immunologique de recherche d’hémoglobine dans les selles
- CCR : cancer colorectal
- DOCCR : dépistage organisé du cancer colorectal
Introduction
En 2013, la HAS avait associé le Conseil National Professionnel (CNP-HGE) et la Fédération des Spécialistes des Maladies de l’Appareil Digestif (FSMAD) pour définir les modalités de surveillance après polypectomie colique, sur la base de recommandations internationales alors en vigueur et d’une revue de la littérature (1).
La plupart de recommandations internationales émanant des sociétés savantes ont depuis été actualisées (2, 3, 4). Ces actualisations tiennent compte de publications récentes consacrées au risque de néoplasie avancée métachrone après la réalisation d’une coloscopie. Les recommandations publiées en 2021 par la SFED sous l’égide du CNP-HGE (5) correspondent à l’adaptation pour la France, des recommandations européennes établies en 2020 par l’ESGE (2). Les modifications principales concernent les définitions des niveaux de risque de cancer colorectal (CCR) après polypectomie ainsi que les modalités de suivi. Elles intègrent par ailleurs dans la stratégie de surveillance une consultation spécialisée de prévention ainsi que le test immunologique de recherche d’hémoglobine dans les selles (FIT) pour certains patients ayant un faible niveau de risque de CCR après polypectomie. En effet, la SFED et le CNP-HGE ont estimé que certaines recommandations proposées par l’ESGE n’étaient pas transposables directement en France car l’organisation du dépistage organisé du cancer colorectal (DOCCR) y est moins performante que celle mise en place dans la plupart des pays européens. Cette consultation spécialisée de prévention réalisée 5 ans après la coloscopie permet au gastroentérologue d’évaluer les comorbidités et l’espérance de vie du patient et de déterminer les modalités ultérieures de suivi, en fonction de la qualité du programme de DOCCR local et du choix du patient. Le gastroentérologue peut ainsi proposer soit un contrôle par coloscopie, soit un dépistage par le FIT en fonction de la balance bénéfice/risque de chaque attitude.
Objectif des recommandations
Le but des recommandations est d’élaborer un suivi approprié des patients après une coloscopie de référence, afin de trouver un équilibre entre le risque de développement ultérieur d’une néoplasie et la charge de travail, le coût de la coloscopie et ses complications potentielles. Elles visent à orienter les ressources consacrées à la surveillance vers les patients présentant un risque accru de développer une néoplasie avancée après une polypectomie, tout en allégeant de surveillance des patients à faible risque. L’objectif est d’aider la profession à améliorer la qualité des pratiques. Ces recommandations sont complémentaires et indissociables des recommandations sur les critères de qualité de la coloscopie publiés en 2019 (6). Rappelons que l’objectif ultime de la surveillance après une polypectomie colique est de réduire l’incidence et la mortalité du CCR.
Définition des niveaux de risque de néoplasie avancée métachrone après l’ablation de polypes coliques
Dans cette actualisation des recommandations, le risque de néoplasie avancée métachrone après l’ablation de polypes coliques est stratifié en fonction de la taille, de l’histologie et du nombre de polypes réséqués.
Nous ne reprendrons pas tout l’argumentaire qui a permis d’étayer les recommandations de la SFED et du CNP que le lecteur pourra consulter dans le texte publié (5). Une méta-analyse récente postérieure à la rédaction de ces recommandations est venue renforcer cet argumentaire (7). Cette méta-analyse portait sur 12 études ayant inclus plus de 500 000 patients avec une durée moyenne du suivi de 8,5 ans ; les auteurs ont montré que le risque de CCR métachrone et la mortalité liée au CCR étaient significativement plus élevés chez les patients ayant des adénomes à haut risque, et que ce risque était comparable chez les patients avec des adénomes à faible risque et les patients ne présentant pas d’adénomes (tableau 1). Les auteurs de cette méta-analyse concluaient que les modalités de suivi des patients ayant des adénomes à faible risque devaient être identiques à celles des patients sans adénomes.
La SFED et le CNP-HGE ont retenu les critères suivants pour définir les niveaux de risque de CCR après polypectomie : Les sujets ayant un niveau de risque élevé sont ceux qui ont subi l’exérèse :
- de 5 adénomes ou plus ;
- d’au moins un adénome de taille supérieure ou égale à 10 mm ou en dysplasie de haut grade (y compris pTis) ;
- d’au moins un polype festonné de taille supérieure ou égale à 10 mm ou comportant des lésions de dysplasie (y compris polype hyperplasique).
Les sujets ayant un niveau de risque faible sont ceux qui ont subi l’exérèse :
- de moins de 5 adénomes, tous de taille < 10 mm et en dysplasie de bas grade ;
- d’un ou de plusieurs polype(s) festonné(s), tous de taille inférieure à 10 mm et ne comportant pas de dysplasie.
Synthèse des recommandations de la SFED et du CNP-HGE
Ces recommandations concernent tous les patients chez lesquels un ou plusieurs polypes ont été traités par une résection complète lors d’une coloscopie initiale de haute qualité. Si la coloscopie initiale n’était pas de qualité, la réalisation d’une nouvelle coloscopie dans un délai maximal d’un an est recommandée pour assurer une exploration optimale de la muqueuse colique et permettre l’exérèse des polypes qui n’auraient pas été détectés lors du premier examen.
Pour rappel, une coloscopie de haute qualité est une coloscopie :
- complète jusqu’au cæcum (≥ 90 % des cas) ;
- avec une préparation adéquate (Boston ≥ 7 dans ≥ 90 % des cas) ;
- avec résection complète de tous les polypes ;
- avec un taux de détection des adénomes ≥ 25 % lorsqu’il est mesuré à partir de toutes les coloscopies ou ≥ 45 % pour les coloscopies réalisées pour un test immunologique de recherche de sang dans les selles positif.
En cas de découverte de polypes lors d’une coloscopie, il est suggéré que l’endoscopiste et l’anatomo-pathologistes utilisent une méthode standardisée pour apprécier la taille des polypes et que celle-ci soit évaluée par rapport à une référence.
Modalités d’information des patients sur la programmation de la surveillance
Il est recommandé de fournir au patient un document écrit mentionnant le délai préconisé pour la coloscopie de contrôle. Étant donné que l’analyse histologique d’un polype n’a pas lieu le même jour que la polypectomie, l’endoscopiste doit tracer cette information dans le dossier du patient et le cas échéant, compléter et/ ou finaliser son compte-rendu de coloscopie après avoir reçu le compte-rendu de l’examen anatomo-pathologique. Il doit également en informer le patient par tout moyen disponible. Cette information écrite doit mentionner l’intervalle de surveillance approprié selon les caractéristiques endoscopiques et histologiques des polypes et les facteurs liés au patient. Tout écart par rapport aux recommandations standard doit être dûment mentionné et expliqué dans le compte-rendu.

Tableau 1 : Incidence et mortalité du CCR en fonction des résultats de la coloscopie index – Méta-analyse de Duvvuri et al. (7)
Définition des intervalles pour la coloscopie de contrôle post-polypectomie
Deux niveaux de risque pour l’incidence et la mortalité du CCR après polypectomie sont définis : le risque élevé et le risque faible. Le caractère villeux ou tubulo-villeux d’un polype ne modifie en rien son mode de surveillance, seuls la taille et le degré de dysplasie sont pris en compte. Intervalles de surveillance chez les sujets ayant un niveau de risque élevé de CCR après polypectomie (Figure 1)
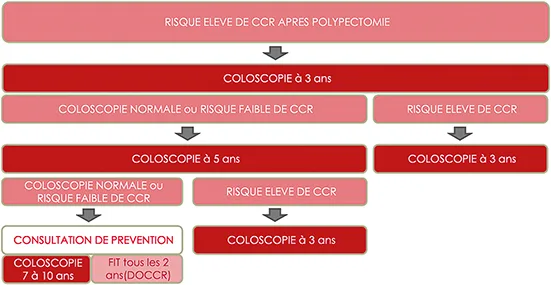
Chez les sujets ayant un niveau de risque élevé de CCR après polypectomie, il est recommandé de réaliser une première coloscopie de contrôle à 3 ans. Lorsque la première coloscopie de contrôle ne détecte pas de polype conférant un risque élevé de CCR, il est recommandé de réaliser une deuxième coloscopie de contrôle à 5 ans. Lorsque cette deuxième coloscopie ne montre que des polypes conférant un risque faible de CCR et a fortiori aucun polype, il est recommandé que le patient soit vu par le gastroentérologue lors d’une consultation de prévention personnalisée, à l’issue de laquelle il proposera, de manière concertée, soit la réalisation d’une troisième coloscopie entre 7 à 10 ans, soit la poursuite du dépistage par FIT tous les deux ans à partir de 5 ans.
Intervalles de surveillance chez les sujets ayant un niveau de risque faible de CCR après polypectomie (Figure 2)
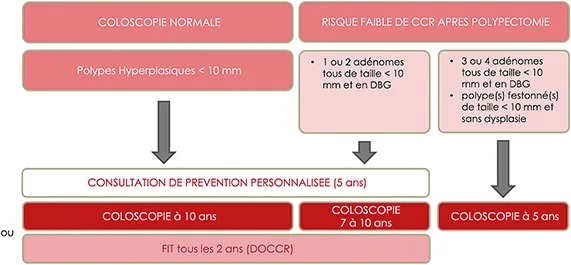
En cas de résection complète de 3 ou 4 adénomes de moins de 10 mm en dysplasie de bas grade, ou d’un ou de plusieurs polypes festonnés de moins de 10 mm sans dysplasie, il est recommandé de réaliser un contrôle par coloscopie à 5 ans.
En cas de résection complète de 1 ou 2 adénomes de moins de 10 mm en dysplasie de bas grade, il est recommandé que le patient soit revu par le gastroentérologue au bout de 5 ans lors d’une consultation de prévention personnalisée, à l’issue de laquelle sera proposée la réalisation d’une coloscopie entre 7 à 10 ans ou la poursuite du dépistage par FIT tous les 2 ans.
Chez les patients ayant une coloscopie normale ou des polypes hyperplasiques de moins de 10 mm, il est recommandé que le patient soit revu par le gastroentérologue au bout de 5 ans lors d’une consultation de prévention personnalisée, à l’issue de laquelle sera proposée la réalisation d’une coloscopie à 10 ans ou la poursuite du dépistage par FIT tous les 2 ans.
NB : Si les polypes hyperplasiques du rectosigmoïde de taille < 10 mm ne doivent pas être surveillés, les polypes hyperplasiques du côlon droit peuvent correspondre à des adénomes festonnés, ce qui doit conduire à proposer une double lecture anatomopathologique en raison d’une grande variabilité inter-observateur du diagnostic.

Figure 1 : Intervalles de surveillance chez les sujets ayant un niveau de risque élevé de CCR après polypectomie

Figure 2 : Intervalles de surveillance chez les sujets ayant un niveau de risque faible de CCR après polypectomie
Cas particuliers
Suivi après exérèse d’un polype colorectal en plusieurs fragments
Chez les patients ayant eu une exérèse endoscopique macroscopiquement complète en plusieurs fragments d’un polype ≥ 20 mm non dégénéré, il est recommandé de réaliser une coloscopie de contrôle entre 3 à 6 mois, puis 12 mois après cette coloscopie pour détecter une récidive tardive.
L’exérèse endoscopique en plusieurs fragments de polypes de moins de 20 mm doit être évitée. Toutefois, en cas d’exérèse endoscopique macroscopiquement complète, un contrôle endoscopique précoce peut se discuter pour les polypes d’exérèse complexe.
Lors du suivi endoscopique, Il est recommandé d’évaluer le site d’exérèse au moyen d’une technique d’imagerie avancée (endoscope haute définition, chromoendoscopie) pour détecter une récidive sans avoir recours de façon systématique à des biopsies de la cicatrice post-exérèse.
En cas d’exérèse macroscopiquement incomplète, en dehors d’un cancer, il est recommandé de référer le patient à un centre expert avec des photos du polype.
Suivi après exérèse chirurgicale/endoscopique à visée curative d’un cancer colorectal « sporadique »
Chez les patients ayant eu une exérèse chirurgicale à visée curative d’un cancer colorectal, il est recommandé une surveillance par coloscopie selon
le schéma suivant :
- une coloscopie péri-opératoire de bonne qualité dans les 6 mois suivant la chirurgie en l’absence de coloscopie totale de bonne qualité avant la chirurgie colorectale ;
- une première coloscopie de contrôle 1 an après la chirurgie pour le cancer colorectal ; une deuxième coloscopie de contrôle 3 ans plus tard, et une troisième 5 ans après la deuxième ;
- si de nouveaux polypes sont détectés lors des coloscopies de contrôle, des intervalles de surveillance plus courts peuvent être envisagés (coloscopie de contrôle à 3 ans en cas de polype(s) ≥ 10 mm ou en dysplasie de haut grade, ou de 5 adénomes ou plus, ou de tout polype festonné ≥ 10 mm ou avec dysplasie).
Il n’est pas recommandé de stratégie de surveillance endoscopique plus « intensive », par exemple, par une coloscopie annuelle, faute de bénéfice démontré.
La surveillance post-chirurgicale par coloscopie doit être suspendue dès que l’espérance de vie du patient est limitée du fait de son âge et/ou de comorbidités (à discuter au cas par cas).
Chez les patients pris en charge pour un cancer colorectal pT1 à faible risque de récidive ou d’envahissement ganglionnaire** traité par exérèse endoscopique avec une résection R0 à visée curative et discuté en RCP dédiée aux cancers superficiels du tube digestif, il est proposé le même schéma de surveillance par coloscopie que pour un cancer colorectal traité par exérèse chirurgicale à visée curative.
En cas de cancer colorectal pT1 à risque élevé de récidive locale ou d’envahissement ganglionnaire**, la stratégie de prise en charge doit être discutée et proposée en RCP dédiée aux cancers superficiels du tube digestif.
Antécédents familiaux d’adénome avancé ou de cancer colorectal (hors syndrome de prédisposition génétique au cancer colorectal)
Il est recommandé de ne pas de raccourcir les intervalles entre les coloscopies de surveillance post-polypectomie chez les patients ayant des antécédents familiaux de cancer colorectal quel que soit l’âge du cas index.
Sujets âgés
Il est recommandé de suspendre la surveillance dès que l’espérance de vie du patient est limitée du fait de son âge et/ou de comorbidités (à discuter au cas par cas).
Recours au test de recherche d’un saignement occulte dans les selles en dehors des recommandations de dépistage et de surveillance du cancer colorectal
Dans le cas d’un test immunologique de recherche sang occulte fécal positif non planifié, il est proposé une coloscopie, y compris entre deux coloscopies de contrôle.
Symptôme(s) clinique(s), anomalie(s) biologique(s) et/ou radiologique(s) susceptibles d’orienter vers une pathologie digestive dans un intervalle de surveillance par coloscopie.
En cas de symptôme(s) clinique(s), d’anomalie(s) biologique(s) et/ou radiologique(s) susceptible(s) d’orienter vers une pathologie digestive dans un intervalle de surveillance par coloscopie, le patient doit être pris en charge selon une démarche diagnostique conforme aux pratiques standards.
Conclusion
Cette actualisation des recommandations de suivi après polypectomie colique, publiée en septembre 2021, se substitue au protocole publié par la HAS en 2013. Ces nouvelles recommandations ne sont pas rétroactives. Elles tiennent compte des données récentes de la littérature qui individualisent deux niveaux de risque de CCR métachrone après la résection de polypes : le risque faible et le risque élevé. Les patients appartenant au premier groupe ont un risque de survenue d’un CCR et de mortalité qui est proche de celui de patients qui n’ont pas de polypes. Des études ont démontré qu’il y a une surutilisation de la coloscopie de surveillance après la résection de polypes à faible risque et une sous-utilisation en cas de résection de polypes à risque élevé. Il est donc crucial de différencier les patients à risque élevé nécessitant une surveillance intensive des patients à faible risque. Ces nouvelles recommandations devraient permettre de réorienter les ressources vers une surveillance soutenue des patients à risque élevé. Elles introduisent la consultation spécialisée de prévention qui replace le gastroentérologue au centre de la stratégie de prévention en orientant les patients à faible risque vers le dépistage organisé par FIT ou la poursuite d’une surveillance endoscopique. La décision est laissée à l’appréciation du gastroentérologue dans le cadre du colloque singulier avec son patient. Le suivi par coloscopie des sujets à haut risque et le dépistage organisé du CCR par le FIT sont complémentaires et ne doivent pas être opposés. Une réorganisation profonde de l’organisation et du pilotage institutionnel du dépistage organisé du CCR est toutefois urgente aux vues des faibles taux de participation enregistrés en France que la crise sanitaire a majorés.
Références
- Protocole de Surveillance Post Polypectomie (H.A.S.)
- Hassan C, Antonelli G, Dumonceau JM, Regula J, Bretthauer M, Chaussade S, et al. Post-polypectomy colonoscopy surveillance: European Society of Gastrointestinal Endoscopy (ESGE) Guideline – Update 2020. Endoscopy. 2020 Aug;52(8):687-700. doi: 10.1055/a-1185-3109. Epub 2020 Jun 22. PMID: 32572858
- Gupta S, Lieberman D, Anderson JC, Burke CA, Dominitz JA, Kaltenbach T, et al. Recommendations for Follow-Up After Colonoscopy and Polypectomy: A Consensus Update by the US Multi-Society Task Force on Colorectal Cancer. Gastrointest Endosc. 2020 Mar;91(3):463-485.e5. doi: 10.1016/j.gie.2020.01.014. Epub 2020 Feb 7. PMID: 32044106
- Rutter MD, East J, Rees CJ, Cripps N, Docherty J, Dolwani S, et al. British Society of Gastroenterology/Association of Coloproctology of Great Britain and Ireland/Public Health England post-polypectomy and post-colorectal cancer resection surveillance guidelines. Gut. 2020 Feb;69(2):201- 223. doi: 10.1136/gutjnl-2019-319858. Epub 2019 Nov 27. PMID: 31776230
- Robaszkiewicz M, Rahmi G, Lecomte T, Denis B, Vaillant E, Gronier O, et al., et les membres du groupe de travail. Modalités de surveillance après polypectomie colique. Hépato-Gastro et Oncologie Digestive 2021;28:805-816. doi: 10.1684/hpg.2021.2218
- Lapuelle J, Bernardini D, Robaszkiewicz M, Chaussade S. Critères de qualité de la coloscopie – Recommandations du CNP-HGE et de la SFED. Hépato-Gastro et Oncologie Digestive 2019;26:15-28. doi: 10.1684/hpg.2018.1731
- Duvvuri A, Chandrasekar VT, Srinivasan S, Narimiti A, Dasari C, Nutalapati V, et al. Risk of Colorectal Cancer and Cancer Related Mortality After Detection of Low-risk or High-risk Adenomas, Compared With No Adenoma, at Index Colonoscopy: A Systematic Review and Meta-analysis. Gastroenterology.2021 May;160(6):1986-1996.e3. doi:10.1053/j.gastro.2021.01.214. Epub 2021 Jan 29. PMID: 33524401
** facteurs de risque de récidive ou d’envahissement ganglionnaire des CCR pT1 : envahissement en profondeur ≥ 1 000 microns ; faible différenciation tumorale ; présence d’emboles vasculaires ou lymphatiques ; présence de budding 2 ou 3 ; tranche de section envahie ou non évaluable.