LIEN D’INTÉRÊTS
Absence de conflit d’intérêt dans cette thématique
MOTS-CLÉS
Rectite post-radique, Coagulation par Plasma Argon, Formaline
ABRÉVIATIONS
RT : radiothérapie
RPRC : rectite post-radique chronique CPA : coagulation au plasma d’argon OHB : oxygénothérapie hyperbare ARF : ablation par radiofréquence
Introduction et position du problème
La radiothérapie (RT) occupe une place importante dans le traitement des cancers pelviens (prostate, utérus, vessie, rectum et canal anal), avec en France 80 000 nouveaux cas par an, dont 50 000 pour un adénocarcinome de prostate. Le rectum est particulièrement exposé aux complications de cette irradiation en raison de sa position fixe dans le pelvis. La rectite post radique se définit comme des lésions chroniques de la muqueuse et de la sous muqueuse du rectum secondaire aux radiations ionisantes. Parmi les complications possibles, les rectites hémorragiques sont les plus fréquentes, à côté des troubles fonctionnels ano-rectaux dont des phénomènes dyschésiques souvent associés et parfois une altération de la continence fécale.
Les rectites radiques évoluent en deux temps : précoces ou aiguës, très fréquentes mais qui régressent spontanément en quelques semaines et surtout tardives ou rectite post-radique chronique (RPRC). Les progrès de l’optimisation des paramètres de la RT ont permis une diminution de la prévalence des RPRC, mais leur survenue reste invalidante et leur prise en charge peut s’avérer complexe (Bauer 2015, Horaist 2017, Ferini 2021).
Physiopathologie, facteurs de risques et moyens de préventions
Physiopathologie
Les radiations ionisantes sont responsables de dommages cellulaires, d’autant plus importants que les tissus ont un renouvellement rapide comme la muqueuse intestinale. Les lésions de rectite aiguës consistent en une disparition cellulaire par une cytotoxicité sur les cellules souches et par conséquence un mécanisme d’apoptose, une infiltration inflammatoire de la lamina propria, avec présence de leucocytes, formation de micro- abcès cryptiques à éosinophiles, altération de la micro-vascularisation par atteintes des cellules endothéliales et un œdème de la sous-muqueuse.
Cette inflammation de la muqueuse rectale altère la fonction de barrière intestinale, autorisant des translocations antigéniques, incluant des microorganismes. Si les lésions muqueuses restent modérées, les cellules épithéliales régénèrent spontanément et le processus disparaît en restituant ad integrum une muqueuse digestive normale (Kintzinger 2012, Costa 2021).
La physiopathologie des RPRC repose sur des lésions plus tardives, dont le mécanisme physiologique n’est pas complétement élucidé, mais qui affecte avant tout la microvascularisation. Le stress oxydatif via les dérivés réactifs de l’oxygène induit une endartérite oblitérante par un phénomène d’apoptose des cellules endothéliales de la crypte intestinale. Cette réduction progressive de la micro-vascularisation de la paroi intestinale est responsable d’une ischémie locale, formation et diffusion d’une fibrose muqueuse et sous muqueuse via une cascade de cytokynes pro-inflammatoires (IL-1béta, IL-2, IL -6, IL-8 et TGF-béta), favorisée par les macrophages et par la différentiation des fibroblastes en myofibroblastes. Ce processus pathologique de régénération transmural accentue la dévascularisation, la déplétion cellulaire et l’atrophie muqueuse, puis une angiogénèse anormale formant une néo-vascularisation superficielle ou télangiectasies à l’origine des saignements. Ce processus ischémique entraîne également une rigidité de la paroi anorectale, qui couplée à une atteinte des plexus myentériques, peut altérer les fonctions d’exonération et de continence. Il peut entraîner le cas échéant des phénomènes de sténoses, d’ulcérations et quelquefois de perforation ou de fistule. Plusieurs études récentes suggèrent une modification du microbiote intestinal induite par la RT, avec une dysbiose « pro-inflammatoire » susceptible d’accroître ces lésions radiques (Kumagai 2018). Ces altérations chroniques peuvent se stabiliser, partiellement régresser ou au contraire progressivement s’aggraver avec une physiopathologie complexe non complétement élucidée (Kintzinger 2012, Hauer-Jensen 2014, Costa 2021).
Facteurs de risque
Les facteurs de risque de survenue ou de sévérité d’une RPRC peuvent être liés aux traitements ou au patient. Les modalités de la RT sont clairement les facteurs prépondérants, associant la dose totale délivrée, le volume total de rectum irradié, la dose par fraction, le mode de radiothérapie (externe et/ou curiethérapie) et l’association à une chimiothérapie concomitante (RR=3,5) (Hernandez Moreno 2015). Moins bien définis, les facteurs aggravants liés au patient pourraient être un diabète (RR=1,64), une MICI, un antécédent de chirurgie abdominale, un tabagisme, la carence en vit D, l’artériosclérose, l’hypertension artérielle, ainsi qu’un indice de poids corporel bas, un âge > 70 ans (West 2011, Ali 2020, Costa 2021). Plus récemment, le développement récent de la radiogénomique a mis en évidence des variations génétiques individuelles susceptibles d’augmenter la toxicité de la radiothérapie, mais il n’existe encore pas de test prédictif qui permettrait d’adapter le protocole de radiothérapie à un patient donné pour limiter cette radio-toxicité (Brothwel 2019, Kerns 2020)
Moyens de prévention
La prévention repose avant tout sur une optimisation des paramètres de la radiothérapie. La radiothérapie conformationnelle en modulation d’intensité permet d’être plus précis sur les tissus cibles et de réduire la dose délivrée sur les tissus sains adjacents comme le rectum. En association, le recours à la radiothérapie guidée par l’image permet une parfaite reproductibilité du positionnement du patient afin de rester optimal dans la délivrance des rayons. Grâce à ces avancées techniques, la diminution des RPRC pourrait atteindre 50 % (OR 0,54) dans certaines études récentes, résultats qui ne sont cependant pas tous homogènes (Hama 2018, Ferini 2021). L’intérêt de la curiethérapie mérite d’être réévaluée au vu de ces nouvelles modalités de la RT.
De multiples études, contrôlées ou non, ont tenté d’évaluer l’intérêt préventif de divers médicaments administrés souvent localement en cours de RT pour diminuer la toxicité précoce ou tardive de la RT pelvienne, comme le misoprostol, le sucralfate, la corticothérapie, l’acide hyaluronique, la glutamine, les dérivés salicylés ou les probiotiques, avec des résultats discordants. Deux études contrôlées récentes suggèrent une protection partielle de l’aloe vera ou d’une prise orale d’un symbiotique (Sahebnasagh 2020, Nascimento 2020). L’utilisation de l’amifostine, prodrogue probablement la plus étudiée pour son efficacité radioprotectrice et validée par la FDA depuis plus de 20 ans, a toujours été limitée en raison de ses effets secondaires et son bénéfice-risque doit être réévalué au vu des progrès actuel de la RT. À ce jour, aucune molécule utilisée en cours de RT ne fait l’objet de recommandation et n’est utilisée en pratique courante pour la prévention des RPRC (Lawrie 2018, Paquette 2018, Ferini 2021). Une injection par voie transpérinéale d’un hydrogel dans la partie antérieure du mésorectum a récemment été proposée pour éloigner le rectum de la zone irradiée. L’intérêt de cette technique interventionnelle plus invasive est actuellement en cours d’évaluation. Elle pourrait réduire de 77 % les RPRC dans une méta analyse récente (Miller 2020).
Diagnostic clinique et endoscopique des rectites post-radiques
Rectites post-radiques précoces
Les rectites post-radiques précoces ou aiguës se manifestent pendant la RT et jusque quatre semaines après son arrêt. Elles concernent 30 à 50 % des patients. Le diagnostic est clinique à l’interrogatoire et le contexte de RT en cours ou très récente ne justifie habituellement aucune investigation complémentaire. Le mécanisme correspond à une diminution du renouvellement de la muqueuse pendant l’irradiation conduisant à des érosions muqueuses suffisantes pour conduire à une défaillance fonctionnelle transitoire. Cliniquement, elles se caractérisent par un syndrome rectal et des douleurs, avec ou sans rectorragies. Les lésions histologiques sont surtout muqueuses superficielles, associant érythème, œdème ou micro-ulcérations et perte des microvillosités, avec un aspect endoscopique peu spécifique. Elles régressent spontanément en quelques semaines sans séquelle et une toxicité aiguë sévère est estimée à moins de 5 % (Kintzinger 2012, Nelamangala 2016). La survenue d’une rectite radique précoce sévère, avec des lésions endoscopiques marquées, est un facteur indépendant exposant 5 fois plus les patients au risque de développer une RPRC (Campostrini 2013).
Rectites post-radiques tardives
Les RPRC ou tardives s’installent progressivement à distance de l’arrêt de la RT, à partir du 6e mois et jusqu’au 24e mois, rarement plus tardivement, et évoluent de façon chronique. Elle concernait classiquement jusque 30 % des patients, mais ces chiffres historiques élevés ont beaucoup diminué en raison de l’optimisation actuelle de la RT. Son incidence réelle est difficile à établir, mais les études récentes suggèrent plutôt la nécessité d’une prise en charge thérapeutique secondaire sur une fourchette de 2 à 5 % des patients ayant bénéficié d’une RT pelvienne (Nelamangala 2016, Hama 2018, Ferini 2021, Paquette 2018).
Les rectorragies sont les symptômes les plus fréquents de ces RPRC, d’intensité très variable, pouvant conduire à une carence en fer et à une anémie. Elles sont souvent associées à l’émission de glaires, une augmentation de la fréquence des selles, des douleurs et quelquefois à un véritable syndrome rectal invalidant avec émissions nombreuses, souvent afécales, ténesmes et faux besoins. Des troubles de la continence anale sont alors souvent présents. D’autres complications post-radiques plus rares peuvent survenir comme une anodermite radique sévère de la marge et du canal anal, une béance anale ou au contraire une sténose ano-rectale, des ulcérations ano-rectales profondes parfois nécrosantes, des fistules ano-recto-génito- urinaires dont l’orifice ano-rectal est souvent situé au fond d’une ulcération, ou une atteinte des organes pelviens de voisinage. En présence de ces complications sévères post-radiques, la principale crainte doit être la persistance ou la récidive du cancer, diagnostic souvent difficile à affirmer en raison de tissus radiques très remaniés, d’une imagerie d’interprétation difficile et de biopsies potentiellement dangereuses. L’examen clinique pelvi- périnéal permet un bilan lésionnel précis et exhaustif. L’examen proctologique, incluant une anuscopie, apprécie au plus juste la localisation des lésions par rapport à la ligne pectinée et du tissu hémorroïdaire interne (figure 1), ce qui peut conditionner les choix thérapeutiques ultérieurs (Bauer 2015, Horaist 2017).

Figure 1 : Rectite post radique débutant au niveau du canal anal
Diagnostic endoscopique et scores
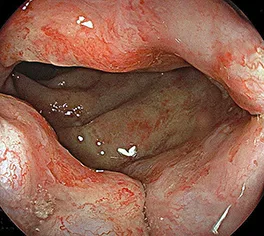
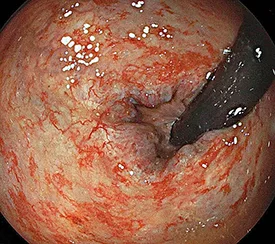
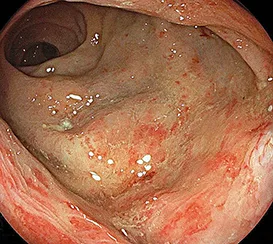
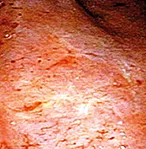
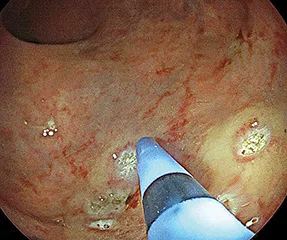
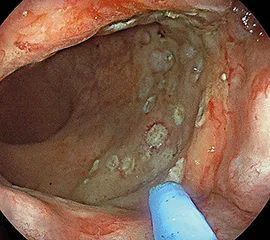
La recto-sigmoïdoscopie est l’examen qui permet d’affirmer le diagnostic de RPRC hémorragique. L’aspect endoscopique caractéristique inclut la présence de télangiectasies sur une muqueuse atrophique pâle et dépolie (figures 2 et 3), plus rarement une muqueuse uniformément congestive, friable et hémorragique au moindre contact (figure 4), siège quelquefois d’ulcérations rectales planes ou plus creusantes. Sur le plan anatomo-pathologique, l’épithélium est atrophique et érodé, le tissu congestif œdématié riche en fibroblastes. Les vaisseaux sont caractérisés par des capillaires dilatés, des veines thrombosées et surtout une endartérite oblitérante. Devant un contexte post-radiothérapique, les constatations endoscopiques caractéristiques sont les plus souvent suffisantes pour retenir le diagnostic et les biopsies doivent rester prudentes en raison d’exceptionnelles complications fistuleuses qui ont pu être rapportées (Bauer 2015, Horaist 2017).


Figures 2 et 3 : Rectite post radique chronique avec télangiectasies sur muqueuse pâle atrophique

Figure 4 : Rectite post radique uniformément congestive, fiable et hémorragique
Parmi les scores proposés dans le but d’homogénéiser la description des RPRC, le « Vienna Rectoscopy Score (VRS) est le plus utilisé (tableau 1) (Goldner 2007, Krol 2014). Le VRS divise la muqueuse rectale en 12 zones, avec des scores évaluant dans chacune d’elles les télangiectasies, la congestion muqueuse, la présence d’ulcérations, de sténose ou de nécrose. Les télangiectasies et la congestion muqueuse sont les constations endoscopiques les plus fréquentes, avec respectivement une prévalence de 73 % et 33 %. Les ulcérations sont présentes dans moins de 4% des cas et les sténoses ou les nécroses encore moins fréquentes. Ces lésions muqueuses post-radiques prédominent logiquement sur la face antérieure du rectum. Très rarement présentes à 3 mois sur des études endoscopiques prospectives, ces modifications de la muqueuse surviennent avec un pic entre un et deux ans après l’arrêt de la radiothérapie. Très à distance, ces lésions peuvent aussi spontanément régresser, avec à 5 ans globalement une disparition de celles-ci chez un tiers des patients et une simple amélioration chez un autre tiers (Krol 2014). Dans ces études, l’intensité des rectorragies semblent plus corrélées à l’importance des télangiectasies qu’une muqueuse congestive ou ulcérée.
Diagnostic différentiel
La question du diagnostic différentiel sur la nature des lésions est rarement posée devant l’aspect endoscopique souvent très évocateur des lésions rectales associé au contexte connu de radiothérapie pelvienne. Cependant une coloscopie est toujours indiquée lors du diagnostic initial et peut être réalisée de première intention en substitution de la rectosigmoïdoscopie car il convient d’écarter une autre source de saignement, même en présence d’une RPRC avérée. Cette possibilité avait été évaluée à 44 % des patients dans une étude prospective déjà ancienne. De même, des troubles digestifs d’allure fonctionnelle ne doivent pas être systématiquement imputés de prime abord à l’irradiation (Williams, 2005, Min 2014).
Traitement des RPRC
Indications d’un traitement
L’objectif de la prise en charge des RPRC est de contrôler les symptômes invalidants, en premier lieu les rectorragies. Celles-ci doivent être traitées si elles sont responsables d’une carence en fer significative ou d’une anémie ou si elles participent activement au syndrome rectal. L’objectif n’est pas la disparition de tout saignement, en particulier pauci-symptomatique, ce qu’il faut bien expliquer au patient (Bauer 2015, Paquette 2018). Avant de faire le choix d’un traitement, il est important de préciser les caractères de l’atteinte rectale : télangiectasies isolées ou confluentes, zones de muqueuse congestive et fragile, atteinte diffuse ou localisée, ainsi que son étendue et son siège, en particulier par rapport à la ligne pectinée. Il est également important de rechercher d’éventuelles lésions radiques associées en amont du rectum, volontiers en rapport avec la topographie du champ d’irradiation initial. Les options thérapeutiques sont multiples, médicales en nombre très limité et au bénéfice aléatoire, endoscopiques plus efficaces mais ne ciblant que les manifestations hémorragiques de la RPRC et physiques par l’application de formaline ou l’oxygénothérapie hyperbare. Le recours à la chirurgie dans ce contexte est exceptionnel dans des situations d’impasse thérapeutique.
Traitement médicaux
Les traitements médicaux ne s’adressent qu’aux manifestations fonctionnelles modérées, mais très peu ont fait l’objet d’études contrôlées.
Le sucralfate
Le sucralfate, sel d’aluminium qui a un effet cytoprotecteur en adhérant à la muqueuse rectale, est administré par lavement à la posologie de 2 g matin et soir, dans 4,5 ml ou 20 ml d’eau. Proposé depuis 1991 sur les saignements des RPRC modérées, il a fait l’objet de 3 études contrôlées, mais jamais contre placebo. Elles suggèrent globalement une diminution des saignements chez plus de 2/3 des patients, et la combinaison de deux études prospectives aboutit à un odd ratio favorable de 1,67 (Hanson 2012). Du fait de son innocuité et bien que sans AMM en France pour cette indication, il peut être proposé dans les manifestations cliniques modérées. Dans les recommandations américaines récentes, le sucralfate est la seule thérapeutique médicamenteuse qui soit préconisée, recommandation forte 1C avec un très faible niveau de preuve (Paquette 2018).
Les autres traitements médicaux ne font l’objet d’aucune recommandation
Plusieurs molécules en topique ou par voie orale pourraient avoir un effet bénéfique modéré sur les rectorragies et les symptômes fonctionnels (Bauer 2015, Grodsky 2015, Weiner 2016, Ferini 2021). Les dérivés salicylés per os et/ou en suppositoire améliorent les saignements dans une étude ouverte, mais ce bénéfice modeste mériterait d’être confirmé dans une étude prospective contrôlée contre placebo. Les corticoïdes administrés en topiques n’ont pas d’efficacité clairement établie, alors même que l’hydrocortisone (mousse Colofoam*) possède une AMM en France dans cette indication. Les résultats des études contrôlées concernant les acides gras à chaînes courtes (butyrate) utilisés en lavements sont contradictoires, et son utilisation est complexe en l’absence de préparation commerciale disponible. La vitamine A per os (10 000 UI de rétinol/j pendant 3 mois) améliore les signes fonctionnels des RPRC dans une seule étude prospective contrôlée déjà ancienne. Le métronidazole pourrait avoir un effet bénéfique significatif dans deux études contrôlées mais il n’a été évalué qu’en association avec d’autres thérapeutiques, à court terme et jamais contre placebo. Au total, en l’absence de données plus factuelles, aucune de ces molécules ne fait actuellement l’objet d’une recommandation dans le traitement des RPRC (Paquette 2018, Ali 2020).
Traitements endoscopiques
L’objectif du traitement endoscopique est de contrôler les saignements liés à la RPRC. Il s’adresse aux saignements significatifs qui altèrent la qualité de vie et/ou qui sont responsables d’une anémie devant être compensée. Ces traitements ne sont pas dénués de risques, même si la morbidité reste limitée, justifiant de ne pas traiter les rectorragies mineures sans retentissement.
Coagulation au Plasma d’Argon (CPA)
Proposée depuis 1994 dans le traitement des RPRC, la CPA est devenue ces dernières années la technique de référence du traitement endoscopique des RPRC hémorragiques, plus simple et moins morbide que les techniques plus anciennes comme le laser YAG, l’électrocoagulation bipolaire ou la sonde chauffante dont l’inconvénient majeur est de moins bien contrôler la profondeur de la coagulation (Weiner 2016, Lee 2019). La CPA réalise une coagulation monopolaire, sans contact direct avec le tissu, par le biais de l’argon, gaz inerte non inflammable et non toxique. Le gaz argon sert de conducteur en transmettant l’énergie qui permet la coagulation de la muqueuse. Il est extériorisé à l’extrémité d’un cathéter flexible contenant une électrode de tungstène qui délivre un courant à haute fréquence. La puissance de tir doit être comprise entre 40 et 60 W et le débit du gaz entre 0,6 et 1 l/min, mais le générateur propose le plus souvent un programme dédié déjà réglé pour le traitement des RPRC. L’application pendant une à deux secondes peut se faire point par point en cas de télangiectasies éparses bien individualisées (figures 5 et 6) ou par balayage en présence de lésions conjointes ou de rectite congestive diffuse. Des saignements mal contrôlés en cours de procédure peuvent absorber le courant électrique généré et limiter l’efficacité de la technique. L’intérêt majeur de la technique est de canaliser la coagulation en profondeur en la limitant à 2-3 millimètres, ce qui en réduit la morbidité. Des explosions intra-coliques ont été rapportées lors de simple préparation par lavements, ce qui impose une préparation colique rigoureuse préalable. La procédure endoscopique est le plus souvent réalisée sous anesthésie, en raison d’une part de l’inconfort lié à l’insufflation entraînant volontiers une distension recto-colique qui doit être contrôlée en cours de procédure et d’autre part en cas de lésions proches de la jonction ano-rectale dont le traitement peut être douloureux. Une antibioprophylaxie n’est pas utile dans cette indication car la CPA n’induit pas de bactériémie significative (Horaist 2017). Les autres complications de la CPA rapportées dans la littérature sont plus spécifiques du tissu irradié, plutôt rares car évaluées à 3 %, mais non négligeables par leur gravité, comme des ulcérations secondaires, des nécroses, des fistules ou des sténoses. Leur incidence augmente lorsque les séances sont trop rapprochées et lorsque la puissance et le débit sont augmentés, sans gain évident d’efficacité, d’où découle la recommandation prudente de ne pas dépasser 50 W et 0,8 l/min de débit. La présence d’emblée avant traitement de ces lésions radiques sévères sont de facto une contre-indication de la CPA sur ces sites ulcérés (Weiner 2016, Ali 2020). De nombreuses études regroupant plus de 900 patients, prospectives pour un tiers d’entre elles, montrent sur une analyse groupée un contrôle des saignements dans 87 % des cas, et leur disparition dans 74 % des cas (Weiner 2016, Bauer 2015, Lee 2019). Le nombre moyen de séances est de 2,5 (1-3,7) pour obtenir une efficacité complète. L’intervalle moyen entre deux séances doit être d’au moins 3 à 4 semaines afin de permettre la cicatrisation de la muqueuse. Dans une étude prospective plutôt optimiste, les saignements disparaissaient totalement après une séance chez 68 % des patients et en 2 séances chez 96 % d’entre eux (Swan 2010). Peu d’études rapportent l’efficacité de la CPA sur les RPRC hémorragiques à moyen et long terme. Une étude prospective sur 24 patients confirme l’absence de récidive dans 92 % des cas pour un suivi minimal de 24 mois (24-60), et un essai contrôlé randomisé avec 17 patients dans le bras CPA rapporte une seule récidive sur un suivi moyen de 111 mois (29-170). Ces récidives à distance, plus fréquentes en cas de prise d’un anticoagulant ou d’aspirine, ont toutes été traitées avec succès par une nouvelle séance de CPA (Rotondano 2003, Yeoh 2013). Pour le traitement des RPRC hémorragiques, la CPA fait actuellement l’objet d’une recommandation forte 1 B avec un niveau de preuve modéré par les sociétés américaines de Gastroentérologie et de Chirurgie Colo-Rectale (Paquette 2018, Lee 2019).


Figures 5 et 6 : Traitement des télangiecctasies post radiques par CPA
Ablation par Radiofréquence (ARF)
L’ARF utilise une électrode pour transmettre un courant alternatif de radiofréquence dans les tissus à proximité de l’extrémité de l’électrode. Les ions changent de direction en suivant le courant alternatif, ce qui induit un mouvement qui augmente la chaleur par effet de friction. Lorsque la température atteint les 60°C, les cellules environnantes se nécrosent. L’intérêt de la technique est la possibilité de traiter une large surface par quadrant successif, avec une profondeur de coagulation se limitant à un millimètre de profondeur (Weiner 2016, Mac Carty 2019). L’utilisation de l’ARF pour traiter les RPRC est récente, avec une première étude pilote en 2009. Une étude rétrospective sur 39 patients rapporte une efficacité de 100 % avec un recul de 28 mois, sans morbidité significative et un nombre moyen de séance de 1,5 (1-4) (Rustagi 2015). Une méta-analyse récente regroupant 6 études non comparatives englobant 71 patients dont 38 % en échec de CPA confirme un taux de succès de 99 % sans morbidité significative, obtenu après 1,7 séances en moyenne, mais un suivi limité dans le temps (MacCarty 2019). L’ARF se positionne comme une technique prometteuse en raison de son efficacité remarquable et de sa faible morbidité dans les études publiées, mais en l’absence d’essai contrôlé comparatif avec la CPA, les recommandations demeurent divergentes, positionnant l’ARF à équivalence de la CPA dans le traitement des RPRC pour la Société Américaine d’Endoscopie Digestive (Lee 2019), au contraire de la Société Américaine de Chirurgie Colo-Rectale qui ne se prononce pas (Paquette 2018).
Traitements physiques non endoscopiques
Formaline
La formaline, solution de formaldéhyde à 4 %, mise en contact avec la muqueuse rectale pathologique, induit des lésions superficielles de nécrose de coagulation et thrombose des néo-vaisseaux radiques, avec la survenue secondairement d’une régénération de la muqueuse. Publiée pour la première fois en 1986, le traitement se réalise préférentiellement par tamponnement, soit l’application étagée de compresses imbibées de formaline pendant un temps limité de 2 à 4 minutes, idéalement à travers un écarteur au bloc opératoire. La technique nécessite une à deux séances, rarement trois et requiert un apprentissage spécifique pour en limiter la morbidité. Sur des lésions distales et limitées, l’application de cotons imbibées au travers d’un anuscope ou d’un rectoscope est une alternative possible, simple et peu onéreuse. Les complications potentielles, très diversement rapportées dans la littérature initiale, ont pu limiter la diffusion de la technique. Le risque principal est d’induire des ulcérations anales secondaires si la formaline est au contact de l’épithélium de la marge anale ou du canal anal qui doivent être soigneusement protégés, beaucoup plus rarement celui d’ulcérations rectales, de fistules ou de sténoses. Malgré une efficacité publiée légèrement supérieure, l’application par lavement doit être évitée du fait d’une morbidité du même type plus fréquente et plus sévère, incluant la description de colite aigüe distale ou de nécrose rectale (de Parades 2007). Du fait de ces effets secondaires potentiels, la présence d’emblée lors d’une RPRC d’ulcérations rectales profondes, d’une fistule ou d’une sténose sont une contre-indication au traitement par formaline. Pour la technique de tamponnement, plus de quinze études regroupant plus de 400 patients, dont 3 prospectives, rapportent une efficacité complète ou partielle dans 88 % (70-100) des cas, et un arrêt complet des saignements chez plus de deux patients sur trois (39-100) (Bauer 2015). Lors d’un essai prospectif, les rectorragies ont disparu en une seule séance chez 63 % des patients, en deux séances chez 89,5 % et 100 % après une troisième application, avec un suivi moyen de 12 mois (2-36) (Samalavicius 2013). L’efficacité à moyen et long terme est moins bien évaluée, mais une étude prospective suggère le maintien de ce bénéfice à presque 10 ans de suivi (Yeoh 2013). La formaline fait l’objet d’une recommandation forte 1 B avec un niveau de preuve modéré, au même niveau que la CPA par l’Association Américaine de Chirurgie Colo-Rectale (Paquette 2018), contrairement à l’Association Américaine d’Endoscopie Digestive qui recommande les techniques de coagulation endoscopiques de première intention, en particulier la CPA et l’AFR (Lee 2019). L’argument avancé par cette dernière est un taux de morbidité supérieur de la formaline dans la littérature qui tend à disparaître en excluant la technique par lavement. L’expérience endoscopique exclusive des gastroentérologues, contrairement aux chirurgiens colo-rectaux ou proctologues chirurgicaux qui maîtrisent les deux techniques, participe probablement à ces recommandations contradictoires des deux sociétés savantes.
Alors comment choisir entre CPA ou Formaline ?
L’efficacité de la CPA et de la formaline est comparable, comme l’a démontré un essai prospectif randomisé : 94 % d’efficacité pour la CPA (17 patients) versus 100 % pour la formaline par tamponnements (13 patients), avec paradoxalement des formes plus sévères dans le groupe formaline : 64 % de sujets transfusés versus 31 % de ceux traités par CPA (Yeoh 2013). Le nombre moyen de 2 (1-5) séances nécessaires était comparable, avec un suivi moyen de 111 mois (29-170), soit 9 ans sans récidive à l’exception d’un patient dans chaque groupe. Dans cette étude, la morbidité était comparable, avec davantage d’altérations de la compliance rectale et des volumes de perception dans le bras CPA, ne confirmant pas une morbidité supérieure de la formaline rapportée dans d’autres études, probablement liée à la technique d’application par lavements qu’il convient d’éviter (De Parades 2007, Bauer 2015). Une seconde étude prospective randomisée récente confirme à nouveau une efficacité et une morbidité comparable des deux techniques, avec la réserve d’une évaluation à court et moyen terme plus discutable (Furtado 2021). En pratique, les deux techniques sont probablement plus complémentaires que concurrentielles, même si les données factuelles sont faibles. Il paraît raisonnable de proposer en première intention la CPA en raison de sa facilité de mise en œuvre dans un environnement endoscopique classique. Elle est probablement plus performante sur des lésions télangiectasiques du moyen rectum, et la seule technique utilisable sur le haut rectum et le colon sigmoïde. La formaline, qui nécessite une organisation proctologique opératoire et dont la morbidité reste débattue dans la littérature, est plutôt à réserver aux échecs de la CPA, en particulier s’il y a une nécessité de poursuivre les transfusions (Lee 2019). Toutefois des présentations particulières de RPRC suggèrent de proposer l’application de formaline en première intention car la technique pourrait être plus pertinente et mieux adaptée que la CPA dans ces circonstances. C’est le cas en présence de lésions hémorragiques en zone hémorroïdaire sus-pectinéale immédiate pour laquelle l’exposition endoscopique peut s’avérer difficile, ou en présence d’une rectite diffuse hémorragique au moindre contact, en particulier si la localisation est très distale, l’efficacité de la CPA pouvant être amoindrie sur une muqueuse très hémorragique avec une exposition endoscopique plus difficile (Bauer 2015, Horaist 2017). En complément, le caractère simple et peu onéreux de l’application de formaline est un argument parfois mis en avant pour recommander cette technique en première intention, en particulier lorsque les techniques endoscopiques interventionnelles sont peu accessibles (Ali 2020). Enfin une publication récente suggère la faisabilité une application ciblée de formaline par voie endoscopique (Li 2019).
Oxygénothérapie hyperbare (OHB)
L’OHB repose sur l’inhalation d’oxygène à 100 % dans une pièce hermétique ou caisson hyperbare, le plus souvent à deux atmosphères de pression.
Trente séances d’une demi journée sont habituellement nécessaires, qui peuvent être prolongées. L’objectif est d’induire un effet angiogénique sur les tissus mous et une réparation des dommages endothéliaux, par restauration du gradient de pression en oxygène dans les territoires hypovascularisés et donc de favoriser la cicatrisation des lésions (Costa 2021). Depuis 1991, date du premier cas rapporté dans la littérature de RPRC traitée par OHB, de nombreuses publications non contrôlées, le plus souvent pour des patients en échec des autres thérapeutiques pour une RPRC, rapportent un bénéfice sur les saignements dans 2/3 des cas, avec une efficacité complète dans 25 à 45 % des cas, mais souvent aussi sur les symptômes fonctionnels, en particulier le transit, le syndrome rectal et sur la continence anale (Bauer 2015, Costa 2021). Une étude sur 120 patients, contrôlée randomisée en double aveugle avec cross over et un suivi de 18 mois, a validé factuellement en 2008 l’indication de l’OHB dans les RPRC. Son évaluation concernait aussi bien des critères objectifs avec le LENT-SOMA score (Late Effects Normal Tissue – Subjective Objective Management Analytic) que la qualité de vie qui sont tous deux significativement améliorés sous OHB, la différence disparaissant après le cross over (Clarke 2008). La négativité d’une seconde étude contrôlée randomisée publiée en 2016 (Glover 2016) n’a pas remis fondamentalement en cause l’efficacité de l’OHB sur les RPRC dans une méta-analyse très récente, du fait d’un moindre effectif de patients dans cette dernière étude et de biais potentiels dans l’analyse des résultats (Yuan 2020, Costa 2021). L’OHB dans les RPRC fait toujours l’objet d’une recommandation forte 1B avec un niveau de preuve modéré dans les dernières publications internationales des sociétés scientifiques (Mathieu 2017, Paquette 2018). En pratique, l’OHB peut s’inscrire dans plusieurs stratégies thérapeutiques. Elle paraît tout particulièrement intéressante pour traiter les atteintes radiques hémorragiques simultanées du rectum et de la vessie et/ou les troubles ano-rectaux ou pelvi-périnéaux fonctionnels sévères associés (Bauer 2015). Les bénéfices pourraient être meilleurs si le traitement par OHB est réalisé précocement (Clarke 2008, Yuan 2020) La cicatrisation des ulcérations radiques ano-rectales et des fistules radiques recto-vaginales est moins bien documentée, avec simplement quelques cas rapportés dans la littérature. Les limites de l’OHB sont son accessibilité, ses possibles effets secondaires et la disponibilité nécessaire pour le patient, ce qui en fait souvent une option thérapeutique plus difficile à proposer.
Les RPRC en échec des traitements conventionnels
Quelle place pour la chirurgie ?
Dans un contexte de RPRC hémorragique, la chirurgie peut être exceptionnellement discutée en cas de saignements majeurs, en échec des autres thérapeutiques conservatrices.
La colostomie d’amont
Il est difficile d’anticiper si une colostomie d’amont, qui permet une dérivation du flux fécal, permettra de contrôler les rectorragies. Elle est plus particulièrement indiquée s’il existe des ulcérations profondes ou nécrotiques, avec des risques de perforation, une sténose ou une fistule, circonstances dans lesquelles les patients sont volontiers très symptomatiques et les traitements conservateurs limités ou contre-indiqués à l’exception de l’OHB. Une étude rétrospective comparative sur 47 patients, 22 colostomies transverses d’amont versus 25 traitements conservateurs, rapporte un arrêt des saignements dans 94 % vs. 12 %, avec une amélioration objective de la qualité de vie, en réduisant drastiquement les phénomènes douloureux (Yuan 2016). Le caractère réversible de la stomie est aléatoire, jusque 30 % lorsque les lésions rectales initiales se limitent à des ulcérations (Yuan 2016, Huan 2020).
Les chirurgies de résection rectale
En dernier recours, dans des situations non contrôlées, avec le plus souvent une atteinte post radique sévère extensive au périnée, associant volontiers sténose, ulcération, nécrose ou fistule, une chirurgie de résection peut être discutée. Elle ne doit être décidée et réalisée que par des équipes médico- chirurgicales expérimentées car la morbidité est importante en présence de complications post-radiques sévères, avec une mortalité non négligeable.
Conclusions
Le traitement curatif des rectorragies des RPRC s’est considérablement amélioré au cours des 25 dernières années. Les rectorragies sont habituellement accessibles à la thérapeutique, la CPA et/ ou l’application de formaline permettant de contrôler la plupart des saignements. Mais d’autres symptômes ano-rectaux ou pelviens sont souvent associés à des degrés divers aux rectorragies et plus complexe à prendre en charge, avec une place alors privilégiée de l’OHB. En cas d’échec, les ressources thérapeutiques concernant la pathologie fonctionnelle ano-rectale, en particulier les troubles de la continence, sont beaucoup plus limitées. Il en est de même pour les atteintes très sévères de type sténoses, suppuration et/ ou nécroses, heureusement exceptionnelles. La prévention de ces RPRC est un enjeu capital et ne repose actuellement que sur les progrès récents de la RT qui ont permis de diminuer leur incidence, en particulier les atteintes post-radiques pelvi-périnéales les plus graves. À défaut de pouvoir recommander un médicament ayant un effet radioprotecteur en cours de RT, les progrès pourraient venir de l’identification dans un avenir proche de facteurs prédictifs de toxicité liés au patient lui-même et ainsi encore réduire ces risques de complications.
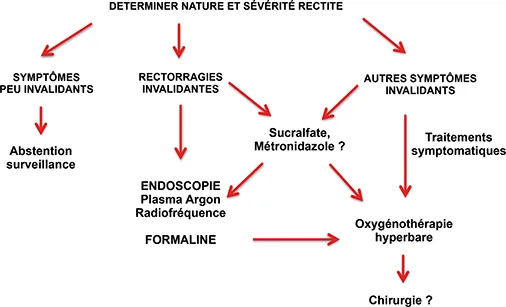
Algorithme de prise en charge des RPRC

Schéma 1 : Algorithme de prise en charge des RPRC
Références
- Ali F, Hu KY. Evaluation and management of chronic radiation Dis Colon Rectum. 2020;63:285-289.
- Bauer P, Berrod JL, de Parades V, Chauveinc L. Lésions radiques de l’anus et du rectum. Hépato Gastro. 2015;22:488-499.
- Brothwell MRS, West CM, Dunning AM, Burnet NG, Barnett GC. Radiogenomics in the era of advanced radiotherapy. Clin Oncol. 2019;31:319-325.
- Campostrini F, Musola R, Marchiaro G, Lonardi F, Verlato G. Role of early proctoscopy in predicting late symptomatic proctitis after external radiation therapy for prostate carcinoma. Int J Radiat Oncol Biol Phys. 2013;85:1031-1037.
- Clarke RE, Tenorio LM, Hussey JR, Toklu AS, Cone DL, Hinojosa JG, et al. Hyperbaric oxygen treatment of chronic refractory radiation proctitis: a randomized and controlled double-blind crossover trial with long-term follow-up. Int J Radiat Oncol Biol Phys. 2008;72:134-143.
- Costa D, Amaro CE, Nunes A, Cardoso JS, Daniel PM, Rosa I, et al. Hyperbaric oxygen therapy as a complementary treatment for radiation proctitis: Useless or useful? A literature World J Gastroenterol. 2021;27:4413-4428.
- De Parades V, Bauer P, Marteau P, Chauveinc L, Bouillet T, Atienza Traitement non chirurgical des rectites radiques chronique. Gastroenterol Clin Biol. 2007;31:919-28.
- Ferini G, Pergolizzi S. A ten-year-long update on radiation proctitis among prostate cancer patients treated with curative external beam In Vivo. 2021;35:1379-1391
- Furtado FS, Furtado GB, Oliveira AT, Oliveira FAA, Pinho CS, Sampaio JPA, et al. Endorectal formalin instillation or argon plasma coagulation for hemorrhagic radiation proctopathy therapy: a prospective and randomized clinical trial. Gastrointest Endosc. 2021;93:1393-1400.
- Goldner G, Tomicek B, Becker G, Geinitz H, Wachter S, Zimmermann F, et al. Proctitis after external-beam radiotherapy for prostate cancer classified by Vienna Rectoscopy Score and correlated with EORTC/RTOG score for late rectal toxicity: results of a prospective multicenter study of 166 patients. Int J Radiat Oncol Biol Phys. 2007;67:78-83.
- Glover M, Smerdon GR, Andreyev HJ, Benton BE, Bothma P, Firth O, et Hyperbaric oxygen for patients with chronic bowel dysfunction after pelvic radiotherapy (HOT2): a randomised, double-blind, sham-controlled phase 3 trial. Lancet Oncol. 2016;17:224-233.
- Goldner G, Tomicek B, Becker G, Geinitz H, Wachter S, Zimmermann F, et Proctitis after external-beam radiotherapy for prostate cancer classified by Vienna Rectoscopy Score and correlated with EORTC/RTOG score for late rectal toxicity: results of a prospective multicenter study of 166 patients. Int J Radiat Oncol Biol Phys. 2007;67:78-83
- Grodsky MB, Sidani SM. Radiation proctopathy. Clin Colon Rectal Surg. 2015;28:103-111
- Hama Y, Kaji T. Long-term follow-up results of CT-guided daily adaptive radiation therapy for localized prostate cancer. Anticancer 2018;38:5959-5962.
- Hanson B, MacDonald R, Shaukat Endoscopic and medical therapy for chronic radiation proctopathy: a systematic review. Dis Colon Rectum. 2012;55:1081-1095.
- Hauer-Jensen M, Denham JW, Andreyev HJ. Radiation enteropathy–pathogenesis, treatment and prevention. Nat Rev Gastroenterol 2014; 11: 470-479
- Hernández-Moreno A, Vidal-Casariego A, Calleja-Fernández A, Kyriakos G, Villar Taibo R, Urioste Fondo A, et Chronic enteritis in patients undergoing pelvic radiotherapy: prevalence, risk factors and associated complications.Nutr Hosp. 2015;32:2178-2183.
- Horaist C, Geffrier C, Bauer P, de Parades V. Rectites radiques. EMC – Gastro-entérologie 2017;0(0):1-9 [article 9-087-G-10]..
- Huang X, Zhong Q, Wang H, Zhao J, Kuang Y, Guan Q, et al. Diverting colostomy is an effective procedure for ulcerative chronic radiation proctitis patients after pelvic malignancy radiation. BMC Surg. 2020;20:267-276.
- Kerns SL, Fachal L, Dorling L et al. Radiogenomics Consortium Genome-Wide Association Meta-analysis of late toxicity after prostate cancer Radiotherapy. J Natl Cancer Inst. 2020;112:179-190.
- Kintzinger C, Demoor Golschmidt C, Abderrahmani R, Paris F, Supiot S. Toxicité rectale de la radiothérapie : signes cliniques, physiopathologie et prise en charge. Cancer Radiother 2012;16:372-376.
- Krol R, Smeenk RJ, van Lin EN, Yeoh EE, Hopman WP. Systematic review: anal and rectal changes after radiotherapy for prostate Int J Colorectal Dis. 2014;29:273-283.
- Kumagai T, Rahman F, Smith AM. The microbiome and radiation induced-bowel injury: evidence for potential mechanistic role in disease Nutrients. 2018;10:1405-1421.
- Lawrie TA, Green JT, Beresford M, Wedlake L, Burden S, Davidson SE, et al. Interventions to reduce acute and late adverse gastrointestinal effects of pelvic radiotherapy for primary pelvic cancers. Cochrane Database Syst Rev. 2018 Jan 23;1(1):CD012529.
- Lee JK, Agrawal D, Thosani N, Al-Haddad M, Buxbaum JL, Calderwood AH, et al. ASGE guideline on the role of endoscopy for bleeding fromchronic radiation proctopathy. Gastrointest Endosc. 2019;90:171-182.
- Li YD, Xu JH, Lin JJ, Zhu WF. Application of 4% formaldehyde under electronic colonoscope as a minimally invasive treatment of chronic hemorrhagic radiation proctitis. World J Emerg Med. 2019;10:228-231.
- Mathieu D, Marroni A, Kot Tenth European Consensus Conference on Hyperbaric Medicine: recommendations for accepted and non-accepted clinical indications and practice of hyperbaric oxygen treatment. Diving Hyperb Med. 2017;47: 24-32.
- McCarty TR, Garg R, Rustagi Efficacy and safety of radiofrequency ablation for treatment of chronic radiation proctitis: A systematic review and meta-analysis. J Gastroenterol Hepatol. 2019;34:1479-1485.
- Miller LE, Efstathiou JA, Bhattacharyya SK, Payne HA, Woodward E, Pinkawa M. Association of the placement of a perirectal hydrogel spacer with the clinical outcomes of men receiving radiotherapy for prostate cancer: A systematic review and meta-analysis. JAMA Netw Open. 2020;3:208-221.
- Min M, Chua B, Guttner Y, Abraham N, Aherne NJ, Hoffmann M, et al. Is “pelvic radiation disease” always the cause of bowel symptoms following prostate cancer intensity-modulated radiotherapy? Radiother Oncol. 2014;110:278-283.
- Nascimento M, Caporossi C, Eduardo Aguilar-Nascimento J, Michelon Castro-Barcellos H, Teixeira Motta R, Reis Lima S. Efficacy of synbiotics to reduce symptoms and rectal inflammatory response in acute radiation proctitis: a randomized, double-blind, Placebo-controlled pilot trial. Nutr Cancer. 2020;72:602-609.
- Nelamangala Ramakrishnaiah VP, Krishnamachari S. Chronic haemorrhagic radiation proctitis: A review. World J Gastrointest. Surg. 2016;8:483-491.
- Paquette IM, Vogel JD, Abbas MA, Feingold DL, Steele SR. The American Society of Colon and Rectal Surgeons clinical practice guidelines for the treatment of chronic radiation proctitis. Dis Colon Rectum. 2018;61:1135-1140.
- Rotondano G, Bianco MA, Marmo R, Piscopo R, Cipolletta L. Long-term outcome of argon plasma coagulation therapy for bleeding caused by chronic radiation proctopathy. Dig Liver Dis. 2003;35:806-810.
- Rustagi T, Corbett FS, Mashimo H. Treatment of chronic radiation proctopathy with radiofrequency ablation (with video). Gastrointest 2015;81:428-436.
- Sahebnasagh A, Ghasemi A, Akbari J, Alipour A, Lashkardoost H, Ala S, Hosseinimehr SJ, et al. Prevention of acute radiation-induced proctitis by Aloe vera: a prospective randomized, double-blind, placebo controlled clinical trial in pelvic cancer BMC Complement Med Ther. 2020;20:146-155.
- Samalavicius NE, Dulskas A, Kilius A, et al. Treatment of hemorrhagic radiation-induced proctopathy with a 4% formalin application under perianal anesthetic World J Gastroenterol. 2013;19:4944-4949.
- Swan MP, Moore GT, Sievert W, Devonshire Efficacy and safety of single-session argon plasma coagulation in the management of chronic radiation proctitis. Gastrointest Endosc. 2010;72:150-154.
- Weiner JP, Wong AT, Schwartz D, Martinez M, Aytaman A, Schreiber D. Endoscopic and non-endoscopic approaches for the management of radiation-induced rectal bleeding. World J Gastroenterol. 2016;22:6972-6986.
- West CM, Barnett GC. Genetics et genomics of radiotherapy toxicity : towards prediction. Genome Medicine. 2011;3:52-67.
- William HRT, Vlavianos P, Blake P, Dearnaley DP, Tait D, Andreyev The significance of rectal bleeding after pelvic radiotherapy. Aliment Pharmacol Ther. 2005;21:1085–1090.
- Yeoh E, Tam W, Schoeman M, et al. Argon plasma coagulation therapy versus topical formalin for intractable rectal bleeding and anorectal dysfunction after radiation therapy for prostate carcinoma. Int J Radiat Oncol Biol Phys. 2013;87:954-959.
- Yuan JH, Song LM, Liu Y, Li MW, Wang R, Zhang CS, et al. The effects of hyperbaric oxygen therapy on pelvic radiation induced gastrointestinal complications (rectal bleeding, diarrhea, and pain): a meta-analysis. Front 2020;10:390-403.
- Yuan ZX, Ma TH, Wang HM, Zhong QH, Yu XH, Qin QY, et al. Colostomy is a simple and effective procedure for severe chronic radiation proctitis. World J Gastroenterol. 2016;22:5598-5608.