Diabète et troubles moteurs œso-gastriques : des symptômes aux traitements
Les points forts
Vidéo
Liens d’intérêt
Guillaume GOURCEROL a perçu des honoraires de consultant auprès de KyowaKyrin, Naturex et de conférencier auprès de Laborie et Medtronic.
Mots-clés
Gastroparésie diabétique, Trouble moteur œsophagien, Vidange gastrique, reflux gastro-œsophagien, Prokinétiques.
Introduction
En France, l’assurance maladie a identifié près de 4 millions de personnes diabétiques en 2019. L’ensemble des études de population générale retrouvent globalement 20 % de symptômes digestifs haut chez les malades diabétiques contre environ 15 % dans la population générale. Cette revue détaille les principales complications motrices liées au diabète de l’œsophage à l’estomac.
Physiopathologie
Les troubles de la motricité gastro-intestinale au cours du diabète sont multifactoriels. La neuropathie diabétique est le mécanisme le plus fréquent puisque l’hyperglycémie induit un stress oxydatif, un dysfonctionnement mitochondrial, conduisant à une neurodégénérescence et une apoptose neuronale (1). Cette neuropathie touche le système nerveux végétatif extrinsèque (c’est-à-dire sympathique et parasympathique), mais également le système nerveux entérique avec la perte de neurones excitateurs et inhibiteurs et des cellules interstitielles de Cajal (1). De plus, une atteinte des cellules de soutien, comme les cellules de Schwann, les cellules gliales et vasculaires, contribue aux atteintes nerveuses périphériques et centrales observées au cours du diabète (1). Par ailleurs, une hyperglycémie élevée (en général > 3g/L), même isolée, peut influer sur la motricité gastro-intestinale par des mécanismes hormonaux et/ou réflexes. À titre d’exemple, l’hyperglycémie aiguë peut supprimer la motricité antrale et retarder la vidange gastrique chez les sujets atteints de diabète de type 1 (2-3). Enfin, certains médicaments utilisés dans le cadre de la maladie diabétique et/ ou de ses complications peuvent engendrer des troubles de la motricité gastro-intestinale. Parmi les plus fréquents, on peut citer les opioïdes dont le tramadol utilisés dans le cadre de la neuropathie diabétique, les analogues du GLP1, et les anti-cholinergiques (antidépresseurs, antiépileptiques…).
En plus de ces facteurs, il est également important de considérer le rôle des facteurs psychologiques dans la perception des symptômes gastro- intestinaux. En effet, l’anxiété et la dépression sont significativement associées à la survenue de symptômes digestifs dans la population générale (4,5). De même, l’anxiété et la dépression ne sont pas associées au retard de la vidange gastrique mais prédisent de manière indépendante la sévérité des symptômes et de la gastroparésie diabétique (6). Cela peut également expliquer en partie la prévalence similaire des symptômes digestifs entre les personnes atteintes de diabète et les témoins dans les études de population générale (4).
Reflux gastro-œsophagien
Sur le plan physiopathologique, plusieurs arguments laissent à penser que les malades diabétiques seraient plus exposés au reflux gastro-œsophagien (RGO). Le surpoids et l’obésité, plus fréquent dans le diabète de type 2, pourraient favoriser le RGO tandis que la neuropathie viscérale pourrait favoriser les troubles moteurs œsophagiens et/ou gastriques. Les données de population générale laissent néanmoins penser que cette association est plutôt ténue. Par exemple, Une étude taïwanaise réalisée chez des sujets bénéficiant d’un dépistage endoscopique retrouvait enfin une prévalence comparable du symptôme régurgitation chez les patients diabétiques (7,7 %) et non diabétiques (9 %) (7). Une seconde étude de population générale australienne trouvait également que la fréquence du pyrosis était non différente entre les malades diabétiques (13,5 %) et non diabétiques (10,8 %) (8). Il est important de noter que ces deux études ont essentiellement porté sur des malades présentant un diabète de type 2 (92,8 % dans la première et 94,8 % dans la seconde). Aucune différence concernant la fréquence des symptômes de reflux n’était néanmoins notée entre diabète de type 1 et de type 2 (8). De manière surprenante, une étude américaine a même retrouvé que ce symptôme était moins fréquent (11,6 % vs. 22,9 %) chez les diabétiques que dans la population générale, et que les malades diabétiques prenaient moins d’antiacides que les non diabétiques (4). Dans cette étude, cette diminution de fréquence du pyrosis était plus prononcée chez les malades avec un diabète de type 1 (38,9 % des malades diabétiques) que chez ceux présentant un diabète de type 2. Une des explications serait que la neuropathie viscérale sensitive liée au diabète, en particulier dans le cadre du diabète de type 1 dont la durée d’évolution est plus longue, pourrait diminuer l’expression symptomatique du reflux, à l’instar de la maladie coronarienne (9).
Il n’existe pas de série « pH-métrique » à l’échelle de la population générale, mais deux études endoscopiques sont disponibles, l’une taïwanaise et l’autre sud-coréenne, chez des malades bénéficiant d’un programme de dépistage endoscopique. Dans la première étude, la présence d’une œsophagite érosive peptique était retrouvée chez 34,3 % des diabétiques contre 28,6 % (p= 0,002) des non diabétiques (7). Dans la seconde, le diabète était un facteur de risque de développer une œsophagite peptique en analyse univariée, mais disparaissait lors de l’étude multivariée, probablement au profit d’autres facteurs confondant comme le surpoids (10). Néanmoins, deux études ont démontré que le diabète, en particulier de type 2 était un facteur de risque indépendant, en plus du surpoids ou de l’âge, de développer un œsophage de Barrett (7, 11).
Le traitement du reflux gastro-œsophagien chez les malades diabétiques ne diffère pas des malades non diabétiques puisque la présentation clinique ne semble pas différente des malades non-diabétiques. Néanmoins, la présence de symptômes de reflux gastro-œsophagien peut faire rechercher la présence d’une gastroparésie diabétique puisqu’il existe une association entre retard de vidange et reflux gastro-œsophagien liquides (12).
Troubles moteurs œsophagiens
Une étude de population générale australienne confirme que le symptôme de dysphagie est 3 fois plus fréquent chez les malades diabétiques, dont la majorité (94,8 %) étaient de type 2, que dans la population générale (13). Ceci est sans lien avec une éventuelle prévalence plus élevée de lésions organiques œsophagiennes. À l’inverse, le diabète expose à la survenue de trouble de la motricité œsophagienne. Les études récentes cas témoin utilisant la manométrie haute résolution retrouvent de manière 2 à 3 fois plus fréquente des troubles mineurs de la motricité œsophagienne, comme des contractions absentes, interrompues ou multiphasiques, ainsi qu’une augmentation de la vitesse de propagation ou de la pression intra- bolus (14-16). Seule une étude a retrouvé une différence entre les malades traités par anti-diabétiques oraux par rapport aux malades traités par insuline, avec une fréquence accrue de contractions absentes ou interrompues chez ces derniers (15). Ces anomalies motrices étaient associées le plus souvent à la survenue de complications du diabète, en particulier neurologiques (14). La plupart du temps, les troubles mineurs de la motricité œsophagienne ne requièrent aucun traitement spécifique car leur association avec les symptômes œsophagiens, et la dysphagie en particulier, reste faible. Ils peuvent néanmoins conditionner le recours éventuel à une chirurgie anti-reflux ou orienter, si besoin, vers une ou l’autre des techniques de chirurgie bariatrique parfois utilisées chez les malades diabétiques. Néanmoins, aucune de ces études n’a pu confirmer la prévalence plus élevée de troubles spécifiques de la motricité œsophagienne telle que l’achalasie du sphincter inférieur de l’œsophage, l’hypercontractilité du corps œsophagien ou les spasmes distaux. Dès lors, la prise en charge des troubles spécifiques de la motricité œsophagienne chez les malades diabétiques suit les mêmes recommandations que les malades non diabétiques. Néanmoins, ces troubles spécifiques de la motricité œsophagienne sont à évoquer en cas de diabète déséquilibré et de symptômes œsophagiens, car ils peuvent, à l’instar de la gastroparésie diabétique, conduire à un asynchronisme entre la prise d’insuline et du repas (16).
Gastroparésie : présentation clinique
La gastroparésie est un syndrome caractérisé par un retard de vidange gastrique en l’absence d’obstruction mécanique associé à des symptômes digestifs hauts (17). Les nausées et les vomissements post-prandiaux sont au premier plan mais peuvent manquer. Ils sont souvent, mais pas toujours, associés à d’autres symptômes dyspeptiques (satiété précoce, ballonnements, plénitude gastrique et plus rarement douleurs épigastriques). Ce diagnostic peut également être évoqué devant un diabète déséquilibré, résultant d’un asynchronisme entre la vidange du repas et l’administration d’insuline. Chez certains malades néanmoins, ce retard de vidange gastrique peut rester pauci-symptomatique en raison de la neuropathie végétative diabétique. En l’absence de vidange gastrique ralentie, le terme de dyspepsie diabétique, qui est superposable à la dyspepsie fonctionnelle est plus approprié. La dyspepsie est caractérisée fonctionnelle par un ou plusieurs symptômes gastro-intestinaux supérieurs, généralement postprandiaux.
Une étude en population générale, menée auprès de malades atteints de diabète de type 1 et de type 2 a évalué le risque de développer une gastroparésie chez les diabétiques (18). Sur une période de 10 ans, le risque de développer une gastroparésie était de 5,2 % chez les personnes atteintes de diabète de type 1, et de 1 % chez les personnes atteintes de diabète de type 2 contre 0,2 % chez les témoins. Néanmoins, dans cette étude, la gastroparésie a été documentée essentiellement sur la base des symptômes ou de l’endoscopie et non par un test de vidange gastrique. Peu de données sont disponibles concernant l’histoire naturelle de la gastroparésie diabétique. Classiquement, la gastroparésie diabétique peut entraîner une altération du statut nutritionnel, un déséquilibre du contrôle glycémique et une mauvaise qualité de vie, indépendamment d’autres facteurs,
tels que l’âge, le tabagisme, la consommation d’alcool ou le type de diabète (19). La gastroparésie est également associée à une morbi-mortalité importante. Dans une étude de cohorte portant sur des patients avec gastroparésie diabétiques, environ 25 % étaient décédés lors du suivi au moins 9 ans plus tard (20). Une deuxième étude a comparé des patients diabétiques présentant des symptômes dyspeptiques et vidange gastrique normale ou ralentie, avec une population diabétique asymptomatique (21). Dans cette étude, la gastroparésie diabétique était associée à la présence de maladies cardiovasculaires, à l’hypertension, à la rétinopathie et à une fréquence d’hospitalisations accrue. Enfin, plusieurs études ont retrouvé que la gastroparésie diabétique était associée à une surmortalité par rapport aux malades présentant une gastroparésie idiopathique, mais également par rapports aux malades diabétiques symptomatiques (dyspepsie) mais avec une vidange gastrique normale (22,23).
Gastroparésie : diagnostic
Les tests de diagnostic sont souvent guidés par le profil et la gravité des symptômes. Néanmoins, la clinique seule ne permet pas de distinguer la gastroparésie de la dyspepsie diabétique, car les symptômes de la gastroparésie sont peu spécifiques. Dès lors, le diagnostic de gastroparésie nécessite par définition une preuve objective du ralentissement de la vidange gastrique. Dans tous les cas, une endoscopie digestive haute préalable est recommandée pour éliminer une éventuelle obstruction organique. La scintigraphie gastrique et le test respiratoire à l’acide octanoïque marqué au carbone 13 (13C) sont les deux techniques de références pour mesurer la vidange gastrique (17). Ces deux tests ont en commun de mesurer la vidange des solides après ingestion d’un repas test calibré. Pour cela, les malades doivent être à jeun depuis au moins 12 heures ce qui peut nécessiter une adaptation du traitement par insuline. Les malades doivent également arrêter si possible les traitements modifiant la vidange gastrique, en particulier les opioïdes et les analogues du GLP. Enfin, ce test doit idéalement être réalisé en euglycémie chez les malades diabétiques, et une glycémie > 2 g/L avant de débuter l’examen doit faire remettre en cause celui-ci.
La scintigraphie gastrique mesure la décroissance post-prandiale du rayonnement émis par le repas test marqué au technétium 99m dans l’aire de projection gastrique déterminée à l’aide d’une gamma Caméra. Le critère le plus reproductible et le plus spécifique pour porter le diagnostic de gastroparésie est la rétention des solides > 10 % à 4 h (24) ; Dès lors, il est important que le test de vidange gastrique réalisée par scintigraphie dure au moins 4 h. Le test respiratoire à l’acide octanoïque marqué au 13C mesure la cinétique de production du 13CO dans les gaz expirés, provenant de l’absorption et de la métabolisation de l’acide octanoïque fixé à la phase solide du repas test. Cette cinétique est le reflet de la rapidité de la vidange gastrique. Là encore, ce test doit être idéalement poursuivi plus de 4 heures, ce qui augmente sa reproductibilité (25).
Un complément d’exploration peut être réalisé par la mesure de la pression et de la distensibilité du pylore par la technique de planimétrie d’impédance (Endoflip ®). Ceci est effectué par l’intermédiaire d’une sonde introduite dans le pylore le plus souvent au décours d’une endoscopie digestive (figure 1). Cette mesure est corrélée à la vidange gastrique et environ la moitié des malades avec gastroparésie diabétique présentent une altération de la distensibilité du pylore et/ou de la pression du pylore (26-27). Ces anomalies ne sont néanmoins pas corrélées à l’équilibre glycémique ou aux complications du diabète (27). Cette mesure peut être proposée lorsque la mesure de vidange gastrique n’est pas envisageable (vomissement du repas test, gastrectomie partielle…). Elle peut également s’avérer utile avant la réalisation d’un geste thérapeutique sur le pylore (injection de toxine botulique, pyloromyotomie endoscopique…), pour prédire la réponse thérapeutique (28).
En pratique, les mesures de la vidange gastrique nécessitent le recours à des centres spécialisés, ce qui peut en limiter la réalisation. Une étude américaine a d’ailleurs récemment confirmé que seuls 10 % des patients présentant des symptômes évocateurs de gastroparésie avaient déjà réalisé une mesure de vidange gastrique (29).
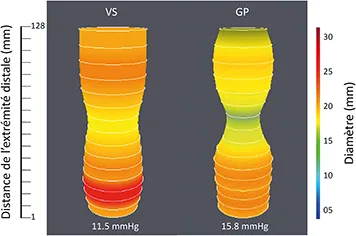
Figure 1 : Mesure de distensibilité pylorique à l’aide de la technique endoflip ® chez un volontaire sain (VS) et un malade avec gastroparésie diabétique (GP)
Gastroparésie : traitement
La première étape du traitement de la gastroparésie diabétique repose sur les mesures hygiéno-diététiques, avec fragmentation des repas (petits repas et collations), en favorisant les liquides par rapport aux solides et en évitant les aliments hypercaloriques ou riches en graisses et en fibres. Le niveau de preuve reste néanmoins faible et son efficacité modeste. Plus important, l’équilibration du diabète permet d’une part de ralentir la progression de la neuropathie diabétique, et d’autre part de réduire le retard de vidange gastrique induit par l’hyperglycémie. Une étude prospective pilote suggère que l’optimisation du contrôle glycémique entraîne une diminution des symptômes de gastroparésie et une amélioration de la qualité de vie (30). Néanmoins, le traitement du diabète et de ses complications doit veiller à éviter autant que possible les traitements ralentissant la vidange gastrique, comme les analogues du GLP1 ou les opioïdes.
La seconde étape du traitement repose sur les prokinétiques (17,31), dont aucun n’a actuellement l’AMM dans la gastroparésie diabétique ou non. Les plus utilisés en France sont les antagonistes des récepteurs D2 de la dopamine. Le metoclopramide exerce un effet central et périphérique, qui lui permet d’accélérer la vidange et d’avoir des propriétés anti-émétiques prononcées. Ses effets secondaires sont dominés par la survenue d’un syndrome extrapyramidal, voire d’un syndrome malin des neuroleptiques, ce qui fait qu’il ne peut être utilisé dans le cadre pédiatrique. La dompéridone a un effet purement périphérique ce qui permet d’éviter la survenue d’un éventuel syndrome extrapyramidal. Son efficacité réside surtout dans la capacité de cette molécule à accélérer la vidange gastrique. Son principal effet secondaire est l’allongement de l’intervalle QT, ce qui peut nécessiter la réalisation d’un ECG pré-thérapeutique et rend difficile son association avec d’autres traitements partageant le même risque. Une alternative est représentée par l’érythromycine qui, en plus de ses propriétés antibiotiques, est également un agoniste des récepteurs à la motiline. Son efficacité pour accélérer la vidange gastrique est bien supérieure par voie veineuse que par voie orale. Son efficacité symptomatique reste néanmoins modeste. Son utilisation au long cours expose à un phénomène de tachyphylaxie, ce qui fait que l’administration intraveineuse est parfois utilisée de manière itérative en hospitalisation. L’érythromycine est également un inhibiteur du cytochrome P450 3A4, ce qui peut induire des interactions médicamenteuses, et peut également entraîner un allongement du QT. Comme pour la dompéridone, un ECG pré-thérapeutique peut également s’avérer nécessaire. Le prucalopride est un agoniste des récepteurs 5-HT4 connu pour sa capacité à stimuler la vidange gastrique (32) : une étude récente contrôlée versus placebo a pu démontrer son intérêt à la dose de 2 mg/j pour améliorer les symptômes dyspeptiques dans un petit groupe de patients avec gastroparésie principalement idiopathique (33).Une seconde étude contrôlée versus placebo menée chez 13 malades avec gastroparésie diabétique a également noté une accélération de la vidange gastrique par le prucalopride à la dose de 4 mg/j sans néanmoins d’amélioration symptomatique significative (34). Cette molécule a reçu l’AMM en France dans le traitement de la constipation, mais n’est pas remboursée.
Il est à noter qu’au-delà de l’amélioration symptomatique, l’accélération de la vidange gastrique permet également d’améliorer le contrôle de la glycémie. Une récente méta-analyse compilant 5 études randomisées versus placebo chez des malades présentant une gastroparésie diabétique a montré que les prokinétiques diminuaient la glycémie à jeun et l’hémoglobine glyquée (35). Néanmoins, aucune étude n’a recherché si un tel effet était également obtenu chez les malades asymptomatiques avec comme seule plainte un déséquilibre glycémique associé à une vidange gastrique ralentie.
En dernier recours et chez les malades les plus sévères, peut se discuter la réalisation d’un traitement instrumental. Ceci est souvent réservé aux centres experts, au mieux dans le cadre d’un essai thérapeutique. Les études de cohortes suggèrent que l’injection intra-pylorique de toxine botulique permet d’accélérer la vidange gastrique ainsi que les symptômes des malades (28,36). Néanmoins, deux essais randomisés contre placebo (de petite taille) retrouvaient que l’injection intra-pylorique de toxine botulique n’était pas plus efficace que le placebo sur les symptômes de la gastroparésie (37,38). Une étude suggère néanmoins que seuls les malades avec altération de la distensibilité pylorique bénéficieraient de ce traitement (28). Une seconde étude a observé que les malades atteints de gastroparésie et répondeurs à l’injection intra-pylorique de toxine botulique étaient également répondeurs à la pyloromyotomie par voie endoscopique (G-POEM) (36). Le G-POEM vise, comme les injections intra-pyloriques de toxine botulique, à diminuer la pression et/ou augmenter le diamètre pylorique afin d’accélérer la vidange gastrique. Cette technique a fait l’objet de nombreuses études de cohortes suggérant une efficacité symptomatique chez les malades diabétiques comme non diabétiques (39-41). Une étude multicentrique française a pu démontrer que cette technique présentait peu de complications sévères (0,4 %) et que plus de 80 % des malades ne présentaient aucune complication (42). Récemment un essai randomisé contrôlé vient de démontrer que le G-POEM réalisé chez 21 malades améliorait les symptômes de gastroparésie et accélérait la vidange gastrique en comparaison avec 20 malades traités par une procédure contrôle (endoscopie sans geste associé) (43). Ces résultats étaient particulièrement significatifs dans le sous-groupe de malades présentant une gastroparésie diabétique qui constituaient le gros de la cohorte. La faible taille de l’effectif et le suivi court n’ont pas permis de rechercher si cette intervention était également efficace sur les paramètres diabétiques. Ces résultats prometteurs demandent donc confirmation. Enfin, la stimulation électrique gastrique peut être une alternative chez les malades décrivant des nausées et/ ou des vomissements réfractaires au traitement médical. En effet, une étude récente randomisée en double aveugle portant sur 179 malades, dont la moitié diabétiques, a montré que la stimulation électrique gastrique réduisait les vomissements chez près de 40 % des malades versus 9 % dans le bras placebo (44). Il est à noter que la stimulation électrique gastrique n’accélérait pas la vidange gastrique, et était aussi efficace chez les malades présentant une vidange gastrique normale avant l’implantation. Cette technique pourrait donc être également proposée aux malades diabétiques avec vomissements chroniques sans ralentissement de la vidange gastrique, à l’exception des vomissements secondaires (médicamenteux, insuffisance rénale ou consommation de cannabis…). On retiendra également de cette étude que malgré la diminution des vomissements par la stimulation électrique gastrique, les paramètres classiques du diabète (glycémie à jeun, hémoglobine glyquée, hypoglycémies) restaient, eux, inchangés. Le frein majeur de cette technique est son coût (> 10 000 €) qui n’est à l’heure actuelle pas remboursé, mais qui pourrait néanmoins se justifier sur le plan médico-économique puisque la stimulation électrique gastrique est associée à une réduction des coûts de santé dont les hospitalisations, en particulier chez les malades diabétiques (45).
Conclusion
Les troubles de la motricité œsophagienne et gastrique liés au diabète ne sont pas rares et peuvent aggraver l’histoire naturelle de la maladie diabétique. Leur identification et leur prise en charge précoce sont donc justifiées et peuvent parfois permettre d’améliorer l’équilibre glycémique nécessaire au contrôle de la maladie diabétique.
Références
- Chandrasekharan B, Srinivasan Diabetes and the enteric nervous system. Neurogastroenterol Motil. 2007 Dec;19(12):951-60.
- Samsom M, Akkermans LM, Jebbink RJ, van Isselt H, vanBerge-Henegouwen GP, Smout AJ. Gastrointestinal motor mechanisms in hyperglycaemia induced delayed gastric emptying in type I diabetes mellitus. Gut. 1997;40(5):641-646.
- Barnett JL, Owyang Serum glucose concentration as a modulator of interdigestive gastric motility. Gastroenterology. 1988;94(3):739-744.
- Maleki D, Locke GR 3rd, Camilleri M, Zinsmeister AR, Yawn BP, Leibson C, Melton LJ 3rd: Gastrointestinal tract symptoms among persons with diabetes mellitus in the community. Arch Intern Med 160:2808-2816, 2000.
- de Kort S, Kruimel JW, Sels JP, Arts IC, Schaper NC, Masclee AA: Gastrointestinal symptoms in diabetes mellitus, and their relation to anxiety and depression. Diabetes Res Clin Pract96:248–255, 2012.
- Hasler WL, Parkman HP, Wilson LA, Pasricha PJ, Koch KL, Abell TL, et al. NIDDK Gastroparesis Clinical Research Consortium: Psychological dysfunction is associated with symptom severity but not disease etiology or degree of gastric retention in patients with Am J Gastroenterol105:2357–2367, 2010.
- Tseng PH, Lee YC, Chiu HM, Chen CC, Liao WC, Tu CH, et al. Association of diabetes and HbA1c levels with Diabetes Care. 2012 May;35(5):1053-60.
- Bytzer P, Talley NJ, Leemon M, Young LJ, Jones MP, Horowitz M. Prevalence of gastrointestinal symptoms associated with diabetes mellitus: a population-based survey of 15,000 adults. Arch Intern Med 161:1989-1996, 2001.
- Ducrotté P, Gourcerol G. Gastroparesis: pathophysiology and management. Presse Med. 2012;41:721-9.
- Kim N, Lee SW, Cho SI, Park CG, Yang CH, Kim HS, et al. pylori and Gerd Study Group of Korean College of Helicobacter and Upper Gastrointestinal Research. The prevalence of and risk factors for erosive oesophagitis and non-erosive reflux disease: a nationwide multicentre prospective study in Korea. Aliment Pharmacol Ther. 2008 Jan 15;27(2):173-85.
- Iyer PG, Borah BJ, Heien HC, Das A, Cooper GS, Chak A. Association of Barrett’s esophagus with type II diabetes mellitus: results from a large population-based case-control study. Clin Gastroenterol Hepatol11:1108-1114.e5, 2013.
- Gourcerol G, Benanni Y, Boueyre E, Leroi AM, Ducrotte Influence of gastric emptying on gastro-esophageal reflux: a combined pH-impedance study. Neurogastroenterol Motil. 2013 Oct;25(10):800-e634.
- Bytzer P, Talley NJ, Leemon M, Young LJ, Jones MP, Horowitz M. Prevalence of gastrointestinal symptoms associated with diabetes mellitus: a population-based survey of 15,000 adults. Arch Intern Med 161:1989-1996, 2001.
- Muroi K, Miyahara R, Funasaka K, Furukawa K, Sawada T, Maeda K, et Comparison of High-Resolution Manometry in Patients Complaining of Dysphagia among Patients with or without Diabetes Mellitus. Digestion. 2021;102(4):554-562.
- George NS, Rangan V, Geng Z, Khan F, Kichler A, Gabbard S, et al. Distribution of Esophageal Motor Disorders in Diabetic Patients With Dysphagia J Clin Gastroenterol. 2017 Nov/Dec;51(10):890-895.
- Roman S, Marjoux S, Thivolet C, Mion Oesophageal function assessed by high-resolution manometry in patients with diabetes and inadequate glycaemic control. Diabet Med. 2014 Nov;31(11):1452-9.
- Schol J, Wauters L, Dickman R, Drug V, Mulak A, Serra J, et ESNM Gastroparesis Consensus Group. United European Gastroenterology (UEG) and European Society for Neurogastroenterology and Motility (ESNM) consensus on gastroparesis. United European Gastroenterol J. 2021 Apr;9(3):287-306. doi: 10.1002/ueg2.12060.
- Choung RS, Locke GR 3rd, Schleck CD, Zinsmeister AR, Melton LJ 3rd, Talley NJ. Risk of gastroparesis in subjects with type 1 and 2 diabetes in the general population. Am J Gastroenterol 107:82–88, 2012
- Talley NJ, Young L, Bytzer P, Hammer J, Leemon M, Jones M, et al. Impact of chronic gastrointestinal symptoms in diabetes mellitus on health-related quality of life. Am J Gastroenterol 96:71-76, 2001
- Kong MF, Horowitz M, Jones KL, Wishart JM, Harding PE. Natural history of diabetic gastroparesis. Diabetes Care 22:503-507, 1999.
- Hyett B, Martinez FJ, Gill BM, Mehra S, Lembo A, Kelly CP, et Delayed radionucleotide gastric emptying studies predict morbidity in diabetics with symptoms of gastroparesis. Gastroenterology 137:445-452, 2009.
- Gourcerol G, Melchior C, Wuestenberghs F, Desprez C, Prevost G, Grosjean J, et Delayed gastric emptying as an independent predictor of mortality in gastroparesis. Aliment Pharmacol Ther. 2022 Apr;55(7):867-875. doi: 10.1111/apt.16827. Epub 2022 Feb 20.
- Jung HK, Choung RS, Locke GR 3rd, Schleck CD, Zinsmeister AR, Szarka LA, et al. The incidence, prevalence, and outcomes of patients with gastroparesis in Olmsted County, Minnesota, from 1996 to 2006. Gastroenterology. 2009 Apr;136(4):1225-33. doi: 10.1053/j.gastro.2008.12.047. Epub 2008 Dec 24.PMID: 19249393.
- Abell TL, Camilleri M, Donohoe K, Hasler WL, Lin HC, Maurer AH, et al. American Neurogastroenterology and Motility Society and the Society of Nuclear Medicine. Consensus recommendations for gastric emptying scintigraphy: a joint report of the American Neurogastroenterology and Motility Society and the Society of Nuclear Medicine. Am J Gastroenterol. 2008 Mar;103(3):753-63. doi: 10.1111/j.1572-0241.2007.01636.x. Epub 2007 Nov 19.PMID: 18028513.
- Wuestenberghs F, Juge M, Melchior C, Desprez C, Leroi AM, Gourcerol G. Association Between Symptoms, Quality of Life, and Gastric Emptying in Dyspeptic Patients. J Neurogastroenterol Motil. 2019 Oct 30;25(4):534-543.
- Gourcerol G, Tissier F, Melchior C, Touchais JY, Huet E, Prevost G, et Impaired fasting pyloric compliance in gastroparesis and the therapeutic response to pyloric dilatation. Aliment Pharmacol Ther. 2015 Feb;41(4):360-7.
- Desprez C, Chambaz M, Melchior C, Basile P, Prevost G, Jacques J, et al. Assessment of pyloric sphincter distensibility and pressure in patients with diabetic gastroparesis. Neurogastroenterol Motil. 2021 Aug;33(8):e14064.
- Desprez C, Melchior C, Wuestenberghs F, Zalar A, Jacques J, Leroi AM, et al. Pyloric distensibility measurement predicts symptomatic response to intrapyloric botulinum toxin injection. Gastrointest Endosc. 2019 Nov;90(5):754-760.e1.
- Ye Y, Yin Y, Huh SY, Almansa C, Bennett D, Camilleri M. Epidemiology, Etiology, and Treatment of Gastroparesis: Real-World Evidence From a Large US National Claims Database. Gastroenterology. 2022 Jan;162(1):109-121.e5. doi: 10.1053/j.gastro.2021.09.064. Epub 2021 Oct 6.PMID: 34624355.
- Calles-Escandón J, Koch KL, Hasler WL, Van Natta ML, Pasricha PJ, Tonascia J, et NIDDK Gastroparesis Clinical Research Consortium (GpCRC). Glucose sensor-augmented continuous subcutaneous insulin infusion in patients with diabetic gastroparesis: an open-label pilot prospective study. PLoS One. 2018;13(4):e0194759.
- Vijayvargiya P, Camilleri M, Chedid V, Mandawat A, Erwin PJ, Murad MH. Effects of Promotility Agents on Gastric Emptying and Symptoms: A Systematic Review and Meta-analysis. Gastroenterology. 2019 May;156(6):1650-1660.
- Kessing BF, Smout AJ, Bennink RJ, Kraaijpoel N, Oors JM, Bredenoord AJ. Prucalopride decreases esophageal acid exposure and accelerates gastric emptying in healthy subjects. Neurogastroenterol Motil. 2014 Aug;26(8):1079-86.
- Carbone F, Van den Houte K, Clevers E, Andrews CN, Papathanasopoulos A, Holvoet L, et al. Prucalopride in Gastroparesis: A Randomized Placebo-Controlled Crossover Study. Am J Gastroenterol. 2019 Aug;114(8):1265-1274.
- Andrews CN, Woo M, Buresi M, Curley M, Gupta M, Tack J, et al. Prucalopride in diabetic and connective tissue disease-related gastroparesis: Randomized placebo-controlled crossover pilot trial. Neurogastroenterol Motil. 2021 Jan;33(1):e13958.
- Kim YJ, Chung WC, Lee A Meta-Analysis of the Efficacy of Prokinetic Agents against Glycemic Control. Gastroenterol Res Pract. 2019 Sep 9;2019:3014973.
- Wadhwa V, Gonzalez A, Franco Azar FX, Singh H, Gupta K, Liang H, et Does a response to botulinum toxin injection predict a futureresponse to peroral pyloric myotomy (POP) in patients with gastroparesis? Endoscopy. In press. doi: 10.1055/a-1986-4292.
- Arts J, Holvoet L, Caenepeel P, Bisschops R, Sifrim D, Verbeke K, Janssens J, et al. Clinical trial: a randomized-controlled crossover study of intrapyloric injection of botulinum toxin in gastroparesis. Aliment Pharmacol Ther. 2007 Nov 1;26(9):1251-8.
- Friedenberg FK, Palit A, Parkman HP, Hanlon A, Nelson DB. Botulinum toxin A for the treatment of delayed gastric emptying. Am J Gastroenterol. 2008 Feb;103(2):416-23.
- Jacques J, Pagnon L, Hure F, Legros R, Crepin S, Fauchais AL, et Peroral endoscopic pyloromyotomy is efficacious and safe for refractory gastroparesis: prospective trial with assessment of pyloric function. Endoscopy. 2019 Jan;51(1):40-49.
- Labonde A, Lades G, Debourdeau A, Ragi O, Lehmann L, Vitton V, et al. Gastric peroral endoscopic myotomy in refractory gastroparesis: long-term outcomes and predictive score to improve patient selection. Gastrointest Endosc. 2022 Sep;96(3):500-508.e2.
- Kamal F, Khan MA, Lee-Smith W, Sharma S, Acharya A, Jowhar D, et al. Systematic review with meta-analysis: one-year outcomes of gastric peroral endoscopic myotomy for refractory gastroparesis. Aliment Pharmacol Ther. 2022 Jan;55(2):168-177.
- Baret F, Jacques J, Pioche M, Albouys J, Vitton V, Vanbiervliet G, et al. Evaluation of the safety profile of endoscopic pyloromyotomy by G-POEM: a French multicenter study. Therap Adv Gastroenterol. In press, doi: 10.1177/17562848221122472.
- Martinek J, Hustak R, Mares J, Vackova Z, Spicak J, Kieslichova E, et al. Endoscopic pyloromyotomy for the treatment of severe and refractory gastroparesis: a pilot, randomised, sham-controlled trial. Gut. 2022 Nov;71(11):2170-2178.
- Ducrotte P, Coffin B, Bonaz B, Fontaine S, Bruley Des Varannes S, Zerbib F, et al. Gastric Electrical Stimulation Reduces Refractory Vomiting in a Randomized Crossover Trial. Gastroenterology. 2020 Feb;158(3):506-514.e2.
- Gourcerol G, Coffin B, Bonaz B, Hanaire H, Bruley Des Varannes S, Zerbib F, et al. Impact of Gastric Electrical Stimulation on Economic Burden of Refractory Vomiting: A French Nationwide Multicentre Study. Clin GastroenterolHepatol. 2022 Aug;20(8):1857-1866.e1.
Abréviations
GLP : glucagon like peptide
RGO : reflux gastro-oesophagien
AMM : autorisation de mise sur le marché
G-POEM : pyloromyotomie par voie endoscopique
ECG : électrocardiogramme
Toute reproduction ou réécriture, totale ou partielle, sans l’accord préalable écrit de la FMC HGE est interdite.
