Liens d’intérêt
Lecture pour le laboratoire Abbvie, Co-fondateur et actionnaire d’Augmented Endoscopy
Mots-clés
Exploration de l’intestin grêle ; Endoscopie ; Radiologie ; Vidéocapsule ; Maladie de Crohn ; Saignement digestif inexpliqué
Introduction
L’exploration des maladies digestives de l’intestin grêle s’est complexifiée ces dernières années grâce notamment aux progrès technologiques de l’imagerie (échographie, entéroscanner et entéro-IRM) associés à l’émergence de nouvelles techniques endoscopiques (vidéocapsule et entéroscopie). L’exploration de l’intestin grêle doit être précise, complète et pluridisciplinaire avec un large panel d’examens à disposition. La pertinence des examens doit rester une priorité. Il est important pour le gastroentérologue prescripteur d’avoir une connaissance maîtrisée des différents examens disponibles, leurs modalités de réalisation ainsi que leurs performances et limites. Le choix des examens varie en fonction de la présentation clinique et biologique mais doit également intégrer les notions de facilité d’accès et de disponibilité en fonction des ressources environnantes.
Indications de l’exploration de l’intestin grêle
La principale indication d’exploration de l’intestin grêle est la suspicion de saignement de l’intestin grêle (SSIG) définie par un saignement dont l’origine reste indéterminée après des endoscopies haute et basse normales. Le diagnostic et le suivi de la maladie de Crohn (MC) représentent une indication fréquente d’exploration de l’intestin grêle suivie par le dépistage des polypes du grêle (syndrome de Lynch, syndrome de Peutz-Jeghers), la suspicion de lésion tumorale (adénocarcinome, tumeur stromale, lymphome) et la recherche de complications de la maladie cœliaque.
Les différentes techniques d’exploration de l’intestin grêle
Les techniques radiologiques
Échographie abdominale
L’échographie est une technique d’imagerie facilement accessible, simple, bien tolérée par les patients et ne présentant pas de contre-indication. Elle ne nécessite aucune préparation spécifique. Une période de jeûne de 4 à 6 heures n’est pas indispensable mais présente l’avantage de réduire le péristaltisme du grêle. Son utilisation dans l’exploration du grêle est croissante notamment dans le suivi de la MC. L’amélioration des techniques de résolution spatiale échographiques permet de mieux apprécier l’épaisseur de la paroi du grêle, considérée comme pathologique si supérieure à 3 mm. L’échographie est recommandée pour l’évaluation de la MC iléale, la recherche de complications (fistules, sténoses, abcès) ainsi que la récidive post opératoire de la MC (1). Cette technique d’exploration est plus largement diffusée en pédiatrie en raison de sa disponibilité et de son caractère non irradiant.
Scanner abdomino-pelvien
Le scanner est une technique d’imagerie répandue et facilement disponible présentant une excellente résolution spatiale avec la possibilité d’obtenir une acquisition de l’ensemble de la cavité abdominale en quelques secondes seulement. Les progrès technologiques permettent aujourd’hui une étude précise de l’abdomen avec des coupes millimétriques. Un scanner abdomino-pelvien de qualité optimale nécessite une acquisition en trois temps : sans injection de produit de contraste, après injection au temps artériel puis portal selon le contexte. Le temps non injecté s’avère utile car il permet parfois d’éliminer une image faussement positive visible sur les temps injectés. Une distension des anses grêles (Entéroscanner) peut s’avérer pertinente pour différencier un épaississement pariétal pathologique d’une anse collabée en cas de recherche de tumeur. Cette distension peut s’obtenir de deux façons différentes : soit après ingestion de produit hyperosmolaire par le patient soit de façon exceptionnelle après placement d’une sonde d’entéroclyse sous scopie au niveau de l’angle de Treitz permettant d’obtenir une meilleure distension du grêle mais souvent plus difficile à mettre œuvre et moins bien tolérée par le patient.
Entéro-IRM
L’entéro-IRM présente l’avantage d’être une technique d’exploration non irradiante. Cependant cette procédure est longue et l’acquisition des différentes séquences est bien plus sensible aux artéfacts de mouvement par rapport à une acquisition en scanner. Elle nécessite une préparation digestive par ingestion au préalable d’un liquide hyperosmolaire (PEG) environ 30 minutes avant l’examen, après avoir respecté un jeûne de 4 à 6 heures précédant la procédure. Une injection d’antipéristaltique (Glucagon) va permettre de diminuer le péristaltisme du grêle et d’améliorer son interprétation. Cet examen est essentiellement utilisé pour le suivi des MC du grêle dans l’évaluation de l’activité de la maladie, la recherche de complications et l’appréciation de la réponse au traitement. L’analyse radiologique se concentre sur les signes pariétaux et extra-pariétaux avec différentes séquences d’acquisition : séquences cinétiques, séquences en pondération T2, séquences de diffusion, plus ou moins associées à des séquences en pondération T1 après injection de produit de contraste gadoliné (2).
Les techniques endoscopiques
La vidéocapsule de l’intestin grêle
L’émergence de la vidéocapsule endoscopique (VCE) dans les années 2000 a révolutionné l’exploration de l’intestin grêle (3). La VCE du grêle est recommandée depuis 2006 par la HAS (Haute Autorité de Santé) comme examen de première intention pour l’exploration de la suspicion de saignement de l’intestin grêle après gastroscopie et iléo-coloscopie normales. Elle est également recommandée en cas de suspicion de MC du grêle après des explorations endoscopiques et radiologiques n’ayant pas mis en évidence d’anomalie. Une VCE peut être discutée dans d’autres indications plus rares telles que la maladie cœliaque résistante au régime sans gluten ou encore les polyposes digestives. Les contre-indications absolues de la VCE sont la présence d’une sténose du tractus digestif responsable d’un syndrome occlusif, la présence d’un diverticule de Zencker ou encore la présence d’un grêle radique. La suspicion de sténose intestinale doit faire réaliser une imagerie ou une capsule de calibrage délitable préalable à la VCE. Avec une rentabilité diagnostique estimée à 60 % et un taux d’exploration complète du grêle supérieur à 80 % (4,5), la VCE est devenue un outil incontournable du gastroentérologue. Cependant, la lecture de ces VCE demeure chronophage et fastidieuse pour le médecin. En effet, chaque enregistrement de VCE comprend en moyenne 15 000 images et demande entre 30 et 45 minutes de lecture attentive. Ces limites pourraient disparaitre très prochainement devant l’émergence des outils d’aide au diagnostic automatique grâce à l’intelligence artificielle (6,7). Les conditions nécessaires avant la réalisation d’une VCE du grêle sont le respect d’un régime liquide la veille de l’examen associé à une période de jeûne d’au moins 6 heures précédant l’ingestion de la capsule. Les modalités de purge autour de l’ingestion de VCE sont variables selon les pays et les centres. La Société Européenne d’Endoscopie Digestive (ESGE) recommande la prise de 2L de PEG avant l’examen (8). L’essai contrôlé randomisé Français (Prepintest) démontrait que la prise de 500 mL de PEG 30 minutes après l’ingestion de la VCE était également une bonne option (9).
L’entéroscopie
L’entéroscopie poussée permet d’explorer une partie de l’intestin grêle avec une rentabilité diagnostique estimée à environ 60 %. Elle est le plus souvent indiquée à visée thérapeutique (hémostase/polypectomie) ou bien pour la réalisation de biopsies ciblées après une première exploration non invasive de l’intestin grêle (Entéroscanner/IRM, VCE). La principale indication de l’entéroscopie demeure la SSIG. La suspicion de MC du grêle peut également justifier la réalisation d’une entéroscopie à visée diagnostique en cas de cible identifiée et accessible après des endoscopies conventionnelles (gastroscopie et iléo-coloscopie) avec biopsies normales. Enfin l’entéroscopie peut être réalisée dans d’autres indications comme l’exploration et le traitement des tumeurs bénignes et malignes du grêle (Syndrome de Peutz Jeghers, tumeurs stromales, lymphomes, adénocarcinomes). Il existe différentes techniques d’entéroscopie disponibles (simple ballon, double ballon, spiralée +/- motorisée) permettant l’exploration de l’intégralité de l’intestin grêle en associant souvent une exploration bidirectionnelle haute et basse. Les progrès récents notamment sur l’entéroscopie motorisée spiralée sont très prometteurs avec un taux de succès de 97 % et 10,6 % d’entéroscopie complète antérograde (atteinte du cæcum) avec une durée moyenne de procédure aux alentours de 25 minutes (10). Malheureusement, la principale limite de cette technique demeure encore sa faible disponibilité sur notre territoire.
Performances et limites en cas de suspicion de MICI
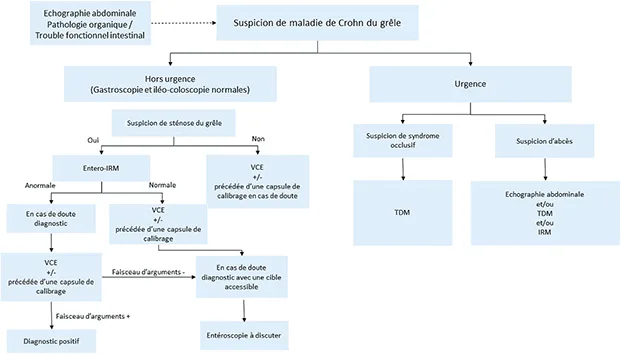
L’exploration d’une suspicion de MC du grêle est avant tout guidée par l’anamnèse ainsi que les données cliniques et biologiques (figure 1). L’exploration de douleurs abdominales associées ou non à des troubles du transit est souvent à l’origine de la réalisation d’examens complémentaires de première intention type échographie/ scanner et endoscopies digestives.

Figure 1 : Proposition d’algorithme pour l’exploration de l’intestin grêle en cas de suspicion de maladie de Crohn
L’échographie est souvent réalisée en première intention devant un tableau de douleurs abdominales et aide à différencier un trouble fonctionnel intestinal d’une pathologie organique. Une échographie normale ne doit pas pour autant écarter le diagnostic de MC du grêle. Une méta-analyse évaluant les performances de l’échographie dans le diagnostic de la MC a montré une excellente spécificité (93 %) et une bonne sensibilité (88 %) selon la localisation iléale ou colique et le seuil d’épaississement de la paroi (11). Cependant, l’exploration par échographie est limitée par la localisation parfois profonde et/ ou pelvienne des lésions rendant difficile leur exploration. L’échographie voit également ses performances diminuées pour les patients en surpoids. Enfin, elle est opérateur dépendant sans possibilité de relecture au décours. En pratique, cette échographie sera rapidement complétée par un scanner abdomino-pelvien souvent en contexte d’urgence ou d’exacerbation des symptômes. La réalisation d’un scanner peut, devant une occlusion mécanique du grêle, faire découvrir un épaississement pathologique du grêle ou encore une MC iléale abcédée mimant une appendicite aiguë. Une méta-analyse évaluant les performances de l’échographie, de l’IRM et du scanner dans le diagnostic de la MC a montré des sensibilités de 90 %, 93 %, 84 % et des spécificités de 96 %, 93 %, 95 % respectivement (12).
La place du scanner dans la MC doit être limitée autant que possible aux urgences (perforation, syndrome occlusif, suspicion d’abcès) afin ne pas surexposer les patients aux rayonnements ionisants (13). En cas d’indisponibilité de l’IRM en urgence ou semi-urgence, les performances du scanner sont excellentes pour faire le bilan d’occlusion, de sténoses ou de complications (14).
La place de l’entéro-IRM est relativement limitée pour le diagnostic initial de la MC car sa négativité n’exclut pas le diagnostic. En l’absence d’atteinte iléale visible en iléoscopie, l’entéro-IRM peut être utile à la phase diagnostique et permet également d’éliminer une éventuelle sténose contre-indiquant la réalisation d’une VCE. L’entéro-IRM devient essentielle une fois le diagnostic posé afin d’établir une cartographie exhaustive de l’atteinte du grêle (topographie, longueur de l’atteinte, focale, multifocale…). L’entéro-IRM permet également l’évaluation précise de l’activité inflammatoire de la maladie et des complications (fistules et abcès/occlusions) avec une sensibilité d’environ 80 % et une spécificité supérieure à 90 % (14). En revanche, l’entéro-IRM est moins facile d’accès que les deux précédentes modalités d’examens. Hors contexte d’urgence, en présence de symptômes obstructifs témoignant d’une probable sténose du grêle, l’examen morphologique indiqué sera de préférence une entéro-IRM. Cependant, l’entéro-IRM peut sous/surestimer la présence d’une sténose du grêle. Dans cette situation, une capsule de calibrage préalable à la VCE devra être réalisée.
La VCE du grêle est de plus en plus indiquée pour le diagnostic et le suivi des patients atteints de MC. Elle est complémentaire de l’entéro-IRM notamment pour son apport diagnostic des lésions jéjunales haut situées et superficielles parfois difficiles à mettre en évidence en entéro-IRM en raison de la plus faible réplétion du jéjunum que de l’iléon (15). L’essai prospectif mené par González-Suárez et al. (16) sur une cohorte de 47 patients atteints et/ ou suspects de MC montrait une meilleure rentabilité diagnostique de la VCE par rapport à l’entéro-IRM (76,6 % vs. 44,7 %, p= 0,001) dans le diagnostic des lésions du grêle mais également dans la détection de lésions jéjunales inflammatoires (31,9 % vs. 6,4 % p= 0,03). Pour autant, le faible effectif de patients inclus dans cette étude ne permet pas de généraliser ces résultats. La qualité de visualisation de la muqueuse du grêle représente une des limites de la VCE. En effet elle peut être réduite notamment en cas de préparation insuffisante et/ ou de non-suivi du régime préalable. À l’instar du score de Boston largement utilisé pour la coloscopie, il n’existe pas à ce jour de score suffisamment robuste permettant une évaluation standardisée et reproductible de la qualité de visualisation en VCE du grêle (17). L’appréciation globale de la propreté de l’intestin grêle doit faire partie du compte rendu de l’examen et est dépendante de l’appréciation du lecteur de VCE. En cas de visualisation insuffisante de la muqueuse, la réalisation d’un nouvel examen peut être discuté si une suspicion forte de MC persiste. La complication principale de la VCE est le risque de rétention de cette dernière au sein d’une sténose du grêle non diagnostiquée au préalable estimée entre 1 et 5 % selon les indications (5). Enfin si les explorations proposées jusqu’ici sont insuffisantes pour affirmer le diagnostic de MC et qu’il existe une cible (ulcérations/ sténoses) paraissant accessible endoscopiquement, alors une entéroscopie haute ou basse doit se discuter. En cas de suspicion de MC, la rentabilité diagnostique de l’entéroscopie varie de 25 % à 70 % selon les études (18,19). L’usage de l’entéroscopie peut également être sollicité dans l’urgence à visée thérapeutique, en cas d’ulcère du grêle hémorragique (hémostase), ou encore en cas de sténose symptomatique accessible à une dilatation hydrostatique.
Performances et limites en cas de suspicion de saignement
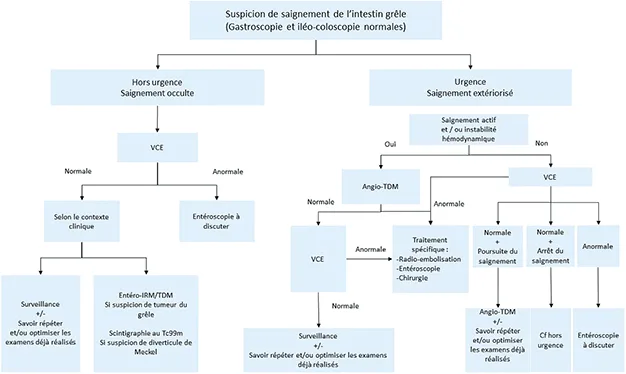
La SSIG est la principale indication d’exploration de l’intestin grêle et représente environ 5 % des hémorragies digestives (20,21). L’angiodysplasie est la principale cause de saignement de l’intestin grêle (40 à 60 %) notamment chez les patients âgés (22). Les autres causes de saignements de l’intestin grêle nécessitant son exploration sont représentées par les tumeurs (tumeurs carcinoïdes, lymphomes, adénocarcinomes, tumeurs stromales…), le diverticule de Meckel chez les patients jeunes, les causes iatrogènes (anti-inflammatoires non stéroïdiens) et les atteintes ischémiques. Il est classiquement admis que 80 % des hémorragies digestives ont une origine haute (avant l’angle de Treitz) (23) et 20 % une origine basse (après l’angle de Treitz) (24,25). Les hémorragies digestives basses sont à 80 % d’origine colo-anale. Les hémorragies digestives liées à l’intestin grêle représentent donc environ 5 % des hémorragies digestives. En cas de SSIG (figure 2), la réalisation d’une VCE est indiquée et permet une exploration optimale de l’intestin grêle. En contexte de SSIG, La rentabilité diagnostique de la VCE est estimée entre 50 et 60 % dans la littérature (26,27). Sa réalisation précoce dans un délai de 14 jours suivant une hémorragie extériorisée représente un critère prédictif de positivité de l’examen (28). L’ESGE préconise dorénavant sa réalisation idéalement dans les 48 heures suivant le début du saignement afin d’optimiser la rentabilité diagnostique de l’examen (29). En termes d’identification de la cause du saignement, des essais prospectifs ont montré que la VCE était plus performante que l’angioscanner (30) ou encore l’entéroscanner (31). En période hémorragique, dans certaines indications spécifiques et si les ressources locales et l’organisation le permettent, le largage per-endoscopique est une option qui semble augmenter la rentabilité diagnostique à 75 % (32). Malgré ses bonnes performances, le caractère différé de l’analyse des VCE, le temps de lecture nécessaire qui leur est dédié, ainsi que la disponibilité variable de cet examen dans les situations d’urgence, représentent les principales limites de cette procédure. Il a également été démontré que les risques inhérents à la lecture humaine, de vigilance réduite et de lésions manquées, augmentent dès la deuxième lecture successive de VCE (33). Il est désormais certain que l’implémentation des outils d’intelligence artificielle va bouleverser tous ces paramètres. Hors contexte d’urgence, à l’issue d’un bilan de SSIG et en cas de VCE non contributive, il est important de savoir répéter et/ ou optimiser les examens déjà réalisés. Dans cette situation, le contexte clinique doit pouvoir nous orienter ou non vers la réalisation d’imagerie complémentaire du grêle (suspicion de tumeur du grêle ?). Les techniques d’imagerie préconisées privilégient alors une distension du grêle pour un examen optimal afin de détecter la cause du saignement. Les tumeurs du grêle représentent 6 à 9 % des causes de saignement digestifs chroniques et sont la première étiologie chez les patients avant 50 ans (34). L’entéro-IRM ou l’entéroscanner peuvent être réalisés dans ce contexte en prenant toujours en considération dans le choix de l’examen le risque au long cours de surexposition répétée aux rayonnements ionisants.

Figure 2 : Proposition d’algorithme pour l’exploration de l’intestin grêle en cas de suspicion de saignement digestif inexpliqué
En contexte d’urgence, en cas de saignement extériorisé important avec instabilité hémodynamique, une exploration la plus précoce possible par angioscanner peut permettre la détection de l’origine du saignement (tumeurs, malformations artério-veineuses, inflammations) et permettre si besoin un traitement radiologique interventionnel adapté. Une méta-analyse a démontré les bonnes performances de l’angioscanner en cas de saignement actif gastro-intestinal avec une sensibilité et spécificité estimées à 85 % et 92 % respectivement (35). Cet examen rapide et largement disponible présente l’avantage majeur de guider un éventuel geste thérapeutique radiologique si nécessaire. Ces limites sont bien connues et représentées par la néphrotoxicité, le risque allergique et l’exposition répétée aux rayonnements. En cas de saignement persistant, un traitement spécifique selon le contexte peut être proposé : radio-embolisation, chirurgie, entéroscopie. Dans certains cas beaucoup plus rares, une prise en charge chirurgicale pourra se discuter avec la possibilité ou non d’une entéroscopie per opératoire qui reste exceptionnelle car associée à une morbi- mortalité élevée (36).
En cas de SSIG, l’entéroscopie est principalement envisagée à visée thérapeutique après une première exploration non invasive du grêle le plus souvent par VCE. Une méta-analyse a montré que la rentabilité diagnostique de la VCE et de l’entéroscopie pour les SSIG étaient similaires (37). Cependant, l’entéroscopie peut également être guidée par une imagerie radiologique préalable ayant identifié l’origine du saignement surtout en cas de saignement extériorisé important. La rentabilité de l’entéroscopie est d’autant plus élevée qu’elle est réalisée précocement (38). Les dernières recommandations de l’ESGE offrent une place nouvelle à la réalisation d’une entéroscopie dans les 48/72 heures suivant l’épisode hémorragique comme alternative de première intention selon la présentation clinique (29), si cette procédure permet d’associer à la fois le diagnostic et le traitement de la cause dans le même temps. Cependant, la limite principale de l’entéroscopie demeure sa faible disponibilité sur notre territoire. Ses principales complications sont dominées par l’hémorragie et la perforation.
Connaître la place des explorations scintigraphiques
En contexte hémorragique
La scintigraphie aux hématies marquées au Technétium 99m (Tc99m) est un examen non invasif permettant d’objectiver un saignement digestif et parfois de le localiser. Elle doit être réalisée en période hémorragique afin d’identifier une éventuelle extravasation sanguine et d’optimiser sa rentabilité diagnostique, ce qui restreint sa place en raison de son accessibilité limitée en urgence (39). La scintigraphie aux érythrocytes marqués au Tc99m est surtout envisagée chez l’homme jeune lorsqu’il existe une suspicion de diverticule de Meckel.
En contexte oncologique
Les tumeurs neuroendocrines (TNE) de l’intestin grêle sont suspectées devant un faisceau d’arguments clinico-biologiques et morphologiques. La tomographie par émission de positons (TEP) est un type particulier d’imagerie permettant d’évaluer l’activité métabolique des tumeurs. La TEP aux analogues de la somatostatine (ASS) offre une sensibilité de détection du rayonnement ainsi qu’une résolution spatiale des images nettement supérieures à la scintigraphie classique ce qui en fait l’examen de référence dans l’exploration des TNE. Les trois ASS classiquement utilisés sont le DOTATOC, le DOTATATE et le DOTANOC. Comparativement à la scintigraphie à l’octréotide, la TEP aux ASS démontre une supériorité dans la détection de la tumeur primitive ainsi que des métastases (40). La F-DOPA (18F-dihydroxy-phénylalanine) est un traceur radioactif extrêmement sensible utilisé pour la détection des TNE bien différenciées. Les données de la littérature mettent en évidence une supériorité de la TEP-F-DOPA par rapport à la scintigraphie à l’octréotide pour les TNE du grêle (41). Enfin l’utilisation du TEP-FDG (Fluorodésoxyglucose) permet une évaluation du niveau d’agressivité des TNE et représente l’examen de référence pour l’exploration des TNE peu différenciées.
Conclusion
Les techniques d’exploration de l’intestin grêle sont nombreuses, variées et souvent complémentaires. Les évolutions technologiques récentes offrent un large choix dans les différentes modalités d’exploration de l’intestin grêle. Les indications, performances et limites des différents examens varient en fonction du contexte clinique et doivent être bien connus du médecin prescripteur. La prescription d’une exploration de l’intestin grêle, qu’elle soit radiologique ou endoscopique doit également intégrer la notion d’accessibilité et de disponibilité en fonction des ressources environnantes.
Références
- Maaser C, Sturm A, Vavricka SR, Kucharzik T, Fiorino G, Annese V, et al. ECCO-ESGAR Guideline for Diagnostic Assessment in IBD Part 1: Initial diagnosis, monitoring of known IBD, detection of complications. J Crohns Colitis. 1 févr 2019;13(2):144-64.
- Biondi M, Bicci E, Danti G, Flammia F, Chiti G, Palumbo P, et al. The Role of Magnetic Resonance Enterography in Crohn’s Disease: A Review of Recent Literature. Diagn Basel Switz. 15 mai 2022;12(5):1236.
- Iddan G, Meron G, Glukhovsky A, Swain P. Wireless capsule endoscopy. Nature. 25 mai 2000;405(6785):417.
- Liao Z, Gao R, Xu C, Li ZS. Indications and detection, completion, and retention rates of small-bowel capsule endoscopy: a systematic review. Gastrointest Endosc. févr 2010;71(2):280-6.
- Cortegoso Valdivia P, Skonieczna-Żydecka K, Elosua A, Sciberras M, Piccirelli S, Rullan M, et al. Indications, Detection, Completion and Retention Rates of Capsule Endoscopy in Two Decades of Use: A Systematic Review and Meta-Analysis. Diagn Basel Switz. 28 avr 2022;12(5):1105.
- Byrne MF, Donnellan F. Artificial intelligence and capsule endoscopy: Is the truly « smart » capsule nearly here? Gastrointest Endosc. 2019;89(1):195-7.
- Dray X, Iakovidis D, Houdeville C, Jover R, Diamantis D, Histace A, et al. Artificial intelligence in small bowel capsule endoscopy – current status, challenges and future promise. J Gastroenterol Hepatol. janv 2021;36(1):12-9.
- Rondonotti E, Spada C, Adler S, May A, Despott EJ, Koulaouzidis A, et al. Small-bowel capsule endoscopy and device-assisted enteroscopy for diagnosis and treatment of small-bowel disorders: European Society of Gastrointestinal Endoscopy (ESGE) Technical Review. Endoscopy. 2018;50(4):423-46.
- Cholet F, et al. Efficacy of Small Bowel Preparation in Capsule Endoscopy for obscure gastrointestinal bleeding (Prepintest). ClinicalTricals. gov identifier NCT01267981.
- Beyna T, Arvanitakis M, Schneider M, Gerges C, Böing D, Devière J, et al. Motorised spiral enteroscopy: first prospective clinical feasibility study. Gut. févr 2021;70(2):261-7.
- Fraquelli M, Colli A, Casazza G, Paggi S, Colucci A, Massironi S, et al. Role of US in detection of Crohn disease: meta-analysis. Radiology. juill 2005;236(1):95-101.
- Horsthuis K, Bipat S, Bennink RJ, Stoker J. Inflammatory bowel disease diagnosed with US, MR, scintigraphy, and CT: meta-analysis of prospective studies. Radiology. avr 2008;247(1):64-79.
- Desmond AN, O’Regan K, Curran C, McWilliams S, Fitzgerald T, Maher MM, et al. Crohn’s disease: factors associated with exposure to high levels of diagnostic radiation. Gut. nov 2008;57(11):1524-9.
- Panés J, Bouzas R, Chaparro M, García-Sánchez V, Gisbert JP, Martínez de Guereñu B, et al. Systematic review: the use of ultrasonography, computed tomography and magnetic resonance imaging for the diagnosis, assessment of activity and abdominal complications of Crohn’s disease. Aliment Pharmacol Ther. juill 2011;34(2):125-45.
- Lee HS, Lim YJ, Shim KN, Moon CM, Song HJ, Kim JO, et al. Diagnostic Value of Small Bowel Capsule Endoscopy in Isolated Ileitis: A CAPENTRY Study. Dig Dis Sci. janv 2017;62(1):180-7.
- González-Suárez B, Rodriguez S, Ricart E, Ordás I, Rimola J, Díaz-González Á, et al. Comparison of Capsule Endoscopy and Magnetic Resonance Enterography for the Assessment of Small Bowel Lesions in Crohn’s Disease. Inflamm Bowel Dis. 19 mars 2018;24(4):775-80.
- Dray X, Houist G, Le Mouel JP, Saurin JC, Vanbiervliet G, Leandri C, et al. Prospective evaluation of third-generation small bowel capsule endoscopy videos by independent readers demonstrates poor reproducibility of cleanliness classifications. Clin Res Hepatol Gastroenterol. 16 mars 2021;45(6):101612.
- Heine GD, Hadithi M, Groenen MJ, Kuipers EJ, Jacobs MA, Mulder CJ. Double-balloon enteroscopy: indications, diagnostic yield, and complications in a series of 275 patients with suspected small-bowel disease. Endoscopy. janv 2006;38(1):42-8.
- Manes G, Imbesi V, Ardizzone S, Cassinotti A, Pallotta S, Porro GB. Use of double-balloon enteroscopy in the management of patients with Crohn’s disease: feasibility and diagnostic yield in a high-volume centre for inflammatory bowel disease. Surg Endosc. déc 2009;23(12):2790-5.
- ASGE Standards of Practice Committee, Gurudu SR, Bruining DH, Acosta RD, Eloubeidi MA, Faulx AL, et al. The role of endoscopy in the management of suspected small-bowel bleeding. Gastrointest Endosc. janv 2017;85(1):22-31.
- Gerson LB, Fidler JL, Cave DR, Leighton JA. ACG Clinical Guideline: Diagnosis and Management of Small Bowel Bleeding. Am J Gastroenterol. sept 2015;110(9):1265-87; quiz 1288.
- Becq A, Rahmi G, Perrod G, Cellier C. Hemorrhagic angiodysplasia of the digestive tract: pathogenesis, diagnosis, and management. Gastrointest Endosc. 2017;86(5):792-806.
- Nahon S, Hagège H, Latrive JP, Rosa I, Nalet B, Bour B, et al. Epidemiological and prognostic factors involved in upper gastrointestinal bleeding: results of a French prospective multicenter study. Endoscopy. nov 2012;44(11):998-1008.
- Chait MM. Lower gastrointestinal bleeding in the elderly. World J Gastrointest Endosc. 16 mai 2010;2(5):147-54.
- Longstreth GF. Epidemiology and outcome of patients hospitalized with acute lower gastrointestinal hemorrhage: a population-based study. Am J Gastroenterol. mars 1997;92(3):419-24.
- Pennazio M, Spada C, Eliakim R, Keuchel M, May A, Mulder CJ, et al. Small-bowel capsule endoscopy and device-assisted enteroscopy for diagnosis and treatment of small-bowel disorders: European Society of Gastrointestinal Endoscopy (ESGE) Clinical Guideline. Endoscopy. avr 2015;47(4):352-76.
- Rahmi G, Samaha E, Vahedi K, Delvaux M, Gay G, Lamouliatte H, et al. Long-term follow-up of patients undergoing capsule and double-balloon enteroscopy for identification and treatment of small-bowel vascular lesions: a prospective, multicenter study. Endoscopy. juill 2014;46(7):591-7.
- Spada C, McNamara D, Despott EJ, Adler S, Cash BD, Fernández-Urién I, et al. Performance measures for small-bowel endoscopy: A European Society of Gastrointestinal Endoscopy (ESGE) Quality Improvement Initiative. United Eur Gastroenterol J. juin 2019;7(5):614-41.
- Pennazio M, Rondonotti E, Despott EJ, Dray X, Keuchel M, Moreels T, et al. Small-bowel capsule endoscopy and device-assisted enteroscopy for diagnosis and treatment of small-bowel disorders: European Society of Gastrointestinal Endoscopy (ESGE) Guideline – Update 2022. Endoscopy. 24 nov 2022;
- Saperas E, Dot J, Videla S, Alvarez-Castells A, Perez-Lafuente M, Armengol JR, et al. Capsule endoscopy versus computed tomographic or standard angiography for the diagnosis of obscure gastrointestinal bleeding. Am J Gastroenterol. avr 2007;102(4):731-7.
- Wang Z, Chen J qiang, Liu J lu, Qin X gan, Huang Y. CT enterography in obscure gastrointestinal bleeding: a systematic review and meta-analysis. J Med Imaging Radiat Oncol. juin 2013;57(3):263-73.
- Schlag C, Menzel C, Nennstiel S, Neu B, Phillip V, Schuster T, et al. Emergency video capsule endoscopy in patients with acute severe GI bleeding and negative upper endoscopy results. Gastrointest Endosc. avr 2015;81(4):889-95.
- Beg S, Card T, Sidhu R, Wronska E, Ragunath K, UK capsule endoscopy users’ group. The impact of reader fatigue on the accuracy of capsule endoscopy interpretation. Dig Liver Dis Off J Ital Soc Gastroenterol Ital Assoc Study Liver. août 2021;53(8):1028-33.
- Pasha SF, Hara AK, Leighton JA. Diagnostic evaluation and management of obscure gastrointestinal bleeding: a changing paradigm. Gastroenterol Hepatol. déc 2009;5(12):839-50.
- García-Blázquez V, Vicente-Bártulos A, Olavarria-Delgado A, Plana MN, van der Winden D, Zamora J, et al. Accuracy of CT angiography in the diagnosis of acute gastrointestinal bleeding: systematic review and meta-analysis. Eur Radiol. mai 2013;23(5):1181-90.
- Voron T, Rahmi G, Bonnet S, Malamut G, Wind P, Cellier C, et al. Intraoperative Enteroscopy: Is There Still a Role? Gastrointest Endosc Clin N Am. janv 2017;27(1):153-70.
- Pasha SF, Leighton JA, Das A, Harrison ME, Decker GA, Fleischer DE, et al. Double-balloon enteroscopy and capsule endoscopy have comparable diagnostic yield in small-bowel disease: a meta-analysis. Clin Gastroenterol Hepatol Off Clin Pract J Am Gastroenterol Assoc. juin 2008;6(6):671-6.
- Mönkemüller K, Neumann H, Meyer F, Kuhn R, Malfertheiner P, Fry LC. A retrospective analysis of emergency double-balloon enteroscopy for small-bowel bleeding. Endoscopy. août 2009;41(8):715-7.
- Expert Panel on Interventional Radiology, Karuppasamy K, Kapoor BS, Fidelman N, Abujudeh H, Bartel TB, et al. ACR Appropriateness Criteria® Radiologic Management of Lower Gastrointestinal Tract Bleeding: 2021 Update. J Am Coll Radiol JACR. mai 2021;18(5S):S139-52.
- Van Binnebeek S, Vanbilloen B, Baete K, Terwinghe C, Koole M, Mottaghy FM, et al. Comparison of diagnostic accuracy of (111) In-pentetreotide SPECT and (68)Ga-DOTATOC PET/CT: A lesion-by-lesion analysis in patients with metastatic neuroendocrine tumours. Eur Radiol. mars 2016;26(3):900-9.
- Montravers F, Grahek D, Kerrou K, Ruszniewski P, de Beco V, Aide N, et al. Can fluorodihydroxyphenylalanine PET replace somatostatin receptor scintigraphy in patients with digestive endocrine tumors? J Nucl Med Off Publ Soc Nucl Med. sept 2006;47(9):1455-62.
Abréviations
VCE : Vidéo-capsule endoscopique
IRM : Imagerie par résonnance magnétique
TDM : Tomodensitométrie
SSIG : Suspicion de saignement de l’intestin grêle
PEG : Poly-éthylène glycol
HAS : Haute autorité de santé
MC : Maladie de Crohn
Tc99m : Technétium 99m
ESGE : Société européenne d’endoscopie digestive
TEP : Tomographie par émissions de positons
ASS : Analogues de la somatostatine
F-DOPA : 18F-dihydroxy-phénylalanine
TNE : tumeurs neuroendocrines
FDG : Fluorodésoxyglucose
Remerciements
Dr Antoine Guilloux, Pr Xavier Dray
Sorbonne Université, Centre d’Endoscopie Digestive, Hôpital Saint-Antoine, APHP, Paris, France. Dr Pauline Iorio
Sorbonne Université, Service de Radiologie, Hôpital Saint-Antoine, APHP, Paris, France.