Liens d’intérêt
AMBU ; MEDTRONIC
Mots-clés
Hématochézie ; Coloscopie ; Diverticules
Introduction
L’hémorragie digestive basse (HDB) se définit historiquement comme un saignement prenant son origine en aval de l’angle de Treitz. Avec l’amélioration des techniques d’exploration de l’intestin grêle (vidéo capsule, entéroscopie), il est communément admis aujourd’hui qu’une HDB correspond à un saignement prenant son origine en aval de la valvule de Bauhin, et correspond à un saignement ano-colorectal.
On définit une HDB aiguë comme un saignement récent (< 3 jours) pouvant entraîner une instabilité hémodynamique, une anémie, et/ ou la nécessité d’une transfusion sanguine. L’HDB chronique est définie par un saignement sur une période supérieure à 3 jours, impliquant en général une perte intermittente ou lente du sang.
Le saignement digestif bas est un motif de consultation fréquent, notamment aux urgences (9). Il est estimé que l’incidence est de 33 à 87/100 000 (10,11). Le sujet âgé est particulièrement concerné avec un risque relatif de 200 pour une personne de 80 ans comparé à 30 ans (12). L’arrêt spontané du saignement est constaté dans près de 80 % des cas, mais le risque de récidive est élevé, estimé à 10-15 % des cas (5,6). Le pronostic est meilleur que celui de l’hémorragie digestive haute. La mortalité globale est de 2 à 5 % (7,8). La morbi-mortalité est plus élevée chez la personne âgée et/ ou avec comorbidité(s) (7). De même, l’HDB intra-hospitalière est 2 à 3 fois plus mortelle en raison des comorbidités des patients (8).
Jusqu’à récemment, très peu de recommandations avaient été publiées sur le sujet, essentiellement américaines (13,14). Plus récemment des recommandations britanniques (15) puis européennes de l’ESGE (16) permettent de mieux appréhender le sujet.
Causes
Les causes d’HDB sont multiples et de nombreuses études ont évalué leur fréquence. Pour autant, le diagnostic étiologique n’est pas aisé et il est estimé qu’une cause n’est pas identifiée dans 23 % des cas (8). Le tableau 1 résume les différentes étiologies d’HDB et les éléments d’orientation de l’étiologie. La plus fréquente est le saignement diverticulaire. La cause diverticulaire est certaine pour 20 % des patients admis à l’hôpital, et fortement suspectée dans 15 % supplémentaires des cas lors du diagnostic de diverticules à la coloscopie sans autre cause identifiée. Les anti- inflammatoires (AINS, Aspirine) constituent un facteur de risque. Les diverticules sont souvent nombreux et il peut être difficile d’identifier le diverticule responsable lors de la coloscopie.
Les maladies ano-rectales sont la seconde cause d’hémorragie digestive basse. Le saignement hémorroïdaire est diagnostiqué pour 12 à 21 % des patients admis à l’hôpital, généralement pour un saignement limité en quantité et en durée, mais des saignements hémorroïdaires massifs sont possibles chez les patients âgés sous anticoagulants. En tout état de cause, il s’agit d’un diagnostic d’élimination.
Les autres causes incluent les différents types de colites (ischémique, infectieuse, inflammatoire, …), la rectopathie radique, le saignement iatrogène (post-résection de polypes), les anomalies vasculaires (angiectasies), et le cancer colorectal.
| Lésions Bénignes | Diverticules |
|---|
| Pathologie ano-rectale | Hémorroïdes |
| | Fissure anale |
| | Ulcère solitaire du rectum |
| | Prolapsus rectal |
| | Rectopathie radique |
| | Traumatisme |
| Lésions vasculaires | Angiectasies |
| | Rendu Osler |
| | Dieulafoy |
| | Varices coliques ou rectales |
| Colites | MICI |
| | Ischémique |
| | Infectieuses |
| | Indéterminées |
| Polypes | |
| Iatrogénique | Post-résection (polypectomie, mucosectomie, dissection sous-muqueuse) |
| Ulcère anastomotique chronique |
| Lésions Malignes | Cancer colorectal |
|---|
| Cancer anal |
| Métastases |
Tableau 1 : Causes des hémorragies digestives basses
Les facteurs de risques
Différents facteurs de risque ont été identifiés de manière inconstante dans la littérature. Le message le plus important est porté par une méta-analyse de 6 études qui conclut que les AINS et l’aspirine, facteur le plus constamment identifiés dans la littérature scientifique, augmentent significativement le risque relatif (RR) de saignement diverticulaire (RR = 2,48, 95 % CI 1,86-3,31) (17).
Diagnostic et évaluation initiale
L’HDB se manifeste par une extériorisation de sang rouge, pur ou de caillots mêlés aux matières fécales par l’anus appelée hématochézie. La rectorragie est une hématochézie dont l’origine est le rectum. Le terme sémiologique « rectorragie » est très largement utilisé à tort pour désigner un saignement digestif bas que celui-ci vienne du côlon ou du rectum.
L’abondance n’est pas évaluable cliniquement. L’émission de sang va toujours être impressionnante pour le patient et l’équipe soignante, mais ne préjuge pas de la gravité du saignement. En effet, un saignement d’hémorroïde interne peut être spectaculaire, pour autant une déglobulisation dans ce contexte est rarissime. On peut dire que la présence de caillots suggère un saignement plus abondant. Il existe de rares cas de méléna (selles noires correspondant à du sang digéré) secondaire à une hémorragie du côlon droit. Une hématochézie ne permet pas pour autant le diagnostic positif certain d’HDB. En effet, il peut s’agir d’un saignement massif d’origine haute. Entre 10 % et 15 % des patients présentant une hématochézie isolée ont une hémorragie digestive haute (5,18). Les facteurs prédictifs du risque d’avoir une hémorragie digestive haute en cas d’hématochézie sévère (transfusion ≥ 2 culots globulaires ou perte ≥ 2 points d’hémoglobine) sont la présence d’une hématémèse ou d’un méléna dans les 30 jours précédents, l’antécédent de cirrhose ou d’hémorragie digestive antérieure ou la prise récente d’aspirine ou d’AINS (19). Chez ces patients avec forte suspicion d’hémorragie digestive haute, une gastroscopie doit être effectuée en urgence après réanimation adéquate.
L’anamnèse, l’examen clinique comportant un toucher rectal et les paramètres hémodynamiques et un bilan sanguin doivent permettre un diagnostic d’hémorragie digestive, de suspecter l’origine basse, éventuellement de suspecter une étiologie et enfin d’évaluer la gravité de l’hémorragie. L’anamnèse permet de chercher des signes qui peuvent orienter le diagnostic étiologique. Ceux-ci sont résumés dans le tableau 2. Le bilan sanguin doit comprendre une NFS, un ionogramme sanguin et un bilan d’hémostase. Un groupage sanguin, rhésus et recherche d’agglutinines irrégulières (RAI) sont également importants dans l’optique d’une transfusion.
| Éléments à chercher | Cause suggérée |
|---|
| Antécédent de diverticules, prise récente d’AINS | Diverticules |
| Antécédent de chirurgie abdominale ou vasculaire, diarrhée et douleurs abdominales associées | Colite ischémique |
| Antécédent de maladie inflammatoire chronique des intestins | Colite inflammatoire |
| Antécédent d’irradiation abdomino-pelvienne | Rectopathie radique |
| Antécédent d’insuffisance rénale chronique, de rétrécissement aortique | Angiectasies |
| Perte de poids, altération de l’état général changement récent du transit ou de l’apparence des selles | Tumeur recto-colique |
Tableau 2 : Éléments d’orientation étiologique à rechercher à l’anamnèse
L’évaluation de la gravité de l’hémorragie est primordiale puisqu’elle va orienter la prise en charge. Elle consiste principalement à mesurer les constantes vitales [pression artérielle systolique (PAS), fréquence cardiaque (FC), saturation en oxygène], à chercher des signes de choc et d’hypovolémie. L’hémoglobine (comparée à une valeur de référence si disponible), le besoin transfusionnel et les comorbidités rentrent aussi en compte dans cette évaluation. La prise d’un traitement antiplaquettaire et/ ou anticoagulant est également à chercher. Il existe plusieurs scores de gravité au moins 7 décrits dans la littérature (Strate, NOBLADS, Sengupta, Oakland, Blatchford, AIMS65, and Charlson Comorbidity Index). Une étude comparative publiée en 2019 et évaluant pas moins de 7 scores montrait qu’aucun d’entre eux n’était particulièrement performant (3) pour prédire une hémorragie grave. En revanche, le score Oakland, ayant fait l’objet d’une publication en 2019, basé sur 7 critères clinico-biologiques (tableau 3) permet d’évaluer, à l’instar du score de Blatchford pour l’hémorragie haute, le retour à domicile peu risqué (< 5 % de risque) c’est-à-dire sans : récidive hémorragique, nécessité de transfusion, nécessité d’intervention pour hémostase, mortalité intra-hospitalière, ou réadmission pour HDB dans les 28 jours (4). Les recommandations européennes et britanniques stipulent que lorsqu’un patient a un score d’Oakland ≤ 8, le patient peut être renvoyé à son domicile avec un rendez-vous de suivi en ambulatoire programmé (15). Selon une métanalyse récente de 2022 (20), l’AUROC pour la prédiction d’une sortie possible sans évènement avec le score d’Oakland est de 0,86 (IC à 95 %, 0,82-0,88). Cette méta-analyse récente a également montré qu’il avait une performance élevée pour juger de la sévérité de l’hémorragie [AUROC 0,93 (IC à 95 %, 0,90-0,95)] et de la nécessité d’une transfusion [(AUROC 0,99 (IC à 95 %, 0,98-1,00)], mais ne permet pas de manière satisfaisante de prédire le recours à un traitement d’hémostase [(AUROC 0,36 (IC à 95 %, 0,32-0,40)].
| Variables | Valeurs |
|---|
| Age (années) | < 40 | 0 |
| 40-69 | 1 |
| ≥ 70 | 2 |
| Sexe | Femme | 0 |
| Homme | 1 |
| Antécédent d’hospitalisation pour HDB | Non | 0 |
| Oui | 1 |
| Toucher rectal | Absence de sang | 0 |
| Présence de sang | 1 |
| Fréquence cardiaque (battements/min) | < 70 | 0 |
| 70-89 | 1 |
| 90-109 | 2 |
| ≥ 110 | 3 |
| Pression artérielle systolique (mmHg) | < 90 | 5 |
| 90-119 | 4 |
| 120-129 | 3 |
| 130-159 | 2 |
| ≥ 160 | 0 |
| Hémoglobine (g/dl) | < 7 | 22 |
| 7,0-8,9 | 17 |
| 9,0-10,9 | 13 |
| 11,0-12,9 | 8 |
| 13,0-15,9 | 4 |
| ≥ 16 | 0 |
Tableau 3 : Score d’Oakland
Le score d’Oakland est utile pour prédire la bonne évolution des patients, mais aucun score n’est à présent validé prospectivement sur une cohorte indépendante à large échelle pour trier les patients stables et instables, autrement dit identifier les patients les plus graves. Les recommandations britanniques suggèrent d’utiliser le shock index. Le shock index (SI) est calculé comme le quotient de la fréquence cardiaque (FC) en nombre de battements par minute/ Pression artérielle systolique (PAS) en mmHg. Un patient avec un shock index > 1 est considéré comme un patient instable, un patient avec un shock index ≤ 1 est un patient considéré comme stable. Ce score a été inclus dans les recommandations britanniques pour sa simplicité et sa praticité, cependant il n’a été validé qu’en traumatologie, ce pourquoi il n’est pas repris dans les recommandations européennes plus récentes.
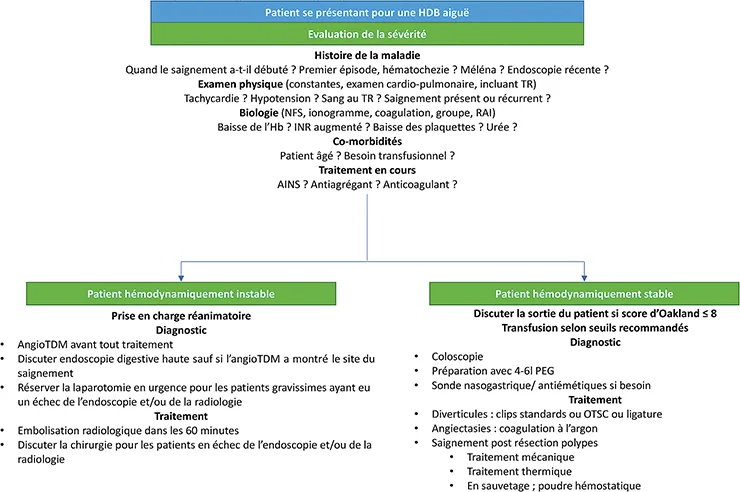
L’algorithme, présenté en figure 1, issue des recommandations de l’EGSE, résume les étapes de l’évaluation et classe les patients en deux groupes : patients instables/ stables afin de déterminer leur prise en charge. L’HDB grave représente 10 % des cas.

Figure 1 : Algorithme de prise en charge de l’hémorragie digestive basse, selon les recommandations de l’ESGE (2021)[16]
Conduite à tenir : diagnostic et management
Hospitalisation
En cas d’HDB aiguë, abondante, pouvant être définie par un score d’Oakland ≥ 8, une hospitalisation est, en général, la règle, et si l’état du patient le nécessite, en réanimation ou unité de soins critiques (15).
Mesures générales
En cas d’hémorragie sévère avec instabilité hémodynamique, les mesures de réanimation s’appuient sur un remplissage vasculaire intraveineux, voire l’adjonction de catécholamines, en urgence. L’objectif premier est de stabiliser le patient sur le plan hémodynamique. Dans cette situation, l’hémorragie pouvant être d’origine haute, une gastroscopie avec anesthésie générale doit être effectuée en urgence.
La transfusion de culots globulaires s’effectue selon une stratégie restrictive, à l’instar de l’hémorragie digestive haute. Chez les patients hémodynamiquement stables présentant une hémorragie digestive basse aiguë et sans antécédent de maladie cardiovasculaire, il est recommandé de transfuser en dessous d’un seuil d’hémoglobine 7 g/dL, avec une cible d’Hb de 7-9 g/dL. En cas de pathologie cardio-vasculaire, le seuil de transfusion est de 8 g/dl et la cible post-transfusionnelle est supérieure ou égale à 10 g/dl.
Geste hémostatique
Plusieurs options s’offrent pour le traitement, l’important est de choisir le bon geste et au bon moment. La coloscopie, l’artériographie et la chirurgie sont les modalités thérapeutiques à considérer. La coloscopie est de loin l’examen le plus pratiqué. L’angiotomodensitométrie (TDM), suivie d’une angiographie pour embolisation et exceptionnellement la chirurgie, sont réservées aux cas de saignements cataclysmiques. Moins de 1 % des patients avec HBD requiert une embolisation.
L‘évaluation de la gravité avec stratification du risque va orienter la prise en charge entre les patients stables et instables et déterminer la stratégie diagnostique et thérapeutique. L’algorithme de prise en charge est présenté en figure 1.
Cas des patients instables
- AngioTDM et artériographie
L’angioTDM, associée ou non à une artériographie, doit être proposée en première ligne dans certains cas sélectionnés. En effet cet examen doit être proposé en urgence chez les patients à haut risque ou avec saignement persistant, instables malgré les mesures de réanimation. Dans ces cas extrêmes, la coloscopie (qui nécessite une préparation !) n’est pas réalisable dans des bonnes conditions et dans un délai raisonnable. En effet, si peu d’HDB sont graves (10 %), surtout comparées aux hémorragies digestives hautes, elles existent et la mortalité n’est pas nulle. L’angioTDM est recommandée avant l’artériographie qui est un examen invasif, afin de déterminer la localisation de la source de l’hémorragie. L’angiographie est réalisée en cas de positivité de l’angioTDM. Cela consiste à la mise en place au niveau du vaisseau qui saigne de coils métalliques, de N-butyle cyanoacrylate ou de particules d’alcool polyvinylique. Les recommandations britanniques suggèrent que l’accès à l’artériographie devrait être possible dans les 60 minutes dans les centres ayant une équipe de radiologues interventionnels 24 h/24 (15).
En termes de performances, la source de saignement est localisée par angioTDM dans 27-70 % des cas (plus fréquemment en cas de patient instable), permettant une embolisation super-sélective dans 93-100 % des cas, avec des taux de récidive à court terme entre 10 et 50 % (15,21-23). L’ischémie digestive est la complication la plus fréquente (7-24 %) (15,21). À noter que dans certains cas, une embolisation empirique peut être effectuée quand le site de saignement n’a pas été identifié à l’angioTDM, notamment en cas de tumeur. Cela étant, la balance avec le risque d’ischémie doit être évaluée au cas par cas en l’absence de données claires (15).
Plusieurs études ont comparé l’intervention radiologique à la coloscopie, ne montrant pas de bénéfice de l’un par rapport à l’autre en termes de survie et de récidive hémorragique notamment (24,25).
Le rôle de la chirurgie dans le contexte de l’HDB est très limité. Elle n’est recommandée que dans les cas où tous les autres moyens ont été mis en œuvre pour traiter l’hémorragie, sans succès. La résection doit être la plus limitée possible, ce qui peut être complexe lorsque la source du saignement n’a pas pu être identifiée. Les résections les plus courtes sont associées à une morbi-mortalité plus faible (15).
Cas des patients stables
Chez les patients stables ou ayant pu être stabilisés, la coloscopie est l’examen le plus pratiqué dans le contexte d’une HDB. Il présente l’avantage de permettre un diagnostic étiologique et un traitement hémostatique dans la foulée. Cet examen doit être réalisé si possible sous anesthésie générale et requiert donc une consultation d’anesthésie en urgence.
Une préparation colique de bonne qualité est primordiale afin de maximiser la probabilité de localiser le saignement (bonne visualisation de la muqueuse colique), mais également afin d’optimiser les conditions dans lesquelles le geste d’hémostase est réalisé. Le taux de coloscopie complète est strictement corrélé à la bonne prise d’une préparation et à sa qualité (26). La préparation est généralement réalisée par du polyéthylène glycol (PEG) soit par voie orale ou par sonde naso-gastrique (33 % des cas). Il est recommandé l’administration de gros volumes (5 à 6 litres) rapidement (en 3 à 4 heures) (24,27). L’apparition de troubles hydro-électrolytiques doit être surveillée dans ce contexte. La coloscopie doit être effectuée après l’obtention de selles claires. Un agent prokinétique peut être administré afin de diminuer les nausées et donc (en théorie) le risque d’inhalation, notamment chez les personnes âgées. La sonde naso-gastrique sera généralement préférée dans ces cas-là (ou si intolérance à la voie orale).
Le timing optimal de la coloscopie a fait l’objet de nombreuses études et recommandations. Globalement, il n’y a pas de différence en termes de récidive et nombre de culots globulaires nécessaires entre coloscopie précoce et retardée, mais la rentabilité diagnostique et la durée d’hospitalisation est raccourcie en cas de coloscopie précoce (< 24 heures) (28). Les recommandations britanniques stipulent que la coloscopie doit être réalisée dès que possible si le patient est stable avec saignement actif (15). Les recommandations américaines stipulent que la coloscopie doit être réalisée dans les 24 heures en cas de saignement actif considéré à risque et dès que possible si le patient n’est pas à haut risque (14). Ainsi, la décision de réaliser la coloscopie et de son délai de réalisation doivent être avant tout pragmatiques. Si le patient a un saignement actif et est instable, une angioTDM suivie d’une artériographie avec embolisation doit être discutée. Il faut alors également penser à éliminer une origine haute si suspectée, dans le cas où le patient est stabilisable. Si le patient est à haut risque ou présente des signes de saignement actif persistant, une coloscopie doit être effectuée après stabilisation et préparation dans les premières 24 heures afin d’optimiser les rendements diagnostique et thérapeutique. En l’absence de facteur clinique de haut risque, de comorbidité sévère, ou de saignement persistant, la coloscopie devrait être réalisée lors du prochain créneau disponible, idéalement dans les 72 heures après l’admission.
La coloscopie revêt un rôle diagnostique et potentiellement thérapeutique. En termes de performances, la cause de saignement est identifiée dans plus de 75 % des cas en général. Un traitement hémostatique est réalisé dans 3 à 35 % des cas devant un saignement actif ou bien en cas de stigmates de saignement (7,18,24,27). Les études principales évaluant les performances de la coloscopie dans l’HDB sont résumées dans le tableau 4.
| Méthodologie | Coloscopie incomplète | Délai | Diagnostic positif | Geste thérapeutique | Complication |
|---|
| Jensen (27) | 121 Prospectif non randomisé | 7 % | 6-12h | 85 % | 20 % | 0% |
| Strate (25) | 144 Rétrospectif | 5 % | Médiane 25h | 89 % | 10 % | – |
| Green (24) | 50 Prospectif randomisé | – | Moyenne 7h | 96 % | 34 % | 2 % |
| Laine (18) | 72 Prospectif randomisé | 7 % | <12h (36 patients)
36 à 60h (36 patients) | 72 % | 3 % | 1 % |
Tableau 4 : Performances de la coloscopie pour hémorragie digestive basse
Lors de la coloscopie, il est préférable de cathétériser l’iléon terminal afin d’en évaluer les derniers centimètres. En effet, la présence de sang peut suggérer un saignement d’origine haute, notamment si la coloscopie est non contributive par ailleurs. Aussi, un retrait minutieux du coloscope avec nettoyage de la muqueuse (résidus de selles et de sang) à l’aide d’une pompe de lavage permet de maximiser la qualité de l’examen et sa rentabilité. L’utilisation d’un capuchon transparent à l’extrémité du coloscope est un facteur indépendant pour identifier la lésion hémorragique, tout comme l’utilisation de la pompe de lavage (29). La coloscopie doit être effectuée dans un environnement adapté, une unité d’endoscopie idéalement, et à défaut dans une unité de réanimation ou de soins intensifs.
Lorsqu’une cause est identifiée, un geste d’hémostase est recommandé en cas de saignement actif (en jet ou suintement en nappe) ou en cas de signe de haut risque de saignement : un vaisseau visible ou un caillot adhérent. Le choix de la technique d’hémostase est laissé à l’appréciation de l’endoscopiste. Son choix va dépendre de son expérience, de ses habitudes, mais également de la cause du saignement et des conditions de l’examen (visualisation de la zone à traiter, apparence de la lésion). Parmi les traitements ‘classiques’, on distingue : l’injection sous muqueuse de sérum adrénaliné (dilution d’adrénaline à 1/10 000) afin d’induire une vasoconstriction des vaisseaux (traitement temporaire à associer à une autre technique) ; les clips métalliques qui permettent une compression mécanique des vaisseaux ; l’électrocoagulation bipolaire avec une sonde au contact de la zone à traiter ou l’électrocoagulation monopolaire par plasma argon sans contact entre la sonde et la zone à traiter. Parmi les traitements plus récents, on peut noter l’arrivée depuis quelques années de poudres hémostatiques, solution de dernier recours, permettant la création temporaire d’une barrière mécanique empêchant le saignement mais induisant également une activation chimique des facteurs de la coagulation. Enfin, on peut citer les clips trans-muraux (OTSC – over the scope clip) qui permettent une compression mécanique d’un vaisseau plus large et/ ou profond, avec des données encore limitées mais très encourageantes (2).
En cas d’électrocoagulation au plasma argon, une préparation complète, même si on ne traite que le rectum (cas de la rectopathie radique), est nécessaire afin d’évacuer les gaz fermentant qui peuvent être à l’origine d’une explosion lors de l’application du plasma argon. L’électrocoagulation doit se faire avec des réglages de faible puissance en dehors du rectum (paroi épaisse et sous péritonéal), afin de réduire le risque de perforation. Pour le côlon, on utilise généralement le mode Precise APC, effet 5, débit 0,8 litre/min. Pour le traitement de la rectopathie radique, on utilise plutôt le mode Pulsed APC, effet 2, débit 0,8 litre/min (réglages pour le ViO3 ERBE, Tuebingen | Germany). Le taux rapporté de complication lors d’une hémostase endoscopique dans le contexte d’une HBD est faible (0,3 % à 1,3 %) (25).
Les traitements d’hémostase de référence en fonction de l’étiologie de l’HDB sont résumés dans le tableau 5. En cas de saignement diverticulaire, toute technique d’hémostase peut être utilisée, mais la pose de clip au niveau du collet du diverticule (zone d’origine du saignement en général) est à privilégier en raison de leur disponibilité, simplicité d’utilisation, efficacité et profil de sécurité. En effet, le risque de perforation étant majoré au niveau du diverticule, l’électrocoagulation semble plus risquée. Des publications suggèrent une efficacité de la ligature de diverticules, similaire aux clips métalliques, avec un risque de récidive moindre (1). Les clips OTSC semble également une nouvelle option séduisante, avec une étude rétrospective de 36 cas au Japon, qui rapporte un succès technique de 100 %, et l’absence de recours à la chirurgie et à l’embolisation pour les 36 patients, avec 3 récidives hémorragiques, retraitées par un nouveau clip OTSC (2).
| Cause | Traitement d’hémostase |
|---|
| Diverticule | TOUT |
| Angiectasie | Plasma argon |
| Post-polypectomie/mucosectomie | Sérum adrénaliné + clips ou électrocoagulation mono ou bipolaire |
| Rectopathie radique | Plasma argon |
Tableau 5 : Traitements d’hémostase en fonction de l’étiologie de l’hémorragie digestive basse
En cas de saignement après résection de polype (polypectomie, mucosectomie), les clips semblent supérieurs à l’électrocoagulation. Le contexte oriente sur la(les) localisation(s) possible(s) du saignement (relecture du compte rendu de la coloscopie récente). Il ne faut pas oublier qu’un saignement retardé (jusqu’à 10 jours après la résection) est possible. Les facteurs de risque sont : polype > 2 cm, pied large pour les polypes pédiculés, polype localisé dans le côlon droit, reprise de traitement antiagrégant/ anticoagulant.
L’électrocoagulation au plasma argon a été prouvée comme efficace dans le traitement des angiectasies et présente l’avantage d’être moins cher que l’électrocoagulation bipolaire. Une injection sous muqueuse est suggérée en cas de lésion supérieure à 1 cm de grand axe et/ ou localisée dans le côlon droit/ cæcum (paroi fine !), afin de réduire le risque de perforation. En cas de saignement d’origine néoplasique, l’endoscopiste est souvent démuni, la poudre hémostatique étant le seul traitement pouvant être efficace, mais le plus souvent temporairement.
Les colites (ischémiques, infectieuses, inflammatoires) ne relèvent pas d’un traitement endoscopique. La colite ischémique va se caractériser par un respect du rectum (doté d’une double vascularisation) et une transition abrupte entre la muqueuse saine et ischémique. Il n’existe pas de signe pathognomonique d’où l’importance de l’évaluation initiale en termes d’orientation. Pour les autres types de coliques, les lésions hémorragiques saignent en général a minima.
En cas d’échec d’hémostase endoscopique ou de récidive hémorragique, il n’y a pas de recommandation spécifique et il existe peu de données dans la littérature. Une seconde coloscopie peut être effectuée en cas de saignement actif et si les conditions de préparation n’étaient pas optimales lors de la première coloscopie. Le chirurgien doit être informé en cas d’échec d’hémostase.
La récidive hémorragique est fréquente en cas d’origine diverticulaire (9-47 %) ou d’angiectasie (58-64 % à 2 ans) (30-32). Les diverticules sont multiples et la technique d’hémostase peut être complexe. De nouvelles angiectasies peuvent apparaître ou des lésions synchrones avoir été ratées lors d’une première endoscopie.
Dans le contexte d’une HDB, la rectosigmoïdoscopie a une place très limitée. La tentation de réaliser un examen court, sans préparation complexe, sans anesthésie est grande. Pour autant, la rentabilité de cet examen est très faible et il ne doit donc pas être demandé dans ce contexte. Même pour une rectopathie radique, une préparation complète est indispensable.
Gestion des antiagrégants et des anticoagulants
L’utilisation des anticoagulants et des antiagrégants est rapporté chez plus de 30 % des patients ayant une HDB aiguë, avec 2 à 5 % des patients recevant des thérapies complexes, incluant une bithérapie antiagrégante, ou une combinaison d’anticoagulant et d’antiagrégant plaquettaire (8,33). La prise en charge de ces traitements antithrombotiques nécessite généralement une approche multidisciplinaire en fonction du risque de récidive hémorragique, et de thrombose. La littérature scientifique est très pauvre pour l’hémorragie digestive basse, les données sont issues de la prise en charge des hémorragies hautes, ou de toute hémorragie. Une méta-analyse incluant 43 essais randomisés contrôlés a montré que l’anticoagulation par dabigatran et rivaroxaban était liée à une augmentation du risque de saignements digestifs en comparaison avec les anticoagulants conventionnels (AVK) (OR > 1,7) (34). Cependant le risque pour l’HDB n’était pas significatif entre les deux groupes (OR = 0,88).
La correction des paramètres hémostatiques est une urgence, mais elle ne doit pas retarder un geste d’hémostase. Si une coloscopie est envisagée, l’obtention de paramètres d’hémostase satisfaisants avant le geste est moins importante que s’il s’agissait d’un examen programmé.
Le tableau 6 résume la gestion des antiagrégants et anticoagulants selon les recommandations européennes de l’ESGE de 2021.
| Anticoagulants | Antiagrégants |
|---|
| L’ESGE suggère de ne pas interrompre les AVK (antivitamine K) ou les AOD (anticoagulant direct) chez les patients ayant une hémorragie digestive de faible abondance, soit un score d’Oakland ≤ 8 Recommandation faible, niveau de preuve faible | L’ESGE ne recommande pas la transfusion de plaquettes, en routine, chez les patients avec hémorragie digestive basse, prenant des antiagrégants. Recommandation forte, faible niveau de preuve. |
| L’ESGE recommande d’arrêter les AVK ou les AOD chez les patients ayant une hémorragie abondante et de corriger les paramètres de la coagulation selon la sévérité de l’hémorragie, et le risque thrombotique. Recommandation forte, niveau de preuve faible | L’ESGE recommande l’arrêt de l’aspirine chez les patients prenant de l’aspirine en prévention cardiovasculaire primaire et considérer l’arrêt permanent en fonction de l’avis du spécialiste référent. Recommandation forte, faible niveau de preuve. | L’ESGE ne recommande pas l’arrêt de l’aspirine chez les patients prenant une faible dose d’aspirine en prévention secondaire d’un évènement cardio-vasculaire. Si l’aspirine est interrompue, elle doit être reprise au plus vite, préférablement dans les 5 jours, ou plus rapidement si hémostase a été effectuée et en l’absence de signe de saignement. Recommandation forte, niveau de preuve moyen. |
| Chez les patients ayant une instabilité hémodynamique, sous AVK, il est recommandé d’administrer en intraveineux de la vitamine K et du PPSP ou à défaut des PFC en l’absence de PPSB disponible. Recommandation forte, niveau de preuve faible | Chez les patients ayant une instabilité hémodynamique, sous AOD, l’ESGE suggère l’utilisation des antidotes (idarucizumab pour le dabigatran, et l’andexanet ou le PPSB chez les patients traités par un anti-facteur Xa) en coordination/consultation avec les spécialiste de l’hémostase si le saignement est persistant et/ou récurrent avec instabilité hémodynamique. Recommandation faible, niveau de preuve faible | L’ESGE ne recommande pas, en routine, l’arrêt de la bi-antiagrégation (faible dose d’aspirine et antagoniste du récepteur P2Y12) avant un avis cardiologique. La poursuite de l’aspirine est recommandée, l’antagoniste du récepteur P2Y12 peut être continué ou arrêté en fonction de la sévérité de l’hémorragie et du risque ischémique. Si l’antagoniste du récepteur P2Y12 est arrêté, il doit être repris dans les 5 jours s’il est toujours indiqué. Recommandation forte, faible niveau de preuve. |
| L’ESGE recommande de reprendre les anticoagulants après une hémorragie digestive basse si en cas d’indication d’anticoagulation à long terme. Recommandation forte, niveau de preuve moyen. | |
| L’ESGE recommande de reprendre l’anticoagulation (AVK ou AOD) le plus rapidement possible à partir de 7 jours après l’interruption. Recommandation faible, niveau de preuve faible. | |
| Chez les patients à haut risque de thrombose, une reprise de l’anticoagulation plus rapide est recommandée, préférablement dans les 72h, par héparine en thérapie temporaire. Forte recommandation, niveau de preuve très bas. | |
Tableau 6 : Recommandations de l’ESGE (2021)16 sur la gestion des anticoagulants et antiagrégants lors d’une hémorragie digestive basse
Conclusion
L’hémorragie digestive basse présente une situation clinique très hétérogène et variée. Elle cesse spontanément dans la majorité des cas, mais la récidive est fréquente. La morbi-mortalité n’est pas négligeable, notamment chez la personne âgée. Les causes les plus fréquentes sont les diverticules, les hémorroïdes et les colites. L’anamnèse, un examen clinique et un bilan sanguin constituent la prise en charge initiale, avec pour objectif de faire le diagnostic positif d’HDB et de déterminer sa gravité, voire la cause potentielle. Une fois les mesures générales mises en œuvre (décision d’hospitalisation, stabilisation, transfusion), le degré de gravité et l’aspect actif ou non du saignement doivent conduire à décider soit d’une coloscopie après préparation colique (rapide ou quand possible) soit d’une angioTDM suivie éventuellement d’une artério-embolisation. Cette seconde option est beaucoup moins souvent nécessaire, mais revêt un caractère urgent à très court terme en cas d’hémorragie grave avec patient non stabilisable. Une gastroscopie doit être envisagée en cas de doute avec une hémorragie d’origine haute. L’hémostase endoscopique est réalisée si une lésion avec saignement actif ou signes de saignement récents est identifiée. Elle s’appuie principalement sur la pose de clips métalliques (standards ou OTSC) ou l’électrocoagulation mono/ bipolaire.
Bibliographie
- Okamoto N, Tominaga N, Sakata Y, et Lower Rebleeding Rate after Endoscopic Band Ligation than Endoscopic Clipping of the Same Colonic Diverticular Hemorrhagic Lesion: A Historical Multicenter Trial in Saga, Japan. Intern Med Tokyo Jpn 2019; 58: 633–638.
- Kawano K, Takenaka M, Kawano R, et Efficacy of Over-The-Scope Clip Method as a Novel Hemostatic Therapy for Colonic Diverticular Bleeding. J Clin Med 2021; 10: 2891.
- Tapaskar N, Jones B, Mei S, et Comparison of clinical prediction tools and identification of risk factors for adverse outcomes in acute lower GI bleeding. Gastrointest Endosc 2019; 89: 1005-1013.e2.
- Oakland K, Jairath V, Uberoi R, et Derivation and validation of a novel risk score for safe discharge after acute lower gastrointestinal bleeding: a modelling study. Lancet Gastroenterol Hepatol 2017; 2: 635–643.
- Farrell JJ, Friedman Review article: the management of lower gastrointestinal bleeding. Aliment Pharmacol Ther 2005; 21: 1281–1298.
- Wong Kee Song LM, Baron Endoscopic management of acute lower gastrointestinal bleeding. Am J Gastroenterol 2008; 103: 1881–1887.
- Strate LL, Ayanian JZ, Kotler G, et Risk factors for mortality in lower intestinal bleeding. Clin Gastroenterol Hepatol Off Clin Pract J Am Gastroenterol Assoc 2008; 6: 1004–1010; quiz 955-.
- Oakland K, Guy R, Uberoi R, et al. Acute lower GI bleeding in the UK: patient characteristics, interventions and outcomes in the first nationwide audit. Gut 2018; 67: 654–662.
- Newman J, Fitzgerald JEF, Gupta S, et al. Outcome predictors in acute surgical admissions for lower gastrointestinal Colorectal Dis Off J Assoc Coloproctology G B Irel 2012; 14: 1020–1026.
- Lanas A, García-Rodríguez LA, Polo-Tomás M, et Time trends and impact of upper and lower gastrointestinal bleeding and perforation in clinical practice. Am J Gastroenterol 2009; 104: 1633–1641.
- Jp H, S G, E K, et al. Lower gastrointestinal bleeding: incidence, etiology, and outcomes in a population-based Eur J Gastroenterol Hepatol; 25. Epub ahead of print January 2013. DOI: 10.1097/MEG.0b013e32835948e3.
- Longstreth GF. Epidemiology and outcome of patients hospitalized with acute lower gastrointestinal hemorrhage: a population-based Am J Gastroenterol 1997; 92: 419–424.
- ASGE Standards of Practice Committee, Pasha SF, Shergill A, et The role of endoscopy in the patient with lower GI bleeding. Gastrointest Endosc 2014; 79: 875–885.
- Strate LL, Gralnek ACG Clinical Guideline: Management of Patients With Acute Lower Gastrointestinal Bleeding. Am J Gastroenterol 2016; 111: 459–474.
- Oakland K, Chadwick G, East JE, et al. Diagnosis and management of acute lower gastrointestinal bleeding: guidelines from the British Society of Gastroenterology. Gut 2019; 68: 776–789.
- Triantafyllou K, Gkolfakis P, Gralnek IM, et al. Diagnosis and management of acute lower gastrointestinal bleeding: European Society of Gastrointestinal Endoscopy (ESGE) Endoscopy 2021; 53: 850–868.
- Yuhara H, Corley DA, Nakahara F, et Aspirin and non-aspirin NSAIDs increase risk of colonic diverticular bleeding: a systematic review and meta-analysis. J Gastroenterol 2014; 49: 992–1000.
- Laine L, Shah Randomized trial of urgent vs. elective colonoscopy in patients hospitalized with lower GI bleeding. Am J Gastroenterol 2010; 105: 2636–2641; quiz 2642.
- Camus M, Khungar V, Jensen DM, et Origin, Clinical Characteristics and 30-Day Outcomes of Severe Hematochezia in Cirrhotics and Non-cirrhotics. Dig Dis Sci 2016; 61: 2732–2740.
- Almaghrabi M, Gandhi M, Guizzetti L, et al. Comparison of Risk Scores for Lower Gastrointestinal Bleeding: A Systematic Review and Meta-analysis. JAMA Netw Open 2022; 5:
- Rossetti A, Buchs NC, Breguet R, et Transarterial embolization in acute colonic bleeding: review of 11 years of experience and long-term results. Int J Colorectal Dis 2013; 28: 777–782.
- Yata S, Ihaya T, Kaminou T, et Transcatheter arterial embolization of acute arterial bleeding in the upper and lower gastrointestinal tract with N-butyl-2-cyanoacrylate. J Vasc Interv Radiol JVIR 2013; 24: 422–431.
- Yi WS, Garg G, Sava Localization and definitive control of lower gastrointestinal bleeding with angiography and embolization. Am Surg 2013; 79: 375–380.
- Green BT, Rockey DC, Portwood G, et Urgent colonoscopy for evaluation and management of acute lower gastrointestinal hemorrhage: a randomized controlled trial. Am J Gastroenterol 2005; 100: 2395–2402.
- Strate LL, Naumann The role of colonoscopy and radiological procedures in the management of acute lower intestinal bleeding. Clin Gastroenterol Hepatol Off Clin Pract J Am Gastroenterol Assoc 2010; 8: 333–343; quiz e44.
- Ohyama T, Sakurai Y, Ito M, et al. Analysis of urgent colonoscopy for lower gastrointestinal tract Digestion 2000; 61: 189–192.
- Jensen DM, Machicado GA, Jutabha R, et al. Urgent colonoscopy for the diagnosis and treatment of severe diverticular N Engl J Med 2000; 342: 78–82.
- Oakland K, Isherwood J, Lahiff C, et al. Diagnostic and therapeutic treatment modalities for acute lower gastrointestinal bleeding: a systematic Endosc Int Open 2017; 5: E959–E973.
- Niikura R, Nagata N, Aoki T, et al. Predictors for identification of stigmata of recent hemorrhage on colonic diverticula in lower gastrointestinal J Clin Gastroenterol 2015; 49: e24-30.
- Aytac E, Stocchi L, Gorgun E, et Risk of recurrence and long-term outcomes after colonic diverticular bleeding. Int J Colorectal Dis 2014;29: 373–378.
- Becq A, Rahmi G, Perrod G, et al. Hemorrhagic angiodysplasia of the digestive tract: pathogenesis, diagnosis, and Gastrointest Endosc 2017; 86: 792–806.
- Swanson E, Mahgoub A, MacDonald R, et Medical and endoscopic therapies for angiodysplasia and gastric antral vascular ectasia: a systematic review. Clin Gastroenterol Hepatol Off Clin Pract J Am Gastroenterol Assoc 2014; 12: 571–582.
- Radaelli F, Frazzoni L, Repici A, et Clinical management and patient outcomes of acute lower gastrointestinal bleeding. A multicenter, prospective, cohort study. Dig Liver Dis Off J Ital Soc Gastroenterol Ital Assoc Study Liver 2021; 53: 1141–1147.
- Miller CS, Dorreen A, Martel M, et Risk of Gastrointestinal Bleeding in Patients Taking Non-Vitamin K Antagonist Oral Anticoagulants: A Systematic Review and Meta-analysis. Clin Gastroenterol Hepatol Off Clin Pract J Am Gastroenterol Assoc 2017; 15: 1674-1683.e3.
Abréviations
AOD : anticoagulants oraux directs
AVK : antivitamine K
ESGE : European Society of Gastrointestinal Endoscopy
HDB : hémorragie digestive basse
RAI : recherche d’agglutinines irrégulières
PAS : pression artérielle systolique
FC : fréquence cardiaque
TDM : tomodensitométrie