Liens d’intérêt
L’auteure déclare n’avoir aucun lien d’intérêt en rapport avec sa communication
Mots-clés
Proctologie ; Traitement instrumental hémorroïdaire ; Suppurations ano-périnéales
Introduction
En consultation de proctologie, plusieurs gestes sont réalisables avec ou sans anesthésie locale, dans un contexte d’urgence ou pas. Ces gestes sont le plus souvent simples, efficaces et les patients en sont volontiers reconnaissants (1). Si vous avez envie de vous y mettre, ce manuscrit vous donnera une idée précise des principaux instruments dont il faut s’équiper, des gestes possibles, ainsi que de leurs indications, contre-indications et précautions d’emploi.
Outils nécessaires pour pratiquer des gestes locaux en consultation de proctologie
Pour pouvoir pratiquer les gestes listés ci-dessous, vous allez devoir vous équiper dans votre cabinet de consultation des instruments suivants (tableau 1).
Tableau 1 : Équipement d’un box de consultation de proctologie- Table d’examen au mieux à hauteur réglable
- Bonne source lumineuse orientable
- Lumière froide
- Anuscopes/rectoscopes rigides
- Photocoagulateur infrarouge + capuchons
- Bistouri électrique avec pointes courtes et longues
- Gants non stériles/compresses stériles/produit désinfectant
- Ligateurs élastiques (plusieurs tailles disponibles : 11 et 13 mm)
- Lidocaïne injectable 10 mg/ml
- Seringues de 10 ml/aiguilles sous cutanées 25G et aiguilles pompeuses 18G/prolongateurs
- Bistouris à lame froide
- Cotons tiges
- Pince à biopsie/punch à biopsie
- Bâtons de nitrate d’argent
- Pansements : hydrofibres/alginates/hydrocellulaires/hydrocolloïdes/non tissés auto-adhésifs
- Kits pour écouvillonnage anal
- Flacons pour biopsie et feuilles de renseignement histologique
- Antalgiques palier 1 et 2
- Crème apaisante et réparatrice
|
Le traitement instrumental de la pathologie hémorroïdaire
La prise en charge de la pathologie hémorroïdaire interne
Environ 40 % de la population générale adulte aurait une pathologie hémorroïdaire interne symptomatique (2). Les symptômes hémorroïdaires internes sont principalement les saignements, le prolapsus et parfois une gêne anale, rarement une vraie douleur. Dans un premier temps, des mesures hygiéno-diététiques (régime riche en fibres) associées à des traitements régulateurs du transit sont prescrits (3). La régularisation du transit est en effet la seule mesure préventive au long cours ayant démontré son efficacité sur les symptômes hémorroïdaires (8,4). En dehors du prolapsus de grade IV de Goligher qui relève plutôt d’une prise en charge chirurgicale, les recommandations françaises (3) et européennes (5) réservent les traitements instrumentaux aux autres grades en cas d’échec du traitement médical (6).
Le principe de ces traitements instrumentaux est de provoquer au sommet des plexus hémorroïdaires internes une fibrose cicatricielle permettant une fixation de la muqueuse anale au plan musculaire sous-jacent et une obturation du réseau vasculaire sous-muqueux issu de l’artère rectale supérieure. Les traitements disponibles sont la photocoagulation infrarouge, la ligature élastique et l’injection sclérosante qu’on ne va pas aborder. En effet, plus aucun produit sclérosant ayant l’autorisation de mise sur le marché dans le traitement de la pathologie hémorroïdaire n’est désormais commercialisé en France. Ceci étant dit, l’efficacité des injections sclérosantes n’était pas supérieure à celle des autres techniques en plus de quelques complications septiques sévères qui ont été décrites.
La photocoagulation infrarouge
Indication
Son indication optimale est les saignements hémorroïdaires avec peu de prolapsus (grades I-II).
Précautions d’utilisation
- Il n’est pas nécessaire de proposer une préparation rectale ou une antibioprophylaxie.
- Ce traitement est contre-indiqué chez la femme enceinte et les patients ayant une maladie inflammatoire chronique de l’intestin active au niveau ano-périnéal.
- Il est également contre-indiqué en cas de troubles de l’hémostase ou de la coagulation, inné ou acquis (traitement anticoagulant ou antiagrégant en dehors de l’aspirine qui ne pose pas de problème).
- Il peut être réalisé prudemment chez des patients ayant une immunodépression ou ayant une ano-rectite radique.
- Il est possible de prescrire un antalgique et des laxatifs avant et après le geste.
- Il est conseillé au patient de ne pas voyager durant les 2 semaines qui suivent le geste afin de gérer au mieux les complications hémorragiques si elles surviennent.
Matériel et déroulement
- Ce traitement thermique nécessite un appareil de photocoagulation infrarouge.
- Ce geste ne nécessite pas d’anesthésie.
- Le réglage de la durée de l’impact se fait selon la taille du paquet hémorroïdaire à traiter et les précédents traitements pratiqués (degré de fibrose) ; il varie entre 0,5 à 2 secondes (le plus souvent entre 0,8 à 1,2 secondes).
- Un capuchon à usage unique doit être mise sur l’embout teflonné pour le protéger avant l’utilisation.
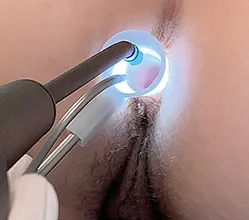
- Les impacts provoquant un blanchiment de la muqueuse se font à travers un anuscope, à la partie haute des hémorroïdes internes, en zone insensible (figure 1).

Figure 1 : Application
de photocoagulation infrarouge dans le canal anal
- Plusieurs impacts peuvent être réalisables pendant la même séance sur la circonférence anale (tige du photocoagulateur orientable) et peuvent varier de 2 à 9 impacts selon la tolérance du patient et les symptômes hémorroïdaires.
- La cicatrisation se fait en trois semaines environ. Elle laisse une cicatrise fibreuse locale par coagulation des petits vaisseaux.
- Il est souvent conseillé de réaliser plusieurs séances pour avoir une amélioration symptomatique (en moyenne 2 à 3 séances espacées d’un minimum de quatre semaines).
Suites immédiates
- Une sensation de chaleur est fréquemment décrite par les patients lors de la coagulation sans réelle douleur.
- Ce geste permet une reprise immédiate des activités quotidiennes.
Effets secondaires
Le patient doit en être informé avant le geste (feuille d’information à donner) avec une conduite à tenir définie pour chaque effet secondaire éventuel.
- Une gêne (environ 25 % des patients), voire des douleurs anales modérées peuvent survenir après le geste et persister jusqu’à 48 heures, aisément soulagées par un antalgique de palier 1.
- Une réaction vagale « exceptionnelle » peut survenir au moment du geste ou dans les suites immédiates. Il est alors conseillé aux patients « sensibles » de venir accompagnés ou de patienter un peu en salle d’attente avant de repartir.
- Des saignements minimes sont fréquents tandis que le saignement abondant par chute d’escarre, pouvant survenir jusqu’à J15, est exceptionnel.
Efficacité
Les études montrent une amélioration, voire une disparition des symptômes dans 50 à 90 % des cas (7). En revanche, à un an, l’efficacité de la photocoagulation infrarouge baisse à 40 % (8). Il est cependant possible de refaire d’autres séances d’entretien.
La Ligature élastique
Indication
Il s’agit d’un traitement mécanique consistant à ligaturer le sommet des paquets hémorroïdaires internes.
Son utilisation est indiquée pour les saignements hémorroïdaires et le prolapsus modéré de grade II ou III.
Précautions d’utilisation
- il n’est pas nécessaire de proposer une préparation rectale.
- Ce traitement contre-indiqué chez la femme enceinte et les patients ayant une maladie inflammatoire chronique de l’intestin active sur le plan ano-périnéal.
- Il est contre-indiqué chez des patients ayant une immunodépression ou ayant une ano-rectite radique.
- Il est également contre-indiqué en cas de troubles de l’hémostase ou de la coagulation, inné ou acquis (traitement anticoagulant ou antiagrégant en dehors de l’aspirine qui ne pose pas de problème).
- Il n’y pas de consensus sur la nécessité d’une antibioprophylaxie systématique en cas de ligatures élastiques. Il paraît cependant licite de la faire, notamment chez les sujets diabétiques et immunodéprimés. La Société Nationale Française de ColoProctologie préconise dans ce cas un traitement par métronidazole 500 mg avant le geste, puis 500 mg trois fois par jour pendant les 48 à 72 h suivant le geste (3).
- Il est possible de prescrire un antalgique et des laxatifs avant et après le geste.
- Il est conseillé au patient de ne pas voyager durant les 2 semaines qui suivent le geste en raison du risque hémorragique retardé par chute d’escarre.
Matériel et déroulement
- Ce traitement nécessite un anuscope à usage unique ou stérilisable et un ligateur et une aspiration. Le choix de la taille du ligateur se fait selon la taille du paquet à traiter (standard 11 mm, sinon XL 13 mm).
- Ce geste ne nécessite pas d’anesthésie.
- Le ligateur est introduit à travers l’anuscope et positionné au sommet de l’hémorroïde interne au moins un centimètre au-dessus de la ligne pectinée.
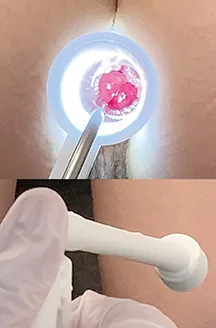
- La muqueuse est alors aspirée, puis étranglée à sa base par le largage de l’élastique (figure 2).

Figure 2 : Ligature élastique hémorroïdaire
- Lors d’une séance, il est possible de réaliser jusqu’à 3 ligatures.
- La cicatrisation se fait en 3 à 4 semaines environ.
- Deux à trois séances peuvent être nécessaires et espacées d’au moins quatre semaines.
Suites immédiates
- Des « faux besoins » douloureux peuvent être ressentis dans les heures qui suivent le geste, le plus souvent soulagés par des antalgiques de palier 1.
- En revanche, une douleur anale intense immédiate doit faire évoquer une malposition de l’élastique trop proche de la ligne pectinée et imposer alors son retrait.
- Les activités quotidiennes peuvent être reprises immédiatement.
Effets secondaires
Le patient doit en être informé avant le geste (feuille d’information à donner) avec une conduite à tenir définie pour chaque effet secondaire éventuel.
- Des malaises vagaux sont plus fréquents que pour la photocoagulation (9). Il faut donc conseiller aux patients « sensibles » de venir accompagnés ou de patienter une heure en salle d’attente.
- Dans la grande majorité des cas, les suites sont simples avec des douleurs modérées et des rectorragies minimes pouvant se poursuivre pendant la première semaine.
- Des réactions thrombotiques internes ou externes peuvent survenir, être particulièrement douloureuses et nécessiter la prise d’anti-inflammatoires non stéroïdiens (AINS).
- Dans 1 à 5 % des cas, des complications graves peuvent survenir à type de :
- douleurs anales intenses, troubles urinaires +/- fièvre, notamment au cours de la première semaine, qui doivent faire évoquer une complication infectieuse. En effet, plusieurs complications septiques sérieuses ont été rapportés dans la littérature, notamment des cellulites et/ ou des septicémies avec abcès hépatiques (10).
- hémorragie par chute d’escarre, survenant le plus souvent entre le 8e et le 15e jour et pouvant nécessiter un geste hémostatique en urgence (11).
Efficacité
Les études montrent une disparition ou une amélioration des symptômes dans 70 à 95 % des cas. L’efficacité de la ligature élastique se maintient à un an dans 80 % des cas (12).
La prise en charge de la pathologie hémorroïdaire externe
L’exérèse d’une marisque
Une marisque est un repli bénin, souple, indolore, de taille variable, de la peau péri-anale. Elle est le plus souvent séquellaire d’une thrombose hémorroïdaire externe ou d’une fissure anale.
Indications
Les marisques sont en général asymptomatiques et ne requièrent alors aucun traitement. Lorsqu’elles sont volumineuses et/ ou multiples, elles peuvent être responsables d’une gêne esthétique et/ ou hygiénique avec des difficultés d’essuyage après la selle. L’exérèse est alors envisageable si le patient est demandeur. Il faut cependant s’assurer que la marisque n’est pas associée à un prolapsus hémorroïdaire interne significatif ou à une fissure non cicatrisée sus-jacente.
Matériel et déroulement
L’exérèse d’une marisque est possible sous anesthésie locale en consultation. En cas de large base d’implantation et/ ou en cas de marisques multiples, il est plus confortable de faire l’exérèse au bloc opératoire sous anesthésie.
Précautions d’utilisation
- Il n’est pas nécessaire de proposer une préparation rectale ou une antibioprophylaxie.
- L’exérèse est possible sous aspirine mais les autres traitements antiagrégants et anticoagulants doivent être arrêtés en concertation avec leur prescripteur.
- En cas de troubles innés de l’hémostase ou surtout de la coagulation, l’ablation d’une marisque est contre-indiquée (pathologie bénigne exposant le patient à un risque hémorragique non acceptable).
- L’exérèse d’une marisque est contre-indiquée pendant la grossesse.
- L’exérèse d’une marisque est contre-indiquée dans le contexte d’une maladie de Crohn si la maladie n’est pas quiescente. Il en est de même en cas de RCH évolutive.
- L’exérèse d’une marisque est contre-indiquée en cas d’antécédent de radiothérapie pelvienne.
Matériel et déroulement
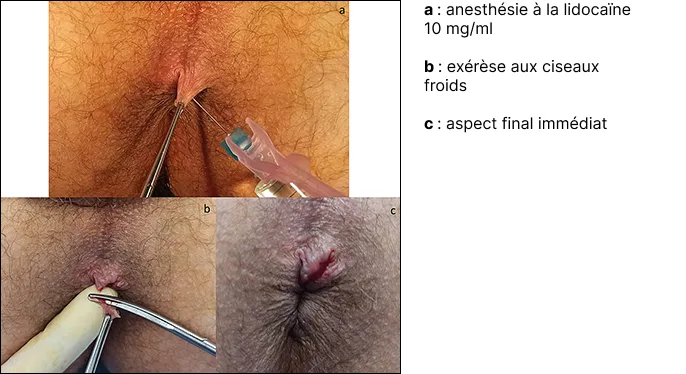
- Le premier temps consiste en une désinfection cutanée.
- Une anesthésie par de la lidocaïne 10 mg/ml est pratiquée sous le capuchon mariscal.
- L’exérèse peut être faite aux ciseaux froids (figure 3), sinon au bistouri électrique.

Figure 3 : Exérèse d’une marisque aux ciseaux (coll. Amine Alam et Déborah Roland)
- Si besoin, la marisque réséquée peut être envoyée pour une analyse histologique.
- La cicatrice est laissée ouverte pour une cicatrisation dirigée.
- Un pansement compressif, éventuellement à base d’un hémostatique (mèche d’alginates), est mis en place en fin de procédure et retiré le lendemain du geste.
Suites immédiates
- Au moment du geste, un éventuel saignement peut être arrêté au bistouri électrique ou par application d’un bâton de nitrate suivie d’un appui prolongé.
- Des soins locaux non spécifiques sont réalisés au domicile.
- Des douleurs sont possibles imposant la prescription systématique d’antalgiques et d’AINS.
Effets secondaires
Le patient doit en être informé avant le geste (feuille d’information à donner) avec une conduite à tenir définie pour chaque effet secondaire éventuel.
- Des douleurs le plus souvent modérées peuvent survenir durant les 2 semaines qui suivent l’exérèse. Parfois, cela exige un arrêt de travail de quelques jours si la plaie est large.
- Pendant les deux premières semaines, une hémorragie peut survenir. Ce risque est certes rare mais impose aux patients de ne pas voyager pendant cette période.
- Des écoulements séro-hématiques nécessitant le port d’une protection peuvent persister jusqu’à la cicatrisation complète.
Efficacité
Le résultat esthétique ne peut pas être garanti car il n’est pas rare qu’une réaction inflammatoire survienne sur l’une des berges cutanées et soit responsable de l’apparition d’une nouvelle marisque avant même que la plaie ne soit complètement fermée. Le patient doit être informé de la nécessité parfois d’une « retouche » pour obtenir le résultat esthétique escompté. La prescription d’AINS après le geste et le conseil au patient d’appuyer de manière prolongée sur les berges de la plaie pendant au moins 1 à 2 minutes tous les jours permettraient peut-être de réduire le risque d’œdème et la constitution d’une nouvelle marisque.
L’excision d’une thrombose hémorroïdaire externe (THE)
La thrombose hémorroïdaire est une affection bénigne fréquente due à une congestion vasculaire du tissu hémorroïdaire externe responsable d’un thrombus vasculaire et d’une réaction œdémateuse douloureuse. Elle survient le plus souvent au niveau des hémorroïdes externes, plus rarement des internes. Dans le dernier cas, la douleur est beaucoup plus marquée. Le diagnostic d’une THE est clinique associant une douleur anale aiguë, en général non insomniante, et une boule violacée au niveau de la marge anale. Le traitement d’une THE est avant tout médical reposant essentiellement sur les AINS, mais également sur des antalgiques de palier 2, des laxatifs et des topiques. Lorsque les AINS sont contre-indiqués (exemple du 3e trimestre de la grossesse), une corticothérapie de 40 mg/j peut être prescrite pour une courte période (2 à 5 jours) (13). Ce traitement permet une régression rapide de la douleur par disparition de l’œdème mais une régression plus lente du thrombus en 2 à 6 semaines. Le traitement médical est de loin le plus souvent suffisant pour traiter une THE et l’excision finalement rarement indispensable.
Indication
L’excision consiste à évacuer le ou les caillots sous pression. L’excision peut être réalisée en première intention si la thrombose est douloureuse, unique, non œdématiée et non soulagée par le traitement médical. Elle peut être également proposée en cas thrombus ouvert en cours d’évacuation et responsable de saignements tâchant le linge. Enfin, elle peut être proposée en cas de thrombus non douloureux mais gênant persistant pendant plusieurs semaines, voire des mois après l’épisode aigu. L’excision permet de raccourcir la durée des symptômes douloureux et d’éviter dans certains cas la formation d’une marisque hypertrophique séquellaire.
Précautions d’utilisation
- Il n’est pas nécessaire de proposer une préparation rectale ou une antibioprophylaxie.
- Même si elle est possible, l’excision d’une thrombose doit être évitée chez la femme enceinte, en cas d’immunodépression, de rectocolite hémorragique ou de maladie de Crohn.
- Elle est également contre-indiquée en cas de troubles de l’hémostase ou de la coagulation, inné ou acquis (traitement anticoagulant ou antiagrégant en dehors de l’aspirine qui ne pose pas de problème).
- L’excision d’une THE doit être évitée en phase œdémateuse en raison du risque plus important de saignements et de majoration des douleurs.
- L’incision simple du thrombus au bistouri à lame froide n’est pas conseillée du fait du sur-risque de saignement et de récidive rapide (par l’absence de l’ablation du sac thrombotique).
- Le prolapsus hémorroïdaire interne thrombosé ne doit pas être excisé ou incisé en consultation du fait du risque de complications hémorragiques et de fissure. Il relève du traitement médical et, en cas d’échec, d’une chirurgie.
Matériel et déroulement
- Le premier temps est une désinfection cutanée.
- Une anesthésie locale par injection de lidocaïne 10 mg/ml en sous-cutanée en regard du thrombus jusqu’au blanchissement de la peau est ensuite réalisée.
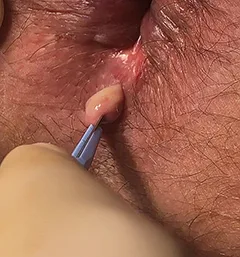
- L’excision cutanée se fait aux ciseaux emportant tout le sac thrombotique en essayant de rester le plus loin possible de la marge anale et d’être perpendiculaire aux plis radiés afin d’éviter les plaies pseudo-fissuraires. Elle permet ainsi l’évacuation de tout le thrombus (figure 4) 14).
![Figure 4 : Excision d’une thrombose hémorroïdaire [14]](data:image/svg+xml;base64,PHN2ZyB4bWxucz0iaHR0cDovL3d3dy53My5vcmcvMjAwMC9zdmciIHdpZHRoPSIyNDAiIGhlaWdodD0iMjQ1IiB2aWV3Qm94PSIwIDAgMjQwIDI0NSI+PHJlY3Qgd2lkdGg9IjEwMCUiIGhlaWdodD0iMTAwJSIgc3R5bGU9ImZpbGw6I2NmZDRkYjtmaWxsLW9wYWNpdHk6IDAuMTsiLz48L3N2Zz4=)
Figure 4 : Excision
d’une thrombose hémorroïdaire [14]
Suites immédiates
- En cas de saignement immédiat, l’hémostase peut être faite par application de nitrate d’argent à l’aide d’un bâton sur la plaie suivi d’une compression, sinon par un point en X ou au bistouri électrique.
- Un saignement retardé de quelques heures est possible et doit être traité par une compression appuyée et soutenue à l’aide de compresses pendant au moins une minute par le patient lui-même. Le saignement nécessite exceptionnellement un geste dédié d’hémostase.
- Des traitements doivent être prescrits après le geste : antalgiques, AINS, laxatifs et soins locaux non spécifiques jusqu’à cicatrisation.
Effets secondaires
Le patient doit en être informé avant le geste (feuille d’information à donner) avec une conduite à tenir définie pour chaque effet secondaire éventuel.
- La récidive est possible quand le geste n’a pas permis l’excision complète de tout le sac thrombotique.
- Des douleurs sont fréquentes pour lesquels les traitements prescrits sont le plus souvent suffisants.
- Une complication hémorragique est toujours possible jusqu’à 15 jours après le geste mais reste exceptionnelle.
L’incision d’un abcès ano-périnéal
L’abcès ano-périnéal est un motif fréquent de consultation d’urgence. Son diagnostic est clinique : douleur pulsatile, continue, insomniante, non rythmée par la défécation et généralement associée à l’apparition d’une tuméfaction anale ou péri-anale. De la fièvre, une constipation et/ ou une dysurie peuvent être présentes. Les facteurs de risque identifiés sont la maladie de Crohn, le diabète sucré, l’obésité et l’immunodépression (15). Le risque d’un abcès anal non traité est l’évolution vers une septicémie et/ ou une cellulite nécrosante dont la mortalité peut atteindre jusqu’à 40 % selon les études (16).
Indication
L’incision d’un abcès ano-périnéal est une urgence thérapeutique. L’objectif de cette incision est de soulager la douleur du patient et de limiter la diffusion de l’infection. Un traitement par antibiotique seul n’est pas recommandé car inefficace.
Précautions d’utilisation
- Il n’est pas nécessaire de proposer une préparation rectale ou une antibioprophylaxie.
- En raison du caractère d’urgence, l’incision peut être pratiquée chez une femme enceinte, chez les patients ayant une maladie inflammatoire chronique de l’intestin et chez les patients qui ont des troubles de la coagulation et/ ou de l’hémostase innés ou acquis.
- En cas d’abcès profond inaccessible à l’incision (abcès intramural rectal ou de la fosse ischio-anale) ou associé à des signes pouvant évoquer une cellulite, une mise à plat chirurgicale doit être pratiquée en urgence.
Matériel et déroulement
- Le premier temps est une désinfection cutanée.
- il faut repérer à la palpation douce la zone la plus rénitente de l’abcès dans laquelle il faut inciser.
- Si l’abcès est sous tension, l’incision peut se faire sans anesthésie avec un petit coup rapide au bistouri à lame froide. Sinon, il est préférable de faire une anesthésie locale sous-cutanée avec de la lidocaïne 10 mg/ml jusqu’à ce que la peau blanchisse.
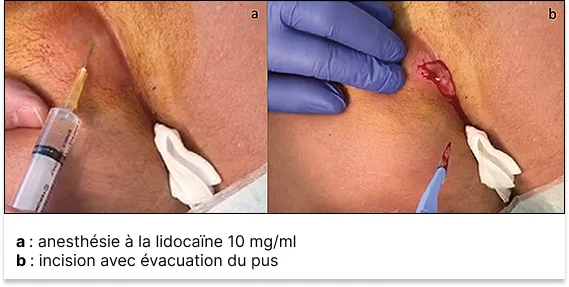
- L’incision doit être large et aussi profonde que nécessaire afin de permettre une évacuation satisfaisante de pus et éviter la fermeture prématurée de l’orifice d’incision qui exposerait à une remise en tension rapide de la collection (figure 5).

Figure 5 : Incision d’un abcès de la marge anale
- En cas d’abcès de la marge, l’incision se fait au mieux perpendiculairement aux plis radiés de l’anus afin d’éviter la survenue d’une plaie pseudo-fissuraire.
- Une fois l’incision réalisée, il faut évacuer le pus par des mouvements de pression sur la coque de l’abcès afin de bien vider la collection.
- Si l’abcès paraît peu collecté, il est possible de reporter l’incision avec une réévaluation précoce (dans les 48-72 heures).
- Si le patient est soulagé par l’incision et qu’il ne présente pas de signes de cellulite, le retour au domicile immédiat est possible. Un bilan biologique et/ ou une imagerie ne sont pas recommandés en première intention.
- La prescription d’une antibiothérapie après une incision efficace n’est pas systématique (17). Elle est seulement recommandée chez les patients présentant des signes de cellulite, les diabétiques, les patients immunodéprimés, les patients à risque d’endocardite et les porteurs de matériel prothétique. Il est conseillé de prescrire une antibiothérapie de large spectre de type amoxicilline/acide clavulanique ou une association de ciprofloxacine ou ofloxacine avec du métronidazole.
Suites immédiates
- Il faut conseiller au patient de continuer à presser autour de l’orifice d’incision une ou deux fois par jour afin de poursuivre l’évacuation du pus et éviter la fermeture prématurée de l’orifice d’incision.
- Les soins locaux au domicile reposent sur une simple toilette avec un savon à PH neutre et mise en place d’une compresse pour absorber les écoulements susceptibles de tacher les sous-vêtements.
- Il faut informer le patient de la contre-indication aux AINS.
- Il est recommandé de revoir le patient en consultation spécialisée, au bout de quelques jours, afin de vérifier la bonne évolution locale et de faire le diagnostic d’une suppuration fistuleuse susceptible de bénéficier d’une prise en charge chirurgicale ultérieure afin d’éviter la récidive de l’abcès.
Effets secondaires
- La survenue d’une plaie pseudo-fissuraire douloureuse est possible à la suite de l’incision.
- L’abcès peut récidiver après quelques jours si l’orifice d’incision s’est refermé.
- Des saignements et écoulements purulents sont fréquents dans les jours suivants l’incision.
L’incision d’un abcès sur sinus pilonidal infecté
Le sinus pilonidal infecté touche l’adulte jeune avec une prédominance masculine. Son mécanisme physiopathologique est largement débattu mais il serait dû à la présence congénitale de fossettes pilonidales du sillon interfessier dans lesquelles viendraient s’implanter des poils décollés sous l’effet de microtraumatismes répétés de follicules pileux créant ainsi des cavités profondes inflammatoires et surinfectées. L’abcès aigu du sinus pilonidal est une tuméfaction douloureuse, rouge, chaude, siégeant au niveau de la ligne médiane du sillon interfessier ou légèrement latéralisé.
L’abcès est le plus souvent à distance de la marge anale, mais dans quelques cas, il peut être proche, voire au niveau de la région périnéale antérieure, posant alors le problème du diagnostic différentiel avec un abcès anal d’origine fistuleuse.
En cas d’abcès aigu, la douleur est le symptôme principal et la fièvre exceptionnelle. En cas de sinus pilonidal infecté chronique, la douleur est moindre et le patient se plaint plutôt d’écoulements séro-hématiques et/ ou purulents provenant des fossettes médianes ou des orifices fistuleux externes latéralisés au niveau des fesses.
Indication
L’incision en urgence d’un abcès sur sinus pilonidal permet de soulager immédiatement la douleur et éviter la progression de l’infection (18).
Précautions d’utilisation
- De même que précédemment, il n’y a aucune préparation spécifique à prévoir et aucune contre-indication à la pratique de ce geste.
- Si l’abcès est profond, très étendu et inaccessible à une simple incision, une prise en charge chirurgicale doit être organisée en urgence mais il s’agit d’une situation rare.
Matériel et déroulement
- Il est conseillé d’installer le malade confortablement en décubitus ventral.
- Le processus d’incision est identique à celui d’un abcès de la marge anale (figure 6). S’il y a des poils qui s’évacuent spontanément au niveau du point d’incision et/ ou des fossettes, il ne faut pas hésiter à les extraire à la pince ou avec une curette.

Figure 6 : Incision d’un abcès sur sinus pilonidal infecté (coll. Manuel Aubert)
- Un traitement antibiotique seul n’est pas recommandé car insuffisant. Cependant, son utilisation peut être proposée en cas d’infiltrat inflammatoire non collecté en association à des antiseptiques et/ ou des antibiotiques en topiques. L’antibiothérapie alors utilisée est à large spectre de type amoxicilline/acide clavulanique ou pristinamycine.
Suites immédiates
- Les mêmes conseils précédemment donnés après incision d’un abcès ano-périnéal sont également donnés après incision d’un abcès sur sinus pilonidal.
- Les patients sont également revus en consultation afin de vérifier la bonne évolution clinique.
- Si l’évolution est bonne après incision, la prise en charge chirurgicale n’est pas systématique. En effet, 80 % des patients ne récidivent pas après un premier épisode d’infection. Il est donc conseillé d’attendre de multiples récidives d’abcès et/ ou un passage à la forme chronique avant de décider d’une prise en charge chirurgicale. Celle-ci peut consister en une excision à ciel ouvert ou plus récemment en des techniques mini-invasives de type SiLaT (Sinus Laser Treatment) ou VAAPS (Video-Assisted Ablation of Pilonidal Sinus) qui permettent de réduire de manière significative les contraintes liées aux soins postopératoires de la technique ouverte (19).
- Si l’évolution n’est pas bonne et que le patient continue à être symptomatique, une chirurgie peut être alors programmée. L’avantage du recours à cette phase transitoire d’incision est de diminuer la réaction inflammatoire et par conséquent l’étendue de l’exérèse chirurgicale.
Effets secondaires
- L’abcès peut récidiver après quelques jours si l’orifice d’incision s’est prématurément refermé.
- Des saignements et écoulements de pus sont fréquents dans les jours suivants l’incision.
Le traitement des condylomes anaux
Les condylomes sont des lésions macroscopiques secondaires à une infection aux papillomavirus humains (HPV). Les condylomes ano-génitaux sont liés le plus souvent à des génotypes d’HPV à faible risque oncogène (principalement le type 6 et 11) et plus rarement à des génotypes plus oncogènes (type 16 et 18). Il s’agit de l’infection sexuellement transmise (IST) la plus fréquente dans le monde : l’infection HPV ano-génitale toucherait 1 à 2 % de la population mondiale (20). À la suite d’un contact avec l’HPV, l’infection disparaît dans la plupart des cas grâce à la clairance immunitaire du virus. Dans 10 % des cas, le virus persiste et induit des lésions visibles. En outre, l’infection peut se réactiver en cas d’immunodépression, notamment chez les patients infectés par le virus de l’immunodéficience humaine (VIH). La population homosexuelle masculine, infectée par le VIH, est probablement celle qui porte le plus de variétés d’HPV notamment oncogènes, les exposant à un sur-risque de cancer de l’anus (21). Le dépistage est donc conseillé chez ces patients. Certains le recommandent également chez les homosexuels masculins ayant des partenaires sexuels multiples, les patientes avec antécédent de conisation, les patients immunodéprimés, etc. En France, ce dépistage repose sur un examen proctologique standard. La tendance actuelle est cependant de proposer un frottis anal et une anuscopie de haute résolution selon le résultat de ce frottis. Pour finir, la moitié des patients infectés par le VIH ayant des condylomes ont une atteinte intracanalaire exclusive (22). En conséquent, le simple déplissement de la marge anale n’est pas suffisant pour éliminer la présence de ces lésions.
Indication
Le traitement des condylomes consiste à détruire les lésions visibles et à surveiller les patients pour détecter les récidives. Le traitement des condylomes anaux est possible en consultation pour des lésions de petites tailles, non confluentes et non suspectes de dégénérescence. Il est également possible de traiter en consultation des récidives postopératoires minimes.
Précautions d’utilisation
- Il n’est pas nécessaire de proposer une préparation rectale ou une antibioprophylaxie.
- Il n’y a pas de contre-indications à détruire des lésions condylomateuses sous anesthésie locale en consultation. En revanche, les patients ayant des troubles de l’hémostase et/ ou de la coagulation, innés ou acquis (traitement anticoagulant ou antiagrégant) doivent être avisés d’un sur-risque d’hémorragie retardée par chute d’escarre. Un traitement par topiques en première intention peut être préféré chez ces patients (tableau 2).
Tableau 2 : Traitements topiques des condylomes, modalités d’utilisation et taux d’efficacité (14)| Molécule | Modalités d’utilisation | Efficacité |
| ALDARA® (imiquimod 5%) | Application au coucher 3 jours par semaine (par exemple Lundi-Mercredi- Vendredi). Si mauvaise tolérance, il faut espacer encore davantage. Le traitement est généralement prescrit pendant un maximum de 16 semaines. | 45-67 % [23] |
| CONDYLINE® (podophyllotoxine condyline 0,5 %) | Application 2 fois par jour pendant 3 jours consécutifs suivi de 4 jours de pause. Le traitement peut être répété chaque semaine pendant généralement un maximum de 5 semaines. | 45-94 % [24] |
| EFUDIX® (fluorouracile 5%) | Application 2 fois par jour 3 fois par semaine. Le traitement peut être répété chaque semaine pendant généralement un maximum de 3 à 4 semaines. | 60-90 % [24] |
| Acide trichloracétique à 85 % | Application en solution aqueuse ou alcoolique par le praticien avec un coton-tige 1 à 3 fois par semaine jusqu’à disparition des lésions. | 70-90 % [25] |
- Si l’aspect est atypique et/ou que la lésion est en échec de plusieurs précédentes tentatives de destruction, il est possible de pratiquer dans un premier temps une biopsie, puis de la détruire dans un second temps après résultat histologique.
- Avant de proposer une méthode de destruction thermique, il est toujours utile de discuter avec le patient de la possibilité d’un traitement topique pour des lésions peu nombreuses de la marge anale ou en cas de lésions planes récidivantes malgré plusieurs lignes de traitements chez des patients immunodéprimés à haut risque de récidive. Les topiques n’ont l’AMM que pour la marge anale mais il est possible de les appliquer en intracanalaire. Ceci étant dit, leur utilisation est limitée par leur faible tolérance locale (irritation de la peau, démangeaisons, brûlures, etc.) et par une efficacité moindre que les traitements de destruction thermique notamment en cas de lésions multiples et surélévées. Pour améliorer cette tolérance, il est conseillé d’administrer une application en soirée, un soir sur deux, d’une quantité limitée de produit, seulement sur les zones concernées, en massant pour faire pénétrer le produit, suivi d’un lavage de la zone traitée le lendemain matin. L’application en alternance de crèmes émollientes ou de pâtes à l’eau permet également de limiter les effets indésirables.
- Il faut dépister les autres IST, rechercher d’autres localisations notamment au niveau des organes génitaux externes et de la sphère ORL et adresser les patientes en gynécologie pour réaliser un frottis cervico-vaginal (tableau 3).
Tableau 3 : Recommandations devant des condylomes anaux (14)- Dépistage des autres infections sexuellement transmises (VIH, virus B et C, syphilis)
|
- Recherche d’autres localisations au niveau des organes génitaux externes et sphère ORL
|
- Réalisation d’un bilan gynécologique, notamment pour le frottis cervico-vaginal
|
- Incitation des partenaires à se faire dépister
|
- Conseil au patient la vaccination contre les papillomavirus (jusqu’à 19 ans chez les femmes et les hommes hétérosexuels et jusqu’à 26 ans chez les
homosexuels masculins) |
- Surveillance après traitement en raison du risque important de récidive
|
- Il faut encourager le dépistage des partenaires.
- Il faut conseiller aux patients qui sont encore dans la tranche d’âge concernée (jusqu’à 19 ans chez les femmes et hommes hétérosexuels, et jusqu’à 26 ans chez les homosexuels masculins) la vaccination contre les HPV qui peut les prévenir des infections par d’autres génotypes oncogènes, même si on sait que l’efficacité du vaccin baisse chez les patients qui ont déjà été en contact avec l’HPV. C’est la raison pour laquelle le mieux est de vacciner avant le premier rapport sexuel.
Matériel et déroulement
- Il est conseillé de se protéger avec un masque et de ventiler la pièce afin d’éviter l’infection laryngée de l’opérateur (même si cette possible infection reste discutable et exceptionnelle).
- Une anesthésie locale est nécessaire soit par une injection sous-cutanée de lidocaïne 10 mg/ml pour les lésions de la marge anale. L’utilisation d’un prolongateur est nécessaire pour les lésions intracanalaires.
- Il est également possible d’utiliser de simples ciseaux froids pour exciser des lésions pédiculées de la marge anale. L’avantage est que ça permet une analyse histologique mais l’inconvénient est que ça peut induire un saignement. Une hémostase peut être faite par application de nitrate suivie d’un appui prolongé avec une compresse, sinon au bistouri électrique.
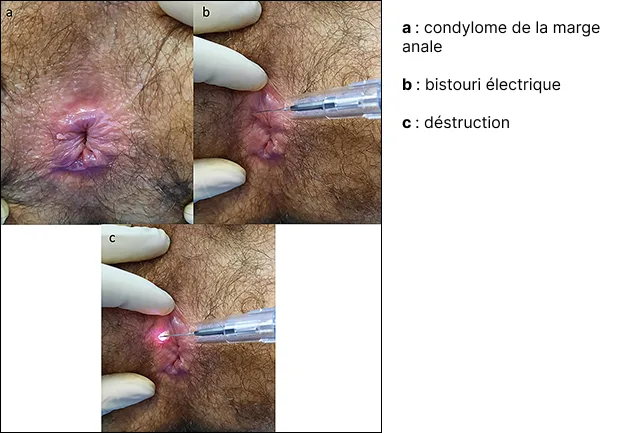
- Plusieurs moyens thermiques peuvent être utilisés pour détruire les lésions (tableau 4). Le bistouri électrique est largement utilisé par les proctologues. Il a l’avantage d’une destruction rapide et efficace (figure 7). Il y a cependant un risque d’explosion au contact des gaz digestifs lors du traitement des lésions intracanalaires. Pour éviter cette complication, il est conseillé de placer une compresse imbibée d’eau au niveau du bas rectum ou de s’équiper d’un bistouri avec un système d’aspiration de fumée. La coagulation des condylomes se fait en appliquant la pointe du bistouri sur les lésions à détruire.
Tableau 4 : Traitements thermiques des condylomes, modalités d’application et taux d’efficacité (14)| Type de traitement | Modalités d’utilisation | Efficacité |
| Bistouri électrique | Application de la pointe du bistouri sur le condylome en appuyant quelques secondes sur le bouton coagulation. Risque d’explosion au contact des gaz digestifs lors du traitement des lésions intracanalaires. | 37-94 % [26] |
| Photocoagulation infrarouge | Plusieurs impacts sur le condylome sont nécessaires avec une durée d’impulsion supérieure ou égale à une seconde. | 75% [27] |
| Cryothérapie à l’azote | Application d’azote liquide à l’aide d’un coton-tige ou d’un pulvérisateur afin de former une plage englobant les lésions condylomateuses. | 46-96 % [28] |
| Laser CO2 | Application pendant quelques secondes sur les lésions. | 23-53% [29] |

Figure 7 : Destruction de lésions condylomateuses
au bistouri électrique (coll. Liza Kassouri)
- Il est possible également d’utiliser le photocoagulateur infrarouge, davantage indiqué sur des lésions planes que bourgeonnantes. Contrairement au bistouri électrique, il ne semble pas y avoir de risque d’explosion. Plusieurs applications sont nécessaires et la durée d’impulsion ne doit pas être inférieure à une seconde. Il est parfois utile de cureter la couche superficielle détruite et d’appliquer de nouveau le photocoagulateur afin de permettre une destruction en profondeur diminuant ainsi le risque de récidive.
- Un traitement par cryothérapie par azote liquide est également possible. Il est le plus souvent réalisé par les dermatologues sans anesthésie sur des lésions de la marge anale.
- Une destruction par laser C02 est enfin possible. Ce type de traitement est davantage utilisé par les gynécologues.
Suites immédiates
- Des soins locaux non spécifiques sont réalisés au domicile.
- Des douleurs sont possibles imposant la prescription systématique d’antalgiques et d’AINS.
- En cas de destruction de lésions intracanalaires, il est peut-être utile de prescrire en plus des suppositoires et des laxatifs.
Effets secondaires
Le patient doit en être informé avant le geste (feuille d’information à donner) avec une conduite à tenir définie pour chaque effet secondaire éventuel.
- Un risque d’hémorragie par chute d’escarre, notamment après traitement des lésions intracanalaires, existe mais est exceptionnel.
- Des douleurs prolongées ainsi qu’une perte de la sensibilité et de la souplesse du canal anal ont été rapportées avec un impact sexuel chez des patients ayant une sexualité anale. Ceci survient en cas de traitements multiples, de lésions circonférentielles et/ ou en cas d’utilisation du laser CO2 qui a l’avantage de détruire en profondeur mais donne en conséquent des cicatrices rétractiles.
Efficacité
Une surveillance régulière est nécessaire pour dépister les récidives qui sont fréquentes et atteignent 50 % des cas chez les patients VIH (30,31).
Le prélèvement à visée microbiologique
Les infections sexuellement transmises (IST) sont en constante augmentation notamment pendant cette dernière décennie et représentent un vrai problème de santé publique. L’organisation mondiale de la santé a estimé à 357,4 millions le nombre de nouveaux cas en 2012 incluant notamment des infections à Neisseria gonorrhée et à Chlamydia trachomatis. La population à risque est essentiellement représentée par les homosexuels masculins (HSM), les VIH +, les personnes utilisant la PreP (prophylaxie pré-exposition) et à partenaires mutiples. Le diagnostic et le traitement de ces infections doit donc faire partie intégrante de la formation d’un gastroentérologue/proctologue.
Indication
Tous les patients faisant partie de la population à risque qui se présentent avec des symptômes ano-rectaux : douleurs, faux besoins, ténesmes, émissions glairo-sanglantes, symptômes urinaires, etc. et/ ou ceux qui présentent à l’examen une atteinte inflammatoire, ulcérée et/ ou purulente de la marge, canal anal et du bas rectum doivent bénéficier d’un prélèvement par écouvillonnage à visée microbiologique. Certaines infections à gonocoques peuvent se présenter sous la forme d’un abcès fistuleux. Certaines lésions de lymphogranulomatose vénérienne (infection à Chlamydia trachomatis sérotypes L1, L2 et L3) peuvent également mimer une maladie inflammatoire chronique de l’intestin et induire en erreur diagnostique. Pour éviter ces situations amenant parfois à une prise en charge complètement décalée, les patients doivent être interrogés sur leurs pratiques sexuelles et y penser au moindre doute (32).
Enfin, certains prélèvements peuvent être pratiqués chez des patients asymptomatiques pour dépister les formes infra-cliniques notamment chez les patients sous PreP.
Précautions d’utilisation
- Aucune préparation rectale ni antibioprophylaxie ne doivent être pratiqués.
- Les prélèvements doivent être pratiqués sans gel lubrifiant afin de ne pas fausser le résultat. Il est possible d’humidifier avec de l’eau afin de simplifier l’introduction chez un patient algique.
Matériel et déroulement
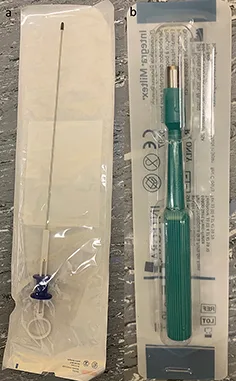
Deux écouvillons spécifiques (figure 8) sont nécessaires pour diagnostiquer une IST ano-rectale. Le premier sert à faire une amplification d’acides nucléaires (NAATs) permettant une détection simultanée moléculaire par PCR multiplex du gonocoque eu du Chlamydia mais également selon la marque utilisée de nombreuses autres infections souvent concomitantes comme le mycoplasme génitalium et hominis, l’Ureaplasme urealyticum et parvum, le trichomonas vaginalis, le Cytomégalovirus, l’Haemophilus ducreyi, l’Herpès simplex de type 1 et 2, le sérotype du Chlamydia trachomatis, le Treponema pallidum et le virus de la varicelle-zona. Le second écouvillon sert à faire une culture systématique standard du gonocoque avec antibiogramme. Les autres IST comme la syphilis, le VIH, l’hépatite B et l’hépatite C sont en revanche détectés par la sérologie. Le prélèvement sera fait au mieux avant l’examen proctologique intracanalaire avec l’anuscope lubrifié avec du gel en introduisant l’écouvillon en intra-anal et en faisant plusieurs rotations afin d’assurer la bonne rentabilité du prélèvement.

Figure 8 : Écouvillons anaux
Suites immédiates
aucun effet indésirable.
Effets secondaires
aucun effet secondaire
Efficacité
Les résultats sont rendus dans les 24 heures et permettent de proposer rapidement un traitement. De la même façon que les condylomes, en cas de positivité, il faut dépister les autres IST et les partenaires.
Le prélèvement à visée histologique
Indication
Beaucoup de lésions dermatologiques, tumorales bénignes ou malignes peuvent siéger au niveau de la région ano-périnéale. Au moindre doute diagnostique ou de malignité et/ ou d’évolution atypique, un prélèvement sous anesthésie locale à visée histologique peut être pratiqué sans aucune difficulté.
Précautions d’utilisation
- Il n’est pas nécessaire de proposer une préparation rectale ou une antibioprophylaxie.
- Il n’y a aucune contre-indication à faire une biopsie sous anesthésie locale tout particulièrement les patients ayant des troubles de l’hémostase et/ou de la coagulation, innés ou acquis (traitement anticoagulant ou antiagrégant). En revanche, s’il s’agit d’une exérèse complète d’une lésion cutanée supra-centimétrique, il faudra discuter de sa pertinence et/ ou de la réalisation d’une fenêtre thérapeutique en accord avec le prescripteur. Matériel et déroulement
- Le premier temps est une désinfection cutanée.
- Une anesthésie locale par injection de lidocaïne 10 mg/ml en sous-cutanée est ensuite réalisée en regard de la zone à biopsier jusqu’à blanchissement de la peau.
- La biopsie peut se faire ensuite avec une pince à biopsie sinon au punch biopsie (figure 9) qui permet d’avoir des prélèvements de meilleure qualité. L’exérèse complète d’une lésion cutanée peut se faire aux ciseaux froids sinon au bistouri électrique. Le prélèvement est ensuite mis dans un pot d’anatomopathologie.

Figure 9 : Instruments
pour biopsies
Suites immédiates
- En cas de saignement immédiat, l’hémostase peut être faite par application de nitrate d’argent à l’aide d’un bâton sur la plaie suivi d’une compression, sinon par un point en X ou au bistouri électrique.
- Un saignement retardé de quelques heures est possible et doit être traité par une compression appuyée et soutenue à l’aide de compresses pendant au moins une minute par le patient lui-même. Le saignement nécessite exceptionnellement un geste dédié d’hémostase.
- Des traitements et de soins locaux peuvent être prescrits après le geste selon la taille de la biopsie : antalgiques, AINS, laxatifs et soins locaux non spécifiques.
Effets secondaires
Le patient doit en être informé avant le geste (feuille d’information à donner) avec une conduite à tenir définie pour chaque effet secondaire éventuel.
- Des douleurs le plus souvent modérées peuvent être rapportées durant les 2 semaines qui suivent le geste. Parfois, cela exige un arrêt de travail de quelques jours si la plaie est large.
- Pendant les deux premières semaines, une hémorragie peut survenir. Ce risque est certes rare mais impose aux patients de ne pas voyager pendant cette période.
- Selon la taille de la biopsie ou de la lésion réséquée, des écoulements séro-hématiques nécessitant le port d’une protection peuvent persister jusqu’à la cicatrisation complète.
Efficacité
Le résultat histologique est le plus souvent concluant notamment lorsqu’un prélèvement de bonne qualité a été pratiqué.
Conclusion
Les gestes instrumentaux en consultation de proctologie sont multiples, nécessitent un matériel spécifique et une connaissance des modalités et des suites de chaque geste. Les patients doivent être informés au préalable des complications potentielles même si elles sont exceptionnelles. Ceci étant dit, ces gestes ont le plus souvent une efficacité immédiate et permettent de soulager rapidement des patients parfois hyperalgiques et d’éviter dans de nombreux cas le recours à un geste chirurgical.
Références
- Bouchard D, Pigot F. Anal acute pain. Rev Prat 2017; 67(2): 148-51.
- S. Riss S, Weiser FA, Schwameis K, et al. The prevalence of hemorrhoids in adults. Int J Colorectal Dis 2012; 27(2): 215-20.
- Higuero T, Abramowitz L, Castinel A, et al. Guidelines for the treatment of hemorrhoids. J Visc Surg 2016; 153(3): 213-8.
- Alonso-Coello P, Mills E, Heels-Ansdell D, et al. Fiber for the treatment of hemorrhoids complications: a systematic review and meta-analysis. Am J Gastroenterol 2006; 101(1): 181-8.
- van Tol RR, Kleijnen J, Watson AJM, et al. European Society of ColoProctology: guideline for haemorrhoidal disease. Colorectal Dis 2020; 22: 650-662.
- Zeitoun JD, de Parades V. Management of haemorrhoidal disease. Presse Med 2011; 40 : 948-54
- Johanson JF, Rimm A. Optimal nonsurgical treatment of hemorrhoids: a comparative analysis of infrared coagulation, rubber band ligation, and injection sclerotherapy. Am J Gastroenterol 1992; 87: 1600-6.
- Walker AJ, Leicester RJ, Nicholls RJ, et al. A prospective study of infrared coagulation, injection and rubber band ligation in the treatment of haemorrhoids. Int J Colorectal Dis 1990; 5: 113-6.
- Watson NFS, Liptrott S, Maxwell-Armstrong CA. A prospective audit of early pain and patient satisfaction following out-patient band ligation of haemorrhoids. Ann R Coll Surg Engl 2006; 88: 275-9.
- McCloud JM, Jameson JS, Scott AND. Life-threatening sepsis following treatment for haemorrhoids: a systematic review. Colorectal Dis 2006 ; 8(9) : 748-55.
- Bat L, Melzer E, Koler M, et al. Complications of rubber band ligation of symptomatic internal hemorrhoids. Dis Colon Rectum 1993; 36: 287-90.
- Gupta PJ. Infrared coagulation versus rubber band ligation in early stage hemorrhoids. Braz J Med Biol Res 2003; 36(10): 1433-9.
- Perier A, Fathallah N, Aubert A, et al. La maladie proctologique de la grossesse et du post-partum (troubles de la continence exclus) : un malheureux événement…. Hépato-Gastro & Oncologie Digestive 2017;24:678-88.
- Sabat C, de Parades V, Pommaret E, Rentien AL, Alam A, Fathallah N. Les gestes proctologiques réalisables en consultation. Hépato-Gastro et Oncologie Digestive 2022 (in Press)
- Adamo K, Sandblom G, Brännström F, et al. Prevalence and recurrence rate of perianal abscess–a population-based study, Sweden 1997-2009. Int J Colorectal Dis 2016; 31: 669-73.
- Sarkis P, Farran F, Khoury, et al. Gangrène de Fournier : revue de la littérature récente. Prog Urol 2009; 19: 75-84.
- Fathallah N, Ravaux A, de Parades V et al. Conduite à tenir face à un abcès ano-périnéal. Ann Fr Med Urgence 2017; 7: 174-182.
- de Parades, Bouchard, Janier et al. Le sinus pilonidal infecté. Journal de Chirurgie Viscérale 2013; 150: 264-75.
- Iesalnieks I, Ommer A, Herold A, Doll D. German National Guideline on the management of pilonidal disease: update 2020. Langenbecks Arch Surg 2021; 406: 2569-80.
- Koshiol JE, Laurent SA, Pimenta JM. Rate and predictors of new genital warts claims and genital warts-related healthcare utilization among privately insured patients in the United States. Sex Transm Dis 2004; 31: 748-52.
- Sobhani I, Walker F, Roudot-Thoraval F, et al. Anal carcinoma: incidence and effect of cumulative infections. AIDS 2004; 18: 1561-69.
- Abramowitz L, Benabderrahmane D, Ravaud P, et al. Anal squamous intraepithelial lesions and condyloma in HIV-infected heterosexual men, homosexual men and women: prevalence and associated factors. AIDS 2007; 21: 1457-1465.
- Edwards L, Ferenczy A, Eron L, et al. Self-administered topical 5 % imiquimod cream for external anogenital warts. HPV Study Grooup. Human PapillomaVirus. Arch Dermatol 1998; 134: 25-30.
- O’Mahony C, Gomberg M, Skerlev M, et al. Position statement for the diagnosis and management of anogenital warts. J Eur Acad Dermatol Venereol 2019; 33: 1006-19.
- Godley MJ, Bradbeer CS, Gellan M, et al. Cryotherapy compared with trichloroacetic acid in treating genital warts. Sexually Transmitted Infections 1987; 63: 390-2.
- Benedetti Panici P, Scambia G, Baiocchi G, et al. Randomized clinical trial comparing systemic interferon with diathermocoagulation in primary multiple and widespread anogenital condyloma. Obstet Gynecol 1989; 74: 393-7.
- Weis SE, Vecino I, Pogoda JM, et al. Treatment of high-grade anal intraepithelial neoplasia with infrared coagulation in a primary care population of HIV-infected men and women. Dis Colon Rectum 2012; 55: 1236-43.
- Damstra RJ, van Vloten WA. Cryotherapy in the treatment of condylomata acuminata: a controlled study of 64 patients. J Dermatol Surg Oncol 1991; 17: 273-6.
- Scheinfeld N, Lehman DS. An evidence-based review of medical and surgical treatments of genital warts. Dermatol Online J 2006; 12: 5.
- Corral J, Parés D, García-Cuyás F, et al. Incidence of Recurrent High-Grade Anal Dysplasia in HIV-1-Infected Men and Women Following Infrared Coagulation Ablation: A Retrospective Cohort Study. Pathogens 2014; 10: 208.
- Gaisa MM, Liu Y, Deshmukh AA, et al. Electrocautery ablation of anal high-grade squamous intraepithelial lesions: Effectiveness and key factors associated with outcomes. Cancer 2020; 126: 1470-79.
- Lourtet-Hascoet J, Mine L, Spindler L, et al. Epidemiology of symptomatic infective anoproctitis in a population of men having sex with men (MSM). Infection 2022; 50: 933-40.
Remerciements
Claire SABAT qui est le premier auteur de l’article « Les gestes proctologiques réalisables en consultation » in press dans la revue HGOD novembre 2022 et qui a été la base de l’écriture de cet article de la FMC.
Vincent de PARADES pour ses contributions actives dans tous les travaux de publication du service de Proctologie du GH Paris Saint-Joseph Amine ALAM, Liza KASSOURI, Déborah ROLAND, et Manuel AUBERT pour leur aide dans les figures.
![Figure 4 : Excision d’une thrombose hémorroïdaire [14]](https://www.fmcgastro.org/wp-content/uploads/2022/07/03_02-Fig-4-jpg.webp)