Objectifs pédagogiques
- Connaître l’épidémiologie et les caractéristiques des CCR BRAF muté
- Connaître l’impact sur la prise en charge thérapeutique en situation métastatique
- Connaître les effets secondaires des thérapies ciblées de seconde ligne
En rapport avec la présentation :
BRAF, MSI, encorafenib
Le cancer colorectal représente, avec une incidence de plus de 43 000 nouveaux cas par an en 2018 en France, un véritable problème de santé publique. Responsable de plus de 17 000 décès, il se situe au deuxième rang de la mortalité par cancer chez l’homme et au troisième rang chez la femme. Si la prise en charge des formes localisées repose essentiellement sur l’endoscopie et la chirurgie, les formes métastatiques nécessitent une approche multidisciplinaire qui sera validée en RCP. La stratégie thérapeutique sera orientée selon la masse tumorale, les possibilités de résection, les caractéristiques du patient mais aujourd’hui le statut moléculaire de la tumeur est devenu un prérequis indispensable pour une prise de décision optimale. Parmi ces données, le statut BRAFV600E occupe une place primordiale, car l’existence d’une mutation, retrouvée chez environ un malade sur 10, confère un mauvais pronostic et conditionnera toute la prise en charge. Nous développerons ici les grandes lignes du traitement des patients atteints de CCRM BRAFmV600E.
Un des principaux mécanismes de prolifération des cellules cancéreuses dans le CCRM est l’activation de la voie de l’EGFR, surexprimée dans près de 50 % des CCRM. Le signal de prolifération est transmis par une cascade de phosphorylations enzymatiques intracellulaires par deux voies principales : la voie des MAPK et la voie AKT-mTOR (schéma 1). La protéine BRAF fait partie de la voie des MAPK. Il s’agit d’une sérine-thréonine kinase dont le gène est situé sur le bras long du chromosome 7. L’activation en cascade de BRAF par RAS active les protéines MEK puis ERK qui vont au niveau du noyau cellulaire activer un grand nombre de gènes impliqués dans la survie et la prolifération cellulaire.
De nombreuses mutations de BRAF ont été décrites, réparties en 3 classes. La mutation dite V600E (car substitution d’une valine en acide glutamique au niveau du codon 600) sur l’exon 15 est la plus fréquente (>90 % des mutations BRAF) et est la seule avec des implications pronostiques et thérapeutiques dans le CCRM. Cette mutation est activatrice car aboutissant à une multiplication par 10 de l’activité kinase, non régulée. Elle ne coexiste pratiquement jamais avec une mutation des gènes RAS : ces mutations sont dites mutuellement exclusives, étant toutes deux des « driver mutations » de la voie MAPK.
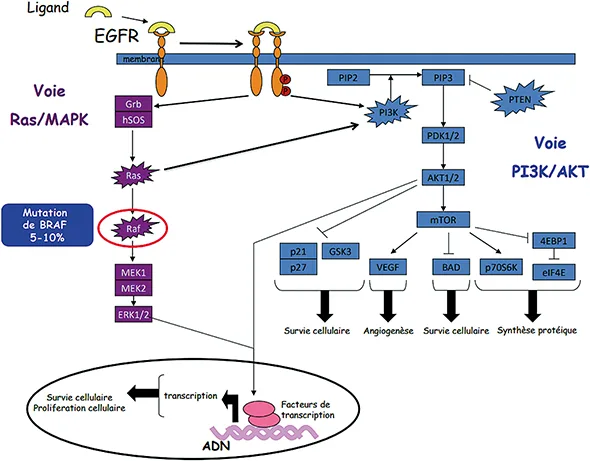
Figure 1 : hysiopathologie
Le diagnostic des mutations RAS/BRAF repose sur des techniques de biologie moléculaire : soit par NGS réalisés sur des plateformes publiques ou privées, soit par technique de PCR dédiée (type machine IdyllaTM). Dans le premier cas, le rendu des résultats est plus long (entre 10 et 21 jours) lié en partie à la phase pré-analytique avec désarchivage/ sélection du bloc tumoral et envoi en plateformes mais permet également l’information sur un panel de gènes plus ou moins complet. Dans le deuxième cas (Biocartis) le résultat est accessible en 24 heures et souvent réalisé en laboratoire d’anatomopathologie équipé du système mais ne donnera l’information que sur des séquences des gènes testés : le financement de ces tests est une contrainte car actuellement à la charge de l’institution prescriptrice du test : de l’ordre de 800 euros pour le NGS et 200 euros pour le Biocartis. Un remboursement partiel dans le cadre du RIHN est possible mais une inscription à la nomenclature est attendue prochainement. Enfin, pour s’affranchir d’une biopsie tumorale, une détermination du statut BRAF sur ADN tumoral circulant (ADNtc) est possible mais la technique n’est ni standardisée, ni remboursée et peut se heurter à un défaut d’ADNtc détectable en particulier en l’absence de métastases hépatiques.
Biologiquement, la mutation BRAFV600E est associée au phénotype hyperméthylateur CIMP (« The CpG Island Methylator Phenotype ») et du coup, les tumeurs BRAF mutées présentent dans 20 à 30 % des cas un phénotype dMMR/MSI dit sporadique, lié une hyperméthylation du promoteur de MLH1. Ces tumeurs présentent donc un déficit du système de réparation des mésappariements de l’ADN (statut dMMR pour « Deficient MisMatch Repair system »). Elles sont éligibles aux traitements par immunothérapie.
Une mutation BRAF V600E est retrouvée environ dans 8 à 12 % des CCRM. Il s’agit le plus souvent de patients âgés, de sexe féminin avec une tumeur colique droite (60 à 80 %), peu différenciée, avec composante mucineuse. L’extension métastatique est souvent ganglionnaire et péritonéale, plus qu’hépatique et pulmonaire.
Au stade localisé, l’analyse poolée des données de survie des principaux essais de chimiothérapie adjuvante a confirmé le mauvais pronostic des cancers stade II et III avec mutation BRAF à la fois en termes de survie sans rechute et de survie globale.
Chez les patients métastatiques, l’impact en survie globale est encore plus spectaculaire avec des médianes de survie globale inférieures à 18 mois dans l’essai randomisé dédié FIRE 4.5 et ce malgré l’utilisation d’associations trichimiothérapie (FOLFOXIRI) plus thérapie ciblée.
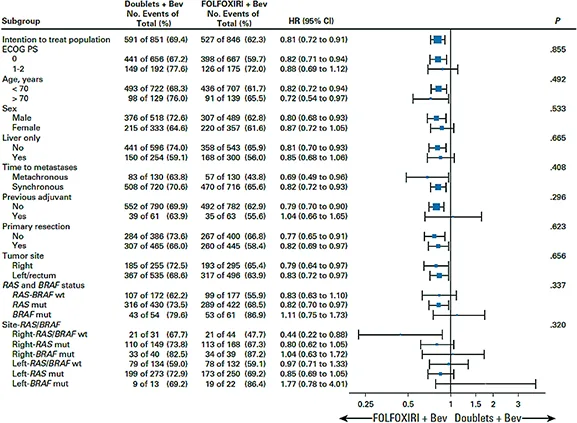
Devant le mauvais pronostic de ces tumeurs, il a rapidement été envisagé un recours à des protocoles intensifs de chimiothérapie type trichimiothérapie (FOLFOXIRI ou FOLFIRINOX). À partir d’une phase I italienne multicentrique dédiée, et de l’analyse des données du sous-groupe de patients avec mutation BRAFV600E dans la phase III TRIBE, le schéma FOLFOXIRI-bevacizumab s’est rapidement imposé comme le standard de première ligne chez les patients capables de le recevoir (OMS 0-1) (figure 2) (1). Toutefois une récente méta-analyse des essais comparant la trichimiothérapie-bevacizumab à la bichimiothérapie-bevacizumab n’a pas montré de bénéfice évident en faveur de la trichimiothérapie (figure 3) (2).
Dans le même temps, l’analyse rétrospective des sous-groupes de patients avec tumeur BRAFV600E mutée traités dans les essais avec anticorps anti-EGFR semblant donner des résultats prometteurs, plusieurs méta-analyses ont été réalisées sans résultat probant. Il a donc été monté par l’intergroupe allemand AIO un essai européen (FIRE 4.5) comparant une trichimiothérapie-cetuximab versus une trichimiothérapie-bevacizumab par le biais d’une randomisation 2/1 en première ligne dans une population de patients atteints de CCRM BRAF V600E mutés pMMR. L’étude était négative sur son objectif principal qui était le taux de réponse (50 % chimio-cetuximab versus 60 % bevacizumab) avec un bénéfice significatif de survie sans progression en faveur du bevacizumab (médiane 10 versus 6 mois, p=0.01) et une tendance dans le même sens en survie globale (17,2 versus 15,1 mois, NS) (3).
À ce jour la recommandation est donc l’utilisation d’une bichimiothérapie avec bevacizumab (recommandation grade C TNCD 2022), l’utilisation d’une trichimiothérapie pouvant être réservée aux patients en bon état général (OMS 0-1) et non exposés à l’oxaliplatine en situation adjuvante. L’utilisation des anticorps anti-EGFR n’est pas recommandée en 1re ligne.
Des essais sont en cours évaluant la place des traitements ciblés anti-BRAF en première ligne et en particulier l’essai BREAKWATER phase III comparant encorafenib + cetuximab à la même association avec chimiothérapie.
Avant la mise en place d’un traitement dédié, l’analyse de plusieurs essais de première ligne montrait un mauvais accès en deuxième ligne et de mauvais résultats de survie des patients avec tumeur BRAFm.
La compréhension des cascades de phosphorylation enzymatique impliquées dans la voie EGFR a permis rapidement de développer des stratégies de blocage combinant différents agents. Le point d’orgue a été l’essai de phase III BEACON qui a démontré en deuxième ou troisième ligne de traitement de patients atteints de CCRM BRAFm, tous exposés au bevacizumab, que les combinaisons anti-EGFR (cetuximab) + anti-BRAF (encorafenib) : double inhibition, ou anti-EGFR + anti-BRAF + anti-MEK (binimetinib) : triple inhibition, étaient supérieures au bras contrôle choisi : irinotécan + cetuximab, en termes de survie globale, survie sans progression et taux de réponse (4). La survie globale était comparable dans les bras double et triple inhibition (9,3 mois versus 5,9 mois dans le bras contrôle) avec un taux de réponse en faveur de la triple inhibition (27 % versus 20 %, non comparé, vs. 2 % dans le bras contrôle). Le taux de complications grade 3-4 était non différent dans les 3 bras, en faveur de la double inhibition (58 % triple, 50 % double, 61 % contrôle) (figures 4 et 5). L’utilisation de binimetinib était en particulier responsable de potentielles toxicités cardiaques, rénales et ophtalmologiques.
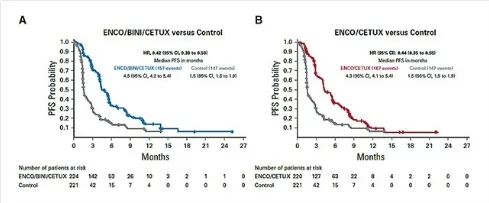
BEACON : courbes de SSP actualisées (Tabernero J, et al., J Clin Oncol 2021)
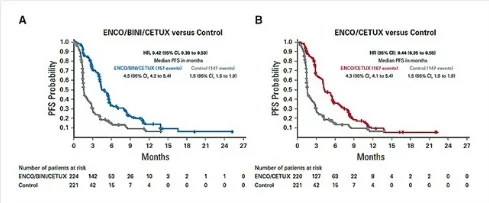
BEACON : courbes de SG actualisées (Tabernero J, et al., J Clin Oncol 2021)
Au final, l’AMM européenne a retenu comme standard thérapeutique l’utilisation de l’encorafenib en association au cetuximab, dans le traitement de patients adultes atteints de CCRM porteur d’une mutation BRAF V600E, ayant progressé après un ou deux traitement(s) antérieur(s) systémique(s) au stade métastatique et présentant un score ECOG 0 ou 1. En cas de score ECOG à 2 une discussion en RCP est recommandée.
L’encorafenib (BRAFTOVI®) se prend par voie orale tous les jours en une prise de 4 gélules de 75 mg soit 300 mg. Il est désormais disponible en officine de ville. Il est associé au cetuximab (administration classique intraveineuse avec dose de charge à J1 de 400 mg/m2 puis perfusion hebdomadaire de 250 mg/m2). Il peut être discuté en RCP une perfusion tous les 14 jours de cetuximab 500 mg/m2 ou l’utilisation de l’autre anti-EGFR (panitumumab 6 mg/kg tous les 14 jours).
De façon remarquable, l’utilisation d’encorafenib bloque les effets secondaires cutanés du cetuximab et l’utilisation prophylactique d’antibiotiques n’est pas utile. Il faut par contre proscrire l’exposition au soleil. Il existe un risque théorique d’augmentation des cancers cutanés (3 % versus 0 % dans BEACON) nécessitant une surveillance dermatologique. Cette surveillance comprend en théorie un examen initial puis tous les deux mois sous traitement, et six mois après la fin du traitement. En cas de lésion cutanée, l’exérèse est recommandée mais pas l’arrêt du traitement. Le risque émétique de l’association est faible ne justifiant pas de traitement préventif systématique. Fréquemment des arthralgies sont notées pouvant justifier l’utilisation de paracétamol, d’AINS ou de faible dose de corticoïdes (6).
Une évaluation du contrôle tumoral toutes les 8 semaines paraît indispensable au vu du coût du traitement et des survies limitées.
Des essais sont en cours combinant immunothérapie anti-PD1 (nivolumab) et traitement par encorafenib/ cetuximab : phase II randomisée du SWOG en cours, les premiers résultats sur 22 malades retrouvant un taux de réponse à 50 % et une survie globale à 15 mois. Le postulat est que les tumeurs BRAFm pMMR ont une charge mutationnelle élevée et que le traitement combiné pourrait favoriser un switch phénotypique pMMR → dMMR.
Tout patient non traité par encorafenib cetuximab en deuxième ligne doit être exposé à ce traitement si son état général le permet. Sinon le recours aux drogues orales comme le regorafenib et le trifluridine-tipiracil a été validé par des essais de phase III (recommandation de grade A, TNCD).
Les différentes séries de la littérature retrouvent toujours la mutation BRAF comme associée à un mauvais pronostic chez les patients atteints de CCRM et opérés de leurs métastases. Cependant, en cas de lésions secondaires opérables, une étude française rétrospective avec appariement a montré que la chirurgie des métastases était possible car associée à la même survie sans rechute (médiane 10 mois versus 13 mois, NS). Par contre, la survie après rechute est plus mauvaise chez les patients BRAFm reflétant leur mauvais pronostic global (médiane 23 versus 44 mois, p= 0,05) (7).
En première ligne métastatique, les résultats de la vaste phase III internationale KEYNOTE 177 ont montré la supériorité d’un traitement par immunothérapie (anticorps anti PD1, 200 mg IV tous les 21 jours) sur la chimiothérapie +/- thérapie ciblée (au choix de l’investigateur) : le bénéfice était significatif en taux de réponse (44 % versus 33 %), médiane de survie sans progression (doublée : 16,5 mois versus 8,2 mois), et non significatif statistiquement mais très pertinent cliniquement en termes de médiane de survie globale (non atteinte versus 36,7 mois) en raison d’un cross-over permettant l’accès à l’immunothérapie dans le bras chimiothérapie. De façon remarquable, la qualité de vie était même améliorée sous traitement dans le bras immunothérapie (figure 5). Dans la population globale de 307 patients, 77 soit 25 % étaient BRAFm V600E. Dans ce sous-groupe, les mêmes bénéfices de l’immunothérapie étaient constatés avec par exemple une amélioration majeure de la survie sans progression (HR 0,48 versus 0,5 pour les non mutés) (8,9).
En conséquence le traitement de première ligne d’un patient atteint de CCRM BRAFmV600 E dMMR est le pembrolizumab (recommandation grade B).
n deuxième ou troisième ligne après échec de l’immunothérapie, il est recommandé chez ces patients d’utiliser l’association encorafenib-cetuximab (grade B). En effet, dans l’essai BEACON, 9,2 % des patients traités dans les bras expérimentaux (41 sur 444) étaient porteurs d’une tumeur dMMR (contre 5 % du bras contrôle). En analyse de sous-groupe le bénéfice de survie globale semblait pertinent dans cette faible population.
En deuxième ligne chez un patient naïf d’immunothérapie, il est recommandé l’accès à un essai d’immunothérapie ou une prescription d’immunothérapie hors AMM validée en RCP.
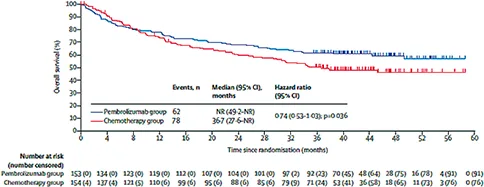
KEYNOTE 177 : courbe de SG actualisée (d’après Diaz LA, et al., Lancet Oncol 2022)
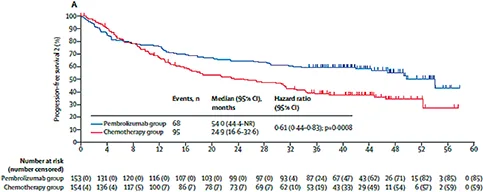
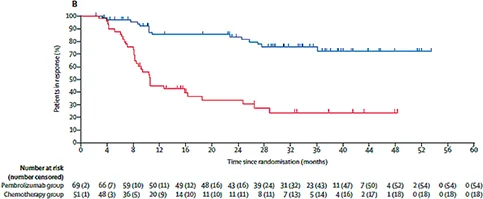
KEYNOTE 177 : courbes de SSP et survie avec réponse actualisées (d’après Diaz LA, et al., Lancet Oncol 2022)
Intérêt de montrer cette courbe pour les patients MSI ? ou montrer l’analyse de sous-groupes des MSI BRAFm
La recherche d’une mutation BRAF V600E est un préalable indispensable pour définir une stratégie optimale de prise en charge d’un patient atteint de CCRM. Elle est associée près d’une fois sur 4 à un phénotype dMMR et dans ce cas le patient doit être traitée par immunothérapie. Chez les patients mutés BRAFV600E, plusieurs lignes de chimiothérapie sont envisageables. Il faudra veiller à surveiller ces patients étroitement en première ligne pour pouvoir offrir au maximum d’entre eux le traitement de recours de deuxième ligne par encorafenib-cetuximab qui peut permettre des survies prolongées sans toxicité majeure. Le développement de nouvelles combinaisons thérapeutiques et en particulier le recours à l’immunothérapie sont indispensables pour améliorer le pronostic de ces patients qui demeure médiocre. Demain, des stratégies adjuvantes et néoadjuvantes seront potentiellement développées aussi dans cette population particulière.
CCRM : cancer colorectal métastatique
dMMR : deficient MisMatch Repair
pMMR : proficient MisMatch Repair
MSI : microsatellite instability
MSS : microsatellite stable
EGFR : epidermal growth factor
MAPK : mitogen activated protein Kinases
NGS : next generation sequencing
RCP : réunion de concertation pluridisciplinaire
RIHN : référentiel des actes innovants hors nomenclature
NB : En cas de recommandation indiquée, le niveau de recommandation est celui du TNCD 2022
Toute reproduction ou réécriture, totale ou partielle, sans l’accord préalable écrit de la FMC HGE est interdite.
FMC HGE : Organisme certifié Qualiopi pour la catégorie ACTIONS DE FORMATION.