Objectifs pédagogiques
- Connaître les symptômes
- Savoir examiner
- Savoir prescrire les examens complémentaires
- Connaître les principes du traitement médical
- Connaître les indications du traitement chirurgical
Aucun
Rectocèle, entérocèle, élytrocèle
Quasi exclusivement observée chez la femme, la rectocèle est une protrusion de la paroi rectale antérieure refoulant la paroi vaginale postérieure. Elle se manifeste par une tuméfaction pouvant faire saillie à la vulve (figure 1). L’élytrocèle se définit comme une hernie du cul de sac de Douglas s’interposant dans la cloison recto-vaginale (figure 2).
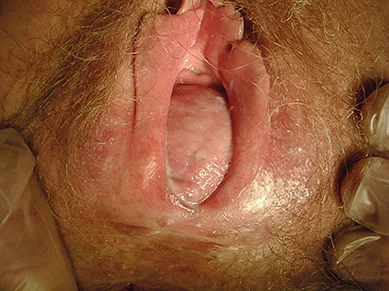
Figure 1 : Colpocèle postérieure en rapport avec une rectocèle
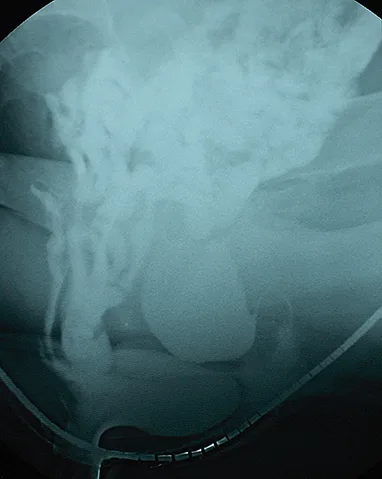
Figure 2 : Défécographie objectivant une rectocèle et une entérocèle
Son contenu peut être variable : péritoine (péritonéocèle), intestin grêle (entérocèle), sigmoïde (sigmoïdocèle). Rectocèle et élytrocèle se manifestent par une colpocèle postérieure, c’est à dire un prolapsus de la paroi vaginale postérieure. Ces anomalies s’intègrent dans le cadre plus large des troubles de la statique pelvienne de la femme associant de façon diverse des pathologies des 3 compartiments pelviens (urinaire antérieur, génital médian, anorectal postérieur).
Ces anomalies sont peu fréquentes chez la femme jeune et nullipare. En revanche 2/3 des femmes ayant accouché présentent des anomalies anatomiques de la statique pelvienne (1). L’âge, la parité, l’obésité, les efforts de poussée excessifs, l’hystérectomie et l’hérédité sont des facteurs de risque identifiés (1).
Le développement des techniques d’imagerie et de la défécographie dans les années 1980 a permis de montrer combien certaines anomalies sont fréquentes. La constatation d’une rectocèle de moins de 2,5 cm est commune et peut être considérée comme physiologique. La prévalence de la rectocèle chez la femme volontaire saine en défécographie varie en effet de 81 à 93 % (2,3). Seules les rectocèles de grande taille peuvent être symptomatiques. L’entérocèle est quant à elle moins commune, présente chez 10 % des volontaires saines dans le travail de Shorvon et al. (3)
Les symptômes sont variés et non spécifiques. Les manifestations digestives sont : une dyschésie, une sensation d’évacuation incomplète ou fragmentée, des efforts de poussée importants ou de manœuvres digitales endovaginales visant à réduire la rectocèle pour en faciliter l’évacuation, des suintements fécaux passifs. Les manifestations gynécologiques sont la perception d’une tuméfaction vaginale pouvant s’extérioriser à la vulve avec parfois une irritation locale liée aux frottements dans les sous-vêtements, des douleurs, une pesanteur pelvienne, une dyspareunie. Certains symptômes peuvent être majorés en position debout ou lors d’efforts physiques, augmentés en fin de journée, soulagés par la position allongée.
Le diagnostic de rectocèle repose sur l’examen clinique réalisé en position gynécologique, préférable à la position genu-pectorale habituellement utilisée pour l’examen proctologique, cette position pouvant sous-estimer l’importance de la rectocèle. La patiente est invitée à pousser de façon à visualiser la saillie de la paroi vaginale postérieure. L’examen peut caractériser les différents éléments des troubles de la statique pelvienne au mieux en utilisant un spéculum de Collin démonté (ou en refoulant au doigt). Placé sur le mur antérieur vaginal, en faisant pousser la malade, l’examen visualise la colpocèle postérieure, dans un second temps l’hémispéculum refoule la paroi vaginale postérieure et permet de mettre en évidence une colpocèle antérieure et de démasquer une incontinence urinaire réduite par « effet pelote ». L’importance de la rectocèle peut être quantifiée selon la classification de Baden-Walker (figure 3). On distingue les rectocèles basses, sus-anales infra-lévatoriennes et des rectocèles hautes sus-lévatoriennes qui intéressent la totalité de la paroi vaginale, souvent associées à une élytrocèle. Le toucher rectal permet de confirmer la rectocèle en plaçant l’index en crochet pour faire saillir dans le vagin, il apprécie la vacuité rectale. La corrélation entre les données de l’examen clinique et celles de la défécographie est bonne et ce d’autant plus que la rectocèle n’est pas de petite taille (4).
| Stade | Localisation du prolapsus |
|---|---|
| 1 | Intravaginal |
| 2 | Affleurant la vulve |
| 3 | Dépassant l’orifice vulvaire |
| 4 | Complètement extériorisé |
Figure 3 : Classification de Baden-Walker des prolapsus
Le diagnostic d’élytrocèle et d’entérocèle est en revanche plus difficile. Classiquement l’entérocèle est recherchée par le toucher bidigital en position debout ou en demandant à la patiente de poser la jambe gauche sur un petit tabouret. La sensation d’interposition entre les 2 doigts d’éléments mobiles, parfois gargouillants, témoigne de la présence dans le cul-de-sac de Douglas d’anses intestinales. Néanmoins, l’examen clinique est le plus souvent très insuffisant au diagnostic d’entérocèle (5) : 50 à 84 % des entérocèles sont en effet méconnues par l’examen clinique.
L’examen clinique recherche par ailleurs des anomalies de la statique pelvienne associées. Au niveau des étages antérieur et médian, il apprécie la distance ano-vulvaire, recherche des cicatrices périnéales, apprécie le tonus anal à l’état basal et la contraction volontaire. Il permet également de rechercher un anisme (contraction paradoxale du canal anal perçue sur le doigt au toucher anorectal à la poussée).
Ils sont habituellement inutiles lors de la prise en charge initiale car leur résultat ne modifie pas celle-ci.
La défécographie est l’examen de référence pour le bilan morphologique des rectocèles. Les alternatives non irradiantes sont l’IRM dynamique et l’échographie transpérinéale ou endovaginale.
La défécographie permet une évaluation dynamique de la morphologie et de la fonction, elle a l’avantage d’être réalisée en position physiologique. Une pâte barytée est introduite dans le rectum, le vagin et le grêle sont également opacifiés, voire pour certains la vessie, réalisant ainsi une colpo- cysto-défécographie. L’examen permet de préciser la capacité du rectum à se vider et l’aptitude de l’appareil sphinctérien à se relâcher. Lorsqu’il existe une rectocèle sa taille et sa vidange en fin de défécation sont précisés.
L’IRM dynamique évite l’irradiation et permet d’étudier les différents compartiments pelviens. Elle n’est habituellement pas réalisée en position physiologique de la défécation. Certaines femmes ne parviennent pas à évacuer pendant l’examen ce qui en limite la pertinence. L’acceptabilité des 2 examens paraît similaire (6). Dans une récente méta analyse de la Cochrane Library regroupant 39 études et 2 483 patients la sensibilité de la défécographie pour le diagnostic respectivement de rectocèle et d’entérocèle était de 98 % (IC 94-99 %), et 91 % (IC 83-97 %) versus 90 % (IC 79-97 %) et 99 % (IC 96-100 %) pour l’IRM dynamique. La spécificité de la défécographie était respectivement pour la rectocèle et l’entérocèle de 78 % (IC 63-90 %) et 96 % (IC 93-99 %) versus 90 % (IC 76-97 %) et 99 % (IC 96-100 %) pour l’IRM dynamique. L’échographie a nettement moins été étudiée que les 2 autres techniques d’imagerie. Le niveau de preuve concernant cet examen est faible mais sa sensibilité et sa spécificité paraissent moins bonnes que celles de la défécographie. Les auteurs concluent à l’avantage de la défécographie (7). Il faut cependant souligner que dans certains centres le choix de l’examen tient aussi compte de la facilité d’accessibilité à la technique et de l’expertise des opérateurs qui peuvent être variables.
La manométrie anorectale permet de confirmer une dyssynergie recto-sphinctérienne suspectée par l’examen clinique, elle quantifie les performances sphinctériennes et apprécie la sensibilité rectale.
Le bilan urodynamique permet de repérer une incontinence urinaire potentielle pouvant se démasquer après correction de la rectocèle (suppression de l’effet « pelote »).
Enfin, selon les cas, d’autres examens peuvent être demandés : échographie endo-anale lorsque des lésions sphinctériennes associées sont suspectées, temps de transit colique aux marqueurs, coloscopie…
Un bilan complémentaire n’a d’intérêt qu’en cas d’échec de la prise en charge initiale lorsqu’un traitement chirurgical est envisagé.
Le traitement médical consiste à traiter la constipation terminale. Outre les habituels conseils diététiques prodigués (alimentation riche en fibre, hydratation), on proposera l’utilisation d’un « accroupisseur » permettant d’évacuer plus efficacement dans une position plus physiologique avec une ouverture de l’angle anorectal améliorée (8). Les laxatifs par voie orale, osmotiques ou mucilages, permettent d’améliorer la consistance des selles, ils sont théoriquement plus utiles en cas de ralentissement du transit associé. Les suppositoires, à dégagement gazeux ou non, facilitant l’exonération (type Eductyl ® ou glycérine) ou les mini lavements peuvent être proposés. La rééducation par biofeedback peut avoir un intérêt en particulier lorsqu’une dys-synergie anorectale associée est suspectée (9).
Concernant les manifestations gynécologiques, il faut souligner que l’efficacité du port d’un pessaire est bien moindre que pour les prolapsus génitaux.
En cas d’échec du traitement médical ou lorsqu’il existe des manifestations gynécologiques invalidantes, la question du traitement chirurgical se pose. Il faut garder à l’esprit que le lien de causalité entre les symptômes de la patiente et les anomalies anatomiques observées ne sont pas systématiquement corrélées. Une cure de rectocèle se discute pour les rectocèles de taille significative, nécessitant des manœuvres digitales évacuatrices ou se vidant mal sur les examens d’imagerie. Il importe de tenir compte du retentissement des troubles sur la qualité de vie et du terrain (comorbidités). En l’absence de facteurs prédictifs du résultat fonctionnel, la patiente doit être informée du risque de d’amélioration incomplète ou d’échec. Ainsi dans une étude contrôlée étudiant la réparation chirurgicale des rectocèles chez 160 femmes, à 1 an, près d’une femme sur 2 reste symptomatique avec des troubles de la défécation persistants (10). L’objectif du traitement est d’améliorer la fonction sans démasquer d’autre troubles de la statique pelvienne et sans engendrer de séquelles.
Les troubles de la statique pelvienne étant fréquemment multi compartimentaux, la décision thérapeutique fait souvent appel à des réunions de concertation pluridisciplinaires.
De multiples techniques chirurgicales de traitement des rectocèles sont décrites. Elles se distinguent par la voie d’abord historiquement très dépendante des chirurgiens la pratiquant, les gynécologues recourant davantage à la voie vaginale ou périnéale, les chirurgiens digestifs à la voie transanale ou abdominale.
La voie transvaginale consiste à ouvrir la paroi vaginale postérieure pour venir plicaturer la paroi rectale herniée, la muqueuse vaginale redondante étant réséquée avant fermeture. Une myorraphie des releveurs peut être associée mais ce geste peut être source de dyspareunie et doit être évité chez la femme sexuellement active (11). Une interposition prothétique peut être réalisée en complément. Actuellement, l’utilisation des prothèses synthétiques est suspendue par la HAS du fait du risque de complications (exposition prothétique, infections, douleurs…). L’utilisation d’une prothèse biologique est sûre mais n’a pas d’avantage en termes d’efficacité (12).
La voie transpérinéale aborde la cloison rectovaginale entre l’anus et le vagin, le principe de la réparation est similaire. L’avantage de cette voie est, pour certains auteurs la possibilité d’une réparation sphinctérienne associée, un risque moindre de dyspareunie mais une étude comparative n’a pas montré de différence significative de ce point de vue (13).
Contrairement à la voie transanale, les voies transvaginale ou transpérinéale permettent d’aborder le cul de sac de Douglas si nécessaire pour traiter une élytrocèle ou une entérocèle associée.
La voie transanale (technique de Sullivan) consiste à réséquer la muqueuse de la face antérieure du rectum en excès jusqu’au sommet de la rectocèle puis à plicaturer à l’aide de fil résorbables la musculeuse rectale de façon longitudinale avant de fermer la muqueuse. La technique dite de STARR (Stapled Transanal Rectal Resection) consiste à réséquer la paroi rectale antérieure avec une pince agrafeuse courbée permettant une suture mécanique. Des complications parfois gravissimes ont été rapportées avec cette technique. Dans un registre européen rapportant 2 838 procédures le taux de complications était de 36 % avec 20 % d’urgences défécatoires, 1,8 % d’incontinence, 5 % de saignements et 4,4 % de sepsis (14).
La voie transanale paraît moins efficace que la voie transvaginale avec un risque relatif de récidive 4 fois supérieur dans une méta-analyse (15). La rectopexie ventrale par voie d’abord abdominale par cœlioscopie consiste à réaliser une promontofixation ventrale du rectum à l’aide d’une prothèse synthétique non résorbable. Cette intervention permet de traiter entérocèle, élytrocèle et d’autres troubles de la statique pelvienne éventuellement associés en rajoutant une bandelette antérieure pour traiter cystocèle ou prolapsus génital. L’efficacité à long terme de cette technique est excellente avec un taux de récidive de 8,2 % à 10 ans dans une série de 919 malades, une régression de la dyschésie dans 74 % des cas (16). Des complications en rapport avec la bandelette étaient observées chez 4,6 % des malades à 10 ans dans cette série. L’intervention peut être réalisée par robot sans différence sur la durée opératoire, avec une durée moyenne d’hospitalisation significativement moindre [-0,42 (IC 95 % -0,67-0,17)], sans que le gain en termes d’efficacité et de sécurité soit démontré (17). Le rapport coût/ efficacité de l’intervention robot reste à préciser.
La rectopexie ventrale paraît peut être finalement l’intervention de choix car elle offre habituellement des suites simples et une meilleure efficacité à long terme par rapport aux voies d’abord gynécologiques et transanales. Il n’existe cependant pas de recommandation concernant la technique chirurgicale à employer et la voie vaginale peut se discuter en cas de rectocèle isolée ayant des manifestations essentiellement d’ordre gynécologique.
Il faut savoir évoquer et rechercher une rectocèle chez les femmes consultant pour dyschésie.
L’examen clinique permet facilement de suspecter le diagnostic et les examens complémentaires ne sont pas systématiquement indiqués en première intention. Lorsque le traitement médical est en échec, un traitement chirurgical se discute mais il est parfois difficile de rattacher les symptômes aux anomalies anatomiques mises en évidence qui peuvent s’observer chez la volontaire saine, notamment pour la rectocèle.
Les techniques chirurgicales sont multiples. La voie laparoscopique tend à s’imposer, offrant une excellente efficacité, une morbidité faible et permet de traiter toutes les composantes des troubles de la statique pelvienne.
IRM : imagerie par résonance magnétique
HAS : haute autorité de santé
Toute reproduction ou réécriture, totale ou partielle, sans l’accord préalable écrit de la FMC HGE est interdite.
FMC HGE : Organisme certifié Qualiopi pour la catégorie ACTIONS DE FORMATION.