Liens d’intérêt
Ambu ; Norgine : participation à des Boards ; Pentax : fonds de recherche, consulting ; Medtronic : consulting ; Dr Falk Pharma : intervention rémunérée. Olympus : organisation de formations
Mots-clés
Reflux gastro-œsophagien ; Hernie hiatale ; pH-métrie ; Fundoplicature.
Introduction
Le reflux gastro-œsophagien est un phénomène physiologique au cours duquel le contenu de l’estomac remonte dans l’œsophage. Ce phénomène peut, par sa fréquence ou son intensité, entrainer des symptômes gênants et des complications. Le RGO pathologique résulte de quatre principaux mécanismes (1) :
- Une déficience de la barrière antireflux au niveau de la jonction œsogastrique, en rapport avec une hernie hiatale et/ ou avec une hypotonie ou encore des relaxations prolongées du tonus du sphincter inférieur de l’œsophage (SIO).
- Une hypo motricité du corps de l’œsophage (péristaltisme absent ou motricité œsophagienne inefficace), entraînant un défaut de clairance œsophagienne au décours d’un épisode de reflux.
- Un retard à la vidange gastrique.
- Une hyperpression abdominale, par exemple secondaire à l’obésité, la grossesse, des efforts de toux ou de poussée chroniques.
Si les symptômes de pyrosis et de régurgitations sont considérés comme typiques, une large gamme de manifestations a été attribuée au RGO, de la toux chronique à la fibrose pulmonaire idiopathique, en passant par la laryngite postérieure et les érosions dentaires.
La prévalence du RGO est évaluée à 13 % dans la population mondiale, à 15 % en Amérique du Nord (2). Dans une étude récente nationale conduite aux États-Unis, 31 % des répondants rapportaient des symptômes de RGO la semaine précédente (3). Les facteurs de risque de RGO incluent un âge de 50 ans ou plus, le sexe féminin, l’intoxication tabagique, la prise d’anti-inflammatoires non stéroïdiens, l’obésité, (IMC > 30 Kg/m2), un faible niveau socio-économique.
Si les explorations fonctionnelles œsophagiennes permettent d’établir ou d’infirmer le diagnostic de RGO, le caractère invasif et contraignant de la pH-métrie/pH-impédancemétrie des 24 heures, ainsi que l’accessibilité du test rendent son utilisation chez tous les patients symptomatiques irréaliste. Cependant, la spécificité des symptômes typiques de RGO n’est que de 70 %, celle d’un test thérapeutique aux inhibiteurs de la pompe à protons (IPP) de 44 %, et l’endoscopie œso-gastro-duodénale (EOGD) est normale chez 60 à 70 % des patients (4). Il faut donc insister sur la faible valeur diagnostique d’une endoscopie normale, et rappeler qu’une œsophagite peptique de grade A est observée chez 5 à 7 % des sujets asymptomatiques pour le RGO (4). 30 % des patients avec un RGO acide pathologique auront donc une œsophagite peptique, et 5 à 12 % un œsophage de Barrett.
Si les premières étapes de la prise en charge thérapeutique impliquent l’application de règles hygiéno-diététiques, parmi lesquelles la perte de poids, la surélévation de la tête du lit, le coucher en décubitus latéral gauche (5), ou encore le respect d’un intervalle de 3 heures entre la fin du repas et le coucher, les traitements pharmacologiques, antiacides (sels d’aluminium), à base d’alginates, antihistaminiques de type H2 (famotidine), et bien sûr inhibiteurs de la pompe à protons sont fréquemment requis. Si la posologie recommandée d’IPP dans le RGO non compliqué est la demi-dose pendant 4 semaines, la question d’un traitement chirurgical du RGO ne peut se poser que chez un patient ayant déjà suivi un traitement par IPP à double dose pendant au moins 8 semaines, sans amélioration significative. En effet, le traitement chirurgical n’est ni efficace à 100 %, ni définitif, ni dépourvu de complications, et les résultats du grand essai multicentrique randomisé LOTUS font état d’un taux de contrôle symptomatique similaire pour les IPP ou la chirurgie antireflux à 3 ans (93 % vs. 90 %, respectivement, p = 0,25) et à 5 ans (92 % vs. 85 %, respectivement, p = 0,048) (6).
Quels patients faut-il adresser au chirurgien ?
La question de la chirurgie antireflux se pose chez les patients présentant un RGO réfractaire. Qu’est-ce qu’un RGO réfractaire ? Un RGO établi, par une pH-métrie sans traitement préalable, la présence d’une œsophagite peptique de grade C ou D, ou un œsophage de Barrett de plus de 1 cm en endoscopie, confirmé histologiquement, et dont certaines manifestations objectives persistent sous traitement médicamenteux. On parle donc bien de patients ayant une œsophagite peptique persistante sous traitement, ou une pH-impédancemétrie sous traitement pathologique par le taux d’exposition acide ou la présence de reflux non ou faiblement acides, et non pas uniquement de symptômes de RGO réfractaires (7,8). Nombre des patients qui se présentent ainsi n’ont en effet pas de RGO réfractaire, mais :
- un pyrosis fonctionnel, avec des symptômes de RGO réfractaires aux IPP, mais pas de RGO objectivé en endoscopie ou en pH/pH-impédancemétrie. Il faut souligner ici la fréquence des symptômes ORL, notamment de douleur ou de gêne pharyngée, souvent attribués au décours d’un examen ORL au reflux gastro-œsophagien, qui sont exceptionnellement au premier plan dans le RGO réfractaire, et ne constituent bien sûr pas en eux-mêmes une indication de chirurgie antireflux.
- un RGO authentique, mais un défaut d’observance aux IPP, ou bien du fait d’oublis de prises ou de prises per/post prandiales, ou bien du fait d’une peur des effets secondaires.
À cet égard, il convient de rappeler l’excellent profil de tolérance des IPP au long cours, l’abondante littérature sur le sujet ayant suggéré que des associations pathologiques avec des infections à C. difficile, des gastroentérites bactériennes, une pullulation microbienne du grêle, des pneumopathies infectieuses, des insuffisances rénales chroniques, des fractures osseuses, des démences, et des infarctus du myocarde, mais sans
jamais établir de rapport de causalité (9,10). Dans un essai randomisé contrôlé incluant plus de 17 000 participants, l’administration de pantoprazole à 40 mg par jour pendant 3 ans était associée à une augmentation statistiquement significative des infections intestinales passant de 1 % à 1,4 % dans le groupe sous IPP, sans qu’aucun autre effet secondaire soit enregistré (11).
Ainsi, non seulement la prise d’IPP, lorsqu’elle est indiquée et efficace, doit être encouragée, mais le choix d’une option chirurgicale par peur de la prise prolongée des IPP paraît une option déraisonnable.
En premier lieu, ces patients se verront proposer, après une réévaluation diagnostique, une adaptation thérapeutique, reposant sur l’ajout d’alginates ou d’antiacides en cas de symptômes d’intervalle, d’antihistaminiques de type anti-H2 (12) en cas de symptômes nocturnes, de baclofene (13) en cas de régurgitations et d’éructations prédominantes, ou encore de prokinétiques (14) en cas de symptômes gastroparétiques associés. Il est à noter que ces deux dernières options sont difficilement applicables en pratique quotidienne, compte tenu d’abord du nombre de prises médicamenteuses, des durées de traitement à envisager, et enfin des effets secondaires, en notamment neurologiques, du baclofène.
Le patient ayant un RGO réfractaire documenté, en particulier si les symptômes réfractaires incluent des régurgitations, peut donc être adressé au chirurgien pour discuter d’une chirurgie antireflux. Bien que l’utilisation de questionnaires de qualité de vie ou de symptômes détaillés du RGO ne soit pas répandue dans la pratique quotidienne, la question d’une chirurgie potentiellement morbide ne peut se poser que chez un patient dont la qualité de vie est significativement altérée au quotidien par ses symptômes de RGO. Le patient doit être informé des symptômes susceptibles d’être améliorés par un traitement chirurgical du reflux : les régurgitations, possiblement la toux ou d’éventuelles manifestations respiratoires, plus rarement les phénomènes douloureux. En effet, il est fort probable qu’un pyrosis non amélioré par les IPP soit d’origine fonctionnelle, et ne soit donc pas plus amélioré par la cure chirurgicale du RGO. Il en est de même pour les symptômes de douleur ou de gêne pharyngée. Enfin, l’âge moyen d’inclusion des patients dans les études chirurgicales du RGO est de 50 ans, et l’inclusion de patients de plus de 70 ans est exceptionnelle. Il n’est donc pas usuel, même devant un RGO réfractaire documenté, de proposer un traitement chirurgical du RGO après 70 ans.
Quel bilan avant une chirurgie du reflux gastro-œsophagien ?
Poser cette question revient à poser la question de la définition du reflux gastro-œsophagien pathologique. La conférence de consensus de Lyon de 2018 rappelle les critères diagnostiques du RGO, et notamment les critères diagnostiques majeurs suffisant à établir le RGO que sont une œsophagite peptique de grade (B), C ou D en endoscopie (figure 1), une sténose peptique, un œsophage de Barrett long, ou encore un temps d’exposition acide supérieur à 6 % du temps d’enregistrement sur la pH-métrie des 24 heures (4). Ces critères sont rappelés dans le tableau 1.

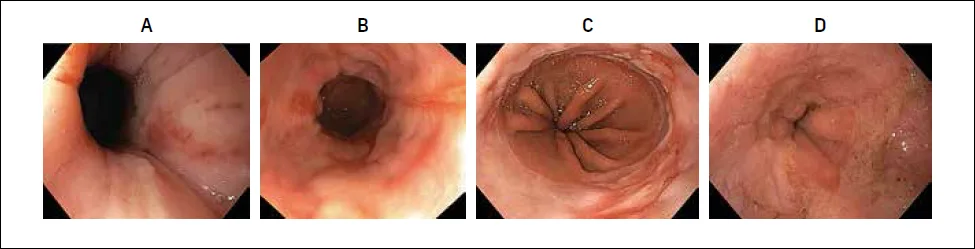
Figure 1 : Classification endoscopique de Los Angeles des oesophagites peptiques (27)
A : Grade A : une ou plusieurs pertes de substance <5 mm
B : Grade B : une ou plusieurs pertes de substance >5 mm limitées à la crête des plis muqueux, sans extension entre eux
C : Grade C : présence d’au moins une perte de substance s’étendant entre 2 plis mais non circonférentielle (<75 % circonférence)
D : Grade D : perte de substance circonférentielle
| | pH-métrie ou pH-impédancemétrie des 24 heures |
|---|
| Endoscopie œsogastroduodénale | | Temps d’exposition acide <4 %, moins de 40 épisodes de reflux | Temps d’exposition acide = 4-6 %, 40-80 épisodes de reflux | Temps d’exposition acide >6 % |
Œsophagite peptique de grade A ou normale | Pas de RGO | RGO possible | RGO certain |
Œsophagite peptique grade B, C ou D | Reflux gastro-œsophagien certain. Pas d’indication à une mesure objective du reflux par pH-métrie. |
| Œsophage de Barrett long (≥ 3 cm) |
Sténose peptique |
Tableau 1 : Les critères diagnostiques du RGO, d’après (4,29)
Même si elle n’apparaît pas dans les critères diagnostiques simplifiés, il faut souligner l’importance de l’analyse de la corrélation reflux-symptômes dans le compte rendu de la pH-métrie œsophagienne. En effet, le recueil des symptômes sur 24 heures permet tout d’abord de confirmer la réalité de la gêne quotidienne ressentie par le patient. De plus, l’analyse par des tests statistiques simples de la corrélation entre ces symptômes et les éventuels évènements de RGO permettront, lors de la consultation préopératoire avec le patient, de lui expliquer quels symptômes sont liés au reflux chez lui et sont donc susceptibles d’être améliorés par la chirurgie, et quels symptômes sont manifestement indépendants du RGO et devraient donc persister après la chirurgie. Ceci souligne l’importance d’une mesure objective du RGO avant une chirurgie du reflux gastro-œsophagien. Il faut cependant rappeler que cette approche, aussi puissante qu’elle soit sur le plan diagnostique et pronostique, suppose une coopération parfaite du patient, qu’il s’agisse de la tolérance de la sonde pendant 24 heures, et surtout du rapport fiable de ses symptômes au moment précis où ils sont ressentis.
Le bilan minimal consiste donc en une endoscopie œso-gastro-duodénale : en l’absence de signes endoscopiques établissant le RGO, une pH-métrie œsophagienne est indispensable. Comme nous venons de le mentionner, en présence de signes endoscopiques établissant le RGO, une mesure objective du reflux par pH-métrie peut être cependant utile en cas de symptômes multiples et atypiques (symptomatologie ORL notamment, toux), non pas pour documenter le RGO, mais pour déterminer le lien entre le RGO et les symptômes rapportés, et donc le bénéfice que l’on peut attendre d’une intervention chirurgicale. Lorsque le RGO n’a jamais été documenté avec certitude par le passé chez un patient, une pH-métrie des 24 heures sans traitement est suffisante. Chez un patient ayant un RGO précédemment documenté, une pH-impédancemétrie des 24 heures sous traitement IPP permet de documenter le lien entre le RGO et les symptômes résiduels sous IPP. Un travail récent a permis d’établir que, sous IPP, le seuil de 4 % de temps d’exposition acide et/ ou de 80 reflux par 24 heures était prédictif de symptômes de RGO persistants et associé à 85 % d’amélioration clinique après cure chirurgicale du RGO (15). Des aspects caractéristiques sont présentés sur la figure 2.

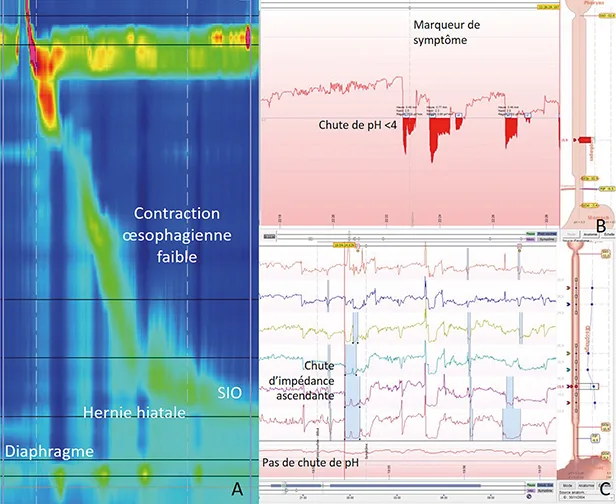
Figure 2 : Exemples d’explorations fonctionnelles oesophagiennes
A : Manométrie oesophagienne haute résolution, montrant une hernie hiatale et une contraction oesophagienne péristaltique hypotonique (index de contraction distale de 190 mmHg.s.cm)
B : Tracé de pH-métrie oesophagienne montrant un épisode de reflux acide (pH < 4) associé à un symptôme rapporté par le patient, considéré comme significatif car survenu dans les 2 mn suivant le reflux acide
C : Tracé de pH-impédancemétrie montrant un épisode de reflux non acide (pH > 4), caractérisé par une chute d’impédance de plus de 50 % sur plus de deux capteurs consécutifs, de mouvement ascendant, et associé à un symptôme rapporté
par la patiente
La manométrie œsophagienne en elle-même n’est pas utile au diagnostic du RGO. Elle peut être réalisée avant une pH-métrie ou pH-impédancemétrie œsophagienne afin de repérer précisément la position du sphincter inférieur de l’œsophage, et ainsi déterminer où positionner la sonde de pH-métrie pour qu’elle soit bien 5 cm en amont du SIO. Il existe cependant des signes manométriques associés au RGO : hernie hiatale et hypotonie de la JOG, syndrome de motricité inefficace. L’absence de péristaltisme œsophagien (apéristaltisme) doit faire évoquer la possibilité d’une achalasie, et doit donc inciter à la prudence avant de poser l’indication de chirurgie anti-reflux. Par ailleurs, un syndrome de motricité inefficace, ou encore une absence de réserve contractile œsophagienne (lors des déglutitions répétées) avaient été proposés comme des critères prédictifs de dysphagie post fundoplicature par certains auteurs (16). Cependant, ces données restent fragiles, reposant sur de petits effectifs et des données rétrospectives. Il reste cependant recommandé de réaliser une manométrie œsophagienne avant toute chirurgie anti-reflux, ne serait-ce qu’à visée médico-légale en cas de survenue de troubles moteurs œsophagiens post-opératoires.
Enfin, si un scanner thoracoabdominal avec opacification digestive haute est fréquemment demandé avant une chirurgie antireflux pour évaluer l’environnement péri-œsophagien, l’utilité du transit œsophagien, moins performant que la manométrie pour le diagnostic d’une hernie hiatale (17), paraît limitée.
Les principaux diagnostics différentiels du RGO réfractaire à éliminer avant une prise en charge chirurgicale sont rappelés dans le tableau 2.
| Symptômes | Outil diagnostique | Critère diagnostique |
|---|
| Achalasie | Dysphagie, régurgitations alimentaires, perte de poids, douleurs thoraciques | Manométrie œsophagienne haute résolution, transit œsophagien | Défaut de relaxation de la jonction œsogastrique |
| Syndrome de rumination | Régurgitation post prandiale du contenu gastrique | Manométrie œsophagienne haute résolution, manométrie avec impédancemétrie | Augmentation simultanée de la pression intraabdominale et thoracique |
| Eructations et éructations supra- gastriques | Déglutition d’air, suivie d’éructations | pH-impédancemétrie | Mouvement antérograde puis rétrograde d’air le long de l’œsophage |
| Œsophagite infectieuse | Dysphagie | Endoscopie œsogastroduodénale | Biopsies œsophagiennes |
| Œsophagite à éosinophiles | Dysphagie | Endoscopie œsogastroduodénale | Aspect endoscopiques suggestifs, biopsies œsophagiennes |
| Diverticule œsophagien | Régurgitations alimentaires post prandiales | Endoscopie œsogastroduodénale, transit œsophagien | Image d’addition périœsophagienne, endoscopique ou radiologique |
| Trouble fonctionnel (Pyrosis, dysphagie fonctionnelle, …) | Tout symptôme œsophagien | Endoscopie œsogastroduodénale, Manométrie œsophagienne haute résolution, pH-impédancemétrie, transit œsophagien | Absence d’anomalie significative objectivée |
Tableau 2 : Quelles pathologies mimant un RGO réfractaire faut-il avoir éliminé avant d’envisager une prise en charge chirurgicale, d’après (30) ?
Quels résultats, et quelles complications de la chirurgie du reflux gastro-œsophagien et comment les prendre en charge ?
Le principe de la chirurgie du reflux gastro-œsophagien est la réintégration du sphincter inférieur de l’œsophage dans la cavité abdominale, au moyen d’une myoraphie des piliers du diaphragme pour les resserrer, et d’une fundoplicature, totale ou partielle. En 2023, cette chirurgie est réalisée par voie laparoscopique ou robotique, avec des résultats comparables. La mortalité est nulle et le taux de complication de moins de 5 %.
L’essai randomisé et multicentrique LOTUS qui a comparé plus de 200 patients souffrant de reflux traités par Oméprazole ou par fundoplicature de Nissen avec 5 ans de suivi concluait à un taux de contrôle des symptômes à 5 ans de 92 % dans le groupe IPP contre 85 % dans le groupe chirurgie, respectivement, p = 0,048. Cependant, il faut noter que le pyrosis était plus fréquent dans le groupe IPP (16 % vs. 8 %, p = 0,14), tout comme les régurgitations, cette fois-ci de façon significative (13 % vs. 2 %, p = 0,001). À l’opposé, la dysphagie était plus fréquente dans le groupe opéré (11 % vs. 5 %, p = 0,01), de même que les ballonnements (40 % vs. 28 %, p = 0,01). Aucune mortalité liée au traitement n’était enregistrée (6). Ces résultats illustrent très bien l’expérience de la chirurgie du reflux, c’est à dire un meilleur contrôle des régurgitations chez les patients opérés, au prix de symptômes fonctionnels de ballonnements. En effet, la difficulté à éructer après fundoplicature explique le phénomène de piégeage de l’air ingéré et donc des ballonnements abdominaux. Une gastroparésie ou une diarrhée motrice, liées au traumatisme du nerf vague, peuvent être rapportées. Enfin, une récidive des symptômes, liée à la laxité du montage antireflux ou plus souvent à son ascension intrathoracique peut être observée. Il faut en effet garder en tête qu’un patient sur cinq opéré du RGO aura repris les IPP à 5 ans (18). La dysphagie post opératoire est une problématique plus rare mais beaucoup plus invalidante. Elle impose un bilan diagnostique associant une endoscopie, un transit œsophagien, et une manométrie. En cas de montage d’emblée trop serré, ou de sclérose secondaire de la valve antireflux, on observe un tableau de pseudo-achalasie, y compris manométrique. Quoique cette complication soit trois fois moins fréquente avec la fundoplicature postérieure partielle qu’avec l’intervention de Nissen (19), justifiant la généralisation de la fundoplicature de Toupet à l’heure actuelle (20), la dysphagie post fundoplicature est une complication de prise en charge difficile. La figure 3 montre des aspects endoscopiques habituels et pathologiques après fundoplicature. Une première étape de la prise en charge consiste à tenter une dilatation pneumatique endoscopique de la jonction œsogastrique. L’efficacité de cette approche est contestée (21,22) : quoiqu’il en soit, une dilatation à 35 mm et 40 mm, jusqu’à effacement de l’encoche sur le ballonnet, ce qui peut nécessiter une augmentation importante des pressions, au delà de 10 atm, est une étape logique avant de proposer une reprise chirurgicale à risque de morbidité et de résection œsogastrique. Au total, 7 à 10 % des patients opérés d’une fundoplicature devront être finalement réopérés. En cas de dysphagie associée à une récidive herniaire, une ascension intrathoracique du montage, ou une valve trop basse, le traitement endoscopique est vain, et la seule alternative au traitement médical sera une reprise chirurgicale avec réfection du montage.
Les facteurs prédictifs de succès du traitement chirurgical du RGO sont l’exposition acide pathologique préopératoire, l’œsophagite peptique en endoscopie, les symptomes typiques de RGO, la présence d’une hernie hiatale, la réponse aux traitements antireflux, l’absence de défaut de relaxation de la jonction œsogastrique en manométrie, et l’expérience du chirurgien (2). Un essai randomisé récent confirmait l’intérêt de la chirurgie par rapport au traitement médical, même optimisé, à la condition d’une stricte sélection des patients : seuls 20 % des patients dits « résistants aux IPP » étaient finalement randomisés ! (8).
Un système d’augmentation magnétique du sphincter inférieur de l’œsophage (LINX, Johnson and Johnson, shoreview, MN, USA), fait de billes de titane avec un centre aimanté, peut être placé, sous cœlioscopie, autour de la jonction œsogastrique pour augmenter la barrière anti-reflux. Son effet sur les régurgitations acides a été établi comme supérieur à celui des IPP à double dose, pour une durée d’au moins un an, et sans complications majeures. Plus de 80 % des patients interrompaient les IPP, et une normalisation de la pH-métrie était observée (23). Cependant, les données prospectives et de long terme liées à cette technique sont actuellement limitées (24), et la perspective de migrations intraœsophagiennes du dispositif rapportées jusqu’à 2 % des cas en limitent l’utilisation actuellement.
Enfin, pour le cas particulier du patient obèse, avec un Index de masse corporelle de 35 Kg/m2 ou plus présentant un RGO, ou présentant un RGO décompensé par une sleeve gastrectomy, la fundoplicature est d’efficacité modeste (ou techniquement impossible dans le cas de la sleeve) et la réalisation d’un bypass avec anse en Y permettra de combiner une intervention bariatrique et un traitement optimal du RGO.

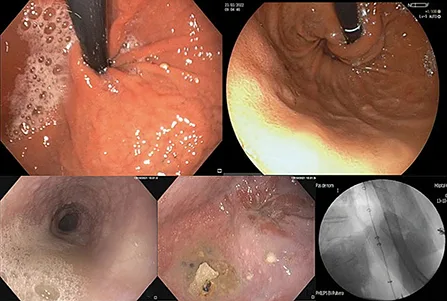
Figure 3 : Aspect endoscopique après fundoplicature
A et B : Aspect normal de la fundoplicature, partielle (A) ou totale (B) en rétrovision
C – E : Aspect de stase oesophagienne avec pseudoachalasie, ressaut au passage de la jonction oesogastrique, et nette empreinte sur le ballon de dilatation pneumatique de 40 mm
Les traitements endoscopiques du reflux gastro-œsophagien : où en sommes-nous ?
L’application d’une énergie de radiofréquence par voie endoscopique au niveau de la jonction œsogastrique, via le dispositif Stretta (Restech, Houston, Texas, USA) dans le but de créer une fibrose sous muqueuse et donc de diminuer la compliance du SIO, a fait l’objet, depuis le début des années 2000, de multiples évaluations, notamment randomisées et contrôlées (25). La première et notable limite de ce traitement est sa contre-indication en cas d’œsophagite peptique. Ensuite, si la sécurité du dispositif est satisfaisante, il n’a démontré qu’une amélioration de scores cliniques, et pas d’effet significatif sur la pH-métrie.
La fundoplicature transorale (TIF pour transoral incisionless fundoplication, EsophyX, Endogastric, Redmond, WA, USA) utilisant un dispositif endoscopique dédié a été évalué contre procédures fictives et contre IPP, dans des essais contrôlés randomisés, et a démontré une amélioration clinique chez 66 % des patients, et une diminution du temps d’exposition acide œsophagien comparable à celle obtenue par les IPP. Les limites de ce traitement sont l’exclusion des patients avec des hernies hiatales de plus de 2 cm et avec des œsophagites peptiques sévères. Malheureusement, les données à long terme montrent une perte d’efficacité, avec une reprise des IPP à 5 ans chez deux patients sur trois (25). Un dispositif voisin, le MUSE (Medigus ultrasonic surgical endostapler (MUSE; Medigus, Omer, Israel), permettant également l’agrafage de la grosse tubérosité sur elle-même par voie endogastrique, n’a cependant pas fait la preuve de son efficacité sur les paramètres objectifs du RGO, et des cas de perforation œsophagienne ont limité considérablement sa diffusion (25).
Depuis 2014, une autre approche thérapeutique endoscopique du RGO, reposant sur la création d’une fibrose cicatricielle sous cardiale, a été proposée. On parle d’ARMI, pour Antireflux Mucosal Interventions, un terme qui regroupe la mucosectomie sous cardiale antireflux (ARMS), l’ablation sous cardiale au plasma argon (ARMA), ou les ligatures élastiques sous cardiales (ARBL). Aucune de ces techniques n’a été évaluée à ce jour dans le cadre d’un essai randomisé, et le niveau de preuve se limite à des séries de cas, chez des patients sélectionnés, notamment sans hernie hiatale significative, de grade III ou IV de Hill (figure 4). L’efficacité clinique rapportée est d’environ 74 %, comparable entre les ARMI, et une amélioration des paramètres pH métriques était notée. En revanche, 2 % de perforations étaient enregistrées avec l’ARMS, et le risque de sténose œsophagienne, estimé à 10 %, est probablement sous-estimé (26). Actuellement, ces techniques ne sont pas recommandées en pratique courante et une évaluation de leur efficacité ainsi que leur potentielle place dans l’algorithme thérapeutique reste à évaluer (25).

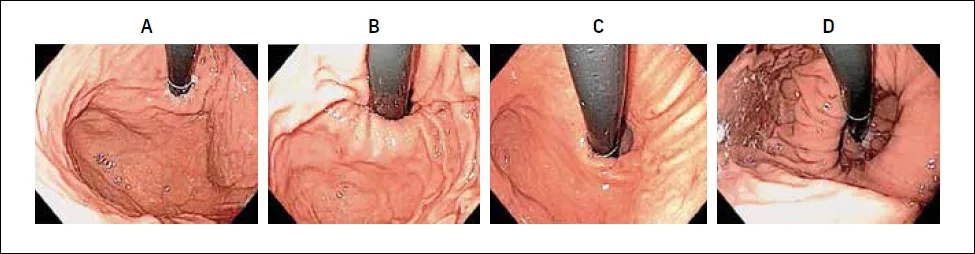
Figure 4 : Classification endoscopique de Hill des hernies hiatales, d’après (28) (en rétro-vision)
A : Grade I, présence d’un pli proéminent au contact de l’endoscope, sur la petite courbure
B : Grade II, le pli est moins proéminent, et la jonction oesogastrique baille par moments
C : Grade III, le pli n’est pas visible, et la jonction oesogastrique n’enserre pas l’endoscope
D : Grade IV, il n’y a pas de pli, et la lumière oesophagienne est visible depuis l’estomac
Les principaux résultats des traitements endoscopiques du RGO sont rappelés dans le tableau 3. Au total, quoique les recommandations européennes autorisent la pratique du Stretta et la TIF chez des patients hautement sélectionnés refusant les IPP et la fundoplicature chirurgicale (25), ces traitements ne sont actuellement pas disponibles en France.
| Intérêt | Limites | Qualité des études | Efficacité sur les paramètres objectifs du RGO | Utilisation actuelle |
|---|
| Radiofréquence du SIO | Faible morbidité | Contre indiqué en cas d’œsophagite | Elevée | Non | Possible, mais pas disponible en France |
| Fundoplicature endoscopique (TIF) | Proche d’une fundoplicature chirurgicale | Coût Exclusion des cas les plus sévères Durabilité des résultats | Elevée | Oui | Possible, mais pas disponible en France |
| Fundoplicature Endoscopique (MUSE) | Proche d’une fundoplicature chirurgicale | Coût Exclusion des cas les plus sévères Cas de morbidité sévère | Faible | Non | Non recommandée |
| ARMI | Pas d’équipement spécifique nécessaire | Sténose cicatricielle | Faible | Oui | Non recommandée |
Tableau 3 : Résultats des principaux traitements endoscopiques du RGO
SIO : Sphincter inférieur de l’oesophage
TIF : Transoral incisionless fundoplication
MUSE : Medigus Ultrasonic Surgical Endostapler
ARMI : Antireflux Mucosal Interventions
Conclusion
La chirurgie n’est pas un traitement de première intention du RGO. Elle ne s’envisage qu’en cas d’échec du contrôle des symptômes par un traitement médicamenteux optimisé, comprenant au moins des inhibiteurs de la pompe à protons à double dose. L’intervention de référence est la fundoplicature partielle postérieure dite de Toupet, laparoscopique. Elle doit être pratiquée par des opérateurs entraînés, chez des patients bien sélectionnés, au mieux par une endoscopie œsogastroduodénale et une pH-impédancemétrie sous traitement IPP, permettant de déterminer les symptômes corrélés au RGO et donc susceptibles d’être améliorés par le geste chirurgical. En 2023, le traitement endoscopique du RGO doit encore rester dans le domaine de la recherche clinique avec une évaluation de l’efficacité à moyen terme, et des pistes prometteuses d’interventions sous cardiales fibrosantes sont à l’étude.
Références
- Bredenoord AJ, Pandolfino JE, Smout Gastro-oesophageal reflux disease. Lancet. 2013 Jun 1;381(9881):1933–42.
- Fass Gastroesophageal Reflux Disease. N Engl J Med. 2022 Sep 29;387(13):1207–16.
- Delshad SD, Almario CV, Chey WD, Spiegel Prevalence of Gastroesophageal Reflux Disease and Proton Pump Inhibitor-Refractory Symptoms. Gastroenterology. 2020 Apr;158(5):1250-1261.e2.
- Gyawali CP, Kahrilas PJ, Savarino E, Zerbib F, Mion F, Smout AJPM, et al. Modern diagnosis of GERD: the Lyon Consensus. Gut. 2018 Jul;67(7):1351–62.
- Schuitenmaker JM, Kuipers T, Oude Nijhuis RAB, Schijven MP, Smout AJPM, Fockens P, et al. Sleep Positional Therapy for Nocturnal Gastroesophageal Reflux: A Double-Blind, Randomized, Sham-Controlled Clin Gastroenterol Hepatol. 2022 Dec;20(12):2753-2762.e2.
- Galmiche JP, Hatlebakk J, Attwood S, Ell C, Fiocca R, Eklund S, et Laparoscopic antireflux surgery vs esomeprazole treatment for chronic GERD: the LOTUS randomized clinical trial. JAMA. 2011 May 18;305(19):1969–77.
- Zerbib F, Bredenoord AJ, Fass R, Kahrilas PJ, Roman S, Savarino E, et al. ESNM/ANMS consensus paper: Diagnosis and management of refractory gastro-esophageal reflux Neurogastroenterol Motil. 2021 Apr;33(4):e14075.
- Spechler SJ, Hunter JG, Jones KM, Lee R, Smith BR, Mashimo H, et al. Randomized Trial of Medical versus Surgical Treatment for Refractory Heartburn. N Engl J Med. 2019 Oct 17;381(16):1513–23.
- Attwood SE, Ell C, Galmiche JP, Fiocca R, Hatlebakk JG, Hasselgren B, et Long-term safety of proton pump inhibitor therapy assessed under controlled, randomised clinical trial conditions: data from the SOPRAN and LOTUS studies. Aliment Pharmacol Ther. 2015 Jun;41(11):1162–74.
- Salvo EM, Ferko NC, Cash SB, Gonzalez A, Kahrilas PJ. Umbrella review of 42 systematic reviews with meta-analyses: the safety of proton pump inhibitors. Aliment Pharmacol Ther. 2021 Jul;54(2):129–43.
- Moayyedi P, Eikelboom JW, Bosch J, Connolly SJ, Dyal L, Shestakovska O, et al. Safety of Proton Pump Inhibitors Based on a Large, Multi-Year, Randomized Trial of Patients Receiving Rivaroxaban or Aspirin. Gastroenterology. 2019 Sep;157(3):682-691.e2.
- Abdul-Hussein M, Freeman J, Castell D. Concomitant Administration of a Histamine2 Receptor Antagonist and Proton Pump Inhibitor Enhances Gastric Acid Suppression. Pharmacotherapy. 2015 Dec;35(12):1124–9.
- Pauwels A, Raymenants K, Geeraerts A, Boecxstaens V, Masuy I, Broers C, et al. Clinical trial: a controlled trial of baclofen add-on therapy in PPI-refractory gastro-oesophageal reflux Aliment Pharmacol Ther. 2022 Jul;56(2):231–9.
- Foocharoen C, Chunlertrith K, Mairiang P, Mahakkanukrauh A, Suwannaroj S, Namvijit S, et al. Effectiveness of add-on therapy with domperidone vs alginic acid in proton pump inhibitor partial response gastro-oesophageal reflux disease in systemic sclerosis: randomized placebo- controlled trial. Rheumatology (Oxford). 2017 Feb;56(2):214–22.
- Gyawali CP, Tutuian R, Zerbib F, Rogers BD, Frazzoni M, Roman S, et al. Value of pH Impedance Monitoring While on Twice-Daily Proton Pump Inhibitor Therapy to Identify Need for Escalation of Reflux Gastroenterology. 2021 Nov;161(5):1412–22.
- Yadlapati R, Kahrilas PJ, Fox MR, Bredenoord AJ, Prakash Gyawali C, Roman S, et al. Esophageal motility disorders on high-resolution manometry: Chicago classification version 0©. Neurogastroenterol Motil. 2021 Jan;33(1):e14058.
- Li L, Gao H, Zhang C, Tu J, Geng X, Wang J, et al. Diagnostic value of X-ray, endoscopy, and high-resolution manometry for hiatal hernia: A systematic review and meta-analysis. J Gastroenterol Hepatol. 2020 Jan;35(1):13–8.
- McKinley SK, Dirks RC, Walsh D, Hollands C, Arthur LE, Rodriguez N, et Surgical treatment of GERD: systematic review and meta-analysis. Surg Endosc. 2021 Aug;35(8):4095–123.
- Andreou A, Watson DI, Mavridis D, Francis NK, Antoniou Assessing the efficacy and safety of laparoscopic antireflux procedures for the management of gastroesophageal reflux disease: a systematic review with network meta-analysis. Surg Endosc. 2020 Feb;34(2):510–20.
- Markar S, Andreou A, Bonavina L, Florez ID, Huo B, Kontouli KM, et al. UEG and EAES rapid guideline: Update systematic review, network meta-analysis, CINeMA and GRADE assessment, and evidence-informed European recommendations on surgical management of GERD. United European Gastroenterol J. 2022 Nov;10(9):983–98.
- Schuitenmaker JM, van Hoeij FB, Schijven MP, Tack J, Conchillo JM, Hazebroek EJ, et al. Pneumatic dilation for persistent dysphagia after antireflux surgery, a multicentre single-blind randomised sham-controlled clinical Gut. 2022 Jan;71(1):10–5.
- Gkolfakis P, Lorenzo D, Blero D, Louis H, Lemmers A, Arvanitakis M, et Pneumatic dilation for the treatment of persistent post-laparoscopic fundoplication dysphagia: long-term efficacy and safety. Expert Rev Gastroenterol Hepatol. 2022 Mar;16(3):289–96.
- Bell R, Lipham J, Louie BE, Williams V, Luketich J, Hill M, et al. Magnetic Sphincter Augmentation Superior to Proton Pump Inhibitors for Regurgitation in a 1-Year Randomized Trial. Clin Gastroenterol Hepatol. 2020 Jul;18(8):1736-1743.e2.
- Ferrari D, Asti E, Lazzari V, Siboni S, Bernardi D, Bonavina L. Six to 12-year outcomes of magnetic sphincter augmentation for gastroesophageal reflux Sci Rep. 2020 Aug 13;10(1):13753.
- Weusten BLAM, Barret M, Bredenoord AJ, Familiari P, Gonzalez JM, van Hooft JE, et al. Endoscopic management of gastrointestinal motility disorders – part 2: European Society of Gastrointestinal Endoscopy (ESGE) Guideline. Endoscopy. 2020 Jul;52(7):600–14.
- Yeh JH, Lee CT, Hsu MH, Lin CW, Hsiao PJ, Chen CL, et Antireflux mucosal intervention (ARMI) procedures for refractory gastroesophageal reflux disease: a systematic review and meta-analysis. Therap Adv Gastroenterol. 2022;15:17562848221094960.
- Armstrong D, Bennett JR, Blum AL, Dent J, De Dombal FT, Galmiche JP, et al. The endoscopic assessment of esophagitis: a progress report on observer agreement. Gastroenterology. 1996 Jul;111(1):85–92.
- Hansdotter I, Björ O, Andreasson A, Agreus L, Hellström P, Forsberg A, et Hill classification is superior to the axial length of a hiatal hernia for assessment of the mechanical anti-reflux barrier at the gastroesophageal junction. Endosc Int Open. 2016 Mar;4(3):E311-317.
- Yadlapati R, Gyawali CP, Pandolfino JE, CGIT GERD Consensus Conference AGA Clinical Practice Update on the Personalized Approach to the Evaluation and Management of GERD: Expert Review. Clin Gastroenterol Hepatol. 2022 May;20(5):984-994.e1.
- Savarino E, Bredenoord AJ, Fox M, Pandolfino JE, Roman S, Gyawali CP, et Expert consensus document: Advances in the physiological assessment and diagnosis of GERD. Nat Rev Gastroenterol Hepatol. 2017 Nov;14(11):665–76.
Abréviations
RGO : reflux gastro-œsophagien
SIO : sphincter inférieur de l’œsophage
IPP : Inhibiteurs de la pompe à protons
EOGD : Endoscopie œsogastroduodénale