Liens d’intérêt
L’auteur déclare n’avoir aucun lien d’intérêt en relation avec sa communication.
Mots-clés
Hémorroïdes ; Hémorroïdectomie ; Techniques mini-invasives ; Ligatures artérielles Doppler ; Radiofréquence hémorroïdaire
Généralités sur la maladie hémorroïdaire
La maladie hémorroïdaire est la pathologie la plus fréquente de l’anus, touchant environ 10 à 40 % de la population générale (1-4). Cette atteinte est mixte, associant une pathologie hémorroïdaire externe responsable de thromboses hémorroïdaires externes, sources de douleurs anales, et une pathologie hémorroïdaire interne. Bien que physiologiques et participant à la continence anale, les hémorroïdes internes peuvent provoquer des symptômes invalidants, en particulier des saignements et un prolapsus, les symptômes les plus fréquemment rapportés, et peuvent avoir un impact majeur sur la qualité de vie ou des conséquences graves en cas d’anémie secondaire à des saignements fréquents et/ou abondants. Leur prise en charge classique repose en première intention sur le respect de règles hygiéno-diététiques (régularisation du transit, régime riche en fibres alimentaires, limitation du temps passé sur la cuvette des WC…) (5-7) et sur des traitements médicaux topiques.
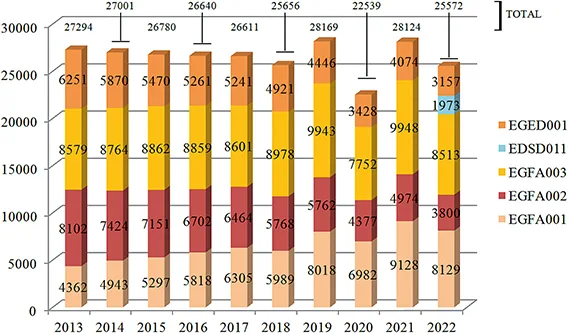
La prise en charge chirurgicale a été représentée presque exclusivement de 1937 à 1998 par l’hémorroïdectomie ouverte type Milligan-Morgan (8) ou semi-fermée type Ferguson (9), la technique de Milligan-Morgan étant la plus pratiquée en France. Cependant, avec ces interventions, la cicatrisation dure 4 à 8 semaines, la douleur postopératoire est souvent au premier plan, effraie les patients et les pousse à retarder leur prise en charge. Ces interventions les exposent par ailleurs à des complications sévères précoces (hémorragies) ou tardives (incontinence anale, sténose anale, même avec les nouveaux outils utilisés pour réséquer les hémorroïdes (10)). Elles représentaient en France, au 31/12/2022, 20442 interventions, soit encore 80 % des interventions chirurgicales effectuées sur les hémorroïdes contre 70 % en Italie (11) et seulement 31 % aux Pays-Bas (12) en 2018 (figure 1). Afin d’éviter ou de réduire ces complications et la durée d’invalidité postopératoires, des procédés instrumentaux ou des techniques dites mini- invasives ont été développées, ne s’intéressant qu’au traitement exclusif de la maladie hémorroïdaire interne.

Figure 1 : Nombre d’interventions chirurgicales à visée hémorroïdaire
effectuées en France
- EGFA001, EGFA002 et EGFA003 : hémorroïdectomies pédiculaires
- EGED001 : réduction de procidence hémorroïdaire par agrafage circulaire (Longo)
- EDSD011 : ligature des artères hémorroïdaires avec guidage doppler avec mucopexie (DGHAL)
- NB : le code CCAM «EGFA001» peut être surcoté car parfois utilisé «par assimilation» pour coter la radiofréquence hémorroïdaire depuis 2016. De même, la ligature doppler avec mucopexie a souvent été cotée HJFD005 avant l’obtention de son propre code. Si on rajoute le code HJFD005, on obtient 6 000 interventions supplémentaires intégrées dans le GHM «hémorroïdectomies»
- (source : https://www.scansante.fr/applications/statistiques-activite-MCO-par-diagnostique-et-actes ; extraction à partir de la répartition des séjours par GHM selon l’acte classant codé)
Le choix entre l’ensemble des techniques disponibles, instrumentales, mini-invasives ou chirurgicales classiques, repose sur la connaissance de leur efficacité, leurs limites et leurs éventuelles complications après une évaluation préalable nécessaire de la maladie hémorroïdaire avant d’envisager une prise en charge (13). Pour la maladie hémorroïdaire externe, on prend en compte la fréquence, l’intensité des épisodes thrombotiques et son retentissement sur la qualité de vie.
Pour la maladie hémorroïdaire interne, la très ancienne classification de Goligher (14), la plus universellement utilisée, quantifie le prolapsus en 4 grades (tableau 1). Pour les saignements, on peut recourir à des échelles verbales analogiques (15) et à la recherche d’une carence martiale ou d’une anémie. Le retentissement sur la qualité de vie doit également être considéré. La prise en compte de l’ensemble de ces données permet alors d’envisager s’il est possible et judicieux d’éviter une hémorroïdectomie standard type Milligan-Morgan.
| Grade de prolapsus | Présentation clinique |
|---|
| Grade I | Hémorroïdes internes congestives, gonflant dans l’anuscope, non prolabées |
| Grade II | Hémorroïdes internes se prolabant à la défécation ou à l’effort physique mais se réintégrant spontanément |
| Grade III | Hémorroïdes internes se prolabant à la défécation ou à l’effort physique mais nécessitant une réintégration
manuelle |
| Grade IV | Hémorroïdes internes prolabées en permanence ou se prolabant immédiatement après tentative de
réintroduction manuelle |
Traitements instrumentaux
Ces procédés thérapeutiques anciens ne sont indiqués que dans la prise en charge de la maladie hémorroïdaire interne, après échec des mesures conservatives. Ils n’ont aucun intérêt dans la prise en charge en urgence ou dans la prévention des récidives des épisodes thrombotiques externes (16).
Le principe commun de ces traitements instrumentaux, qu’ils soient mécaniques (ligatures élastiques), chimiques (injections sclérosantes) ou thermiques (photocoagulation ou coagulation infrarouge, cryothérapie) est d’induire une fibrose cicatricielle du sommet des plexus hémorroïdaires internes. Celle-ci fixe alors la muqueuse anale au plan musculaire profond et obture le réseau vasculaire sous-muqueux issu de l’artère rectale supérieure. Les ligatures élastiques ajoutent un bénéfice supplémentaire en apportant une réduction physique du prolapsus muco-hémorroïdaire interne.
Ces traitements sont le plus souvent réalisés en consultation, sans anesthésie.
Ligatures élastiques hémorroïdaires
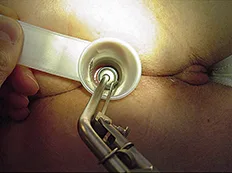
Les ligatures hémorroïdaires sont proposées depuis l’Antiquité dans le traitement de la maladie hémorroïdaire (17). Après la description originale par Olindo Grandesso Silvestri en 1833, elles ont finalement été introduites en 1958 par Blaisdell (18) avec un fil de soie puis modifiées par Baron en 1963 (19) avec l’introduction d’un élastique et demeurent la technique instrumentale la plus utilisée au monde. Elles sont utilisables en consultation ou peuvent être réalisées lors d’une endoscopie, en rétrovision (20-22). Les ligatures élastiques des paquets hémorroïdaires sont réalisées au travers d’un anuscope (figure 2) ou lors d’une coloscopie, avec un système d’aspiration qui permet de libérer un élastique autour du paquet hémorroïdaire, strictement en amont de la ligne pectinée. Cela permet de réduire le volume du prolapsus muco-hémorroïdaire tout en réalisant, comme les autres techniques instrumentales, une réaction inflammatoire locale induisant une fibrose fixant la muqueuse au plan profond. Leur réalisation par des systèmes non aspiratifs à traction est grevée de plus de douleurs et de complications (23).

Figure 2
Indications et efficacité
Les ligatures hémorroïdaires sont indiquées, après échec des mesures conservatives, dans le traitement des saignements hémorroïdaires internes et des prolapsus hémorroïdaires internes grade I à III (5,7,24-26). L’efficacité est de l’ordre de 50 à 90 % des cas à un an mais tombe à 50 % à 4 ans (27). Pour les prolapsus de grade II, leur efficacité est de 66 % à un an. Pour les grades III, les ligatures ne sont recommandées qu’en cas de prolapsus localisé, non circulaire et elles ne sont pas recommandées dans les grades IV (24) du fait d’un taux de récidive symptomatique ou d’échec primaire élevé. Des séances répétées sont le plus souvent nécessaires pour obtenir un résultat (28), idéalement après un délai de 4 semaines (29,30). Les résultats après la mise en place de 3 ligatures dans la même séance ou de 3 séances successives de ligatures uniques sont comparables.
Contre-indications
Les contre-indications habituellement retenues des ligatures élastiques hémorroïdaires, outre les impossibilités techniques de positionnement du ligateur ou les patients ne souhaitant pas de séances répétées, sont les contextes d’immunodépression sévère, les maladies de Crohn avec lésions ano-périnéales, les RCUH actives, les rectites infectieuses concomitantes, les traitements anticoagulants (31,32), les troubles de la coagulation innés ou acquis et les rectites radiques. La grossesse est une contre-indication de prudence (5) mais il ne semblerait pas exister de complications particulières, de même que dans les cas d’infections par VIH (33).
Le diabète sucré est retenu comme contre-indication par le consensus italien (25) mais pas par les recommandations françaises (5), européennes (24) ou américaines (34).
Si plusieurs équipes ont publié des résultats chez des patients ayant des traitements anticoagulants, des cirrhoses ou des troubles innés de la coagulation (33,35), le taux de saignements après ligatures doit faire discuter leur réalisation de façon très prudente. Une étude rétrospective sur 805 patients ayant eu 2 114 ligatures montre un taux de saignement après procédure de 25 % sous AVK (35) contre 7,5 % sous aspirine ou AINS et 2,5 % sans aucun traitement. De même, des accidents graves ont été soulignés en cas d’hémophilie peu sévère (36). Enfin, même si les accidents hémorragiques ne diffèrent pas chez les patients cirrhotiques (sur de petites séries : 18 cas (37), 60 cas (38)), la survenue d’une complication peut avoir des conséquences lourdes par décompensation de l’hépatopathie sous-jacente.
La prise d’aspirine n’est pas une contre-indication et ne nécessite pas son interruption. Il n’y a en revanche pas de consensus pour le clopidogrel (39,40). Cependant, celui-ci représentant 50 % des épisodes hémorragiques post-ligatures chez les patients sous antiagrégants plaquettaires (41), il semble préférable de le remplacer par de l’aspirine avant le geste et pendant 14 jours après celui-ci, jusqu’à la fin habituelle du délai de survenue de la chute d’escarre.
Enfin, les données sont faibles dans la littérature concernant l’innocuité des ligatures élastiques en cas d’antécédents d’irradiation et insuffisantes pour prendre position. Trois équipes ont utilisé les ligatures élastiques pour le traitement des saignements de rectite radique, sans complication apparente (42-44). D’autres ont en revanche observé des complications importantes ou graves (45,46). La taille des effectifs ne permet cependant pas de trancher et un antécédent d’irradiation doit inciter à la plus grande prudence dans l’utilisation de cette technique ou la contre-indiquer (24).
Effets secondaires et complications
Les ligatures élastiques peuvent avoir des effets secondaires mineurs, plus fréquents qu’avec les scléroses hémorroïdaires : malaises vagaux pouvant se produire dans les heures suivant la ligature (jusqu’à 30 % des cas dans une étude prospective (47)), douleurs dans les heures suivant la pose des élastiques, ténesmes, saignements. La douleur immédiate est le témoin d’une pose de l’élastique trop bas située sur la ligne pectinée et peut imposer son retrait immédiat. Pour cela, certains positionnent systématiquement un fil permettant le retrait en cas de complication. La douleur est plus marquée avec les aspirateurs à griffes (23). Elle est également plus fréquente et intense dans le cas des ligatures multiples (48,49).
Dans 1 à 5 % des cas, des complications peuvent survenir : thromboses hémorroïdaires internes ou externes, dysurie, priapisme, abcès périanaux. De rares cas d’hémorragies par chute d’escarre, jusqu’au 15e jour après la pose, peuvent se produire et, exceptionnellement, nécessiter une hémostase chirurgicale ou endoscopique (50).
De nombreuses complications exceptionnelles ont été décrites : tétanos avec les aspirateurs à griffes (51), abcès hépatiques (52,53), endocardite (54), abcès pelviens (55), gangrène périnéale de Fournier (56) potentiellement mortelle (57). Cette dernière complication survient habituellement 3 à 10 jours après l’acte technique et doit être soupçonnée devant l’association «douleur + fièvre + rétention urinaire + œdème» (58).
Enfin, il n’existe pas de consensus dans la littérature sur l’utilisation d’une antibiothérapie pré- et/ou postopératoire pour limiter les complications infectieuses. Les recommandations françaises plaident, en «avis d’expert», pour une antibiothérapie systématique en cas de diabète ou d’immunodépression (5), sans schéma définitivement validé. La Société Nationale Française de Colo-Proctologie (SNFCP) recommande cependant la prise de 500 mg de métronidazole per os 2 h 00 avant le geste puis 500 mg matin et soir pendant 3 jours (59).
Scléroses hémorroïdaires
Les scléroses hémorroïdaires sont indiquées, après échec des mesures conservatives, dans le traitement des saignements hémorroïdaires internes et des prolapsus hémorroïdaires internes grade I et II (5).
Il s’agit du premier traitement instrumental proposé dont les inventeurs restent discutés : John Morgan en 1869 à Dublin, Antoine Desgranges à Lyon ?… Elles sont réellement introduites en France en 1920 par Raoul Bensaude.
Le seul produit ayant eu l’AMM en France était le Kinurea-H®, mélange quinine-urée dichlorate. Mais, en 2016, du fait d’un désaccord entre le laboratoire fabricant et le Comité Économique des Produits de Santé, le produit n’a plus été remboursé et le fabricant a décidé de ne plus le produire. Après écoulement des stocks, la commercialisation a été définitivement interrompue en septembre 2020. Cette technique n’est donc plus accessible en 2023 en France.
Reviendra-t-elle cependant sous la forme d’une «nouvelle sclérothérapie» avec l’utilisation d’autres produits sclérosants (60) ? De multiples produits sont utilisés de par le monde (huile phréniquée 5 %, sérum salé hypertonique 23,4 %, sulfate de tétradecyl sodé, sulfate de potassium d’aluminium +/- acide tannique, dextrose 50 %…) mais ces produits ne sont pas disponibles en France. Il faudrait pour cela autoriser l’emploi du polidocanol
600, déjà disponible en France en forme liquide (Ætoxysclérol®) ou en forme de mousse qui est utilisée dans plusieurs pays, notamment européens et semble combiner efficacité et sécurité (61,62), mais dans des études pas toujours contrôlées ou de faible effectif. Enfin, certaines équipes ont associé les injections sclérosantes de polidocanol 3 % avec les ligatures élastiques («sclerobanding») (63).
Indications et efficacité
Les injections sclérosantes sont préférentiellement utilisées pour les prolapsus hémorroïdaires grade I et II (31).
Contre-indications
Les contre-indications sont identiques à celles des ligatures élastiques avec une mention particulière pour la grossesse, l’insuffisance hépato- cellulaire et l’insuffisance rénale (64).
Effets secondaires et complications
Les complications, outre des douleurs post-procédure, de la fièvre ou des ténesmes, peuvent être sérieuses : ulcères rectaux, sténoses rectales, fistules recto-vaginales (65), fasciites nécrosantes, abcès hépatiques, endocardites…
Photocoagulation infrarouge
Par une technique décrite par A. Neiger (66), un photocoagulateur à rayons infrarouges transforme en chaleur au point d’application le rayonnement émis par une ampoule de tungstène focalisé sur une tige en quartz (figure 3). Généralement, deux à trois points de photocoagulation sont appliqués à la base de chacun des paquets hémorroïdaires.

Figure 3
Indications et efficacité
Elle n’est indiquée, après échec des mesures conservatives, que dans les saignements secondaires à une maladie hémorroïdaire interne grade I, voire II (67).
Dans des études anciennes, son efficacité immédiate est estimée entre 70 et 90 % mais tombe à un an à 40 %. Cependant, une méta-analyse récente indique des taux identiques d’efficacité, de rétention urinaire ou de saignements post-procéduraux qu’avec les ligatures élastiques, les douleurs post- opératoires étant moindres avec la photocoagulation infrarouge (68).
Contre-indications
Elle est contre-indiquée en cas de troubles de la coagulation, innés ou acquis, chez la femme enceinte ou en cas de MICI active.
Effets secondaires et complications
Hormis de rares saignements abondants par chute d’escarre autour du 10e jour après le traitement, seuls des effets mineurs ont été rapportés : gêne anale transitoire (20-35 % des cas), douleurs modérées ne dépassant pas 48 heures (4-8 % des cas), saignements minimes ou suintements séro- hémorragiques pendant une dizaine de jours (5-25 % des cas) (69).
Cryothérapie
La cryothérapie génère une nécrose du tissu muco-hémorroïdaire interne par l’application de froid par l’application d’une cryode au sommet des paquets hémorroïdaires pendant 2 à 3 mn («cryo-sclérose»). L’application plus longue («cryo-chirurgie») a pour but d’entrainer une nécrose plus profonde. Elle peut être associée à une ligature élastique pour accélérer le processus de nécrose («cryo-ligature»).
Indications et efficacité
Cette technique mal évaluée est considérée comme n’apportant aucun avantage par rapport aux autres techniques instrumentales précédentes, est de moins en moins utilisée et n’est plus citée dans les recommandations de la prise en charge de la maladie hémorroïdaire française, italienne, européenne et américaine.
Contre-indications
Ses contre-indications reprennent par assimilation, sans étude précise, celles des ligatures élastiques.
Effets secondaires et complications
On décrit des douleurs dans les suites immédiates (30 %), des saignements parfois importants (5 %) et des suintements anaux quasi constants avec la cryo-chirurgie (67).
Évaluation comparative des différents procédés instrumentaux entre eux
Il est classiquement décrit une efficacité supérieure des ligatures élastiques (LE) par rapport à la photocoagulation infrarouge (PIR) sur le prolapsus à un an mais avec un taux plus élevé de douleurs (69,70). Une méta-analyse plus récente (68) retrouve les mêmes résultats qu’une ancienne étude prospective (71) avec une efficacité comparable, toujours avec plus de douleurs pour la LE. En cas de saignements prédominant, sans prolapsus, la PIR semble plus efficace que la LE (69).
La LE est également plus efficace sur le prolapsus que les injections sclérosantes mais, là aussi, avec plus de douleurs (31,70,72).
Évaluation comparative des différents procédés instrumentaux et des procédures chirurgicales
Comparativement avec l’hémorroïdectomie standard, les LE sont aussi efficaces pour les grades II mais au prix de séances répétées et sont moins efficaces pour les grades III, notamment circulaires. De façon non surprenante, les LE entraînent une durée inférieure d’arrêt de travail, moins de douleur postopératoire et moins de complications à distance mais avec une satisfaction équivalente des patients (73,74).
Par rapport à l’hémorroïdopexie, les LE sont moins efficaces pour les grades II circulaires mais au prix de suites plus compliquées avec l’hémorroïdopexie (75).
En comparaison avec la ligature artérielle sous contrôle doppler +/- mucopexie, les LE répétées et le HAL n’ont pas de différence en termes de récidive sur les grades II-III. Les LE sont moins douloureuses (27).
Une étude sur 46 patients a comparé la sclérothérapie à la mousse de polidocanol 3 % dans le traitement des prolapsus grade II-III versus le HAL-RAR et trouve une supériorité de la sclérothérapie en termes d’efficacité (91,7 % vs. 68,2 %, p= 0,045) et de moindres complications (76).
Par rapport aux techniques laser (LHP® et HeLP®), les LE semblent plus douloureuses (77) et moins efficaces (78).
Traitements mini-invasifs
Les techniques mini-invasives de prise en charge de la maladie hémorroïdaire ont été développées dans le but de diminuer la douleur et les complications post-opératoires de la chirurgie classique. Elles sont caractérisées par l’absence de plaie opératoire cutanée.
Actuellement, 6 techniques sont décrites : l’hémorroïdopexie selon Longo, la ligature artérielle +/- mucopexie, l’hémorroïdoplastie laser (LHP®), la procédure de traitement des hémorroïdes au laser (HeLP®), la thermocoagulation hémorroïdaire par radiofréquence (Rafaelo®) et l’embolisation radiologique des artères hémorroïdaires (Emborrhoid).
Ces différentes techniques ne sont indiquées que dans la prise en charge de la maladie hémorroïdaire interne. Elles n’ont pas de place dans le traitement des thromboses hémorroïdaires externes.
Hormis l’embolisation radiologique, l’ensemble de ces techniques est réalisé sous anesthésie générale ou rachi-anesthésie.
Hémorroïdopexie circulaire par agrafage (longo)
Le principe de l’hémorroïdopexie circulaire par agrafage ou anopexie, décrite initialement par Antonio Longo en 1998 (79), est la résection d’une collerette de muqueuse rectale par une pince mécanique utilisée par voie transanale réalisant la résection de l’excès de tissu (figure 4) et la suture muco-muqueuse dans le même temps par agrafage circulaire. La résection doit impérativement être réalisée au-dessus de la ligne pectinée, idéalement 4 cm au-dessus de celle-ci. Cela provoque un effet de «lifting anal» avec suspension et dévascularisation des paquets hémorroïdaires internes.

Figure 4
Indications et efficacité
L’hémorroïdopexie par agrafage est indiquée dans le traitement des prolapsus hémorroïdaires internes grade II et III (24).
Elle a comme avantages, par rapport à une chirurgie hémorroïdaire classique, une moindre douleur postopératoire et une diminution franche de la durée de l’arrêt de travail postopératoire (25,80,81).
Son efficacité va de 83 à 93 %.
Cependant, le taux de récidive est 3 à 5 fois supérieur à celui d’une hémorroïdectomie standard (82,83) bien qu’il soit complexe à établir du fait de l’intégration dans de nombreuses études de prolapsus de grade IV. Si l’on ne retient que les études portant sur des prolapsus de grade III, la récidive à 10 ans est estimée pour certains jusqu’à 40 % (84,85).
Alors que l’hémorroïdopexie apporte une meilleure qualité de vie dans les premières semaines après intervention, son effet diminue avec le temps et ses scores de qualité de vie semblent inférieurs à 2 ans par rapport à ceux de l’hémorroïdectomie pédiculaire (80,86).
Contre-indications
Les contre-indications habituellement retenues pour cette procédure sont la sténose anale, la rectite radique et les suppurations anales (87). Le prolapsus hémorroïdaire extériorisé grade IV n’est qu’une contre-indication relative du fait d’une moins bonne efficacité (même si la description des «grades IV» est très hétérogène). De même, la réalisation d’une hémorroïdopexie n’est pas recommandée en première intention en cas de pratique de relations sexuelles anales du fait des risques potentiels de blessures ou de transmissions d’infections sexuellement transmissibles liés aux agrafes.
Effets secondaires et complications
On observe des complications à distance dont la fréquence n’est pas supérieure à celles de l’hémorroïdectomie : ténesmes, douleurs chroniques, dyschésie, incontinence de novo (86)… En comparaison avec les autres techniques mini-invasives, elle est grevée de plus de rétentions urinaires précoces et d’incontinence fécale tardive (82).
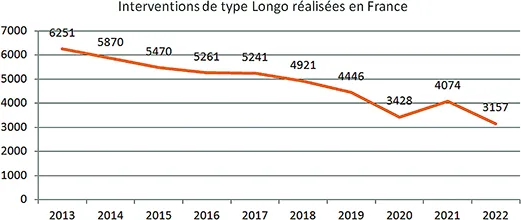
En revanche, même si les taux de complications sont identiques à ceux de l’hémorroïdectomie standard, celles-ci peuvent être particulièrement graves, voire exceptionnellement mortelles. On décrit ainsi des hématomes pré-sacrés, des perforations rectales (88,89), des nécroses rectales, des sténoses rectales, des fistules recto-vaginales, des cellulites pelviennes, des péritonites, des rétropneumopéritoines avec pneumomédiastins, des décès (90)… Si cette technique comprend une courbe d’apprentissage pouvant expliquer des complications par «erreurs de jeunesse», une revue de 1 107 interventions de 12 centres italiens a montré que 65 % des complications survenaient chez des chirurgiens «expérimentés» (91). L’hémorroïdopexie avait rendu de bons services lorsqu’elle était la seule alternative à l’hémorroïdectomie pédiculaire mais ses risques particuliers et le développement d’autres techniques réellement mini-invasives, moins douloureuses et grevées de moins de complications, expliquent son abandon progressif (11), abandon clairement demandé depuis plusieurs années (92). Les données du PMSI montrent une diminution de son utilisation en France de plus de 50 % depuis 2013 (figure 5), la faisant passer à 12,3 % des interventions hémorroïdaires effectuées en 2022 contre 23 % en 2013. L’évolution est la même à l’étranger, y compris dans sa patrie d’origine, puisqu’en Italie sa part est passée de 35 % en 2007 à 5 % en 2018 (11). La fiche d’information de la SNFCP souligne les dangers propres de cette technique qui, s’ils sont clairement expliqués aux patients, devraient peut-être les faire réfléchir à deux fois avant d’y recourir…

Figure 5 : Évolution du nombre des interventions de type Longo réalisées
en France entre 2013 et 2022
(source : https://www.scansante.fr/applications/statistiques-activite-MCO-par-diagnostique-et-actes)
Ligature artérielle guidée par doppler +/- mucopexie
Initialement proposée par Morinaga en 1995 (93), cette technique n’a vraiment pris son essor qu’au milieu des années 2000 avec la mise à disposition d’anuscopes fenêtrés intégrant une sonde Doppler pour le repérage artériel hémorroïdaire. La ligature artérielle seule (Hemorroidal Artery Ligature ou HAL), grâce à une aiguille manœuvrée au travers de la fenêtre de l’anuscope (figure 6), a pour but de «désartérialiser» les plexus hémorroïdaires tout en maintenant le retour veineux. Devant des résultats moyens, la technique a évolué en 2007 (94) avec le rajout quasi systématique d’une mucopexie fixant au plan profond le paquet hémorroïdaire prolabé. On dispose en France des appareils HAL-RAR® (HAL-Rectal Anal Repair) d’AMI, Anuphone® de Legrand et THD® (Transanal Hemorroidal Desarterialization) de THD SpA.

Figure 6
Indications et efficacité
La ligature artérielle guidée par Doppler +/- mucopexie est indiquée dans le traitement des prolapsus hémorroïdaires internes grade II-III.
L’efficacité de la ligature sous Doppler seule est de 73 % à 5 ans. Si on l’associe à une mucopexie, l’efficacité globale à 38 mois est de 88 % ou de 76 % à 7 ans. Le taux de récidive semble situé entre 8 et 20 % (25,95-97) et jusqu’à 36,5 % à 5 ans (98).
Des études ont porté sur le traitement des prolapsus de grade IV, systématiquement avec mucopexie. Le taux de récidive serait de 3 à 9 % à 3 ans (99,100).
L’intérêt du repérage par sonde Doppler pour réaliser les ligatures artérielles reste discuté (101-105). En théorie, la ligature de 6 artères (à 1, 3, 5, 7, 9 et 11 heures en position opératoire de la taille) peut être effectuée sans repérage Doppler avec des résultats identiques sans nécessité de recourir à un matériel coûteux. Néanmoins, un tiers des patients aurait des pédicules artériels supplémentaires non pris en charge dans ce cas par les ligatures faites sans repérage Doppler ce qui en rendrait l’utilisation nécessaire (106-108).
Cependant, les niveaux de preuve des études réalisées ne permettent pas d’établir de recommandations formelles. Selon les recommandations européennes, seule la mucopexie serait indiquée, l’intérêt du Doppler restant discuté (24).
Contre-indications
Il s’agit des contre-indications classiques de toute chirurgie hémorroïdaire : les maladies de Crohn avec lésions ano-périnéales, les RCUH actives (109), les rectites infectieuses concomitantes, les rectites radiques…
Effets secondaires et complications
La ligature artérielle sous contrôle Doppler, éventuellement associée à une mucopexie, a une morbidité faible avec des complications immédiates souvent mineures (saignements [0-8 %], douleurs [18,5 %], ténesmes [10 à 24 %] et thromboses [3 à 8,6 %]) (96,107). D’autres complications immédiates ont été décrites (dyschésie [1,8 %], rétentions urinaires [5,5 %], fistules [0,5 %] et hématomes sous-muqueux [3,7 %]) (67).
À ce jour, aucune complication grave menaçant le pronostic vital n’a été rapportée.
Hémorroïdoplastie laser (LHP®)
L’hémorroïdoplastie laser (LHP®), initialement décrite en 2007, a pour but, par l’application sous-muqueuse de laser, de diminuer le flux sanguin hémorroïdaire en coagulant les branches terminales des artères hémorroïdaires supérieures. Elle nécessite cependant une minime incision cutanée à la base des paquets hémorroïdaires pour insérer la sonde laser après création d’un tunnel sous-muqueux le long du canal anal jusqu’au bas rectum (110) (figure 7).

Figure 7
Elle n’a fait l’objet que d’un nombre restreint d’études rendant difficile son évaluation correcte.
Indications et efficacité
La LHP® est proposée dans le traitement des prolapsus hémorroïdaires internes grade II-III et les recommandations européennes (24) et italiennes (25) considèrent qu’elle peut être «envisagée» avec un «faible niveau de preuves».
La récidive est de 12,5 % à un an selon Poskus (111). L’efficacité à 5 ans serait, sans différence significative entre les grades, de 61 % pour les grades II et 67 % pour les grades III (112).
Une étude française a relevé une efficacité à 1 an de 29 % seulement (113) contre 75 % dans une étude australienne (114). Cependant, ces études ne comprennent que de petits effectifs rendant difficile une extrapolation.
Enfin, une étude prospective ne la recommande pas en cas de prolapsus circulaire (115). Une autre ne trouve pas de gain d’efficacité avec l’utilisation concomitante d’un guidage Doppler (116).
Contre-indications
Il n’existe aucune donnée publiée sur ce point. Il semble raisonnable de reprendre les contre-indications habituelles dans l’attente d’études éventuelles, à savoir la grossesse, les maladies de Crohn avec lésions ano-périnéales, les RCUH actives (109), les rectites infectieuses concomitantes, les rectites radiques, les troubles de coagulation…
Effets secondaires et complications
Cette technique semble peu douloureuse (117-119) et statiquement inférieure à celle des autres prises en charge chirurgicales comparées (120). La reprise d’activité est très rapide (121).
Deux revues systématiques de la littérature (77,122) n’ont pas retrouvé de complications graves, mais Faes (112) a observé des abcès et fistules dans 6 % des cas et l’équipe de l’Hôpital St-Joseph (Paris) a décrit des complications sérieuses dans 18 % des cas (abcès et fistules intersphinctériennes ou transsphinctériennes hautes) (113) conduisant cette équipe à reconsidérer l’intérêt de la technique et à ne pas la recommander en routine (effet centre ?).
Procédure laser (HeLP®)
La technique HeLP® (Hemorrhoidal Laser Procedure), décrite depuis 2009 (123), induit une désartérialisation du tissu hémorroïdaire par coagulation laser des artères hémorroïdaires internes repérées par guidage Doppler à l’aide d’une diode de 980-nm (124,125). Cette intervention ne comporte pas d’incision cutanée, contrairement à la LHP®, le traitement étant réalisé par application transmuqueuse au-dessus de la ligne pectinée.
Elle peut être associée à une mucopexie (HeLPexx) (126).
Comme la LHP®, elle n’a fait l’objet que d’un nombre restreint d’études rendant difficile son évaluation correcte.
Indications et efficacité
La technique HeLP® est proposée dans le traitement des prolapsus hémorroïdaires internes grade II-III (120), surtout avec saignements, et les recommandations européennes (24) et italiennes (25) considèrent qu’elle peut être «envisagée» avec un «faible niveau de preuves».
L’efficacité est estimée entre 60 et 90 % (127-130) à un an. La récidive ne peut pas être évaluée avec les données disponibles.
Contre-indications
Il n’existe aucune donnée publiée sur ce point. Il semble raisonnable de reprendre les contre-indications habituelles dans l’attente d’études éventuelles, à savoir la grossesse, les maladies de Crohn avec lésions ano-périnéales, les RCUH actives (109), les rectites infectieuses concomitantes, les rectites radiques, les troubles de coagulation…
Effets secondaires et complications
Les complications peropératoires sont dominées par les saignements dans 8 % des cas (120).
Deux publications ont relevé la survenue d’une occlusion intestinale postopératoire après HeLP® par hématome pariétal rectal ayant nécessité une colostomie de décharge (131,132).
Thermocoagulation hémorroïdaire par radiofréquence
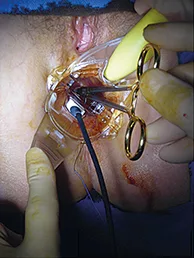
L’utilisation de la thermocoagulation par radiofréquence pour traiter la maladie hémorroïdaire interne a été décrite pour la première fois en 2002 mais en appliquant une électrode bille à la surface des paquets hémorroïdaires (133). En 2008, la technique fut modifiée par l’utilisation d’une électrode transfixiante (134). Elle est utilisée en France depuis 2016 sous l’appellation «procédure Rafaelo®» et a été étudiée pour la première fois en 2018 (135). Peu d’études ont été publiées à ce jour (tableau 2).
| Référence | Date de publication | Type d’étude | Nombre de patients traités initialement | Nombre de patients en fin d’étude | Suivi Moyen (mois) | Suivi Maxi (mois) | Grade (Goligher) | Récidive (%) |
Duben (134) | 11/2008 | PROSP | 18 | 5 | ? | 12 | III-IV | ? |
Duben (136) | 03/2013 | PROSP | 71 | 25 | < 18 | 18 | III-IV | ? |
Schäfer (137) | 06/2018 | PROSP | 102 | 70 | 6 | 6 | III | ? |
Shikhmetov (138) | 2018 | PROSP | 23 (RFA +HAL- RAR) | 23 | ? | 12 | III-IV | 0 % à 12 mois |
| Duben (139) | 07/2018 | PROSP | 217 | ? | ? | 120 | III-IV | 4 % à 14 mois |
Eddama (140) | 08/2019 | PROSP | 27 | 27 | 20 | 32 | II-IV | 4 % à 20 mois |
| Didelot (135) | 03/2021 | RETROSP | 42 | 39 | 15 | 30 | II-IV | ? |
Drissi (141) | 10/2021 | PROSP | 74 | 74 | 3 | 3 | II-IV | 7 % à 3 mois |
| Hassan (142) | 08/2021 | PROSP | 42 | 42 | ? | 12 | I-III | 12 % à 12 mois |
Gandhi (143) | 06/2022 | RETROSP | 47 | 45 | ? | ? | II-IV | 7 % à 2 mois |
Tolksdorf (144) | 06/2022 | PROSP | 98 | 73 | ? | 24 | III | 17,8 % à 24 mois |
| Didelot (145) | 10/2022 | RETROSP | 124 | 107 | 30 | 62 | II-IV | 21 % à 30 mois |
Tableau 2 : Liste des études publiées sur la radiofréquence hémorroïdaire (avec utilisation d’une sonde de radiofréquence transfixiante) au 31/12/2022
Le principe est l’obtention d’une fibrose du tissu hémorroïdaire par l’introduction d’une sonde électrode (sonde HPR45i® [F-Care-Systems, Anvers, Belgique]) au sommet des paquets hémorroïdaires, au-dessus de la ligne pectinée, selon un angle de 30°, délivrant des ondes de radiofréquence basse température à 4 MHz. La fibrose se développe progressivement et le résultat final est constaté après 4 à 8 semaines.
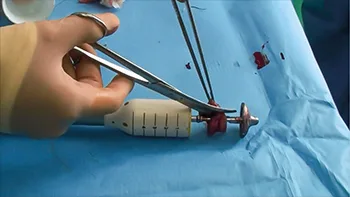
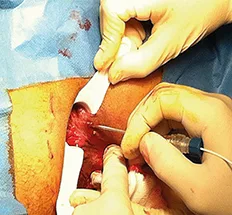
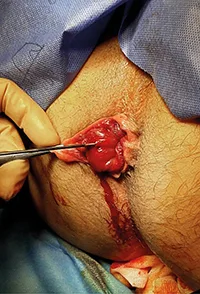
L’intervention est majoritairement réalisée au travers d’un anuscope fenêtré mais peut également être effectuée, plus simplement, par traction des paquets hémorroïdaires à l’extérieur du canal anal (135) (figure 8).

Figure 8
Indications et efficacité
La radiofréquence hémorroïdaire est proposée dans le traitement des prolapsus et des saignements des hémorroïdes grade II à IV.
Il s’agit d’une procédure ambulatoire n’entrainant qu’un arrêt de travail moyen limité, de l’ordre de 2 (140) à 3 (145) jours.
L’efficacité immédiate sur le prolapsus ou les saignements varie de 87 à 96 % (136,144,141). Dans notre étude, l’efficacité est supérieure sur les saignements avec 52 % d’absence de saignements à 30 mois. Pour les patients restant, les saignements diminuent significativement d’une intensité de 7/10 (Échelle Verbale Analogique) à 3/10. La disparition complète du prolapsus n’est retrouvée que dans 30 % des cas à 30 mois (8-62 mois) mais, chez les 70 % restants, on constate une régression d’un grade III à un grade II. L’ensemble de ces résultats confère une amélioration significative de la qualité de vie évaluée par le score HEMO-FISS (146) et un taux de satisfaction de +4/5 à 30 mois (145).
La récidive est estimée entre 0 et 12 % à un an et à 21 % à 30 mois (145).
Contre-indications
Outre la maladie hémorroïdaire externe, cette intervention reprend les contre-indications classiques des interventions hémorroïdaires : les MICI actives, les rectites infectieuses concomitantes, les traitements anticoagulants, les troubles de la coagulation innés ou acquis et les rectites radiques. Ces contre-indications ne sont que des avis d’experts et n’ont pas été étudiées.
Effets secondaires et complications
Les suites opératoires sont habituellement peu douloureuses, 60 (144) à 66 % (145) des patients ne prenant aucun antalgique après l’intervention.
Les complications observées en réalisant l’intervention par traction des pédicules hémorroïdaires à l’extérieur du canal anal sont représentées exclusivement par des thromboses hémorroïdaires externes précoces (8,4 %). Aucune complication à distance n’a été observée jusqu’à 62 mois après l’intervention (145).
Les études ayant étudié la technique réalisée au travers d’un anuscope ont décrit la survenue d’abcès anaux, parfois avec fistules intersphinctériennes (141,147).
Embolisation des artères hémorroïdaires
Alors que le principe en a été étudié depuis de nombreuses années (148,149), l’embolisation des artères hémorroïdaires (Emborrhoid) est une technique mini-invasive véritablement proposée en 2014 par une équipe marseillaise (150,151). Elle consiste à emboliser de façon supersélective les artères hémorroïdaires en cathétérisant, par l’artère radiale ou l’artère fémorale, l’artère mésentérique inférieure puis les artères rectales supérieures. Différents agents, coils, gels ou particules, sont utilisés (152-154).
Indications et efficacité
La technique Emborrhoid est proposée dans le traitement des saignements des prolapsus hémorroïdaires de grade I à III en cas de contre-indications opératoires (patients cirrhotiques, troubles de coagulation, insuffisants cardiaques ou pulmonaires, MICI, rectite radique…) (155) mais certains la proposent en première intention. Sa faisabilité semble élevée avec un taux de réussite technique de 99 % (156).
On note une efficacité avec interruption des besoins transfusionnels chez 18 patients sur 21 au terme d’un suivi moyen de 18,5 mois (155). Les pourcentages d’efficacité varient de 63 à 97 %. Une revue de la littérature conclue à un taux d’efficacité de 82 % (156). Mais, du fait de l’absence d’essais de bonne qualité avec des effectifs suffisants et avec des techniques standardisées, il n’est pas possible de conclure quant à son efficacité et son intérêt dans la prise en charge hémorroïdaire (157). De même, le taux de récidive n’a été évalué que dans une étude et estimé à 14 % à un an (155).
Contre-indications
Il n’existe aucune donnée consensuelle proctologique publiée sur ce point en dehors des prolapsus hémorroïdaires de grade IV (153). On retient par ailleurs les contre-indications classiques des injections de produits de contraste iodé (insuffisance rénale sévère et allergie à l’iode injectable (158)).
Effets secondaires et complications
Des douleurs passagères peuvent être observées, de façon cependant inconstante.
Une seule publication a fait état d’une ischémie recto-sigmoïdienne avec sténose rectale séquellaire et persistance des saignements (159).
Évaluation comparative des différents procédés mini-invasifs
Comparaison avec l’hémorroïdectomie classique
Toutes les méthodes mini-invasives sont, de façon attendue, moins douloureuses que l’hémorroïdectomie, ont moins de risque hémorragique postopératoire et permettent un retour à l’activité plus rapide.
L’hémorroïdopexie et les ligatures sous contrôle Doppler +/- mucopexie ont une efficacité immédiate quasiment comparable à l’hémorroïdectomie mais le taux de récidive à long terme est nettement plus important (jusqu’à 40 % à 10 ans avec le Longo ou 25 % à 3 ans pour les ligatures Doppler). Les complications de l’hémorroïdopexie, quoique comparables en nombre, peuvent être beaucoup plus graves qu’avec l’hémorroïdectomie classique. Il n’est pas possible de conclure sur la différence en termes de récidive après LHP® et HeLP® ou hémorroïdectomie classique, les études étant discordantes.
Il n’y a aucune étude comparative entre la radiofréquence type Rafaelo® ou la technique Emborrhoid et l’hémorroïdectomie classique.
Comparaison entre techniques mini-invasives
La ligature sous contrôle Doppler avec mucopexie est aussi efficace que l’hémorroïdopexie par agrafage, sans en comprendre les risques graves (160-162), argument supplémentaire pour ne réserver le Longo qu’à des cas très particuliers et la remplacer dans la pratique courante par la ligature Doppler (ou la radiofréquence hémorroïdaire mais sans certitude pour cette dernière du fait de l’absence de données suffisantes disponibles). Il n’existe pas de données concernant la comparaison entre les autres techniques mini-invasives entre elles.
Comparaison de l’efficacité et des taux de récidive des différents procédés mini-invasifs
Le tableau 3 compare l’efficacité moyenne des différentes techniques, leurs taux de récidive au-delà d’un an et les taux de réintervention observés pour chaque technique.
| Efficacité | Récidive > 1 an | Taux de réintervention |
| Hémorroïdectomie standard | > 95 % | 0-4 % | < 4 % |
| Hémorroïdopexie | 83-93 % | 1-47 % | 7-15 % |
| Ligatures artérielles Doppler +/- mucopexie | 78-97 % | 3-36 % | 7-11 % |
| Hémorroïdoplastie laser (LHP®) | 60-97 % | 0-36 % | 0-55 % |
| Procédure laser (HeLP®) | 60-90 % | 5-9 % | 8 % |
| Radiofréquence Rafaelo® | 87-96 % | 21 % | 6 % |
| Emborrhoid | 82 % | 5-9 % | — |
L’heure du choix : peut-on éviter le Milligan-Morgan ?
Les modifications anatomiques consécutives à l’hémorroïdectomie classique, ses risques postopératoires d’incontinence ou de sténose et ses suites particulièrement douloureuses et redoutées par les patients ont incité à l’utilisation première de traitements instrumentaux, facilement réalisables en consultation, et au développement de plusieurs techniques chirurgicales ou radiologiques mini-invasives. Il est donc possible d’éviter le Milligan- Morgan grâce à l’ensemble de ces procédés.
Mais, le doit-on ? Oui, lorsqu’il n’est pas nécessaire. Il faut garder à l’esprit que le premier temps de la prise en charge de la maladie hémorroïdaire repose sur le respect de règles classiques d’hygiène défécatoire.
Oui, lorsqu’il est dangereux pour le patient. Ainsi, en plus des contre-indications classiques de toute chirurgie anale (MICI active, antécédent de radiothérapie ano-périnéale…), s’il existe un risque d’incontinence ou de sa survenue, par exemple lors de patients ayant un anus lésé (antécédents de chirurgie anale, complications obstétricales…), la réalisation d’une hémorroïdectomie complémentaire faisant baisser le tonus de base du canal anal est potentiellement dangereuse et à éviter. Avant toute indication de Milligan-Morgan, une évaluation au moins clinique de la tonicité sphinctérienne s’impose. De la même façon, le risque de rétrécissement du canal anal ou de troubles de la sensibilité anale après chirurgie classique peut constituer un handicap majeur pour des patients souhaitant conserver une sexualité anale.
Oui, si l’on peut faire plus simple. Comme l’a dit Aristote, «de deux maux, choisir le moindre». Mais les alternatives à l’hémorroïdectomie pédiculaire classique ne sont pas adaptées à toutes les situations ou sont contre-indiquées. Ainsi, ces techniques ne peuvent pas remplacer l’hémorroïdectomie standard en cas de maladie thrombotique hémorroïdaire prédominante, en cas de marisques développées invalidantes, en cas de fissure anale ou de fistule anale associées ou en présence d’un volumineux prolapsus hémorroïdaire grade IV. De même, il est classiquement contre-indiqué de proposer une hémorroïdopexie pour les patients ayant des rapports anaux du fait du risque de blessure du pénis ou de perforation des préservatifs par les agrafes résiduelles. Enfin, pour des patients fragiles, sous anticoagulants, il peut être préférable de proposer une hémorroïdectomie standard pour ne prendre un risque (post)opératoire qu’une seule fois tout en minimisant le risque de récidive.
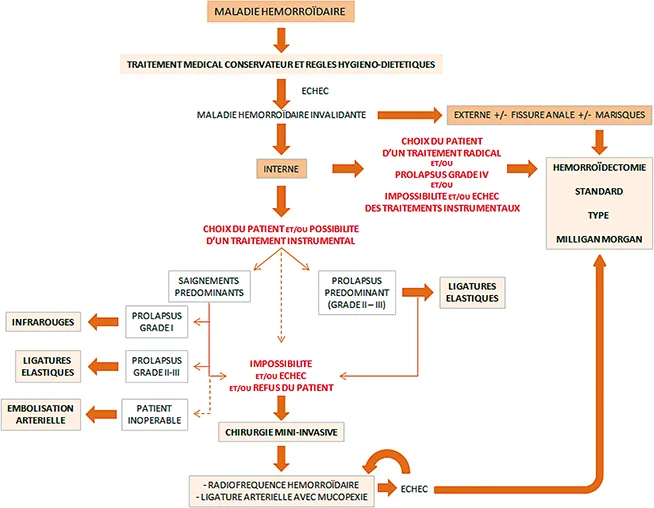
Oui, si le patient le souhaite et qu’il ne se trouve pas dans les situations précédentes. En effet, la prise en charge médicale change peu à peu de paradigme, le patient devenant un acteur de sa propre prise en charge et renvoyant le praticien à la doctrine hippocratique, «primum non nocere». Il peut choisir, pour ses propres raisons, une chirurgie radicale. Il doit en tout cas être parfaitement renseigné sur les différentes possibilités thérapeutiques et en partager le choix. S’il a opté pour une prise en charge instrumentale ou mini-invasive, les résultats seront parfois moins bons aux yeux du clinicien mais ils pourront être considérés comme très satisfaisants pour le patient en termes de qualité de vie. La recherche de la «correction à tout prix» n’est plus l’objectif principal pour une pathologie le plus souvent bénigne et de confort. Mais que choisir ? Si le choix dépend des habitudes du praticien, du matériel dont il dispose et des souhaits du patient, on peut élaborer une prise en charge graduée sachant que le recours au Milligan-Morgan reste toujours possible en cas d’échec. On peut ainsi proposer un algorithme décisionnel synthétisant les propositions thérapeutiques (figure 9).

Figure 9 :Algorithme décisionnel dans la prise en charge de la malalie hémorroïdaire interne
Non car, même si le Milligan-Morgan tendra vraisemblablement à reculer en France grâce à l’avènement des techniques mini-invasives de traitement de la maladie hémorroïdaire, il n’est cependant pas toujours possible de se passer du Milligan-Morgan. Il importe de garder à l’esprit que l’hémorroïdectomie standard reste une intervention extrêmement efficace qui doit être proposée aux patients, en leur en expliquant ses risques mais aussi ses avantages, afin qu’au final ils soient soulagés de leur fardeau hémorroïdaire et ne retardent pas inutilement leur prise en charge.
Références
- Riss S, Weiser FA, Schwameis K, Riss T, Mittlböck M, Steiner G, et al. The prevalence of hemorrhoids in adults. Int J Colorectal Dis. févr 2012;27(2):215-20.
- Nelson RL, Abcarian H, Davis FG, Persky V. Prevalence of benign anorectal disease in a randomly selected population. Dis Colon avr 1995;38(4):341-4.
- Tournu G, Abramowitz L, Couffignal C, Juguet F, Sénéjoux A, Berger S, et Prevalence of anal symptoms in general practice: a prospective study. BMC Fam Pract. 3 août 2017;18(1):78.
- Sheikh P, Régnier C, Goron F, Salmat G. The prevalence, characteristics and treatment of hemorrhoidal disease: results of an international web-based survey. J Comp Eff Res. déc 2020;9(17):1219-32.
- Higuero T, Abramowitz L, Castinel A, Fathallah N, Hemery P, Laclotte, et al. Guidelines for the treatment of hemorrhoids (short report). J Visc juin 2016;153(3):213-8.
- Abramowitz L, Godeberge P, Staumont G, Soudan Recommandations pour la pratique clinique sur le traitement de la maladie hémorroïdaire. Gynécologie Obstétrique Fertil. déc 2001;29(12):942-51.
- Muldoon R. Review of American Society of Colon and Rectal Surgeons Clinical Practice Guidelines for the Management of JAMA Surg. 1 août 2020;155(8):773.
- Milligan ETC, Naunton Morgan C, Jones Lionel E, Officer Surgical anatomy of the canal anal, and the operative treatment of haemorrhoids. The Lancet. nov 1937;230(5959):1119-24.
- Ferguson JA, Heaton RJ. Closed hemorrhoidectomy. Dis Colon Rectum. mars 1959;2(2):176-9.
- Leventoglu S, Mentes B, Balci B, Kebiz HC. New Techniques in Hemorrhoidal Disease but the Same Old Problem: Anal Stenosis. Med Kaunas 1 mars 2022;58(3):362.
- Altomare DF, Picciariello A, Pecorella G, Milito G, Naldini G, Amato A, et al. Surgical management of haemorrhoids: an Italian survey of over 32 000 patients over 17 years. Colorectal Dis Off J Assoc Coloproctology G B Irel. déc 2018;20(12):1117-24.
- Van Tol RR, Bruijnen MPA, Melenhorst J, van Kuijk SMJ, Stassen LPS, Breukink SO. A national evaluation of the management practices of hemorrhoidal disease in the Netherlands. Int J Colorectal Dis. mai 2018;33(5):577-88.
- Picciariello A, Tsarkov PV, Papagni V, Efetov S, Markaryan DR, Tulina I, et al. Classifications and Clinical Assessment of Haemorrhoids: The Proctologist’s Corner. Rev Recent Clin Trials. 15 févr 2021;16(1):10-6.
- Goligher JC, Leacock AG, Brossy The surgical anatomy of the anal canal. Br J Surg. juill 1955;43(177):51-61.
- Kraemer M, Kara D, Rzepisko M, Sayfan J. A simple tool to evaluate common disorders: validation of a “proctological symptom scale”. Int J Colorectal Dis. mai 2015;30(5):679 82.
- Tarasconi A, Perrone G, Davies J, Coimbra R, Moore E, Azzaroli F, et Anorectal emergencies: WSES-AAST guidelines. World J Emerg Surg. déc 2021;16(1):48.
- Pata F, Gallo G, Pellino G, Vigorita V, Podda M, Di Saverio S, et al. Evolution of Surgical Management of Hemorrhoidal Disease: An Historical Overview. Front Surg. 2021;8:727059.
- Blaisdell Office ligation of internal hemorrhoids. Am J Surg. sept 1958;96(3):401-4.
- Barron J, Fallis LS. Non-operative treatment of internal hemorrhoids. Can Med Assoc J. 11 avr 1964;90:910-4.
- Jutabha R, Jensen DM, Chavalitdhamrong D. Randomized prospective study of endoscopic rubber band ligation compared with bipolar coagulation for chronically bleeding internal hemorrhoids. Am J Gastroenterol. août 2009;104(8):2057-64.
- Schleinstein HP, Averbach M, Averbach P, Correa PAFP, Popoutchi P, Rossini LGB. Endoscopic band ligation for the treatment of hemorrhoidal disease. Arq Gastroenterol. 20 mai 2019;56(1):22-7.
- Su MY, Chiu CT, Lin WP, Hsu CM, Chen Long-term outcome and efficacy of endoscopic hemorrhoid ligation for symptomatic internal hemorrhoids. World J Gastroenterol. 21 mai 2011;17(19):2431-6.
- Ramzisham ARM, Sagap I, Nadeson S, Ali IM, Hasni MJ. Prospective Randomized Clinical Trial on Suction Elastic Band Ligator Versus Forceps Ligator in the Treatment of Haemorrhoids. Asian J Surg. oct 2005;28(4):241-5.
- Van Tol RR, Kleijnen J, Watson AJM, Jongen J, Altomare DF, Qvist N, et al. European Society of ColoProctology: guideline for haemorrhoidal disease. Colorectal Dis Off J Assoc Coloproctology G B Irel. juin 2020;22(6):650-62.
- Gallo G, Martellucci J, Sturiale A, Clerico G, Milito G, Marino F, et al. Consensus statement of the Italian society of colorectal surgery (SICCR): management and treatment of hemorrhoidal disease. Tech Coloproctology. févr 2020;24(2):145-64.
- Brown S, Girling C, Thapa Magar H, Chaudry A, Bhatti B, Sayers A, et Guidelines, guidelines and more guidelines for haemorrhoid treatment: A review to sort the wheat from the chaff. Colorectal Dis Off J Assoc Coloproctology G B Irel. juin 2022;24(6):764-72.
- Brown S, Tiernan J, Biggs K, Hind D, Shephard N, Bradburn M, et al. The HubBLe Trial: haemorrhoidal artery ligation (HAL) versus rubber band ligation (RBL) for symptomatic second- and third-degree haemorrhoids: a multicentre randomised controlled trial and health-economic evaluation. Health Technol Assess Winch Engl. nov 2016;20(88):1-150.
- Dekker L, Bak MTJ, Bemelman WA, Felt-Bersma RJF, Han-Geurts Hemorrhoidectomy versus rubber band ligation in grade III hemorrhoidal disease: a large retrospective cohort study with long-term follow-up. Ann Coloproctology. avr 2022;38(2):146-52.
- Poon GP, Chu KW, Lau WY, Lee JM, Yeung C, Fan ST, et al. Conventional vs. triple rubber band ligation for hemorrhoids. A prospective, randomized trial. Dis Colon Rectum. déc 1986;29(12):836-8.
- Khubchandani IT. A randomized comparison of single and multiple rubber band ligations. Dis Colon Rectum. nov 1983;26(11):705-8.
- Tutino R, Massani M, Jospin Kamdem Mambou L, Venturelli P, Della Valle I, Melfa G, et al. A Stepwise Proposal for Low-Grade Hemorrhoidal Disease: Injection Sclerotherapy as a First-Line Treatment and Rubber Band Ligation for Persistent Relapses. Front Surg. 2021;8:782800.
- McKeown DG, Goldstein S. Hemorrhoid Banding. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2022 [cité 18 sept 2022]. Disponible sur: http://www.ncbi.nlm.nih.gov/books/NBK558967/
- Stavrou G, Tzikos G, Malliou P, Panidis S, Kotzampassi K. Rubber band ligation of hemorrhoids: is the procedure effective for the immunocompromised, hemophiliacs and pregnant women? Ann Gastroenterol. oct 2022;35(5):509-13.
- Davis BR, Lee-Kong SA, Migaly J, Feingold DL, Steele SR. The American Society of Colon and Rectal Surgeons Clinical Practice Guidelines for the Management of Hemorrhoids. Dis Colon Rectum. mars 2018;61(3):284-92.
- Iyer VS, Shrier I, Gordon PH. Long-term outcome of rubber band ligation for symptomatic primary and recurrent internal hemorrhoids. Dis Colon Rectum. août 2004;47(8):1364-70.
- Jiang X, Xu M, Ding Y, Cao Y, Pan Y. Recurrent bleeding after rubber band ligation diagnosed as mild hemophilia B: a case report and literature review. BMC Surg. 1 avr 2022;22(1):124.
- Komborozos VA, Skrekas GJ, Pissiotis CA. Rubber band ligation of symptomatic internal hemorrhoids: results of 500 cases. Dig Surg. 2000;17(1):71-6.
- Awad AE, Soliman HH, Saif SALA, Darwish AMN, Mosaad S, Elfert AA. A prospective randomised comparative study of endoscopic band ligation versus injection sclerotherapy of bleeding internal haemorrhoids in patients with liver cirrhosis. Arab J Gastroenterol Off Publ Pan-Arab Assoc Gastroenterol. juin 2012;13(2):77-81.
- Hite N, Klinger AL, Miller P, Beck DE, Whitlow CB, Hicks TC, et al. Clopidogrel bisulfate (Plavix) does not increase bleeding complications in patients undergoing rubber band ligation for symptomatic hemorrhoids. J Surg Res. sept 2018;229:230-3.
- Beattie GC, Rao MM, Campbell WJ. Secondary haemorrhage after rubber band ligation of haemorrhoids in patients taking clopidogrel–a cautionary note. Ulster Med J. nov 2004;73(2):139-41.
- Nelson RS, Ewing BM, Ternent C, Shashidharan M, Blatchford GJ, Thorson AG. Risk of late bleeding following hemorrhoidal banding in patients on antithrombotic prophylaxis. Am J Surg. déc 2008;196(6):994-9; discussion 999.
- De Robles MS, Young CJ. Rubber Band Ligation of Hemorrhoids is often a Necessary Complement in the Management of Hemorrhagic Radiation Proctitis. Scand J Surg SJS Off Organ Finn Surg Soc Scand Surg Soc. juin 2020;109(2):108-14.
- Hawkins M, Billingham R, Bastawrous Hemorrhoid management in patients with radiation proctitis. Int J Colorectal Dis. déc 2012;27(12):1673-7.
- Lamonaca L, Auriemma F, Paduano D, Bianchetti M, Spatola F, Galtieri P, et Rectal band ligation as a treatment for chronic radiation proctitis: a feasibility study. Endosc Int Open. juin 2022;10(6):E787-90.
- Pita I, Bastos P, Dinis-Ribeiro M. Pelvic Catastrophe after Elastic Band Ligation in an Irradiated Rectum. GE – Port J Gastroenterol. 2018;25(1):42-6.
- Thornhill JA, Long RM, Neary P, O’Connor HJ, Ryan B, Fraser I. The pitfalls of treating anorectal conditions after radiotherapy for prostate Ir Med J. mars 2012;105(3):91-3.
- Watson NFS, Liptrott S, Maxwell-Armstrong A prospective audit of early pain and patient satisfaction following out-patient band ligation of haemorrhoids. Ann R Coll Surg Engl. mai 2006;88(3):275-9.
- Komporozos V, Ziozia V, Komporozou A, Stravodimos G, Kolinioti A, Papazoglou A. Rubber band ligation of symptomatic hemorrhoids: an old solution to an everyday problem. Int J Colorectal Dis. août 2021;36(8):1723-9.
- Lee HH, Spencer RJ, Beart Multiple hemorrhoidal bandings in a single session. Dis Colon Rectum. janv 1994;37(1):37-41.
- Jiang YD, Liu Y, Wu JD, Li GP, Liu J, Hou XH, et al. Massive gastrointestinal bleeding after endoscopic rubber band ligation of internal hemorrhoids: A case report. World J Clin Cases. 6 juill 2022;10(19):6656-63.
- Kasher JA, Mathisen G. Acquiring tetanus after hemorrhoid banding and other gastrointestinal procedures. J Gastrointest Surg Off J Soc Surg Aliment Tract. avr 2007;11(4):515-9.
- Parker R, Gul R, Bucknall V, Bowley D, Karandikar S. Double jeopardy: pyogenic liver abscess and massive secondary rectal haemorrhage after rubber band ligation of haemorrhoids. Colorectal Dis Off J Assoc Coloproctology G B Irel. juill 2011;13(7):e184.
- Ku JJK, Marfan M, Wall D. Pyogenic liver abscess after haemorrhoidal banding. ANZ J Surg. sept 2005;75(9):828-30.
- Tejirian T, Abbas Bacterial endocarditis following rubber band ligation in a patient with a ventricular septal defect: report of a case and guideline analysis. Dis Colon Rectum. déc 2006;49(12):1931-3.
- Misheva B, Hajjar R, Mercier F, Schwenter F, Sebajang H. Conservative management of pelvic sepsis with severe shock and multiple organ dysfunction syndrome after rubber-band ligation of internal haemorrhoids: surgery is not the only option. J Surg Case Rep. août 2018;2018(8):rjy199.
- Subramaniam D, Hureibi K, Zia K, Uheba M. The development of Fournier’s gangrene following rubber band ligation of haemorrhoids. BMJ Case Rep. 28 nov 2013;2013:bcr2013201474.
- McCloud JM, Jameson JS, Scott AND. Life-threatening sepsis following treatment for haemorrhoids: a systematic review. Colorectal Dis Off J Assoc Coloproctology G B Irel. nov 2006;8(9):748-55.
- Albuquerque A. Rubber band ligation of hemorrhoids: A guide for complications. World J Gastrointest Surg. 27 sept 2016;8(9):614-20.
- Société Nationale Française de Colo-Proctologie. Fiche technique : Traitement des hémorroïdes par ligature élastique. Disponible sur: https:// snfcp.org/fiches-pratiques/fiches-techniques/hemorroides-fiches-techniques/traitement-hemorroides-ligature-elastique/
- De Parades V, Aubert M, Fathallah N, Alam AA, Spindler L, Benfredj P. The comeback of hemorrhoidal sclerotherapy? Tech août 2022;26(8):599-601.
- Gallo G, Pietroletti R, Novelli E, Sturiale A, Tutino R, Lobascio P, et A multicentre, open-label, single-arm phase II trial of the efficacy and safety of sclerotherapy using 3% polidocanol foam to treat second-degree haemorrhoids (SCLEROFOAM). Tech Coloproctology. août 2022;26(8):627-36.
- Gallo G, Ronconi M, Trompetto Sclerotherapy with 3% polidocanol foam: revolutionizing outpatient treatment in patients with haemorrhoidal disease. Updat Surg. oct 2021;73(5):2029-30.
- Pata F, Bracchitta LM, D’Ambrosio G, Bracchitta S. Sclerobanding (Combined Rubber Band Ligation with 3% Polidocanol Foam Sclerotherapy) for the Treatment of Second- and Third-Degree Hemorrhoidal Disease: Feasibility and Short-Term Outcomes. J Clin Med. 31 déc 2021;11(1):218.
- He A, Chen M. Sclerotherapy in Hemorrhoids. Indian J Surg. 20 avr 2022;1-5.
- Yoshimitsu M, Egi H, Nagamatsu S, Shimomura M, Hakoda K, Miguchi M, et Gluteal-fold flap repair of rectovaginal fistula caused by aluminum potassium sulfate hydrate-tannic acid injection for internal hemorrhoids: a case report. Surg Case Rep. 8 juill 2020;6(1):166.
- Neiger A. Hemorrhoids: recognition and current therapeutic possibilities. Schweiz Med Wochenschr. 1 avr 1978;108(13):500-4.
- Higuero T. Traitement de la pathologie hémorroïdaire : les nouvelles recommandations. Post’U, Paris; 2014.
- Ding Z, Xuan J, Tang G, Shi S, Liang X, An Q, et al. Rubber band ligation versus coagulation for the treatment of haemorrhoids: a meta-analysis of randomised controlled trials. Postgrad Med J. 24 août 2022;postgradmedj-2022-141941.
- Walker AJ, Leicester RJ, Nicholls RJ, Mann CV. A prospective study of infrared coagulation, injection and rubber band ligation in the treatment of haemorrhoids. Int J Colorectal Dis. mai 1990;5(2):113-6.
- MacRae HM, McLeod RS. Comparison of hemorrhoidal treatments: a meta-analysis. Can J Surg J Can Chir. févr 1997;40(1):14-7.
- Ambrose NS, Hares MM, Alexander-Williams J, Keighley MR. Prospective randomised comparison of photocoagulation and rubber band ligation in treatment of haemorrhoids. Br Med J Clin Res Ed. 30 avr 1983;286(6375):1389-91.
- Ng KS, Holzgang M, Young C. Still a Case of « No Pain, No Gain »? An Updated and Critical Review of the Pathogenesis, Diagnosis, and Management Options for Hemorrhoids in 2020. Ann Coloproctology. juin 2020;36(3):133-47.
- Shanmugam V, Thaha MA, Rabindranath KS, Campbell KL, Steele RJC, Loudon Rubber band ligation versus excisional haemorrhoidectomy for haemorrhoids. Cochrane Database Syst Rev. 20 juill 2005;(3):CD005034.
- Dekker L, Han-Geurts IJM, Rørvik HD, van Dieren S, Bemelman WA. Rubber band ligation versus haemorrhoidectomy for the treatment of grade II-III haemorrhoids: a systematic review and meta-analysis of randomised controlled trials. Tech Coloproctology. juin 2021;25(6):663-74.
- Shanmugam V, Muthukumarasamy G, Cook JA, Vale L, Watson AJM, Loudon MA. Randomized controlled trial comparing rubber band ligation with stapled haemorrhoidopexy for Grade II circumferential haemorrhoids: long-term results. Colorectal Dis Off J Assoc Coloproctology G B Irel. juin 2010;12(6):579-86.
- Neves S, Falcão D, Povo A, Castro-Poças F, Oliveira J, Salgueiro P. 3% polidocanol foam sclerotherapy versus hemorrhoidal artery ligation with recto anal repair in hemorrhoidal disease grades II-III: a randomized, pilot trial. Rev Espanola Enfermedades Dig Organo Of Soc Espanola Patol Dig. 31 mai 2022;
- Longchamp G, Liot E, Meyer J, Toso C, Buchs NC, Ris F. Non-excisional laser therapies for hemorrhoidal disease: a systematic review of the Lasers Med Sci. avr 2021;36(3):485-96.
- Giamundo P, Salfi R, Geraci M, Tibaldi L, Murru L, Valente The hemorrhoid laser procedure technique vs. rubber band ligation: a randomized trial comparing 2 mini-invasive treatments for second- and third-degree hemorrhoids. Dis Colon Rectum. juin 2011;54(6):693-8.
- Longo A. Treatment of hemorrhoidal disease by reduction of mucosa and hemorrhoidal prolapse with a circular suturing device: a new In: Proceedings of the 6th World Congress of Endoscopic Surgery, Rome, 3-6 June 1998. Bologna, Italy: Monduzzi Editore; 1998. p. 777-84.
- Watson AJM, Hudson J, Wood J, Kilonzo M, Brown SR, McDonald A, et Comparison of stapled haemorrhoidopexy with traditional excisional surgery for haemorrhoidal disease (eTHoS): a pragmatic, multicentre, randomised controlled trial. Lancet Lond Engl. 12 nov 2016;388(10058):2375-85.
- Aibuedefe B, Kling SM, Philp MM, Ross HM, Poggio JL. An update on surgical treatment of hemorrhoidal disease: a systematic review and meta-analysis. Int J Colorectal Dis. sept 2021;36(9):2041-9.
- Jin JZ, Bhat S, Lee KT, Xia W, Hill AG. Interventional treatments for prolapsing haemorrhoids: network meta-analysis. BJS Open. 6 sept 2021;5(5):zrab091.
- Lumb KJ, Colquhoun PHD, Malthaner RA, Jayaraman S. Stapled versus conventional surgery for hemorrhoids. Cochrane Database Syst 18 oct 2006;(4):CD005393.
- Bellio G, Pasquali A, Schiano di Visconte M. Stapled Hemorrhoidopexy: Results at 10-Year Follow-up. Dis Colon Rectum. avr 2018;61(4):491-8.
- Sturiale A, Fabiani B, Menconi C, Cafaro D, Fusco F, Bellio G, et al. Long-term results after stapled hemorrhoidopexy: a survey study with mean follow-up of 12 years. Tech Coloproctology. sept 2018;22(9):689-96.
- Ruan QZ, English W, Hotouras A, Bryant C, Taylor F, Andreani S, et al. A systematic review of the literature assessing the outcomes of stapled haemorrhoidopexy versus open haemorrhoidectomy. Tech Coloproctology. janv 2021;25(1):19-33.
- Sultan S. Longo procedure (Stapled hemorrhoidopexy): Indications, results. J Visc Surg. avr 2015;152(2):S11-4.
- Faucheron JL, Voirin D, Abba J. Rectal perforation with life-threatening peritonitis following stapled haemorrhoidopexy. Br J Surg. juin 2012;99(6):746-53.
- Ryu S, Bae BN. Rectal free perforation after stapled hemorrhoidopexy: A case report of laparoscopic peritoneal lavage and repair without Int J Surg Case Rep. 2017;30:40-2.
- Porrett LJ, Porrett JK, Ho YH. Documented complications of staple hemorrhoidopexy: a systematic review. Int Surg. janv 2015;100(1):44-57.
- Ravo B, Amato A, Bianco V, Boccasanta P, Bottini C, Carriero A, et al. Complications after stapled hemorrhoidectomy: can they be prevented? Tech Coloproctology. sept 2002;6(2):83-8.
- Aly EH. Stapled haemorrhoidopexy: is it time to move on? Ann R Coll Surg Engl. oct 2015;97(7):490-3.
- Morinaga K, Hasuda K, Ikeda T. A novel therapy for internal hemorrhoids: ligation of the hemorrhoidal artery with a newly devised instrument (Moricorn) in conjunction with a Doppler Am J Gastroenterol. avr 1995;90(4):610-3.
- Dal Monte PP, Tagariello C, Giordano P, Cudazzo E, Shafi A, Sarago M, et al. Transanal haemorrhoidal dearterialisation: nonexcisional surgery for the treatment of haemorrhoidal disease. Tech Coloproctology. déc 2007;11(4):333-9.
- Pucher PH, Sodergren MH, Lord AC, Darzi A, Ziprin P. Clinical outcome following Doppler-guided haemorrhoidal artery ligation: a systematic review. Colorectal Dis Off J Assoc Coloproctology G B Irel. juin 2013;15(6):e284-294.
- Ratto C, Campennì P, Papeo F, Donisi L, Litta F, Parello A. Transanal hemorrhoidal dearterialization (THD) for hemorrhoidal disease: a single- center study on 1000 consecutive cases and a review of the literature. Tech Coloproctology. déc 2017;21(12):953-62.
- Yilmaz İ, Özgür Karakaş D, Sücüllü İ. Long-term Results of Hemorrhoidal Artery Ligation. Am Surg. mars 2016;82(3):216-20.
- Ferrandis C, De Faucal D, Fabreguette JM, Borie F. Efficacy of Doppler-guided hemorrhoidal artery ligation with mucopexy, in the short and long terms for patients with hemorrhoidal disease. Tech Coloproctology. févr 2020;24(2):165-71.
- Giordano P, Tomasi I, Pascariello A, Mills E, Elahi S. Transanal dearterialization with targeted mucopexy is effective for advanced Colorectal Dis Off J Assoc Coloproctology G B Irel. mai 2014;16(5):373-6.
- Faucheron JL, Poncet G, Voirin D, Badic B, Gangner Y. Doppler-guided hemorrhoidal artery ligation and rectoanal repair (HAL-RAR) for the treatment of grade IV hemorrhoids: long-term results in 100 consecutive patients. Dis Colon Rectum. févr 2011;54(2):226-31.
- Gupta PJ, Kalaskar S, Taori S, Heda PS. Doppler-guided hemorrhoidal artery ligation does not offer any advantage over suture ligation of grade 3 symptomatic hemorrhoids. Tech Coloproctology. déc 2011;15(4):439-44.
- Aigner F, Kronberger I, Oberwalder M, Loizides A, Ulmer H, Gruber L, et Doppler-guided haemorrhoidal artery ligation with suture mucopexy compared with suture mucopexy alone for the treatment of Grade III haemorrhoids: a prospective randomized controlled trial. Colorectal Dis Off J Assoc Coloproctology G B Irel. juill 2016;18(7):710-6.
- Alemrajabi M, Akbari A, Sohrabi S, Rezazadehkermani M, Moradi M, Agah S, et Simple mucopexy and hemorrhoidal arterial ligation with and without Doppler guide: a randomized clinical trial for short-term outcome. Ann Coloproctology. 16 mai 2022;
- Zhai M, Zhang YA, Wang ZY, Sun JH, Wen J, Zhang Q, et al. A Randomized Controlled Trial Comparing Suture-Fixation Mucopexy and Doppler-Guided Hemorrhoidal Artery Ligation in Patients with Grade III Hemorrhoids. Gastroenterol Res Pract. 2016;2016:8143703.
- Popovtsev MA, Alekberzade AV, Krylov NN. Hemorrhoidal artery ligation without Doppler navigation in surgical treatment of hemorrhoidal Khirurgiia (Sofiia). 2021;(12):49-55.
- Giamundo P. Advantages and limits of hemorrhoidal dearterialization in the treatment of symptomatic hemorrhoids. World J Gastrointest 27 janv 2016;8(1):1-4.
- Figueiredo MN, Campos FG. Doppler-guided hemorrhoidal dearterialization/transanal hemorrhoidal dearterialization: Technical evolution and outcomes after 20 years. World J Gastrointest Surg. 27 mars 2016;8(3):232-7.
- Popov V, Yonkov A, Arabadzhieva E, Zhivkov E, Bonev S, Bulanov D, et al. Doppler-guided transanal hemorrhoidal dearterilization versus conventional hemorrhoidectomy for treatment of hemorrhoids – early and long-term postoperative results. BMC Surg. 10 janv 2019;19(1):4.
- Alam A, Fathallah N, Spindler L, El Mituialy A, Pommaret E, Benfredj P, et al. Hemorrhoidal surgery in patients with IBD: caution is the parent of safety. Tech Coloproctology. déc 2021;25(12):1319-21.
- Fathallah N, et al. Les techniques mini-invasives en chirurgie hémorroïdaire : la fin du règne de l’hémorroïdectomie ? Hepato déc 2017;24(10):1019-29.
- Poskus T, Danys D, Makunaite G, Mainelis A, Mikalauskas S, Poskus E, et Results of the double-blind randomized controlled trial comparing laser hemorrhoidoplasty with sutured mucopexy and excisional hemorrhoidectomy. Int J Colorectal Dis. mars 2020;35(3):481-90.
- Faes S, Pratsinis M, Hasler-Gehrer S, Keerl A, Nocito A. Short- and long-term outcomes of laser haemorrhoidoplasty for grade II-III haemorrhoidal disease. Colorectal Dis Off J Assoc Coloproctology G B Irel. juin 2019;21(6):689-96.
- Thierry ML, Portal A, Fathallah N, Aubert M, Lemarchand N, de Parades V. Laser haemorrhoidoplasty: is it time to rethink the procedure? Tech Coloproctology. juill 2020;24(7):779-80.
- Jain A, Lew C, Aksakal G, Hiscock R, Mirbagheri N. Laser hemorrhoidoplasty in the treatment of symptomatic hemorrhoids: a pilot Australian Ann Coloproctology. 19 mai 2022;
- Weyand G, Theis CS, Fofana AN, Rüdiger F, Gehrke T. Laserhämorrhoidoplastie mit dem 1470-nm-Diodenlaser in der Behandlung des zweit- bis viertgradigen Hämorrhoidalleidens – eine Kohortenstudie mit 497 Fällen. Zentralblatt Für Chir – Z Für Allg Visz Thorax- Gefäßchirurgie. août 2019;144(04):355-63.
- Lim SY, Rajandram R, Roslani Comparison of post-operative bleeding incidence in laser hemorrhoidoplasty with and without hemorrhoidal artery ligation: a double-blinded randomized controlled trial. BMC Surg. 21 avr 2022;22(1):146.
- Maloku H, Gashi Z, Lazovic R, Islami H, Juniku-Shkololli A. Laser Hemorrhoidoplasty Procedure vs Open Surgical Hemorrhoidectomy: a Trial Comparing 2 Treatments for Hemorrhoids of Third and Fourth Degree. Acta Inform Medica AIM J Soc Med Inform Bosnia Herzeg Cas Drustva Za Med Inform BiH. déc 2014;22(6):365-7.
- Naderan M, Shoar S, Nazari M, Elsayed A, Mahmoodzadeh H, Khorgami Z. A Randomized Controlled Trial Comparing Laser Intra- Hemorrhoidal Coagulation and Milligan-Morgan Hemorrhoidectomy. J Investig Surg Off J Acad Surg Res. oct 2017;30(5):325-31.
- Lie H, Caesarini EF, Purnama AA, Irawan A, Sudirman T, Jeo WS, et Laser hemorrhoidoplasty for hemorrhoidal disease: a systematic review and meta-analysis. Lasers Med Sci. 12 sept 2022;
- Trigui A, Rejab H, Akrout A, Trabelsi J, Zouari A, Majdoub Y, et al. Laser utility in the treatment of hemorrhoidal pathology: a review of Lasers Med Sci. mars 2022;37(2):693-9.
- Brusciano L, Gambardella C, Terracciano G, Gualtieri G, Schiano di Visconte M, Tolone S, et al. Postoperative discomfort and pain in the management of hemorrhoidal disease: laser hemorrhoidoplasty, a minimal invasive treatment of symptomatic hemorrhoids. Updat Surg. sept 2020;72(3):851-7.
- Tan VZZ, Peck EW, Sivarajah SS, Tan WJ, Ho LML, Ng JL, et al. Systematic review and meta-analysis of postoperative pain and symptoms control following laser haemorrhoidoplasty versus Milligan-Morgan haemorrhoidectomy for symptomatic haemorrhoids: a new standard. Int J Colorectal Dis. août 2022;37(8):1759-71.
- Salfi A New Technique for Ambulatory Hemorrhoidal Treatment: Doppler-Guided Laser Photocoagulation of Hemorrhoidal Arteries*. coloproctology. avr 2009;31(2):99-103.
- De Nardi P, Tamburini AM, Gazzetta PG, Lemma M, Pascariello A, Asteria CR. Hemorrhoid laser procedure for second- and third-degree hemorrhoids: results from a multicenter prospective study. Tech Coloproctology. juill 2016;20(7):455-9.
- Giamundo P, Cecchetti W, Esercizio L, Fantino G, Geraci M, Lombezzi R, et Doppler-guided hemorrhoidal laser procedure for the treatment of symptomatic hemorrhoids: experimental background and short-term clinical results of a new mini-invasive treatment. Surg Endosc. mai 2011;25(5):1369-75.
- Giamundo P, De Angelis M, Mereu A. Hemorrhoid laser procedure with suture-pexy (HeLPexx): a novel effective procedure to treat hemorrhoidal disease. Tech Coloproctology. févr 2020;24(2):199-205.
- Giamundo P, Braini A, Calabrò G, Crea N, De Nardi P, Fabiano F, et al. Doppler-guided hemorrhoidal dearterialization with laser (HeLP): indications and clinical outcome in the long-term. Results of a multicenter trial. Surg Endosc. janv 2022;36(1):143-8.
- Giamundo P, Braini A, Calabro’ G, Crea N, De Nardi P, Fabiano F, et al. Doppler-guided hemorrhoidal dearterialization with laser (HeLP): a prospective analysis of data from a multicenter trial. Tech Coloproctology. août 2018;22(8):635-43.
- Ram E, Bachar GN, Goldes Y, Joubran S, Rath-Wolfson Modified Doppler-guided laser procedure for the treatment of second- and third- degree hemorrhoids. Laser Ther. 30 juin 2018;27(2):137-42.
- Crea N, Pata G, Lippa M, Tamburini AM, Berjaoui AH. Hemorrhoid laser procedure (HeLP) for second- and third-degree hemorrhoids: results from a long-term follow-up analysis. Lasers Med Sci. févr 2022;37(1):309-15.
- Gallo G, Podzemny V, Pescatori Intestinal obstruction requiring fecal diversion due to rectal hematoma following a hemorrhoid laser procedure (HeLP). Tech Coloproctology. juill 2016;20(7):507-8.
- Giamundo P, De Nardi P. Intestinal obstruction following a hemorrhoid laser procedure (HeLP). Tech Coloproctology. oct 2016;20(10):727-8.
- Gupta PJ. Novel technique: radiofrequency coagulation–a treatment alternative for early-stage hemorrhoids. MedGenMed Medscape Gen 31 juill 2002;4(3):1.
- Duben J, Hnátek L, Dudesek B, Musil T, Gatek J. Initial results of the bipolar RFITT coagulation in advanced stages of hemorrhoidal disorder Rozhl V Chir Mesicnik Ceskoslovenske Chir Spolecnosti. nov 2008;87(11):576-9.
- Didelot JM, Didelot R. Radiofrequency thermocoagulation of haemorrhoidal bundles, an alternative technique for the management of internal Int J Colorectal Dis. mars 2021;36(3):601-4.
- Duben J, Hnatek L, Dudesek B, Humpolicek P, Gatek J. Bipolar radiofrequency-induced thermotherapy of haemorrhoids: a new minimally invasive method for haemorrhoidal disease treatment. Early results of a pilot study. Videosurgery Miniinvasive Tech. 2013;1:43-8.
- Schäfer H, Tolksdorf S, Vivaldi C. Radiofrequenzablation (Rafaelo®-Prozedur) zur Therapie von prolabierenden Hämorrhoiden III°: Technik und erste Ergebnisse. coloproctology. juin 2018;40(3):204-10.
- Shikhmetov AN, Lebedev NN, Ryazanov NV, Krishchanovich OS. The first experience of har-rar and radiofrequency ablation for hemorrhoidal disease treatment in hospitalization replacement Khirurgiia (Sofiia). 2018;(11):53-9.
- Duben J, Ponížil P, Dudešek B, Hnátek L, Gatěk J. Bipolar radiofrequency-induced thermotherapy of haemorrhoids: a 10-year Rozhl V Chir Mesicnik Ceskoslovenske Chir Spolecnosti. Summer 2018;97(9):419-22.
- Eddama MMR, Everson M, Renshaw S, Taj T, Boulton R, Crosbie J, et al. Radiofrequency ablation for the treatment of haemorrhoidal disease: a minimally invasive and effective treatment modality. Tech Coloproctology. août 2019;23(8):769-74.
- Drissi F, Jean MH, Abet Evaluation of the efficacy and morbidity of radiofrequency thermocoagulation in the treatment of hemorrhoidal disease. J Visc Surg. oct 2021;158(5):385-9.
- Hassan S, McGrath D, Barnes R, Middleton S. Radiofrequency Ablation (Rafaelo Procedure) for the Treatment of Hemorrhoids: A Case Series in the United Kingdom. Ann Coloproctology. 18 août 2021;
- Gandhi JA, Shinde PH, Banker A, Chaudhari SN. Initial experience of radiofrequency ablation for the treatment of advanced haemorrhoidal Przeglad Gastroenterol. 2022;17(3):234-9.
- Tolksdorf S, Tübergen D, Vivaldi C, Pisek M, Klug F, Kemmerling M, et al. Early and midterm results of radiofrequency ablation (Rafaelo® procedure) for third-degree haemorrhoids: a prospective, two-centre study. Tech Coloproctology. juin 2022;26(6):479-87.
- Didelot JM, Raux B, Didelot R, Rudler F, Mulliez A, Buisson A, et al. What can patients expect in the long term from radiofrequency thermocoagulation of hemorrhoids on bleeding, prolapse, quality of life, and recurrence: “no pain, no gain” or “no pain but a gain”? Ann Coloproctol. 2022 Oct 11. doi: 10.3393/ac.2022.00311.0044. Epub ahead of print. PMID: 36217810.
- Abramowitz L, Bouchard D, Siproudhis L, Trompette M, Pillant H, Bord C, et al. Psychometric properties of a questionnaire (HEMO-FISS-QoL) to evaluate the burden associated with haemorrhoidal disease and anal fissures. Colorectal Dis. janv 2019;21(1):48-58.
- Laurain A, Bouchard D, Rouillon JM, Petit P, Liddo A, Vinson-Bonnet B, et Evaluation prospective multicentrique française du traitement chirurgical de la maladie hémorroïdaire par radiofréquence. Communication Orale présenté à; 2022 mars 17; JFHOD 2022 – Paris.
- Uflacker Transcatheter embolization for treatment of acute lower gastrointestinal bleeding. Acta Radiol Stockh Swed 1987. août 1987;28(4):425-30.
- Galkin EV. Interventional radiology of chronic hemorrhoids. Vestn Rentgenol Radiol. août 1994;(4):52-6.
- Vidal V, Louis G, Bartoli JM, Sielezneff I. Embolization of the hemorrhoidal arteries (the emborrhoid technique): a new concept and challenge for interventional radiology. Diagn Interv Imaging. mars 2014;95(3):307-15.
- Vidal V, Sapoval M, Sielezneff Y, De Parades V, Tradi F, Louis G, et al. Emborrhoid: a new concept for the treatment of hemorrhoids with arterial embolization: the first 14 Cardiovasc Intervent Radiol. févr 2015;38(1):72-8.
- Panneau J, Mege D, Di Bisceglie M, Duclos J, Habert P, Bartoli A, et Rectal Artery Embolization for Hemorrhoidal Disease: Anatomy, Evaluation, and Treatment Techniques. Radiogr Rev Publ Radiol Soc N Am Inc. oct 2022;42(6):1829-44.
- Rebonato A, Maiettini D, Patriti A, Giurazza F, Tipaldi MA, Piacentino F, et al. Hemorrhoids Embolization: State of the Art and Future J Clin Med. 12 août 2021;10(16):3537.
- Wang X, Sheng Y, Wang Z, Wang W, Xia F, Zhao M, et al. Comparison of different embolic particles for superior rectal arterial embolization of chronic hemorrhoidal bleeding: gelfoam versus microparticle. BMC Gastroenterol. 14 déc 2021;21(1):465.
- Campennì P, Iezzi R, Marra AA, Posa A, Parello A, Litta F, et al. The Emborrhoid Technique for Treatment of Bleeding Hemorrhoids in Patients with High Surgical Risk. J Clin Med. 21 sept 2022;11(19):5533.
- Nguyenhuy M, Xu Y, Kok HK, Maingard J, Joglekar S, Jhamb A, et al. Clinical Outcomes Following Rectal Artery Embolisation for the Treatment of Internal Haemorrhoids: A Systematic Review and Meta-Analysis. Cardiovasc Intervent Radiol. sept 2022;45(9):1351-61.
- Talaie R, Torkian P, Moghadam AD, Tradi F, Vidal V, Sapoval M, et al. Hemorrhoid embolization: A review of current evidences. Diagn Interv Imaging. janv 2022;103(1):3-11.
- De Gregorio MA, Bernal R, Ciampi-Dopazo JJ, Urbano J, Millera A, Guirola JA. Safety and Effectiveness of a New Electrical Detachable Microcoil for Embolization of Hemorrhoidal Disease, November 2020-December 2021: Results of a Prospective Study. J Clin Med. 28 mai 2022;11(11):3049.
- Eberspacher C, Ficuccilli F, Tessieri L, D’Andrea V, Lauro A, Fralleone L, et Annoyed with Haemorrhoids? Risks of the Emborrhoid Technique. Dig Dis Sci. nov 2021;66(11):3725-9.
- Sajid MS, Parampalli U, Whitehouse P, Sains P, McFall MR, Baig MK. A systematic review comparing transanal haemorrhoidal de-arterialisation to stapled haemorrhoidopexy in the management of haemorrhoidal disease. Tech Coloproctology. févr 2012;16(1):1-8.
- Venara A, Podevin J, Godeberge P, Redon Y, Barussaud ML, Sielezneff I, et al. A comparison of surgical devices for grade II and III hemorrhoidal disease. Results from the LigaLongo Trial comparing transanal Doppler-guided hemorrhoidal artery ligation with mucopexy and circular stapled hemorrhoidopexy. Int J Colorectal Dis. oct 2018;33(10):1479-83.
- Song Y, Chen H, Yang F, Zeng Y, He Y, Huang H. Transanal hemorrhoidal dearterialization versus stapled hemorrhoidectomy in the treatment of hemorrhoids: A PRISMA-compliant updated meta-analysis of randomized control trials. Medicine (Baltimore). juill 2018;97(29):e11502.