Liens d’intérêt
Abbvie, Amgen, MSD, Celltrion, Tillots, Pfizer, Janssen, Takeda
Mots-clés
Maladie de Crohn ; Stratégie thérapeutique ; Seconde ligne de biothérapie
Abréviations
Maladie de Crohn (MC), European Crohn’s and Colitis Organisation (ECCO), Maladie inflammatoire chronique intestinale (MICI), Autorisation de Mise sur le Marché (AMM)
Introduction
La maladie de Crohn (MC) est une maladie inflammatoire chronique intestinale pouvant toucher l’ensemble du tube digestif. En raison de la nature progressive et destructrice du processus inflammatoire, il est important de réaliser rapidement des choix thérapeutiques afin d’obtenir une rémission précoce et durable et de prévenir les complications.
Notre décision thérapeutique doit être guidée par la connaissance du patient dans sa globalité et de l’arsenal thérapeutique à disposition. En effet, chaque patient est différent et chaque patient répondra différemment à une même molécule. Aujourd’hui, nous ne disposons d’aucun test permettant de prédire l’efficacité d’un traitement chez un patient donné et de guider notre choix thérapeutique.
En France, le choix de la première ligne est dicté par l’AMM et le remboursement. Seuls les anti-TNF, adalimumab et infliximab, remplissent ces critères dans la MC aujourd’hui. Le libellé de l’indication en France autorise les anti-TNF dans la maladie de Crohn chez « les adultes ayant une poussée modérée à sévère de la maladie de Crohn, non contrôlée malgré l’utilisation des corticoïdes et/ou d’un immunosuppresseur (méthotrexate, azathioprine), ou chez lesquels ces traitements sont mal tolérés ou contre-indiqués ». L’AMM inclut également les malades ayant une fistule et les Crohn pédiatriques. Une littérature abondante soutient leur efficacité depuis plus de 20 ans et les recommandations ECCO de 2020 confirment leur utilisation en première ligne, préférentiellement en combothérapie (1). Le choix de traitement en première ligne participe pleinement à la décision du traitement de deuxième ligne.
De quels traitements dispose-t-on en seconde ligne après échec d’une première ligne d’anti-TNF ?
Nous disposons en seconde ligne après échec d’anti-TNF de 4 classes thérapeutiques : les anti-TNF (infliximab, adalimumab), le vedolizumab, l’ustekinumab et le rizankizumab.
L’infliximab est un anticorps monoclonal chimérique dirigé contre le TNF alpha. C’est le plus ancien des traitements disponibles aujourd’hui. Il a obtenu une première autorisation de mise sur le marché (AMM) dans la maladie de Crohn en France dès 2000. Il bénéficie également d’une AMM dans les maladies inflammatoires articulaires et cutanées, ce qui représente un avantage notable lors de pathologies associées. Ce traitement augmente les risques infectieux. Un dépistage de la tuberculose, avant l’instauration d’un traitement, doit être réalisé. Des cas de cancers chez des patients traités par l’infliximab ont été signalés. Mais, à l’exception du mélanome dont le risque pourrait être légèrement augmenté sous infliximab, le nombre de cas de cancer ne paraît pas augmenté par comparaison à ceux survenus chez des patients ayant une MICI et n’ayant pas reçu ce traitement. Le risque de faciliter la survenue de lymphomes ne peut être écarté à ce jour. Enfin, la famille des anti-TNF est contre-indiquée en cas d’insuffisance cardiaque sévère et de sclérose en plaque. Les recommandations concernant l’infliximab préconisent sa prescription en association avec un immunosuppresseur du fait du risque immunogène (consensus ECCO et recommandations françaises). Cette combothérapie infliximab/ immunosuppresseur augment de manière significative les risques infectieux. Cela aura donc toute son importance dans le choix thérapeutique. Enfin, l’infliximab nécessite une induction intraveineuse, le traitement d’entretien quant à lui peut être réalisé soit en perfusions IV sous en injections sous-cutanées. La possibilité récente du traitement d’entretien en SC facilite sa prescription en ville.
L’adalimumab est un anticorps monoclonal 100 % humanisé dirigé contre le TNF alpha. Il a obtenu une AMM dans la maladie de Crohn en France en 2007. L’adalimumab a obtenu d’autres AMM, pour des rhumatismes inflammatoires chroniques (polyarthrite rhumatoïde, spondylarthrite ankylosante, rhumatisme psoriasique et arthrite juvénile idiopathique), la maladie de Verneuil et le psoriasis cutané. Ces différentes AMM lui procurent les mêmes avantages que l’infliximab lors de pathologies croisées. Il a aussi l’avantage de ne pas nécessiter de perfusion en milieu hospitalier, son induction se réalisant via des injections sous-cutanées. Il présente les mêmes contre-indications et la même tolérance que les autres anti-TNF alpha.
Le vedolizumab est un anticorps monoclonal bloquant l’intégrine 4-7. En 2014, il a obtenu une AMM en France et en Europe. Son traitement d’induction se fait exclusivement par voie IV tandis que le traitement d’entretien peut se faire selon des modalités intraveineuses ou sous-cutanées. Des infections respiratoires hautes (pharyngites, angines, laryngites) non sévères ont été un peu plus souvent observées sous vedolizumab que sous placebo. Des cas de cancers ont été observés chez des patients traités mais le nombre de cas ne paraît pas augmenter par comparaison à ceux survenus chez des patients ayant une MICI et n’ayant pas reçu ce traitement. Sa tolérance est considérée comme très satisfaisante. Sa très faible immunogénicité, conduit à le prescrire en monothérapie, permettant d’écarter ainsi les risques propres aux immunosuppresseurs.
L’ustekinumab est un anticorps monoclonal dirigé contre la sous unité p40 commune aux interleukines 12 et 23. Il est peu contraignant pour le patient avec une seule administration intra-veineuse au départ (environ 6 mg/kg) puis un traitement d’entretien sous forme d’une injection sous- cutanée toutes les 8 à 12 semaines. Il a en outre obtenu une AMM dans le traitement du psoriasis en France en 2009 et est commercialisé dans cette indication depuis 2010. Depuis, cette AMM a été élargie aux rhumatismes associés au psoriasis. Depuis novembre 2016, l’ustekinumab a obtenu une AMM européenne dans l’indication maladie de Crohn. L’antériorité de l’AMM dans le psoriasis nous permet d’avoir du recul concernant les effets indésirables de ce traitement. Il ne semble pas augmenter le risque d’infections sévères. Par ailleurs, les patients ayant reçu l’ustekinumab dans des études cliniques n’ont pas développé plus de tumeurs malignes que les patients qui recevaient le placebo. Sa tolérance est considérée comme très satisfaisante. Du fait de sa faible immunogénicité, il est également prescrit en monothérapie.
Le risankizumab, dernier arrivé, est un anticorps monoclonal dirigé contre la sous unité p19 spécifique de l’interleukine 23. Une AMM et un remboursement ont été obtenus dans les indications psoriasis, rhumatisme psoriasique, puis dans la maladie de Crohn depuis novembre 2022. Deux études portant sur 1 549 patients ont évalué l’efficacité du risankizumab en induction et en entretien dans la maladie de Crohn. En induction, 35 % des patients à la semaine 8 étaient en rémission contre 19 % dans le groupe placebo et 29 % présentaient une réponse endoscopique (11 % dans le groupe placebo). À la semaine 52, 44 % des patients répondeurs à l’induction étaient en rémission clinique (22 % dans le groupe placebo). L’induction se fait en milieu hospitalier et nécessite 3 perfusions aux semaines 0, 4 et 8, puis le traitement d’entretien est réalisé toutes les 8 semaines par voie sous-cutanée. Pour les injections sous-cutanées, un injecteur corporel spécifique permet de réaliser l’injection d’une cartouche contenant 360 mg de risankizumab. Comme tous les immunomodulateurs, le risankinumab pourrait théoriquement augmenter le risque de cancer. Les patients ayant reçu le risankinumab dans les essais cliniques n’ont pas développé plus de tumeurs malignes que les patients qui recevaient le placebo. Sa tolérance est considérée comme très satisfaisante. Il est, lui aussi, prescrit en monothérapie du fait de sa faible immunogénicité.
Stratégie thérapeutique
La notion de stratégie thérapeutique a été largement étudiée ces dernières années et le concept de « treat to target » a été développé. L’objectif est d’identifier des lésions de MC ainsi que des facteurs de risque associés, de proposer un traitement adapté et enfin d’évaluer l’efficacité de cette stratégie, c’est-à-dire de contrôler si les objectifs du traitement (cibles) ont bien été atteints. En l’absence d’atteinte des objectifs, la thérapeutique sera optimisée ou changée. Ce concept est repris dans les objectifs du consensus STRIDE II (2). Ces objectifs sont définis comme l’obtention d’une rémission clinique associée à une cicatrisation endoscopique, une normalisation de la CRP, une amélioration de la calprotectine fécale mais également à long terme l’absence de handicap et la restauration de la qualité de vie. Cet objectif de « retour à la vie normale » doit être intégré à notre décision et participe pleinement à la question que nous nous posons : quel traitement pour quel patient ?
Pendant de nombreuses années, le seul traitement disponible en seconde ligne de biothérapie était un second anti-TNF. Aujourd’hui, nous avons la possibilité de prescrire l’ensemble des thérapeutiques détaillées précédemment. Le choix du traitement se complexifie du fait de l’augmentation du nombre de traitements disponibles mais cette variété de molécules apporte également plus d’opportunités à nos patients. Trois piliers majeurs vont guider notre décision : l’efficacité, la tolérance mais également l’acceptabilité du patient.

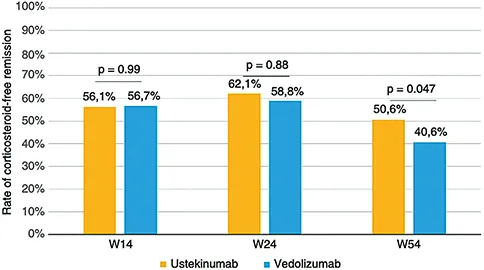
Figure 2 : Rémission clinique sans corticoïdes aux semaines 14, 24 et 48. Comparaison ustekinumab vs. vedolizumab. Manlay L, et al. Aliment Pharmacol Ther. 2021.Jun
Efficacité des traitements
Les études princeps des différentes molécules, randomisées contre placebo, ne semblent pas dégager de supériorité franche d’une molécule vis-à-vis d’une autre. Des méta-analyses en réseaux, des études rétrospectives et maintenant des données prospectives comparatives vont nous permettre d’affiner notre choix thérapeutique.
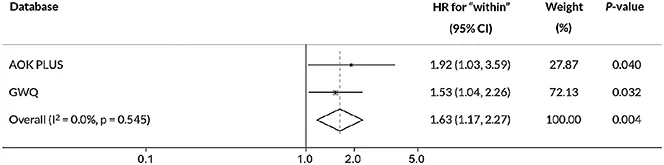
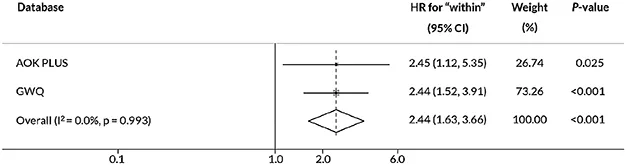
La question du switch pour un deuxième anti-TNF a été posée à plusieurs reprises. La méta analyse de Singh et al. publiée en 2021 identifie les anti-IL-23, ustekinumab et risankisumab, comme une stratégie thérapeutique potentiellement plus efficace chez les patients ayant déjà été exposés à une première ligne d’anti-TNF ; et ce, plus qu’un deuxième anti-TNF (3). Dans une étude rétrospective parue en 2022, Zhuleku et al. confirment qu’un changement de classe thérapeutique pour un traitement par ustekinumab ou vedolizumab est plus efficace qu’un changement pour une deuxième ligne d’anti-TNF (4) (figures 1a et 1b). Au regard de ces différents travaux, il semble préférable de changer de classe thérapeutique après une première ligne par anti-TNF.
Dans les cohortes rétrospectives, il existe une tendance en faveur de l’ustekinumab par rapport au vedolizumab, notamment en termes de persistance thérapeutique. Le groupe national espagnol du GETECCU a publié des données allant dans ce sens en 2023 avec une différence significative en faveur de l’ustekinumab en termes de rémission clinique sans corticoïdes et de survie sans chirurgie (5). Une cohorte rétrospective française publiée en 2021 confirme ces données (6) (figure 2). Cette étude comparait l’efficacité à court et long terme de l’ustekinumab et du vedolizumab chez des patients en échec d’une première ligne d’anti-TNF. La supériorité de l’ustekinumab est particulièrement observée pour plusieurs sous-groupes de patients : en cas de maladie iléale, de forme fistulisante, d’antécédent de lésion ano-périnéale, de chirurgie abdominale et d’âge supérieur à 35 ans.
Un score prédictif de la rémission sans corticoïdes sous vedolizumab (Clinical Decision Support Tool –CDST) a été construit et validé à partir de cinq critères clinico-biologiques : l’absence de résection intestinale antérieure, l’absence d’exposition antérieure à un anti-TNF, l’absence de maladie fistulisante, le taux d’albumine et le taux de protéine C-réactive. La proportion de patients atteignant une rémission clinique et une cicatrisation muqueuse à la semaine 26 était significativement de 38 % et 31 % en cas de score> 19, et plus faible dans le cas contraire (7). Testé dans une cohorte française, des résultats similaires de prédiction de ce score ont été observés. Il a été démontré que ce score n’est pas prédictif de la réponse à l’ustekinumab. Lors de la récente mise à jour des algorithmes décisionnels en France, les experts étaient en faveur de l’utilisation de l’ustekinumab sans que le consensus soit atteint (61 % en faveur, consensus atteint si plus de 66 % d’accord), laissant ainsi une ouverture sur l’utilisation du vedolizumab, particulièrement en cas de CDST> 19. En pratique courante, ce score reste très peu utilisé. (Tableau 1)
Enfin, la première étude face-face dans la MC a été présentée au congrès européen de l’UEGW en octobre 2023. Cette étude appelée SEQUENCE comparait l’efficacité du rizankizumab versus l’ustekinumab chez des patients suivis pour une MC modérée à sévère et en échec d’au moins un anti-TNF. Il a été mis en évidence une non-infériorité du risankizumab concernant la rémission clinique à la semaine 24 et une supériorité du risankizumab concernant la rémission endoscopique à la semaine 48, les 2 objectifs principaux étant ainsi atteints. Ces résultats sont très encourageants et pourraient positionner le risankizumab en seconde ligne de traitement dans la maladie de Crohn.

Figure 1a : Risque de corticothérapie prolongée X 1,6 dans le groupe switch anti-TNF vs. swap de classe ; Zhuleku E, et al. Therap Adv Gastroenterol. 2022

Figure 1b : Risque de 2e changement de biothérapie X 2,4 dans le groupe switch anti-TNF ; Zhuleku E, et al. Therap Adv Gastroenterol. 2022
Tableau 1 : Score d’aide à la décision clinique (CDST)
| Absence d’ATCD de chirurgie abdominale | +2 points |
| Naïf d’anti-TNF | +3 points |
| Absence de maladie fistulisante | +2 points |
| Taux d’albumine | +0,4 points par g/l |
| CRP mg/l | -0,5 points si 3,0-10,0 mg/l -3 points si >10 mg/l |
Tolérance des traitements
À efficacité équivalente, le traitement présentant le moins de risque doit être privilégié. Aucune alerte particulière n’a été actuellement signalée pour l’ustekinumab, le risankizumab et le védolizumab. En revanche, les risques sous anti-TNF sont connus : infections, réactions paradoxales, mélanomes. Les données de tolérance sont donc également en faveur d’un changement de classe thérapeutique après un premier anti-TNF dans la MC.

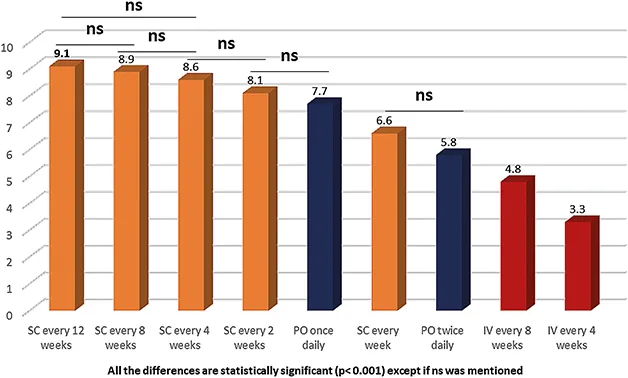
Figure 3 : Acceptabilité de la voie d’administration chez les exposés aux biothérapies SC (aucun traitement IV antérieur), ACCEPT 2, Buisson et al. Inflamm Bowel Dis 2022
Acceptabilité des traitements
Ce paramètre est essentiel, le but étant d’améliorer l’observance du traitement prescrit. En effet, la non-observance est la première cause d’échec thérapeutique. Dans l’étude multicentrique française ACCEPT 2 (8), plus l’espacement entre les injections sous-cutanées était important, meilleur était l’acceptabilité ; ceci inciterait donc à privilégier l’ustekinumab ou le risankizumab, du fait d’un traitement d’entretien SC toutes les 8 semaines. Le nombre de perfusions nécessaires au traitement d’induction doit cependant être pris en compte. (Figure 3).
Perspectives thérapeutiques
La question de la combiothérapie (association de 2 biothérapies) est de plus en plus souvent posée. Des études prospectives sont actuellement en cours pour en évaluer leur efficacité et leur tolérance. Des données rétrospectives devraient nous informer prochainement de la tolérance des stratégies d’association de biothérapies. Les combiothérapies les plus utilisées associent un anti-TNF soit à un anti-Il 23 soit au védolizumab.
La question de l’impact de la séquence thérapeutique sur l’efficacité se pose également. Dans quel ordre prescrire les différentes biothérapies pour être le plus efficace possible avec chaque traitement ? Il est déjà connu que le vedolizumab est moins efficace après une première ligne d’anti-TNF. La question est de savoir pourquoi des traitements ayant un mécanisme d’action différent sont moins efficaces en 2e ligne thérapeutique. Plusieurs hypothèses sont développées : i. l’échec au traitement de première ligne pourrait être un marqueur de sévérité et donc d’échec en 2e ligne, ii. la première ligne pourrait également induire une modification de la réponse immunitaire, impactant alors les lignes suivantes. Des études de positionnement des traitements sont indispensables pour répondre à cette question et améliorer notre stratégie thérapeutique.
Des études futures visant à identifier les facteurs prédictifs de réponse chez un patient donné sont essentielles pour le développement d’une médecine personnalisée dans les MICI.
Il reste à noter que les anti-JAK, à l’exception de l’upadacitinib, n’ont actuellement pas leur place en 2e ligne dans la maladie de Crohn. Un avis favorable au remboursement de l’upadacitinib dans la MC active modérée à sévère chez les patients adultes qui ont une réponse inadéquate, une perte de réponse ou une intolérance aux traitements conventionnels et à au moins un anti-TNF (et lorsque les alternatives sont moins appropriées) a été publié par la Commission de Transparence en novembre 2023.
Conclusion
En dehors d’une perte de réponse par immunisation après l’anti-TNF en première ligne, une séquence anti-TNF, anti IL-23 (en particulier anti Il-23p19) semble la plus favorable, sauf si le CDST est favorable au vedolizumab. L’upadacitinib va devenir également une option disponible dès l’obtention de son remboursement après échec d’un anti-TNF. L’ensemble de ces traitements semble plus efficace lorsque ceux-ci sont administrés précocement. La stratégie thérapeutique doit être adaptée à chaque patient, reposant sur le triptyque efficacité/acceptabilité/tolérance, avec pour objectif le retour à la vie normale. En cas d’échec en première ligne par immunisation, un second anti-TNF peut être prescrit mais il devra systématiquement être associé à un immunosuppresseur.
Des études sont essentielles pour accéder au développement d’une médecine personnalisée dans les MICI. De même, l’impact de la séquence thérapeutique reste inconnu ; des études de positionnement sont actuellement en cours (GETAID) pour répondre à cette question.
Références
- Torres J, et ECCO Guidelines on Therapeutics in Crohn’s Disease: Medical Treatment. J Crohns Colitis. 2020 ;14(1):4-22
- Turner D, et al. Gastroenterology 2021;160:1570–83.
- Singh, et Comparative Efficacy and Safety of Biologic Therapies for Moderate-to-Severe Crohn’s Disease: A Systematic Review and Network Meta-Analysis. Lancet Gastroenterol Hepatol. 2021 December ; 6(12): 1002–1014.
- Zhuleku, et al. Real-world outcomes associated with switching to anti-TNFs versus other biologics in Crohn’s Disease patients: A retrospective analysis using German claims data. Ther Adv Gastroenterol 2022, Vol. 15: 1–13
- García MJ, et al. Comparative Study Of The Effectiveness Of Vedolizumab Versus Ustekinumab After Anti-Tnf Failure In Crohn’s Disease (Versus-Cd): Data From Eneida Registry. J Crohns Colitis. 2023;Jul 31;jjad124.
- Manlay L, et al. Comparison of short- and long-term effectiveness between ustekinumab and vedolizumab in patients with Crohn’s disease refractory to anti-tumour necrosis factor therapy. Aliment Pharmacol Ther. 2021;Jun;53(12):1289-99.
- Dulai PS, et al. Development and Validation of a Scoring System to Predict Outcomes of Vedolizumab Treatment in Patients With Crohn’s Disease. Gastroenterology. 2018;Sep;155(3):687-95.e10.
- Buisson, et al. Comparative Acceptability of Therapeutic Maintenance Regimens in Patients With Inflammatory Bowel Disease: Results From the Nationwide ACCEPT2 Study. Inflamm Bowel Dis 2022