Liens d’intérêt
L’auteur déclare avoir reçu des honoraires de consultance de la part d’Abbvie et Janssen
Mots-clés
Maladie de Crohn ; Récidive post-opératoire ; Score de Rutgeerts
Abréviations
TNF : Tumor Necrosis Factor
Introduction
La résection iléo-colique est recommandée en cas de maladie de Crohn iléale, localisation la plus fréquente de la maladie de Crohn, qu’elle soit compliquée ou en alternative au traitement médical en cas de maladie peu étendue et de phénotype inflammatoire (1). Bien que le recours à la chirurgie ait diminué depuis le début des années 2000, il est actuellement estimé qu’environ un patient sur six a besoin d’une résection iléo-colique dans les cinq ans suivant le diagnostic de maladie de Crohn contre plus de 50 % dans les années 1990 (2). Outre le recours classique à la chirurgie en cas de maladie de Crohn compliquée d’une fistule, d’un abcès ou d’une sténose, les données de l’essai LIR!C suggèrent que la résection iléo-colique est une alternative raisonnable à l’infliximab en première intention chez les patients atteints d’une maladie de Crohn iléo-cæcale inflammatoire courte (< 40 cm) (3). Néanmoins, la chirurgie, même lorsqu’elle permet la résection de tous les segments macroscopiquement atteints, ne guérit pas la maladie de Crohn et la majorité des patients finit par connaître une récidive (4).
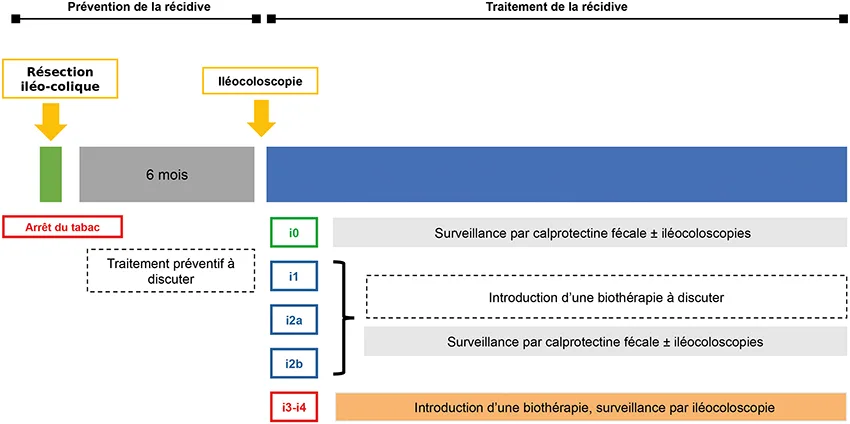
Les travaux fondateurs de l’équipe de Louvain, menés par Paul Rutgeerts, dans les années 1990 ont montré que la récidive post-opératoire de la maladie de Crohn survenait de façon quasi systématique au niveau de l’anastomose iléo-colique et selon une séquence récidive microscopique – endoscopique – clinique, les signes endoscopiques précédant les symptômes de quelques mois, voire années selon leur intensité (5). Au cours de la prise en charge d’un patient opéré, il faut donc différencier deux problématiques distinctes : la prévention de la récidive dans les mois suivant la chirurgie – éviter que l’inflammation microscopique, puis endoscopique se réinstalle – et le traitement de la récidive patente, endoscopique avant l’apparition de symptômes ou clinique chez un patient déjà symptomatique (figure 1). L’objectif à long terme est de limiter le risque de récidive post-opératoire chirurgicale, c’est-à-dire nécessitant une nouvelle résection iléo-colique.

Figure 1 : Représentation des deux phases et des stratégies possibles après une résection iléocolique en termes de prévention et de traitement de la récidive de maladie de Crohn
Nous verrons dans cette revue quels sont les facteurs de risque de récidive post-opératoire, quels sont les outils permettant de diagnostiquer la récidive post-opératoire, quelles stratégies peuvent être utilisées en prévention puis en traitement de la récidive et comment suivre les patients après une résection iléo-colique.
Facteurs de risque de récidive post-opératoire
Facteurs de risque pré-opératoires
Certaines caractéristiques de la maladie de Crohn, telles qu’un phénotype fistulisant ou un autre antécédent de résection iléo-colique, ont été identifiées dans des études rétrospectives comme des facteurs de risque potentiels de récidive post-opératoire et sont incluses dans les recommandations de l’European Crohn’s and Colitis Organization (1, 6). Toutefois, elles n’ont jamais été confirmées dans les études prospectives et des données récentes viennent directement remettre en cause leur validité (7). Ainsi, Joustra et al. ont analysé une cohorte rétrospective multicentrique comprenant 142 patients ayant subi une résection iléo-colique. Aucune association significative avec la récidive post-opératoire endoscopique n’a été observée lors de la comparaison entre les patients à haut risque et à faible risque, selon les définitions données par les recommandations européennes, américaines et britanniques (8). De façon similaire, dans une récente étude de cohorte néerlandaise prospective multicentrique incluant 213 patients après une résection iléo-colique, à six mois, des taux similaires de récidive post-opératoire endoscopique ont été observés chez ceux considérés à faible risque par rapport aux patients à haut risque (9).
Des données beaucoup plus robustes plaident en faveur d’un lien entre tabagisme actif et récidive post-opératoire. Une méta-analyse regroupant les données de 2 962 patients a conclu qu’il doublait le risque de récidive post-opératoire clinique et chirurgicale (10). Le meilleur moment pour arrêter de fumer afin d’obtenir un bénéfice sur le risque de récidive post-opératoire n’a pas encore été clairement établi, car les effets du tabagisme pourraient persister plusieurs mois. Dans le contexte spécifique de la maladie de Crohn opérée, une seule étude, menée par le groupe français REMIND, a abordé les mécanismes potentiels de l’effet délétère du tabagisme et met en évidence un possible rôle des lymphocytes T (11). De plus, les fumeurs ont un risque accru de complications après une chirurgie colorectale pour d’autres indications (12). Par conséquent, l’effet néfaste du tabagisme sur la récidive post-opératoire pourrait également être en partie lié à une cicatrisation anastomotique moins efficace.
Facteurs de risques opératoires
Au cours des 20 dernières années, les chirurgiens se sont attelés à développer des stratégies visant à réduire la récidive post-opératoire, en se concentrant notamment sur la configuration de l’anastomose iléo-colique et les marges de résection.
Type d’anastomose iléo-colique
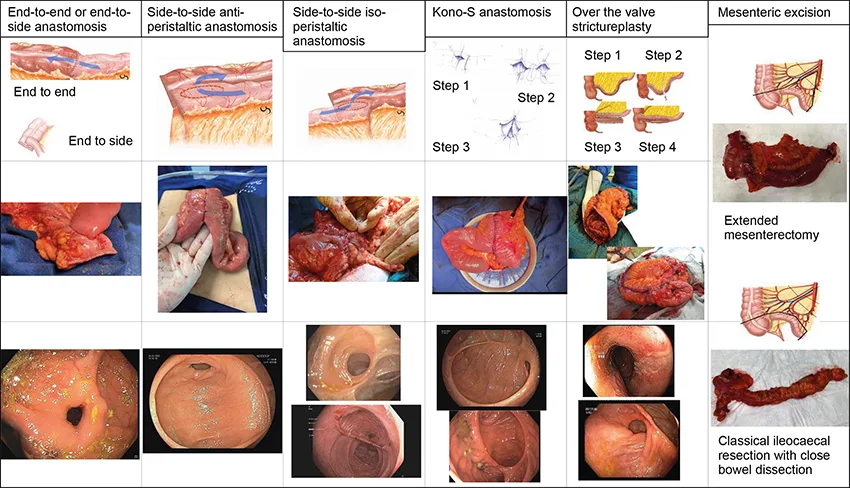
Historiquement, les anastomoses iléo-coliques étaient termino-terminales ou termino-latérales manuelles. À partir des années 2000, s’est développée l’anastomose latéro-latérale, mécanique, anti-péristaltique ou isopéristaltique (figure 2). Dans la méta-analyse la plus récente, publiée en 2018, Feng et al. ont comparé simultanément plusieurs types d’anastomoses (13). Les critères principaux utilisés étaient la récidive post-opératoire endoscopique, clinique et chirurgicale, soit individuellement, soit en combinaison. Cependant, il existait une hétérogénéité dans la définition de la récidive, la prise en charge médicale post-opératoire et la durée du suivi entre les études. Néanmoins, ils pouvaient conclure que l’anastomose latéro-latérale était plus à même de réduire le risque de récidive post-opératoire clinique et chirurgicale. L’hypothèse principale est celle d’un bénéfice lié au calibre plus important de la jonction iléo-colique avec l’anastomose latéro-latérale, prévenant la stase fécale qui pourrait entraîner une prolifération bactérienne et une dysrégulation de la réponse immunitaire (14).
Il existe également probablement une différence de cicatrisation entre les anastomoses manuelles et les anastomoses mécaniques. D’après une étude récente où des vidéos d’endoscopie six mois après résection iléo-colique ont été relues, à la fois pour des patients atteints de maladie de Crohn et des patients opérés pour un cancer colorectal, des ulcérations au niveau de la ligne d’agrafage mécanique étaient mises en évidence chez plus de 75 % des patients dans les deux groupes. Ces lésions pourraient donc être liées à des phénomènes cicatriciels et ischémiques notamment sous l’agrafe et indépendants d’une récidive de la maladie de Crohn (15).

Figure 2 : Description des différents types d’anastomoses et de techniques chirurgicales développées pour diminuer le risque de récidive post-opératoire
Ligne supérieure : représentation schématique, ligne du milieu : vue chirurgicale ; ligne inférieure : vue endoscopique. Tiré de (7)
Anastomose Kono-S
Décrite pour la première fois en 2011, l’anastomose Kono-S est une anastomose hybride, combinant une approche manuelle et agrafée, basée sur le concept d’exclusion mésentérique (16). Un des principes sous-tendant cette technique est qu’une anastomose large sans un cul-de-sac tel que celui d’une anastomose latéro-latérale isopéristaltique, réduit le risque de stase fécale et de prolifération bactérienne mentionnés plus haut. Dans le seul essai randomisé publié à ce jour, 79 patients atteints de maladie de Crohn iléo-colique ont été opérés soit avec une anastomose Kono-S soit une anastomose latéro-latérale par agrafage. Le critère principal d’évaluation, la récidive post-opératoire à 6 mois, s’est avéré significativement plus faible dans le groupe Kono-S (23 % contre 63 %, p< 0,001). Une récidive post-opératoire sévère en endoscopie (score de Rutgeerts≥ i3) a été observée chez 14 % des patients du groupe Kono-S contre 35 % des patients du groupe anastomose latéro-latérale (p= 0,03) (17). La surévaluation de la récidive post-opératoire endoscopique dans les anastomoses latéro-latérales lors de l’évaluation postopératoire (les endoscopistes n’étaient pas aveugles quant aux groupes de traitement) aurait potentiellement pu influencer les résultats rapportés, en particulier en raison de la nature mécanique de l’anastomose latéro-latérale souvent associée à des ulcérations transitoires (15). Cependant, étant donné les limites décrites ci-dessus, les résultats de deux grandes études multicentriques en cours sont très attendus (NIHR131988 et NCT03256240). S’inspirant de la théorie selon laquelle le mésentère peut influencer la pathogenèse de la maladie de Crohn, une approche chirurgicale combinant une anastomose Kono-S et une excision mésentérique étendue est également actuellement en cours d’étude dans l’essai MEErKAT, un essai multicentrique de supériorité, randomisé et en ouvert au Royaume-Uni.
Les marges de résection microscopiques
Plusieurs études ont montré que la présence de stigmates microscopiques de maladie de Crohn au niveau des marges de résection sur la pièce opératoire était associée à un risque plus élevé de récidive post-opératoire (18, 19). Néanmoins, dans la pratique chirurgicale de routine, ces résultats ne plaident pas en faveur de la réalisation d’une histologie per-opératoire ou de résection très à distance des lésions comme ce qui est préconisé en oncologie. L’objectif demeure de préserver le maximum de longueur d’intestin grêle chez des patients qui connaîtront potentiellement plusieurs chirurgies dans leur vie. L’atteinte inflammatoire des plexus sur la pièce opératoire, la plexite, a également été identifiée comme facteur de risque de récidive. Cependant, la littérature à ce sujet est très hétérogène en ce qui concerne les définitions de la plexite, les techniques d’évaluation (par exemple, la coloration à l’hématoxyline-éosine par rapport aux colorations spécifiques) et les critères utilisés (20, 21). Il reste encore difficile de conclure si la plexite pourrait être le reflet d’une inflammation microscopique au niveau de la marge de résection ou un facteur de risque indépendant.
Pour l’instant, il n’est pas recommandé de traiter les patients de façon préventive en fonction de la présence d’inflammation microscopique sur les marges de résection, mais cette attitude pourrait se modifier en fonction de l’avancée des études en cours.
Quelle place pour le microbiote ?
Dans les années 1990, l’équipe de Louvain avait pu montrer que la récidive était dépendante du flux fécal passant à travers l’anastomose, et qu’elle ne survenait pas chez les patients laissés en iléostomie (22). Depuis, le rôle du contenu luminal dans la physiopathologie de la récidive post- opératoire continue d’être étudié de manière approfondie. Cependant, les mécanismes exacts demeurent énigmatiques. La composition du microbiote iléal au moment de la chirurgie est reconnue comme un des acteurs clés de la récidive (23). Néanmoins, davantage de recherche est nécessaire avant que des facteurs de risque spécifiques, par profil microbien au cours de la chirurgie par exemple, puissent être intégrés à la pratique clinique.
Diagnostic de la récidive post-opératoire : outils et scores validés
Attention à la diarrhée post-opératoire !
Après une résection iléo-colique, les patients peuvent présenter des symptômes (diarrhée, douleur abdominale) mimant une récidive de la maladie, mais plutôt liés à la résection de la valvule de Bauhin, à une prolifération bactérienne excessive, à une malabsorption des sels biliaires ou à une hypersensibilité viscérale post-chirurgicale sans qu’il y ait de lésions spécifiques de maladie de Crohn. Par conséquent, la définition de la récidive clinique post-opératoire reste débattue, car se fier uniquement aux symptômes pour définir la récidive expose les patients au risque de sur-traitement. La récidive clinique post-opératoire doit donc être définie comme la combinaison de symptômes évocateurs et de preuves morphologiques (endoscopiques et/ou radiologiques) d’inflammation au niveau du site de l’anastomose iléo-colique ou du néo-iléon terminal (24).
Diagnostic endoscopique
Le score de Rutgeerts

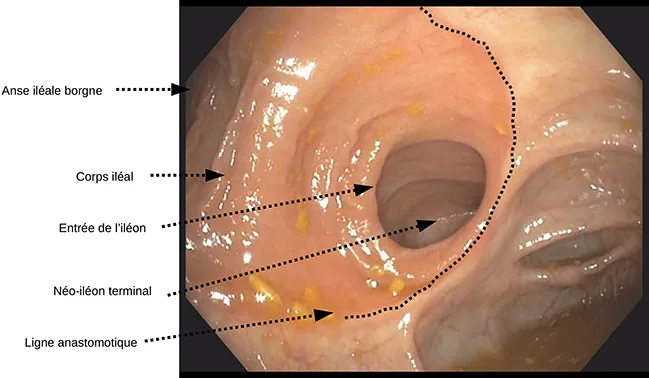
Figure 3 : Zones anatomiques d’une anastomose latéro-latérale utilisées pour coter le score de Rutgeerts
Tableau 1 : Score de Rutgeerts modifié adapté aux anastomoses latéro-latérales [d’après (26)]
| Score | Description |
| i0 | Aucune lésion dans le néo-iléon terminal, la ligne anastomotique, l’entrée de l’iléon ou le corps iléal. |
| i1 | Moins de 5 lésions aphtoïdes dans le néo-iléon terminal, l’entrée de l’iléon ou le corps iléal avec une muqueuse intercalaire normale. |
| i2a | Lésions de la ligne anastomotique avec ou sans moins de 5 lésions aphtoïdes dans le néo-iléon terminal, l’entrée de l’iléon ou le corps iléal avec une muqueuse intercalaire normale. |
| i2b | 5 lésions aphtoïdes ou plus, ou ulcérations plus importantes, avec une muqueuse intercalaire normale dans le néo-iléon terminal, l’entrée de l’iléon ou le corps iléal avec ou sans lésions de la ligne anastomotique. |
| i3 | Lésions aphtoïdes, quel que soit leur nombre, au sein d’une muqueuse inflammatoire de façon diffuse dans le néo-iléon terminal, l’entrée de l’iléon ou le corps iléal. |
| i4 | Ulcères plus volumineux au sein d’une muqueuse inflammatoire de façon diffuse ou nodules ou sténose infranchissable dans le néo-iléon terminal, l’entrée de l’iléon ou le corps iléal. |
En 1990, Rutgeerts et al. ont montré que la gravité des lésions endoscopiques identifiées au niveau du néo-iléon terminal et au niveau de l’anastomose iléo-colique dans l’année suivant la chirurgie permettait de prédire la survenue ultérieure d’une récidive clinique (5). Bien que non formellement validé, le score de récidive endoscopique post-opératoire développé au cours de cette étude, également connu sous le nom de score de Rutgeerts, a été largement adopté dans la pratique clinique et représente actuellement l’outil de référence. Ce score se compose de cinq niveaux progressifs de gravité : i0 – pas de lésions ; i1 – ≤ 5 lésions aphtoïdes dans le néo-iléon terminal ; i2 – > 5 lésions aphtoïdes ou lésions plus importantes dans le néo-iléon terminal avec une muqueuse normale entre les lésions, ou lésions confinées à l’anastomose iléo-colique ; i3 – iléite aphtoïde diffuse avec une muqueuse intercalaire inflammatoire ; i4 – inflammation diffuse du néo-iléon terminal avec ulcères plus importants que des aphtes, nodules et/ou un sténose.
Limites du score de Rutgeerts
Malheureusement, le score de Rutgeerts présente certaines limites. Comme mentionné précédemment, il n’a jamais été formellement validé. Sa reproductibilité inter-observateur est seulement modérée (25). De plus, le score de Rutgeerts a été initialement développé pour l’évaluation d’une anastomose iléo-colique termino-terminale. Les nouvelles techniques s’accompagnent de la présence de nouveaux repères anatomiques qui ne permettent pas de coter la récidive de façon fiable en utilisant ce score dans sa forme actuelle. Une définition plus précise de chacune des catégories du score adaptée notamment aux anastomoses latéro-latérales a donc été proposée récemment (26) (figures 2, 3 et 4, tableau 1). Elle s’appuie sur la caractérisation de différentes zones de l’anse iléale accolée latéralement au colon : la partie borgne à proprement parler ; à l’opposé, l’entrée de l’iléon et entre les deux, le corps iléal. L’entrée de l’iléon et le corps iléal sont considérés comme faisant partie du néo-iléon terminal alors que les lésions de l’anse borgne ne sont pas prises en compte pour la cotation du score. Ces zones iléales sont à distinguer de la ligne anastomotique, terme choisi pour être plus précis que celui d’anastomose, et qui correspond strictement à la jonction iléo-colique formée par le chirurgien manuellement ou par agrafage.
Rappelons également qu’initialement, le score de Rutgeerts regroupait les lésions légères au niveau de l’anastomose et les lésions multiples mais isolées du néo-iléon terminal dans la catégorie i2. Par conséquent, une distinction des résultats i2 en i2a (lésions anastomotiques) et i2b (> 5 ulcères aphtoïdes ou lésions plus importantes du néo-iléon terminal avec une muqueuse normale entre les lésions) a été suggérée (27). Par la suite, plusieurs articles aux résultats discordants ont été publiés pour étudier la possibilité d’un pronostic différent entre les lésions i2a et i2b. Ainsi, dans une cohorte franco-belge rétrospective incluant 180 patients avec un score i2 dans l’année suivant la chirurgie, aucune différence dans les taux de récidive clinique n’était retrouvée (28). À l’inverse, Ollech et al. ont rapporté que des patients i2b (n= 25) présentaient un risque plus élevé de progression endoscopique vers i3-i4 et de nouvelle résection iléo-colique que des patients i2a (n= 40) (29). Cette observation a ensuite été confirmée par le groupe REMIND (30) mais une méta-analyse récente sur données individuelles regroupant 400 patients n’a pas mis en évidence de différence en termes de risque de récidive clinique et chirurgicale entre les patients i2a et i2b (31). Du fait des difficultés à repérer les zones anatomiques iléales en fonction des anastomoses, il est possible que dans certaines études, les lésions i2a et i2b aient été définies de façon différente. Le score de Rutgeerts est donc l’outil de référence mais comme nous le verrons plus bas, il ne permet pas de guider efficacement la stratégie thérapeutique, notamment en cas de récidive modérée.
Diagnostic biochimique : la calprotectine fécale
Dans une cohorte espagnole de 119 patients, la valeur de la calprotectine fécale réalisée au même moment qu’une endoscopie ayant pour but de diagnostiquer une récidive post-opératoire était fortement corrélée au résultat de cette endoscopie (32). Lorsque la calprotectine fécale était utilisée avec un seuil>100 µg/g et combinée à un taux de C-Reactive Proteine sérique> 5 mg/L, la valeur prédictive négative était de 81 % pour éliminer la récidive endoscopique. Dans l’essai contrôlé randomisé POCER, la valeur moyenne de la calprotectine fécale à six mois pour les patients en rémission endoscopique était de 72 µg/g, tandis qu’elle était de 275 µg/g pour les patients avec une récidive endoscopique (score de Rutgeerts≥ i2) (33). Une bonne valeur prédictive négative a été retrouvée dans d’autres cohortes prospectives, concluant qu’un seuil de 100 µg/g pourrait être cliniquement utile pour déterminer la probabilité de rémission endoscopique (34). Néanmoins, les seuils utilisés sont très hétérogènes en fonction des études, certaines ne retrouvant pas d’association claire entre endoscopie et calprotectine fécale (35) et il est donc peu probable qu’une valeur seuil unique soit optimale pour distinguer de manière précise la récidive endoscopique post-opératoire chez chaque patient. De façon pragmatique, la calprotectine fécale doit probablement être utilisée dans le suivi postopératoire en utilisant chaque patient comme son propre témoin, c’est-à-dire en évaluant la variation par rapport à la calprotectine fécale de base, mesurée au moment de la première coloscopie d’évaluation.
Diagnostic radiologique : place de l’échographie et de l’IRM
L’iléocoloscopie est l’outil de référence pour le diagnostic de la récidive post-opératoire. Néanmoins, d’après les recommandations ECCO, l’échographie abdominale et l’IRM peuvent être utilisées également (36). Ces techniques d’imagerie qui permettent de mettre en évidence des anomalies bien corrélées à la présence de lésions endoscopiques trouvent toute leur place en complément de l’endoscopie dans l’année suivant la chirurgie, et comme alternative au cours des années suivantes. L’échographie est surtout utile pour mettre en évidence une récidive sévère. Ainsi, une méta-analyse a montré que la présence d’un épaississement pariétal iléal supérieur à 5,5 mm en échographie était associé à un score de Rutgeerts i3 ou i4 avec une spécificité de 98 % (37). En cas de récidive sévère à l’échographie, on pourrait éventuellement se passer de l’endoscopie. En revanche, la normalité de l’échographie ne présume pas de l’absence de lésions endoscopiques et il faudra dans ce cas-là la coupler avec un dosage de calprotectine fécale pour espérer égaler les performances diagnostiques de la coloscopie. Néanmoins, cette attitude doit encore être validée dans des essais prospectifs (24). L’échographie est très bien acceptée par les patients (38), mais pour l’instant, peu de centres disposent de cette expertise en France. Une réflexion pour déployer des formations est actuellement en cours et son utilisation dans la prise en charge des patients atteints de maladie de Crohn devrait se généraliser dans les années à venir. En IRM, il existe également des critères validés permettant de définir des lésions associées avec une récidive endoscopique mais avec une spécificité plus basse que l’échographie, à 55 % (39). Cette technique d’imagerie est également moins bien acceptée par les patients (38). Elle est donc surtout utile pour évaluer la longueur de l’atteinte en cas de sténose infranchissable à l’endoscopie, avant de discuter une éventuelle dilatation, ou rechercher des complications en cas de récidive sévère ou avant une nouvelle prise en charge chirurgicale (24).

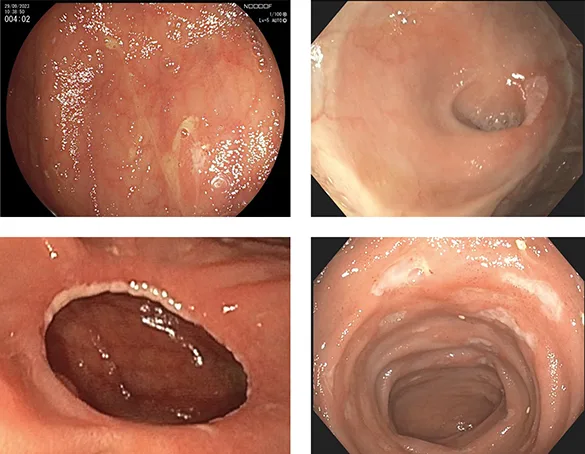
Figure 4 : Lésions élémentaires visibles en cas de récidive endoscopique de la maladie de Crohn.
En haut à gauche, deux ulcérations aphtoides du corps iléal au sein d’une muqueuse normale. En haut à droite, un ulcère isolé de l’entrée de l’iléon entouré d’une muqueuse normale. En bas à gauche, ulcération isolée de la ligne anastomotique. En bas à droite, ulcères du néo-iléon terminal au sein d’une muqueuse érythémateuse.
Stratégies thérapeutiques en prévention de la récidive
Sevrage tabagique
Comme indiqué plus haut, le facteur de risque de récidive le mieux décrit est le tabagisme. Malheureusement, les patients sont peu sensibilisés aux avantages de l’arrêt du tabac (40) et les mesures pour aider les patients à arrêter de fumer sont sous-utilisées (41). Cependant, lorsque des mesures actives sont mises en œuvre, elles sont efficaces pour une partie des patients. Ainsi, dans l’étude espagnole multicentrique TABACROHN incluant plus de 400 fumeurs atteints de maladie de Crohn, lorsque des informations sur le tabagisme et des conseils étaient donnés pour le sevrage, 31 % des patients arrêtaient de fumer, dont 23 % n’avaient pas repris après un suivi de 18 mois (42). Il existe un réseau national de services d’aide au sevrage tabagique, en ville ou hospitaliers, probablement sous-utilisé par la plupart des services de gastro-entérologie. Lors de la prise en charge d’un patient fumeur atteint d’une maladie de Crohn, il est essentiel pour le gastro-entérologue d’insister sur la nécessité du sevrage tabagique, notamment en cas de chirurgie. Il s’agit d’une première étape indispensable pour prévenir la récidive, avant toute discussion thérapeutique.
D’autres moyens non médicamenteux tels que les probiotiques, la curcumine ou la vitamine D ont été étudiés mais aucun ne s’est révélé efficace pour prévenir la récidive (43).
Prévention médicamenteuse
Lorsque l’on parle de prévenir la récidive post-opératoire, l’idée est d’éviter l’apparition de nouvelles lésions endoscopiques, qui peuvent se développer en quelques semaines. Par conséquent, ce traitement préventif, s’il est indiqué, doit être commencé dans les premières semaines suivant la chirurgie. Sont exclus de ce raisonnement les patients dont l’ensemble des segments inflammatoires n’ont pu être réséqués, ceux avec une maladie périnéale active ou des atteintes extra-digestives nécessitant une biothérapie telles qu’une spondyloarthropathie. Dans ces cas-là, la résection n’est pas considérée comme « curative » et un traitement doit être initié ou poursuivi en post-opératoire immédiat. Pour le reste des patients, l’intérêt d’un traitement post-opératoire immédiat reste débattu et nous présenterons ici les principaux éléments qui peuvent guider la décision et les molécules qui peuvent être utilisées dans cette indication (figure 1).
Trouver un équilibre entre sur- et sous-traiter
Cette stratégie repose sur le fait que jusqu’à 70 à 80 % des patients développeront des lésions endoscopiques dans les 18 mois, ce qui est clairement associé à un risque accru de récidive clinique et à un risque de nouvelle complication de la maladie puisque la plupart des patients ont été opérés pour une maladie de Crohn compliquée (5). Néanmoins, cette stratégie conduit à sur-traiter les 20 à 30 % des patients qui n’auraient pas développé de récidive post-opératoire endoscopique sans traitement, et les 40 % à 50 % des patients qui n’auraient développé que des lésions intermédiaires (Rutgeerts i1-i2) associées à un faible risque de récidive clinique et chirurgicale. Chez ces patients, le risque d’effets secondaires liés aux traitements pourrait l’emporter sur leurs éventuels avantages préventifs (43). Pour éviter le sur-traitement et tirer parti de la rémission « profonde » induite par une résection curative, une surveillance endoscopique à six mois, sans traitement post-opératoire immédiat, mais avec adaptation du traitement en fonction des lésions endoscopiques a donc été proposée. Théoriquement, il existe un risque qu’une partie des patients ayant déjà des lésions installées à six mois ne s’améliorent pas sous traitement et développent ultérieurement une récidive clinique et chirurgicale. Les données actuellement disponibles plaident plutôt en faveur de cette approche basée sur l’endoscopie. Au cours d’un essai dans lequel des patients ont été randomisés pour une prévention systématique avec de l’azathioprine ou un traitement basé sur l’endoscopie à six mois et à un an, aucune différence n’a été observée en termes de récidive endoscopique 18 mois après la chirurgie (44). Dans une étude rétrospective multicentrique néerlandaise portant sur 376 patients, l’approche basée sur l’endoscopie était associée à plus de récidives endoscopiques au cours de la première année par rapport à une prophylaxie systématique comme attendu, mais pas à un risque accru de récidive clinique dans les trois ans (45).
L’idéal serait de pouvoir identifier les patients à haut risque de récidive post-opératoire et de n’utiliser une prévention systématique que chez eux. Néanmoins, nous avons vu plus haut que nous manquions de facteurs de risque fiables, en dehors du tabagisme actif. Chez les patients fumeurs qui n’envisagent pas d’arrêter de fumer après la chirurgie, même après information et prise en charge tabacologique spécialisée, il est probablement raisonnable d’introduire un traitement en post-opératoire immédiat. Pour les autres patients, les avantages du traitement post-opératoire sont moins clairs et doivent se discuter en réunion de concertation multi-disciplinaire et avec le patient. L’étude SOPRANO-CD actuellement en cours en Belgique et en Italie aborde spécifiquement cette question en randomisant les patients pour recevoir une prophylaxie systématique avec une biothérapie ou être traités selon une approche guidée par l’endoscopie (NCT05169593). Ses résultats permettront de mieux guider nos décisions dans quelques années. Pour l’instant, les traitements les mieux étudiés en post-opératoires immédiats sont l’azathioprine et les anti-Tumor Necrosis Factor (TNF).
Azathioprine
L’efficacité des thiopurines (azathioprine, mercaptopurine) pour prévenir la récidive endoscopique post-opératoire a été évaluée dans plusieurs essais contrôlés randomisés. La méta-analyse Cochrane la plus récente a conclu que les thiopurines sont plus efficaces que le placebo pour prévenir la récidive post-opératoire clinique après 12 à 36 mois de suivi (51 % vs. 64 %, RR 0,79, IC à 95 % 0,67–0,92) (46). Cependant, aucune différence significative entre les thiopurines et le placebo n’a pu être observée en ce qui concerne la récidive endoscopique.
Anti-TNF
Quelques études prospectives et un essai randomisé en ouvert avec un effectif relativement faible ont suggéré un bénéfice potentiel des anti-TNF dans la prévention de la récidive post-opératoire (47). L’étude PREVENT, un essai de grande ampleur, randomisé, en double aveugle, contre placebo évaluant l’infliximab postopératoire chez 297 patients atteints de la maladie de Crohn, n’a pas réussi à démontrer une réduction statistiquement significative de la récidive clinique à 76 semaines, mais a montré une réduction claire de la récidive endoscopique (30,6 % vs. 60,0 %, p<0,001) (48). Il est important de noter que les patients ont commencé immédiatement après la chirurgie l’infliximab à 5 mg/kg toutes les huit semaines sans induction et que les taux de rechute clinique observés étaient assez faibles, bien que les patients aient été inclus en fonction de la présence d’au moins un facteur de risque de récidive.
Pour l’adalimumab, à ce jour, aucun essai contrôlé randomisé contre placebo n’a été réalisé. Un essai randomisé italien de faible effectif a montré un taux de récidive endoscopique significativement plus faible chez les patients traités par adalimumab (6 %) par rapport à l’azathioprine (65 % ; OR=0,036 (IC à 95 % 0,004–0,347)). Dans un autre essai randomisé espagnol comparant l’adalimumab et l’azathioprine pour la prévention de la récidive post-opératoire chez 84 patients, aucune différence n’a été observée dans le taux de récidive endoscopique ou de récidive endoscopique sévère entre les deux groupes (49). Récemment, une méta-analyse sur les données individuelles de 645 participants de six essais contrôlés originaux a démontré un effet supérieur des anti-TNF par rapport aux thiopurines en ce qui concerne la récidive clinique (RR 0,50 ; IC à 95 % 0,26–0,96), la récidive endoscopique (RR 0,52 ; IC à 95 % 0,33–0,80) et la récidive endoscopique sévère (RR, 0,41 ; IC à 95 %, 0,21–0,79) (50). Il semble donc que lorsqu’un traitement préventif immédiat doit être introduit en post-opératoire, un anti-TNF soit à préférer à l’azathioprine (43). Peu de données permettent de savoir si un anti-TNF sera efficace pour prévenir la récidive si le patient a été traité par anti-TNF, le même ou un autre, avant la chirurgie.
Autres biothérapies
Cette année, les résultats préliminaires d’un essai randomisé ont montré que le vedolizumab était supérieur au placebo pour prévenir la récidive post-opératoire endoscopique à six mois mais les résultats ne sont pas encore publiés dans leur version intégrale. Des données rétrospectives ont montré que l’ustekinumab pourrait être efficace pour prévenir la récidive post-opératoire (51). Aucune étude prospective n’a été réalisée dans cette indication. Le choix de la biothérapie doit donc se discuter en réunion de concertation multidisciplinaire et avec le patient, en fonction de l’exposition antérieure aux biothérapies, en tenant compte du faible niveau de preuves décrit plus haut.
Stratégies thérapeutiques en cas de récidive et modalités de surveillance
L’essentiel : une iléo-coloscopie six mois après la chirurgie
Il est recommandé de réaliser une iléo-coloscopie six à douze mois après une résection iléo-colique pour évaluer la récidive endoscopique post- opératoire (1). Cette recommandation se base notamment sur les résultats de l’essai randomisé POCER, un essai fondateur dans la prise en charge de la maladie de Crohn opérée. Dans cette étude, 174 patients qui avaient eu une résection iléo-colique et avaient éventuellement reçu une prophylaxie immédiate par azathioprine ou adalimumab en cas de facteur de risque, ont été randomisés soit pour réaliser une endoscopie six mois après la chirurgie (« stratégie active ») soit pour un suivi clinique uniquement (« stratégie standard ») (33). La décision de traitement basée sur l’endoscopie postopératoire s’est avérée supérieure aux soins guidés par la clinique, puisqu’un taux de récidive endoscopique de 49 % était retrouvé 18 mois après la chirurgie dans le groupe « stratégie active », contre 67 % dans le groupe « stratégie standard » (p= 0,03). Cette étude fournit des preuves convaincantes qu’une évaluation endoscopique précoce est cruciale pour une adaptation rapide du traitement en cas de récidive indépendamment de l’utilisation d’une prophylaxie immédiate après la chirurgie. Nous allons voir ici quelle attitude adopter immédiatement et pour le suivi en fonction des résultats de cette endoscopie à six mois (figure 1).
Que faire en cas d’absence de récidive à six mois ?
Lorsqu’il n’y a pas de lésion à la première endoscopie (score de Rutgeerts i0), il est aisé de comprendre qu’il n’est pas recommandé d’introduire un traitement (43). Ce sont les modalités de suivi qui restent plus floues. Malgré les résultats de l’essai POCER, les données sont actuellement insuffisantes pour décider du moment opportun pour réaliser la deuxième évaluation endoscopique, voire pour éviter totalement de refaire une endoscopie. Par conséquent, la programmation des examens endoscopiques de suivi peut se faire de façon flexible et individualisée en fonction des symptômes du patient, et surtout de la surveillance non invasive par calprotectine fécale (24). Dans une enquête récente en Europe, 90 % des gastro-entérologues participants ont déclaré utiliser la calprotectine fécale comme outil de suivi des patients en rémission endoscopique lors de la première évaluation (52). Dans cette indication, il peut être intéressant de doser la calprotectine fécale au moment de la première endoscopie pour avoir un niveau de référence, puis de répéter le dosage tous les trois à six mois et en fonction des symptômes du patient. En cas d’élévation de la calprotectine fécale par rapport au niveau de base, il faudra alors réaliser une endoscopie pour grader la sévérité de la récidive.
Que faire en cas de récidive sévère ?
En cas de récidive sévère, c’est-à-dire en présence d’une inflammation diffuse d’un segment du néo-iléon terminal, associée à des ulcères aphtoïdes (Rutgeerts i3) ou des ulcères plus volumineux, voire une sténose (Rutgeerts i4), il est largement admis qu’un traitement spécifique doit être débuté (43). Les données sur le traitement médical de la récidive endoscopique post-opératoire sont pourtant rares et de qualité limitée. La grande hétérogénéité dans les définitions de la récidive et de la réponse au traitement complique davantage l’interprétation des études disponibles. Certaines incluent les patients ayant une récidive i2b, voire i2a alors que d’autres ne portent que sur les patients avec récidive sévère. La plupart des données actuelles portent sur les immunosuppresseurs et les anti-TNF.
Concernant les immunosuppresseurs, dans l’essai clinique sus-mentionné comparant l’efficacité de l’azathioprine en post-opératoire immédiat à son introduction après l’endoscopie, la rémission endoscopique était obtenue à la semaine 102 chez 42 % des patients qui avaient débuté le traitement aux semaines 26 ou 52 en raison d’une récidive endoscopique (n=31) (44). Pour ce qui est des anti-TNF, dans l’étude POCER, 33 patients du groupe « stratégie active » qui avaient initialement été traités par azathioprine ont été traité par adalimumab du fait d’une récidive endoscopique à six mois (33). La rémission endoscopique à 18 mois a été atteinte chez 13 sur 33 patients (39 %).
Dans la plus grande série rétrospective sur l’utilisation des anti-TNF (83 infliximab et 96 adalimumab) pour le traitement de la récidive endoscopique post-opératoire, une amélioration endoscopique (définie comme toute réduction du score de Rutgeerts de référence) a été observée chez 61 % des patients, dont 42 % ont atteint une rémission endoscopique (53). L’utilisation concomitante de thiopurines et le traitement par infliximab (par rapport à l’adalimumab) étaient associés à une rémission endoscopique. Fait intéressant, 53 patients (30 %) de cette étude étaient déjà traités par anti-TNF avant la chirurgie, et près de la moitié d’entre eux (24/53) étaient même traités par le même anti-TNF avant et après la chirurgie, en particulier l’infliximab. Néanmoins, l’exposition à un traitement par anti-TNF avant la chirurgie n’a pas influencé le résultat du traitement par anti-TNF après la chirurgie. L’efficacité de l’ustekinumab et du védolizumab n’a été étudiée que dans des séries de cas dans cette indication spécifique du traitement de la récidive post-opératoire (43).
En pratique, en cas de récidive i3 ou i4, il semble raisonnable d’introduire une biothérapie sans qu’il n’y ait d’argument fort pour guider le choix vers une biothérapie en particulier. Il est possible d’utiliser un anti-TNF même chez les patients exposés antérieurement aux anti-TNF. La surveillance doit être rapprochée, en utilisant la calprotectine fécale et probablement en réévaluant l’aspect endoscopique à un an, notamment chez les patients fumeurs. Il faut aussi à ce moment-là savoir ré-insister auprès du patient pour obtenir un sevrage tabagique. L’enjeu principal est d’éviter d’avoir recours à une nouvelle résection iléo-colique. Malheureusement, des données récentes en population montrent que, bien que le taux de première résection iléo-colique ait diminué au cours des dernières années, celui de deuxième chirurgie reste stable, aux alentours de 15 % cinq ans après la première chirurgie (2).
Que faire en cas de récidive minime à modérée ?
Alors que la conduite à tenir est plutôt claire en cas de score de Rutgeerts extrême (i0 ou i4), elle est beaucoup plus floue dans les autres cas. En cas de récidive minime, c’est-à-dire quelques lésions aphtoïdes du néo-iléon terminal au sein d’une muqueuse normale et sans lésion de la ligne anastomotique (Rutgeerts i1), il n’est pour l’instant pas recommandé d’introduire un traitement spécifique (43). Néanmoins, des données de la cohorte REMIND semblent montrer que le risque de récidive clinique des patients ayant des lésions i1 à six mois pourrait se rapprocher de celui des patients ayant des lésions i2b (30). En cas de récidive localisée à la ligne anastomotique (Rutgeerts i2a), l’intérêt d’introduire un traitement spécifique est également débattu puisqu’il a pu être supposé qu’il s’agissait plutôt de lésions ischémiques notamment liées à l’agrafage (15). Il est plus communément admis qu’un traitement doit être initié en cas de récidive modérée dans le néo-iléon terminal (Rutgeerts i2b) mais cette catégorie regroupe des situations pouvant être différentes, allant de six ulcérations aphtoïdes dans le néo-iléon terminal, proche du i1, à des ulcérations plus importantes mais avec une muqueuse intercalaire normale, proche du i4. Néanmoins, comme mentionné précédemment, du fait des limites inhérentes au score de Rutgeerts, il est possible que les catégories i1 et i2 soient confondues dans certaines études, notamment celles n’ayant pas utilisé une relecture centralisée, et il n’a pas pu être formellement démontré que les lésions i2a étaient moins susceptibles d’entraîner une récidive clinique que les lésions i2b (26, 31). De plus, il n’a jamais été prouvé que l’introduction d’un traitement en cas de lésions i2 permettait de diminuer le risque de récidive clinique ultérieure. Ainsi, dans une étude rétrospective multicentrique incluant 158 patients ayant des lésions i2 dans l’année suivant la chirurgie, aucune différence en termes de survie sans récidive clinique n’était observée lorsque l’on comparait les patients chez qui un immunosuppresseur ou un anti-TNF était introduit à ceux qui ne recevaient aucun traitement (54). Un essai randomisé international actuellement en cours est dédié à répondre à cette question : l’étude POMEROL inclut des patients ayant des lésions i2 dans l’année suivant une résection iléo- colique en comparant un traitement par infliximab à une surveillance simple (NCT05072782).
La décision thérapeutique chez un patient présentant des lésions i1 ou i2 à la première endoscopie doit donc être guidée par les antécédents du patient, son statut tabagique, ses expositions antérieures aux traitements et discutée en réunion de concertation multi-disciplinaire et avec le patient lui-même. Quelle que soit l’option retenue, l’essentiel est de surveiller le patient de façon rapprochée, en utilisant la calprotectine fécale pour éviter les endoscopies trop rapprochées.
Conclusion
En 2023, la prise en charge de la maladie de Crohn opérée reste donc un vaste champ de recherche semé d’interrogations : comment identifier efficacement les patients qui doivent bénéficier d’un traitement post-opératoire immédiat ? comment affiner la classification endoscopique afin de pouvoir vraiment guider la prise en charge thérapeutique ? faut-il traiter les patients ayant une récidive minime à modérée ? Nous espérons que les études randomisées en cours permettront de répondre à ces questions de façon robuste. En attendant leurs résultats, il est clairement établi que le tabagisme est un facteur de risque majeur de récidive et que les patients doivent être encouragés à arrêter de fumer au plus tôt, en utilisant les outils de tabacologie. Chez les patients fumeurs, un traitement doit être introduit en post-opératoire immédiat. Pour les autres, la prophylaxie post- opératoire immédiate doit se décider au cas par cas avec le patient et en réunion de concertation multi-disciplinaire. La récidive endoscopique doit être dépistée à six mois de la chirurgie et cotée en utilisant le score de Rutgeerts et en prenant soin de décrire les différentes zones de l’iléon en cas d’anastomose latéro-latérale. En cas d’absence de récidive, aucun traitement n’est introduit et la surveillance peut se poursuivre en utilisant la calprotectine fécale, le niveau mesuré au moment de l’endoscopie servant de référence pour chaque patient. En cas de récidive sévère, un traitement est indiqué, qui doit permettre d’éviter une évolution vers une récidive clinique puis chirurgicale. Son efficacité devra être vérifiée par une endoscopie rapprochée. En cas de récidive minime à modérée, la stratégie thérapeutique optimale est floue et doit se discuter au cas par cas, en maintenant une surveillance stricte. À chaque étape, la discussion avec le patient est indispensable pour obtenir une adhésion thérapeutique et éviter une rupture de suivi qui pourrait se solder par une nouvelle complication plusieurs années après et la nécessité d’une résection étendue du grêle, situation qui est hélas encore trop fréquemment rencontrée en réunion de concertation multi-disciplinaire.
Remerciements
Ce texte est le fruit d’une longue collaboration avec le Pr Marc Ferrante (UZ Leuven) et le Pr David Laharie (CHU de Bordeaux) et de nombreuses discussions au sein du groupe de travail de l’ECCO sur la récidive post-opératoire.
Références
- Bemelman WA, Warusavitarne J, Sampietro GM, Serclova Z, Zmora O, Luglio G, et al. ECCO-ESCP Consensus on Surgery for Crohn’s Disease. J Crohns Colitis [Internet]. 11 mai 2017 [cité 4 mars 2019]; Disponible sur: https://academic.oup.com/ecco-jcc/article-lookup/doi/10.1093/ ecco-jcc/jjx061
- Kalman TD, Everhov ÅH, Nordenvall C, Sachs MC, Halfvarson J, Ekbom A, et al. Decrease in primary but not in secondary abdominal surgery for Crohn’s disease: nationwide cohort study, 1990–2014. BJS Br J Surg. 2020;107(11):1529-38.
- Ponsioen CY, de Groof EJ, Eshuis EJ, Gardenbroek TJ, Bossuyt PMM, Hart A, et Laparoscopic ileocaecal resection versus infliximab for terminal ileitis in Crohn’s disease: a randomised controlled, open-label, multicentre trial. Lancet Gastroenterol Hepatol. 2017;2(11):785-92.
- Rutgeerts P, Geboes K, Vantrappen G, Kerremans R, Coenegrachts JL, Coremans Natural history of recurrent Crohn’s disease at the ileocolonic anastomosis after curative surgery. Gut. 1984;25(6):665.
- Rutgeerts P, Geboes K, Vantrappen G, Beyls J, Kerremans R, Hiele Predictability of the postoperative course of Crohn’s disease. Gastroenterology. oct 1990;99(4):956-63.
- Auzolle C, Nancey S, Tran-Minh ML, Buisson A, Pariente B, Stefanescu C, et Male gender, active smoking and previous intestinal resection are risk factors for post-operative endoscopic recurrence in Crohn’s disease: results from a prospective cohort study. Aliment Pharmacol Ther. nov 2018;48(9):924-32.
- Rivière P, Bislenghi G, Hammoudi N, Verstockt B, Brown S, Oliveira-Cunha M, et al. Results of the Eighth Scientific Workshop of ECCO: Pathophysiology and risk factors of postoperative Crohn’s disease recurrence after an ileocolic resection. J Crohns Colitis. 18 avr 2023;jjad054.
- Joustra V, Duijvestein M, Mookhoek A, Bemelman W, Buskens C, Koželj M, et al. Natural History and Risk Stratification of Recurrent Crohn’s Disease After Ileocolonic Resection: A Multicenter Retrospective Cohort Study. Inflamm Bowel Dis. 5 janv 2022;28(1):1-8.
- Arkenbosch JHC, Beelen EMJ, Dijkstra G, Romberg-Camps M, Duijvestein M, Hoentjen F, et Prophylactic medication for the prevention of endoscopic recurrence in Crohn’s disease: a prospective study based on clinical risk stratification. J Crohns Colitis. 12 sept 2022;jjac128.
- Reese GE, Nanidis T, Borysiewicz C, Yamamoto T, Orchard T, Tekkis The effect of smoking after surgery for Crohn’s disease: a meta-analysis of observational studies. Int J Colorectal Dis. 1 déc 2008;23(12):1213.
- Allez M, Auzolle C, Ngollo M, Bottois H, Chardiny V, Corraliza AM, et T cell clonal expansions in ileal Crohn’s disease are associated with smoking behaviour and postoperative recurrence. Gut. nov 2019;68(11):1961-70.
- Gustafsson UO, Scott MJ, Hubner M, Nygren J, Demartines N, Francis N, et Guidelines for Perioperative Care in Elective Colorectal Surgery: Enhanced Recovery After Surgery (ERAS®) Society Recommendations: 2018. World J Surg. 1 mars 2019;43(3):659-95.
- Feng J shan, Li J yu, Yang Z, Chen X yan, Mo J jie, Li S Stapled side-to-side anastomosis might be benefit in intestinal resection for Crohn’s disease. Medicine (Baltimore). 13 avr 2018;97(15):e0315.
- Komatsu S, Nimura Y, Granger Intestinal stasis associated bowel inflammation. World J Gastroenterol. 15 déc 1999;5(6):518-21.
- van der Does de Willebois EML, Duijvestein M, Wasmann KA, D’Haens GRAM, van der Bilt JDW, Mundt MW, et Endoscopic Recurrence or Anastomotic Wound Healing Phenomenon after Ileocolic Resection for Crohn’s Disease: The Challenges of Accurate Endoscopic Scoring. J Crohns Colitis. 16 nov 2022;jjac175.
- Kono T, Ashida T, Ebisawa Y, Chisato N, Okamoto K, Katsuno H, et A new antimesenteric functional end-to-end handsewn anastomosis: surgical prevention of anastomotic recurrence in Crohn’s disease. Dis Colon Rectum. mai 2011;54(5):586-92.
- Luglio G, Rispo A, Imperatore N, Giglio MC, Amendola A, Tropeano FP, et Surgical Prevention of Anastomotic Recurrence by Excluding Mesentery in Crohn’s Disease: The SuPREMe-CD Study – A Randomized Clinical Trial. Ann Surg. août 2020;272(2):210-7.
- Wasmann KATGM, van Amesfoort J, van Montfoort ML, Koens L, Bemelman WA, Buskens The Predictive Value of Inflammation at Ileocecal Resection Margins for Postoperative Crohn’s Recurrence: A Cohort Study. Inflamm Bowel Dis. 23 oct 2020;26(11):1691-9.
- Hammoudi N, Cazals-Hatem D, Auzolle C, Gardair C, Ngollo M, Bottois H, et al. Association Between Microscopic Lesions at Ileal Resection Margin and Recurrence After Surgery in Patients With Crohn’s Disease. Clin Gastroenterol Hepatol. 1 janv 2020;18(1):141-149.e2.
- Lemmens B, de Buck van Overstraeten A, Arijs I, Sagaert X, Van Assche G, Vermeire S, et al. Submucosal Plexitis as a Predictive Factor for Postoperative Endoscopic Recurrence in Patients with Crohn’s Disease Undergoing a Resection with Ileocolonic Anastomosis: Results from a Prospective Single-centre Study. J Crohns Colitis. févr 2017;11(2):212-20.
- Sokol H, Polin V, Lavergne-Slove A, Panis Y, Treton X, Dray X, et al. Plexitis as a predictive factor of early postoperative clinical recurrence in Crohn’s disease. Gut. 1 sept 2009;58(9):1218-25.
- D’Haens GR, Geboes K, Peeters M, Baert F, Penninckx F, Rutgeerts Early lesions of recurrent Crohn’s disease caused by infusion of intestinal contents in excluded ileum. Gastroenterology. févr 1998;114(2):262-7.
- Mondot S, Lepage P, Seksik P, Allez M, Tréton X, Bouhnik Y, et Structural robustness of the gut mucosal microbiota is associated with Crohn’s disease remission after surgery. Gut. 1 juin 2016;65(6):954-62.
- Dragoni G, Allocca M, Myrelid P, Noor NM, Hammoudi N, 8 th Scientific Workshop of the European Crohn’s and Colitis Organisation, et al. Results of the Eighth Scientific Workshop of ECCO: Diagnosing postoperative recurrence of Crohn’s disease after an ileocolonic resection with ileocolonic anastomosis. J Crohns Colitis. 18 avr 2023;jjad055.
- Marteau P, Laharie D, Colombel JF, Martin L, Coevoet H, Allez M, et Interobserver Variation Study of the Rutgeerts Score to Assess Endoscopic Recurrence after Surgery for Crohn’s Disease. J Crohns Colitis. sept 2016;10(9):1001-5.
- Rivière P, Bislenghi G, Vermeire S, Domènech E, Peyrin-Biroulet L, Laharie D, et al. Postoperative Crohn’s Disease Recurrence: Time to Adapt Endoscopic Recurrence Scores to the Leading Surgical Techniques. Clin Gastroenterol Hepatol. 1 juin 2022;20(6):1201-4.
- Gecse K, Lowenberg M, Bossuyt P, Rutgeerts PJ, Vermeire S, Stitt L, et Sa1198 Agreement Among Experts in the Endoscopic Evaluation of Postoperative Recurrence in Crohn’s Disease Using the Rutgeerts Score. Gastroenterology. 1 mai 2014;146(5):S-227.
- Rivière P, Vermeire S, Irles-Depe M, van Assche G, Rutgeerts P, de Buck van Overstraeten A, et No Change in Determining Crohn’s Disease Recurrence or Need for Endoscopic or Surgical Intervention With Modification of the Rutgeerts Scoring System. Clin Gastroenterol Hepatol [Internet]. oct 2018 [cité 7 févr 2019]; Disponible sur: https://linkinghub.elsevier.com/retrieve/pii/S1542356518310796
- Ollech JE, Aharoni-Golan M, Weisshof R, Normatov I, Sapp AR, Kalakonda A, et Differential risk of disease progression between isolated anastomotic ulcers and mild ileal recurrence after ileocolonic resection in patients with Crohn’s disease. Gastrointest Endosc. août 2019;90(2):269-75.
- Hammoudi N, Auzolle C, Tran Minh ML, Boschetti G, Bezault M, Buisson A, et Postoperative Endoscopic Recurrence on the Neoterminal Ileum But Not on the Anastomosis Is Mainly Driving Long-Term Outcomes in Crohn’s Disease. Off J Am Coll Gastroenterol ACG. juill 2020;115(7):1084-93.
- Rivière P, Pekow J, Hammoudi N, Wils P, De Cruz P, Wang CP, et Comparison of the Risk of Crohn’s Disease Postoperative Recurrence Between Modified Rutgeerts Score i2a and i2b Categories: An Individual Patient Data Meta-analysis. J Crohns Colitis. 18 sept 2022;jjac137.
- Garcia-Planella E, Mañosa M, Cabré E, Marín L, Gordillo J, Zabana Y, et Fecal Calprotectin Levels Are Closely Correlated with the Absence of Relevant Mucosal Lesions in Postoperative Crohn’s Disease: Inflamm Bowel Dis. déc 2016;22(12):2879-85.
- De Cruz P, Kamm MA, Hamilton AL, Ritchie KJ, Krejany EO, Gorelik A, et al. Crohn’s disease management after intestinal resection: a randomised trial. Lancet Lond Engl. 11 avr 2015;385(9976):1406-17.
- Boschetti G, Laidet M, Moussata D, Stefanescu C, Roblin X, Phelip G, et Levels of Fecal Calprotectin Are Associated With the Severity of Postoperative Endoscopic Recurrence in Asymptomatic Patients With Crohn’s Disease. Am J Gastroenterol. juin 2015;110(6):865-72.
- Verdejo C, Hervías D, Roncero Ó, Arias Á, Bouhmidi A, Lorente R, et al. Fecal calprotectin is not superior to serum C-reactive protein or the Harvey-Bradshaw index in predicting postoperative endoscopic recurrence in Crohn’s Eur J Gastroenterol Hepatol. déc 2018;30(12):1521-7.
- Maaser C, Sturm A, Vavricka SR, Kucharzik T, Fiorino G, Annese V, et ECCO-ESGAR Guideline for Diagnostic Assessment in IBD Part 1: Initial diagnosis, monitoring of known IBD, detection of complications. J Crohns Colitis. 1 févr 2019;13(2):144-164K.
- Rispo A, Imperatore N, Testa A, Nardone OM, Luglio G, Caporaso N, et Diagnostic Accuracy of Ultrasonography in the Detection of Postsurgical Recurrence in Crohn’s Disease: A Systematic Review with Meta-analysis. Inflamm Bowel Dis. 23 avr 2018;24(5):977-88.
- Buisson A, Gonzalez F, Poullenot F, Nancey S, Sollellis E, Fumery M, et Comparative Acceptability and Perceived Clinical Utility of Monitoring Tools: A Nationwide Survey of Patients with Inflammatory Bowel Disease. Inflamm Bowel Dis. 1 août 2017;23(8):1425-33.
- Schaefer M, Laurent V, Grandmougin A, Vuitton L, Bourreille A, Luc A, et A Magnetic Resonance Imaging Index to Predict Crohn’s Disease Postoperative Recurrence: The MONITOR Index. Clin Gastroenterol Hepatol. 1 mai 2022;20(5):e1040-9.
- De Bie C, Ballet V, Hendriks N, Coenen S, Weyts E, Van Assche G, et Smoking behaviour and knowledge of the health effects of smoking in patients with inflammatory bowel disease. Aliment Pharmacol Ther. déc 2015;42(11-12):1294-302.
- Biedermann L, Fournier N, Misselwitz B, Frei P, Zeitz J, Manser CN, et High Rates of Smoking Especially in Female Crohn’s Disease Patients and Low Use of Supportive Measures to Achieve Smoking Cessation–Data from the Swiss IBD Cohort Study. J Crohns Colitis. oct 2015;9(10):819-29.
- Nunes T, Etchevers MJ, Merino O, Gallego S, García-Sánchez V, Marín-Jiménez I, et High smoking cessation rate in Crohn’s disease patients after physician advice–the TABACROHN Study. J Crohns Colitis. avr 2013;7(3):202-7.
- Ferrante M, Pouillon L, Mañosa M, Savarino E, Allez M, Kapizioni C, et Results of the Eighth Scientific Workshop of ECCO: Prevention and treatment of postoperative recurrence in patients with Crohn’s disease undergoing an ileocolonic resection with ileocolonic anastomosis. J Crohns Colitis. 18 avr 2023;jjad053.
- Ferrante M, Papamichael K, Duricova D, D’Haens G, Vermeire S, Archavlis E, et Systematic versus Endoscopy-driven Treatment with Azathioprine to Prevent Postoperative Ileal Crohn’s Disease Recurrence. J Crohns Colitis. août 2015;9(8):617-24.
- Joustra V, van Sabben J, van der Does de Willebois E, Duijvestein M, de Boer N, Jansen J, et al. Benefit of Risk-stratified Prophylactic Treatment on Clinical Outcome in Postoperative Crohn’s Disease. J Crohns Colitis. 3 avr 2023;17(3):318-28.
- Gjuladin_Hellon T, Iheozor_Ejiofor Z, Gordon M, Akobeng Azathioprine and 6_mercaptopurine for maintenance of surgically_induced remission in Crohn’s disease. Cochrane Database Syst Rev [Internet]. 2019 [cité 30 avr 2022];2019(8). Disponible sur: https://www.readcube.com/articles/10.1002%2F14651858.cd010233.pub3
- Regueiro M, Schraut W, Baidoo L, Kip KE, Sepulveda AR, Pesci M, et Infliximab prevents Crohn’s disease recurrence after ileal resection. Gastroenterology. févr 2009;136(2):441-450.e1; quiz 716.
- Regueiro M, Kip KE, Baidoo L, Swoger JM, Schraut Postoperative Therapy With Infliximab Prevents Long-term Crohn’s Disease Recurrence. Clin Gastroenterol Hepatol. sept 2014;12(9):1494-1502.e1.
- López-Sanromán A, Vera-Mendoza I, Domènech E, Taxonera C, Vega Ruiz V, Marín-Jiménez I, et al. Adalimumab vs Azathioprine in the Prevention of Postoperative Crohn’s Disease A GETECCU Randomised Trial. J Crohns Colitis [Internet]. [cité 5 juin 2017]; Disponible sur: https://academic.oup.com/ecco-jcc/article-abstract/doi/10.1093/ecco-jcc/jjx051/3574893/Adalimumab-vs-Azathioprine-in-the-Prevention-of
- Beelen EMJ, Nieboer D, Arkenbosch JHC, Regueiro MD, Satsangi J, Ardizzone S, et Risk Prediction and Comparative Efficacy of Anti-TNF vs Thiopurines, for Preventing Postoperative Recurrence in Crohn’s Disease: A Pooled Analysis of 6 Trials. Clin Gastroenterol Hepatol Off Clin Pract J Am Gastroenterol Assoc. déc 2022;20(12):2741-2752.e6.
- Mañosa M, Fernández-Clotet A, Nos P, Martín-Arranz MD, Manceñido N, Carbajo A, et al. Ustekinumab and vedolizumab for the prevention of postoperative recurrence of Crohn’s disease: Results from the ENEIDA Dig Liver Dis Off J Ital Soc Gastroenterol Ital Assoc Study Liver. janv 2023;55(1):46-52.
- Dragoni G, Ding N, Gecse KB, Mansfield JC, Kopylov U, Beaugerie L, et The prevention and management of Crohn’s disease postoperative recurrence: results from the Y-ECCO/ClinCom 2019 Survey. Eur J Gastroenterol Hepatol. août 2020;32(8):1062-6.
- Cañete F, Mañosa M, Pérez-Martínez I, Barreiro-de Acosta M, González-Sueyro RC, Nos P, et al. Antitumor Necrosis Factor Agents to Treat Endoscopic Postoperative Recurrence of Crohn’s Disease: A Nationwide Study With Propensity-Matched Score Clin Transl Gastroenterol. août 2020;11(8):e00218.
- Rivière P, Vermeire S, Irles-Depe M, Van Assche G, Rutgeerts P, Denost Q, et Rates of Postoperative Recurrence of Crohn’s Disease and Effects of Immunosuppressive and Biologic Therapies. Clin Gastroenterol Hepatol. avr 2021;19(4):713-720.e1.