Liens d’intérêt
Pas de lien d’intérêt pour cet article
Mots-clés
Dysplasie, MICI, coloscopie
Abréviations
CCR : cancer colorectal
CSP : cholangite sclérosante primitive
HD : haute définition
MICI : maladies inflammatoires chroniques de l’intestin
MC : Maladie de Crohn
RCH : rectocolite hémorragique
Introduction
L’avènement des moyens de surveillance non invasif dans les maladies inflammatoires de l’intestin (MICI) a permis de diminuer le recours à la coloscopie pour déterminer la réponse aux traitements. Néanmoins la pratique de la coloscopie dans cette population reste indispensable pour le dépistage de la dysplasie colorectale et nécessite de connaître ses indications et ses modalités de réalisation qui conditionnent son efficacité.
L’enjeu pour le gastroentérologue est d’une part de sélectionner et prioriser les patients selon leur niveau de risque et d’autre part de définir les modalités pratiques de réalisation du dépistage. L’essor récent des techniques endoscopiques de résection fait évoluer le traitement des lésions dysplasiques avec plus de recours à des résections endoluminales moins invasives que la chirurgie, qui doivent néanmoins être suivies d’une surveillance adaptée et serrée.
Particularités de la dysplasie associée aux MICI
Les patients atteints d’une MICI colique, rectocolite hémorragique (RCH) ou maladie de Crohn (MC) de topographie colique (L2 ou L3 de la classification de Montréal), ont un risque augmenté de cancer colorectal (CCR) au cours de la vie. Le risque global de cancer colorectal chez les patients atteints de MICI est multiplié par 2,5 par rapport à la population non MICI (1). Dans une méta-analyse de données en population, le risque de CCR a été estimé à 1 % après 10 ans, 3 % après 20 ans et 7 % après 30 ans (1). Les patients atteints de MICI ont un « double » risque de CCR : les lésions pré néoplasiques coliques rencontrées dans les MICI peuvent être comme en population générale des adénomes ou des polypes festonnés de type sporadiques, siégeant au sein des lésions inflammatoires ou en zone saine ; et/ou il peut également s’agir de lésions de dysplasie inflammatoire qui peuvent se développer dans des zones inflammatoires, ou anciennement inflammatoires. Ces dernières ont été étudiées d’un point de vue histologique et génétique. Des caractéristiques histologiques spécifiques ont été décrites, appelées « dysplasie non conventionnelle », incluant la dysplasie mucineuse, les lésions festonnées, la dysplasie avec différentiation des cellules de Paneth et la dysplasie avec déficit en cellules caliciformes (2). Pour finir, les altérations génétiques observées dans les tumeurs CR issues de patients MICI sont différentes des tumeurs sporadiques avec notamment des mutations somatiques des gènes APC et KRAS moins fréquentes dans les CRC associés aux MICI que dans les CRC sporadiques (3) et des mécanismes distincts de dysrégulation de la voie WNT orientent les MICI-CR vers un sous-type de tumeur mésenchymateuse.
La coloscopie est actuellement le seul moyen de dépistage de la dysplasie colorectale et a démontré son efficacité pour réduire la survenue de cancer colorectal (4, 5). Il a été observé au cours des dernières années une diminution de l’incidence des CCR dans les populations de MICI, potentiellement du fait d’un meilleur contrôle de l’inflammation colorectale et d’une meilleure surveillance coloscopique des patients à risque. Néanmoins ce dépistage est difficile en pratique et impacté par les facteurs suivants : côlon cicatriciel et/ou sténose, pseudo polypes parfois innombrables, lésions inflammatoires actives, les lésions de dysplasie inflammatoire peuvent présenter un aspect macroscopique différent et atypique par rapport à la néoplasie sporadique. Pour finir, la répétition des coloscopies peut limiter l’observance au programme de dépistage chez certains patients. Ainsi, une étude publiée récemment montre que les cancers survenant dans les 3 ans après une coloscopie, ce qui correspond à la nouvelle définition des cancers d’intervalle, sont 6 fois plus fréquents qu’en population générale, représentant près de 30 % des CCR dépistés chez les MICI (6). Ceci illustre la nécessité de s’améliorer dans cette population spécifique.
Situations à risque et modalités de dépistage
Les facteurs de risque de néoplasie colique, identiques à la population générale et spécifiquement liés à l’inflammation (7-10), sont résumés dans le tableau 1. Une attention particulière doit être portée aux patients atteints d’une cholangite sclérosante primitive (CSP) qui présentent un risque trois fois plus élevé de CCR par rapport à une MICI sans CSP (11).
Les recommandations françaises concernant le rythme de dépistage selon les facteurs de risque ont été publiées en 2022 et sont basées sur une revue des données issues de la littérature en privilégiant les meilleurs niveaux de preuve (12). La figure 1 synthétise ce consensus. Il est recommandé de réaliser une coloscopie de dépistage 6 à 8 ans après les premiers symptômes de la MICI quelle que soit son extension cumulée, à l’exception des patients qui ont une CSP qui doivent être dépistés dès le diagnostic de CSP, quel que soit l’âge de la MICI. Les patients qui présentent un très haut risque de CCR – antécédent personnel de dysplasie de bas grade (hors adénome sporadique), sténose colique, cholangite sclérosante primitive – doivent avoir une coloscopie de dépistage annuelle. Les patients qui ont au moins deux facteurs de risque intermédiaire parmi les suivants : pancolite, persistance d’une activité inflammatoire histologique ou endoscopique, antécédent familial de cancer colorectal avant 50 ans et présence de pseudopolypes inflammatoires doivent avoir une coloscopie de dépistage dans les 1 à 3 ans. Chez les patients qui ont un seul ou aucun facteur de risque intermédiaire, il est proposé une coloscopie tous 3 à 5 ans. Il n’y a pas d’indication à un dépistage endoscopique spécifique de du CCR en cas de RCH limitée au rectum (E1) et en cas de MC limitée à l’intestin grêle (L1), après s’être assuré de l’absence d’extension à la première coloscopie proposée à 6-8 ans du diagnostic. Ces patients doivent néanmoins avoir des coloscopies à partir de 50 ans pour le dépistage classique qui ne peut pas être réalisé par test de détection de sang dans les selles en raison de la MICI sous-jacente. Le consensus européen ECCO a pour sa part été actualisé en 2023 dans un article dédié aux cancers (14). Les recommandations concernant le dépistage de la dysplasie sont très proches des françaises puisqu’elles reposent également sur une revue de la littérature et des preuves disponibles. Quelques variantes existent néanmoins ; les patients à haut risque justifiant d’une surveillance annuelle sont définis par les caractéristiques suivantes : antécédents familiaux de CCR chez un parent au premier degré âgé de≤ 50 ans et colite étendue avec inflammation active sévère, sténose ou dysplasie colique, CSP. Les facteurs de risque intermédiaires sont communs, hormis les pseudo-polypes qui ne sont pas retenus par ces recommandations.
Tableau 1 : Facteurs de risque de néoplasie colorectale chez les patients atteints de MICI
| Facteurs de risque identiques à la population générale | Facteurs de risque spécifiquement liés à l’inflammation |
| Age Antécédents familiaux 1er degré Sexe masculin Mode de vie (tabac, alimentation, sédentarité) Antécédent personnel de dysplasie | Cholangite sclérosante primitive X3 Colite étendue Age jeune au diagnostic Durée d’évolution de la MICI > 10 ans Inflammation macroscopique et microscopique Sténose Antécédent personnel de dysplasie |
Figure 1 : Modalités de surveillance de la dysplasie par coloscopie des patients atteints de MICI. (12)
- Patients avec au moins un facteur à haut risque ® dépistage annuel
CSP, sténose colique, dysplasie (hors adénome sporadique)
- Patients avec au moins 2 facteurs de risque intermédiaires ® dépistage / 1-3 ans
Pancolite, persistance activité inflammatoire macro ou microscopique, antécédent familial de CCR< 50 ans, présence de pseudo-polypes
- Patients avec 0 ou 1 facteur de risque intermédiaire ® dépistage / 3-5 ans
Pancolite, persistance activité inflammatoire macro ou microscopique, antécédent familial de CCR < 50 ans, présence de pseudo-polypes
La coloscopie de dépistage de la dysplasie nécessite une préparation parfaite (12). Les facteurs de qualité de la préparation sont les mêmes qu’en population générale, à savoir, prise fractionnée, délai minimum entre la dernière prise de préparation et la coloscopie, régime sans résidus la veille et utilisation d’une pompe de lavage. Une étude multicentrique française a montré l’efficacité, la sécurité d’emploi et une tolérance significativement meilleure de préparations de faible volume à base de picosulfate de sodium (13). La coloscopie est réalisée au mieux en période de rémission si un traitement a été introduit récemment, néanmoins l’activité persistante qui est un facteur de risque majeur ne doit pas empêcher sa réalisation.
Pour la réalisation du dépistage les consensus internationaux insistent sur l’expérience de l’opérateur dans l’endoscopie spécifique des MICI, et sur l’utilisation d’endoscopes de haute définition (HD) et de dernière génération. À défaut, le recours à un centre expert est conseillé. (14, 15). Dans les MICI, de nombreuses études ont démontré le gain diagnostique obtenu grâce à l’emploi d’une coloration au bleu (bleu d’indigo carmin ou bleu de méthylène) pour dépister les lésions pré-néoplasiques (15). À l’ère des endoscopes haute définition, avec magnification de l’image, la chromoendoscopie au bleu reste d’actualité et est toujours recommandée (12, 15). En pratique, le bleu peut être dilué avec du sérum physiologique ou de l’eau (dilution 1/6-1/10), et utilisé directement dans la pompe de lavage. Les études avec les colorations virtuelles ont jusqu’ici concerné le système de narrow band imaging (NBI) d’Olympus® ; elles n’ont pas montré de bénéfice par rapport à l’endoscopie en lumière blanche HD ou à la chromoendoscopie au bleu en HD (1). À noter que la société européenne d’endoscopie (ESGE) (16) propose la coloration virtuelle HD comme alternative chez les opérateurs entraînés à cette technique.
La réalisation de biopsies aléatoires n’a pas démontré de supériorité par rapport aux biopsies ciblées après chromo-endoscopie pour détecter de la dysplasie (17). Il est cependant recommandé de réaliser les biopsies aléatoires tous les 10 cm en cas de cholangite sclérosante primitive (CSP) associée, d’antécédent personnel de dysplasie, de sténose ou d’aspect tubulisé du côlon, qui sont des situations à risque de dysplasie « invisible » (12, 15). Pour les autres patients, au cours du suivi, des biopsies coliques segmentaires systématiques permettent de déterminer le niveau d’inflammation histologique, lui-même corrélé à la rémission prolongée, en particulier dans la RCH, et au risque de dysplasie.
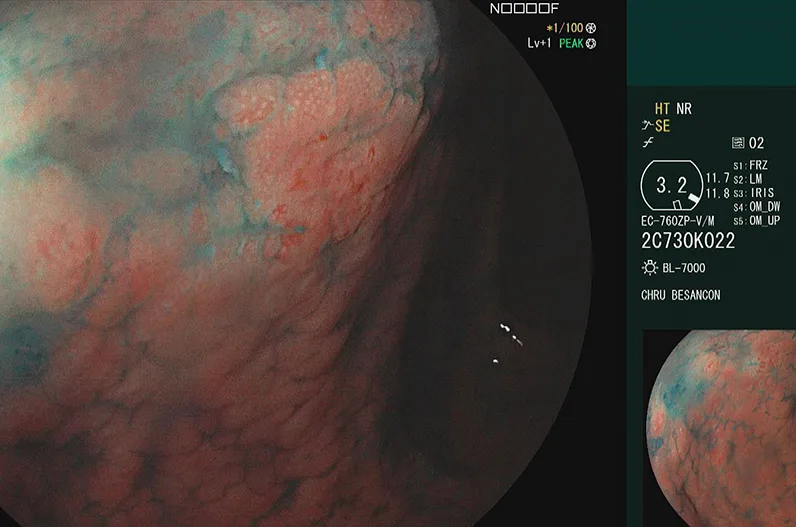
Figure 2 : Lésion plane sans limites nettes de pit pattern atypique chez un patient aux antécédents de RCH ancienne pancolique avec CSP associée (histologie : dysplasie de bas grade). Image CHU Besançon

Reconnaître et décrire les lésions à risque
Les lésions pré néoplasiques coliques rencontrées dans les MICI peuvent être des adénomes ou des polypes festonnés sporadiques, siégeant au sein des lésions inflammatoires ou en zone saine. Il peut également s’agir de lésions de dysplasie non adénomateuses (exemple figure 2) qui peuvent se développer dans des zones inflammatoires, ou anciennement inflammatoires, comme par un exemple au sein des sténoses La caractérisation des lésions observées tente de distinguer les lésions adénomateuses, des lésions spécifiques d’une MICI. La description doit être faite, comme pour le dépistage des adénomes, grâce à la classification de Paris (lésion pédiculée 0-1p, sessile 0-1s, plane 0-II a et b, déprimée 0-IIc, ulcérée 0-III) ; elle doit préciser le motif muqueux appelé «pit pattern» (selon Kudo par exemple), et la taille de la lésion. Plus spécifiquement, il faut préciser si la lésion se situe au sein de lésions inflammatoires, de sténoses, ou cicatrices, et décrire la présence ou l’absence de bords, et de limites nettes qui pourront faire envisager une résection endoscopique. La terminologie des lésions associées aux MICI a été précisée dans le consensus international SCENIC (15) et distingue les lésions visibles (décrites selon la classification de Paris), des lésions invisibles identifiées lors de biopsies aléatoires sans anomalie macroscopique vue par l’endoscopiste.
Si la lésion n’est pas résécable d’emblée pour obtenir une histologie complète, une lésion suspecte de dysplasie doit être biopsiée. Cette recommandation qui n’est pas valable pour les lésions sporadiques, du fait du risque de compromettre la résection, reste valable dans le cas d’une MICI en raison de la possibilité d’aspect atypique dans les cas de dysplasie inflammatoire. Les biopsies doivent être ciblées et limitées pour ne pas compromettre une éventuelle résection. Les alentours de la lésion doivent être biopsiées pour ne pas méconnaitre de la dysplasie invisible.
Récemment des classifications spécifiques aux MICI ont été proposées. La classification « Kudo IBD » proposée par une équipe italienne (18), non validée, ajoute deux modifications à la classification de Kudo, basé sur l’observation d’experts avec une coloration virtuelle Fuji® : cap fibreux sur un Kudo de type III IV non en faveur de dysplasie et au contraire vaisseaux ou puits en faveur de lésion bénigne sur Kudo I et II. Un autre score développé par un panel d’expert à partir de coloration virtuelle [Frankfurt Advanced Chromoendoscopic IBD LEsions [FACILE] classification] a également été publié (19). Les experts ont d’abord sélectionné des critères tels que la morphologie, la couleur, la surface, l’architecture des vaisseaux, les signes d’inflammation et le bord de la lésion. L’analyse multivariée a identifié que les lésions non polypoïdes, l’architecture irrégulière des vaisseaux, la configuration irrégulière de la surface et les signes d’inflammation sur la lésion étaient des facteurs prédictifs de dysplasie. Le score a secondairement été validé.
Traitement des lésions dysplasiques et modalités de surveillance
Les modalités de résection endoscopique des lésions néoplasiques colorectales ont beaucoup évolué ces dix dernières années avec l’évolution et le perfectionnement des techniques endoscopiques mini-invasives, permettant notamment grâce aux techniques de dissection sous muqueuse d’obtenir des résections en marge saine et curatives de lésions larges et avancées. Une étude française multicentrique a récemment colligé 88 cas de dissections sous-muqueuse sur MICI chez 82 patients et montre de bons résultats en termes de résection R0 et curative, respectivement de 81,8% et 79,5% (20).
L’avènement de ces techniques rend obsolète un grand nombre de consensus. Le consensus européen ECCO sur MICI et cancers (14) est le plus récemment actualisé et prend en compte ces alternatives à la chirurgie en précisant le cadre des indications et les précautions.
Les recommandations sont les suivantes :
- les lésions indéfinies pour la dysplasie et la dysplasie « invisible » (sur biopsies aléatoires) nécessitent une double lecture, par un deuxième pathologiste et de répéter la coloscopie, si possible et si applicable après un meilleur contrôle de l’inflammation et en centre expert.
- les lésions dysplasiques polypoïdes (Paris Ip ou Is) peuvent être traitées par résection endoscopique lorsque la lésion peut être réséquée entièrement en monobloc, à condition qu’il n’y ait pas de dysplasie multifocale ou invisible ailleurs dans le côlon.
- les lésions dysplasiques non polypoïdes (lésion planes Paris II) sans stigmates de cancer invasif peuvent être traitées par résection endoscopique classique (pour une taille< 2 cm) ou une dissection sous-muqueuse (pour une taille> 2 cm) par des endoscopistes formés, dans des cas sélectionnés, à condition qu’il n’y ait pas de preuve de dysplasie multifocale ou invisible ailleurs dans la L’objectif est une résection complète en monobloc.
- Une intervention chirurgicale doit être proposée lorsque les lésions dysplasiques ne peuvent pas être réséquées par endoscopie.
- Les facteurs qui peuvent rendre la résection endoscopique impossible ou défavorable sont les frontières indistinctes, le grade de dysplasie détecté lors de l’analyse de la biopsie (adénocarcinome) et la preuve d’une dysplasie multifocale ou invisible ailleurs.
- Les polypes en dysplasie qui surviennent dans une « zone non colitique », sans implication de la maladie au niveau macroscopique ou histologique, doivent être considérés comme des adénomes sporadiques et faire l’objet d’une résection endoscopique.
Chez les patients atteints de MICI la récidive locale et métachrone est fréquente dans les études en base de population. Dans une méta-analyse explorant les taux de cancers synchrones incidents dans les pièces de résection de colectomie chez les patients atteints de MICI à l’ère du dépistage par coloscopie et chromoendoscopie, les taux de cancers synchrones étaient de 13,7 % chez les patients ayant déjà présenté une dysplasie de haut grade et de 2,7 % chez les patients ayant déjà présenté une dysplasie de bas grade (21). Ainsi, lorsque la résection endoscopique est effectuée à la place de la chirurgie, la surveillance est non seulement essentielle pour détecter la récidive locale, mais aussi pour évaluer les lésions synchrones potentiellement manquées lors de la coloscopie initiale.
Les recommandations concernant la surveillance des lésions en zone colitique (14) proposent en cas de résection de lésions< 2 cm de haut grade et de lésion> 2 cm quel que soit le grade de dysplasie une première coloscopie de surveillance à 3 mois puis une surveillance annuelle. Pour les lésions de taille< 2 cm de bas grade, une surveillance à 6 mois puis annuelle est proposée. Les lésions adénomateuses sporadiques doivent quant à elles être surveillées selon les consensus classique hors MICI.
Conclusion
La coloscopie n’est plus un examen de routine pour la surveillance de l’activité des MICI, mais l’est pour la surveillance de la dysplasie. Elle a démontré son efficacité dans la réduction du risque de cancer pour nos patients, car elle permet le dépistage et maintenant très souvent le traitement des lésions pré-néoplasiques et dans des cas sélectionnés le traitement des lésions néoplasiques précoces. Le point clef à retenir est que la prise en charge de la dysplasie dans les MICI repose sur une médecine personnalisée centrée sur le patient : il faudra déterminer le niveau de risque du patient, établir ses spécificités pour lui proposer le rythme de surveillance, le temps et les modalités d’examen adaptés. Ensuite, en cas de lésion dysplasique non sporadique, la proposition d’un traitement endoscopique sera faite à l’issue de l’évaluation endoscopique spécialisée de la lésion et prendra en compte le terrain du patient, le côlon environnant et l’histoire de la MICI. Les décisions de traitement et de surveillance des lésions dysplasiques inflammatoires doivent être prises en concertation avec des spécialistes en MICI, en endoscopie et des chirurgiens.
Références
- Jess T, Rungoe C, Peyrin-Biroulet Risk of colorectal cancer in patients with ulcerative colitis: a meta-analysis of population-based cohort studies. Clin Gastroenterol Hepatol 2012;10:639–645.
- Choi WT, Yozu M, Miller GC, et al. Nonconventional dysplasia in patients with inflammatory bowel disease and colorectal carcinoma: a multicentre clinicopathologic study. Modern Pathology (2020) 33:933–943.
- Rajamäki K, Taira A, Katainen R, et al. Genetic and Epigenetic Characteristics of Inflammatory Bowel Disease-Associated Colorectal Gastroenterology. 2021;161:592-607.
- Choi C-HR, Rutter MD, Askari A, et Forty-Year Analysis of Colonoscopic Surveillance Program for Neoplasia in Ulcerative Colitis: An Updated Overview. Am J Gastroenterol 2015;110:1022–1034.
- Ananthakrishnan AN, Cagan A, Cai T, et Colonoscopy is Associated with a Reduced Risk for Colon Cancer and Mortality in Patients with Inflammatory Bowel Diseases. Clin Gastroenterol Hepatol. 2015
- Kader R, Hadjinicolaou AV, Burr NE, et al. Systematic Review and Meta-analysis: The Three-year Post-colonoscopy Colorectal Cancer Rate as per the World Endoscopy Organization Methodology. Clin Gastroenterol Hepatol. 2024 27:S1542-3565.
- Beaugerie L, Svrcek M, Seksik P, et Risk of colorectal high-grade dysplasia and cancer in a prospective observational cohort of patients with inflammatory bowel disease. Gastroenterology 2013 ; 145 : 166-75
- Wijnands AM, de Jong ME, Lutgens M, et al. Prognostic Factors for Advanced Colorectal Neoplasia in Inflammatory Bowel Disease: Systematic Review and Meta-analysis. Gastroenterology 2021;160:1584–1598.
- Wan J, Wang X, Zhang Y, et Systematic review with meta-analysis: incidence and factors for progression to advanced neoplasia in inflammatory bowel disease patients with indefinite and low-grade dysplasia. Aliment Pharmacol Ther. 2022 ;55:632-644.
- Fumery M, Dulai PS, Gupta S, Prokop LJ, Ramamoorthy S, Sandborn WJ, et al. Incidence, Risk Factors, and Outcomes of Colorectal Cancer in Patients With Ulcerative Colitis With Low-Grade Dysplasia: A Systematic Review and Meta-analysis. Clin Gastroenterol 2017;15:665-674
- Zheng H-H, Jiang X-L. Increased risk of colorectal neoplasia in patients with primary sclerosing cholangitis and inflammatory bowel disease: a meta- analysis of 16 observational studies. Eur J Gastroenterol Hepatol 2016; 28 :383-90.
- Amiot A, Viennot S, Uzzan M, et Recommandations de pratique pour le diagnostic et la prise en charge de la rectocolite hémorragique. Hépato-Gastro et Oncologie Digestive 2022 ; 29 : e297-e351.
- Briot C, Faure P, Parmentier AL, and the CLEAN Study Group. Efficacy, Tolerability, and Safety of Low-Volume Bowel Preparations for Patients with Inflammatory Bowel Diseases: The French Multicentre CLEAN Study. J Crohns Colitis. 2019 19;13:1121-1130.
- Gordon H, Biancone L, Fiorino G, et ECCO Guidelines on Inflammatory Bowel Disease and Malignancies. Journal of Crohn’s and Colitis, 2023, 17, 827–854.
- Laine L, Kaltenbach T, Barkun A, et SCENIC international consensus statement on surveillance and management of dysplasia in inflammatory bowel disease. Gastrointest Endosc 2015;81:489–501.
- Dekker E, Nass K, Iacucci M, et al. Performance measures for colonoscopy in inflammatory bowel disease patients: European Society of Gastrointestinal Endoscopy (ESGE) Quality Improvement Initiative. Endoscopy 2022; 54:904-915.
- Moussata D, Allez M, Cazals-Hatem D; the Are random biopsies still useful for the detection of neoplasia in patients with IBD undergoing surveillance colonoscopy with chromoendoscopy? Gut. 2018;67:616-624.
- Cassinotti A, Fociani P, Duca P, et al. Modified Kudo classification can improve accuracy of virtual chromoendoscopy with FICE in endoscopic surveillance of ulcerative colitis. Endosc Int Open. 2020 ;8:E1414-E1422.
- Iacucci M, McQuaid K, Gui XS, et A multimodal (FACILE) classification for optical diagnosis of inflammatory bowel disease associated neoplasia. Endoscopy. 2019;51:133-141.
- Geyl S, Jacques J, Anneraud A, et Endoscopic submucosal dissection for visible dysplasia in IBD patients: A nationwide multicenter cohort from the GETAID and the SFED. Journal of Crohn’s and colitis. In press.
- Kabir M, Fofaria R, Arebi N, et Systematic review with metaanalysis: IBD-associated colonic dysplasia prognosis in the videoendoscopic era [1990 to present]. Aliment Pharmacol Ther 2020;52:5–19.