LIENS D’INTÉRÊTS
Non communiqués
MOTS-CLÉS
Hernie hiatale ; Reflux Gastro Œsophagien ; Fundoplicature
ABRÉVIATIONS
EOGD : Endoscopie œsogastroduodénale JOG : Jonction œsogastrique
RGO : Reflux gastro-œsophagien
SIO : Sphincter inferieur de l’œsophage TOGD : transit œsogastroduodénal
Définition et classification
Définition
La hernie hiatale se définit par le passage (partiel ou total) de structures abdominales (généralement une portion de l’estomac) à travers l’orifice hiatal du diaphragme vers la cavité thoracique
Classification
On distingue quatre types de hernies hiatales, décrits par la classification « A, B, C, D » ou la classification classique « I, II, III, IV » (les deux sont très proches, la première étant davantage utilisée dans certains pays anglo-saxons) (annexe 1).
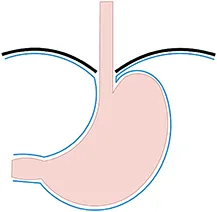
- Type I ou hernie par glissement : la jonction est remontée en intrathoracique mais le fundus gastrique reste en dessous de la jonction. L’estomac conserve son orientation C’est le type le plus fréquent (environ 80 à 90 % des cas) et le plus souvent associé à un reflux gastro-œsophagien (RGO).
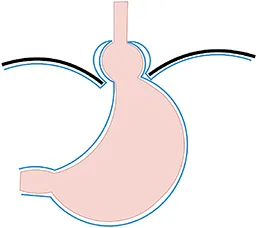
- Type II ou hernie par roulement : La jonction œsogastrique (JOG) reste en place au niveau du diaphragme, mais une partie du fundus gastrique passe à travers l’orifice hiatal le long de l’œsophage. Cette forme expose à un risque plus élevé d’étranglement, même si le reflux peut parfois être moins prononcé.
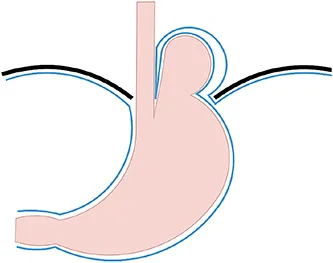
- Type III Combinaison des types I et II : la JOG et une portion du fundus sont ascensionnés au-dessus du diaphragme et le fundus est au-dessus de la jonction remontant le long de l’œsophage. Cette forme est souvent symptomatique et à haut risque de complications.
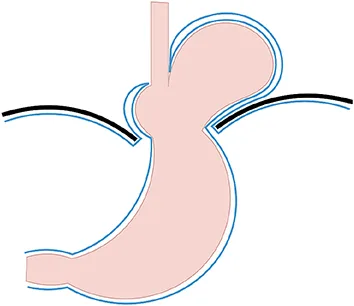
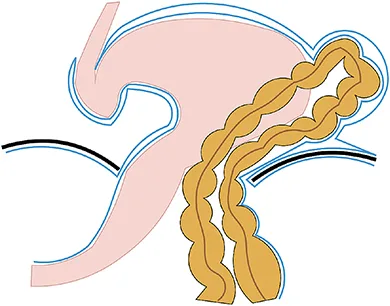
- Type IV : Forme la plus complexe : d’autres organes (côlon, grand épiploon, pancréas, rate, intestin grêle) peuvent remonter dans le thorax en plus de l’estomac. C’est la forme la plus rare mais potentiellement grave.
Les Types I et III sont le plus souvent associés à un RGO.
Les Types II et III forment le groupe de hernies para-œsophagiennes et ont une forme de présentation clinique assez similaire sous la forme de conflit hiatal.
Le Type IV regroupe les hernies hiatales complexes avec une symptomatologie variable en fonction de leur configuration et des organes herniés.
Annexe 1 : Types de hernies hiatales





Épidémiologie
Les hernies hiatales sont très fréquentes, surtout dans la population occidentale.
Leur prévalence augmente avec l’âge : on estime qu’au-delà de 50 ans, une proportion importante de la population peut présenter une hernie hiatale [jusqu’à 50 % dans les études endoscopique, 80 % dans des études autopsiques (1)]. Le type I (glissement) est de loin le plus fréquent (80-90 %).
L’augmentation croissante de l’obésité dans la population générale participe à l’augmentation de la fréquence d’observation des hernies hiatales par augmentation des pressions abdominales (2).
Physiopathologie et facteurs de risque
Le développement d’une hernie hiatale s’explique par la combinaison d’un ou plusieurs facteurs :
- L’augmentation de la pression intra-abdominale : L’obésité, la grossesse, l’ascite, la toux chronique, les efforts de vomissements ou éternuements répétés exposent au risque de développer une hernie hiatale.
- La faiblesse des structures de soutien (3) : les piliers du diaphragme peuvent être affaiblis par des facteurs congénitaux portant sur des anomalies du tissu conjonctif (4) ou acquis comme le vieillissement, l’intoxication tabagique, le traumatisme (accident, chirurgie) ou par la soumission à une hyperpression abdominale chronique. La détérioration progressive des tissus facilite la migration de la JOG.
- Le brachy-œsophage (5) ou œsophage court est une entité clinique accompagnant certaines hernies hiatales. Il existe de rares formes congénitales. Le brachy-œsophage est le plus souvent acquis secondairement aux séquelles d’inflammations chroniques, engendrant perte d’élasticité et fibrose de la musculature de l’œsophage, – provoquant un raccourcissement progressif et une attraction de la JOG en
Manifestations cliniques
La hernie hiatale est le plus souvent asymptomatique et découverte de manière fortuite sur un examen endoscopique ou bien visualisée sur un examen d’imagerie.
Les manifestations cliniques pouvant accompagner une hernie hiatale peuvent être les suivantes :
- Le Reflux gastro-œsophagien (RGO) : Il se manifeste le plus souvent par un pyrosis en rapport avec une brûlure de l’œsophage par le contenu acide de l’estomac, et les régurgitations qui peuvent aller de la simple sensation de remontée alimentaire dans l’œsophage et la bouche, à des inhalations compliquées de pneumopathies. Le RGO est très fréquent dans les hernies de type I. Le glissement de la JOG au travers du hiatus œsophagien altère le fonctionnement de la barrière anti-reflux composée d’éléments anatomiques et fonctionnels, principalement le sphincter inférieur de l’œsophage (SIO) et le diaphragme (6). La perte des moyens de fixation de JOG par élongation des tissus altère l’anatomie de l’angle de His, et en conséquence le bon fonctionnement du SIO. Par ailleurs, le régime de pressions inversé entre la cavité thoracique et la cavité abdominale favorise le RGO et le développement d’une hernie hiatale. La contraction du muscle diaphragmatique pendant la phase inspiratoire engendre une dépression à l’étage sus diaphragmatique et une hyperpression à l’étage sous diaphragmatique. Le contenu gastrique abdominal est écrasé et remonte dans l’estomac hernié favorisant le reflux.
- La dysphagie : la dysphagie est observée en cas de conflit hiatal, que l’on observe plus fréquemment dans les hernies de grande taille altérant la vidange de l’œsophage ou du contenu gastrique hernié.
- Douleurs thoraciques ou épigastriques : plus fréquemment observées dans les hernies para œsophagiennes. L’engouement gastrique au travers du hiatus peut entraîner une douleur par mise en tension, jusqu’à une souffrance ischémique. Devant une douleur thoracique, après avoir éliminé une cause cardiaque ou pulmonaire, il faut penser à rechercher une hernie hiatale potentiellement compliquée. Le remplissage du contenu gastrique hernié peut aussi comprimer les organes adjacents, les cavités cardiaques, les bases pulmonaires, entraînant des manifestations atypiques orientant vers des troubles cardiaques d’où l’importance de l’examen diagnostique différentiel.
- Anémie par ulcération ischémique de la muqueuse gastrique en regard du collet hiatal (lésion de Cameron) (7) : Les lésions de Cameron sont des érosions ou ulcérations linéaires de la muqueuse gastrique (corps ou fundus) qui surviennent principalement chez les patients ayant une hernie hiatale, notamment de grande taille (> 5 cm). Elles résultent de la combinaison d’une ischémie locale due à la pression du diaphragme sur le sac hiatal et de l’agression acide gastrique sur la zone fragilisée. Les mouvements respiratoires aggravent l’effet mécanique de constriction. Leur fréquence varie de 1 % (petites hernies) jusqu’à 13 % (hernies de grande taille). Elles peuvent provoquer un saignement microscopique (responsable d’anémie ferriprive) ou un saignement manifeste (hématémèse, méléna). Le diagnostic est souvent difficile : les lésions, parfois discrètes ou transitoires, peuvent échapper à l’endoscopie. Dans le bilan d’une anémie ferriprive dont le bilan étiologique a éliminé les causes fréquentes de saignement digestif, l’existence d’une hernie hiatale doit faire discuter son imputabilité et l’introduction d’un traitement médical voir chirurgical.
- Complications aiguës (surtout dans les hernies de type II, III, IV) : Le volvulus gastrique est la complication la plus redoutée dans les grandes hernies hiatales. Cette situation rare complique 4 % des hernies hiatales, c’est une urgence absolue car le risque de mortalité est élevé (30 %) par ischémie voire nécrose gastrique (8). Dans les hernies de type IV, tout organe ascensionné peut s’engouer et souffrir d’une ischémie.
Diagnostic
- l’endoscopie œsogastroduodénale (EOGD) est l’examen de première intention pour évaluer la muqueuse œsophagienne, la JOG et l’estomac. La constatation d’une œsophagite et sa gradation peut être observée chez un patient souffrant d’un reflux acide pathologique favorisé par une hernie L’examen doit par ailleurs rechercher un endobrachyœsophage et le biopsier pour confirmation histologique de la métaplasie et rechercher une dysplasie exposant au risque de dégénérescence. L’endoscopie peut visualiser une hernie hiatale, mais l’estimation de sa taille peut être difficile. Par ailleurs, la constatation endoscopique ne se traduit par forcément par une objectivation morphologique radiologique ou lors de l’exploration chirurgicale. L’endoscopie peut visualiser les ulcérations de la muqueuse gastrique accompagnant une hernie hiatale (Cameron). L’endoscopie peut évoquer également l’existence d’un brachy-œsophage par mesure externe sur l’endoscope de la position de la ligne Z.
- Transit baryté (TOGD) est un examen radiologique balisé simple permettant la visualisation de l’œsophage et de l’estomac. Cet examen est utile pour caractériser le type de hernie (glissement para-œsophagienne), pour évaluer la dynamique de la déglutition et l’existence d’un reflux, et pour évaluer la longueur de l’œsophage (rechercher un brachy-œsophage). Il ne donne pas d’information sur la configuration anatomique de l’anneau hiatal ou l’association d’autres organes herniés dans les types IV.
- La pH-métrie œsophagienne sur 24 heures est l’examen qui confirme et quantifie le reflux acide (temps d’exposition acide et score de Meester). La pH-métrie n’a pas d’intérêt pour le diagnostic d’une hernie hiatale, mais a un intérêt thérapeutique pouvant conditionner le geste opératoire. La pH-métrie peut être demandée dès qu’un reflux gastro œsophagien est évoqué chez un patient rapportant un pyrosis ou des régurgitations en l’absence de complication du reflux telles qu’une œsophagite peptique grade B ou la constatation d’un endobrachyœsophage signant le reflux acide pathologique. Plus largement une pH-métrie doit être demandée dans le bilan préopératoire d’une hernie hiatale pour rechercher un reflux acide pathologique frustre ou au second plan des plaintes, et permettre d’adapter le geste opératoire par confection d’une valve anti-reflux en cas de hernie hiatale relevant d’une indication chirurgicale.
- La manométrie œsophagienne évalue le fonctionnement du sphincter inférieur de l’œsophage et de la motricité œsophagienne. Cet examen est très utile dans le bilan préopératoire chez un patient présentant un RGO pathologique associé à la hernie hiatale, pour ne pas méconnaître un trouble du péristaltisme œsophagien exposant au risque de dysphagie postopératoire après fundoplicature.
- Le scanner thoraco-abdominal est l’examen de référence à visée morphologique, il permet de confirmer l’existence ou non d’une hernie hiatale, précise son type et évalue la longueur œsophagienne à la recherche d’un brachy œsophage. Il permet la mesure de la surface du défect hiatal, observe la vascularisation et d’éventuelles complications (strangulation, ischémie).
Traitement
L’indication opératoire.
Il est important de distinguer les hernies hiatales symptomatiques des formes asymptomatiques découvertes fortuitement.
Dans les formes symptomatiques, il faut distinguer les hernies hiatales accompagnant un RGO pathologique symptomatique dans les formes par glissement, et les hernies hiatales symptomatiques responsables d’une autre gêne au premier plan (dysphagie, douleur, anémie) dans les formes para œsophagiennes
Hernie hiatale par glissement (type I) asymptomatique
Aucune opération n’est recommandée en l’absence de symptômes. Seule une fraction réduite de patients pourra développer ultérieurement des signes cliniques ne justifiant pas d’une chirurgie préventive.
Hernie hiatale par glissement (type I) accompagnant un reflux gastro œsophagien
L’indication opératoire repose sur le reflux acide pathologique, et non pas sur la hernie elle-même. La présence d’une hernie hiatale (le plus souvent de type I, dans 30-50 % des RGO) est un facteur prédisposant au reflux. Toutefois un patient répondeur au traitement médical bien conduit et ne souffrant pas de régurgitation ou de complications du reflux (œsophagite peptique, EBO) ne nécessite pas forcément de traitement chirurgical. Le traitement médical par IPP tamponne l’acidité du reflux et peut parfaitement effacer le pyrosis, mais nécessite une prise régulière sur le long terme. Le traitement chirurgical a vocation à supprimer totalement le reflux, et par là même le pyrosis sans nécessité de poursuivre le traitement par IPP. La régurgitation relève d’un traitement chirurgical. Les patients répondeurs au traitement médical sont les meilleurs candidats à la chirurgie. Les dossiers des patients présentant une complication évolutive du RGO doivent être discutés pour un traitement chirurgical. Si l’option chirurgicale est retenue, le geste anti-reflux doit nécessairement combiner la réparation d’une hernie hiatale à une fundoplicature.
Hernie hiatale para œsophagienne (type II III IV) asymptomatique
La discussion de l’indication opératoire portera autour de la balance bénéfice/risque entre une prise en charge prophylactique et l’évolution naturelle de la hernie hiatale. Le terrain du patient, l’âge, les comorbidités, la taille de la hernie hiatale et les difficultés opératoires présumées seront à évaluer. Le risque opératoire est très faible avec une mortalité inférieure à 1 %, mais le risque de complication évolutive est assez faible 2-5 %. Toutefois en cas de complication aiguë le risque de mortalité est significatif pouvant monter jusqu’à 30 %.
Hernie hiatale para œsophagienne (type II III IV) symptomatique
L’indication opératoire est justifiée, car le risque de complications sévères est augmenté. Les complications telles que le volvulus gastrique, l’hémorragie digestive, l’étranglement d’une viscère abdominal hernié peuvent conduire à une intervention en urgence s’accompagnant d’une morbi mortalité significative, d’où l’intérêt de traiter les patients dès qu’ils sont symptomatiques. Dans ce cas l’indication opératoire repose sur la hernie hiatale elle-même. Le reflux gastro-œsophagien peut y être associé mais n’est pas au premier plan. Le bilan préopératoire doit cependant rechercher un RGO pathologique qui devra être traité dans le même temps que la hernie hiatale, pour adapter au mieux le geste.
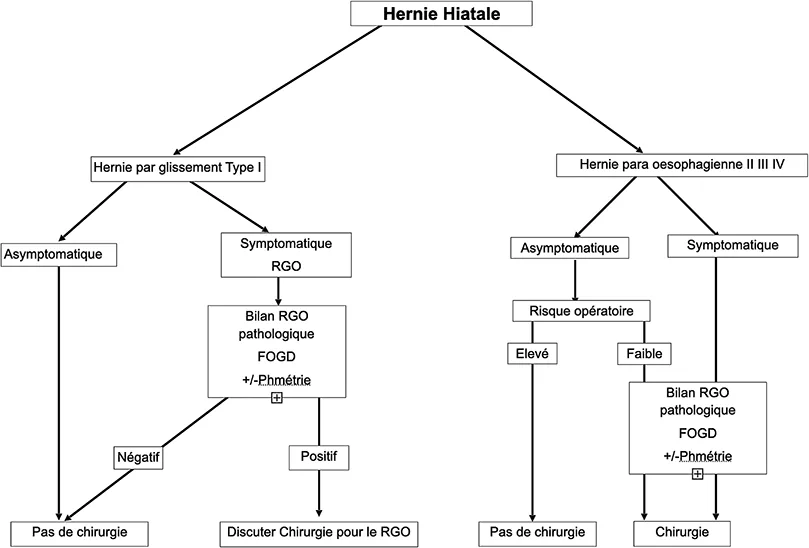
Le diagramme décisionnel résume les indications opératoires. (Annexe 2)
Annexe 2 : Diagramme décisionnel pour la prise en charge d’une hernie hiatale

Le traitement chirurgical
Il existe une grande variabilité dans les approches chirurgicales rendant difficile l’analyse des données publiées dans la littérature.
Toutefois, il existe un consensus général pour reconnaître la supériorité de la voie laparoscopique par rapport à la chirurgie ouverte, tant en termes de complications que de durée d’hospitalisation et de qualité de vie (9).
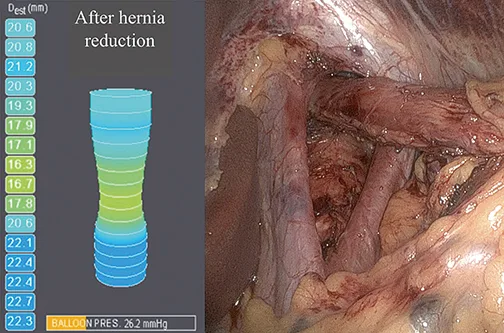
L’intervention chirurgicale comporte plusieurs étapes : réduction herniaire en position abdominale, curoplastie, fundoplicature. Chaque étape participe significativement à améliorer la barrière anti reflux (10) (annexes 3) et prévenir la récidive herniaire.
Annexe 3



Réduction de la hernie
Le hiatus œsophagien doit être disséqué, avec identification des piliers droit et gauche. Le sac péritonéal accompagnant la hernie hiatale doit être totalement libéré du médiastin et idéalement réséqué dans son intégralité (9) pour prévenir le risque de récidive. L’œsophage, l’estomac, les plèvres, le péricarde, les piliers diaphragmatiques, et les nerfs vagues cheminant sur les faces antérieure et postérieure de l’œsophage doivent être identifiés et respectés.
La réintégration en place abdominale de la JOG sans tension nécessite une mobilisation de l’œsophage médiastinal inférieur jusqu’aux veines pulmonaires inférieures.
Dans le cas d’un brachy-œsophage ne permettant pas la réintégration de la JOG en position abdominale sans tension malgré une dissection médiastinale poussée, une plastie d’allongement œsophagien peut être nécessaire par résection atypique et tubulisation du fundus gastrique sur un tube de calibration [colli-Nissen (11)]. Cet artifice permet d’allonger l’œsophage par un tube gastrique, l’estomac retrouvant sa place en position abdominale.
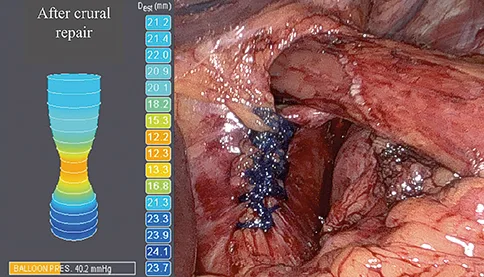
Cruroplastie
Une fois l’estomac et la jonction en place abdominale sans tension, le geste se poursuit par une plastie hiatale ou cruroplastie. Ce temps consiste en la recalibration du hiatus au passage œsophagien par une suture (raphie) rapprochant les berges du hiatus. En fonction des constatations opératoires, notamment la mesure peropératoire de la surface du défect hiatal ainsi que l’évaluation de la trophicité des piliers diaphragmatiques, la raphie hiatale peut être renforcée par un implant prothétique pour limiter le risque de récidive herniaire. L’utilisation d’une prothèse dans la réparation de la hernie hiatale reste un sujet débattu (12), le bénéfice en termes de diminution du taux de récidive étant à pondérer avec le risque de complication sur le matériel implanté (infection, migration). Toutefois l’utilisation de prothèses biosynthétiques (13) lentement résorbables semble prometteuse s’affranchissant des principaux risques redoutés avec les implants synthétiques non résorbables.
Fundoplicature
Dans le cas d’une hernie hiatale de type I symptomatique avec un reflux acide pathologique, la confection d’une valve anti-reflux est une étape indispensable. Le plus souvent, il est réalisé une valve postérieure qui peut être partielle [Toupet (14)] ou circonférentielle [Nissen(15)], plus rarement une valve antérieure [Dor (16)]. À ce jour il n’y a pas de différence démontrée en termes d’efficacité sur le reflux entre les valves postérieures partielles ou circonférentielles, mais il est observé moins de dysphagie après une fundoplicature partielle (17).
La confection d’une valve anti-reflux est également retenue de manière systématique pour la cure d’une hernie hiatale para œsophagienne sans reflux ressenti ou retrouvé sur les explorations, en prévention d’un RGO qui pourrait survenir ultérieurement une fois la hernie réduite (9, 18). On considère par ailleurs que la fundoplicature postérieure pourrait également mécaniquement participer au maintien de la JOG en bonne position abdominale limitant la migration au travers de la plastie hiatale.
La gastropexie
La fixation de l’estomac aux structures adjacentes dans l’abdomen a une place très limitée, en raison de la faible efficacité et du risque de récidive herniaire important. Il peut être proposé en alternative à la fundoplicature pour les patients fragiles (19).
Résultats de la chirurgie
La morbi mortalité de la chirurgie de hernie hiatale est très faible, inférieure à 1 %.
Les conséquences fonctionnelles sont dominées par celles de la chirurgie du reflux : dysphagie le plus souvent transitoire en raison de l’œdème postopératoire majorant la compression de l’œsophage abdominal (20), et le gaz bloating (20).
L’analyse des résultats de la prise en charge chirurgicale est rendue difficile par la diversité des interventions rapportées dans la littérature et l’absence de standardisation des prises en charge. Par ailleurs, il n’existe pas de critères strictement objectifs pour mesurer la réussite d’intervention, hormis la perception subjective du patient (9). Les taux de récidive documentée par radiologie oscillent entre 15 % et 66 % (9), cependant les récidives semblent le plus souvent pauci symptomatiques. En l’absence de plainte clinique, aucun examen de suivi spécifique n’est préconisé. En revanche, chez les patients qui présentent à nouveau des symptômes et dont la récidive est confirmée radiologiquement, une nouvelle intervention peut être proposée.
Bien qu’il s’agisse d’un défi chirurgical, la réapparition du problème nécessite une réintervention, réduction itérative d’une récidive herniaire, identification et correction d’un brachy-œsophage si méconnu lors de l’intervention initiale, réparation itérative du défect hiatal avec discussion de la pose d’un renfort prothétique, démontage puis réfection de la fundoplicature.
Conclusion
La hernie hiatale, affection très fréquente dont la prévalence augmente avec l’âge et l’obésité, peut se présenter sous des formes cliniques variées, allant de l’asymptomatique à des tableaux sévères (volvulus, ischémie). Son diagnostic repose sur des examens complémentaires adaptés à chaque situation (endoscopie, transit baryté, pH-métrie, manométrie, scanner).
La prise en charge doit être individualisée : un traitement médical (inhibiteurs de pompe à protons, règles hygiéno-diététiques) suffit souvent dans les formes de type I associées à un reflux bien contrôlé, tandis que les hernies para-œsophagiennes (types II, III, IV) ou symptomatiques justifient plus volontiers une approche chirurgicale. Les avancées technologiques, notamment la cœlioscopie, permettent aujourd’hui de réduire la morbidité opératoire et d’améliorer le confort des patients. Malgré un risque de récidive pouvant atteindre 15 % à 66 % selon les séries, le taux de complications cliniquement significatives reste relativement bas.
En définitive, la reconnaissance précoce des hernies hiatales et l’adaptation du traitement en fonction du type de hernie, de la présence de symptômes et de la balance bénéfice/risque demeurent les clés d’une prise en charge optimale.
Bibliographie
- Roman, & Kahrilas, P. J. The diagnosis and management of hiatus hernia. BMJ 349, g6154 (2014).
- Wilson, J., Ma, W. & Hirschowitz, B. I. Association of obesity with hiatal hernia and esophagitis. Am. J. Gastroenterol. 94, 2840–2844 (1999).
- Fei, et al. Hiatal hernia recurrence : surgical complication or disease ? Electron microscope findings of the diaphragmatic pillars. J. Gastrointest. Surg. Off. J. Soc. Surg. Aliment. Tract 13, 459–464 (2009).
- von Diemen, , Trindade, E. N. & Trindade, M. R. M. Hiatal hernia and gastroesophageal reflux : Study of collagen in the phrenoesophageal ligament. Surg. Endosc. 30, 5091–5098 (2016).
- Lugaresi, et al. The frequency of true short oesophagus in type II-IV hiatal hernia. Eur. J. Cardio-Thorac. Surg. Off. J. Eur. Assoc. Cardio- Thorac. Surg. 43, e30-36 (2013).
- Yassi, et al. Modeling of the mechanical function of the human gastroesophageal junction using an anatomically realistic three-dimensional model. J. Biomech. 42, 1604–1609 (2009).
- Brar, S., Aloysius, M. M. & Shah, N. J. Cameron Lesions. In StatPearls (StatPearls Publishing, Treasure Island (FL), 2025).
- Light, , Links, D. & Griffin, M. The threatened stomach : management of the acute gastric volvulus. Surg. Endosc. 30, 1847–1852 (2016).
- Peters, H. SAGES guidelines for the management of hiatal hernia. Surg. Endosc. 27, 4407–4408 (2013).
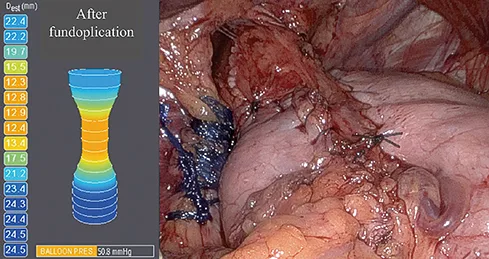
- Su, et al. Using impedance planimetry (EndoFLIPTM) in the operating room to assess gastroesophageal junction distensibility and predict patient outcomes following fundoplication. Surg. Endosc. 34, 1761–1768 (2020).
- Horvath, D., Swanstrom, L. L. & Jobe, B. A. The short esophagus : pathophysiology, incidence, presentation, and treatment in the era of laparoscopic antireflux surgery. Ann. Surg. 232, 630–640 (2000).
- Johnson, M. et al. Laparoscopic mesh hiatoplasty for paraesophageal hernias and fundoplications : a critical analysis of the available literature. Surg. Endosc. 20, 362–366 (2006).
- Lima, L. et al. Hiatal hernia repair with biosynthetic mesh reinforcement : a qualitative systematic review. Surg. Endosc. 37, 7425–7436 (2023).
- Toupet, [Technic of esophago-gastroplasty with phrenogastropexy used in radical treatment of hiatal hernias as a supplement to Heller’s operation in cardiospasms]. Memoires Acad. Chir. Fr. 89, 384–389 (1963).
- Nissen, [A simple operation for control of reflux esophagitis]. Schweiz. Med. Wochenschr. 86, 590–592 (1956).
- Dor, , Humbert, P., Paoli, J. M., Miorclerc, M. & Aubert, J. [Treatment of reflux by the so-called modified Heller-Nissen technic]. Presse Med. 75, 2563–2565 (1967).
- Broeders, a. J. L. et al. Systematic review and meta-analysis of laparoscopic Nissen (posterior total) versus Toupet (posterior partial) fundoplication for gastro-oesophageal reflux disease. Br. J. Surg. 97, 1318–1330 (2010).
- Bonrath, M. & Grantcharov, T. P. Contemporary management of paraesophaegeal hernias : establishing a European expert consensus. Surg. Endosc. 29, 2180–2195 (2015).
- Daigle, R. et al. Laparoscopic repair of paraesophageal hernia with anterior gastropexy : a multicenter study. Surg. Endosc. 29, 1856–1861 (2015).
- Richter, E. Gastroesophageal reflux disease treatment : side effects and complications of fundoplication. Clin. Gastroenterol. Hepatol. Off. Clin. Pract. J. Am. Gastroenterol. Assoc. 11, 465–471 ; quiz e39 (2013).