Lien d’intérêts
Le projet SURVI est soutenu financièrement par MSDAvenir.
Mots-clés
Ischémie mésentérique ; ischémie intestinale ; urgences vasculaires intestinales ; angor mésentérique
Abréviations
IMA : ischémie mésentérique aiguë, ESC : European Society of Cardiology, ESPEN : European Society of Parenteral and Enteral Nutrition, WSES : World Society of Emergency Surgery, ACR : American College of Radiology, ESVS : European Society of Vascular Surgery, VALDIG : Vascular Liver Disease Group, CMV : cytomégalovirus, AMS : artère mésentérique supérieure, IPP : inhibiteurs de la pompe à protons, SIRS : syndrome inflammatoire de réponse systémique
Introduction
L’ischémie mésentérique aiguë (IMA) est une urgence vitale, vasculaire et digestive, parmi les plus graves. Bien qu’elle concerne une large population à risque cardiovasculaire, elle reste sous-étudiée, en raison de difficultés diagnostiques et du manque de cohortes bien caractérisées. Son incidence en Europe est estimée à 10 pour 100 000 personnes-années, comparable à celle du cancer du pancréas ou de la maladie de Crohn, et augmente exponentiellement avec l’âge, passant respectivement de 25 à 217 pour 100 000 chez les plus de 70 ans à 85 ans (1, 2).
Comme le cœur et le cerveau, l’intestin est un organe vital doté d’une vascularisation terminale particulièrement vulnérable à l’hypoperfusion. Celle-ci entraîne rapidement une ischémie puis une nécrose intestinale irréversible (infarctus), aggravée par une composante infectieuse propre à l’intestin. Cette cascade pathologique, souvent imprévisible, reste associée à une mortalité très élevée, atteignant 60 % selon la cohorte internationale AMESI en 2023, soit 6 fois celle de l’infarctus du myocarde et 2 fois celle du choc septique, ou à des séquelles intestinales majeures chez les survivants (3). Ces évolutions défavorables sont principalement dues à un retard ou à une insuffisance du traitement, en l’absence de critères diagnostiques fiables et de centres spécialisés. Il est donc crucial de reconnaître et traiter l’IMA à un stade réversible (4). En l’absence de biomarqueur disponible, cette démarche nécessite un haut degré de suspicion diagnostique devant toute douleur abdominale et la conduite d’une thérapeutique d’urgence visant deux objectifs majeurs et indissociables : sauver l’intestin pour sauver la vie (5). Ainsi, l’hépato-gastroentérologue devrait occuper un rôle central dans la prise en charge de l’IMA, ses manifestations, ses complications et ses séquelles étant intégralement digestives. Cet article propose une synthèse des actualités et recommandations pour la prise en charge de l’IMA en 2025, incluant les guidelines de l’European Society of Cardiology (ESC, 2024) (6), de l’European Society of Parenteral and Enteral Nutrition (ESPEN, 2023) (7), de la World Society of Emergency Surgery (WSES, 2022) (8), de l’American College of Radiology (ACR, 2018) (9) et de l’European Society of Vascular Surgery (ESVS, 2017, actualisation prévue en 2025) (10), ainsi que les avis d’experts du Vascular Liver Disease Group (VALDIG, 2024) (11).
Rappels physiopathologiques et caractérisation de l’IMA
Recommandation
- La présentation clinique, les facteurs de risque et l’imagerie permettent de différencier les formes d’IMA : artérielles thrombotiques, emboliques, veineuses et non-occlusives (Grade IIIC, WSES 2022) (8). Cette distinction est essentielle pour identifier et traiter la cause cardiovasculaire ou thrombo-embolique sous-jacente (athérosclérose, cardiopathie emboligène, thrombophilie, vascularite).
L’IMA est définie par l’association 1) d’une insuffisance vasculaire mésentérique, et 2) d’une souffrance intestinale hypoxique, 3) en l’absence d’autre cause (5, 12). L’insuffisance vasculaire peut être occlusive, due à une embolie (50 %), une thrombose artérielle (25 %) ou veineuse (15 %), et confirmée par l’imagerie ; ou non occlusive (10 %), résultant d’un vasospasme, généralement associé à un contexte de bas débit systémique ou à l’utilisation de vasoconstricteurs (12, 13). Les principales causes sont résumées dans le tableau 1. La forme embolique est évoquée en présence d’une cardiopathie emboligène et/ou d’emboles synchrones fréquents (70 %), affectant notamment les membres inférieurs (27 %), les reins (18 %), le cerveau (15 %) ou la rate (10 %) (14). Les thromboses artérielles sont principalement dues à l’athérosclérose, suivie par les dissections et les vascularites. La thrombose porto-mésentérique peut compliquer une hypertension portale cirrhotique ou non. En l’absence d’hépatopathie, les causes sont souvent associées (15 à 36 % des cas) et justifient un bilan exhaustif recherchant des facteurs locaux (traumatique ou inflammatoire), des anomalies hématologiques (syndrome myéloprolifératif, déficits en anticoagulants, mutations génétiques) ou des causes générales (obésité, grossesse/ contraception hormonale, infection à COVID-19 ou CMV) (15). Dans 30 % des cas, aucune cause de thrombose porto-mésentérique n’est identifiée (11, 15).
Tableau 1 : Causes d’ischémie mésentérique et facteurs favorisants
| Ischémie mésentérique | Causes et facteurs favorisants à rechercher |
| Occlusive | Maladie vasculaire | – Athérome (principale cause) – Anévrysme, dissection – Dysplasie fibro-musculaire – Vascularites – Traumatisme vasculaires (manœuvres chirurgicale ou endovasculaires, arrachements, compression tumorale, notamment neuroendocrine) |
| Maladie pro- thrombotique ou embolique | – Thombophillie – Inflammation intra-abdominale ou systémique – Hypertension portale – Cardiopathie emboligène – Embolies de cholesterol |
| Non-occlusive | – Bas débit systémique (hypovolémie, choc, déplétion dialytique) – Clampages vasculaires, circulation extra-corporelle – Toxiques et iatrogénie (cocaïne, amphétamines, catécholamines) – Drépanocytose, leucostase – Effort intense et prolongé (marathon) |
L’artère mésentérique supérieure (AMS) est la principale artère, irriguant l’ensemble de l’intestin grêle et le côlon droit (tableau 2). Toute atteinte ischémique du côlon droit doit ainsi être considérée comme une IMA, et faire rechercher une lésion de l’AMS et du grêle associée (16-18). À l’inverse, l’artère mésentérique inférieure est souvent occluse de façon asymptomatique chez 10 % des plus de 60 ans, et 50 % des patients opérés pour anévrysme de l’aorte abdominale, en raison d’une suppléance vasculaire cœlio-mésentérique supérieure et iliaque (19-21). Ainsi, l’ischémie du côlon gauche (ou colite ischémique gauche) est à différencier de l’IMA, car elle est généralement transitoire, limitée au côlon, et liée à une ischémie-reperfusion microvasculaire (hypovolémie, vasoconstriction iatrogène ou hyperpression luminale/constipation), sans indication à une revascularisation.
Tableau 2 : Vascularisation et systématisation des lésions digestives ischémiques en fonction du mécanisme et du vaisseau impliqué
| Vaisseau Digestif | Organes vascularisés | Topographie des lésions digestives |
| Ischémie occlusive proximale (ex : thrombose athéromateuse) | Ischémie non occlusive ou occlusive distale (ex : embolies, vascularite) |
| Tronc coeliaque | Estomac, Duodénum Vésicule biliaire, Pancréas Foie, rate | Ulcères gastro-duodénaux Cholecystite, pancréatite Infarctus spléniques | Ischémie gastro-intestinale segmentaire et (multi) focale sans systématisation vasculaire |
| Artère et veine mésentérique supérieure | Jéjunum, iléon Côlons droit et transverse | Ischémie intestinale étendue et colite ischémique droite |
| Artère et veine mésentérique inférieure | Côlon gauche, haut rectum | Colite ischémique gauche épargnant le rectum |
L’hypoperfusion intestinale entraine une nécrose épithéliale débutant au sommet des villosités et progressant en profondeur, aggravée par l’inflammation et la rupture de la barrière épithéliale (22). L’invasion tissulaire et la translocation du microbiote transforme l’intestin ischémique en un foyer infectieux majeur (23). En l’absence d’une revascularisation rapide, la progression vers une nécrose transmurale irréversible entraîne une péritonite, un syndrome inflammatoire de réponse systémique (SIRS) et une défaillance multi-viscérale souvent fatale (24). Paradoxalement, la revascularisation peut aggraver les lésions et leur retentissement systémique par une explosion oxydative liée à l’ischémie-reperfusion. Des thérapies ciblant les mécanismes d’ischémie-reperfusion spécifiques de l’intestin pourraient réduire les complications digestives et systémiques, améliorer la cicatrisation muqueuse et la survie après IMA.
Reconnaître l’IMA au stade précoce
Recommandations
- Il n’existe aucun biomarqueur assez sensible et spécifique du diagnostic d’IMA, qui requiert un haut degré de suspicion Un lactate normal n’élimine pas la diagnostic (Grade IC, WSES 2022 et ESVS 2017) (8)
- Une douleur abdominale sévère, disproportionnée par rapport à l’examen physique, doit être considérée comme une IMA jusqu’à preuve du contraire. (Grade IC, WSES 2022) (8)
Contrairement aux idées reçues, la majorité des patients atteints d’IMA consultent à un stade précoce, potentiellement réversible, mais souvent sous- diagnostiqué. Près de 70 % ne présentent ni défaillance d’organe, ni abdomen chirurgical, ni élévation du lactate plasmatique, et pour un tiers, l’IMA constitue le premier événement vasculaire (25-28). La douleur abdominale aiguë, présente dans 95 % des cas, est typiquement brutale ou rapidement progressive, intense et résistante aux antalgiques de palier 2, souvent péri-ombilicale ou diffuse (12, 13, 29). Elle contraste avec une palpation abdominale initialement (faussement) rassurante. Dans 19 à 52 % des cas, elle succède à un angor mésentérique méconnu et non traité (25, 30). Elle peut s’accompagner de vomissements (48 %), diarrhée (31 %), hémorragie digestive (18 %) et d’un syndrome inflammatoire biologique (25, 27).
À ce jour, aucun test biologique ne permet de suspecter une IMA devant une douleur abdominale et d’orienter vers un angioscanner abdominal en urgence. Les biomarqueurs usuels (hyperleucocytose, lactate, CRP, LDH, CPK, D-Dimères) ou plus spécifiques de l’intestin (I-FABP, D-lactate, et citrulline) ont montré une faible performance diagnostique (31, 32, 33). Un lactate plasmatique normal, identifié comme facteur indépendant de retard diagnostique (34), peut faussement rassurer le clinicien, et ne devrait plus être utilisé pour exclure une IMA.
Une étude menée dans notre Structure d’URgences Vasculaires Intestinales (SURVI) à l’Hôpital Beaujon a identifié deux facteurs indépendamment associés à l’IMA devant une douleur abdominale aiguë : son caractère brutal et son intensité nécessitant l’administration de morphine (AUROC = 0,84) (28). Ni l’âge ni le terrain vasculaire n’était suffisamment discriminant en analyse multivariée. En appliquant ces critères à une prévalence de l’IMA estimée à 1 % chez les patients présentant une douleur abdominale aiguë, la probabilité d’IMA était d’environ 0,01 % pour un patient ne présentant aucun de ces facteurs et 10 % (multipliée par 100) en présence de ces deux paramètres. Ces résultats suggèrent que l’une de ces caractéristiques de la douleur abdominale (brutale ou morphino-requérante) justifie une suspicion diagnostique d’IMA et la réalisation d’un angioscanner en urgence, y compris chez des patients sans antécédent vasculaire (13, 28, 35). Le scanner permettra en outre d’écarter les principales urgences diagnostiques différentielles, telles qu’une pancréatite, une perforation, une occlusion intestinale, une dissection vasculaire ou encore une complication lithiasique biliaire ou rénale.
Confirmer le diagnostic par l’angioscanner triphasique
Recommandations
- Toute suspicion d’IMA nécessite un angioscanner abdominal triphasique en urgence (sans puis avec contraste aux temps artériel et portal) (Grade 1A à C, ESC 2024, WSES 2022, ACR 2018, ESVS 2017) (8, 9)
- En cas d’insuffisance rénale, l’angioscanner avec injection reste recommandé en raison du risque vital de méconnaître une (Grade IIC, ESVS 2017)
L’angioscanner abdomino-pelvien triphasique est l’examen de référence pour le diagnostic d’IMA, avec une sensibilité et une spécificité de 93 % à 100 % (9, 12, 36). Il doit être réalisé sans délai, même en cas d’insuffisance rénale, le risque lié à une injection de produit de contraste étant largement inférieur à celui de méconnaître une IMA (9, 12, 37). Dans une étude sur 55 IMA artérielles, aucun effet néphrotoxique sévère n’a été observé, malgré des injections répétées de produits de contraste (angioscanners et artériographies) et une insuffisance rénale aiguë initiale chez 50 % des patients (38). En revanche, le scanner sans injection, non diagnostique voire souvent faussement rassurant, est un facteur indépendant de retard diagnostique dans l’IMA et devrait être évité (34).
L’angioscanner confirme le diagnostic d’IMA en détectant 1) une occlusion ou une sténose> 70 % de l’AMS (significative même en cas d’opacification d’aval par la collatéralité), 2) des signes de souffrance intestinale (épaississement pariétal, diminution de rehaussement, iléus, pneumatose, aéroportie, ascite) et 3) l’absence d’autre cause d’abdomen aigu (figure 1) (25). Dans les formes très précoces d’IMA, les signes de souffrance intestinale peuvent être discrets (simple diminution du rehaussement, sans épaississement pariétal, fèces sign) ou exceptionnellement absents (39), et la suspicion d’IMA repose alors sur les lésions vasculaires significatives et l’absence d’autre cause d’abdomen aigu sur le scanner. L’angioscanner guide également la stratégie thérapeutique en précisant les lésions vasculaires nécessitant une revascularisation et les lésions intestinales potentiellement chirurgicales.

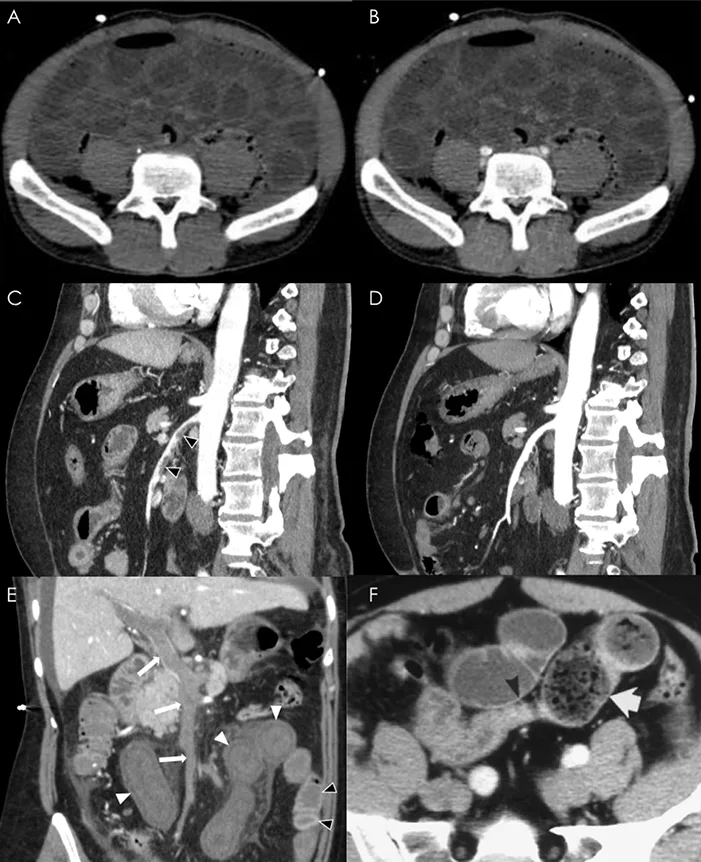
Figure 1 : L’angioscanner abdominal triphasique aux temps non injecté, artériel et portal
A-B : Coupes transversales, (A) montrant une hyperdensité de la paroi intestinale par souffrance/ suffusion hémorragique au temps non injecté, à ne pas confondre avec un rehaussement, dont l’aspect est inchangé après injection aux temps portal (B).
C-D : Coupes sagittales, temps artériel, sténose à 90 % par un thrombus aigu de l’artère mésentérique supérieure (flèche noires) avant (C) et après thrombolyse intra-artérielle (D).
E-F : Signes de nécrose intestinale. (E) Coupe frontale, temps portal, thrombose porto-mésentérique complète (flèches) associée à une dilatation et un défaut de rehaussement pariétal du jéjunum proximal (têtes de flèche blanches) en comparaison aux anses iléales normales (têtes de flèche noires). (F) Coupe transversale, temps portal, dilatation intestinale avec fécès sign (flèches).
En vie réelle, les performances de l’angioscanner sont néanmoins assez dépendantes de la probabilité clinique pré-test et de l’expertise du radiologue, avec des sensibilités diminuées à 72 % en cas de phase portale seule ou lorsque le radiologue n’est pas informé de la suspicion diagnostique (40, 41, 34). Dans le travail de Lehtimaki et al., le diagnostic était significativement amélioré lorsque la suspicion d’IMA était mentionnée sur la demande d’examen (97 % vs. 81 %, p=0.04). Notre équipe a récemment proposé une première segmentation anatomique angioscannographique de l’AMS avec une excellente reproductibilité inter-observateurs (42) (figure 2). Dans ce travail ayant inclu 95 patients, la localisation des lésions vasculaires n’était correctement rapportée dans le compte-rendu initial que dans 17 % des cas. En cardiologie et neurologie, des segmentations standardisées existent depuis 1938 et 1975, et ont largement contribué à l’harmonisation et à l’amélioration des pratiques. Une démarche similaire pour la description des occlusions de l’AMS dans l’IMA pourrait améliorer la qualité des comptes-rendus, la comparabilité des études et, in fine, la prise en charge des patients.

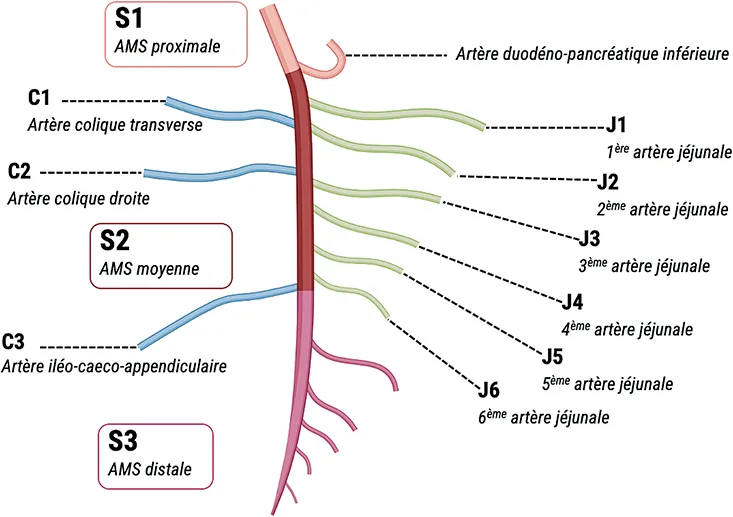
Figure 2 : Segmentation de l’artère mésentérique supérieure
Une sténose de l’artère mésentérique supérieure (AMS) est considérée significative et potentiellement responsable d’une ischémie mésentérique au-delà de 70%, même en cas d’opacification satisfaisante en aval. L’AMS est divisée en 3 segments :
S1 (proximal) de l’ostium à la naissance de l’artère duodéno-pancréatique inférieure ;
S2 (moyen), après la duodéno-pancréatique inférieure jusqu’à l’artère iléo-cæco-appendiculaire, d’où naissent les jéjunales ;
S3 (distal), après l’iléo-cæco-appendiculaire, d’où naissent les iléales.
Connaître le traitement d’urgence de l’IMA
Recommandations
- Une antibiothérapie à large spectre est indiquée précocement dans l’IMA, ainsi qu’en cas de chirurgie digestive (Grade IA et C, WSES 2022, ESVS 2017) (8)
- Une stratégie de revascularisation doit être discutée en urgence avec une équipe de vasculaire devant toute IMA artérielle, et si possible avant toute chirurgie digestive (Grade IC, WSES 2022, Grade IIB, ESVS 2017) (8)
- La revascularisation endovasculaire devrait être préférée à la chirurgie ouverte, chaque fois que (Grade IB ESC 2024, Grade IC WSES 2022, Grade IIB ESVS 2017) (8)
- Une fois le diagnostic d’IMA retenu, l’élévation du lactate peut aider à identifier la présence d’une nécrose (Grade IIB, WSES 2022) (8)
- La présence d’une défaillance d’organe, une élévation du lactate sanguin, et une dilatation des anses intestinales au scanner sont trois paramètres du score de nécrose intestinale devant faire suspecter un infarctus et réaliser une laparotomie exploratrice (Grade IB, VALDIG 2024 et AFEF 2018)
Une stratégie médicale multimodale et multidisciplinaire
Le traitement de l’IMA est une urgence absolue visant à préserver la viabilité intestinale pour 1) éviter ou limiter une résection intestinale, prévenir le grêle court et la dépendance à la nutrition parentérale, et 2) améliorer la survie (5, 25). Aucun essai clinique randomisé n’ayant été réalisé, la stratégie repose sur des études précliniques et observationnelles. Elle combine : 1) un protocole médical incluant jeûne strict, antithrombotiques, IPP, et antibiothérapie orale systématique pour ralentir le processus lésionnel ; 2) une revascularisation systématique, chaque fois que possible, seule capable de reverser les lésions ; 3) une résection intestinale selon un score de nécrose, avant les complications (perforation, péritonite) (tableau 3, figure 3). Cette approche multidisciplinaire d’urgence, coordonnée par un gastroentérologue dans un centre spécialisé, nécessite un accès 24h/24 à la revascularisation, à la chirurgie digestive, et à un environnement de réanimation.
Tableau 3 : Protocole médical systématique de l’ischémie mésentérique
| Systématique | 1. Repos digestif complet (jeûne strict) |
| 2. Oxygénothérapie 4l/min même en l’absence d’hypoxie, adaptée en cas d’hypoxie |
| 3. Remplissage vasculaire, même lorsque l’hémodynamique systémique est conservée et limiter l’utilisation de catécholamines |
| 4. Inhibiteurs de la pompe à protons IV (Esoméprazole 80 mg/j) |
| 5. Anticoagulation par héparine non fractionnée (HNF) avec objectif d’anti-Xa entre 0,5 et 0,8 ; y compris en cas d’hémorragie digestive non grave |
| 6. Antibiothérapie orale / entérale : – Gentamycine 80 mg/j – Métronidazole 1,5 g/j |
| Optionnel | Aspirine IV 100 mg/j si atteinte artérielle |
| Piperacilline-tazobactam IV 4×3 grammes/j en cas de SIRS, défaillance d’organe ou chirurgie digestive |
| Aspiration digestive en cas d’iléus |
| Transfusion sanguine si Hb < 8g/dL |
| HBPM plutôt qu’HNF en cas d’ischémie veineuse |
| Nutrition parentérale – d’emblée en cas de dénutrition préalable – ou en cas de jeûne > 5 jours |

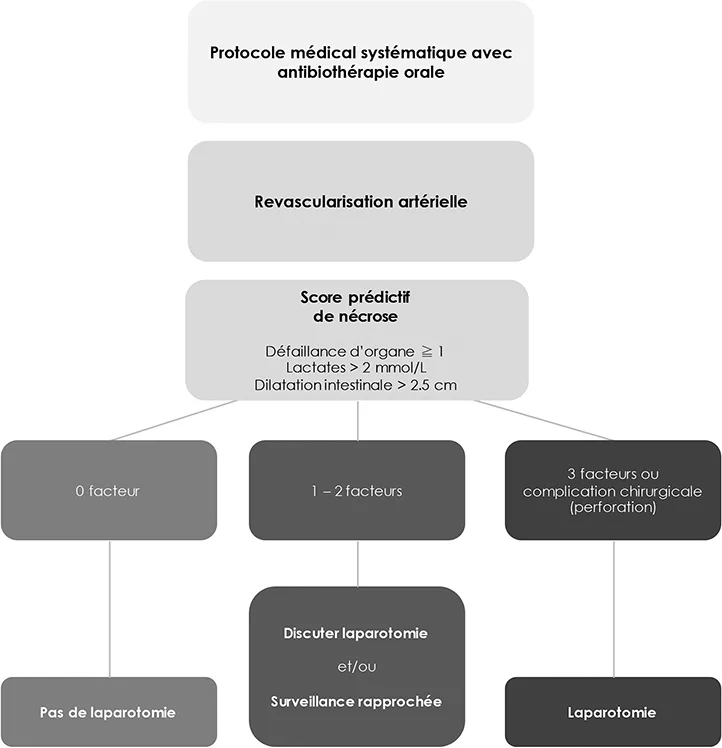
Figure 3 : Principes thérapeutiques de l’ischémie mésentérique aiguë occlusive et critères de résection intestinale (chirurgie selon le score)
Dans une étude observationnelle prospective, l’administration systématique d’une antibiothérapie par voie orale (tableau 3) dès le diagnostic d’IMA était associée à une diminution du risque de nécrose intestinale (HR=0.16, IC95 % : 0.03-0.62, p=0.01), probablement via une limitation de la composante septique de l’ischémie intestinale (pullulation/translocation bactérienne) et une optimisation de sa biodisponibilité luminale au site ischémique (43). Ce traitement est actuellement évalué par un essai randomisé contrôlé contre placebo (ORIAMI, NCT06387147).
Une revascularisation systématique
En fonction de l’accessibilité des lésions vasculaires et de l’expertise locale, la revascularisation artérielle est idéalement réalisée par voie endovasculaire (angioplastie, stenting, thrombectomie, thrombolyse intra-artérielle) et avant toute résection digestive pour préserver un maximum d’intestin viable (13, 35, 44). Deux méta-analyses d’études observationnelles ont montré sa supériorité par rapport à la chirurgie ouverte en termes de mortalité et de résection intestinale (45, 46). La surveillance post-revascularisation doit être continue en soins intensifs pour anticiper trois complications principales : 1) un syndrome hémorragique (lié aux ulcérations ischémiques digestives ou à la voie d’abord), 2/ un syndrome de reperfusion (SIRS, iléus, choc, défaillances d’organe), et 3) un syndrome de renutrition inappropriée en cas de dénutrition sévère (en cas d’angor mésentérique préalable notamment). En cas de ré-occlusion vasculaire, l’identification précoce des signes de récidive ischémique peut être difficile en post-opératoire chez un patient en iléus et/ou sédaté. Une surveillance répétée par angioscanner, notamment à J1, avant réalimentation ou en cas d’aggravation, est conseillée. Une nutrition parentérale exclusive est maintenue tant que l’ischémie persiste, en particulier en cas de dénutrition préexistante ou de syndrome de grêle court. La reprise de l’alimentation orale/entérale doit être progressive, après disparition de la douleur abdominale et du syndrome inflammatoire biologique.
Une résection intestinale en cas de nécrose transmurale
Un score prédictif de nécrose intestinale simple, basé sur trois facteurs (défaillance d’organe, lactate> 2 mmol/L, dilatation intestinale> 25 mm au scanner), permet de guider la décision chirurgicale d’urgence en identifiant les patients nécessitant une laparotomie sans délai (figure 3) (25). Le risque de nécrose intestinale augmente de 3 % en l’absence de ces facteurs, à 38 %, 89 % et 100 % en présence d’un, deux ou trois facteurs, avec une AUROC excellente (=0.94 ; IC95 %=0.87–0.99) (25). En l’absence ou en présence de ces facteurs, une laparotomie devrait être évitée ou proposée (figure 3). En cas de chirurgie, les segments intestinaux jugés non nécrotiques sont laissés en stomie pour surveillance et anastomose ultérieure, et la longueur d’intestin restant doit être précisée. Si elle n’a pas été réalisée avant la chirurgie digestive, une revascularisation doit être envisagée en cas d’intestin encore viable, même après une résection étendue : un grêle court peut toujours devenir plus court. En cas de doute, une réévaluation par angioscanner et/ou une chirurgie de second look est envisagée à 24-48 h. Le caractère systématique d’une chirurgie de second look est controversé chez les patients revascularisés, car une deuxième résection lors du second look n’est nécessaire que dans 7 à 25 % des cas (47-49). Elle est au mieux décidée au cas par cas, guidée par l’aspect peropératoire du grêle ou l’évolution post-opératoire du score de nécrose.
Cas particuliers
L’ischémie mésentérique non-occlusive (IMNO)
Recommandations
- L’IMNO doit être suspectée chez les patients hypovolémiques ou recevant des vasoconstricteurs présentant une distension ou des douleurs abdominales, ou des multi-défaillances inexpliquées. (Grade IIC, WSES 2022) (8)
- La première mesure thérapeutique est la correction du bas débit systémique à l’origine de l’IMNO. (Grade 1C, WSES 2022) (8)
- En cas d’aggravation malgré les mesures hémodynamiques, il est recommandé de discuter 1) une laparotomie pour résection d’une nécrose intestinale ; et/ou 2) une angiographie avec angioplastie en cas de sténose significative de l’AMS ou une perfusion intra-artérielle de vasodilatateurs (Grade 1C, ESVS 2017, WSES 2022) (8)
- La nutrition orale ou entérale est à éviter en cas d’IMNO ou chez les patients à risque (hypoxie ou état de choc non contrôlés) (ESPEN 2023) (7)
L’IMNO représente 10 à 20 % des IMA et se développe lors d’une hypoperfusion intestinale prolongée, dans un contexte d’hypovolémie (déshydratation/dialyse/bas débits), de vasoconstricteurs ou d’une consommation de cocaïne. Sa particularité qui la définit et rend son diagnostic encore plus difficile, est l’absence d’occlusion artérielle visible sur le scanner. Son diagnostic repose donc sur le contexte et des signes scannographiques, inconstants et non validés, de vasospasme splanchnique ou de souffrance digestive. L’artériographie reste le gold standard diagnostique en mettant en évidence le vasospasme microvasculaire diffus, mais est peu utilisée en dehors d’indications thérapeutiques. Les endoscopies digestives sont probablement peu utiles en l’absence d’hémorragie digestive, leur normalité n’excluant pas l’IMNO. De plus, la présence d’ulcères gastriques ou d’une colite ischémique gauche n’est pas prédictive d’une atteinte de l’intestin grêle ni de sa gravité (50). Le traitement priorise la restauration de l’hémodynamique splanchnique (traitement de la cause) via un remplissage vasculaire ou une optimisation cardiaque, tout en limitant l’usage des vasopresseurs. La souffrance ischémique de la muqueuse digestive justifie le maintien du protocole médical commun incluant les antibiotiques administrés par voie entérale et systémiques (tableau 3). En l’absence d’amélioration rapide, il est recommandé de discuter d’une artériographie avec revascularisation en cas de lésions vasculaires sténosantes associées, ou avec perfusion intra-artérielle de vasodilatateurs (papavérine) (51, 52). La chirurgie reste un dernier recours, proposée en cas d’aggravation persistante ou en cas de péritonite (25). La mortalité est alors très élevée> 80 % (8).
Afin de mieux guider les indications chirurgicales, un score spécifique pour l’IMNO a été publié par l’équipe du CHU de Besançon à partir de 154 patients (53). Ce score inclut : bicarbonate< 15 mmol/L (HR=1.9), TP< 40 % (HR=1.8), absence de rehaussement pariétal (HR=4.3) et amincissement pariétal intestinal au scanner (HR=2.8). Une laparotomie pourrait être discutée en présence de 2-3 facteurs, notamment en l’absence de rehaussement pariétal, facteur le plus prédictif de nécrose.
IMA veineuse
Recommandations
- L’anticoagulation au long cours est recommandée en cas d’antécédent d’infarctus mésentérique par thrombose porto-mésentérique. (Grade 1B, AFEF 2018, VALDIG 2024) (11).
La thrombose veineuse mésentérique représente 15 à 20 % des IMA avec une mortalité de 5 à 45 % selon les études (1). L’IMA complique une thrombose porto-mésentérique aiguë dans 4 à 58 % des cas (1, 54-56). Les facteurs de risque d’IMA dans ce contexte sont l’extension du thrombus aux petites veinules, et le diabète de type 2 (suggérant une composante artérielle associée) (55). Le traitement repose sur le protocole médical commun à l’IMA, avec une anticoagulation curative (HBPM préférée à l’HNF en l’absence d’indication chirurgicale), poursuivie généralement au long cours. La recanalisation veineuse par thrombolyse ou voie endovasculaire, évaluée dans de petites séries, offre des taux élevés de recanalisation mais un risque accru d’hémorragie majeure (1, 11). Cette approche devrait être réservée à des patients très sélectionnés, en centres spécialisés, en cas de détérioration malgré le traitement médical afin d’éviter une laparotomie et une résection intestinale.
Réhabilitation et suivi après une ischémie intestinale
Recommandations
- Une prévention secondaire cardiovasculaire est recommandée après IMA artérielle : consultation cardiologique, sevrage tabagique, antithrombotiques au long cours, statines. (Grade IA, ESVS 2017)
- Après revascularisation, une surveillance de la perméabilité vasculaire est proposée, par exemple à 1, 6 et 12 mois puis annuellement (Grade IIC WSES) (8, 57).
- Les patients avec syndrome de grêle court (< 200 cm) devraient être précocement transféré dans un centre expert en insuffisance intestinale et nutrition parentérale (ESPEN 2023) (7).
Toute IMA peut entraîner des séquelles fonctionnelles intestinales, notamment motrices. Dans la plupart des cas, ces lésions sont liées à une souffrance intestinale dépassée ayant saturé les mécanismes de réparation et évolué vers une fibrose pariétale sténosante et/ou des ulcérations muqueuses chroniques (entérite post-ischémique). Cliniquement révélées, dans des délais variables après la réalimentation, par un syndrome pseudo- occlusif, une diarrhée chronique et/ou des épisodes septiques d’origine digestive (translocations microbiennes), leur traitement est principalement chirurgical. Dans certains cas, le trouble moteur est transitoire et pourrait être lié à un certain degré de sidération du muscle lisse intestinal en réponse à l’ischémie-reperfusion s’améliorant progressivement après revascularisation (58, 59).
En cas de résection intestinale proximale ou étendue, les patients avec syndrome de grêle court (< 200 cm de grêle en continuité) doivent être adressés à un centre expert d’insuffisance intestinale, où la réhabilitation permet une survie prolongée avec une nutrition parentérale souvent sevrée à long terme (26, 60). La réhabilitation après IMA est triple et multidisciplinaire :
- Nutritionnelle : correction des déficits hydro-électrolytiques, caloriques et/ou en vitamines/oligo-éléments ;
- Vasculaire : dépistage et traitement d’une sténose vasculaire résiduelle à risque de récidive ischémique, prévention cardiovasculaire secondaire avec traitement antithrombotique au long cours (61) ;
- Digestive : rétablissement de continuité digestive, avec anticipation du risque de récidive ischémique si la perfusion du segment d’aval reste insuffisante (62).
Perspectives ouvertes par les structures d’urgences vasculaires intestinales
Recommandations
- Les patients avec IMA devraient idéalement être pris en charge dans une unité spécialisée dédiée, utilisant un protocole de soins standardisé et une équipe multidisciplinaire. (Grade IC, WSES 2022) (8)
Les unités de soins intensifs spécialisées, telles que les «stroke centers» en neurologie, ont démontré leur efficacité dans de nombreux essais randomisés en améliorant significativement le pronostic vital et fonctionnel des urgences vasculaires (63). Ces unités reposent sur une formation spécifique du personnel médical et paramédical, une coordination multidisciplinaire et des protocoles standardisés. Le bénéfice de telles structures pourrait être encore plus marqué pour l’IMA, compte tenu de sa mortalité plus élevée et de besoins de coordination plus complexe (notamment chirurgicaux vasculaires et digestifs).
Depuis 2016, la première SURVI a ouvert en France (Hôpital Beaujon, APHP), offrant une prise en charge experte 24h/24, standardisée, multidisciplinaire, et coordonnée, réunissant autour d’un gastroentérologue spécialisé, radiologues interventionnels, chirurgiens digestifs et vasculaires, et anesthésistes-réanimateurs. Elle a également permis le recrutement de patients et la standardisation des soins, indispensables à leur évaluation scientifique et à leur amélioration. Jusqu’à présent, la recherche sur l’IMA était limitée par l’absence de centres experts collectant des cas dans des cohortes bien caractérisées. Une première étude pilote a montré des taux de survie> 80 %, sans résection intestinale chez 50 % des patients (64). Ces résultats ont été confirmés par l’analyse de la cohorte SURVIBASE (493 IMA entre 2016 et 2022), présentée aux JFHOD/DDW (65). Chez les patients artériels pris en charge précocement (< 7 jours) à SURVI, le taux de revascularisation atteignait 75 %, avec une survie de 79 % et une absence de résection intestinale dans 61 % des cas. Une analyse préliminaire des données du SNDS sur 10 126 patients, présentée aux JFHOD/DDW, a montré une amélioration de la survie à 1 an de plus de 10 % chez les patients pris en charge en SURVI, comparé à 11 CHU français (HR=0,81 [0,73-0,90], p<0.001) (66). Dans la cohorte AMESI (418 patients recrutés prospectivement sur 10 mois dans 32 centres internationaux en 2023), les taux de revascularisation et de survie hospitalière pour les IMA artérielles étaient significativement meilleurs en SURVI (77 % et 89 %) que dans les centres non spécialisés (36 % et 42 %, respectivement) (3). En Finlande, l’implémentation d’un centre spécialisé en 2018 avec un parcours et protocole standardisé a permis une sensibilisation accrue à l’IMA des médecins intra- et extra-hospitaliers régionaux, une augmentation des revascularisations endovasculaires (64 % vs. 33 % avant implémentation, p<0.001), une accélération de la prise en charge et une amélioration de la survie (75 % vs. 49 %, p=0.001) (67). En France, une deuxième SURVI (SOS Ischémie) a ouvert à l’APHM en 2022. (Coordonnées disponibles sur le site internet www.survi.fr)
Conclusion
L’ischémie mésentérique est aujourd’hui potentiellement réversible lorsqu’elle est diagnostiquée et traitée précocement et de façon adaptée. À l’instar des « stroke centers », le développement d’unités de soins intensifs spécialisées, Structures d’URgences Vasculaires Intestinales, coordonnées par des gastroentérologues et capables de réaliser 24 h/24 une revascularisation, une résection intestinale dans un environnement réanimatoire en collaboration proche avec une unité d’insuffisance intestinale, constituent un espoir tant thérapeutique que diagnostique pour les malades. Leur recrutement au sein de services médicaux et de recherche dédiés est un prérequis indispensable au progrès scientifique et nourrit l’espoir d’obtenir bientôt un biomarqueur du diagnostic précoce, dont l’application clinique pourrait être généralisée à l’évaluation et la prise en charge de toute douleur abdominale et dont la place pourrait être majeure dans la gastroentérologie et la médecine d’urgence de demain.
Remerciements : Au Pr Olivier Corcos pour sa relecture, à l’équipe pluridisciplinaire SURVI et aux patients pour leur contribution continue à l’amélioration des connaissances sur l’ischémie mésentérique.
Références
- Acosta Epidemiology of mesenteric vascular disease: clinical implications. Semin Vasc Surg 2010; 23(1):4-8.
- Terlouw LG, Moelker A, Abrahamsen J, et European guidelines on chronic mesenteric ischaemia – joint United European Gastroenterology, European Association for Gastroenterology, Endoscopy and Nutrition, European Society of Gastrointestinal and Abdominal Radiology, Netherlands Association of Hepatogastroenterologists, Hellenic Society of Gastroenterology, Cardiovascular and Interventional Radiological Society of Europe, and Dutch Mesenteric Ischemia Study group clinical guidelines on the diagnosis and treatment of patients with chronic mesenteric ischaemia. United European Gastroenterol J 2020; 8(4):371-395.
- Reintam Blaser A, Mandul M, Bjorck M, et Incidence, diagnosis, management and outcome of acute mesenteric ischaemia: a prospective, multicentre observational study (AMESI Study). Crit Care 2024; 28(1):32.
- Nuzzo A, Corcos Reversible Acute Mesenteric Ischemia. N Engl J Med 2016; 375(15):e31.
- Nuzzo A, Corcos [Management of mesenteric ischemia in the era of intestinal stroke centers: The gut and lifesaving strategy]. Rev Med Interne 2017; 38(9):592-602.
- Mazzolai L, Teixido-Tura G, Lanzi S, et 2024 ESC Guidelines for the management of peripheral arterial and aortic diseases. Eur Heart J 2024; 45(36):3538-3700.
- Pironi L, Cuerda C, Jeppesen PB, et ESPEN guideline on chronic intestinal failure in adults – Update 2023. Clin Nutr 2023; 42(10):1940- 2021.
- Sermonesi G, Tian B, Vallicelli C, et Cesena guidelines: WSES consensus statement on laparoscopic-first approach to general surgery emergencies and abdominal trauma. World J Emerg Surg 2023; 18(1):57.
- Oliva IB, Davarpanah AH, Rybicki FJ, et ACR Appropriateness Criteria (R) imaging of mesenteric ischemia. Abdom Imaging 2013; 38(4):714-9.
- Bjorck M, Koelemay M, Acosta S, et al. Editor’s Choice – Management of the Diseases of Mesenteric Arteries and Veins: Clinical Practice Guidelines of the European Society of Vascular Surgery (ESVS). Eur J Vasc Endovasc Surg 2017; 53(4):460-510.
- Elkrief L, Hernandez-Gea V, Senzolo M, et Portal vein thrombosis: diagnosis, management, and endpoints for future clinical studies. Lancet Gastroenterol Hepatol 2024; 9(9):859-883.
- Clair DG, Beach JM. Mesenteric Ischemia. N Engl J Med 2016; 374(10):959-
- Corcos O, Nuzzo Gastro-intestinal vascular emergencies. Best Pract Res Clin Gastroenterol 2013; 27(5):709-25.
- Acosta S, Ogren M, Sternby NH, et al. Clinical implications for the management of acute thromboembolic occlusion of the superior mesenteric artery: autopsy findings in 213 patients. Ann Surg 2005; 241(3):516-22.
- Hernandez-Gea V, De Gottardi A, Leebeek FWG, et Current knowledge in pathophysiology and management of Budd-Chiari syndrome and non-cirrhotic non-tumoral splanchnic vein thrombosis. J Hepatol 2019; 71(1):175-199.
- Nuzzo A, Huguet A, Maggiori L, et Ischémies coliques. EMC – Gastro-entérologie 2018; 1-12.
- Ten Heggeler LB, van Dam LJ, Bijlsma A, et Colon ischemia: Right-sided colon involvement has a different presentation, etiology and worse outcome. A large retrospective cohort study in histology proven patients. Best Pract Res Clin Gastroenterol 2017; 31(1):111-117.
- Lui RN, Lau Right-Sided Colon Ischemia and Acute Mesenteric Insufficiency: Are They Separate Entities? Clin Gastroenterol Hepatol 2015; 13(11):1969-71.
- Dickson Three cases of ischaemic colitis. Gut 1968; 9(4):376-80.
- Bailey JA, Jacobs DL, Bahadursingh A, et al. Endovascular treatment of segmental ischemic Dig Dis Sci 2005; 50(4):774-9.
- Seeger JM, Coe DA, Kaelin LD, et Routine reimplantation of patent inferior mesenteric arteries limits colon infarction after aortic reconstruction. J Vasc Surg 1992; 15(4):635-41.
- Hoang QT, Nuzzo A, Louedec L, et Peptide binding to cleaved CD31 dampens ischemia/reperfusion-induced intestinal injury. Intensive Care Med Exp 2018; 6(1):27.
- Alverdy JC, Chang The re-emerging role of the intestinal microflora in critical illness and inflammation: why the gut hypothesis of sepsis syndrome will not go away. J Leukoc Biol 2008; 83(3):461-6.
- Deitch EA, Xu D, Kaise Role of the gut in the development of injury- and shock induced SIRS and MODS: the gut-lymph hypothesis, a review. Front Biosci 2006; 11:520-8.
- Nuzzo A, Maggiori L, Ronot M, et Predictive Factors of Intestinal Necrosis in Acute Mesenteric Ischemia: Prospective Study from an Intestinal Stroke Center. Am J Gastroenterol 2017; 112(4):597-605.
- Adaba F, Rajendran A, Patel A, et Mesenteric Infarction: Clinical Outcomes After Restoration of Bowel Continuity. Ann Surg 2015; 262(6):1059-64.
- Kougias P, Lau D, El Sayed HF, et Determinants of mortality and treatment outcome following surgical interventions for acute mesenteric ischemia. J Vasc Surg 2007; 46(3):467-74.
- Nuzzo A, Peoc’h K, Vaittinada Ayar P, et Improving clinical suspicion of acute mesenteric ischemia among patients with acute abdomen: a cross-sectional study from an intestinal stroke center. World J Emerg Surg 2023; 18(1):37.
- Park WM, Gloviczki P, Cherry KJ, , et al. Contemporary management of acute mesenteric ischemia: Factors associated with survival. J Vasc Surg 2002; 35(3):445-52.
- Kolkman JJ, Mensink PB, van Petersen AS, et Clinical approach to chronic gastrointestinal ischaemia: from ‘intestinal angina’ to the spectrum of chronic splanchnic disease. Scand J Gastroenterol Suppl 2004(241):9-16.
- Nuzzo A, Guedj K, Curac S, et al. Accuracy of citrulline, I-FABP and D-lactate in the diagnosis of acute mesenteric Sci Rep 2021; 11(1):18929.
- Blauw JTM, Metz FM, Nuzzo A, et The Diagnostic Value of Biomarkers in Acute Mesenteric Ischaemia Is Insufficiently Substantiated: A Systematic Review. Eur J Vasc Endovasc Surg 2024; 67(4):554-569.
- Acosta S, Blaser AR, Nuzzo A, et D-Dimer in Acute Mesenteric Venous Thrombosis: A Prospective Case-Control International Multicenter Study. Biomark Insights 2024; 19:11772719241296631.
- Nuzzo A, Joly F, Ronot M, et Normal Lactate and Unenhanced CT-Scan Result in Delayed Diagnosis of Acute Mesenteric Ischemia. Am J Gastroenterol 2020; 115(11):1902-1905.
- Nuzzo A, Huguet A, Corcos [Modern treatment of mesenteric ischemia]. Presse Med 2018; 47(6):519-530.
- Copin P, Zins M, Nuzzo A, et Acute mesenteric ischemia: A critical role for the radiologist. Diagn Interv Imaging 2018; 99(3):123-134.
- Copin P, Ronot M, Nuzzo A, et Inter-reader agreement of CT features of acute mesenteric ischemia. Eur J Radiol 2018; 105:87-95.
- Acosta S, Bjornsson S, Ekberg O, et CT angiography followed by endovascular intervention for acute superior mesenteric artery occlusion does not increase risk of contrast-induced renal failure. Eur J Vasc Endovasc Surg 2010; 39(6):726-30.
- Nuzzo A, Ronot M, Maggiori L, et al. [Abdominal pain of vascular cause]. Rev Med Interne 2019; 40(2):129-
- Lehtimaki TT, Karkkainen JM, Saari P, et Detecting acute mesenteric ischemia in CT of the acute abdomen is dependent on clinical suspicion: Review of 95 consecutive patients. Eur J Radiol 2015; 84(12):2444-53.
- Wadman M, Block T, Ekberg O, et Impact of MDCT with intravenous contrast on the survival in patients with acute superior mesenteric artery occlusion. Emerg Radiol 2010; 17(3):171-8.
- Tual A, Garzelli L, Nuzzo A, et Strengthening the Description of Superior Mesenteric Artery Occlusions in Acute Mesenteric Ischaemia: Proposition for an Anatomical Classification. Eur J Vasc Endovasc Surg 2023; 65(6):802-808.
- Nuzzo A, Maggiori L, Paugam-Burtz C, et Oral antibiotics reduce intestinal necrosis in acute mesenteric ischemia: a prospective cohort study. Am J Gastroenterol 2018.
- Roussel A, Castier Y, Nuzzo A, et Revascularization of acute mesenteric ischemia after creation of a dedicated multidisciplinary center. J Vasc Surg 2015; 62(5):1251-6.
- Salsano G, Salsano A, Sportelli E, et What is the Best Revascularization Strategy for Acute Occlusive Arterial Mesenteric Ischemia: Systematic Review and Meta-analysis. Cardiovasc Intervent Radiol 2018; 41(1):27-36.
- El Farargy M, Abdel Hadi A, Abou Eisha M, et Systematic review and meta-analysis of endovascular treatment for acute mesenteric ischaemia. Vascular 2017; 25(4):430-438.
- Yanar H, Taviloglu K, Ertekin C, et al. Planned second-look laparoscopy in the management of acute mesenteric World J Gastroenterol 2007; 13(24):3350-3.
- Acosta-Merida MA, Marchena-Gomez J, Saavedra-Santana P, et Surgical Outcomes in Acute Mesenteric Ischemia: Has Anything Changed Over the Years? World J Surg 2020; 44(1):100-107.
- Nassar A, Bajul M, Nuzzo A, et Is Systematic Second Look for Acute Mesenteric Ischemia Still Justified? A Prospective Cohort Study in a Structure Dedicated to Intestinal Vascular Emergencies (SURVI) DOI:. Annals of Vascular Surgery 2024(December 2024 109:544-545).
- Ksouri A, Copin P, Bonvalet F, et Colonic involvement in acute mesenteric ischemia: prevalence, risk factors, and outcomes. Eur Radiol 2022; 32(4):2813-2823.
- Kozuch PL, Brandt Review article: diagnosis and management of mesenteric ischaemia with an emphasis on pharmacotherapy. Aliment Pharmacol Ther 2005; 21(3):201-15.
- Brandt LJ, Boley AGA technical review on intestinal ischemia. American Gastrointestinal Association. Gastroenterology 2000; 118(5):954-68.
- Calame P, Winiszewski H, Doussot A, et Evaluating the Risk of Irreversible Intestinal Necrosis Among Critically Ill Patients With Nonocclusive Mesenteric Ischemia. Am J Gastroenterol 2021; 116(7):1506-1513.
- Plessier A, Darwish-Murad S, Hernandez-Guerra M, et Acute portal vein thrombosis unrelated to cirrhosis: a prospective multicenter follow-up study. Hepatology 2010; 51(1):210-8.
- Elkrief L, Corcos O, Bruno O, et Type 2 diabetes mellitus as a risk factor for intestinal resection in patients with superior mesenteric vein thrombosis. Liver Int 2014; 34(9):1314-21.
- Schoots IG, Koffeman GI, Legemate DA, et al. Systematic review of survival after acute mesenteric ischaemia according to disease Br J Surg 2004; 91(1):17-27.
- Zierler RE, Jordan WD, Lal BK, et The Society for Vascular Surgery practice guidelines on follow-up after vascular surgery arterial procedures. J Vasc Surg 2018; 68(1):256-284.
- Somarajan S, Muszynski ND, Cheng LK, et al. Noninvasive biomagnetic detection of intestinal slow wave dysrhythmias in chronic mesenteric ischemia. Am J Physiol Gastrointest Liver Physiol 2015; 309(1):G52-8.
- Gauci JL, Stoven S, Szarka L, et Prolonged idiopathic gastric dilatation following revascularization for chronic mesenteric ischemia. Ann Gastroenterol 2014; 27(3):273-275.
- Joly F, Baxter J, Staun M, et Five-year survival and causes of death in patients on home parenteral nutrition for severe chronic and benign intestinal failure. Clin Nutr 2018; 37(4):1415-1422.
- Roussel A, Nuzzo A, Pellenc Q, et al. Surgical revascularization of the celiac artery for persistent intestinal ischemia in short bowel Int J Surg 2018; 49:39-44.
- Layec S, Beyer L, Corcos O, et Increased intestinal absorption by segmental reversal of the small bowel in adult patients with short-bowel syndrome: a case-control study. Am J Clin Nutr 2013; 97(1):100-8.
- Collaborative systematic review of the randomised trials of organised inpatient (stroke unit) care after Stroke Unit Trialists’ Collaboration. BMJ 1997; 314(7088):1151-9.
- Corcos O, Castier Y, Sibert A, et Effects of a multimodal management strategy for acute mesenteric ischemia on survival and intestinal failure. Clin Gastroenterol Hepatol 2013; 11(2):158-65 e2.
- Nuzzo A, Abdallah IB, Garzelli L, et Tu1913 First intestinal Stroke Center for the Care of Acute Mesenteric Ischemia: A 7-Year Prospective Cohort Study. Gastroenterology 2023; 164(6).
- Nuzzo A, Zarca K, Bessonneau P, et Tu1914 Treatment in a Specialized Intestinal Stroke Center Improves Survival after Acute Mesenteric Ischemia: A Study from the French National Health Data System. Gastroenterology 2023; 164(6).
- Tolonen M, Lemma A, Vikatmaa P, et The implementation of a pathway and care bundle for the management of acute occlusive arterial mesenteric ischemia reduced mortality. J Trauma Acute Care Surg 2021; 91(3):480-488.