Lien d’intérêt
L’auteur déclare n’avoir aucun lien d’intérêt en rapport avec sa présentation
Mots-clés
Cirrhose ; insuffisance rénale ; syndrome hépatorénal (SHR)
Abréviations
ACLF : acute-on-chronic liver failure ;
CysC : cystatin C ;
eDFG : taux estimé du débit de filtration glomérulaire ;
EER : épuration extra-rénale ;
ETT : échocardiographie ;
FeNa : fraction d’excrétion du sodium ;
ICA : club international de l’ascite ;
IRA : insuffisance rénale aiguë ;
IRC : insuffisance rénale chronique ;
NTA : nécrose tubulaire aiguë ;
SHR : syndrome hépatorénal ;
TH : transplantation hépatique.
Introduction
L’insuffisance rénale aiguë (IRA) est fréquemment observée chez les patients cirrhotiques nécessitant une hospitalisation. La survenue d’une IRA est associée à une mortalité élevée avec un risque de décès majoré de 300 % environ (1). L’IRA pré-rénale en contexte d’hypovolémie efficace, le syndrome hépatorénal (SHR) et la nécrose tubulaire aiguë (NTA) sont les causes les plus courantes d’IRA chez les patients cirrhotiques. La distinction de ces causes peut être difficile mais elle est nécessaire pour optimiser la prise en charge des patients. Le SHR est la conséquence fonctionnelle de modifications circulatoires en lien avec la cirrhose et l’hypertension portale. Il occupe une place particulière puisqu’il est spécifique de la maladie hépatique et est caractérisé par un mauvais pronostic à court terme. Parallèlement, un nombre croissant de patients cirrhotiques éligibles à la transplantation hépatique, ont une insuffisance rénale chronique (IRC). Ceci semble être en lien avec l’augmentation des patients avec maladie hépatique d’origine dysmétabolique qui associent des facteurs de risques cardiovasculaires propices au développement d’une l’IRC. Cette revue a pour objectif de faire un état des lieux sur les avancées récentes concernant les critères diagnostiques, la physiopathologie, et la prise en charge de l’IRA chez les patients atteints de cirrhose mais aussi sur les causes et complications de l’IRC, les indications et les modalités d’épuration extra-rénale et les indications de transplantation combinée foie-rein.
Insuffisance rénale aiguë
Épidémiologie et définition
L’IRA est fréquente puisque son incidence varie de 20 % à 50 % chez les patients atteints de cirrhose admis à l’hôpital (2, 3). La définition de l’IRA chez les patients cirrhotiques a connu de nombreuses et récentes mises à jour. Traditionnellement, l’IRA dans la cirrhose était définie par une valeur de créatinine sérique supérieure à 15 mg/l (132 μmol/l) (4). Elle ne reposait donc que sur un seuil fixe, ne tenant pas compte des variations dynamiques de la créatinine sérique, essentielles pour distinguer l’IRA de l’IRC. En 2004, la conférence de consensus du groupe Acute Dialysis Quality Initiative a défini la classification RIFLE (Risk, Injury, Failure, Loss and End-stage kidney disease) basée sur l’évolution dynamique de la créatinine sérique, du débit de filtration glomérulaire (DFG) et du débit urinaire (5). En 2007, cette définition a été modifiée par le réseau Acute Kidney Injury Network (AKIN) pour inclure l’ensemble du spectre de l’IRA en prenant en compte une augmentation de la créatinine sérique de base de 3 mg/l (26,4 μmol/l) en 48 heures (6). En 2012, le groupe Kidney Disease Improving Global Outcome (KDIGO) a encore précisé cette définition. En effet, une IRA est désormais définie par une augmentation de la créatinine sérique d’au moins 3 mg/l (26,4 μmol/l) en 48 heures ou une augmentation de la créatinine sérique d’au moins 1,5 fois la valeur de base au cours des 7 derniers jours, ou un débit urinaire à 0,5 ml/kg/h pendant 6 heures (7). En 2015, le Club International de l’Ascite (ICA) a adopté les critères de KDIGO en prenant soin d’ôter le débit urinaire de la définition compte tenu de ses difficultés d’interprétation chez les patients cirrhotiques (tableau 1) (8). La définition du SHR a également évolué au fil du temps. Initialement, le SHR était classé en type 1 et type 2. Le type 1 était défini par une altération rapide de la fonction rénale se manifestant en moins de deux semaines par un doublement de la créatinine sérique initiale à un niveau supérieur à 25 mg/l (220 μmol/l) ou une réduction de 50 % de la clairance de la créatinine à un niveau inférieur à 20 ml/min. Le type 2 était défini par une altération moins rapide de la fonction rénale (4). Lors d’une première révision, le seuil de créatinine définissant le SHR avait été abaissé à 15 mg/l (133 microl/l) (9). Les changements proposés par les directives KDIGO ont amené l’ICA en 2015 à reclasser le précédent SHR de type 1 en forme aiguë de SHR (SHR–IRA), et en 2019, le SHR de type 2 en SHR non-IRA (tableau 2) (10). La nouvelle définition du SHR–IRA a supprimé l’intervalle de 2 semaines, facilitant ainsi le diagnostic et un traitement plus précoce. Le SHR non-IRA est défini par la valeur estimée du débit de filtration glomérulaire (eDFG) plutôt que par la créatinine sérique, et est qualifié de subaigu si l’eDFG est inférieur à 60 ml/min/1,73 m2 depuis moins de 3 mois, et chronique si l’eDFG est inférieur à ce seuil depuis plus de 3 mois.
Il est important de noter qu’une diminution de la créatinine sérique est observée en cas de cirrhose. En effet, chez ces patients, sont observées une diminution de production de créatinine en lien avec la diminution de la masse musculaire (sarcopénie), et une dilution de la créatinine en lien avec la rétention hydrosodée et l’augmentation du volume de distribution. Enfin, le dosage de créatinine peut être faussé en cas d’hyperbilirubinémie (11). L’eDFG reposant sur des formules incluant la créatinine sérique (tels que MDRD ou le CKD-EPI) est donc souvent surestimé. Des formules spécifiques à la population cirrhotique ont été développées. Elles sont basées sur des cohortes pour lesquelles une mesure du DGF était réalisée par radio-isotope. C’est plus particulièrement le cas du RFHC-GFR (Royal Free Hospital Cirrhosis Glomerular Filtration Rate) qui inclue la créatinine sérique, l’urémie, l’âge, le sodium, l’INR, le sexe et l’ascite et dont la formule est disponible en ligne (http://rfh-cirrhosis-gfr.ucl.ac.uk) (12). D’autres biomarqueurs de la fonction rénale sont actuellement évalués dans la population des patients cirrhotiques. C’est le cas de la cystatine C (CysC), une protéine secrétée par toutes les cellules nucléées, passant librement le glomérule et dont les taux circulants ne sont pas influencés par le sexe, la masse musculaire et la bilirubine. Cette protéine est un meilleur biomarqueur d’insuffisance rénale que la créatininémie chez les patients cirrhotiques et même si, à l’heure actuelle, la créatinine sérique et l’eDFG estimé par celle-ci restent la référence, la place de la CysC pour le diagnostic de l’insuffisance rénale du patient atteint de cirrhose devrait augmenter dans les années à venir (11).
Tableau 1
| Stades d’insuffisance rénale aiguë définie selon la classification du club international de l’ascite (ICA) |
| Stade 1 | • majoration de la créatininémie ≥ 3 mg/l (26,5 μmol/l) en 48 h ou • majoration de la créatininémie ≥ 1,5 fois et < 2 fois la créatininémie de base en 7 jours • Stade 1A : créatininémie < 15 mg/l (133 μmol/l) et 1B ≥ 15 mg/l (133 μmol/l) |
| Stade 2 | • majoration de la créatininémie ≥ 2 fois et < 3 fois la créatininémie de base en 7 jours |
| Stade 3 | • majoration de la créatininémie ≥ 3 fois la créatininémie de base en 7 jours ou • créatininémie ≥ 40 mg/l (354 μmol/l) avec une majoration aiguë de 3 mg/l (26,5 μmol/l) en 48 h ou • recours à une épuration extra-rénale |
Tableau 2
| Critères diagnostiques du syndrome hépatorénal selon le club international de l’ascite (ICA) |
| SHR-IRA | • majoration de la créatininémie ≥ 3 mg/l (26,5 μmol/l) en 48 h et/ou débit urinaire ≤ 0,5 ml/kg en 6 heures ou • majoration de la créatininémie ≥ 1,5 fois la créatininémie de base sur les 7 derniers jours* et • absence de réponse à l’arrêt des diurétiques et deux jours d’expansion volémique par 1 g/kg/jour d’albumine 20 % • cirrhose avec ascite • absence de choc • absence de prise de traitements néphrotoxiques • absence d’argument pour une pathologie structurelle définie par une protéinurie > 0,5 g/jour, une micro-hématurie ou une échographie rénale anormale |
| SHR-non-IRA | • subaigu : eDFG < 60 ml/min/1,73 m2 depuis < 3 mois en l’absence d’autres pathologie rénale et majoration de la créatininémie < 1,5 de la créatininémie de base en 3 mois • chronique: eDFG > 60 ml/min/1,73 m2 depuis < 3 mois en l’absence d’autres pathologies rénales |
*La valeur de référence doit être prise au maximum dans la période de 3 mois.
Physiopathologie du syndrome hépatorénal
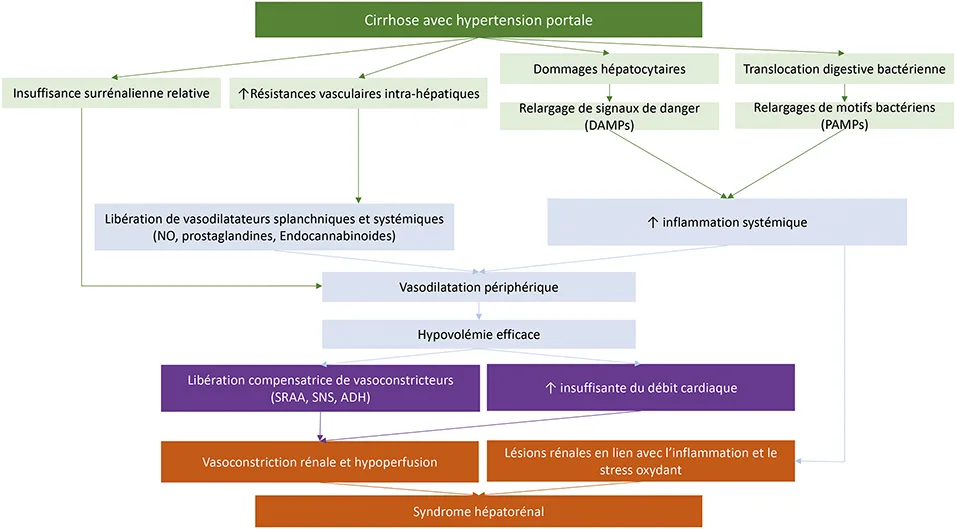
Le SHR fait référence à une dysfonction rénale spécifique aux patients atteints de maladie avancée du foie. Il présente une physiopathologie unique dont la compréhension a évolué au cours des dernières décennies et est centrée sur les conséquences d’une vasodilatation artérielle splanchnique et systémique (13). La présence d’une cirrhose entraîne, en effet, une augmentation des résistances vasculaires intra-hépatiques associées à une surproduction et à une libération de vasodilatateurs (oxyde nitrique, prostaglandines, endocannabinoïdes) dans la circulation splanchnique et systémique. En conséquence, est observée une hypovolémie artérielle efficace, centrale dans la physiopathologie du syndrome, associée à une hypotension artérielle systémique, entraînant, à son tour, une augmentation compensatoire du débit cardiaque et l’activation des voies de vasoconstriction systémique, telles que celles du système rénine–angiotensine–aldostérone, du système nerveux sympathique et de l’hormone anti-diurétique (ADH – vasopressine). Ces mécanismes sont généralement efficaces pour maintenir le volume circulatoire chez les patients avec cirrhose compensée. En cas de cirrhose décompensée, ces mécanismes sont dépassés, ce qui entraîne une diminution du débit sanguin rénal et une atteinte rénale fonctionnelle et ischémique (14, 15). L’inflammation systémique est un mécanisme plus récemment décrit dans la physiopathologie du SHR. Celle-ci est liée d’une part à une augmentation de la translocation de bactéries intestinales et de motifs moléculaires associés aux pathogènes, tels que le lipopolysaccharide ou la flagelline dans la circulation portale. D’autre part, à la libération de motifs moléculaires associés aux dommages hépatocytaires, tels que les protéines de choc thermique (heat shock protein – HSP), de l’ADN génomique bicaténaire et de l’adénosine triphosphate (ATP). Cette réponse pro-inflammatoire entraîne une augmentation de la production de vasodilatateurs artériels participant à la réduction du volume sanguin artériel efficace et des résistances vasculaires systémiques (14, 15). Enfin, une insuffisance surrénalienne relative est observée chez 20 % à 50 % des patients atteints de cirrhose décompensée. Celle-ci est responsable d’une baisse de la pression artérielle et une augmentation compensatrice des systèmes vasoconstricteurs, plaçant ainsi ces patients à plus grand risque de développer un SHR (16). Un impact de l’hypertension intra- abdominale en lien avec une ascite abondante dans le développement du SHR est également supposé mais reste difficile à démontrer. La physiopathogénèse du SHR est illustré en figure 1.

Figure 1 : Physiophatologie du syndrome hépatorénal.
ADH : anti-diuretic hormone ; DAMPs : danger-associated molecular patterns ; NO : monoxyde d’azote ; PAMPs : pathogen-associated molecular patterns SNS : système nerveux sympathique ; SRAA : sytème rénine angiotensine aldostérone
Diagnostic différentiel
En dehors du SHR–IRA, d’autres causes courantes d’IRA sont observées chez les patients atteints de cirrhose. Celles-ci comprennent, par exemple, les IRA pré-rénales sur hypovolémie efficace, les atteintes parenchymateuses incluant les nécroses tubulaires aiguës (NTA) et les atteintes néphrotoxiques. Bien que se chevauchant parfois, la distinction du principal facteur de l’insuffisance rénale dans la cirrhose est importante à des fins pronostiques et thérapeutiques. Le SHR est en effet la cause d’IRA associée au moins bon pronostic à court terme avec une survie sans transplantation estimée entre 15 % et 30 % à trois mois en comparaison au 50-80 % observés dans les autres atteintes (17, 18). En pratique clinique, la distinction entre le SHR–IRA et la NTA peut être difficile. Bien que le diagnostic de SHR–IRA requiert l’absence de choc, de protéinurie, de micro-hématurie et une échographie rénale normale, les patients répondant à ces critères peuvent toujours présenter des lésions tubulaires, de sorte que la NTA ne peut pas être totalement exclue. De plus, les biomarqueurs urinaires classiques tels que le sodium urinaire et la fraction d’excrétion de sodium (FeNa), utilisés pour le diagnostic différentiel de l’IRA, présentent des limites chez les patients atteints de cirrhose qui ont, pour la plupart, une hypoperfusion rénale associée à une natriurèse et une FeNa basse. En conséquence, le sodium urinaire et la FeNa ne font plus partie des critères diagnostiques du SHR–IRA (10). Les protéines tubulaires libérées lors des lésions cellulaires (neutrophil gelatinase-associated lipocalin [NGAL]), kidney injury molecule-1 [KIM-1], liver-type fatty acid-binding protein [LFAP]), ainsi que des marqueurs de l’inflammation telle que l’interleukine-18 (IL-18) font partie des biomarqueurs qui pourraient permettre la distinction entre le SHR-IRA et la NTA. Parmi ceux-ci, le NGAL et l’IL-18 sont les plus largement étudiés et présentent les résultats les plus prometteurs. Le NGAL est une protéine exprimée par les épithéliums tubulaires rénaux lésés et dont la concentration dans les urines augmente de manière exponentielle en cas de lésions tubulaires. Plusieurs études ont démontré que le NGAL urinaire a une grande précision pour différencier la NTA du SHR–IRA et de l’IRA induite par l’hypovolémie en particulier après expansion plasmatique avec de l’albumine (recommandée dans la prise en charge de l’IRA chez le patient cirrhotique) (19-22). Dans ce contexte, une valeur de NGAL urinaire supérieure à 220 mg/g de créatinine avait la plus grande précision pour le diagnostic de NTA (20, 22). Ce biomarqueur a aussi été associé au risque de décès indépendamment de la sévérité de la maladie hépatique évaluée par les scores usuels. Il est cependant important de noter que le NGAL augmente aussi en cas d’infection des voies urinaires en raison de son expression par les leucocytes (15). L’IL-18 est une cytokine pro-inflammatoire exprimée dans le tubule proximal, qui est libérée lors des lésions tubulaires. Des niveaux urinaires significativement plus élevés d’IL-18 ont été observés chez les patients atteints de cirrhose et de NTA par rapport à d’autres causes de lésions rénales (23). Comme pour le NGAL, les données suggèrent également une association indépendante entre les niveaux d’IL-18 et le risque de décès à court terme. Dans les dernières recommandations européennes, il est stipulé que les biomarqueurs urinaires et plus particulièrement le NGAL, devraient être implémentés en pratique courante pour distinguer le SHR de la NTA (24).
Facteurs de risque et prévention
La prévalence du SHR–IRA chez les patients cirrhotiques avec ascite en l’absence d’événements déclenchants identifiables est faible et inférieure à 2 % (25). Le facteur déclenchant le plus courant du SHR–IRA est la paracentèse évacuatrice de grand volume sans administration d’albumine. La supplémentation en albumine (6 à 8 g/L de liquide ascitique retiré) après une paracentèse de grand volume (≥ 4-5 L) réduit significativement le risque de SHR–IRA et la mortalité à court terme (26). Cet effet protecteur est propre à l’albumine par rapport aux autres solutés de remplissage, et semble donc être aussi en lien avec ses propriétés antioxydantes, anti-inflammatoires et d’inactivation des endotoxines (27-29). Les changements hémodynamiques aigus secondaires à une infection sont un autre facteur de risque majeur de SHR–IRA. Environ 30 % des patients atteints d’infection spontanée du liquide d’ascite (ISLA) développent un SHR–IRA (30). L’administration d’albumine (à une dose recommandée de 1,5 g/kg le jour 1 et de 1 g/kg le jour 3), en plus du traitement antibiotique, réduit l’incidence du SHR–IRA associé à l’ISLA et améliore la survie globale (31). De plus, les patients présentant un faible taux de protéines dans le liquide ascitique (< 15 g/L) associé à une dysfonction hépatique ou rénale (score Child-Turcotte-Pugh ≥ 9 avec une bilirubine ≥ 30 mg/l (51 μmol/l), ou une créatinine sérique ≥ 12 mg/l (105,6 μmol/l), ou une natrémie ≤ 130 mEq/l présentent un risque accru d’ISLA. La prophylaxie antibiotique prévient le développement de l’ISLA, réduit le risque de SHR–IRA ainsi que le risque de décès qui y est associé (24, 32).
Prise en charge
La reconnaissance précoce et le traitement de l’IRA sont importants car ils permettent d’en améliorer le pronostic. Ainsi, la prise en charge doit débuter dès que le diagnostic d’IRA est posé. En premier lieu, les agents néphrotoxiques, notamment les anti-inflammatoires non stéroïdiens, de même que les traitements vasodilatateurs et les bêta-bloquants doivent être arrêtés. En parallèle, le traitement diurétique doit être interrompu. Une infection doit être recherchée et traitée. Le stade 1A de l’IRA (créatinine sérique < 15 mg/l – 132 μmol/l) est le plus souvent dû à insuffisance rénale pré-rénale en lien avec une hypovolémie efficace isolée et plus de 90 % des cas se résolvent avec la seule gestion de ces facteurs de risque. En comparaison, seulement 50 % des IRA des patients atteints de stade 1B se résolvent sans expansion volémique (2, 24). Ainsi, les patients qui présentent une IRA de stade au moins égal à 1B doivent, en plus des mesures initiales, bénéficier d’une expansion volémique par de l’albumine concentrée à 20 % à la posologie de 1 g/kg/j pendant deux jours. Cette posologie standardisée d’albumine pourrait ne pas être adaptée à la situation du patient (patient avec cardiomyopathie cirrhotique ou ayant déjà été optimisé sur le plan volémique). Cette prescription devrait, idéalement, être confrontée aux données d’évaluation hémodynamiques cliniques mais aussi échocardiographiques ou de la pression veineuse centrale lorsque leur mesures est possible. Cette étape d’optimisation volémique est importante pour exclure une IRA pré-rénale sur hypovolémie efficace seule et est nécessaire avant de poser un diagnostic de SHR–IRA (10). Si la fonction rénale ne s’améliore pas et si les patients satisfont aux critères diagnostiques du SHR–IRA, il convient d’initier un traitement par vasoconstricteurs en association avec de l’albumine (10, 24) (figure 2). Les vasoconstricteurs splanchniques sont responsables d’une diminution du débit portal, et par conséquent de la pression portale, en parallèle d’une augmentation du volume sanguin artériel systémique efficace entrainant une augmentation du débit sanguin rénal et de la pression artérielle moyenne (PAM). Une augmentation de la PAM après l’introduction d’un traitement vasoconstricteur est prédictif de la réversibilité du SHR-IRA (33) et est un paramètre clinique important à prendre en compte après instauration du traitement. Les vasoconstricteurs les plus utilisés dans le traitement du SHR-AKI sont la terlipressine, la norépinéphrine et la combinaison d’octréotide et de midodrine.

Figure 2 : Algorithme de prise en charge de l’insuffisance rénale aiguë chez le patient cirrhotique [adapté de (24)]
IRA, insuffisance rénale aiguë ; NGAL, neutrophil gelatinase-associated lipocalin ; NTA, nécrose tubulaire aiguë ; SHR, syndrome hépatorénal.
La terlipressine, un puissant agoniste de la vasopressine 1a, joue essentiellement le rôle de vasoconstricteur splanchnique. Dans le cadre du SHR-IRA, elle peut être administrée en bolus intraveineux (0,5 mg à 1 mg toutes les 4 à 6 heures jusqu’à 2 mg toutes les 4 heures) ou en perfusion continue (1 mg/jour à 12 mg/jour). Les doses initiales recommandées sont donc de 0,5 à 1 mg toutes les 4-6 h en bolus ou 2 mg/jour en perfusion continue (24, 34). La dose de terlipressine doit être augmentée de manière progressive, toutes les 48 heures, en fonction de la réponse de la créatinine sérique et ne peut être maintenue au-delà de 14 jours (figure 3). Une réponse complète (créatinine sérique finale à moins de 3 mg/l – 26,4 μmol/l – de la valeur de référence ou inférieure à 15 mg/l – 132 μmol/l) ou une réponse partielle (amélioration de l’IRA mais créatinine sérique finale à plus de 3 mg/l – 26,4 μmol/l – de la valeur de référence) est obtenue chez 40 % à 70 % des patients (17, 35-43). La récidive du SHR–IRA est inférieure à 20 %, et en cas de récidive, la plupart des patients répondent à la reprise du traitement. La terlipressine peut être responsable d’effets indésirables significatifs et en particulier d’événements respiratoires en lien avec l’augmentation des résistances vasculaires systémiques (post-charge cardiaque). Ainsi, dans la récente étude CONFIRM, une insuffisance respiratoire aiguë, une hypoxie, et un œdème pulmonaire étaient observés chez 39,5 % des patients sous terlipressine contre 25,3 % sous placebo (17). Le risque d’événements pulmonaires peut être diminué en évitant son utilisation chez les patients atteints de défaillance d’organe multiples dans le cadre d’un acute-on-chronic liver failure de grade 3 (ACLF-3) ou de créatinine supérieure ou égale à 50 mg/l (440 μmol/l), en raison d’un taux de réponse plus faible et d’un risque accru d’insuffisance respiratoire observé chez ces patients lors d’une analyse en sous-groupe (44). Une dysfonction cardiaque diastolique est fréquente chez les patients avec SHR-IRA (45). Ainsi, chez des patients à plus haut risque d’évènements respiratoires, un nombre croissant d’experts suggère l’utilisation d’une échocardiographie ciblée permettant d’évaluer la volémie afin de mieux adapter l’expansion volémique administrée au patient (44, 46). Il faut noter, que la terlipressine administrée par perfusion continue a été associée à moins d’événements indésirables, en particulier respiratoires, par rapport à l’administration en bolus (38). Considérant ces éléments, une surveillance clinique pluriquotidienne est nécessaire pour dépister précocement les potentielles complications cardiovasculaires et respiratoires des patients sous terlipressine. Un examen clinique cardiorespiratoire et une radiographie de thorax avant l’instauration de terlipressine devraient être réalisés.
La norépinéphrine est un vasoconstricteur systémique qui agit en activant les récepteurs -1 adrénergiques des cellules musculaires lisses vasculaires. La norépinéphrine est administrée en perfusion continue (à partir de 0,5 mg/h et titrée pour obtenir une augmentation de 10 mmHg de la PAM) et doit être administrée via une voie veineuse centrale en unité de soins critiques. Les données vis-à-vis de son efficacité en comparaison à la terlipressine sont contradictoires (39-43). Une large métanalyse regroupant 394 patients issus de 9 études randomisées controlées conclu en une supériorité de la terlipressine pour le traitement du SHR motivant les experts de l’AFEF et de la SFAR ainsi que ceux de l’EASL et de l’AASLD à recommander l’utilisation de la terlipressine en perfusion continue en première intention pour le traitement du SHR-IRA (34, 24, 70, 71).

Figure 3 : Algorithme de prise en charge du syndrome hépatorénal-insuffisance rénale aiguë (SHR-IRA)
ACLF-3 : acute-on-chronic liver failure grade 3 ; EER : épuration extra-rénale ; ETT : échocardiographie ; IVSE : voie intra veineuse à la seringue électrique ; PVC : pression veineuse centrale ; TH : transplantation hépatique.
La troisième option thérapeutique est représentée par l’association de la midodrine, un agoniste oral des récepteurs a-1 adrénergiques et de l’octréotide, un analogue de la somatostatine qui agit en tant que vasoconstricteur mésentérique direct. La midodrine, administrée à des posologies entre 5 et 15 mg trois fois par jour, est titrée avec pour objectif d’augmenter la PAM d’environ 10 mmHg. L’octréotide peut être administrée soit par voie sous-cutanée (100 à 200 µg trois fois par jour) soit en perfusion continue (50 µg/h). À ce jour, il n’y a eu qu’une seule étude comparant l’effet de la terlipressine avec la combinaison midodrine et octréotide rapportant un taux de réponse global de 28,6 % contre 70,4 % pour la terlipressine (47).
L’infusion d’albumine permet de corriger l’hypovolémie efficace et doit être utilisée en association avec la thérapie vasoconstrictrice. L’albumine a aussi des effets inotropes positifs sur le cœur et exerce des propriétés antioxydantes et immunomodulatrices. Son administration, comprise entre 20 et 40g/j doit être guidée par l’évaluation clinique de la volémie, et idéalement de l’échocardiographique et de la mesure de la pression veineuse centrale (10, 24).
Dès lors qu’un traitement vasoconstricteur associé à des perfusions d’albumine est instauré, un projet de TH, seul traitement définitif du SHR, doit être envisagé (figure 3).
Shunt intra-hépatique porto-systémique par voie transjugulaire (TIPS)
L’hypertension portale peut être traitée par la mise en place d’un shunt porto-systémique intrahépatique par voie transjugulaire (TIPS). Alors que le TIPS est bénéfique chez les patients cirrhotiques avec ascite réfractaire ou récidivante, ou chez les patients avec hémorragie variqueuse gastro- œsophagienne aiguë ou récidivante (TIPS pré-emptif, de sauvetage ou en prophylaxie secondaire), sa place dans le traitement du SHR est encore à l’étude. Une amélioration de la fonction rénale et une réduction de l’activité du système rénine-angiotensine et du système nerveux sympathique après l’insertion d’un TIPS pour le SHR–IRA ont été démontrées dans une étude pilote non randomisée (48). Une méta-analyse de 128 patients ayant bénéficié de la mise en place d’un TIPS dans le cadre d’un SHR–IRA a rapporté une amélioration de la créatinine sérique, de la natrémie et du débit urinaire chez ces patients (49). Cependant, les patients présentant une insuffisance hépato-cellulaire sévère, une infection active ou une encéphalopathie hépatique ont été exclus de l’étude limitant les résultats à un groupe restreint de patients. Aussi, et malgré ce biais de sélection, la survie des patients avec SHR-IRA à 1 an n’était que de 47 % (49). Ceci illustre l’impact de la dysfonction hépatique sur le pronostic de ces patients et place la TH comme meilleur traitement du SHR-IRA. Ainsi les recommandations AFEF sur le TIPS parues en 2023 stipulent qu’il n’y a probablement pas lieu de recommander un TIPS chez les patients ayant un SHR-IRA avec ou sans projet de TH, la mortalité de ces patients restant liée à l’insuffisance hépatique (50). Le TIPS serait plus intéressant dans le SHR-non IRA, prévalent chez les patients présentant une ascite réfractaire ou récidivante, car permettant une amélioration de l’eDFG (51). Une normalisation complète de la fonction rénale était cependant rarement atteinte après mise en place de TIPS dans cette population soulignant une part organique à l’atteinte rénale (hypoperfusion chronique, néphropathie hypertensive ou à IgA, etc.). Considérant ces données, les recommandations françaises stipulent que un SHR-non IRA ne doit pas être une contre- indication au TIPS (50). Récemment, une large étude de cohorte observationnelle allemande rapportait une augmentation de la proportion de TIPS mis en place pour traitement d’un SHR, IRA et non-IRA, passant de 13,5 % des indications à 18,7 % en 10 ans, associé à une diminution de la mortalité intra-hospitalière (17,1 % contre 43,3 % chez les patients non traités par TIPS) soulignant l’expertise grandissante des praticiens dans la sélection des patients dans cette indication (52).
Épuration extra-rénale et transplantation hépatique ou combinée foie-rein
La décision d’initier une épuration extra-rénale (EER) chez les patients atteints de cirrhose et d’IRA est essentiellement basée sur l’étiologie de l’IRA et le projet d’un TH (figure 2). Ainsi, dans le cadre du SHR-IRA, une EER peut être envisagée en cas de projet de TH ou si la cause de l’atteinte hépatique responsable du développement du SHR-IRA est potentiellement réversible comme dans certaines hépatites liées à l’alcool ou un sepsis (34). Dans les autres cause d’IRA, une EER peut être discutée dans l’attente de la TH ou d’une transplantation combinée foie-rein. Les indications d’EER sont les mêmes que dans la population générale et incluent l’acidose métabolique sévère, les troubles ioniques dont l’hyperkaliémie menaçante et l’anasarque avec œdème aigu pulmonaire (24). Le bénéfice d’une initiation précoce de l’EER permettant d’optimiser la volémie dans l’attente de la TH ou pour le traitement de l’hyperammoniémie et la prévention de l’encéphalopathie hépatique sévère est suggérée mais reste à démontrer (24, 53, 54). Les modalités d’EER continue (hémofiltration, ou hémodiafiltration continue) doivent être privilégiées car mieux tolérées sur le plan hémodynamique que les dialyses intermittentes et l’anticoagulation des circuits d’EER peut être réalisée selon l’expertise locale (héparine, epoprostenol ou citrate) (53-55).
La probabilité de récupération d’une fonction rénale normale est importante (entre 60 % et 90 %) en cas de TH seule chez les patients ayant présenté un SHR-IRA ou une NTA (56-58). Cependant une IRA persistante ou une EER prolongée avant la TH ont été associées à une probabilité faible de normalisation de la fonction rénale après TH. Ainsi, il est admis que le recours à une EER pendant plus de 6 semaines avant la TH ou la persistance d’un eDFG ≤ 25 ml/min après 6 semaines doit faire discuter une transplantation combinée foie-rein à l’instar de ce qui est recommandé aux États-Unis (59).
Insuffisance rénale chronique
Généralités
Le nombre de patients cirrhotiques présentant une insuffisance rénale chronique (IRC) a augmenté ces dernières années dans un contexte épidémique de maladie du foie d’origine dysmétabolique (60). En effet, la présence de facteurs de risques métaboliques (en particulier l’hypertension artérielle, l’insulinorésistance et le diabète) est responsable de lésions rénales principalement microvasculaires participant au développement d’une IRC. Les patients avec maladie du foie dysmétabolique ont une augmentation du risque de 50 % environ de développer une IRC sévère (61). Ainsi, ces 15 dernières années, à mesure que la prévalence de la maladie hépatique d’origine dysmétabolique a augmenté parmi les candidats à la transplantation hépatique, la proportion de receveurs atteints d’IRC a augmenté et toucherait désormais près de 15 % des candidats à la greffe (62). Chez les patients en attente de greffe avec suspicion de maladie rénale chronique, il a été démontré qu’environ 2/3 présentaient des lésions modérées à sévère de glomérulonéphrites ou glomérulosclérose et de fibrose interstitielle (63). Il faut noter aussi que les infections chroniques par les virus de l’hépatite B et C peuvent également être associées à des maladies glomérulaires et au développement d’IRC de même que les dépôts d’IgA en lien avec l’étiologie éthylique et virale C de la cirrhose. Une prise en charge conjointe avec le néphrologue permettra de faire le bilan à la recherche des causes d’IRC et discuter de la réalisation d’une biopsie rénale afin d’identifier la sévérité et les causes des lésions glomérulaires, tubulaires et interstitielles. Plus spécifiquement, le rapport protéinurie / créatininurie > 0,5 g/g faisant évoquer une glomérulopathie doit faire réaliser un bilan étiologique dédié permettant de dépister maladies inflammatoires chroniques (lupus, vascularite, cryoglobulinémie, amylose primitive ou secondaire), infections (hépatites virales, VIH, maladies parasitaires), hémopathies et causes médicamenteuses. En plus de l’IRC sous-jacente liée à une maladie rénale intrinsèque, l’hypertension portale peut également contribuer à une dysfonction rénale chronique, généralement dans le contexte d’une ascite réfractaire. Auparavant connue sous le nom de SHR de type 2, certains patients atteints de cirrhose et d’hypertension portale peuvent développer une forme d’insuffisance rénale plus progressivement évolutive. En fonction de la chronologie de la progression de la maladie dans le contexte des critères actualisés de l’IRA, ces patients atteints de SHR non-IRA peuvent être classés en fonction de la durée de leur dysfonction rénale avec une présentation subaiguë dans les 3 mois, ou chronique au-delà de 3 mois (tableau 1). L’IRC pré-transplantation est étroitement liée à la survie post-transplantation et est associée à un sur-risque de décès d’environ 15 % après TH (62). Considérant ces éléments, il est recommandé de dépister précocement une dysfonction rénale afin de mettre en œuvre des mesures pouvant prévenir l’aggravation des lésions rénales et minimiser les complications de l’IRC (anémie, altérations du métabolisme osseux et ostéoporose, évènements cardiovasculaires). Dans le cadre du SHR non-IRA, la terlipressine associée à la perfusion d’albumine semble être efficace, même si le niveau de preuve est faible. Cependant, le risque élevé de récidive du SHR non-IRA et l’absence de bénéfice de ce traitement sur l’évolution de la fonction rénale après TH ne permettent pas d’en recommander l’emploi (10, 42, 64).
Épuration extra-rénale (EER), transplantation hépatique ou rénale isolée ou transplantation combinée foie-rein
La décision de débuter une EER chez les patients cirrhotiques avec IRC terminale est complexe car le risque de décès, en l’absence de transplantation combinée foie-rein, est majeur. En effet, dans une large série rétrospective française, il était observé que deux ans après l’initiation de l’EER, 40 % des patients compensés et 60 % des patients décompensés étaient décèdés (65). De plus, il n’est pas démontré que l’instauration d’une EER chez les patients cirrhotiques avec IRC permette d’améliorer la survie sans transplantation. Ainsi, en l’absence de projet de transplantation combinée foie-rein, la décision de débuter une EER doit être discutée au cas par cas, prenant en compte les facteurs associés au pronostic dans cette population (âge et comorbidités incluant les antécédents cardiologiques, métaboliques et oncologiques) et la volonté du patient (65). La balance bénéfice risque de la dialyse péritonéale a souvent été considérée en défaveur de cette approche (risques infectieux, hémorragiques et d’encéphalopathie hépatique en particulier). Quelques études observationnelles et de faible effectif rapportent cependant une absence de sur-risque liée à cette technique avec une meilleure tolérance hémodynamique en comparaison à l’EER intermittente. La place de la dialyse péritonéale reste donc à définir plus précisément dans cette population (66).
Chez les patients candidats à la greffe d’organes, l’attitude la plus consensuelle est celle d’une transplantation combinée foie-rein en cas de cirrhose et d’IRC (≥ 3 mois) nécessitant un recours aux EER ou avec un eDFG ≤ 35 ml/min (59). Alors que le bénéfice d’une transplantation combinée est certain chez les patients nécessitant une EER, celui-ci est plus discutable pour ceux avec eDFG ≤ 35 ml/min n’ayant pas recours à l’EER. La transplantation combinée n’est pas indiquée pour les patient dont le eDGF est compris entre 35 et 60 ml/min, le bénéfice de cette approche étant nul (67, 68). Chez certains patients avec IRC présentant une cirrhose compensée sans hypertension portale cliniquement significative et dont la maladie causale est contrôlée (éradication du virus de l’hépatite C ou abstinence suivie de consommation d’alcool), et en l’absence de cofacteurs de progression de la maladie hépatique, il a été suggéré qu’une transplantation rénale isolée pourrait être entreprise (65, 69). Ces patients auraient en effet un risque faible d’évènement hépatique au cours du temps ne justifiant pas le recours à une transplantation combinée foie-rein.
Conclusion
L’insuffisance rénale aiguë complique fréquemment l’histoire naturelle de la cirrhose et est associée au pronostic de celle-ci. Le SHR–IRA, dont les critères ont été revus récemment, correspond à une IRA d’allure fonctionnelle spécifique du patient cirrhotique dont le pronostic, en lien avec la gravité de la maladie hépatique, est plus sévère que celui des autres causes d’IRA. Au-delà de la dysfonction circulatoire, la place de l’inflammation systémique comme facteur important dans la physiopathologie du SHR-IRA a été récemment suggérée. La prévention du SHR-IRA est importante et comprend entre autres les perfusions d’albumine lors des ponctions évacuatrices de large volume et en cas d »infection spontanée du liquide d’ascite. De nouveaux biomarqueurs tels que le NGAL peuvent être utiles pour distinguer le SHR-IRA et la nécrose tubulaire aiguë. Le traitement de première intention du SHR–IRA est la combinaison d’un traitement vasoconstricteur et l’administration intraveineuse d’albumine. Alors que la place du TIPS nécessite encore d’être déterminée, l’EER, lorsqu’elle est indiquée, peut être proposée en traitement d’attente de la TH ou en cas de réversibilité de la cause de l’insuffisance rénale aigüe. La transplantation hépatique doit être discutée chez tous patients présentant un SHR-IRA et ne doit être associée à une transplantation rénale que pour les patients ayant une faible probabilité de récupération de la fonction rénale après TH.
La prévalence de l’insuffisance rénale chronique est en augmentation chez les patients atteints de cirrhose. Ceci est lié à une prévalence plus élevée des patients avec maladies dysmétaboliques hépatiques présentant des facteurs de risque de développement de maladie rénale chronique. La transplantation combinée foie-rein est indiquée chez les patients avec IRC et nécessitant une EER ou avec eDFG ≤ 35 ml/min. En l’absence de projet de TH, le pronostic des patients cirrhotiques en indication d’EER reste sombre même en cas de cirrhose compensée. Ainsi, la décision doit être prise au cas par cas après prise en compte des comorbidités et de la volonté du patient.
Références
- Belcher JM, Garcia-Tsao G, Sanyal AJ, Bhogal H, Lim JK, Ansari N, et Association of AKI with mortality and complications in hospitalized patients with cirrhosis. Hepatology. févr 2013;57(2):753-62.
- Piano S, Rosi S, Maresio G, Fasolato S, Cavallin M, Romano A, et Evaluation of the Acute Kidney Injury Network criteria in hospitalized patients with cirrhosis and ascites. J Hepatol. sept 2013;59(3):482-9.
- Garcia-Tsao G, Parikh CR, Viola Acute kidney injury in cirrhosis. Hepatology. déc 2008;48(6):2064-77.
- Arroyo V, Ginès P, Gerbes AL, Dudley FJ, Gentilini P, Laffi G, et Definition and diagnostic criteria of refractory ascites and hepatorenal syndrome in cirrhosis. International Ascites Club. Hepatology. janv 1996;23(1):164-76.
- Bellomo R, Ronco C, Kellum JA, Mehta RL, Palevsky P, Acute Dialysis Quality Initiative Acute renal failure – definition, outcome measures, animal models, fluid therapy and information technology needs: the Second International Consensus Conference of the Acute Dialysis Quality Initiative (ADQI) Group. Crit Care. août 2004;8(4):R204-212.
- Mehta RL, Kellum JA, Shah SV, Molitoris BA, Ronco C, Warnock DG, et al. Acute Kidney Injury Network: report of an initiative to improve outcomes in acute kidney injury. Crit Care. 2007;11(2):R31.
- Summary of Recommendation Kidney Int Suppl (2011). mars 2012;2(1):8-12.
- Angeli P, Gines P, Wong F, Bernardi M, Boyer TD, Gerbes A, et Diagnosis and management of acute kidney injury in patients with cirrhosis: revised consensus recommendations of the International Club of Ascites. Gut. avr 2015;64(4):531-7.
- Salerno F, Gerbes A, Ginès P, Wong F, Arroyo Diagnosis, prevention and treatment of hepatorenal syndrome in cirrhosis. Gut. sept 2007;56(9):1310-8.
- Angeli P, Garcia-Tsao G, Nadim MK, Parikh News in pathophysiology, definition and classification of hepatorenal syndrome: A step beyond the International Club of Ascites (ICA) consensus document. J Hepatol. oct 2019;71(4):811-22.
- Piano S, Romano A, Di Pascoli M, Angeli Why and how to measure renal function in patients with liver disease. Liver Int. janv 2017;37 Suppl 1:116-22.
- Kalafateli M, Wickham F, Burniston M, Cholongitas E, Theocharidou E, Garcovich M, et Development and validation of a mathematical equation to estimate glomerular filtration rate in cirrhosis: The royal free hospital cirrhosis glomerular filtration rate. Hepatology. févr 2017;65(2):582-91.
- Wong The evolving concept of acute kidney injury in patients with cirrhosis. Nat Rev Gastroenterol Hepatol. déc 2015;12(12):711-9.
- Simonetto DA, Gines P, Kamath Hepatorenal syndrome: pathophysiology, diagnosis, and management. BMJ. 14 sept 2020;370:m2687.
- Matchett CL, Simonetto DA, Kamath Renal Insufficiency in Patients with Cirrhosis. Clin Liver Dis. févr 2023;27(1):57-70.
- Piano S, Favaretto E, Tonon M, Antonelli G, Brocca A, Sticca A, et Including Relative Adrenal Insufficiency in Definition and Classification of Acute-on-Chronic Liver Failure. Clin Gastroenterol Hepatol. mai 2020;18(5):1188-1196.e3.
- Wong F, Pappas SC, Curry MP, Reddy KR, Rubin RA, Porayko MK, et Terlipressin plus Albumin for the Treatment of Type 1 Hepatorenal Syndrome. N Engl J Med. 4 mars 2021;384(9):818-28.
- Martín-Llahí M, Guevara M, Torre A, Fagundes C, Restuccia T, Gilabert R, et Prognostic importance of the cause of renal failure in patients with cirrhosis. Gastroenterology. févr 2011;140(2):488-496.e4.
- Verna EC, Brown RS, Farrand E, Pichardo EM, Forster CS, Sola-Del Valle DA, et Urinary neutrophil gelatinase-associated lipocalin predicts mortality and identifies acute kidney injury in cirrhosis. Dig Dis Sci. sept 2012;57(9):2362-70.
- Huelin P, Solà E, Elia C, Solé C, Risso A, Moreira R, et Neutrophil Gelatinase-Associated Lipocalin for Assessment of Acute Kidney Injury in Cirrhosis: A Prospective Study. Hepatology. juill 2019;70(1):319-33.
- Fagundes C, Pépin MN, Guevara M, Barreto R, Casals G, Solà E, et Urinary neutrophil gelatinase-associated lipocalin as biomarker in the differential diagnosis of impairment of kidney function in cirrhosis. J Hepatol. août 2012;57(2):267-73.
- Gambino C, Piano S, Stenico M, Tonon M, Brocca A, Calvino V, et al. Diagnostic and prognostic performance of urinary neutrophil gelatinase- associated lipocalin in patients with cirrhosis and acute kidney injury. Hepatology. 1 mai 2023;77(5):1630-8.
- Puthumana J, Ariza X, Belcher JM, Graupera I, Ginès P, Parikh Urine Interleukin 18 and Lipocalin 2 Are Biomarkers of Acute Tubular Necrosis in Patients With Cirrhosis: A Systematic Review and Meta-analysis. Clin Gastroenterol Hepatol. juill 2017;15(7):1003-1013.e3.
- European Association for the Study of the Electronic address: [email protected], European Association for the Study of the Liver. EASL Clinical Practice Guidelines for the management of patients with decompensated cirrhosis. J Hepatol. août 2018;69(2):406-60.
- Wong F, Jepsen P, Watson H, Vilstrup Un-precipitated acute kidney injury is uncommon among stable patients with cirrhosis and ascites. Liver Int. oct 2018;38(10):1785-92.
- Ginès P, Titó L, Arroyo V, Planas R, Panés J, Viver J, et Randomized comparative study of therapeutic paracentesis with and without intravenous albumin in cirrhosis. Gastroenterology. juin 1988;94(6):1493-502.
- Bernardi M, Caraceni P, Navickis RJ, Wilkes Albumin infusion in patients undergoing large-volume paracentesis: a meta-analysis of randomized trials. Hepatology. avr 2012;55(4):1172-81.
- Bernardi M, Angeli P, Claria J, Moreau R, Gines P, Jalan R, et Albumin in decompensated cirrhosis: new concepts and perspectives. Gut. juin 2020;69(6):1127-38.
- Fernández J, Monteagudo J, Bargallo X, Jiménez W, Bosch J, Arroyo V, et A randomized unblinded pilot study comparing albumin versus hydroxyethyl starch in spontaneous bacterial peritonitis. Hepatology. sept 2005;42(3):627-34.
- Follo A, Llovet JM, Navasa M, Planas R, Forns X, Francitorra A, et Renal impairment after spontaneous bacterial peritonitis in cirrhosis: incidence, clinical course, predictive factors and prognosis. Hepatology. déc 1994;20(6):1495-501.
- Sort P, Navasa M, Arroyo V, Aldeguer X, Planas R, Ruiz-del-Arbol L, et Effect of intravenous albumin on renal impairment and mortality in patients with cirrhosis and spontaneous bacterial peritonitis. N Engl J Med. 5 août 1999;341(6):403-9.
- Fernández J, Navasa M, Planas R, Montoliu S, Monfort D, Soriano G, et Primary prophylaxis of spontaneous bacterial peritonitis delays hepatorenal syndrome and improves survival in cirrhosis. Gastroenterology. sept 2007;133(3):818-24.
- Velez JCQ, Nietert Therapeutic response to vasoconstrictors in hepatorenal syndrome parallels increase in mean arterial pressure: a pooled analysis of clinical trials. Am J Kidney Dis. déc 2011;58(6):928-38.
- Admin Insuffisance hépatique en soins critiques – La SFAR [Internet]. Société Française d’Anesthésie et de Réanimation. 2018 [cité 20 sept 2023]. Disponible sur: https://sfar.org/insuffisance-hepatique-en-soins-critiques/
- Boyer TD, Sanyal AJ, Wong F, Frederick RT, Lake JR, O’Leary JG, et al. Terlipressin Plus Albumin Is More Effective Than Albumin Alone in Improving Renal Function in Patients With Cirrhosis and Hepatorenal Syndrome Type 1. Gastroenterology. juin 2016;150(7):1579-1589.e2.
- Martín-Llahí M, Pépin MN, Guevara M, Díaz F, Torre A, Monescillo A, et al. Terlipressin and albumin vs albumin in patients with cirrhosis and hepatorenal syndrome: a randomized study. Gastroenterology. mai 2008;134(5):1352-9.
- Rodríguez E, Elia C, Solà E, Barreto R, Graupera I, Andrealli A, et al. Terlipressin and albumin for type-1 hepatorenal syndrome associated with sepsis. J Hepatol. mai 2014;60(5):955-61.
- Cavallin M, Piano S, Romano A, Fasolato S, Frigo AC, Benetti G, et Terlipressin given by continuous intravenous infusion versus intravenous boluses in the treatment of hepatorenal syndrome: A randomized controlled study. Hepatology. mars 2016;63(3):983-92.
- Sharma P, Kumar A, Shrama BC, Sarin An open label, pilot, randomized controlled trial of noradrenaline versus terlipressin in the treatment of type 1 hepatorenal syndrome and predictors of response. Am J Gastroenterol. juill 2008;103(7):1689-97.
- Facciorusso A, Chandar AK, Murad MH, Prokop LJ, Muscatiello N, Kamath PS, et al. Comparative efficacy of pharmacological strategies for management of type 1 hepatorenal syndrome: a systematic review and network meta-analysis. Lancet Gastroenterol févr 2017;2(2):94-102.
- Arora V, Maiwall R, Rajan V, Jindal A, Muralikrishna Shasthry S, Kumar G, et Terlipressin Is Superior to Noradrenaline in the Management of Acute Kidney Injury in Acute on Chronic Liver Failure. Hepatology. févr 2020;71(2):600-10.
- Alessandria C, Ottobrelli A, Debernardi-Venon W, Todros L, Cerenzia MT, Martini S, et Noradrenalin vs terlipressin in patients with hepatorenal syndrome: a prospective, randomized, unblinded, pilot study. J Hepatol. oct 2007;47(4):499-505.
- Singh V, Ghosh S, Singh B, Kumar P, Sharma N, Bhalla A, et al. Noradrenaline vs. terlipressin in the treatment of hepatorenal syndrome: a randomized study. J Hepatol. juin 2012;56(6):1293-8.
- Belcher JM, Parada XV, Simonetto DA, Juncos LA, Karakala N, Wadei HM, et Terlipressin and the Treatment of Hepatorenal Syndrome: How the CONFIRM Trial Moves the Story Forward. Am J Kidney Dis. mai 2022;79(5):737-45.
- Izzy M, VanWagner LB, Lin G, Altieri M, Findlay JY, Oh JK, et Redefining Cirrhotic Cardiomyopathy for the Modern Era. Hepatology. janv 2020;71(1):334-45.
- Koratala A, Ronco C, Kazory Albumin Infusion in Patients with Cirrhosis: Time for POCUS-Enhanced Physical Examination. Cardiorenal Med. 2021;11(4):161-5.
- Cavallin M, Kamath PS, Merli M, Fasolato S, Toniutto P, Salerno F, et Terlipressin plus albumin versus midodrine and octreotide plus albumin in the treatment of hepatorenal syndrome: A randomized trial. Hepatology. août 2015;62(2):567-74.
- Guevara M, Ginès P, Bandi JC, Gilabert R, Sort P, Jiménez W, et Transjugular intrahepatic portosystemic shunt in hepatorenal syndrome: effects on renal function and vasoactive systems. Hepatology. août 1998;28(2):416-22.
- Song T, Rössle M, He F, Liu F, Guo X, Qi Transjugular intrahepatic portosystemic shunt for hepatorenal syndrome: A systematic review and meta-analysis. Dig Liver Dis. avr 2018;50(4):323-30.
- Recommandations de l’association française pour l’étude du foie (AFEF) sur le shunt hépatique par voie transjugulaire (TIPS).
- Allegretti AS, Ortiz G, Cui J, Wenger J, Bhan I, Chung RT, et Changes in Kidney Function After Transjugular Intrahepatic Portosystemic Shunts Versus Large-Volume Paracentesis in Cirrhosis: A Matched Cohort Analysis. Am J Kidney Dis. sept 2016;68(3):381-91.
- Gu W, Zeleke Y, Hortlik H, Schaaf L, Uschner FE, Schulz M, et Use and outcome of TIPS in hospitalized patients in Germany: A Nationwide study (2007-2018). Hepatol Commun. 1 oct 2023;7(10):e0237.
- Karvellas CJ, Gustot T, Fernandez Management of the acute on chronic liver failure in the intensive care unit. Liver Int. 27 juin 2023.
- Bernal W, Karvellas C, Saliba F, Saner FH, Meersseman Intensive care management of acute-on-chronic liver failure. J Hepatol. juill 2021;75 Suppl 1:S163-77.
- Slowinski T, Morgera S, Joannidis M, Henneberg T, Stocker R, Helset E, et al. Safety and efficacy of regional citrate anticoagulation in continuous venovenous hemodialysis in the presence of liver failure: the Liver Citrate Anticoagulation Threshold (L-CAT) observational Crit Care. 29 sept 2015;19:349.
- Wong F, Leung W, Al Beshir M, Marquez M, Renner Outcomes of patients with cirrhosis and hepatorenal syndrome type 1 treated with liver transplantation. Liver Transpl. mars 2015;21(3):300-7.
- Marik PE, Wood K, Starzl The course of type 1 hepato-renal syndrome post liver transplantation. Nephrol Dial Transplant. févr 2006;21(2):478-82.
- Nadim MK, Genyk YS, Tokin C, Fieber J, Ananthapanyasut W, Ye W, et Impact of the etiology of acute kidney injury on outcomes following liver transplantation: acute tubular necrosis versus hepatorenal syndrome. Liver Transpl. mai 2012;18(5):539-48.
- Organ Procurement and Transplantation Policies. 2023. [Internet]. Disponible sur: chrome-extension:// efaidnbmnnnibpcajpcglclefindmkaj/https://optn.transplant.hrsa.gov/media/eavh5bf3/optn_policies.pdf
- Estes C, Anstee QM, Arias-Loste MT, Bantel H, Bellentani S, Caballeria J, et Modeling NAFLD disease burden in China, France, Germany, Italy, Japan, Spain, United Kingdom, and United States for the period 2016-2030. J Hepatol. oct 2018;69(4):896-904.
- Mantovani A, Petracca G, Beatrice G, Csermely A, Lonardo A, Schattenberg JM, et Non-alcoholic fatty liver disease and risk of incident chronic kidney disease: an updated meta-analysis. Gut. janv 2022;71(1):156-62.
- Cullaro G, Verna EC, Lee BP, Lai Chronic Kidney Disease in Liver Transplant Candidates: A Rising Burden Impacting Post-Liver Transplant Outcomes. Liver Transpl. avr 2020;26(4):498-506.
- Wadei HM, Abader P, Alsaad AA, Croome K, Cortese C, Geiger XJ, et Arterial Blood Pressure at Liver Transplant Evaluation Predicts Renal Histology in Candidates With Renal Dysfunction. Liver Transpl. déc 2019;25(12):1756-67.
- Rodriguez E, Henrique Pereira G, Solà E, Elia C, Barreto R, Pose E, et Treatment of type 2 hepatorenal syndrome in patients awaiting transplantation: Effects on kidney function and transplantation outcomes. Liver Transpl. nov 2015;21(11):1347-54.
- Artru F, Louvet A, Glowacki F, Bellati S, Frimat M, Gomis S, et The prognostic impact of cirrhosis on patients receiving maintenance haemodialysis. Aliment Pharmacol Ther. juill 2019;50(1):75-83.
- Rajora N, De Gregorio L, Saxena Peritoneal Dialysis Use in Patients With Ascites: A Review. Am J Kidney Dis. nov 2021;78(5):728-35.
- Tinti F, Mitterhofer AP, Umbro I, Nightingale P, Inston N, Ghallab M, et al. Combined liver-kidney transplantation versus liver transplant alone based on KDIGO stratification of estimated glomerular filtration rate: data from the United Kingdom Transplant registry – a retrospective cohort study. Transpl Int. sept 2019;32(9):918-32.
- Sharma P, Goodrich NP, Schaubel DE, Guidinger MK, Merion Patient-specific prediction of ESRD after liver transplantation. J Am Soc Nephrol. déc 2013;24(12):2045-52.
- Kidney Disease: Improving Global Outcomes (KDIGO). KDIGO clinical practice guidelines for the prevention, diagnosis, evaluation, and treatment of hepatitis C in chronic kidney disease. Kidney Int Suppl. avr 2008;(109):S1-99.
- Flamm SL, Wong F, Ahn J, Kamath Aga Clinical Practice Update on the Evaluation tion and Management of Acute Kidney Injury in Patients With Cirrhosis: Expert Review. Clin Gastroenterol Hepatol. 2022 Dec;20(12):2707-2716.
- Israelsen M, Krag A, Allegretti AS, Jovani M, Goldin AH, Winter RW, Gluud Terlipressin versus other vasoactive drugs for hepatorenal syndrome. Cochrane Database Syst Rev. 2017 Sep 27;9(9):CD011532.