Liens d’intérêts
MEDTRONIC – Fourniture de matériel pour étude clinique (2012-2015)
SANDHILL – Fourniture de matériel pour étude clinique (2012-2015)
TAKEDA – Honoraires recherche clinique (2012-2016)
SHIRE – Honoraires recherche clinique + consultant (2012-2013)
MEDTRONIC/COVIDIEN – Consultant / intervenant (2012-2014)
ALLERGAN – Consultant (2016-2017)
RECKITT-BENKISER – Consultant (2014-2016)
TAKEDA – Intervenant – 2016
VIFOR PHARMA – Intervenant – 2015
Mots-clés : Achalasie – Manométrie haute résolution – Dysphagie
Introduction
Les troubles moteurs de l’œsophage (TMO) sont essentiellement responsables de dysphagie et de douleurs thoraciques, plus rarement de régurgitations, voire de pyrosis. En première intention, la dysphagie doit être explorée par endoscopie haute pour éliminer une pathologie obstructive, au cours de laquelle des biopsies œsophagiennes seront pratiquées pour éliminer une éventuelle œsophagite à éosinophiles. En l’absence d’anomalie muqueuse ou histologique, c’est la manométrie œsophagienne qui permettra d’identifier d’éventuels TMO [1].
La manométrie œsophagienne haute résolution
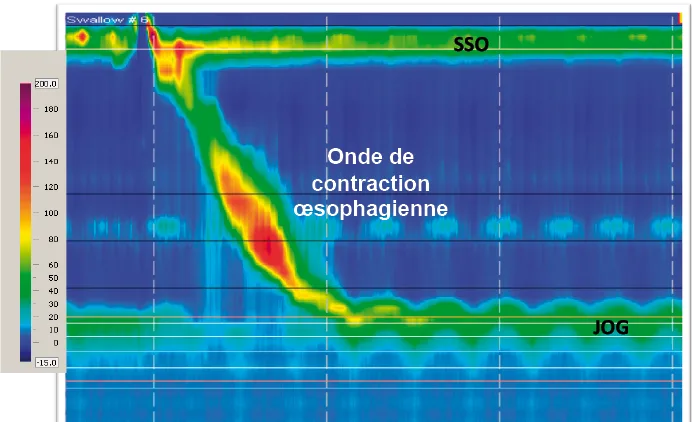
La manométrie œsophagienne haute résolution (MHR) est maintenant l’examen de référence pour le diagnostic des TMO [2]. Par rapport à la manométrie conventionnelle, la MHR est plus rapide et mieux tolérée [3]. En effet, son positionnement est aisé : les 2 zones de haute pression correspondant respectivement au sphincter supérieur et à la jonction œso-gastrique sont facilement repérables et permettent de vérifier le positionnement correct de la sonde. Une fois en place, le retrait progressif de la sonde n’est pas nécessaire puisque, compte tenu du nombre de capteurs de pression, des mesures sont effectuées simultanément du pharynx jusqu’à l’estomac, ce qui raccourcit considérablement la durée de l’examen. De plus, la représentation graphique en code couleur des variations de pression facilite l’apprentissage de l’analyse et améliore la reproductibilité inter-observateur, y compris chez des non experts (Figure 1). D’un point de vue diagnostique, les pathologies identifiées par la manométrie conventionnelle le sont évidemment aussi par la MHR avec une sensibilité qui pourrait être meilleure, même si ce n’est pas encore formellement démontré. Le gain diagnostique serait de 10 à 20 % pour l’exploration des dysphagies inexpliquées. Même s’il diminue, le coût du matériel reste élevé et en limite la diffusion pour l’instant, mais de plus en plus de centres « non experts » en France sont maintenant équipés. La classification des troubles moteurs œsophagiens proposée par l’équipe de Chicago à partir des données fournies par la MHR est basée sur l’étude de la relaxation de la jonction œso-gastrique et de la motricité dans le corps de l’œsophage [4].

Figure 1. Exemple de manométrie oesophagienne normale
(SSO : sphincter supérieur de l’oesophage, JOG : jonction oeso-gastrique)
La classification de Chicago
La dernière version de la classification de Chicago (version 3.0) date de 2014 ; elle définit les principaux troubles moteurs œsophagiens en distinguant les troubles dits « majeurs », jamais observés chez des sujets sains, des troubles « mineurs » dont la signification est incertaine, en particulier pour expliquer une dysphagie (Figure 2).

Figure 2. Classification de Chicago 3.0.
(PRI : pression de relaxation intégrée, JOG : jonction oeso-gastrique,ICD : intégrale de contraction distale, LD : latence distale)
Les principaux paramètres utilisés (Figure 3)
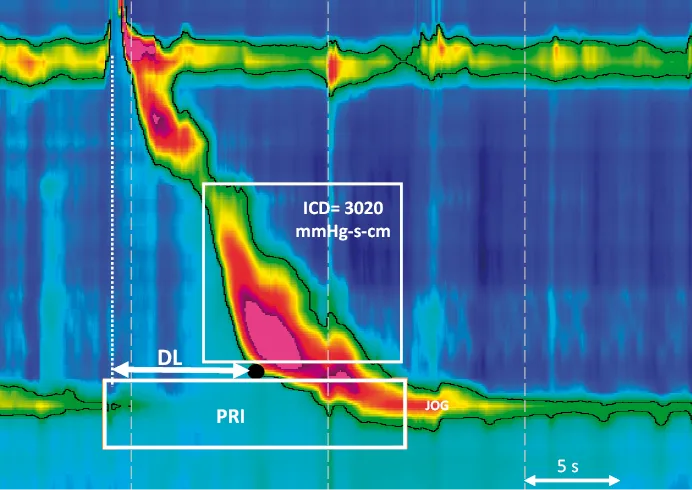
- La pression de relaxation intégrée 4s (PRI-4s) est le paramètre essentiel évaluant la relaxation de la jonction œso-gastrique (JOG) ; elle correspond à la pression la plus basse de la JOG enregistrée durant 4 secondes non forcément consécutives en réponse à une déglutition. Les seuils de 15 mmHg avec le système Medtronic° et de 28 mmHg avec les systèmes MMS° et Sandhill° permettent de mieux discriminer les patients ayant une achalasie des sujets témoins.
- La vigueur d’une onde de contraction est appréciée dans le segment œsophagien distal par le calcul de l’intégrale de contraction distale (ICD). L’ICD est le produit de la longueur du segment œsophagien distal (mesuré en cm depuis la zone de transition jusqu’au bord supérieur de la JOG) par la durée de la contraction en secondes et par la pression moyenne dans cette fenêtre en mm Hg. Elle est normale lorsqu’elle est inférieure à 5 000 mm Hg.s.cm. Une onde de contraction est dite « absente » lorsqu’elle a une ICD < 100 mmHg.s.cm, « faible » avec ICD > 100 mmHg.s.cm mais < 450 mmHg.s.cm et « hypercontractile » avec une ICD > 8,000 mmHg.s.cm.
- La latence distale (LD) d’une onde de contraction est mesurée à l’aide du « Point de décélération de la contraction » (PDC) au niveau de l’isocontour de 30 mmHg. La latence distale évalue l’intégrité de l’innervation à l’origine de l’onde inhibitrice qui précède une contraction œsophagienne. Une onde de contraction est dite « prématurée » lorsque la latence distale est inférieure à 4,5 sec.
- Un défect de plus de 5 cm de l’onde de contraction à l’isocontour 20 mmHg définit une onde dite « fragmentée ».
- La présence d’une pressurisation œsophagienne est également évaluée. Une pressurisation dite « pan-œsophagienne » est présente dans tout le corps de l’œsophage.

Figure 3. Les principaux paramètres utilisés en manométrie haute résolution. Le point noir correspond au point de décélération de la contraction qui sert à déterminer la latence distale. PRI : pression de relaxation intégrée, LD : latence distale, ICD : intégrale de contraction distale, JOG : jonction oeso-gastrique.
Achalasie et obstruction fonctionnelle de la jonction œso-gastrique (Figure 4)
Dans les 2 cas, il existe une PRI médiane supérieure aux valeurs normales. Dans l’achalasie, outre l’IRP élevée, il existe un apéristaltisme. Trois types d’achalasie ont été définis : le type I est caractérisé par l’absence d’onde de contraction et de pressurisation, le type II par une pressurisation pan-œsophagienne dans plus de 20 % des déglutitions, et le type III par au moins 20 % de contractions prématurées. Dans l’obstruction fonctionnelle de la JOG, il persiste des séquences propagées. Elle peut correspondre à une forme précoce d’achalasie, être secondaire à une infiltration néoplasique de la JOG, ou une volumineuse hernie hiatale.

Figure 4. Les 3 types d’achalasie : type I (absence de contraction et de pressurisation), type II (pressurisation pan-oesophagienne), type III (plus de 20 % de contractions prématurées).
Troubles majeurs du péristaltisme œsophagien (Figure 5)
Ils ne sont jamais observés chez des sujets asymptomatiques.
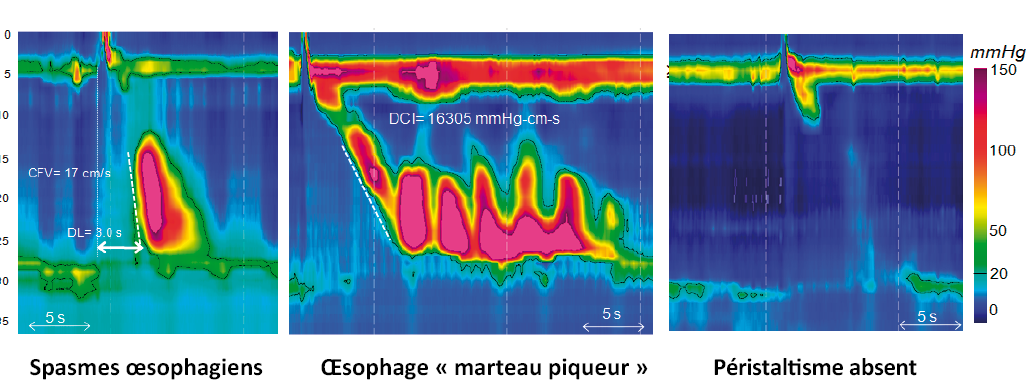
Le péristaltisme absent est défini par une PRI normale et 100 % de contractions absentes (comme ce qui est décrit dans la sclérodermie systémique).
Les spasmes distaux de l’œsophage sont définis par la présence d’au moins 20 % d’ondes prématurées (ICD > 450 mmHg.s.cm et LD < 4.5 s) associées à une PRI normale.
L’œsophage « marteau piqueur » est défini par au moins 20 % d’ondes œsophagiennes dont la DCI est supérieure à 8 000 mmHg.s.cm [5].

Figure 5. Troubles majeurs du péristaltisme oesophagien (voir texte).
Troubles mineurs du péristaltisme œsophagien (Figure 6)

Figure 6. Troubles mineurs du péristaltisme oesophagien
Le syndrome de motricité inefficace (« ineffective esophageal motility ») correspond à un hypopéristaltisme défini par au moins 50 % d’ondes œsophagiennes avec une ICD < 450 mmHg.s.cm
Le péristaltisme fragmenté est défini par au moins 50 % d’ondes avec défect de plus de 5 cm. Il faut remarquer que l’œsophage « casse-noisettes » a disparu de la classification. Il était défini dans la version précédente de la classification par une ICD moyenne > 5 000 mmHg.s.cm mais était fréquemment observé chez des sujets asymptomatiques et donc de signification incertaine [4]. Néanmoins, dans la littérature, il existe beaucoup d’études ayant inclus des patients avec dysphagie et « œsophage casse-noisettes ».
Ces troubles mineurs ont un impact sur le transit du bolus dans l’œsophage mais leur signification clinique n’est pas clairement établie. Ils peuvent être observés chez des sujets sains, en cas de reflux gastro-œsophagien, en cas de dysphagie ou de douleurs thoraciques. Des tests de provocation tels que des déglutitions répétées, l’ingestion de 200 ml d’eau ou de solides, pourraient démasquer des troubles dans les cas limites [6]. Ces tests n’ont pas encore été retenus dans la classification de Chicago en raison de données insuffisantes et/ou non concordantes entre les études.
Traitement de l’achalasie de l’œsophage
L’objectif du traitement est de réduire l’obstruction fonctionnelle de la JOG afin d’améliorer la vidange œsophagienne et donc les symptômes.
Les traitements médicamenteux tels que les inhibiteurs calciques ou les dérivés nitrés pris avant les repas ont été proposés car ils réduisent la pression du SIO. Les études contrôlées évaluant leur efficacité sont rares, ont inclus peu de patients et n’ont pas démontré de manière claire leur supériorité par rapport au placebo. De plus, ils peuvent être mal tolérés (céphalées, hypotension) [7]. Le sildenafil a fait la preuve de son efficacité pour diminuer la pression et la relaxation du SIO mais son coût est un frein à son utilisation en pratique. Il n’existe pas de données de résultats des traitements médicaux en fonction des différents types d’achalasie.
Les injections de toxine botulique au niveau de la JOG (80 à 100 UI réparties en 4 quadrants) ont fait la preuve de leur efficacité dans les études contrôlées contre placebo. Les taux de réponse à 1 mois sont de l’ordre de 90 % mais ils chutent à 30-50 % à un an et à moins de 5 % à 2 ans [8]. Des injections répétées sont donc nécessaires pour obtenir un résultat qui se maintienne à long terme. De plus, des études randomisées ont démontré la supériorité des dilatations pneumatiques et de la myotomie chirurgicale [9]. Il n’y a pas de données de résultats des injections de toxine botulique en fonction des différents types d’achalasie.
Les dilatations pneumatiques permettent de réduire la pression du SIO si elles sont effectuées avec des ballonnets d’au moins 30 mm de diamètre. La technique n’est pas bien standardisée mais il est admis que les dilatations doivent être réalisées en augmentant progressivement le diamètre des ballonnets (jusqu’à 35 ou 40 mm) en cas de persistance des symptômes. Dans les centres experts, le taux de perforation est de l’ordre de 2 %, le plus souvent lors de la 1re session. Les dilatations progressives permettent d’obtenir des taux de rémission clinique de 75 à 90 %, mais environ un tiers des patients rechutent dans les 2 à 3 ans [8, 10]. Ces rechutes sont le plus souvent traitées efficacement par de nouvelles séances de dilatation « à la demande » permettant ainsi d’obtenir des rémissions prolongées chez 70 à 80 % des patients. Les facteurs de réponse les plus souvent retrouvés dans la littérature sont le sexe féminin, l’âge supérieur à 40 ans et une pression du SIO après dilatation inférieure à 10 mmHg [8]. Surtout, il est maintenant bien établi que les achalasies de type III répondent nettement moins bien aux dilatations que les types I et II. Parmi les nombreuses études qui ont rapporté de tels résultats, l’analyse post-hoc de l’étude randomisée comparant les dilatations à la myotomie chirurgicale, il était retrouvé des taux de 85 %, 100 %, et 40 % pour les types I, II, et III, respectivement [11]. Certaines études ont suggéré que la présence d’une pressurisation pan-œsophagienne était également un facteur de succès des dilatations, expliquant les excellents taux de réponses dans les types II. Quoiqu’il en soit, il est communément admis aujourd’hui que les dilatations ne devraient plus être proposées en 1re intention dans les achalasies de type III [2].
La myotomie chirurgicale laparoscopique (intervention de Heller) consiste à réaliser une myotomie (sans perforation muqueuse) de la couche circulaire de la musculeuse de la JOG remontant sur 4-5 cm dans l’œsophage et descendant sur 2-3 cm vers l’estomac. Elle doit être associée à la création d’une valve anti-reflux partielle antérieure ou postérieure, ce qui permet de réduire de 30 à moins de 15 % la fréquence du RGO postopératoire [12]. Les taux de succès de cette intervention sont de l’ordre de 90 % mais ils chutent à 50-60 % à long terme. Les résultats de la myotomie sont également influencés par le type d’achalasie, mais dans une moindre mesure que les dilatations. Dans la littérature, les taux de succès sont de 67-85 %, 95-100 % et 70-85 % pour les types I, II et III respectivement [13 , 14]. Dans l’étude randomisée précédemment citée, les taux de réponse dans les types III étaient respectivement de 86 % et 40 % pour la chirurgie et les dilatations, sans différence significative cependant en raison des faibles effectifs [11]. La cible des dilatations étant uniquement la JOG, la myotomie chirurgicale serait plus efficace en raison de son extension en hauteur vers l’œsophage.
La myotomie endoscopique per-orale (« POEM ») a connu un essor considérable au cours des dernières années. Cette technique endoscopique consiste à créer un tunnel sous muqueux permettant d’accéder directement à la couche circulaire interne de la musculeuse œsophagienne et de la JOG, afin de réaliser une myotomie 6 cm au-dessus de la JOG et 2 cm en dessous vers l’estomac [15]. Il s’agit d’une technique sûre quand elle est effectuée dans des centres experts, le taux de complication étant très faible, essentiellement représentées par des pneumothorax, épanchements pleuraux, perforations et saignements. Dans la mesure où, contrairement à la technique chirurgicale, il n’est possible de réaliser de valve anti-reflux, le taux de RGO peut atteindre 60 % après POEM, RGO le plus souvent bien contrôlé par les IPP [16]. Néanmoins des études à long terme sont nécessaires pour s’assurer de l’absence d’évolution péjorative chez ces patients dont on rappelle qu’ils ont une clairance œsophagienne très altérée du fait de l’apéristaltisme. Plusieurs milliers de patients ont maintenant été traités et dans la littérature les taux de succès à court terme sont de l’ordre de 90 %. Des données à long terme sont nécessaires compte tenu de la dégradation des résultats constatée avec les autres types de traitement. Des comparaisons indirectes suggèrent une efficacité similaire des techniques endoscopiques et chirurgicales. Une étude contrôlée récente suggère une supériorité de la POEM sur les dilatations mais le protocole de dilatation dans cette étude n’était pas optimal [17]. Enfin des données rétrospectives non contrôlées suggèrent une efficacité intéressante de la POEM dans les achalasies de type III.
La figure 7 propose un algorithme de traitement prenant en compte les différents types d’achalasie selon la classification de Chicago [2]. Les patients à haut risque chirurgical sont plutôt candidats à des injections de toxine botulique, voire un traitement médicamenteux en cas d’échec. En cas de risque chirurgical faible, les patients avec achalasie de type I ou II relèvent soit des dilatations, soit d’une myotomie (chirurgicale ou endoscopique) en fonction des expertises de chaque centre. Les dilatations doivent être abandonnées en première intention dans les types III qui relèvent plutôt de la myotomie endoscopique ou chirurgicale. La myotomie peut être proposée en cas d’échec des dilatations et vice versa. Dans des cas exceptionnels réfractaires aux traitements habituels, une œsophagectomie peut être proposée, en particulier en cas d’œsophage « sigmoïde » très évolué. Dans les années à venir, les résultats des études randomisées en cours auront probablement un impact sur cet algorithme de prise en charge.

Figure 7. Algorithme de traitement de l’achalasie.
(* la myotomie peut être chirurgicale ou endoscopique)
Traitement de l’obstruction fonctionnelle de la JOG
Cette entité peut correspondre à une variante d’achalasie ou être secondaire à une infiltration tumorale ou une compression vasculaire qui seront mises en évidence par écho-endoscopie. L’obstruction fonctionnelle de la JOG est de description récente et les données dans la littérature sont rares. Une étude rétrospective chez 36 patients traités par injections de toxine botulique a rapporté un taux de réponse de 58,3 %, similaire à ce qui était obtenu dans l’achalasie [18]. Une autre étude fait état d’un taux de réponse de 60 % à 6 mois chez 6 patients [19].
Traitement des troubles moteurs hypercontractiles
Selon la classification de Chicago, ces troubles correspondent à l’œsophage marteau-piqueur et aux spasmes œsophagiens, mais la plupart des données de la littérature ont été rapportées avant l’avènement de la manométrie haute résolution et la confusion avec les autres troubles moteurs est fréquente. Dans tous les cas, des mesures simples doivent être préconisées comme privilégier les aliments semi solides et/ou prendre le temps d’une mastication suffisante.
Maladie des spasmes de l’œsophage
Comme dans l’achalasie, les inhibiteurs calciques et les dérivés nitrés ont été proposés mais ont une efficacité limitée et des effets secondaires significatifs. Les anti-dépresseurs, en tant que modulateurs de la douleur, pourraient améliorer les symptômes douloureux mais pas les troubles moteurs et donc la dysphagie. Les injections de toxine botulique peuvent être effectuées soit au niveau de la JOG comme dans l’achalasie, soit le long du corps de l’œsophage, technique paraissant plus adaptée à ce trouble moteur œsophagien sans anomalie de la JOG. Les études ouvertes font état de 50 à 100 % de répondeurs. Une étude randomisée en crossover a rapporté un taux de répondeurs de 50 % avec la toxine versus 10 % avec les injections de placebo [20]. Dans cette étude chez 22 patients, seulement 15 avaient une maladie des spasmes œsophagiens (dont 30 % étaient répondeurs à un ana), 7 un œsophage hyperpéristaltique (« casse-noisettes »), et seulement 7 avaient été évalués en manométrie haute résolution. Un cas de médiastinite fatale a été rapporté dans la littérature. En attendant les résultats d’autres études contrôlées qui permettront peut-être de définir les meilleurs candidats à cette technique, les injections de toxine botulique semblent représenter une option valide dans cette indication. La myotomie chirurgicale étendue au corps de l’œsophage jusqu’à la crosse aortique peut être proposée en cas de symptômes sévères, mais il n’y a que très peu de données rétrospectives et non contrôlées dans la littérature. Si la myotomie est suffisamment étendue, de bons résultats peuvent être obtenus chez 80 % des patients [21]. La place de la POEM mérite d’être précisée, mais des courtes séries ont rapporté des résultats intéressants. Cette technique pourrait permettre de réaliser des myotomies dont la longueur pourrait être déterminée par les données obtenues en manométrie haute résolution.
Œsophage hypercontractile (« marteau-piqueur »)
La plupart des études de la littérature ont inclus des œsophages hypercontractiles correspondant en fait à des œsophages casse-noisettes, qui ont disparu de la classification de Chicago. Contrairement à l’œsophage casse-noisettes, l’œsophage marteau-piqueur est une maladie rare (4,1 % des cas chez 2 000 patients consécutifs) jamais observée chez des sujets asymptomatiques [5]. Il faut penser à éliminer une œsophagite à éosinophiles, un obstacle de la JOG et un reflux gastro-œsophagien particulièrement quand une œsophagite est présente. Comme pour les autres troubles moteurs, les inhibiteurs calciques, les dérivés nitrés, voire le sildenafil, peuvent être utilisés mais avec un niveau de preuve très faible. Il n’y a pas de données contrôlées disponibles avec la toxine botulique dans cette pathologie mais quelques séries avec des résultats satisfaisants [21]. Des cas traités efficacement par POEM ont été rapportés, mais il semble que cette technique soit moins efficace que dans l’achalasie et des études prospectives sont nécessaires pour préciser la place de cette technique endoscopique.
Traitement des troubles moteurs « hypotensifs »
Ces troubles correspondent au péristaltisme absent, au syndrome de motricité œsophagienne inefficace, et au péristaltisme fragmenté. Les options thérapeutiques de ces troubles sont limitées car aucun traitement pharmacologique n’est capable de restaurer une contractilité musculaire lisse et la fonction œsophagienne. Les patients doivent prendre l’habitude de privilégier les aliments semi-solides et liquides, de bien mastiquer, et de boire en mangeant afin de faciliter la clairance œsophagienne. Ces troubles étant fréquemment associés à un RGO, un traitement du reflux doit être proposé, le plus souvent par IPP. La fundoplicature chirurgicale doit être envisagée avec beaucoup prudence compte tenu des troubles du péristaltisme œsophagien et du risque de dysphagie postopératoire. Le concept de « réserve péristaltique » correspond à la mise en évidence d’ondes de contractions d’amplitude augmentée après déglutitions multiples en manométrie. Une réserve péristaltique conservée serait associée à moins de dysphagie après fundoplicature [22]. Ces résultats doivent être confirmés par des études prospectives contrôlées.
Aucun prokinétique susceptible d’améliorer les contractions œsophagiennes n’est actuellement disponible. Les antidépresseurs (imipramine, amitriptyline, citalopram, trazodone) peuvent réduire les symptômes tels que douleurs, pyrosis, ou globus mais n’ont pas d’efficacité sur la dysphagie [23].
Conclusion
La manométrie haute résolution est devenue le « gold standard » pour le diagnostic des troubles moteurs œsophagiens, permettant une distinction plus facile entre troubles moteurs majeurs et mineurs. Elle permet d’identifier différents types d’achalasie selon la classification de Chicago, avec des implications significatives dans la prise en charge thérapeutique de ces patients. Pour l’instant cette classification n’a pas d’impact sur la prise en charge des autres types de troubles moteurs œsophagiens, mais pourrait à l’avenir aider à préciser la place de nouvelles techniques comme la myotomie endoscopique qui prend une place de plus en plus importante dans l’arsenal thérapeutique des troubles moteurs de l’œsophage.
Références
- Zerbib F, Omari T. Oesophageal dysphagia: manifestations and diagnosis. Nat Rev Gastroenterol Hepatol 2015;12:322-31.
- Zerbib F, Roman S. Current Therapeutic Options for Esophageal Motor Disorders as Defined by the Chicago Classification. J Clin Gastroenterol 2015;49:451-60.
- Roman S, Bruley Des Varannes S, Cargill G, et al. Manométrie œsophagienne de haute résolution avec analyse topographique des pressions œsophagiennes : conseils pour la pratique et adaptation française de la classification de Chicago. Hépato-Gastro et Oncologie Digestive 2012;19:316-28.
- Kahrilas PJ, Bredenoord AJ, Fox M, et al. The Chicago Classification of esophageal motility disorders, v3.0. Neurogastroenterol Motil 2015;27:160-74.
- Roman S, Tutuian R. Esophageal hypertensive peristaltic disorders. Neurogastroenterol Motil 2012;24 Suppl 1:32-9.
- Sweis R, Anggiansah A, Wong T, et al. Assessment of esophageal dysfunction and symptoms during and after a standardized test meal: development and clinical validation of a new methodology utilizing high-resolution manometry. Neurogastroenterol Motil 2014;26:215-28.
- Bassotti G, Annese V. Review article: pharmacological options in achalasia. Aliment Pharmacol Ther 1999;13:1391-6.
- Boeckxstaens GE. Achalasia. Best Pract Res Clin Gastroenterol 2007;21:595-608.
- Wang L, Li YM, Li L. Meta-analysis of randomized and controlled treatment trials for achalasia. Dig Dis Sci 2009;54:2303-11.
- Zerbib F, Thetiot V, Richy F, et al. Repeated pneumatic dilations as long-term maintenance therapy for esophageal achalasia. Am J Gastroenterol 2006;101:692-7.
- Rohof WO, Salvador R, Annese V, et al. Outcomes of treatment for achalasia depend on manometric subtype. Gastroenterology 2013;144:718-725; quiz e713-14.
- Stefanidis D, Richardson W, Farrell TM, et al. SAGES guidelines for the surgical treatment of esophageal achalasia. Surg Endosc 2012;26:296-311.
- Pandolfino JE, Kwiatek MA, Nealis T, et al. Achalasia: a new clinically relevant classification by high-resolution manometry. Gastroenterology 2008;135:1526-33.
- Salvador R, Costantini M, Zaninotto G, et al. The preoperative manometric pattern predicts the outcome of surgical treatment for esophageal achalasia. J Gastrointest Surg 2010;14:1635-45.
- Inoue H, Minami H, Kobayashi Y, et al. Peroral endoscopic myotomy (POEM) for esophageal achalasia. Endoscopy 2010;42:265-71.
- Kumbhari V, Familiari P, Bjerregaard NC, et al. Gastroesophageal reflux after peroral endoscopic myotomy: a multicenter case-control study. Endoscopy 2017;49:634-42.
- Ponds FA, Fockens P, Neuhaus H, et al. Peroral Endoscopic Myotomy (POEM) Versus Pneumatic Dilatation in Therapy-Naive Patients with Achalasia: Results of a Randomized Controlled Trial. Gastroenterology 2017;152:S139.
- Porter RF, Gyawali CP. Botulinum toxin injection in dysphagia syndromes with preserved esophageal peristalsis and incomplete lower esophageal sphincter relaxation. Neurogastroenterol Motil 2011;23:139-44, e127-138.
- Marjoux S, Brochard C, Roman S, et al. Botulinum toxin injection for hypercontractile or spastic esophageal motility disorders: may high-resolution manometry help to select cases? Dis Esophagus 2015;28:735-41.
- Vanuytsel T, Bisschops R, Farre R, et al. Botulinum toxin reduces Dysphagia in patients with nonachalasia primary esophageal motility disorders. Clin Gastroenterol Hepatol 2013;11:1115-1121 e1112.
- Bashashati M, Andrews C, Ghosh S, et al. Botulinum toxin in the treatment of diffuse esophageal spasm. Dis Esophagus 2010;23:554-60.
- Shaker A, Stoikes N, Drapekin J, et al. Multiple rapid swallow responses during esophageal high-resolution manometry reflect esophageal body peristaltic reserve. Am J Gastroenterol 2013;108:1706-12.
- Weijenborg PW, de Schepper HS, Smout AJ, et al. Effects of antidepressants in patients with functional esophageal disorders or gastroesophageal reflux disease: a systematic review. Clin Gastroenterol Hepatol 2015;13:251-259 e251.