Colite ischémique
Objectifs pédagogiques
- Connaître les circonstances de survenue
- Savoir différencier les formes emboliques des formes thrombotiques
- Savoir reconnaître les formes sévères
- Prise en charge thérapeutique
La colite ischémique est la pathologie vasculaire du tube digestif la plus fréquente [1]. Son incidence est en augmentation et elle est responsable d’une morbimortalité non négligeable, en particulier chez les sujets âgés. Sa présentation clinique a évolué ses dernières années. En effet, si le tableau typique associant douleurs abdominales, diarrhée et rectorragies reste fréquent, le diagnostic est désormais très souvent évoqué devant des symptômes moins typiques mais associés à une sémiologie tomodensitométrique évocatrice. Cette pathologie représente pour les cliniciens un challenge diagnostique dans ses formes transitoires et un challenge thérapeutique dans sa forme gangréneuse.
Physiopathologie de la colite ischémique
Rappel anatomique
Le cadre rectocolique a une vascularisation assurée par l’artère mésentérique supérieure (AMS) pour le côlon ascendant et les deux tiers droits du côlon transverse et par l’artère mésentérique inférieure (AMI) pour le tiers gauche du côlon transverse, le côlon descendant et le haut rectum. Les deux tiers inférieurs du rectum sont vascularisés par l’artère rectale moyenne, branche de l’artère iliaque interne et l’anus et la marge anale sont vascularisés par l’artère rectale inférieure, branche de l’artère honteuse interne. L’AMS donne deux branches : l’artère iléo-colique et l’artère colique supérieure droite et l’AMI fournit l’artère colique gauche supérieure et le tronc des artères sigmoïdiennes. Ces artères sont reliées par des arcades bordantes. Ces arcades font du côlon un organe peu sensible à l’ischémie. Toutefois, il existe deux points faibles à cette vascularisation. L’arcade de Riolan est parfois grêle, voire absente au niveau de l’angle gauche : il s’agit du point de Griffiths. L’arcade bordante est inconstante entre le sigmoïde et le haut rectum et ce point faible est appelé point de Südek. En cas de défaillance vasculaire, l’atteinte colique est étroitement corrélée à la fonctionnalité des réseaux de suppléance. En cas de défaillance de l’AMI, le côlon descendant est épargné si l’arcade de Riolan est fonctionnelle alors que le sigmoïde est plus sensible car la suppléance vasculaire issue des artères iliaques internes est inconstante [2].
Physiologie de la circulation splanchnique
Le territoire splanchnique reçoit environ un quart du débit cardiaque (35 % en période postprandiale) avec 30 % de sang artériel et 70 % de sang veineux. La muqueuse digestive reçoit la majorité du flux sanguin (70 % contre 30 % pour la musculeuse et la séreuse). Le débit sanguin au niveau du tronc cœliaque (700 ml/min) est égal au débit de l’AMS et au double de celui de l’AMI et dépend principalement du débit cardiaque et du calibre artériel. Au niveau des artérioles et des sphincters précapillaires, la régulation du flux sanguin splanchnique met en jeu des facteurs hormonaux (catécholamines, sérotonine, angiotensine, vasopressine) et nerveux (système nerveux sympathique et parasympathique). En cas de chute du débit cardiaque, ce système de régulation provoque une redistribution du sang au profit des organes « nobles » (cœur et cerveau). De même, pendant l’activité physique, le débit sanguin colique diminue au profit des muscles, ce qui peut favoriser la survenue d’une ischémie colique.
Mécanismes de formation des lésions coliques
Les deux principaux mécanismes lésionnels impliqués dans les colites ischémiques sont l’hypoxie et l’ischémie-reperfusion.
L’hypoxie tissulaire du côlon occlusive ou non occlusive
Les colites ischémiques sont souvent multifactorielles, sans atteinte aiguë des gros vaisseaux, la colite ischémique est dite non occlusive. Plus rarement, la colite ischémique est la conséquence d’une embolie ou d’une thrombose, elle est alors dite occlusive. L’augmentation de la tension pariétale peut aussi contribuer à l’ischémie colique quand elle dépasse la pression capillaire. Le côlon peut s’adapter en augmentant l’extraction en oxygène jusqu’à un seuil critique au-dessus duquel ses capacités sont dépassées. À l’état basal, 20 % seulement des capillaires sont ouverts et l’ouverture des sphincters précapillaires permet d’améliorer la tolérance à l’ischémie. Une occlusion d’un vaisseau mésentérique va entraîner l’ouverture de ces réseaux de suppléance. Cette adaptation permet au côlon de tolérer une baisse de 75 % du débit de l’AMS pendant 12 heures. Au-delà les lésions s’installent. La muqueuse et la sous-muqueuse sont les premières touchées, ce qui entraîne une augmentation de la perméabilité et des phénomènes de translocation bactérienne et d’endotoxinémie qui peuvent induire une aéromésentérie ou une aéroportie. Les cellules de la musculeuse sont, elles, plus résistantes à l’anoxie. Mais en cas d’ischémie sévère, elles peuvent perdre leurs propriétés contractiles.
L’ischémie-reperfusion
Le rétablissement de la perfusion peut induire une aggravation des lésions tissulaires liées à l’ischémie. En effet, des espèces réactives de l’oxygène sont produites dès les premières minutes de reperfusion, elles altèrent les membranes cellulaires par peroxydation lipidique, induisent des lésions de l’ADN, favorisent l’activation de NF-κB et entraînent l’expression des cytokines pro-inflammatoires à l’origine des défaillances multiviscérales qui font toute la gravité clinique de l’ischémie colique dans sa forme gangréneuse [3].
Conséquences de l’hypo-vascularisation colique : les différents types anatomo-cliniques d’atteintes coliques
L’examen anatomopathologique des biopsies coliques ou des pièces de colectomie permet de distinguer schématiquement les colites ischémiques aiguës gangréneuses ou non gangréneuses et les colites ischémiques chroniques cicatricielles.
Colites ischémiques aiguës
Colite ischémique aiguë non gangréneuse
Ces formes de CI sont le plus souvent segmentaires et transitoires. Les lésions les plus fréquemment retrouvées sont les érosions épithéliales, l’œdème du chorion, les altérations de la microcirculation (hémorragies de la lamina propria et thromboses fibrineuses) et l’atrophie glandulaire. Parmi ces lésions, la plus spécifique semble être l’atrophie glandulaire en aire, caractérisée par une diminution de hauteur et de diamètre des cryptes glandulaires de Lieberkühn avec un épithélium atrophique ayant perdu toute mucosécrétion [4].
Colite ischémique aiguë gangréneuse
Le méso est macroscopiquement normal en l’absence de péritonite ou de perforation. L’aspect de la face séreuse du côlon varie en fonction du mécanisme impliqué : il est rougeâtre, voire noirâtre en cas de colite ischémique gangréneuse obstructive, mais reste souvent proche de la normale (en dehors d’une ectasie colique fréquente) en cas de colite ischémique gangréneuse non obstructive, sous-estimant ainsi l’étendue des lésions. Sur le versant muqueux (visualisé en endoscopie ou lors de l’exploration chirurgicale), la zone ischémiée est noirâtre et bien limitée en amont et en aval en cas de colite ischémique obstructive. Inversement, les limites lésionnelles sont souvent floues et les zones de nécrose alternent avec des zones saines en cas de colite ischémique non obstructives. Histologiquement, la muqueuse est en nécrose de coagulation. Cette nécrose dépasse la muscularis mucosæ, atteint la sous-muqueuse et la musculeuse dans les zones gangréneuses. Dans les colites ischémiques gangréneuses obstructives, les lésions vasculaires intra-murales sont souvent retrouvées avec présence de thrombi fibrino-cruoriques dans les capillaires et les veinules. L’évolution spontanée de cette nécrose se fait vers la chute d’escarre et l’apparition d’ulcérations creusantes susceptibles de se surinfecter.
Colite ischémique chronique
L’ischémie provoque des ulcérations aiguës de la muqueuse dont l’évolution spontanée se fait vers la constitution de bandes fibreuses disséquant la musculeuse. À ces lésions s’associent souvent des lésions vasculaires (endartérite, thromboses veineuses et artérielles), un infiltrat inflammatoire sous-muqueux et la présence de macrophages chargés d’hémosidérine. Les sténoses constituent une complication classique de l’ischémie colique chronique. Il s’agit dans ce cas de sténoses fibreuses courtes (10 à 15 cm), régulières, bien que parfois ulcérées, et concentriques.
Épidémiologie
La colite ischémique est caractérisée par une grande hétérogénéité clinique allant de la forme transitoire pauci-symptomatique à la forme gangréneuse pouvant engager le pronostic vital. Si les formes gangréneuses constituent une urgence chirurgicale, les formes frustes à la symptomatologie peu spécifique ne donnent pas systématiquement lieu à une hospitalisation et entraîne donc surement une sous-estimation de la fréquence de cette pathologie. L’épidémiologie de la colite ischémique repose en grande partie sur l’étude des cas hospitalisés est de ce fait faussée par un biais de recrutement. La majorité des auteurs s’accorde néanmoins à dire que la colite ischémique constitue l’atteinte vasculaire digestive la plus fréquente (50 à 60 % des ischémies digestives) et la deuxième cause d’hémorragie digestive basse (10 à 20 % des cas selon les études) après les saignements d’origine diverticulaire [5]. La CI atteint les deux sexes mais touche plus souvent les femmes avec un sex ratio estimé entre 1/2 et 2/3 et plus fréquemment les personnes âgées de plus de 60 ans (moyenne d’âge des patients comprise entre 60 et 75 ans) [5, 6] et au cours syndrome de l’intestin irritable ou un risque relatif de 7,5 a été rapporté [6]. Concernant sa fréquence de survenue, les quelques études épidémiologiques descriptives réalisées rapportent une incidence comprise entre 5 et 45 cas pour 100 000 années-personnes [5, 6]. Un travail récent de la Mayo Clinic rapporte une augmentation de cette incidence en population générale, qui serait passée de 6,1 cas pour 100 000 années-personnes dans les années 1976-1980 à 22,9 pour la période 2005-2009 [7]. Il existe un lien épidémiologique fort entre les colites ischémiques et les autres pathologies cardiovasculaires avec un odd ratio à 2,6 pour les pathologies coronariennes et 7,9 pour les artériopathies périphériques [7].
Les colites ischémiques sont associées à mortalité hospitalière non négligeable de 11,5 % dans l’étude en population générale de la Mayo Clinic et cette mortalité était associée de manière indépendante à l’âge supérieur à 40 ans, au sexe masculin, à l’ischémie concomitante du grêle, aux formes coliques droites et aux broncho-pneumopathies chroniques obstructives [7]. Un doublement de la mortalité et un risque de chirurgie multiplié par 5 ont également été rattachés à la localisation droite des lésions coliques [8, 9].
Formes cliniques
L’enjeu pour le clinicien est double, il s’agit d’une part de diagnostiquer les colites ischémiques transitoires qui nécessitent souvent une démarche diagnostique complexe et d’autre part de reconnaître la sévérité des formes gangréneuses dont la prise en charge thérapeutique conditionne le pronostic.
Colite ischémique non gangréneuse
Les colites ischémiques transitoires représentent 80 à 85 % des CI [5, 7]. Elles surviennent le plus souvent brutalement, sans prodromes, chez un patient ambulatoire. Les symptômes ne sont pas pathognomoniques et varient en fonction de la sévérité des lésions. Classiquement, le diagnostic clinique repose sur la triade « Douleur – Diarrhée – Rectorragies ». Ces symptômes sont effectivement retrouvés dans environ 90, 60, et 90 % des cas respectivement, mais la triade complète n’est présente que chez 40 % des patients [6, 7]. Ces symptômes peuvent être associés à une fébricule, des nausées, voire un syndrome subocclusif. Les rectorragies sont le plus souvent modérées, sans déglobulisation associée et ne nécessitent pas de transfusion. L’examen clinique est pauvre et retrouve en général un météorisme abdominal, parfois associé à une défense localisée.
Colite ischémique gangréneuse
La colite ischémique gangréneuse représente 15 à 20 % de l’ensemble des CI. Elle survient soit dans le côlon droit par atteinte de l’AMS ou dans les autres situations, le plus souvent chez un patient de plus de 60 ans présentant des facteurs de risque cardio-vasculaires, en postopératoire de chirurgie de l’aorte abdominale. Les études les plus récentes estiment entre 1 et 3 % l’incidence des CI dans les suites de la chirurgie des anévrismes de l’aorte abdominale. La survenue d’une CI en postopératoire semble associée aux ruptures d’anévrisme, à l’existence d’une insuffisance rénale préopératoire et à la durée de la chirurgie. Une colite ischémique est possible quel que soit le type de chirurgie (laparotomie ou pose de prothèse endovasculaire) [10].
Le tableau clinique correspondant à ces formes gangréneuses est le plus souvent franc, associant des douleurs abdominales intenses, une instabilité hémodynamique et une diarrhée sanglante. La palpation retrouve une douleur abdominale diffuse, une défense localisée ou généralisée et l’auscultation une disparition des bruits hydro-aériques. L’existence d’un syndrome péritonéal, d’une tachycardie ou d’une hyponatrémie, doit faire craindre ce diagnostic.
Dans les suites opératoires, la colite ischémique gangréneuse peut s’installer d’emblée ou de façon retardée. Dans une étude portant sur 88 patients opérés de l’aorte, une coloscopie a été réalisée systématiquement dans les 24 heures suivant la chirurgie pour chaque patient. Une colite ischémique non grave (i.e. œdémateuse ou ulcérée) a été mise en évidence chez 18 patients et une colite ischémique nécrotique a été retrouvée chez 10 patients. Deux des 18 patients présentant initialement des lésions ischémiques légères à modérées ont secondairement développé une nécrose colique sévère [11].
Colite ischémique chronique
L’évolution des colites ischémiques aiguës en colites ischémiques chroniques sténosantes semble rare en pratique courante, bien que les séries anciennes aient rapporté la survenue de telles complications dans 10 à 20 % des cas [12]. Les sténoses coliques peuvent être asymptomatiques ou générer des manifestations cliniques à distance d’une CI transitoire, parfois passée inaperçue [4]. Le tableau clinique est constitué de troubles du transit avec émission de selles afécales, liquides, voire purulentes parfois associés à des rectorragies persistantes. Il existe souvent des douleurs abdominales à type de coliques, associées à un ballonnement, parfois un syndrome subocclusif. L’évolution peut se faire vers l’aggravation des symptômes, nécessitant une prise en charge chirurgicale. Parfois, les lésions se stabilisent ; elles régressent plus rarement [12].
Diagnostic positif
Le diagnostic positif de colite ischémique repose actuellement exclusivement sur des explorations morphologiques. En effet, aucun marqueur biologique n’est spécifique de l’ischémie colique. Les patients présentent généralement (60 à 80 % des cas) une hyperleucocytose modérée associée à une augmentation aspécifique de la lactate déshydrogénase et de la créatinine phospho-kinase. Le taux plasmatique de lactates est un marqueur parfois utilisé. Cependant, l’élévation du taux de lactates n’est pas spécifique du côlon et le métabolisme hépatique des lactates provenant du tube digestif permet souvent de maintenir initialement un taux de lactates normal en cas d’ischémie colique modérée. L’élévation du taux de lactates n’est donc ni un marqueur sensible ni un marqueur spécifique de l’ischémie colique. Dans les formes gangréneuses peuvent survenir des perturbations de l’équilibre acido-basique (acidose métabolique) et une insuffisance rénale aiguë.
La coloscopie
Elle est devenue l’examen de référence pour le diagnostic positif de colite ischémique et pour le diagnostic différentiel, car elle permet d’une part la visualisation de lésions muqueuses modérées, et d’autre part la réalisation de biopsies. Elle doit être réalisée avec prudence en limitant l’insufflation car une pression intraluminale supérieure à 30 mmHg pourrait théoriquement diminuer le flux sanguin colique et participer à l’aggravation des lésions. Classiquement, il est admis qu’il n’existe pas de signe endoscopique pathognomonique de colite ischémique. Le diagnostic repose le plus souvent sur l’association d’un contexte clinique évocateur, de lésions muqueuses et d’une histologie compatible [14]. La coloscopie doit être réalisée précocement en raison du caractère rapidement réversible de certaines lésions. Les lésions endoscopiques segmentaires à limites nettes et rapidement évolutives sont évocatrices d’une origine ischémique. La fréquence des localisations décroît du rectum vers le cæcum : 75 % intéressent le côlon gauche et le rectosigmoïde, 15 % environ le côlon transverse et 10 % le côlon droit. Trois stades endoscopiques initiaux ont été décrits (Fig. 1) : a) stade 1 : œdème et érythème de la muqueuse ; b) stade 2 : ulcérations non nécrotiques, reposant sur une muqueuse œdématiée ; c) stade 3 : nécrose extensive avec aspect gris-noir du côlon. La constatation de lésions de stade 3 doit faire stopper l’examen. Si la nécrose est de petite taille et qu’il n’existe pas d’indication chirurgicale, l’endoscopie doit être répétée 2 à 3 jours après pour juger de l’évolutivité des lésions. Les lésions évoluent en 3 stades évolutifs : a) la phase aiguë dure environ 24 heures avec une muqueuse alternant entre des plages blanchâtres avec perte du lacis vasculaire et des plages érythémateuses et œdématiées, b) la phase subaiguë dure environ 48 heures pendant lesquelles les plages érythémateuses fusionnent tandis qu’apparaissent de petites érosions et des plaques purpuriques, et c) la phase chronique au cours de laquelle les ulcérations deviennent extensives et confluentes, parfois nécrotiques. À ces lésions classiques, il faut ajouter l’aspect en bande inflammatoire linéaire (ou Colonic Single Stripe Sign) [14]. Cette bande inflammatoire siège sur le bord mésentérique du côlon et mesure le plus souvent au moins 5 cm de long avec une largeur comprise entre 5 mm et une hémi-circonférence et correspond à une forme mineure de CI associée à une durée d’hospitalisation, un taux de colectomie et un taux de mortalité inférieurs aux formes plus étendues [14].
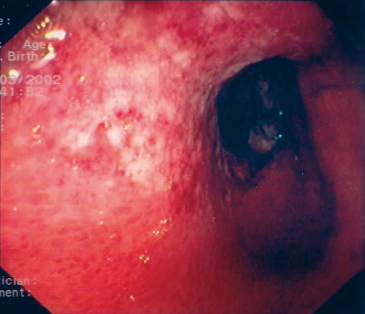

Figure 1 : Trois stades endoscopiques de colite ischémique. A. Stade 1 : œdème et érythème de la muqueuse ;B. Stade 2 : ulcérations non nécrotiques, reposant sur une muqueuse œdématiée ;C. Stade 3 : nécrose extensive avec aspect gris-noir du côlon
Lorsque la colite ischémique évolue vers la chronicité, la muqueuse s’amincit, s’atrophie et disparaît par endroits au profit d’un tissu fibreux. Cette évolution fibrosante peut parfois se compliquer d’une sténose. Dans ce cas, la coloscopie met en évidence une sténose régulière concentrique endoscopiquement non suspecte, sur une muqueuse pâle et peu vascularisée, parfois ulcérée [12].
L’examen tomodensitométrique avec injection de produit de contraste
Le scanner injecté est une modalité diagnostique très utilisée en pratique clinique quotidienne. Il est devenu fréquent que l’endoscopie ne soit utilisée que pour confirmer une image scanographique suspecte d’ischémie colique. Le scanner injecté présente une sémiologie qui repose sur la mise en évidence d’images coliques en cible ou en cocarde avec un double halo [16-18] (Fig. 2). Cet aspect d’épaississement pariétal souvent inférieur à 1 cm est expliqué par l’hyperdensité de la muqueuse et de la musculeuse qui contraste avec l’œdème sous-muqueux [16]. On note fréquemment un signal inflammatoire dans la graisse péricolique. La cinétique de prise de contraste de la paroi colique renseigne également sur sa viabilité et la sévérité de l’atteinte peut être appréciée par la présence d’une pneumatose pariétale, d’une aéroportie ou encore d’un épanchement péritonéal liquidien ou d’un pneumopéritoine qui signe la perforation. Le scanner apprécie également la longueur et la localisation de l’atteinte repérable par les signes pariétaux et la perte des haustrations. Si la sensibilité du scanner est excellente, sa spécificité est médiocre hors d’un contexte évocateur [16, 17]. De plus, il ne permet pas toujours l’identification des causes occlusives, notamment lorsque l’occlusion intervient en distalité sur les vaisseaux mésentériques [17].

Figure 2. Aspect scanographique (coupe réalisée après injection de produit de contraste) objectivant une colite ischémique gauche avec signe du halo(flèche)
Diagnostic différentiel
Colite ischémique transitoire
L’aspect endoscopique des CI transitoires peut également faire évoquer une colite inflammatoire (maladie de Crohn ou rectocolite hémorragique), une colite infectieuse, une colite médicamenteuse ou radique. Le diagnostic différentiel repose sur l’interrogatoire, l’examen clinique et la coloscopie avec biopsies étagées pour examen anatomopathologique et bactériologique.
L’interrogatoire permet d’orienter vers une origine ischémique en cas de facteurs de risque cardio-vasculaires ou d’antécédents thrombo-emboliques et en l’absence d’antécédent personnel ou familial de maladie inflammatoire chronique intestinale (MICI), de voyage à l’étranger, d’antécédent de radiothérapie locorégionale ou de prise médicamenteuse récente (antibiothérapie, AINS, chimiothérapie…). L’examen clinique doit rechercher un syndrome infectieux, des manifestations extra-digestives (rhumatologiques, dermatologiques ou oculaires) évocatrices de MICI et des signes cliniques orientant vers une origine ischémique (arythmie en particulier).
| Pathologie | |
|---|---|
| Colite ischémique | Desquamation et nécrose muqueusesAtrophie épithéliale en aireHémorragies au niveau de la lamina propriaMacrophages chargés d’hémosidérineThrombi fibrineux |
| Colite infectieuse | Infiltrat neutrophiliqueAbcès cryptiquesAbsence de plasmocytose basaleArchitecture des cryptes préservéeÉrosions muqueuses, œdème muqueux |
| Maladie de Crohn | Infiltrat inflammatoire en aireInfiltrat histiocytaireInflammation sous-muqueuseMicroscopic skip areasAbcès cryptiquesGranulomes épithélioïdes |
| Rectocolite hémorragique | Infiltrat inflammatoire muqueux diffusPlasmocytose basaleAbcès cryptiquesDistorsion des cryptesDiminution de la densité cryptiqueForte déplétion en mucusSurface muqueuse villeuse |
| Colite radique | Hyalinisation de la lamina propriaFibrose sous-muqueuseEctasies vasculairesNécrose fibrinoïde des petits vaisseaux |
Tableau I. Apport de l’anatomopathologieau diagnostic différentiel des colites ischémiques
L’examen anatomopathologique des biopsies est un élément clé du diagnostic différentiel. Il permet l’identification de lésions plus ou moins spécifiques des différents types d’atteinte colique (Tableau I) et de préciser le diagnostic lorsqu’il est couplé aux renseignements cliniques.
L’examen anatomopathologique doit nécessairement être complété par une analyse bactériologique des biopsies. En plus des bactéries systématiquement recherchées en cas de diarrhée aiguë (Salmonella, Shigella, Campylobacter Jejuni, Yersinia), il est nécessaire de rechercher Escherichia coli entéro-hémorragique O157H7, Klebsiella oxytoca et Clostridium difficile. Des colites infectieuses à E. coli O157H7 ont été rapportées après consommation de viande de bœuf mal cuite, de lait non pasteurisé ou d’eau souillée. Chez l’adulte, la symptomatologie se développe 3 à 4 jours après la contamination avec apparition de douleurs abdominales suivies d’une diarrhée aqueuse puis sanglante, résolutive en 4 à 10 jours [19]. L’aspect endoscopique comme l’examen anatomopathologique (signes d’ischémie) peuvent être source de confusion diagnostique et justifient la réalisation d’un examen bactériologique systématique [20]. Les colites à K. oxytoca surviennent le plus souvent brutalement entre le deuxième et le huitième jour d’un traitement antibiotique (pénicillines, céphalosporines, macrolides) avec apparition d’une diarrhée hémorragique avec un aspect endoscopique compatible avec une CI (œdème, plages purpuriques, érosions muqueuses). L’évolution est le plus souvent très rapidement favorable dès l’arrêt du traitement antibiotique. Enfin, les colites à C. difficile, favorisées par une antibiothérapie, une chirurgie ou une chimiothérapie récente, peuvent dans certains cas (souches virulentes) provoquer une diarrhée sanglante. La surinfection d’une colite ischémique n’est pas exceptionnelle il convient dans ce cas de rechercher C. Difficile de principe [21].
Enquête étiologique
Cette enquête ne doit être entreprise qu’une fois le diagnostic de certitude acquis.
La classification la plus fréquemment utilisée pour les colites ischémiques distingue les colites ischémiques occlusives (thrombose ou embole vasculaire) et les CI non occlusives, plus fréquentes (Tableau II). Les étiologies de colites ischémiques sont très nombreuses et s’additionnent souvent chez un même patient. Compte tenu de la multiplicité des étiologies rapportées de CI, la recherche systématique de toutes ces conditions prédisposantes n’est pas réalisable en routine (Tableau II).
| Causes occlusives | Causes non occlusives |
|---|---|
| Occlusions des gros vaisseaux | Bas débit |
| Traumatismes abdominaux | Choc hypovolémique, cardiogénique |
| Thromboses et embolies des artères mésentériques :– embolies artérielles (troubles du rythme, rétrécissement mitral, CIV), embolie cholestérolique, ligature de l’AMI, anévrysme et reconstruction aortique, aortographie, dissection aortique, thrombose veineuse mésentérique ;– hypercoagulabilité, cirrhose, pancréatite aiguë, sepsis intra-abdominal | Choc septique, anaphylactiqueInsuffisance cardiaque, déshydratation |
| Occlusions des petits vaisseaux | Médicaments : |
| Vascularites :– périartérite noueuse, Horton, lupus, collagénoses, Takayasu, dermatomyosite, maladie de Behcet, granulomatose, purpura rhumatoïde, amylose, diabète, séquelles de radiothérapie, syndrome hémolytique et urémique | Antihypertenseur, vasopressine, danazol, œstroprogestatifs, flutamine, interféron alpha, AINS, pénicilline, diurétiques, digitaliques, neuroleptiques, préparations coliques, phényléphrine, sumatriptan, alosétron, tégaserod |
| Obstruction colique :– cancer, volvulus, sténose, fécalome, invagination, syndrome d’Ogilvie | Effort physique prolongé |
| Maladies hématologiques : drépanocytose, déficit en protéine C et S, déficit en anti-thrombine III, syndrome myéloprolifératif, mutation JAK 2, CIVD, polyglobulies primitives ou secondaires, hémoglobinurie nocturne paroxystique | Cocaïne |
| Crise d’asthme | |
| Cytopathie mitochondriales |
Tableau II. Principales causes de colites ischémiques
À l’exception de CI gangréneuses survenant dans les suites d’une chirurgie de l’aorte abdominale, le diagnostic étiologique est souvent difficile et il repose d’abord sur un interrogatoire précis à la recherche de facteurs de risques cardiovasculaires, d’antécédents thrombo-emboliques ou ischémiques et de prises médicamenteuses récentes, puis sur un examen clinique complet incluant une auscultation cardiaque à la recherche d’une arythmie. L’absence de signe clinique ou d’antécédent évoquant une origine cardiologique ne permet cependant pas d’exclure une cardiopathie. Par ailleurs, bien que de nombreux médicaments aient été impliqués dans la survenue de colites ischémiques (Tableau II) l’imputabilité de la CI à un médicament est le plus souvent insuffisante pour affirmer un lien causal et la notion de prise médicamenteuse ne dispense pas de la réalisation d’un bilan étiologique exhaustif. Les niveaux de preuve sont en effet très variables à l’exception des anti-inflammatoires non stéroïdiens (AINS) et des œstro-progestatifs. Pour les AINS, une association significative avec un odds ratio à 5,9 (2,5-14,0) entre la consommation d’AINS et la survenue de colite ischémique chez les sujets de plus de 60 ans a été rapportée [22]. L’association entre la survenue de colite ischémique et la prise d’œstro-progestatifs est également supporté par un odds ratio de 6 [12].
Certaines circonstances très particulières permettent d’éviter une enquête étiologique longue et coûteuse. On reconnaît dans cette catégorie les colites ischémiques postcoloscopie et celles faisant suite à un effort physique prolongé ou à une prise de cocaïne.
Les colites ischémiques secondaires à une coloscopie semblent être liées à une insufflation excessive capable par hyperpression de réduire le flux sanguin colique pariétal. Elles semblent survenir chez des sujets jeunes, sans antécédents cardio-vasculaires, souvent chez des femmes, et elles sont d’évolution rapidement favorable [23, 24].
Lors d’un effort physique prolongé, il existe une redistribution vasculaire aux dépens de la vascularisation du cadre colique et au profit de la vascularisation musculaire. Par ailleurs, il existe une sécrétion physiologique de catécholamines à l’origine d’une vasoconstriction splanchnique. Ces deux mécanismes sont susceptibles d’expliquer la survenue de colites ischémiques parfois sévères chez certains jeunes patients à l’issue d’un effort physique prolongé, en l’absence de facteur de risque cardio-vasculaire ou de thrombophilie associée [25]. Dans ce contexte évocateur, l’imputabilité de la CI à l’effort physique prolongé est suffisamment forte pour dispenser d’un bilan étiologique exhaustif.
De même, la cocaïne est une substance vaso-active susceptible d’induire une CI via deux mécanismes : une action vasoconstrictrice d’une part, et l’induction d’un état prothrombotique via la stimulation de l’activation plaquettaire d’autre part. La consommation de cocaïne est une cause rare de CI, mais lorsque la notion de consommation de cocaïne est retrouvée, l’imputabilité de la CI à la cocaïne est suffisamment forte pour dispenser également le clinicien d’un bilan étiologique exhaustif surtout si la dernière prise de cocaïne a moins de 3 jours [26]. L’examen du côlon peut mettre en évidence la coexistence de lésions d’âges différents (lésions aiguës et plus anciennes). Leur évolution est le plus souvent favorable mais, en cas de prise en charge chirurgicale, la mortalité est proche de 50 % [27].
En dehors de ces circonstances, un bilan étiologique doit être effectué et comprendra un bilan cardiologique à la recherche d’une cardiopathie emboligène, un bilan de thrombophilie, voire une exploration des vaisseaux mésentériques en fonction de l’âge du patient et de la situation clinique (Figs 3 et 4).

Figure 3. Exploration d’une colite ischémique certaine chez un patient de moins de 50 ans

Figure 4. Exploration d’une colite ischémique certaine chez un patient de plus de 50 ans
Les explorations cardiologiques
Ni l’absence d’élément anamnestique en faveur d’une cardiopathie ni l’absence de trouble du rythme sur un électrocardiogramme (ECG) ne permettent d’exclure l’existence d’une cardiopathie emboligène. En effet, il a été montré en 2003, sur une série de 60 patients ayant présenté une colite ischémique transitoire, que la réalisation d’un ECG ne permettait d’identifier que 28 % des cardiopathies emboligènes. Le bilan cardiologique doit donc comprendre un ECG, une échocardiographie trans-thoracique (ETT) et un Holter-ECG. La réalisation de ce bilan permet de mettre en évidence une cardiopathie emboligène chez environ 1/3 des patients et permettra l’instauration d’un traitement anticoagulant ou antiarythmique pour respectivement 32 % et 25 % des patients dans les suites d’une CI transitoire [28, 29].
Le bilan de thrombophilie
La survenue d’une colite ischémique, chez un sujet jeune sans facteur de risque cardio-vasculaire ni antécédent thrombo-embolique personnel, peut être révélatrice d’une affection hématologique prothrombotique, y compris lorsqu’un facteur médicamenteux est suspecté [30-32]. L’identification d’une thrombophilie chez un patient présente un intérêt thérapeutique majeur car elle peut permettre l’instauration d’un traitement préventif par anticoagulants avec un impact positif sur la morbi-mortalité. Les thrombophilies sont le plus souvent des déficits en anticoagulants naturels (protéine S, protéine C, antithrombine) ou des mutations constitutionnelles touchant les gènes codant les facteurs de coagulation tels que le facteur V ou le facteur II. Pour la pratique, il est important de noter que la recherche d’un déficit en protéine S ou en protéine C est affectée par les traitements par antagonistes de la vitamine K et que la recherche d’un déficit en antithrombine est perturbée en cas d’héparinothérapie. Par ailleurs, la recherche de la mutation du gène codant le facteur V Leiden et de la mutation 20210G>A du gène codant le facteur II nécessitent un consentement écrit signé des patients.
Exploration des vaisseaux mésentériques
L’exploration des vaisseaux mésentériques par angiographie digestive ou écho-Doppler abdominal n’est actuellement pas préconisée en première intention dans le bilan étiologique des colites ischémiques. Il semble légitime de réserver ces explorations aux patients présentant une récidive. Dans ce cas, un écho-Doppler abdominal sera réalisé en priorité du fait de son caractère non invasif. L’angiographie conserve, elle, un intérêt en cas d’ischémie mésentérique aiguë avec une atteinte colique droite pour rechercher une ischémie mésentérique supérieure associée qui relèverait de mesures thérapeutiques spécifiques.
Prise en charge thérapeutique
Le traitement des CI varie en fonction de la gravité du tableau clinique et de l’étiologie de la maladie.
Colites ischémiques transitoires
Une fois le diagnostic posé, les colites ischémiques non graves ne justifient pas nécessairement une hospitalisation. Leur traitement est essentiellement symptomatique et repose sur la prescription d’antalgique associée si besoin à la mise au repos du tube digestif et à la correction des troubles hydro-électrolytiques. La prescription d’antibiotiques n’est pas recommandée dans les formes non compliquées [32]. En dehors des CI iatrogènes pour lesquelles il convient d’interrompre le médicament impliqué, il n’existe pas de traitement spécifique pour les CI à la phase aiguë. À distance, l’équilibration du traitement anti-arythmique ou l’instauration d’un traitement anticoagulant pourront prévenir la récidive en cas de CI secondaire à une cardiopathie emboligène ou à une thrombophilie.
Colites ischémiques gangréneuses
En présence de signes cliniques de gravité tels qu’un syndrome péritonéal, un état de choc ou une hémorragie digestive massive, la prise en charge chirurgicale s’impose en urgence. En dehors de ces indications, l’indication chirurgicale repose sur des critères endoscopiques et notamment l’existence de lésions endoscopiques de stade 3 ou de stade 2 associés à une défaillance d’organe ou encore face à des signes de gravité scanographiques pour certains [33, 34]. En présence de signes cliniques et endoscopiques de gravité intermédiaire, la prise en charge nécessite une surveillance rapprochée et toute aggravation clinique ou biologique nécessitera une intervention [34]. La nécrose n’atteignant pas systématiquement la séreuse, notamment en cas de colite ischémique gangréneuse non obstructive, le temps exploratoire de l’intervention peut nécessiter la réalisation d’une coloscopie peropératoire. Une résection exhaustive de toutes les zones ischémiées doit ensuite être réalisée et la confection d’une stomie temporaire est systématique. Même avec ce type d’approche, la mortalité des formes sévères (stade 3 ou présence d’une défaillance multiviscérale) reste importante et dépasse les 50 % alors qu’elle est nulle dans les types 1 ou 2 [34].
Colites ischémiques chroniques
Pour les CI chroniques symptomatiques, le traitement de référence repose sur la chirurgie de la zone sténosée (colectomie segmentaire). Bien que non démontré, l’intérêt de l’administration locale ou systémique de corticoïdes et des dilatations pneumatiques au ballonnet a été suggéré [12]. De même, une étude récente suggère l’intérêt des prothèses coliques couvertes dans la prise en charge des sténoses coliques ischémiques symptomatiques à la phase aiguë de l’occlusion comme un « bridge to surgery » pour permettre une chirurgie à froid dans de meilleures conditions une fois l’obstacle levé [35].
Références
- Brandt LJ, Boley SJ. AGA technical review on intestinal ischemia: American Gastrointestinal Association. Gastroenterology 2000; 118:954-68.
- Frileux P, Attal E, Boutami B, L’helgouarc’h JL, Burdy G. Ischémies coliques spontanées. Ann Chir 1999;53:1044-53.
- Schoenberg MH, Beger HG. Reperfusion injury after intestinal ischemia. Crit Care Med 1993;21:1376-86.
- Hémet J, Métayer J, Lemoine F, Laquerrière A, Elmaleh AM. Les colites ischémiques transitoires. Valeur diagnostique de l’atrophie épithéliale en aires. Ann Pathol 1989;9:33-7.
- Higgins PD, Davis KJ, Laine L. Systematic review: the epidemiology of ischaemic colitis. Aliment Pharmacol Ther 2004; 19: 729-38.
- Hervé S, Beaugerie L, Bouhnik Y, Savoye G, Colombel JF, Dyard F, et al. Irritable bowel syndrome is more frequent in patients hospitalized for ischaemic colitis: results of a case-control study. Neurogastroenterol Motil 2009;21:1170-e102.
- Yadav S, Dave M, Varayil JE, Harmsen WS, Tremaine WJ, Zinsmeister AR, et al. A population based study of incidence, risk factors, clinical spectrum and outcomes of ischemic colitis. Clin Gastroenterol Hepatol 2014; in press.
- Sotiriadis J, Brandt LJ, Behin DS, Southern WN. Ischemic colitis has a worse prognosis when isolated to the right side of the colon. Am J Gastroenterol 2007;102:2247-52.
- O’Neill S, Yalamarthi S. Systematic review of the management of ischemic colitis. Colorectal Disease 2012;14:e751-63.
- Becquemin JP, Majewski M, Fermani N, Marzelle J, Desgrandes P, Allaire E, et al. Colon ischemia following abdominal aortic aneurysm repair in the era of endovascular abdominal aortic repair. J Vasc Surg. 2008; 47:58-63.
- Champagne BJ, Darling RC 3rd, Daneshmand M, Kreienberg PB, Lee EC, Mehta M, et al. Outcome of agressive surveillance colonoscopy in ruptured abdominal aortic aneurysm. J Vasc Surg 2004;39:792-6.
- Savoye G, Ben Soussan E, Hochain P, Lerebours E. Comment et jusqu’où explorer une colite ischémique. Gastroenterol Clin Biol 2002;26:B12-B23.
- Scowcroft CW, Sanowski RA, Kozarek RA. Colonoscopy in ischemic colitis. Gastrointest Endosc 1981;27:156-61.
- Zuckerman GR, Prakash C, Merriman RB, Sawhney MS, DeSchryver-Kecskemeti K, Clouse RE The colon single-stripe sign and its relationship to ischemic colitis. Am J Gastroenterol 2003;98:2018-22.
- Moszkowicz D, Mariani A, Tresallet C, Menegaux F. Ischemic colitis: the ABCs of diagnosis and surgical management. J Visc Surg 2013;150:19-28.
- Romano S, Romano L, Grassi R. Multidetector row computed tomography findings from ischemia to infarction of the large bowel. Eur J Radiol 2007;61:433-41.
- Iacobellis F, Berritto D, Fleischmann D, Gagliardi G, Brillantino A, et al. CT finding in acute, subacute, and chronic ischemic colitis: suggestions for diagnosis. Biomed Research International 2014:1-7.
- Balthazar EJ, Yen BC, Gordon RB. Ischemic colitis: CT evaluation of 54 cases. Radiology 1999;211:381-8.
- Griffin PM, Olmstead LC, Petras RE. Escherichia coli O157:H7-associated colitis. A clinical and histological study of 11 cases. Gastroenterology 1990;99:142-9.
- Su C, Brandt LJ. Escherichia coli O157: H7 infection in humans. Ann Intern Med 1995; 123:698-714.
- Leffler DA, Lamont JT. Treatment of Clostridium difficile-associated disease. Gastroenterology 2009;136:1899-912.
- Hochain P, Berkelmans I, Czernichow P, Duhamel C, Tranvouez JL, Lerebours E, et al. Which patients taking non-aspirin non-steroidal anti-inflammatory drugs bleed? A case-control study. Eur J Gastroenterol Hepatol 1995;7:419-26.
- Arhan M, Onal IK, Odemis B, Ibiş M, Saşmaz N. Ischemic colitis in a young patient with no risk factor . Am J Gastroenterol 2009;104: 250-1.
- Yüksel O, Bolat AD, Köklü S, Altiparmak E, Albayrak M, Caner S Ischemic colitis, an unusual complication of colonoscopy. South Med J 2008;101:972-3.
- Lucas W, Schroy PC. Reversible ischemic colitis in a high endurance athlete. Am J Gastroenterol 1998;93:2231-4.
- Simmerts TA, Vidakovic-Vukic M, Van Meyel JJ. Cocaine-induced ischemic colitis. Endoscopy 1998;30 (suppl):S8-S9.
- Ellis CN, McAlexander WW. Enterocolitis associated with cocaine use. Dis Colon Rectum 2005;48:2313-6.
- Collet T, Even C, Bouin M, Lecluse E, Piquet MA, Crampon D, Grollier G, Dao T, Verwaerde JC. Prevalence of electrocardiographic and echocardiographic abnormalities in ambulatory ischemic colitis. Dig Dis Sci 2000;45: 23-5.
- Hourmand-Ollivier I, Bouin M, Saloux E, Morello R, Rousselot P, Piquet MA, DaoT, Verwaerde JC. Cardiac sources of embolism should be routinely screened in ischemic colitis. Am J Gastroenterol 2003;98:1573-7.
- Koutroubakis IE, Sfiridaki A, Theodoropoulou A, Kouroumalis EA. Role of acquired and hereditary thrombotic risk factor in colon ischemia of ambulatory patients. Gastroenteorlogy 2001;121:561-5.
- Midian-Singh R, Polen A, Durishin C, Crock RD, Whittier FC, et al. Ischemic colitis revisited: a prospective study identifying hypercoagulability as a risk factor. South Med J 2004;97:120-3.
- Theodoropoulou A, Koutroubakis IE. Ischemic colitis: clinical practice in diagnosis and treatment. World J Gastroenterol 2008; 14:7302-8.
- Corcos O, Nuzzo A. Gastro-intestinal vascular emergencies. Best Practice Resarch Clin Gastroenterol 2013;27:709-25.
- Moszkowicz D, Tresallet C, Mariani A, Lefevre JH, Godiris-Petit G, et al. Ischemic colitis: indications, extent, and results of standardized emergency surgery. Dig Liver Dis 2014;46:505-11.
- Zeitoun JD, Van Nhieu JT, Brunetti F, Luciani A, Karoui M, Delchier JC, Charachon A. Self-expanding metallic stent for ischemic colonic obstruction. Am J Gastroenterol 2009 Sep;104:2372-3.
Les Cinq points forts
- La colite ischémique est une pathologie dont l’incidence est en augmentation.
- Le diagnostic de colite ischémique repose sur la coloscopie et l’examen TDM injecté.
- La gravité de la colite est appréciée par la clinique et l’aspect endoscopique.
- Dans les formes non gangréneuses, c’est l’enquête étiologique qui prime.
- Dans les formes gangréneuses, c’est la décision chirurgicale rapide qui importe.
FMC HGE : Organisme certifié Qualiopi pour la catégorie ACTIONS DE FORMATION
