Conflits d’intérêt
RC : pas de conflits
TA : consultant et ou Honoraires : Amgen, Bayer, Baxter, Bristol-Myers Squibb, HallioDx, Eli-Lilly, MSD Oncology, Sanofi, Servier, Roche/Genentech, Xbiotech, Yakult
Mots-clés : oxaliplatine ; 5-fluorouracile ; capecitabine
Introduction
Le cancer colorectal représente un problème de santé publique en France, avec 44 000 nouveaux cas estimés en 2015 (4e localisation la plus fréquente après les cancers du sein, de la prostate et du poumon), près de 18 000 décès par an (2e cause de mortalité par cancer après le cancer du poumon) avec une survie à 5 ans tous stades confondus de l’ordre de 60 % [1]. La mise en place des campagnes de dépistage a permis une amélioration de la mortalité liée à ce cancer, avec un diagnostic de la maladie à des stades plus précoces. La majorité des patients a un cancer de stade II ou III au diagnostic et environ un tiers d’entre eux récidiveront sous une forme métastatique. La chimiothérapie adjuvante a pour objectif d’augmenter les taux de guérison après chirurgie d’exérèse carcinologique et ses indications sont à mettre en balance avec ses effets secondaires potentiels et la situation clinique de chaque patient. L’indication d’une chimiothérapie adjuvante par fluoropyrimidines et oxaliplatine est clairement démontrée pour les tumeurs de stade III (diminution du risque absolu de rechute d’environ 15 à 20 %), et est en revanche soumise à discussion pour les tumeurs de stade II, en raison d’un faible bénéfice (diminution du risque absolu de rechute de 2 à 4 %). Les principaux protocoles de chimiothérapie indiqués en situation adjuvante dans le cancer du côlon sont résumés dans le tableau I. Si les dernières années ont été marquées par l’échec des thérapies ciblées en situation adjuvante, les résultats récemment présentés de l’essai IDEA (International Duration Evaluation of Adjuvant) qui a comparé 3 mois et 6 mois de chimiothérapie adjuvante associant fluoropyrimidines et oxaliplatine, amènent à rediscuter des modalités de traitement pour les patients opérés d’un cancer colique localisé de stade III.
Tableau I. Principaux protocoles de chimiothérapie en adjuvant du cancer du côlon
| Capecitabine |
|---|
| J1 à J14 : capecitabine 1 250 mg/m2, 2 fois par jour toutes les 3 semaines |
| LV5FU2 simplifié |
|---|
| J1 : AF 400 mg/m2 ; 5-FUb 400 mg/m2 ; 5-FUc 2 400 mg/m2 sur 46 h toutes les 2 semaines |
| CAPOX |
|---|
J1 : oxaliplatine 130 mg/m2
J1 à J14 : capecitabine 1 000 mg/m2, 2 fois par jourtoutes les 3 semaines |
| FOLFOX4 |
|---|
J1 : oxaliplatine 85 mg/2 ; AF 400 mg/m2 ; 5-FUb 400 mg/m2 ; 5-FUc 600 mg/m2
J2 : AF 400 mg/m 2 ; 5-FUb 400 mg/m 2 ; 5-FUc 600 mg/m 2toutes les 2 semaines |
| FOLFOX6m |
|---|
J1 : oxaliplatine 85 mg/m2 ;
AF 400 mg/m2 ; 5-FUb 400 mg/m2 ;
5-FUc 2 400 mg/m2 sur 46 htoutes les 2 semaines |
AF : acide folinique ; 5-FUb : bolus de 5-fluorouracile ; 5-FUc : 5-fluorouracile en continu
Anatomopathologie et biologie moléculaire
La Société Française de Pathologie a standardisé le compte-rendu anatomo-pathologique d’un cancer du côlon opéré. Il doit comprendre : type histologique, grade histo-pronostique, extension tumorale, autres facteurs pronostiques et/ou prédictifs, critères permettant de déterminer le pT/pN). L’examen d’un minimum de 12 ganglions est recommandé.
Le test moléculaire tumoral à recommander dans le cadre de la prise en charge des cancers du côlon de stade II-III est la recherche d’un phénotype tumoral moléculaire MSI/dMMR (MicroSatellite Instable/déficience du système MisMatch Repair) par PCR et ou immunohistochimie en raison de sa valeur pronostique (pour les stades II) et de son intérêt pour la recherche d’un syndrome de Lynch (environ 20 % des cancers colorectaux de stade II et 12 % des stades III sont MSI). Il s’agit d’une caractéristique moléculaire dont la fréquence augmente avec l’âge des patients (> 20 % après 75 ans et > 30 % après 85 ans) [2].
La détermination du statut RAS ou RAF n’est pas nécessaire pour les décisions thérapeutiques concernant la prise en charge d’un cancer de stade II ou III. En cas de récidive de la maladie pour laquelle un traitement par anti-EGFR sera discuté, la détermination du statut RAS sera alors nécessaire. Les statuts BRAF et MSI seront aussi utiles en cas de rechute car ils apportent des informations pronostiques et permettent de sélectionner le patient pour des essais thérapeutiques dédiés à ces formes rares.
En situation adjuvante, on peut préciser qu’aucun facteur biologique prédictif de l’efficacité d’une chimiothérapie adjuvante n’a été à ce jour identifié avec un niveau de preuve suffisant.
La détermination du statut MSI en routine doit être recommandée pour discuter de l’indication d’une chimiothérapie adjuvante pour un patient opéré d’un cancer du côlon de stade II, car en cas de statut MSI, il n’y a pas d’indication à un traitement adjuvant. Le statut MSI n’intervient pas dans la décision de chimiothérapie adjuvante des patients avec stade III, sauf chez les sujets âgés de plus de 70 ans où l’association de fluoropyrimidines et d’oxaliplatine – si elle est possible – est à privilégier (recommandation d’expert), les fluoropyrimidines seules semblant peu ou pas efficaces en cas de statut MSI [2].
Patients avec un cancer du côlon de stade III
L’arrivée des traitements adjuvants dans les années 1990
Le premier essai thérapeutique randomisé ayant démontré l’efficacité de la chimiothérapie en adjuvant des cancers colorectaux de stade III a été publié en 1990 [3]. Dans cette étude, était comparée la surveillance seule au levamisole et à l’association 5-fluorouracile/levamisole pendant 1 an. Les patients traités par 5-FU/levamisole présentaient une diminution de 41 % du risque relatif de récidive (P < 0,0001) et une réduction de 33 % du risque relatif de décès (P = 0,006) par rapport aux patients sans traitement adjuvant. Le taux rapporté de survie sans récidive à 3 ans et demi était de 71 % dans le bras 5-FU/levamisole contre 55 % dans le bras contrôle. Le levamisole seul n’était pas supérieur à la surveillance seule. Cette étude a permis de définir l’association 5-FU/levamisole pendant 12 mois comme le premier traitement standard en adjuvant des cancers coliques de stade III.
La modulation du 5-fluorouracile par l’acide folinique
Différents essais thérapeutiques ont évalué la modulation d’activité du 5-FU par l’acide folinique, d’abord au stade métastatique de la maladie, puis en situation adjuvante [4]. L’essai IMPACT (International Multicentre Pooled Analysis of CRC Trials) a montré une amélioration significative à 3 ans du taux de survie sans récidive de 44 % à 62 % et de survie globale de 64 % à 76 % chez les patients avec un cancer colique de stade III traités par l’association du 5-FU à 370-400 mg/m2 à l’acide folinique (AF) 200 mg/m2 tous les jours pendant 5 jours, tous les 28 jours pendant 6 mois, comparés aux patients traités par chirurgie seule [5]. De même, l’étude du NCCTG (North Central Cancer Treatment Group) a montré une amélioration significative de la survie sans récidive et de la survie globale chez les patients avec un cancer colique de stade II à haut risque ou de stade III traités par 6 cycles de 5-FU/LV selon le protocole Mayo Clinic (6 cycles de 5-FU à 425 mg/m2 et AF 20 mg/m2 tous les jours pendant 5 jours toutes les 4 à 5 semaines) en comparaison aux patients traités par chirurgie seule [6].
La modulation du 5-FU par l’acide folinique a été comparée à l’association 5-FU/levamisole. L’étude C-04 du NSABP (National Surgical Adjuvant Breast and Bowel Project) a montré une augmentation non significative de la survie sans récidive avec le 5-FU/LV par rapport au standard 5-FU/levamisole. L’ajout du levamisole au 5-FU/AF, qui était également évalué dans cette essai randomisé à 3 bras, n’apportait pas de bénéfice de survie [7]. L’étude Intergroup 0089 a confirmé ces résultats. Cet essai randomisait les patients avec un cancer colique de stade II à haut risque ou de stade III dans 3 bras expérimentaux (bras standard : 5-FU/levamisole pendant 12 mois) : 5-FU/AF selon Mayo Clinic, 5-FU/AF selon Roswell Park (AF 500 mg/m2 et 5-FU 500 mg/m2 en bolus hebdomadaire, 6 semaines sur 8 pendant 4 cycles) et 5-FU/AF/levamisole. Aucune différence significative n’était retrouvée entre les 4 bras de traitement, montrant ainsi que le 5-FU/AF pendant 6 mois (selon Mayo Clinic ou Roswell Park) pouvait remplacer le schéma standard 5-FU/levamisole pendant 1 an [8]. L’association 5-FU/AF (selon Mayo Clinic ou Roswell Park) devenait ainsi en 1996 le nouveau standard de traitement en adjuvant des cancers coliques de stade III.
L’essai C96-1 du GERCOR a comparé le schéma 5-FU/AF de la Mayo Clinic au schéma dit de de Gramont (LV5FU2) sur 2 jours toutes les 2 semaines (AF 200 mg/m2 et bolus de 5-FU de 400 mg/2 suivi d’une perfusion continue sur 22 heures de 5-FU à 600 mg/2, 2 jours de suite). Associé à une toxicité réduite et à des taux de survie similaires, le protocole LV5FU2 est une alternative moins toxique du 5-FU/AF selon Mayo Clinic ou Roswell Park [9, 10].
5-fluorouracile/acide folinique ou capecitabine ?
La capecitabine est une prodrogue du 5-FU à prise orale. En monothérapie, elle a été comparée en situation adjuvante au protocole 5-FU/AF (schéma de la Mayo Clinic). Dans l’étude de non-infériorité X-ACT réalisée entre 1998 et 2001, la capecitabine (2 500 mg/m2/j, 2 semaines sur 3) a été comparée au 5FU/AF selon Mayo Clinic en adjuvant des cancers coliques de stade III. Malgré une augmentation d’incidence des syndromes mains-pieds (Tous grades : 60 % versus 9 % ; grade 3-4 : 17 % vs < 1 %), la tolérance globale était meilleure avec la capecitabine qu’avec le 5-FU/AF (P < 0,001) [11]. Après un suivi médian de 6.9 années, la capecitabine était associée à une efficacité au minimum équivalente à celle du 5FU/AF en termes de survie sans maladie (HR = 0,88 ; IC95 % 0,77-1,01) et de survie globale (HR = 0,86 ; IC95 % 0,74-1,01). Les taux de survie sans maladie et de survie globale à 5 ans étaient respectivement de 60,8 % versus 56,7 % et de 71,4 % versus 68,4 % pour les patients traités par capecitabine et par 5FU/AF. Après ajustement, la capecitabine était associée à une amélioration significative de la survie sans maladie et de la survie globale [12].
L’intérêt du traitement adjuvant par fluoropyrimidines (± levamisole et ou acide folinique) versus surveillance simple pour les patients avec un cancer colique de stade III a par ailleurs été confirmé par la méta-analyse du groupe ACCENT (Adjuvant Colon Cancer Endpoints Group). À partir des données individuelles de plus de 20 000 patients inclus dans des essais de traitement adjuvant entre 1978 et 1999, les auteurs de cette analyse ont rapporté un bénéfice absolu de 10 % à 8 ans chez les patients ayant reçu un traitement adjuvant pour un cancer colique de stade III [13].
L’avènement de l’oxaliplatine
Sur la base de résultats positifs en situation métastatique, l’oxaliplatine a été évalué en association au 5-FU/AF. L’essai de phase 3 MOSAIC a ainsi comparé le schéma LV5FU2 au FOLFOX4 (oxaliplatine 85mg/m2 à J1 du protocole LV5FU2), pour 12 cycles. Les résultats de cette étude ont montré une réduction relative de 24 % du risque de rechute (HR = 0,76, P = 0,005) pour les patients atteints de cancer du côlon de stade III recevant FOLFOX4. Sur la base de ces résultats, FOLFOX4 a été approuvé comme traitement adjuvant pour les patients avec cancer du côlon de stade III [14]. Les résultats mis à jour en 2009 ont montré une survie sans rechute de 66,4 % à 5 ans pour FOLFOX4 versus 58,9 % pour LV5FU2 (HR = 0,78, P = 0,005) [15]. L’actualisation des résultats avec un suivi de 10 ans, a montré une amélioration de la survie globale de 59 % à 67 % (HR 0,80 ; P = 0,016) pour les patients avec un cancer colique de stade III, recevant le schéma FOLFOX4 [14, 16]. Parallèlement, l’essai C-07 du NSABP comparait l’ajout de l’oxaliplatine (85 mg/m2, toutes les 2 semaines) au schéma hebdomadaire de 5-FU/AF du Roswel Park (FLOX vs 5-FU/AF). Cette étude a également montré une supériorité statistique du bras avec oxaliplatine, avec une survie sans maladie à 5 ans passant de 64,2 % à 69,4 % (HR 0,82 ; P = 0,002) (Tableau II) [17]. L’association de l’oxaliplatine au 5-FU/AF est ainsi devenue et reste à ce jour le standard de traitement en adjuvant des cancers coliques de stade III (Tableau II ; Fig. 1).
Tableau II. Taux de survie dans 3 études de phase III comparant la combinaison du 5-fluorouracile et acide folinique
seule ou en association à l’oxaliplatine en adjuvant pour les patients avec un cancer du côlon de stade III
| Survie sans récidive | Survie globale |
|---|
| Suivi (années)
(years) | HR (IC95 %) | P | SSR | Suivi (années) | HR (IC95 %) | P | SG |
|---|
| MOSAIC [14-16] | 3 | 0,76 (0,62-0,92) | 0,005 | 65,3 % vs 72,2 % | 3 | – | – | – |
| 5 | 0,78 (0,65-0,93) | 0,005 | 58,9 % vs 66,4 % | 10 | 0,80 (0,66-0,96) | 0,015 | 59 % vs 67,1 % |
| NSABP 07 [17] | 5 | 0,78 (0,68-0,90) | 0,0007 | 57,8 % vs 64,4 % | 5 | 0,85 (0,72-1,00) | 0,052 | 73,8 % vs 76,5 % |
| NO1698 [18] | 3 | 0,80 (0,69-0,93) | 0,0045 | 66,5 % vs 70,9 % | 7 | 0,83 (0,70-0,99) | 0,04 | 67 % vs 73 % |
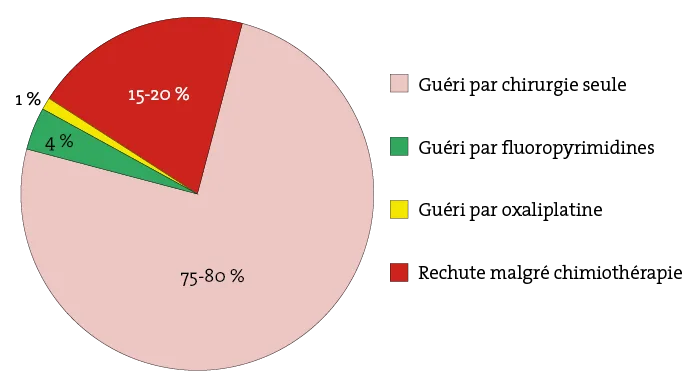
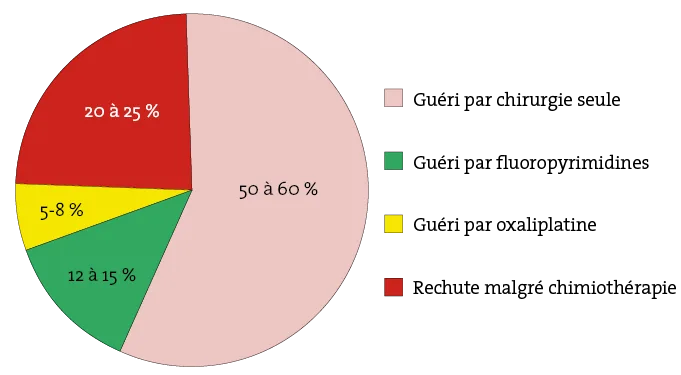
Figure 1. Efficacité de la chimiothérapie adjuvante dans les cancers du côlon stades II et III
A. Cancers coliques de stade II

B. Cancers coliques de stade III

FOLFOX4 ou FOLFOX6 modifié ?
Le protocole FOLFOX6 modifié (mFOLFOX6 : oxaliplatine 85 mg/m2, AF 400 mg/m2 suivi d’un bolus de 400 mg/m2 de 5-FU puis 2 400 mg/m2 de 5-FU en continu sur 46 heures) est plus confortable pour le patient que le FOLFOX4 : le patient ne doit se présenter à l’hôpital qu’au J1 (suppression du bolus à J2) au lieu du J1 et du J2, et l’augmentation de dose du 5-FU continu n’est pas associé à une augmentation de la toxicité (Tableau III). Aucune comparaison directe de ces 2 protocoles n’a été réalisée. Cependant les résultats en termes de survie sont bien que non comparatif, proche entre le mFOLFOX6 (essais NSABP C-08 et Intergroup/NCCTG Trial N0147) le FOLFOX4 (essais MOSAIC, AVANT, PETACC-8) ou le FLOX (essai NSABP C-07). Les sociétés savantes NCCN et ESMO recommandent ainsi l’utilisation du protocole mFOLFOX6 en adjuvant des cancers coliques de stade III.
Tableau III. Essais de combinaison pour le traitement adjuvant des cancers coliques : les échecs
| Hazard ratio (survie sans récidive) | P |
|---|
| 5FU/AF +/– irinotecan |
|---|
| CALGB 89803 [45] PETACC-3 [20] ACCORD2 [46] | – 0,90 1,11 | 0,80 0,11 0,42 |
| Oxaliplatine et fluoropyrimidine +/– bevacizumab |
|---|
| NSABP C08 [21] AVANT (FOLFOX bevacizumab) [22] AVANT (Capeox bevacizumab) [22] QUASAR 2 [25] | 0,93 1,17 1,07 1,06 | 0,34 0,08 0,44 0,54 |
| Oxaliplatine et fluoropyrimidine +/– cetuximab (KRAS sauvage) |
|---|
| US Intergroup 0147 [23] PETACC 8 [24] | 1,21 1,092 | 0,08 0,56 |
5-fluorouracile/acide folinique ou capecitabine en association avec l’oxaliplatine ?
L’association de l’oxaliplatine à la capecitabine a été évaluée dans l’essai N016968 comparant le Capeox (oxaliplatine 130 mg/m2 à J1 et capecitabine 2 000 mg/m2/j, 2 semaines sur 3 pour 8 cycles) au 5FU/AF (selon Mayo Clinic ou Roswell Park). Cette étude confirme le bénéfice apporté par l’oxaliplatine avec une survie globale à 7 ans passant de 67 % à 73 % (HR 0,83 ; P = 0,04) (Tableau I) [18]. L’un des intérêts de ce protocole de traitement est la possibilité de se passer, chez la plupart des patients, d’un abord veineux central, avec des perfusions d’oxaliplatine par voie veineuse périphérique [19].
L’échec des thérapies ciblées et de l’irinotecan
Les études de phase III qui ont évalué l’irinotecan en association au LV5FU2 et les thérapies ciblées (bevacizumab et cetuximab) en association à la chimiothérapie (fluoropyrimidine + oxaliplatine) n’ont pas montré de bénéfice, ni de l’irinotecan, ni du bevacizumab ni du cetuximab avec des HR dans la majorité des études en défaveur de la thérapie ciblée (Tableau III) [20-25]. Un traitement par irinotecan, bevacizumab ou cetuximab n’est pas indiqué dans le traitement adjuvant d’un cancer du côlon de stade III.
L’importance pronostique des mutations RAS et BRAF V600E est maintenant établie pour les stades III, mais ne doit pas intervenir dans le choix thérapeutique qui est une chimiothérapie associant fluoropyrimidines et l’oxaliplatine [26].
Quelle durée de traitement ?
Initialement démontré comme efficace sur une durée de 12 mois, le traitement adjuvant des cancers coliques s’est ensuite imposé sur 6 mois grâce à la démonstration de la non-infériorité du LV5FU2 pour 12 cycles bimensuels comparé à l’association 5-FU/levamisole pendant 1 an, et de la non-infériorité du LV5FU2 pendant 6 mois comparé à 9 mois [3, 8, 9]. En 2005, Chau et al. rapportèrent les résultats d’une étude de phase III ne montrant pas de différence significative entre 3 mois et 6 mois de traitement par 5-fluorouracile [27].
Les résultats de l’essai IDEA ont été présentés lors du congrès annuel 2017 de la société américaine d’oncologie médicale (ASCO) [28]. Cette collaboration internationale a été établie pour analyser ensemble six études de phase III réalisées dans 12 pays : SCOT, TOSCA, Alliance/SWOG 80702, IDEA France (PRODIGE), ACHIEVE et HORG, et posait la question de la durée (3 ou 6 mois) de traitement adjuvant après chirurgie chez les patients atteints CC de stade III. Toutes ces études ont été menées avec le même plan d’analyse statistique (étude de non-infériorité) ayant pour but de comparer la survie sans rechute ou décès (DFS) à 3 ans de patients opérés d’un cancer du côlon de stade III et traités par fluoropyrimidine et oxaliplatine en adjuvant pendant 3 ou 6 mois. Les patients étaient traités par FOLFOX4 ou FOLFOX6m ou capecitabine et oxaliplatine (CapeOX), selon le choix du médecin et du patient. L’hypothèse de non-infériorité de cette analyse était validée si l’intervalle de confiance du Hazard Ratio (HR) obtenu selon le modèle de Cox ne dépassait pas la valeur de 1,12.
Au total l’analyse a inclus 12 834 patients entre juin 2007 et décembre 2015 dans 12 pays. La neurotoxicité Grade ≥ 2 était inférieure dans le bras 3 mois (FOLFOX 16,6 %, CapeOX 14,2 %) comparé au bras 6 mois (FOLFOX 47,7 %, CapeOX 44,9 %). Avec 3 263 évènements (3390 étaient attendus) la non-infériorité de 3 mois de traitement n’a pas pu être établie (HR 1,07, 95 % CI 1,00-1,15). La DFS à 3 ans était de 74,6 % pour le bras 3 mois versus 75,5 % pour le bras 6 mois On notait dans les analyses de sous-groupe une non-infériorité de 3 mois de traitement pour les patients traités par CapeOX (HR 0,95, 95 % CI 0,85-1,06) et pour les patients opérés d’une tumeur de stade III à bas risque de récidive (T1-T3N1 ; HR 1,01, 95 % CI 0,9-1,12). Les patients traités pour une tumeur de stade III de haut risque de récidive (T4 et/ou N2) bénéficiaient statistiquement d’un traitement prolongé de 6 mois (HR 1,12, 95 % CI 1,03-1,23, valeur P de supériorité = 0,011).
L’analyse globale d’IDEA n’a pas démontré une non-infériorité de 3 mois de traitement adjuvant dans CC de stade III ; les résultats dépendent du type de chimiothérapie (FOLFOX ou CapeOX) et du groupe à risque (T1-T3N1 et T4 et/ou N2) (Tableau IV). Le choix du protocole et de la durée de traitement doit dépendre des caractéristiques du patient et du risque de neurotoxicité chronique persistante. Pour les patients traités par CApeOX, la durée de 3 mois est non-inférieure à une durée de 6 mois,dans la population à bas risque (T1-T3N1), et constitue un nouveau standard pour ce groupe. Pour la population à haut risque (T4 ou N2), il est recommandé une durée de traitement de 6 mois par FOLFOX ou CApeOX, avec arrêt de l’oxaliplatine en cas de neuropathie de stade ≥ 2. Plusieurs publications de cette étude sont attendue en 2018.
Tableau IV. Définition des cancers coliques de stade III et de stade II à bas ou haut risque
| Cancer colique de stade II (T3 ou T4 N0) |
|---|
| Bas risque | Cancer MSI ou MSS avec facteurs de bon pronostic : tumeur T3, > 12 ganglions analysés, tumeur moyennement à bien différenciée, pas d’EV ni d’EPN, pas de tumor budding, pas de perforation tumorale |
| (Haut) risque | Cancer MSS avec facteur(s) de mauvais pronostic : Consensuels : tumeur T4 et en particulier T4b, ou perforée, < 12 ganglions analysés Discutés : tumeur peu différenciée (MSS), présence d’EV ou d’EPN, tumor budding, marges positives, N0(i+) |
| Cancer colique de stade III : T1 à T4 N+ |
|---|
| Bas risque* | Tumeur T1 à T3 et N1 |
| Haut risque* | Tumeur T4 et/ou N2 |
EPN : engainements périnerveux ; EV : emboles vasculaires ; MSI : microsatellites instables ;
MSS : microsatellites stables ; N0(i+) : cellules tumorales isolées* : classification selon les résultats de l’étude IDEA présentée au congrès 2017 de l’ASCO |
Patients avec un cancer du côlon de stade II
Les cancers coliques de stade II (T3 ou T4 N0 M0) représentent un groupe hétérogène sur le plan pronostique avec des taux de survie globale à 5 ans variant de 45 % à 85 % entre les tumeurs stade IIc et IIa et l’intérêt de la chimiothérapie adjuvante reste controversée dans cette situation.
Des résultats discordants
Dans la méta-analyse du groupe ACCENT, la réalisation d’un traitement adjuvant à base de fluoropyrimidine était associée à une amélioration significative du taux de survie globale à 8 ans (72,2 % versus 66,8 %, P = 0,026) [13]. Par ailleurs, dans une analyse poolée de 4 essais en adjuvant du NSABP, le bénéfice observé d’un traitement adjuvant à base de fluoropyrimidine pour les patients avec une tumeur de stade II était au minimum équivalent à celui observé pour les tumeurs de stade III (30 % et 18 % de réduction de risque de décès, respectivement) ; il faut néanmoins souligner le fait que les bras contrôles n’étaient pas les mêmes dans les 4 essais [29]. Inversement, plusieurs méta-analyses ont montré l’absence d’amélioration de la survie sans maladie et de la survie globale chez les patients avec un cancer colique de stade II traité par chimiothérapie adjuvante [30, 31]. Cependant, une méta-analyse plus récente publiée en 2008 par la Cochrane Library a montré une amélioration significative de la survie sans maladie (HR 0,83-0,83, IC95 % 0,75-0,92) et une amélioration non significative de la survie globale (HR 0,96, IC95 % 0,88-1,05) avec un traitement adjuvant comparé à la chirurgie seule [32].
Dans l’étude QUASAR (3 239 patients inclus dont 91 % avec des tumeurs de stade II), le risque de récidive et le risque de décès étaient diminués respectivement de 22 % (P = 0,001) et 18 % (P = 0,008) dans le bras 5-FU/AF par rapport au bras observation [33]. Dans l’étude MOSAIC, 40 % des patients présentaient une tumeur de stade II. Il n’y a pas dans cette étude de différence significative des taux de survie sans maladie et de survie globale à 10 ans entre les bras LV5FU2 et FOLFOX4 (73,6 % versus 75,2 %, HR = 0,89, IC95 % 0,68-1,16, P = 0,390 et 79,5 % versus 78,4 %, HR 1,00, P = 0,980, respectivement) [16]. Enfin, l’étude C-07 du NSABP n’a pas montré d’amélioration significative de la survie globale à 5 ans pour les tumeurs de stade II traitées par 5-FU/AF ou 5-FU/AF et oxaliplatine (89,6 % versus 89,7 %, respectivement) [17].
Il a été démontré, par le groupe ACCENT, que les patients avec stade II traités par chimiothérapie adjuvante par fluoropyrimidines, pris en charge entre 1996 et 2007 avaient un meilleur pronostic que ceux traités entre 1978 et 1995 [34]. La principale différence entre les deux périodes était un nombre de ganglions analysés plus important pour la période plus récente, expliquant un phénomène de migration de stage (phénomène de Will Rogers). Dans la mesure où les études ayant évalué les fluoropyrimidines contre surveillance ont inclus leurs patients avant 1995, il est possible, qu’en 2018, le bénéfice de la chimiothérapie adjuvante par fluoropyrimidines soit inférieur à ce qui a été démontré dans l’étude QUASAR et dans la méta-analyse ACCENT.
Le gain potentiel d’une chimiothérapie adjuvante dans les stades II est à pondérer en fonction de la toxicité de la chimiothérapie et du rapport bénéfice/risque, le bénéfice en survie étant modéré (entre 2 à 5 % en valeur absolue selon le risque de récidive avec les fluoropyrimidines seules).
Stade II à bas risque, stade II à (haut) risque
Les résultats contradictoires des essais en adjuvant des cancers coliques de stade II peuvent être expliqués par la grande variabilité pronostique de ces tumeurs. Ainsi, les paramètres liés à la tumeur et retenus par les sociétés savantes (ESMO, NCCN, thésaurus national de cancérologie digestive) comme associés à un risque plus élevé de récidive pour les cancers coliques de stade II sont essentiellement : T4 et surtout en cas de T4 avec envahissement des organes (T4b) de voisinage, nombre de ganglions analysés inférieur à 12 et perforation tumorale. D’autres facteurs, bien que considérés à risque, sont plus discutés : degré de différenciation, emboles vasculaires ou lymphatiques, engainements péri-nerveux, occlusion inaugurale. Pour certains experts, la présence d’emboles veineux, péri-nerveux et/ou lymphatiques ne peut être considérée quand il s’agit d’un seul facteur de risque comme un risque élevé. Le caractère peu différencié de la tumeur est associé à un risque plus élevé uniquement en cas de tumeur MSS (les tumeurs MSI sont très souvent peu différenciées et sont de bon pronostic). La présence de cellules néoplasiques isolées dans un ganglion (Isolated Tumor Cells : ITC ; tumeurs T3N0(i+), est une situation rare qui est considérée par certains comme un facteur de risque élevé (Tableau IV) [35].
La détection de « tumor budding » est également un facteur de mauvais pronostic pour les tumeurs de stade II [36]. Les statuts mutationnels de KRAS, NRAS ou BRAF n’ont pas d’intérêt dans l’évaluation du risque de récidive pour les cancers coliques localisés de stade II.
La présence d’une instabilité microsatellitaire (MSI) est associée à un bon pronostic pour les tumeurs de stade II. De plus, les résultats des essais en adjuvant ont montré l’absence d’efficacité des chimiothérapies à base de fluoropyrimidines pour les cancers coliques MSI de stade II [2].
Pour les tumeurs de stade II sans facteur de mauvais pronostic, la réalisation d’une chimiothérapie adjuvante n’est pas recommandée.
Pour les tumeurs de stade II à risque de récidive, un traitement adjuvant par 6 mois de LV5FU2 ou de capecitabine est à discuter ; l’ajout de l’oxaliplatine peut être envisagé chez les patients de moins de 70 ans compte tenu de l’amélioration non significative des taux de survie globale et sans récidive à 10 ans avec le FOLFOX pour les patients avec un cancer colique de stade II à risque (T4, perforation, moins de 10 ganglions analysés) [16, 37]. Il est important d’insister sur le fait que l’association fluoropyrimidines et oxaliplatine n’a pas statistiquement démontré son intérêt en situation adjuvante pour des patients avec un cancer du côlon de stade II, et que l’indication d’une telle chimiothérapie impose impérativement, comme toute décision de chimiothérapie adjuvante, d’être prise en réunion de concertation multidisciplinaire (Fig. 1).
Si l’indication d’une chimiothérapie est posée pour un patient avec un stade II (mais également pour stade III), en raison du bénéfice attendu modéré et d’une toxicité possible, il est recommandé par certains experts de faire une recherche d’un déficit en dihydropyrimidine déshydrogénase (DPD) avant l’administration d’une chimiothérapie à base d’une fluoropyrimidine. Ce test est fait en routine dans plusieurs centres français, qui acceptent les prélèvements venant d’autres centres [38].
Concernant la durée du traitement, l’étude IDEA sus-citée évaluait des patients avec des cancers du côlon de stade III. Certaines des études participant à IDEA, incluaient des patients de stade II (SCOT, TOSCA, ACHIEVE et HORG) et l’analyse poolée est attendue pour évaluer la durée de chimiothérapie par fluoropyrimidines et oxaliplatine (3 versus 6 mois) dans cette population. Il faut cependant insister sur le fait que chimiothérapie par fluoropyrimidines et oxaliplatine, n’a pas démontré son efficacité, pour la population des stades II. Si une chimiothérapie par fluoropyrimidine seule est entreprise (capecitabine ou LV5FU2 simplifié) la durée standard reste 6 mois.
Cas particuliers
Patients âgés
La preuve du concept de l’intérêt de la chimiothérapie adjuvante chez les personnes âgées a été apportée en 2001. Dans une analysée poolée d’essais ayant comparé une chimiothérapie à base de 5-FU à la chirurgie seule, le bénéfice de survie observé avec le 5-FU était similaire chez les patients de plus de 70 ans et de moins de 70 ans, sans augmentation des effets secondaires [39].
Concernant l’intérêt de l’oxaliplatine chez les patients de plus de 70 ans, une analyse poolée des essais MOSAIC, NSABP C-07 et XELOXA n’a pas permis de montrer d’amélioration statistiquement significative de la survie sans maladie, ni de la survie globale chez les patients de plus de 70 ans (N = 1 119 ; HR = 0,94, IC95 % 0,78-,13 et HR = 1,04, IC95 % 0,85-1,27, respectivement) [40]. Cependant les tests d’interaction étaient non significatifs, suggérant l’absence d’impact de l’âge sur l’efficacité de l’oxaliplatine. De plus, une seconde analyse poolée d’essais randomisés (NSABP C-08, XELOXA, X-ACT et AVANT) a montré une amélioration significative de la survie sans maladie et de la survie globale chez les patients de plus de 70 ans (N = 904 ; HR = 0,77, IC95 % 0,62-0,95, P = 0,014 et HR = 0,78, IC95 % 0,61-0,99, P = 0,045) [41]. Les patients âgés semblent donc tirer un moindre bénéfice de l’ajout de l’oxaliplatine que les patients plus jeunes ; le choix du protocole thérapeutique doit donc être discuté selon l’état général et les comorbidités du patient. L’étude PRODIGE 34 – ADAGE, en cours d’inclusion, permettra de préciser ces données pour les patients âgés.
Patients à haut risque cardiaque
Compte tenu de la cardiotoxicité des fluoropyrimidines, tout patient présentant une indication théorique à la réalisation d’un traitement adjuvant pour un cancer colique doit être évalué sur le plan cardiaque. En cas d’épisode ischémique récent (classiquement moins de 6 mois), le dossier doit être discuté avec une équipe de cardiologie. En cas de risque cardiaque élevé ou en cas de cardiotoxicité avéré des fluoropyrimidines, le remplacement du 5-FU ou de la capecitabine par le raltitrexed peut être discuté, en cas de stade III, d’autant plus que le risque de rechute est important (T4 et/ou N2). En effet Ransom et al. ont montré, que chez des patients ayant présenté une complication cardiaque du 5-FU ou de la capecitabine, le traitement par raltitrexed était faisable, sans risque sur le plan cardiaque [42]. Dans le cadre du cancer colique localisé, l’essai randomisé de non-infériorité PETACC-1 comparant le raltitrexed au 5-FU/AF a été interrompu prématurément, après inclusion de 993 patients, en raison de décès toxiques sous raltitrexed (1,9 %) ; après un suivi médian de 4 ans, le hazard ratio pour la survie sans rechute et pour la survie globale étaient respectivement de 1,16 (IC90 % 0,99-1,37) et de 1,01 (IC90 % 0,84-1,23) [43]. Par ailleurs, plusieurs essais ont évalué l’association du raltitrexed à l’oxaliplatine (TOMOX) en situation métastatique, avec des résultats comparables à ceux obtenus avec le FOLFOX [44]. Par conséquent, chez les patients à haut risque cardiaque, il est licite de ne pas réaliser de chimiothérapie adjuvante pour les cancers coliques de stade II (ou de l’interrompre en cas de toxicité cardiaque sous fluoropyrimidine) et de proposer un traitement par TOMOX pour les cancers coliques de stade III (avis d’experts).
Conclusion
Le développement des techniques chirurgicales et des traitements adjuvants par chimiothérapie à base de fluoropyrimidines ± oxaliplatine ont permis une amélioration de la survie des patients atteints d’un cancer colique localisé. En cas de stade III, le traitement adjuvant par chimiothérapie à base de fluoropyrimidines et oxaliplatine diminue d’environ 20 % le risque absolu de récidive, et constitue le standard de traitement dans cette situation. Concernant les tumeurs de stade II, le bénéfice de la chimiothérapie en termes de réduction du risque de rechute est modéré, de 2 à 5 % et un traitement par fluoropyrimidines, de type LV5FU2 ou capecitabine, doit être discuté en fonction des facteurs de risque associés. Si la durée de traitement optimale était jusqu’à présent de 6 mois, les résultats de l’étude internationale IDEA ont changé les standards et 3 mois de chimiothérapie par l’association capecitabine et oxaliplatine est le nouveau standard pour les stades T1-T3N1. En cas de stade III, T4 ou N2, 6 mois de chimiothérapie par FOLFOX ou CAPOX est recommandé.
Références
- Les cancers en France, édition 2016, collection Les Données, Institut national du cancer, avril 2017.
- Cohen R, Cervera P, Svrcek M, Dumont C, Garcia M-L, Chibaudel B, et al. [DNA mismatch repair and BRAF status in colorectal cancer: Interest for the therapeutic management?]. Bull Cancer (Paris) 2015;102:S72-81. doi: 10.1016/S0007-4551(15)31220-0.
- Moertel CG, Fleming TR, Macdonald JS, Haller DG, Laurie JA, Goodman PJ, et al. Levamisole and fluorouracil for adjuvant therapy of resected colon carcinoma. N Engl J Med 1990;322:352-8. doi: 10.1056/NEJM199002083220602.
- Modulation of fluorouracil by leucovorin in patients with advanced colorectal cancer: evidence in terms of response rate. Advanced Colorectal Cancer Meta-Analysis Project. J Clin Oncol Off J Am Soc Clin Oncol 1992;
10:896-903. doi: 10.1200/JCO.1992.10.6.896. - Labianca R, Marsoni S, Pancera G, Torri V, others. Efficacy of adjuvant fluorouracil and folinic acid in colon cancer. The Lancet 1995;345:939.
- O’Connell MJ, Mailliard JA, Kahn MJ, Macdonald JS, Haller DG, Mayer RJ, et al. Controlled trial of fluorouracil and low-dose leucovorin given for 6 months as postoperative adjuvant therapy for colon cancer. J Clin Oncol Off J Am Soc Clin Oncol 1997;15:246-50. doi: 10.1200/JCO.1997.15.1.246.
- Wolmark N, Rockette H, Mamounas E, Jones J, Wieand S, Wickerham DL, et al. Clinical trial to assess the relative efficacy of fluorouracil and leucovorin, fluorouracil and levamisole, and fluorouracil, leucovorin, and levamisole in patients with Dukes’ B and C carcinoma of the colon: results from National Surgical Adjuvant Breast and Bowel Project C-04. J Clin Oncol Off J Am Soc Clin Oncol 1999;17:3553-9. doi: 10.1200/JCO.1999.17.11.3553.
- Haller DG, Catalano PJ, Macdonald JS, O’Rourke MA, Frontiera MS, Jackson DV, et al. Phase III Study of Fluorouracil, Leucovorin, and Levamisole in High-Risk Stage II and III Colon Cancer: Final Report of Intergroup 0089. J Clin Oncol 2005;23:8671-8. doi: 10.1200/JCO.2004.00.5686.
- André T, Quinaux E, Louvet C, Colin P, Gamelin E, Bouche O, et al. Phase III Study Comparing a Semimonthly With a Monthly Regimen of Fluorouracil and Leucovorin As Adjuvant Treatment for Stage II and III Colon Cancer Patients: Final Results of GERCOR C96.1. J Clin Oncol 2007;25:3732-8. doi: 10.1200/JCO.2007.12.2234.
- Andre T, Colin P, Louvet C, Gamelin E, Bouche O, Achille E, et al. Semimonthly versus monthly regimen of fluorouracil and leucovorin administered for 24 or 36 weeks as adjuvant therapy in stage II and III colon cancer: results of a randomized trial. J Clin Oncol Off J Am Soc Clin Oncol 2003;21:2896-903. doi: 10.1200/JCO.2003.10.065.
- Twelves C, Wong A, Nowacki MP, Abt M, Burris H, Carrato A, et al. Capecitabine as adjuvant treatment for stage III colon cancer. N Engl J Med 2005;352:2696-704. doi: 10.1056/NEJMoa043116.
- Twelves C, Scheithauer W, McKendrick J, Seitz J-F, Van Hazel G, Wong A, et al. Capecitabine versus 5-fluorouracil/folinic acid as adjuvant therapy for stage III colon cancer: final results from the X-ACT trial with analysis by age and preliminary evidence of a pharmacodynamic marker of efficacy. Ann Oncol 2012;23:1190-7. doi: 10.1093/annonc/mdr366.
- Sargent D, Sobrero A, Grothey A, O’Connell MJ, Buyse M, Andre T, et al. Evidence for Cure by Adjuvant Therapy in Colon Cancer: Observations Based on Individual Patient Data From 20,898 Patients on 18 Randomized Trials. J Clin Oncol 2009;27:872-7. doi: 10.1200/JCO.2008.19.5362.
- André T, Boni C, Mounedji-Boudiaf L, Navarro M, Tabernero J, Hickish T, et al. Oxaliplatin, Fluorouracil, and Leucovorin as Adjuvant Treatment for Colon Cancer. N Engl J Med 2004;350:2343-51. doi: 10.1056/NEJMoa032709.
- André T, Boni C, Navarro M, Tabernero J, Hickish T, Topham C, et al. Improved Overall Survival With Oxaliplatin, Fluorouracil, and Leucovorin As Adjuvant Treatment in Stage II or III Colon Cancer in the MOSAIC Trial. J Clin Oncol 2009;27:3109-16. doi: 10.1200/JCO.2008.20.6771.
- André T, Gramont A de, Vernerey D, Chibaudel B, Bonnetain F, Tijeras-Raballand A, et al. Adjuvant Fluorouracil, Leucovorin, and Oxaliplatin in Stage II to III Colon Cancer: Updated 10-Year Survival and Outcomes According to BRAF Mutation and Mismatch Repair Status of the MOSAIC Study. J Clin Oncol 2015;33:4176-87. doi: 10.1200/JCO.2015.63.4238.
- Yothers G, O’Connell MJ, Allegra CJ, Kuebler JP, Colangelo LH, Petrelli NJ, et al. Oxaliplatin As Adjuvant Therapy for Colon Cancer: Updated Results of NSABP C-07 Trial, Including Survival and Subset Analyses. J Clin Oncol 2011;29:3768-74. doi: 10.1200/JCO.2011.36.4539.
- Schmoll H-J, Tabernero J, Maroun J, de Braud F, Price T, Van Cutsem E, et al. Capecitabine Plus Oxaliplatin Compared With Fluorouracil/Folinic Acid As Adjuvant Therapy for Stage III Colon Cancer: Final Results of the NO16968 Randomized Controlled Phase III Trial. J Clin Oncol 2015;33:3733-40. doi: 10.1200/JCO.2015.60.9107.
- Lapeyre-Prost A, Hug de Larauze M, Chibaudel B, Garcia ML, Guering-Meyer V, Bouché O, et al. Feasibility of Capecitabine and Oxaliplatin Combination Chemotherapy Without Central Venous Access Device in Patients With Stage III Colorectal Cancer. Clin Colorectal Cancer 2016;15:250-6. doi: 10.1016/j.clcc.2015.11.004.
- Van Cutsem E, Labianca R, Bodoky G, Barone C, Aranda E, Nordlinger B, et al. Randomized phase III trial comparing biweekly infusional fluorouracil/leucovorin alone or with irinotecan in the adjuvant treatment of stage III colon cancer: PETACC-3. J Clin Oncol Off J Am Soc Clin Oncol 2009;
27:3117-25. doi: 10.1200/JCO.2008.21.6663. - Allegra CJ, Yothers G, O’Connell MJ, Sharif S, Petrelli NJ, Colangelo LH, et al. Phase III Trial Assessing Bevacizumab in Stages II and III Carcinoma of the Colon: Results of NSABP Protocol C-08. J Clin Oncol 2011;29:11-6. doi: 10.1200/JCO.2010.30.0855.
- de Gramont A, Van Cutsem E, Schmoll H-J, Tabernero J, Clarke S, Moore MJ, et al. Bevacizumab plus oxaliplatin-based chemotherapy as adjuvant treatment for colon cancer (AVANT): a phase 3 randomised controlled trial. Lancet Oncol 2012;13:1225-33. doi: 10.1016/S1470-2045(12)70509-0.
- Alberts SR, Sargent DJ, Nair S, Mahoney MR, Mooney M, Thibodeau SN, et al. Effect of oxaliplatin, fluorouracil, and leucovorin with or without cetuximab on survival among patients with resected stage III colon cancer: a randomized trial. JAMA 2012;307:1383-93. doi: 10.1001/jama.2012.385.
- Taieb J, Tabernero J, Mini E, Subtil F, Folprecht G, Van Laethem J-L, et al. Oxaliplatin, fluorouracil, and leucovorin with or without cetuximab in patients with resected stage III colon cancer (PETACC-8): an open-label, randomised phase 3 trial. Lancet Oncol 2014;15:862-73. doi: 10.1016/S1470-2045(14)
70227-X. - Kerr RS, Love S, Segelov E, Johnstone E, Falcon B, Hewett P, et al. Adjuvant capecitabine plus bevacizumab versus capecitabine alone in patients with colorectal cancer (QUASAR 2): an open-label, randomised phase 3 trial. Lancet Oncol 2016;17:1543-57. doi: 10.1016/S1470-2045(16)
30172-3. - Blons H, Emile JF, Le Malicot K, Julié C, Zaanan A, Tabernero J, et al. Prognostic value of KRAS mutations in stage III colon cancer: post hoc analysis of the PETACC8 phase III trial dataset. Ann Oncol Off J Eur Soc Med Oncol 2014;25:2378-85. doi: 10.1093/annonc/mdu464.
- Chau I. A randomised comparison between 6 months of bolus fluorouracil/leucovorin and 12 weeks of protracted venous infusion fluorouracil as adjuvant treatment in colorectal cancer. Ann Oncol 2005;16:549-57. doi: 10.1093/annonc/mdi116.
- Shi Q, Sobrero A, Shields AF, Yoshino T, Paul J, Taieb J, et al. Prospective pooled analysis of six phase III trials investigating duration of adjuvant (adjuv) oxaliplatin-based therapy (3 vs 6 months) for patients (pts) with stage III colon cancer (CC): The IDEA (International Duration Evaluation of Adjuvant chemotherapy) collaboration. J Clin Oncol 35 2017 Suppl Abstr LBA1 n.d.
- Mamounas E, Wieand S, Wolmark N, Bear HD, Atkins JN, Song K, et al. Comparative efficacy of adjuvant chemotherapy in patients with Dukes’ B versus Dukes’ C colon cancer: results from four National Surgical Adjuvant Breast and Bowel Project adjuvant studies (C-01, C-02, C-03, and C-04). J Clin Oncol 1999;17:1349-1349.
- Figueredo A, Charette ML, Maroun J, Brouwers MC, Zuraw L. Adjuvant therapy for stage II colon cancer: a systematic review from the Cancer Care Ontario Program in evidence-based care’s gastrointestinal cancer disease site group. J Clin Oncol Off J Am Soc Clin Oncol 2004;22:3395-407. doi: 10.1200/JCO.2004.03.087.
- Efficacy of adjuvant fluorouracil and folinic acid in B2 colon cancer. International Multicentre Pooled Analysis of B2 Colon Cancer Trials (IMPACT B2) Investigators. J Clin Oncol Off J Am Soc Clin Oncol 1999;17:
1356-63. - Figueredo A, Coombes ME, Mukherjee S. Adjuvant Therapy for completely resected Stage II Colon Cancer. In: The Cochrane Collaboration, editor. Cochrane Database Syst. Rev., Chichester, UK: John Wiley & Sons, Ltd; 2008. doi: 10.1002/14651858.CD005390.pub2.
- QUASAR Collaborative Group. Adjuvant chemotherapy versus observation in patients with colorectal cancer: a randomised study. The Lancet 2007;370:2020-9. doi: 10.1016/S0140-6736(07)61866-2.
- Shi Q, Andre T, Grothey A, Yothers G, Hamilton SR, Bot BM, et al. Comparison of outcomes after fluorouracil-based adjuvant therapy for stages II and III colon cancer between 1978 to 1995 and 1996 to 2007: evidence of stage migration from the ACCENT database. J Clin Oncol Off J Am Soc Clin Oncol 2013;31:3656-63. doi: 10.1200/JCO.2013.49.4344.
- Mescoli C, Albertoni L, Pucciarelli S, Giacomelli L, Russo VM, Fassan M, et al. Isolated tumor cells in regional lymph nodes as relapse predictors in stage I and II colorectal cancer. J Clin Oncol Off J Am Soc Clin Oncol 2012;30:965-71. doi: 10.1200/JCO.2011.
35.9539. - Koelzer VH, Zlobec I, Lugli A. Tumor budding in colorectal cancer—ready for diagnostic practice? Hum Pathol 2016;47:4-19. doi: 10.1016/j.humpath.2015.08.007.
- Tougeron D, Mouillet G, Trouilloud I, Lecomte T, Coriat R, Aparicio T, et al. Efficacy of Adjuvant Chemotherapy in Colon Cancer With Microsatellite Instability: A Large Multicenter AGEO Study. J Natl Cancer Inst 2016;108:djv438. doi: 10.1093/jnci/djv438.
- Lecomte T, André T, Panis Y, Laurent-Puig P, Bibeau F, Taieb J. « Cancer du côlon ». Thésaurus National de Cancérologie Digestive, 11-2016, [En ligne] http://www.tncd.org.
- Sargent DJ, Goldberg RM, Jacobson SD, Macdonald JS, Labianca R, Haller DG, et al. A pooled analysis of adjuvant chemotherapy for resected colon cancer in elderly patients. N Engl J Med 2001;345:1091-1097.
- McCleary NJ, Meyerhardt JA, Green E, Yothers G, de Gramont A, Van Cutsem E,
et al. Impact of Age on the Efficacy of Newer Adjuvant Therapies in Patients With Stage II/III Colon Cancer: Findings From the ACCENT Database. J Clin Oncol 2013;31:2600-6. doi: 10.1200/JCO.2013.49.6638. - Haller DG, O’Connell MJ, Cartwright TH, Twelves CJ, McKenna EF, Sun W, et al. Impact of age and medical comorbidity on adjuvant treatment outcomes for stage III colon cancer: a pooled analysis of individual patient data from four randomized, controlled trials. Ann Oncol 2015;26:715-24. doi: 10.1093/annonc/mdv003.
- Ransom D, Wilson K, Fournier M, Simes RJ, Gebski V, Yip D, et al. Final results of Australasian Gastrointestinal Trials Group ARCTIC study: an audit of raltitrexed for patients with cardiac toxicity induced by fluoropyrimidines. Ann Oncol Off J Eur Soc Med Oncol 2014;25:117-21. doi: 10.1093/annonc/mdt479.
- Popov I, Carrato A, Sobrero A, Vincent M, Kerr D, Labianca R, et al. Raltitrexed (Tomudex) versus standard leucovorin-modulated bolus 5-fluorouracil: Results from the randomised phase III Pan-European Trial in Adjuvant Colon Cancer 01 (PETACC-1). Eur J Cancer Oxf Engl 1990 2008;44:2204-11. doi: 10.1016/j.ejca.2008.07.002.
- Gravalos C, Salut A, García-Girón C, García-Carbonero R, León AI, Sevilla I, et al. A randomized phase II study to compare oxaliplatin plus 5-fluorouracil and leucovorin (FOLFOX4) versus oxaliplatin plus raltitrexed (TOMOX) as first-line chemotherapy for advanced colorectal cancer. Clin Transl Oncol Off Publ Fed Span Oncol Soc Natl Cancer Inst Mex 2012;14:606-12. doi: 10.1007/s12094-
012-0843-x. - Saltz LB, Niedzwiecki D, Hollis D, Goldberg RM, Hantel A, Thomas JP, et al. Irinotecan fluorouracil plus leucovorin is not superior to fluorouracil plus leucovorin alone as adjuvant treatment for stage III colon cancer: results of CALGB 89803. J Clin Oncol Off J Am Soc Clin Oncol 2007;25:3456-61. doi: 10.1200/JCO.2007.11.2144.
- Ychou M, Hohenberger W, Thezenas S, Navarro M, Maurel J, Bokemeyer C, et al. A randomized phase III study comparing adjuvant 5-fluorouracil/folinic acid with FOLFIRI in patients following complete resection of liver metastases from colorectal cancer. Ann Oncol Off J Eur Soc Med Oncol 2009;20:1964-70. doi: 10.1093/annonc/mdp236.