Conflits d’intérêt
Aucun
Mots-clés : cholangite biliaire primitive, cholestase, acide ursodésoxycholique.
Abrévations
AUDC : acide ursodésoxycholique
CBP : cholangite biliaire primitive
Ig : Immunoglobulines
PAL : phosphatases alcalines
Introduction
La cholangite biliaire primitive (CBP), nouvelle dénomination de la cirrhose biliaire primitive, est une maladie cholestatique d’étiologie auto-immune et représente la première cause de cholestase intra-hépatique. Elle se caractérise par une destruction des canaux biliaires de petite taille liée à une infiltration lymphocytaire. La prévalence de la CBP est de 10 à 40 pour 100 000 habitants. La CBP affecte préférentiellement la femme (dans 90 % des cas) d’un âge médian de 55 ans au diagnostic. Ainsi, chez la femme de plus de 40 ans, la prévalence de la CBP est de 1 pour 1 000 [1].
Présentation clinico-biologique
Le signe fonctionnel le plus fréquent est le prurit [2] auquel peut s’associer une asthénie d’intensité variable. Le patient est parfois asymptomatique, le diagnostic sera alors porté devant des anomalies du bilan hépatique. De façon moins fréquente, le diagnostic pourra se faire à un stade avancé de la maladie hépatique devant une cirrhose décompensée ou une rupture de varices œsophagiennes. La CBP est souvent associée à d’autres pathologies auto-immunes qui sont par ordre décroissant de fréquence : syndrome de Sjogren, dysthyroïdie auto-immune, sclérodermie, polyarthrite rhumatoïde, lupus et maladie cœliaque [3].
Sur le plan biologique, la CBP se manifeste par une cholestase chronique (élévation des phosphatases alcalines (PAL) > 1,5 fois la limite supérieure de la normale et gamma-glutamyl transférase (GGT) > 3 fois la limite supérieure de la normale) avec ou sans augmentation de la bilirubinémie. À cette cholestase s’associe souvent une élévation modérée de l’activité des transaminases. Au cours de la CBP, on note une élévation des Immunoglobulines (Ig) M. Les autres signes biologiques peuvent être en rapport avec les complications de la cholestase chronique telles que déficit en vitamines liposolubles et hypercholestérolémie.
Dans 10 % des cas, la CBP est associée à une hépatite auto-immune, réalisant alors un syndrome de chevauchement ou overlap syndrome. Dans cette forme particulière, la biologie montre une élévation importante de l’activité des transaminases (supérieure à 5 fois la normale), une hypergammaglobulinémie avec élévation des Ig G et la présence d’anticorps anti-muscles lisses. L’histologie hépatique est indispensable pour poser le diagnostic d’overlap syndrome. Dans le cadre de l’overlap syndrome, les 2 pathologies peuvent apparaître simultanément ou bien de façon décalée, parfois de plusieurs années.
Démarche diagnostique
Les anticorps anti-mitochondries sont l’examen clef pour le diagnostic de CBP avec une sensibilité et une spécificité sont de 90 % et 97 % respectivement [2]. Le titre minimal d’anticorps anti-mitochondrie ayant une valeur diagnostique est de 1/40. Si la recherche d’anticorps anti-mitochondrie est négative, il conviendra de rechercher les anticorps antinucléaires spécifiques de la CBP : les anticorps anti-gp210 et anti-sp100.
L’association d’une cholestase intra-hépatique et de la positivité des anticorps spécifiques (anti-mitochondrie ou anti gp-210 ou anti-sp100) suffit pour poser le diagnostic de CBP. Ainsi, l’histologie hépatique n’est pas nécessaire. Néanmoins, dans 10 % des cas, les anticorps spécifiques sont négatifs et la réalisation d’une ponction biopsie hépatique est alors indiquée pour le diagnostic de CBP alors qualifiée de CBP séronégative.
Certains patients présentent des anticorps anti-mitochondries positifs sans cholestase associée (PAL normales), notamment des patients atteints d’autres pathologies auto-immunes. Une étude récente a montré que parmi ces patients, seulement 1 sur 6 développera une CBP après 5 ans [4]. Il est donc recommandé de surveiller ces patients par un bilan hépatique annuel.
Une fois le diagnostic de CBP posé, la gravité de l’atteinte hépatique devra être évaluée, en particulier en dépistant une fibrose avancée. La mesure de l’élastométrie hépatique par le Fibroscan est une méthode validée pour le diagnostic non invasif de la fibrose au cours de la CBP [5]. Le seuil de 9,6 kPa a été retenu pour différencier une CBP débutante (≤ 9,6 kPa) d’une CBP avancée (> 9,6 kPa). Lors du diagnostic de CBP, des complications extra-hépatiques devront être recherchées telles que l’ostéoporose. En effet, les patients atteints de CBP présentent un risque augmenté d’ostéoporose [6]. Enfin, il faudra rechercher d’autres maladies auto-immunes associées car celles-ci peuvent aggraver les symptômes des patients (asthénie, prurit) mais aussi retentir sur les tests hépatiques. Le tableau 1 résume le bilan initial qui doit être réalisé lors du diagnostic de CBP.
| But | Moyen |
|---|
| Évaluation de la fonction hépatique | - ASAT, ALAT, GGT, PAL
- Bilirubine totale et conjuguée
- TP, Facteur V, INR
- Albumine
- NFS, plaquettes
- Urée, créatinine
Échographie hépatique* |
| Marqueurs non invasifs de fibrose | Élastométrie hépatique (Fibroscan) |
Recherche de complications :- Carence en vitamine K
- Carence en vitamine D et calcium
- Ostéoporose
- Dyslipidémie secondaire
| - TP, Facteur V
- Vitamine D, Calcémie
- Ostéodensitométrie
- Cholestérol total, LDL, HDL, Triglycérides
|
| Recherche de maladies auto-immunes associées | TSH (+ autres examens selon signes cliniques) |
Tableau I. Bilan initial à réaliser au diagnostic de CBP
* Si l’échographie n’a pas été faite lors de la démarche diagnostique de la cholestase chronique, il faudra la réaliser lors du bilan initial pour rechercher des signes de maladie hépatique avancée : dysmorphie, signes d’hypertension portale.
Histologie
La biopsie hépatique est indiquée en cas d’absence d’auto-anticorps spécifiques de la CBP ou en cas de suspicion d’un overlap syndrome (transaminases élévées > 5 fois la limite supérieure de la normale, élévation des gammaglobuines ou des Ig G).
La biopsie hépatique a pour but de rechercher des lésions en faveur du diagnostic de CBP. Ces lésions peuvent être des signes histologiques spécifiques : la cholangite destructrice non suppurée granulomateuse et la cholangite destructrice lymphocytaire. Ces signes spécifiques sont parfois absents car l’atteinte histologique peut être segmentaire. Il existe d’autres lésions histologiques souvent rencontrées au cours de la CBP mais qui ne sont pas spécifiques de cette pathologie : granulome épithélioïde, inflammation lympho-plasmocytaire, cholestase histologique, réaction ductulaire. La biopsie hépatique a également pour but d’évaluer la sévérité de la maladie par l’appréciation de la fibrose hépatique et par la recherche d’une ductopénie définie par un ratio d’espaces portes sans canal biliaire sur le nombre total d’espaces portes inférieur à 50 %. La fibrose hépatique et la présence d’une ductopénie constituent 2 facteurs pronostiques importants. Plusieurs classifications histologiques ont été proposées pour la CBP [7-9] (Tableau II). En cas de suspicion d’overlap syndrome, la biopsie hépatique doit rechercher des signes histologiques d’hépatite auto-immune et principalement une hépatite d’interface.
| Nom | Année | Référence | Stades |
|---|
| Ludwig | 1978 | [7] | - Stade 1 : Lésions limitées à l’espace portale
- Stade 2 : Réaction ductulaire périportale ou hépatite d’interface
- Stade 3 : Septa fibreux
- Stade 4 : Cirrhose
|
| Classification Japonaise | 2010 | [8] | - Score de Fibrose (0-3)
- Score de Ductopénie (0-3)
- Score de dépots de granules orcéine positifs (0-3)
- Grade d’activité de la cholangite (0-3)
- Grade d’activité de l’hépatite (0-3)
|
| Classification française (FBI) | 2015 | [9] | - Fibrose (0-4)
- Bile Duct Ratio : espace porte avec canal biliaire/ nombre total d’espaces portes
- Inflammation (hépatite d’interface) (0-3)
|
Tableau II. Classifications histologiques de la CBP
Pronostic
La CBP est une maladie sévère évoluant vers la cirrhose biliaire secondaire et ses propres complications. Sans traitement, la survie médiane sans transplantation est estimée à 10 ans [2]. Les facteurs de mauvais pronostic sont les suivants : l’âge jeune au diagnostic, le sexe masculin, le fait d’avoir des symptômes (prurit et asthénie), la bilirubinémie élevée, l’albuminémie basse. La fibrose hépatique est un élément fondamental pour le pronostic qu’elle soit évaluée par l’histologie ou bien par des méthodes non invasives telles que le score de fibrose ELF [10] ou l’élastométrie hépatique par le Fibroscan [5]. La réponse au traitement est un autre élément majeur qui conditionne le pronostic [2]. Ainsi, les patients répondeurs au traitement par acide ursodésoxycholique (AUDC) ont une survie sans transplantation identique à celle de la population générale [2]. Des scores continus complexes ont été récemment développés pour évaluer le pronostic à l’échelle individuelle : le GLOBE score et le UK-PBC score [11-12]. Ces scores tiennent compte de paramètres au diagnostic et à 1 an du traitement par AUDC.
Traitement
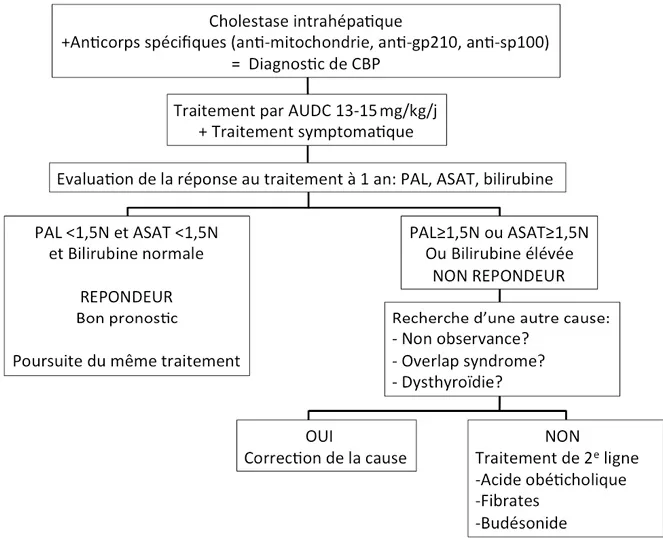
Longtemps, le seul traitement de la CBP a été l’AUDC. L’AUDC est un acide biliaire naturel hydrophile dont l’action est sous-tendue par plusieurs mécanismes : la modification de la composition de la bile qui, enrichie en AUDC, devient plus hydrophile, l’augmentation du flux biliaire (notamment via l’activation de l’expression du transporteur ABCB4) et enfin un effet anti-apoptotique. Les données de la littérature ont démontré que l’AUDC était capable d’améliorer non seulement l’histologie hépatique des patients atteints de CBP mais aussi leur survie sans transplantation [13-14]. C’est pourquoi l’AUDC est recommandé en première intention pour le traitement de la CBP. Il est indiqué dès le diagnostic posé et quel que soit le degré de fibrose [2]. La posologie de l’AUDC est de 13-15 mg/kg/j. La tolérance de l’AUDC est excellente, le seul effet secondaire est la diarrhée. L’efficacité du traitement par AUDC est évaluée par la réponse biologique à 1 an du début du traitement. De nombreuses définitions de cette réponse biologique ont été proposées [14-16]. La définition de réponse biologique la plus largement utilisée est celle des critères de Paris II [16] : PAL < 1,5 fois la limite supérieure de la normale et ASAT < 1,5 fois la limite supérieure de la normale et bilirubine normale à 1 an du début du traitement. Cependant, 40 % des patients atteints de CBP sont non-répondeurs à l’AUDC et il a été montré que leur survie sans transplantation était significativement inférieure à celle des patients répondeurs [16]. En cas de non réponse au traitement par AUDC, il faut rechercher une mauvaise observance, une hépatite auto-immune associée (overlap syndrome) ou une autre maladie auto-immune responsable d’anomalies des tests hépatiques comme une hyperthyroïdie ou une maladie cœliaque. Si aucun de ces éléments n’est trouvé, un traitement de 2e ligne est indiqué.
Récemment, de nouvelles molécules ont montré leur efficacité dans le traitement de la CBP. L’acide obéticholique est un acide biliaire qui agit comme agoniste du récepteur FXR avec des propriétés anti-cholestatique et anti-fibrosante. Une étude a montré l’efficacité de l’acide obéticholique pour améliorer la biologie et l’élastométrie des patients atteints de CBP [17]. L’acide obéticholique a désormais l’AMM pour le traitement de la CBP en deuxième intention, soit en monothérapie en cas d’intolérance à l’AUDC, soit en association à l’AUDC en cas d’absence de réponse biologique à l’AUDC [2]. L’acide obéticholique a pour principal effet secondaire, la majoration du prurit. L’augmentation progressive de la posologie de l’acide obéticholique (5 mg/j puis après 6 mois : 10 mg/j) permet de diminuer ce risque de majoration du prurit. Le recul est encore insuffisant pour savoir si ce traitement par acide obéticholique est capable augmenter la survie des patients atteints de CBP.
Les fibrates (agonistes PPAR) sont utilisés pour le traitement de l’hypertriglycéridémie ont une action anti-cholestatique impliquant un effet anti-inflammatoire, une diminution de la synthèse des acides biliaires et une augmentation de la sécrétion des phospholipides [18]. De nombreuses études ont montré que les fibrates, associés à l’AUDC, étaient capables d’améliorer les tests hépatiques au cours de la CBP [19]. Ces résultats prometteurs ont été confirmés par un essai contrôlé randomisé multicentrique mené chez les patients avec CBP non répondeurs à l’AUDC [20]. Les effets secondaires possibles des fibrates sont une hépatotoxicité, une insuffisance rénale et la survenue de douleurs musculaires. Contrairement à l’acide obéticholique, les fibrates présentent l’avantage de pouvoir améliorer le prurit au cours de la CBP [21]. Néanmoins, ce traitement n’a pas encore l’AMM au cours de la CBP.
Un autre traitement prometteur pour la prise en charge des patients CBP non répondeurs à l’AUDC est le budésonide. Le budésonide est un corticoïde à forte extraction hépatique avec moins d’effets secondaires que les corticoïdes classiques. Des données préliminaires ont montré son efficacité pour améliorer les tests hépatiques et l’histologie hépatique au cours de la CBP [22]. Le budésonide fait actuellement l’objet d’une étude contrôlée randomisée dont les résultats sont en attente. Ce traitement n’est pas indiqué chez les patients cirrhotiques.
La prise en charge thérapeutique des patients atteints de CBP est résumée dans la figure 1.

Figure 1. Prise en charge thérapeutique de la CBP
Le traitement des patients atteints de CBP doit également comprendre le traitement des symptômes que sont le prurit et l’asthénie. Pour le traitement du prurit, les recommandations préconisent un traitement médicamenteux par paliers : cholestyramine, rifampicine, naltrexone, sertraline. En cas d’échec des ces traitements médicamenteux, un traitement instrumental doit être envisagé par échanges plasmatiques ou par drainage naso-biliaires voire une transplantation hépatique en cas de prurit réfractaire. Pour le traitement de l’asthénie, aucun médicament n’a été validé et il est donc recommandé une prise en charge multidisciplinaire pouvant faire intervenir psychothérapie de soutien, thérapie comportementale, hypnose et association de malades [2]. Le traitement des patients a également pour objectif de corriger les déficits en vitamines liposolubles induites par la cholestase chronique, notamment le déficit en vitamine D. En raison du risque augmenté d’ostéoporose chez les patients avec CBP [6], une supplémentation en calcium et en vitamine D est recommandée. Enfin, il faudra toujours rechercher et traiter une dysthyroïdie qui peut être associée à la CBP et qui risque d’aggraver le prurit, l’asthénie et l’ostéoporose.
La transplantation hépatique est le seul traitement curatif de la CBP. Elle est indiquée en cas de cirrhose décompensée, d’ictère avec bilirubinémie supérieure à 50 mmol/l, ou exceptionnellement en cas de prurit réfractaire. Les taux de survie globale et du greffon après transplantation sont parmi les plus élevés enregistrés. La survie à 5 ans après transplantation hépatique pour CBP est estimée à 80 % [23]. Le risque de récidive de la CBP sur le greffon est de 50 % à 10 ans et pourrait justifier d’un traitement préventif par AUDC au long cours à la même posologie que le traitement curatif [24].
Surveillance
Il est recommandé de surveiller les patients atteints de CBP par une consultation tous les 6 mois. Une mesure de l’élastométrie hépatique par Fibroscan tous les ans est proposée. En cas de cirrhose, les recommandations de surveillance sont les mêmes que pour les cirrhoses d’autre étiologie : dépistage du carcinome hépatocellulaire par une échographie hépatique tous les 6 mois et dépistage des varices œsophagiennes selon les critères de Baveno VI [25]. De plus, il conviendra d’évaluer l’efficacité et la tolérance des traitements en cours : à la fois les traitements de la CBP et les traitements symptomatiques. Il est recommandé d’effectuer une ostéodensitométrie de façon régulière afin de dépister l’ostéoporose.
Conclusion
La CBP est une maladie rare mais dont le diagnostic est aisé dès lors qu’il est évoqué. Le traitement repose sur l’AUDC qui permet d’améliorer la survie sans transplantation hépatique. Le pronostic repose sur la fibrose hépatique évaluée par le Fibroscan et sur la réponse biologique au traitement par AUDC. L’acide obéticholique a maintenant l’AMM en 2e intention soit en cas d’intolérance à l’AUDC soit en cas d’absence de réponse biologique à l’AUDC
Références
- Boonstra K, Kunst AE, Stadhouders PH, et al. Rising incidence and prevalence of primary biliary cirrhosis: a large population-based study. Liver Int 2014;34:e31-8.
- European Association for the Study of the Liver. Electronic address eee, European Association for the Study of the L. EASL Clinical Practice Guidelines: The diagnosis and management of patients with primary biliary cholangitis. J Hepatol 2017;67:145-72.
- Chalifoux SL, Konyn PG, Choi G, et al. Extrahepatic Manifestations of Primary Biliary Cholangitis. Gut Liver 2017;11:771-80.
- Dahlqvist G, Gaouar F, Carrat F, et al. Large-scale characterization study of patients with antimitochondrial antibodies but nonestablished primary biliary cholangitis. Hepatology 2017;65:152-63.
- Corpechot C, Carrat F, Poujol-Robert A, et al. Noninvasive elastography-based assessment of liver fibrosis progression and prognosis in primary biliary cirrhosis. Hepatology 2012;56:198-208.
- Pares A, Guanabens N. Osteoporosis in primary biliary cirrhosis: pathogenesis and treatment. Clin Liver Dis 2008;12:407-24; x.
- Ludwig J, Dickson ER, McDonald GS. Staging of chronic nonsuppurative destructive cholangitis (syndrome of primary biliary cirrhosis). Virchows Arch A Pathol Anat Histol 1978;379:103-12.
- Nakanuma Y, Zen Y, Harada K, et al. Application of a new histological staging and grading system for primary biliary cirrhosis to liver biopsy specimens: Interobserver agreement. Pathol Int 2010;60:167-74.
- Wendum D, Boelle PY, Bedossa P, et al. Primary biliary cirrhosis: proposal for a new simple histological scoring system. Liver Int 2015;35:652-9.
- Mayo MJ, Parkes J, Adams-Huet B, et al. Prediction of clinical outcomes in primary biliary cirrhosis by serum enhanced liver fibrosis assay. Hepatology 2008;48:1549-57.
- Lammers WJ, Hirschfield GM, Corpechot C, et al. Development and Validation of a Scoring System to Predict Outcomes of Patients With Primary Biliary Cirrhosis Receiving Ursodeoxycholic Acid Therapy. Gastroenterology 2015;149:1804-1812 e4.
- Carbone M, Sharp SJ, Flack S, et al. The UK-PBC risk scores: Derivation and validation of a scoring system for long-term prediction of end-stage liver disease in primary biliary cholangitis. Hepatology 2016;63:930-50.
- Corpechot C, Carrat F, Bahr A, et al. The effect of ursodeoxycholic acid therapy on the natural course of primary biliary cirrhosis. Gastroenterology 2005;128:297-303.
- Pares A, Caballeria L, Rodes J. Excellent long-term survival in patients with primary biliary cirrhosis and biochemical response to ursodeoxycholic Acid. Gastroenterology 2006;130:715-20.
- Corpechot C, Abenavoli L, Rabahi N, et al. Biochemical response to ursodeoxycholic acid and long-term prognosis in primary biliary cirrhosis. Hepatology 2008;48:871-7.
- Corpechot C, Chazouilleres O, Poupon R. Early primary biliary cirrhosis: biochemical response to treatment and prediction of long-term outcome. J Hepatol 2011;55:1361-7.
- Nevens F, Andreone P, Mazzella G, et al. A Placebo-Controlled Trial of Obeticholic Acid in Primary Biliary Cholangitis. N Engl J Med 2016;375:631-43.
- Ghonem NS, Assis DN, Boyer JL. Fibrates and cholestasis. Hepatology 2015;62:635-43.
- Levy C, Peter JA, Nelson DR, et al. Pilot study: fenofibrate for patients with primary biliary cirrhosis and an incomplete response to ursodeoxycholic acid. Aliment Pharmacol Ther 2011;33:235-42.
- Corpechot C, Chazouilleres O, Rousseau A, et al. A 2-year multicenter, double-blind, randomized, placebo-controlled study of bezafibrate for the treatment of primary biliary cholangitis in patients with inadequate biochemical response to ursodeoxycholic acid therapy (Bezurso). J Hepatol 2017;66:S89.
- Reig A, Sese P, Pares A. Effects of Bezafibrate on Outcome and Pruritus in Primary Biliary Cholangitis With Suboptimal Ursodeoxycholic Acid Response. Am J Gastroenterol 2017.
- Rautiainen H, Karkkainen P, Karvonen AL, et al. Budesonide combined with UDCA to improve liver histology in primary biliary cirrhosis: a three-year randomized trial. Hepatology 2005;41:747-52.
- Liermann Garcia RF, Evangelista Garcia C, McMaster P, et al. Transplantation for primary biliary cirrhosis: retrospective analysis of 400 patients in a single center. Hepatology 2001;33:22-7.
- Bosch A, Dumortier J, Maucort-Boulch D, et al. Preventive administration of UDCA after liver transplantation for primary biliary cirrhosis is associated with a lower risk of disease recurrence. J Hepatol 2015;63:1449-58.
- de Franchis R, Baveno VIF. Expanding consensus in portal hypertension: Report of the Baveno VI Consensus Workshop: Stratifying risk and individualizing care for portal hypertension. J Hepatol 2015;63:
743-52.