Conflits d’intérêt
Aucun
Mots-clés : cirrhose, infections bactériennes, résistance aux antibiotiques
Les infections bactériennes sont une complication tardive de la cirrhose. Elles surviennent chez des patients ayant une maladie évoluée, compliquée d’insuffisance hépatocellulaire et d’hypertension portale, le plus souvent décompensée. À ce stade, elles sont particulièrement fréquentes et leur signification pronostique est très péjorative. Marqueur de gravité, elles contribuent également à dégrader une situation déjà très précaire. Leur prévention est donc un enjeu majeur, d’autant que la progression constante de l’antibiorésistance rend leur prise en charge de plus en plus complexe. Dans ce contexte préoccupant, de nouvelles stratégies thérapeutiques ont été récemment proposées.
Complication tardive
Si les infections bactériennes apparaissent tard dans l’évolution de la cirrhose, c’est qu’il faut du temps pour que soient réunies les conditions de leur survenue. Tout d’abord, la translocation bactérienne intestinale – favorisée par la pullulation microbienne et l’augmentation de la perméabilité intestinale – et les altérations de l’immunité – humorale et cellulaire – ne prennent toute leur ampleur qu’avec la progression de l’insuffisance hépatocellulaire et de l’hypertension portale. Ensuite, ces infections sont souvent elles-mêmes des complications des autres complications de la cirrhose, en premier lieu l’ascite (pour l’infection du liquide d’ascite) et l’hémorragie digestive (qui est un facteur majeur de translocation bactérienne intestinale). Enfin, la prise en charge de toutes ces complications nécessite souvent des gestes invasifs et des séjours prolongés en milieu hospitalier à leur tour à l’origine d’infections nosocomiales.
La survenue d’une infection bactérienne est bien évidemment possible au stade de cirrhose compensée, mais cela reste, somme toute, rare. L’étiologie de la maladie hépatique peut également jouer un rôle. Ainsi, l’alcool pourrait ajouter ses effets délétères propres à la cirrhose et favoriser certaines infections [1].
Fréquence
Au stade de cirrhose décompensée, les infections bactériennes sont donc fréquentes. La littérature estime entre 25 et 35 % la prévalence des infections bactériennes chez les patients cirrhotiques hospitalisés [2-4]. Dans l’étude RESIST [5] , ayant inclus 1093 patients dans 42 centres français en 2016, elle était de 36 %, plus élevée dans les centres universitaires que dans les hôpitaux généraux (46 % vs 29 %). Il s’agissait principalement d’infections du liquide d’ascite (29 %), d’infections urinaires (20 %), de pneumonies (17 %), de bactériémies spontanées (9 %) et d’infections des tissus mous (8,5 %). Dans 3/4 des cas, l’infection était diagnostiquée dans les 48 premières heures de l’hospitalisation ; dans 25 % des cas, elle était nosocomiale.
Germes en cause
Classiquement, les infections bactériennes du patient cirrhotique sont à bacilles Gram négatif (BGN). Cependant, la part relative des cocci Gram positif (CGP) a fortement augmenté au cours des deux dernières décennies en rapport avec la réalisation de plus en plus fréquente de gestes invasifs chez ces patients [2]. Si les BGN restent largement prédominants dans les infections communautaires, les CGP sont maintenant majoritaires dans les infections nosocomiales. Dans l’étude RESIST, un germe était isolé dans 2/3 des infections. Les BGN restaient globalement prédominants (53 % ; Escherichia coli dans 2/3 cas). Les CGP étaient en cause dans 39 % des cas, se répartissant équitablement entre staphylocoques, entérocoques et streptocoques. Il est à noter que, à l’exception des colites à Clostridium difficile, les infections à anaérobies sont rares (seulement 2 cas d’infection à Bacteroides dans l’étude RESIST).
Signification pronostique péjorative
Les infections bactériennes peuvent avoir une évolution rapidement sévère chez les patients cirrhotiques et le risque de décès par sepsis est particulièrement élevé. Cela s’explique par un état circulatoire souvent précaire, du fait de la vasodilatation artérielle splanchnique et d’altérations de la contractilité cardiaque, ainsi que par une diminution de la tolérance du foie, mais aussi d’autres organes (reins, cerveau), à l’agression. À cela s’ajoute une réponse excessive à l’infection, avec la production de grandes quantités de molécules et de cytokines pro-inflammatoires. Tout cela conduit, beaucoup plus rapidement que chez un autre patient, à une détérioration circulatoire avec diminution de la perfusion tissulaire, à des altérations directes des organes, et in fine à des défaillances d’organes qui caractérisent ce que l’on appelle maintenant l’acute-on-chronic liver failure (ACLF) [6].
À travers une large revue de la littérature (178 études publiées entre 1978 et 2009 ; 11 987 patients), Arvaniti et al. ont montré que la survenue d’une infection bactérienne multipliait par 4 la mortalité des patients cirrhotiques [7]. Elle était de 30 % à 1 mois, 44 % à 3 mois, et 63 % à 1 an. Lorsque l’on comparait les études publiées avant et après 2000, une diminution de la mortalité à 1 mois – de 37 % à 26 % – était observée, témoignant probablement de progrès dans la prise en charge de ces infections. En revanche, chez les patients survivants à 1 mois, la mortalité à 1 an ne différait guère (51 % vs 46 %). Cela suggère que des altérations du milieu intérieur persistent au décours de l’infection, qui vont favoriser la survenue de nouvelles complications potentiellement létales.
Les résultats de l’étude RESIST vont dans le même sens : chez les patients infectés, la mortalité hospitalière et à 3 mois était de 18 % et 33 %, versus 3 % et 14 % chez les patients non infectés.
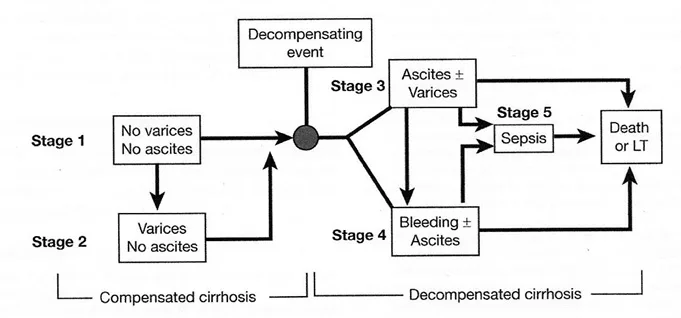
On distingue habituellement deux stades, compensé et décompensé, à la cirrhose. En 2006, D’Amico a voulu affiner cette classification en définissant quatre stades, de sévérité pronostique croissante, basés sur les varices, l’ascite et l’hémorragie [8]. À la suite de leur travail, Arvaniti et al. ont proposé d’en ajouter un cinquième, caractérisé par la survenue d’un sepsis, avec une probabilité de décès à 1 an supérieure à 60 % (Figure 1) [7]. Tout cela reste assez théorique, mais a l’intérêt de bien positionner le sepsis dans l’histoire de la cirrhose.

Figure 1. Stades de la cirrhose selon Arvaniti et al. [7]. Ces auteurs ont proposé de classer la cirrhose en 5 stades de sévérité croissante. La mortalité à 1 an est estimée à < 1 % pour le stade 1 (absence de varice et d’ascite), 3-4 % pour le stade 2 (varices sans ascite), 20 % pour le stade 3 (ascite ± varices), 50 % pour le stade 4 (hémorragie digestive ± ascite) et > 60 % pour le stade 5 (sepsis).
Le point important à retenir est que près de la moitié des patients cirrhotiques ayant survécu à un sepsis vont décéder dans l’année qui suit. De ce fait, si la question de la transplantation hépatique n’a pas encore été évoquée, la survenue d’un sepsis doit conduire à se la poser.
Prévention
On comprend donc l’enjeu de la prévention de ces infections, notamment chez les patients en attente de greffe. L’antibioprophylaxie en est un premier moyen et a toute sa place dans deux complications de la cirrhose : l’hémorragie digestive et l’ascite. Mais d’autres mesures sont également importantes et ne doivent pas être négligées. (Tableau I).
| Antibioprophylaxie : doit être restreinte aux situations à haut risque d’infection |
| Hémorragie digestive | Norfloxacine 400 mg × 2 PO
En cas de cirrhose grave : C3G (céfotaxime 1 g × 3/j ou ceftriaxone 1 g/j) IV
à débuter le plus tôt possible et à restreindre à la période hémorragique |
| Prévention secondaire de l’infection du liquide d’ascite | Norfloxacine 400 mg/j PO jusqu’à disparition de l’ascite vérifiée par échographie |
| Prévention primaire de l’infection du liquide d’ascite | Norfloxacine 400 mg/j PO chez les patients à haut risque : cirrhose Child C + protéines dans l’ascite <15 g/l |
Autres mesures- Utilisation appropriée et surveillance des cathéters veineux, des sondes urinaires et gastriques ; respect des mesures d’hygiène et d’asepsie en cas de procédure invasive
- Prescription des IPP dans le cadre strict de leurs indications
- Traitement d’une carence profonde (< 10 ng/ml) en vitamine D
- Vaccinations antipneumococcique et antigrippale
- Informer le patient et son médecin traitant du risque d’infections bactériennes et de la nécessité de consulter sans tarder en cas de syndrome fébrile
|
Tableau I. Prévention des infections bactériennes.
Antibioprophylaxie
La plupart des infections bactériennes spontanées du patient cirrhotique résultent de la translocation intestinale de BGN. L’antibioprophylaxie doit donc cibler ces germes en priorité tout en respectant la flore anaérobie. Pour cela, on utilise préférentiellement la norfloxacine, qui est une quinolone faiblement absorbable. Étant donné le risque de sélection de bactéries résistantes, cette antibioprophylaxie doit être restreinte aux situations à haut risque d’infection [9].
Hémorragie digestive
En cas d’hémorragie digestive haute, environ la moitié des patients cirrhotiques vont développer une infection bactérienne dans la semaine qui suit. L’antibioprophylaxie permet de réduire ce taux d’infection à 10-15 %, de diminuer l’incidence de la récidive hémorragique et d’améliorer la survie [10]. Elle repose sur la norfloxacine per os (400 mg × 2/j). Cependant, chez les patients à très haut risque – c’est-à-dire ayant une cirrhose grave avec ictère, ascite et/ou encéphalopathie – il est préférable d’utiliser une céphalosporine de 3e génération (C3G) par voie intraveineuse [11, 12]. L’antibioprophylaxie doit être débutée le plus tôt possible et se limiter à la période hémorragique. Elle est probablement inutile chez les patients Child A [12, 13].
Prévention secondaire de l’infection du liquide d’ascite
Chez les patients qui ont survécu à une infection du liquide d’ascite, le risque de récidive dans l’année est estimé à 60-70 %. Une prophylaxie secondaire (norfloxacine 400 mg/j) est donc recommandée tant que persiste l’ascite [9, 14]. Avant de l’interrompre, il faut s’assurer de la disparition complète de l’ascite par une échographie.
Prévention primaire de l’infection du liquide d’ascite
La prophylaxie primaire de l’infection du liquide d’ascite est plus controversée. Elle doit être réservée aux patients à risque élevé – cirrhose Child C + taux de protéines dans l’ascite inférieur à 15 g/l [15] – en particulier s’il existe un projet de transplantation. Elle repose de la même manière sur la norfloxacine à la dose de 400 mg/j.
Ces recommandations sont déjà anciennes. Une enquête de pratique réalisée en 2012 a montré qu’elles étaient largement suivies en France [16].
Autres mesures
Cathéters, sondes, et autres gestes invasifs
Attention aux cathéters : il faut les surveiller, les changer régulièrement, et les enlever dès que possible, afin de prévenir la survenue d’infections locales et de bactériémies. Attention aux sondes urinaires : il faut réévaluer quotidiennement leur indication et éviter les sondages abusifs. Attention aux sondes gastriques, rarement utiles, mais qui peuvent favoriser une pneumopathie d’inhalation. Attention à toutes les procédures diagnostiques et thérapeutiques invasives, pour lesquelles les règles d’hygiène et d’asepsie doivent être scrupuleusement respectées.
Inhibiteurs de la pompe à protons (IPP)
Le rôle favorisant des IPP dans la survenue d’une infection du liquide d’ascite est controversé [17-19]. Dans le doute, il convient de ne les prescrire que dans le cadre strict de leurs indications et jamais de façon prolongée, a fortiori si la cirrhose est décompensée.
Carence en vitamine D
Il a été suggéré qu’une carence en vitamine D pourrait favoriser la survenue d’infections bactériennes chez le patient cirrhotique [20, 21]. Si cela est loin d’être établi, il est néanmoins probable qu’une carence profonde (<10 ng/ml) est délétère et il est raisonnable de la corriger.
Vaccinations
La vaccination contre le pneumocoque est recommandée chez les patients cirrhotiques. Elle repose sur l’administration d’une dose de vaccin conjugué 13-valent suivie huit semaines plus tard d’une dose de vaccin polyosidique non conjugué 23-valent. Il n’y a pas lieu de faire de rappel ultérieurement. La vaccination antigrippale doit être également conseillée.
Information du patient
Le patient cirrhotique – ainsi que son médecin traitant – doit être informé qu’il est à risque de faire des infections bactériennes potentiellement graves et qu’il doit consulter sans tarder en cas de syndrome fébrile. Cette information, qui ne coûte rien, peut lui sauver la vie en permettant la mise en route précoce d’une antibiothérapie avant la survenue d’un sepsis sévère et d’une ACLF.
Antibiorésistance
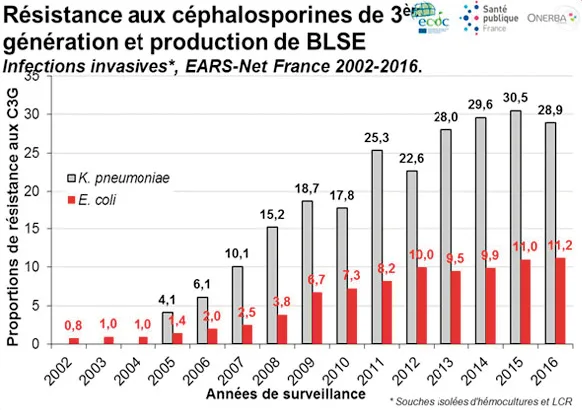
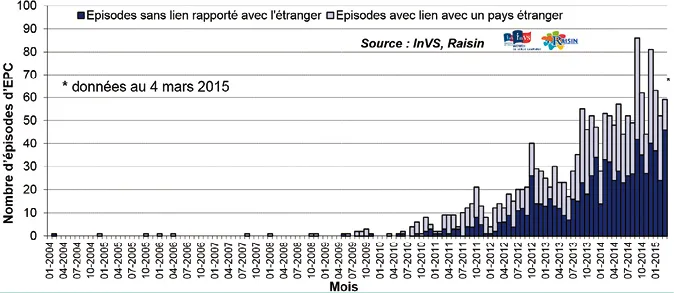
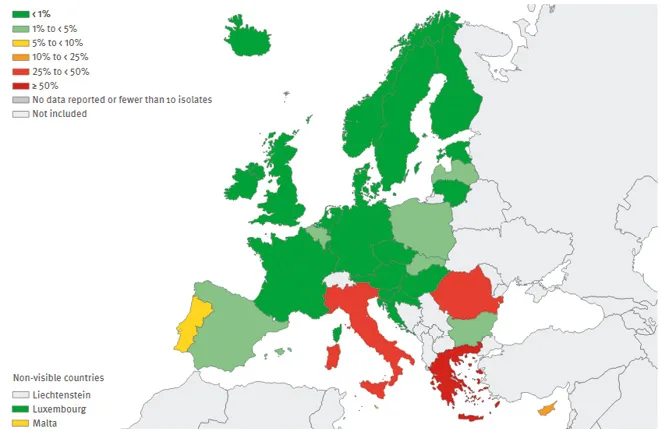
Les antibiotiques sont probablement les médicaments qui ont permis de sauver le plus de vies humaines. Malheureusement, leur utilisation massive a conduit à l’apparition de bactéries résistantes. Le cas actuellement le plus préoccupant est celui des entérobactéries – précisément en cause dans la majorité des infections du patient cirrhotique – avec la sélection de souches productrices de bêtalactamases à spectre étendu (EBLSE) [22]. Leur incidence est en augmentation constante depuis 15 ans pour certaines espèces comme E. coli et Klebsiella pneumoniae (Figure 2) qui deviennent ainsi résistantes aux C3G [23]. Plus menaçante encore est l’émergence de souches d’entérobactéries productrices de carbapénémases (EPC), encore rares – bien qu’en progression (Figure 3) – en France [24], mais dont l’incidence est déjà catastrophique dans certains pays européens comme l’Italie et la Grèce (Figure 4) [22].

Figure 2. Évolution de la résistance aux C3G de E. coli et K. pneumoniae de 2002 à 2016 en France. En 2002, elle était <1 %. Quinze ans plus tard, elle atteint 11,2 % pour E. coli et 28,9 % pour K. pneumoniae. Source : EARS-Net France [23].

Figure 3. Nombre d’épisodes impliquant des entérobactéries productrices de carbapénémases (EPC) par mois de signalement, France, 2004-2014.
Source : InVS-Raisin [24].

Figure 4. Klebsiella pneumoniae : pourcentage de souches résistantes aux carbapénèmes dans les infections invasives, 2016.
Source : ECDC [22]
Colonisation par des bactéries résistantes
La survenue d’une infection à bactérie résistante se fait habituellement en 2 temps (Figure 5). Il faut avoir été préalablement colonisé par cette bactérie. Les infections faisant immédiatement suite à une contamination sont beaucoup moins fréquentes. Deux facteurs vont concourir à cette colonisation : l’exposition aux antibiotiques et le séjour en établissement de santé [25].
Antibiotiques
Pression de sélection
+ effondrement de la résistance
à la colonisation| Contamination | ➡ | Colonisation | ➡ | Infection |
Pression de colonisation
Séjour en établissement de santé |
Figure 5. Phases de l’infection à BMR.
Pression de sélection
Un traitement antibiotique a pour but de détruire les bactéries pathogènes responsables d’une infection. Mais il a un effet secondaire constant qui est d’altérer les flores commensales (principalement digestive, mais également naso- et oro-pharyngée, bronchique, vaginale, et cutanée) du sujet traité. L’antibiotique va éliminer les bactéries sensibles, ne laissant survivre que les bactéries résistantes qui vont se multiplier et prendre la place de celles qui ont été éliminées. On parle de pression de sélection. La résistance peut être acquise par sélection d’un mutant résistant à l’antibiotique (résistance chromosomique) ou par transfert de matériel génétique mobile (plasmide, transposon) entre bactéries de même espèce ou d’espèces différentes (ces structures mobiles accumulant souvent des gènes de résistance vis-à-vis de plusieurs familles d’antibiotiques). Tous les antibiotiques sélectionnent. Il n’y a pas d’antibiothérapie « sans risque ».
Pression de colonisation
Dans l’environnement de tout un chacun, il y a peu de bactéries résistantes (encore que cela soit de moins en moins vrai). En revanche, elles sont particulièrement fréquentes dans les établissements de santé (hôpitaux, cliniques, SSR) qui concentrent les patients porteurs de bactéries résistantes et où l’environnement peut être contaminé par leurs excreta. Dans ces établissements (peu !) hospitaliers où les réservoirs et les vecteurs sont multiples, un patient est exposé à être colonisé par des bactéries résistantes. On parle de pression de colonisation. La transmission peut être croisée manuportée (par les soignants et les autres patients) ou indirecte (par les matériels et les surfaces). Cette pression de colonisation est d’autant plus forte que les germes résistants sont nombreux dans l’environnement, que les vecteurs sont multiples et que les règles d’hygiène sont mal respectées.
Effondrement de la résistance à la colonisation
Lorsqu’un patient hospitalisé reçoit un traitement antibiotique, son risque d’acquisition de bactéries résistantes s’en trouve démultiplié car, bien évidemment, les pressions de sélection et de colonisation s’associent, mais aussi, parce que sa résistance à la colonisation s’effondre. En effet, tant que le microbiote est préservé, les micro-organismes introduits par voie orale – entre autres, les bactéries résistantes – ont du mal à s’insérer et sont éliminés. En revanche, sous l’effet d’un traitement antibiotique, l’appauvrissement en espèces indigènes leur laisse le champ libre pour s’implanter et se développer. Ainsi, plus on prescrit d’antibiotiques et plus on les prescrit longtemps, plus le microbiote est altéré et plus il héberge des bactéries résistantes. Le phénomène est particulièrement marqué avec les antibiotiques à effet anti-anaérobies (C3G, amoxicilline-acide clavulanique, fluoroquinolones [FQ]) et/ou à élimination biliaire (ceftriaxone). Cette colonisation par des bactéries résistantes va perdurer plusieurs semaines à plusieurs mois après l’arrêt du traitement antibiotique.
Distinguer 3 (et non pas 2) catégories d’infection bactérienne
On distingue classiquement les infections communautaires (et on comprend par là : apparues en dehors de l’hôpital et habituellement sensibles aux antibiotiques usuels) et les infections nosocomiales (c’est-à-dire : survenues à l’hôpital et à haut risque de bactéries résistantes). Ce qui précède nous permet de comprendre que cette dichotomie est simpliste et inadaptée. Ainsi, un patient cirrhotique hospitalisé pour une infection apparue à son domicile, 1 mois après un premier séjour de 10 jours pour une hémorragie digestive durant lequel il a reçu une antibioprophylaxie par ceftriaxone, a très probablement été colonisé et a donc un risque augmenté d’infection à bactérie résistante. À l’évidence, il n’est pas possible de classer son infection dans l’une ou l’autre de ces deux catégories. Il faut donc en ajouter une troisième, que l’on appellera comme dans la littérature [3, 9] : infection associée aux soins (faute de mieux car, dans la terminologie officielle française, les infections associées aux soins englobent, de façon très large, tout évènement infectieux en rapport avec un processus, une structure, une démarche de soins, et donc les infections nosocomiales [26]). Cette troisième catégorie est caractérisée par un risque d’infection à bactérie résistante intermédiaire entre celui (faible) d’une infection communautaire et celui (élevé) d’une infection nosocomiale. Doivent y être rangées toutes les infections apparues en dehors d’un établissement de santé, mais chez un patient à haut risque d’avoir été colonisé par des bactéries résistantes, c’est-à-dire un patient ayant récemment reçu un traitement antibiotique et/ou été hospitalisé. (Tableau II).
| Nosocomiale | Infection se développant plus de 48h après l’admission |
| Associée aux soins | Infection présente à l’admission ou se développant dans les 48h suivant l’admission chez un patient ayant eu un contact avec le système de soins au cours des 3 mois précédents (hospitalisation, séjour en institution ou en maison de convalescence, hémodialyse) |
| Communautaire | Infection présente à l’admission ou se développant dans les 48h suivant l’admission en l’absence de contact avec le système de soins au cours des 3 mois précédents |
Tableau II. Catégories d’infection bactérienne.
Infections à bactéries résistantes et cirrhose
Études internationales
En 2002, Fernandez et al. ont publié une première étude prospective [2] sur les changements survenus dans l’épidémiologie des infections bactériennes du patient cirrhotique. Ils observaient alors deux modifications principales : d’une part, une augmentation de la fréquence des infections à CGP, en rapport avec l’augmentation des procédures invasives notamment en réanimation, et d’autre part, l’émergence des infections du liquide d’ascite à germes résistants aux quinolones chez les patients sous antibioprophylaxie au long cours par la norfloxacine. En revanche, à cette époque, seulement 1,2 % des infections à entérobactéries étaient résistantes au céfotaxime.
Dix ans plus tard, les choses avaient bien changé. Dans une deuxième étude publiée en 2012 [3], la même équipe faisait le constat de l’émergence rapide des infections à BMR. Les EBLSE en étaient la première cause, devant Pseudomonas aeruginosa, Staphylococcus aureus méti-R (SARM) et Enterococcus faecium. Ces infections à BMR étaient plus fréquentes en cas d’infection nosocomiale (35 %) qu’en cas d’infection associée aux soins (14 %) ou communautaire (4 %). Elles avaient une évolution plus sévère, caractérisée par la survenue plus fréquente d’un choc septique (26 vs 10 %) et une mortalité plus élevée (25 vs 12 %). Leurs facteurs prédictifs étaient l’origine nosocomiale de l’infection (HR 4,43), une antibioprophylaxie par quinolones (HR 2,69), un traitement par bêta-lactamines au cours des 3 derniers mois (HR 2,29) et une infection à BMR au cours des 6 derniers mois (HR 2,45).
De nombreuses études, prospectives et rétrospectives, ont confirmé ces données [27-30]. Sur tous les continents (Europe, Amérique, Asie), la prévalence des infections à BMR augmente. En corollaire, le taux d’échec de l’antibiothérapie classique basée sur les C3G augmente et la mortalité associée à ces infections est élevée. Ces infections à BMR sont associées, d’une part, au caractère nosocomial ou associé aux soins de l’infection, et d’autre part, à l’administration récente d’antibiotiques, qu’elle soit à visée curative ou prophylactique.
Ce que l’on observe chez les patients cirrhotiques n’est que le reflet de ce qui se passe dans la population générale. Partout sur la planète, l’antibiorésistance progresse. Pour autant, il est important de noter qu’il existe des différences importantes entre les pays [22]. Ainsi, en Europe en 2016, la proportion de SARM dans les infections invasives à S. aureus était de 1,2 % aux Pays-Bas, 10,3 % en Allemagne, 25,8 % en Espagne et 50,5 % en Roumanie. Pour ce qui est des souches d’E. coli résistantes aux C3G, leur taux atteignait 30 % en Italie quand il était inférieur à 10 % dans les pays scandinaves et en Angleterre. Enfin, dans la plupart des pays européens, moins de 1 % des souches de K. pneumoniae étaient résistantes aux carbapénèmes, contre 34 % en Italie et 67 % en Grèce.
Étude RESIST
Si l’on regarde maintenant la situation en France, en 2016, les taux de SARM, d’E. coli résistants aux C3G et de K. pneumoniae résistantes aux carbapénèmes étaient respectivement de 18,3 %, 11,2 % et 0,4 %. La résistance aux antibiotiques n’atteint donc pas dans notre pays la magnitude observée chez certains de nos voisins, comme l’Italie, la Grèce, ou les pays d’Europe de l’Est. Elle est cependant bien supérieure à celle des pays scandinaves, des Pays-Bas, et de l’Allemagne. Et encore la France n’a pas la résistance aux antibiotiques qu’elle « mériterait » en regard de la consommation qu’elle fait de ces médicaments (elle se situe au 3e rang européen pour la consommation antibiotique en ville et au 8e pour celle en milieu hospitalier). Cela s’explique peut-être par de bonnes mesures d’hygiène dans les hôpitaux et la mise en place de mesures d’isolement drastiques lors de toute infection ou colonisation par des BMR. Mais, quoiqu’il en soit, la situation française a des spécificités dont il faut tenir compte.
Il est également important de noter que les différences de consommation antibiotique et d’antibiorésistance observées au niveau national se prolongent au niveau régional (Figure 6) et au niveau local (Figure 7) [31].

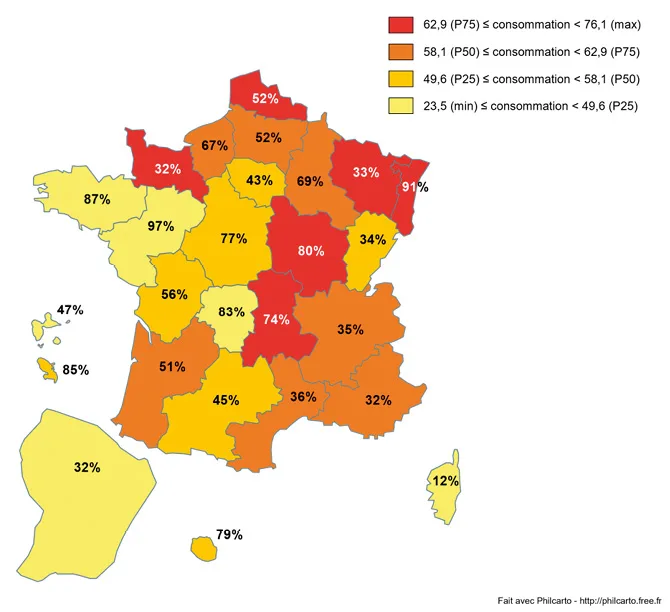
Figure 6. Consommation (taux global régional) de ceftriaxone en nombre de doses définies journalières (DDJ)/1000 journées d’hospitalisation (JH) en court séjour et couverture de lits (en %).
Carte réalisée à partir de données descriptives provenant d’établissements de santé (ES) volontaires dont les données de consommation en court séjour étaient disponibles. La participation n’est pas homogène d’une région à l’autre et le nombre d’ES inclus dans les analyses régionales est faible. Des différences dans l’activité des ES et le type de patients pris en charge peuvent expliquer une partie des variations observées. Source : INVS [31].

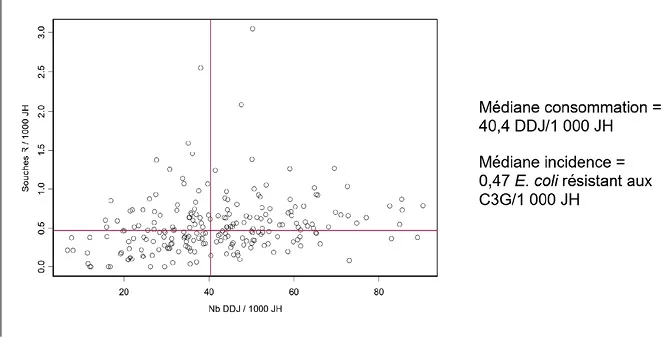
Figure 7. Consommation de céphalosporines de 3e génération (C3G) et incidence des souches d’E. coli résistant aux C3G dans les centres hospitaliers ayant plus de 33 % de lits de court séjour (N=224)
Les centres hospitaliers situés dans le quadrant inféro-gauche ont une faible consommation de C3Get une faible incidence d’E. coli résistant aux C3G. Ceux situés dans le quadrant inféro-droit ont une forte consommationde C3G,mais une incidence de résistance encore faible.En revanche, les centres hospitaliers situés dans les quadrants supérieurs ont une incidence de résistance élevée : ceux situés dans le quadrant supéro-gauche ont une consommation faible de C3G et doivent avant tout maîtriser la transmission croisée ; tandis que ceux situés dans le quadrant supéro-droit ont une consommation élevée de C3Get doivent tout à la fois réduire leur consommation de C3G et maîtriser la transmission croisée. Source : INVS [31].
Toutes les études internationales concernant des patients cirrhotiques proviennent de centres tertiaires et sont majoritairement monocentriques. Les données françaises sont peu nombreuses [32-34]. C’est ce qui nous a conduits à réaliser l’étude RESIST [5] qui est une étude observationnelle prospective multicentrique sur les infections à germes résistants chez les patients cirrhotiques hospitalisés pour une complication de leur maladie. Elle a impliqué 42 centres tertiaires et secondaires (14 CHU, 28 CHG) répartis sur tout le territoire français. De janvier à juin 2016, 1 093 patients ont été inclus dans cette étude. La prévalence des infections bactériennes était de 36,1 %. Elle était plus élevée dans les CHU que dans les CHG (46,2 % vs 29,1 %). Pour autant, les patients ne différaient pas entre les CHU et les CHG, que ce soit en termes de gravité de la cirrhose ou de fréquence des infections nosocomiales/associées aux soins. Les cultures étaient positives dans 63 % des cas, permettant d’isoler un total de 263 bactéries. Les BGN étaient prédominants (53 % vs 39 % pour les CGP). La sensibilité des bactéries aux C3G diminuait de 78 % pour les infections communautaires à 65 % pour les infections associées aux soins et à 57 % pour les infections nosocomiales (p<0,04), sans différence significative entre les CHU et les CHG. Il en était de même pour l’association amoxicilline-acide clavulanique et pour les FQ. Les BMR représentaient 14,3 % des bactéries isolées, sans différence entre les CHU et les CHG (14,2 % vs 14,4 %). Il s’agissait principalement d’EBLSE. Ces infections à BMR étaient plus fréquentes en cas d’infection nosocomiale (19 %) ou associée aux soins (20 %) qu’en cas d’infection communautaire (5 %). En analyse multivariée, le seul facteur prédictif d’infection à BMR était l’origine nosocomiale/associée aux soins de l’infection. Lorsque le clinicien jugeait l’antibiothérapie initiale inefficace, les taux de mortalité hospitalière et à 3 mois étaient respectivement de 41 % et de 59 %, vs 12 % et 27 % en cas d’antibiothérapie efficace.
Stratégie thérapeutique actuelle
Antibiothérapie
L’antibiothérapie probabiliste des infections bactériennes du patient cirrhotique a longtemps reposé sur les C3G qui couvraient la grande majorité des germes en cause tout en ayant une grande sécurité d’emploi. L’émergence des infections à BMR a changé la donne. En 2014, un groupe d’experts de l’EASL a formulé de nouvelles recommandations (Tableau III) [9]. Pour ce qui est des infections communautaires, l’antibiothérapie probabiliste reste basée sur les C3G (et l’amoxicilline-acide clavulanique). En revanche, pour les infections nosocomiales et certaines infections associées aux soins, il est maintenant recommandé de recourir d’emblée à une antibiothérapie à large spectre. Différentes stratégies antibiotiques ont été proposées en fonction de la prévalence des EBLSE et des SARM dans les centres.
| Type d’infection | Infections communautaires | Infections nosocomiales * |
|---|
Infection du liquide d’ascite
Bactériémie | céfotaxime
ou ceftriaxone
ou amoxicilline-acide clavulanique | pipéracilline/tazobactam 1
ou méropénème 2 ± glycopeptide 3 |
| Infection urinaire | En cas d’infection non compliquée :
ciprofloxacine
ou cotrimoxazole
En cas de sepsis :
céfotaxime
ou ceftriaxone
ou amoxicilline-acide clavulanique | En cas d’infection non compliquée :
nitrofurantoïne
ou fosfomycine
En cas de sepsis :
pipéracilline/tazobactam 1
ou méropénème 2 ± glycopeptide 3 |
| Pneumonie | amoxicilline-acide clavulanique
ou ceftriaxone + macrolide
ou levofloxacine
ou moxifloxacine | pipéracilline/tazobactam 1
ou
méropénème/ceftazidime+ciprofloxacine 4
± glycopeptide 5 |
| Infections des tissus mous | amoxicilline-acide clavulanique
ou ceftriaxone + oxacilline | méropénème/ceftazidime 4 + oxacilline
ou glycopeptide |
| * Également recommandé en cas d’infections urinaires et de pneumonies associées aux soins. Pour les infections du liquide d’ascite, les bactériémies et les infections des tissus mous associées aux soins, l’antibiothérapie probabiliste doit être décidée en fonction de la sévérité de l’infection (les patients présentant un sepsis sévère doivent recevoir le traitement proposé pour les infections nosocomiales). 1 dans les régions à faible prévalence de BMR 2 pour couvrir les entérobactéries BLSE 3 dans les régions à forte prévalence de SARM ou d’entérocoque vanco-S 4 pour couvrir Pseudomonas aeruginosa 5 si facteur de risque de SARM : pneumonie associée à la ventilation, antibiothérapie récente, portage nasal de SARM |
Tableau III. Recommandations EASL 2014 d’antibiothérapie probabiliste des infections bactériennes au cours de la cirrhose [9].
Les données de l’étude RESIST nous ont permis d’évaluer ces recommandations à partir de l’analyse des antibiogrammes des germes isolés (Tableau IV). Les C3G couvraient 90 % des germes isolés en cas d’infection communautaire. En revanche, ce pourcentage tombait à 67 % pour les infections associées aux soins et à 60 % pour les infections nosocomiales. La pipéracilline-tazobactam permettait d’élargir la couverture à 80 % des germes isolés en cas d’infection nosocomiale. De même, elle permettait de couvrir 88 % des germes isolés lors des infections associées aux soins. Hormis certaines infections nosocomiales, notamment en réanimation, on peut donc considérer qu’en France une antibiothérapie probabiliste basée sur l’association pipéracilline-tazobactam, en accord avec les recommandations EASL 2014, permet de couvrir la grande majorité des infections bactériennes associées aux soins et nosocomiales des patients cirrhotiques.
| Origine de l’infection | Taux de couverture avec l’antibiothérapie conventionnelle
Tous : C3G | Taux de couverture avec recommandations EASL 2014
Communautaires : C3G
Associées aux soins et nosocomiales : pipéracilline-tazobactam |
|---|
| Communautaire (n=51), % | 90,2 | 90,2 |
| Associée aux soins (n=43), % | 67,4 | 88,4 |
| Nosocomiale (n=40), % | 60 | 80 |
Tableau IV. Évaluation des recommandations EASL 2014 pour l’antibiothérapie probabiliste chez le patient cirrhotique à partir des données de l’étude RESIST.
Cette évaluation était basée sur les résultats de l’antibiogramme des germes isolés chez les patients ayant :
1) une infection classique (infection du liquide d’ascite, bactériémie, infection urinaire, pneumonie, infection des tissus mous) ;
2) un sepsis ;
et 3) une culture positive.
La prescription de l’antibiothérapie doit respecter les règles de bon usage et, en premier lieu, celle des 3 temps : évaluation initiale, réévaluation à 48-72 h, réévaluation à J5-J7 (Tableau V). L’évaluation initiale vise à réunir les arguments en faveur de l’existence d’une infection bactérienne, à déterminer son site, à la documenter sur le plan microbiologique, et in fine, à décider de l’indication d’une antibiothérapie probabiliste. Il faut absolument éviter les antibiothérapies inutiles, qu’il s’agisse d’un pic fébrile isolé, d’une infection virale, ou qu’elles soient à visée respiratoire (bronchite aiguë, infection pulmonaire incertaine), urinaire (bactériurie asymptomatique) ou cutanée (dermohypodermite non infectieuse).
| 1 Évaluation initiale en cas de suspicion d’infection bactérienne |
|---|
- Examen clinique complet à la recherche de signes locaux
- Dosage des marqueurs biologiques d’infection : leucocytes, CRP, procalcitonine
- Prélèvements bactériologiques systématiques (sang, urines, ascite), même s’ils ont déjà été faits récemment
Si la réalité de l’infection reste incertaine, évaluer l’état clinique du patient et le risque que lui ferait courir de laisser évoluer une infection :
– S’il est faible, surseoir à l’antibiothérapie, surveillance étroite, et réévaluation à 12-24 h (clinique, marqueurs biologiques)
– S’il est élevé, antibiothérapie probabiliste selon les recommandations EASL 2014 |
| 2 – Réévaluation systématique à 48-72 h |
|---|
– Infection confirmée (évolution clinique et biologique, résultats des cultures) :- poursuite de l’antibiothérapie
- en l’adaptant aux résultats de l’antibiogramme : choisir l’antibiotique ayant le spectre le plus étroit (désescalade thérapeutique)
– Infection non confirmée : - arrêt de l’antibiothérapie
|
| 3 – Réévaluation à J5-J7 |
|---|
| – Adapter la durée de l’antibiothérapie à l’évolution clinique : 7 jours sont suffisants dans la majorité des cas (5 jours en cas d’infection du liquide d’ascite sans signe de sepsis) |
Tableau V. Bon usage des antibiotiques : la règle des 3 temps.
Si une C3G est prescrite, il est préférable de choisir le céfotaxime. En effet, l’impact des antibiotiques sur le microbiote anaérobie ne dépend pas exclusivement de l’étendue de leur spectre bactérien. Les antibiotiques à excrétion biliaire favorisent la colonisation du microbiote par les EBLSE. Cela a été bien démontré pour la ceftriaxone [35, 36]. Par ailleurs, les infections à anaérobies étant rares chez le patient cirrhotique, il est inutile de vouloir les couvrir par une prescription associée de métronidazole.
Une première réévaluation doit être faite à 48-72 h. Si l’infection n’a pas été confirmée, l’antibiothérapie doit être arrêtée. En revanche, si les cultures sont positives, il faut désescalader si l’antibiogramme le permet, c’est-à-dire remplacer l’antibiotique initialement prescrit par un antibiotique couvrant également le germe mais ayant un spectre plus étroit. L’objectif étant de réduire les pressions de sélection et de colonisation exercées sur le microbiote du patient tout en conservant l’efficacité du traitement.
Enfin une deuxième réévaluation doit être faite à J5-J7 pour apprécier l’évolution de l’infection sous traitement et déterminer la durée de celui-ci. Dans la majorité des cas, un traitement de 7 jours est suffisant. Il peut même être réduit à 5 jours en cas d’infection du liquide d’ascite sans sepsis associé.
Utilisation de l’albumine
L’intérêt des perfusions d’albumine est bien démontré dans les infections du liquide d’ascite. Elles permettent de réduire l’incidence du syndrome hépatorénal et la mortalité [37]. Toutefois, seuls les patients les plus graves (bilirubine 70 µmol/l et/ou créatinine 90 µmol/l) en tirent un réel bénéfice [38]. En ce qui concerne les autres infections bactériennes, deux études réalisées chez des malades non sélectionnés se sont révélées négatives [39, 40].
Et demain ?
L’avenir est peut-être sombre. Les perspectives en termes de nouveaux antibiotiques sont plus que réduites, les situations d’impasse thérapeutique devraient se multiplier, et l’OMS s’en est récemment alarmée [41]. Pour préserver et mieux utiliser les antibiotiques dont nous disposons, plusieurs axes de recherche ont été proposés [9] : développer des stratégies prophylactiques non antibiotiques ; trouver des biomarqueurs plus efficaces pour le diagnostic précoce d’infection bactérienne et du pathogène responsable ; restaurer la fonction immunitaire du patient cirrhotique et protéger ses organes contre la dysfonction induite par l’infection. Mais cela demandera du temps. En attendant, que faire ? La situation de l’Italie interroge. Alors que ce pays est confronté à des niveaux de résistance bactérienne quasi sans équivalents en Europe, des équipes italiennes publient des études encourageant la prescription d’antibiothérapie probabiliste à très large spectre chez les patients cirrhotiques [42, 43] en le justifiant par des arguments économiques [44]. Ailleurs, en Espagne, on réfléchit à prévenir les infections bactériennes du patient cirrhotique par une décontamination intestinale à la colistine. Fuite en avant ? Il semble que tout cela ne puisse que conduire à la multiplication des souches de bactéries multi-, hautement – et pan-résistantes.
Conclusion
Les patients ayant une cirrhose évoluée sont à haut risque de développer des infections bactériennes. Le diagnostic de ces infections est parfois difficile car des signes importants comme la fièvre peuvent manquer et leur expression peut se résumer à une altération de l’état général ou à une encéphalopathie. Leur évolution peut cependant être rapide vers une ACLF ou un choc septique, et leur mortalité est élevée dès lors que la prise en charge est tardive et que l’antibiothérapie initialement prescrite n’est pas adaptée. L’émergence des infections à BMR nous amène à changer nos stratégies thérapeutiques et à prescrire d’emblée une antibiothérapie probabiliste à large spectre en cas d’infection nosocomiale ou associée aux soins. Ne pas le faire serait une perte de chance pour nos patients.
Pour autant, il existe une autre forme de perte de chance pour le patient, bien moins visible, mais tout aussi réelle. Celle qui consisterait à être hospitalisé dans un service hospitalier où les germes résistants seraient multiples dans l’environnement, où les mesures d’hygiène seraient mal respectées, où des cures d’antibiotiques inutiles et/ou prolongées lui seraient prescrites. Tout cela augmenterait pour lui la probabilité d’être colonisé, puis de développer une infection à BMR pour laquelle l’antibiothérapie pourrait être en échec, avec en corollaire une morbidité et une mortalité élevées. De cela aussi, nous devons être particulièrement soucieux.
La progression de l’antibiorésistance n’est pas une fatalité. Il n’y a qu’à voir comment elle diffère selon les pays et les régions, les établissements de santé et les services hospitaliers, pour comprendre qu’elle dépend en partie de nos comportements. Déclencher une antibiothérapie à la moindre suspicion et, en tout cas, ne pas la réévaluer à 24-48h, n’est pas raisonnable. Certes, les infections bactériennes sont fréquentes et potentiellement graves chez le patient cirrhotique. Certes, l’émergence des BMR rend leur traitement plus complexe et il faut parfois maintenant recourir d’emblée à une antibiothérapie probabiliste à large spectre. Mais, dans le contexte actuel de développement rapide de l’antibiorésistance et de quasi absence de perspective en matière de nouveaux antibiotiques, l’essentiel n’est peut-être pas là. Outre la prévention de ces infections, il importe d’essayer de limiter la colonisation de nos patients par des BMR agissant à deux niveaux : sur la pression de sélection, par un bon usage des antibiotiques, et sur la pression de colonisation, par un strict respect des mesures d’hygiène. Cela afin d’éviter de « pourrir » leur microbiote par des BMR et des BHR … Ce qui, à des hépato gastroentérologues, pourrait apparaître comme la moindre des choses.
Remerciements : L’auteur remercie vivement les Drs Amélie Carrër-Causeret, Gabriela Chitic, Karine Gourlain, Abdelkrim Medini et Agathe Simo pour leur relecture du texte, leurs remarques et leurs suggestions.
Références
- Gustot T, Fernandez J, Szabo G, et al. Sepsis in alcohol-related liver disease. J Hepatol 2017;67:1031-1050.
- Fernandez J, Navasa M, Gomez J, et al. Bacterial infections in cirrhosis: epidemiological changes with invasive procedures and norfloxacin prophylaxis. Hepatology 2002;35:140-8.
- Fernandez J, Acevedo J, Castro M, et al. Prevalence and risk factors of infections by multiresistant bacteria in cirrhosis: a prospective study. Hepatology 2012;55:1551-61.
- Merli M, Lucidi C, Giannelli V, et al. Cirrhotic patients are at risk for health care-associated bacterial infections. Clin Gastroenterol Hepatol 2010;8:979-85.
- Pauwels A, Meunier L, Boivineau G, et al. Resistant bacterial infections in cirrhosis: a French observational prospective multicentre nationwide study (RESIST study). J Hepatol 2017;66:S131-S132.
- Fernandez J, Acevedo J, Wiest R, et al. Bacterial and fungal infections in acute-on-chronic liver failure: prevalence, characteristics and impact on prognosis. Gut 2017.
- Arvaniti V, D’Amico G, Fede G, et al. Infections in patients with cirrhosis increase mortality four-fold and should be used in determining prognosis. Gastroenterology 2010;139:1246-1256.
- D’Amico G, Garcia-Tsao G, Pagliaro L. Natural history and prognostic indicators of survival in cirrhosis: a systematic review of 118 studies. J Hepatol 2006;44:217-31.
- Jalan R, Fernandez J, Wiest R, et al. Bacterial infections in cirrhosis: a position statement based on the EASL Special Conference 2013. J Hepatol 2014;60:1310-24.
- Bernard B, Grange JD, Khac EN, et al. Antibiotic prophylaxis for the prevention of bacterial infections in cirrhotic patients with gastrointestinal bleeding: a meta-analysis. Hepatology 1999;29:1655-61.
- Fernandez J, Ruiz del Arbol L, Gomez C, et al. Norfloxacin vs ceftriaxone in the prophylaxis of infections in patients with advanced cirrhosis and hemorrhage. Gastroenterology 2006;131:1049-56; quiz 1285.
- de Franchis R. Expanding consensus in portal hypertension: Report of the Baveno VI Consensus Workshop: Stratifying risk and individualizing care for portal hypertension. J Hepatol 2015;63:743-52.
- Pauwels A, Mostefa-Kara N, Debenes B, et al. Systemic antibiotic prophylaxis after gastrointestinal hemorrhage in cirrhotic patients with a high risk of infection. Hepatology 1996;24:802-6.
- Gines P, Rimola A, Planas R, et al. Norfloxacin prevents spontaneous bacterial peritonitis recurrence in cirrhosis: results of a double-blind, placebo-controlled trial. Hepatology 1990;12:716-24.
- Fernandez J, Navasa M, Planas R, et al. Primary prophylaxis of spontaneous bacterial peritonitis delays hepatorenal syndrome and improves survival in cirrhosis. Gastroenterology 2007;133:818-24.
- Thevenot T, Degand T, Grelat N, et al. A French national survey on the use of antibiotic prophylaxis in cirrhotic patients. Liver Int 2013;33:389-97.
- Miozzo SA, Tovo CV, John JA, et al. Proton pump inhibitor use and spontaneous bacterial peritonitis in cirrhosis: An undesirable association? J Hepatol 2015;63:529-30.
- Dam G, Vilstrup H, Watson H, et al. Proton pump inhibitors as a risk factor for hepatic encephalopathy and spontaneous bacterial peritonitis in patients with cirrhosis with ascites. Hepatology 2016;64:1265-72.
- Nahon P, Lescat M, Layese R, et al. Bacterial infection in compensated viral cirrhosis impairs 5-year survival (ANRS CO12 CirVir prospective cohort). Gut 2017;66:330-341.
- Anty R, Tonohouan M, Ferrari-Panaia P, et al. Low Levels of 25-Hydroxy Vitamin D are Independently Associated with the Risk of Bacterial Infection in Cirrhotic Patients. Clin Transl Gastroenterol 2014;5:e56.
- Finkelmeier F, Kronenberger B, Zeuzem S, et al. Low 25-Hydroxyvitamin D Levels Are Associated with Infections and Mortality in Patients with Cirrhosis. PLoS One 2015;10:e0132119.
- ECDC. Surveillance of antimicrobial resistance in Europe. Surveillance report 2016. www.ecdc.europa.eu.
- EARS-Net France. Synthèse 2002-2016. Contribution de la France au réseau européen de surveillance de la résistance microbienne aux antibiotiques. http://invs.santepubliquefrance.fr//ratb/EARS.
- INVS et ANSM. Consommation d’antibiotiques et résistance aux antibiotiques en France : nécessité d’une mobilisation déterminée et durable. Bilan des données de surveillance. 15 novembre 2015. http://www.invs.sante.fr.
- Lepelletier D, Caroff N, Riochet D, et al. Risk-factors for gastrointestinal colonisation with resistant Enterobacteriaceae among hospitalised patients: a prospective study. Clin Microbiol Infect 2006;12:974-9.
- CTINILS. Actualisation de la définition des infections nosocomiales. Ministère de la Santé, de la Jeunesse et des Sports, mai 2007.
- Ariza X, Castellote J, Lora-Tamayo J, et al. Risk factors for resistance to ceftriaxone and its impact on mortality in community, healthcare and nosocomial spontaneous bacterial peritonitis. J Hepatol 2012;56:825-32.
- Cheong HS, Kang CI, Lee JA, et al. Clinical significance and outcome of nosocomial acquisition of spontaneous bacterial peritonitis in patients with liver cirrhosis. Clin Infect Dis 2009;48:1230-6.
- Merli M, Lucidi C, Di Gregorio V, et al. The spread of multi drug resistant infections is leading to an increase in the empirical antibiotic treatment failure in cirrhosis: a prospective survey. PLoS One 2015;10:e0127448.
- Tandon P, Delisle A, Topal JE, et al. High prevalence of antibiotic-resistant bacterial infections among patients with cirrhosis at a US liver center. Clin Gastroenterol Hepatol 2012;10:1291-8.
- INVS. Surveillance de la consommation des antibiotiques. Réseau ATB-Raisin. Résultats 2014. http://www.invs.sante.fr.
- Bert F, Andreu M, Durand F, et al. Nosocomial and community-acquired spontaneous bacterial peritonitis: comparative microbiology and therapeutic implications. Eur J Clin Microbiol Infect Dis 2003;22:10-5.
- Piroth L, Pechinot A, Minello A, et al. Bacterial epidemiology and antimicrobial resistance in ascitic fluid: a 2-year retrospective study. Scand J Infect Dis 2009;41:847-51.
- Piroth L, Pechinot A, Di Martino V, et al. Evolving epidemiology and antimicrobial resistance in spontaneous bacterial peritonitis: a two-year observational study. BMC Infect Dis 2014;14:287.
- Grohs P, Kerneis S, Sabatier B, et al. Fighting the spread of AmpC-hyperproducing Enterobacteriaceae: beneficial effect of replacing ceftriaxone with cefotaxime. J Antimicrob Chemother 2014;69:786-9.
- Muller A, Lopez-Lozano JM, Bertrand X, et al. Relationship between ceftriaxone use and resistance to third-generation cephalosporins among clinical strains of Enterobacter cloacae. J Antimicrob Chemother 2004;54:173-7.
- Sort P, Navasa M, Arroyo V, et al. Effect of intravenous albumin on renal impairment and mortality in patients with cirrhosis and spontaneous bacterial peritonitis. N Engl J Med 1999;341:403-9.
- Sigal SH, Stanca CM, Fernandez J, et al. Restricted use of albumin for spontaneous bacterial peritonitis. Gut 2007;56:597-9.
- Guevara M, Terra C, Nazar A, et al. Albumin for bacterial infections other than spontaneous bacterial peritonitis in cirrhosis. A randomized, controlled study. J Hepatol 2012;57:759-65.
- Thevenot T, Bureau C, Oberti F, et al. Effect of albumin in cirrhotic patients with infection other than spontaneous bacteriperitonitis. A randomized trial. J Hepatol 2015;62:822-30.
- WHO. Global priority list of antibiotic-resistant bacteria to guide research, discovery and development of new antibiotics. Février 2017. www.who.int.
- Merli M, Lucidi C, Di Gregorio V, et al. An empirical broad spectrum antibiotic therapy in health-care-associated infections improves survival in patients with cirrhosis: A randomized trial. Hepatology 2016;63:1632-9.
- Piano S, Fasolato S, Salinas F, et al. The empirical antibiotic treatment of nosocomial spontaneous bacterial peritonitis: Results of a randomized, controlled clinical trial. Hepatology 2016;63:1299-309.
- Lucidi C, Di Gregorio V, Ceccarelli G, et al. A cost analysis of a broad-spectrum antibiotic therapy in the empirical treatment of health care-associated infections in cirrhotic patients. Clinicoecon Outcomes Res 2017;9:385-390.