Lien d’intérêt
L’auteur déclare n’avoir aucun lien d’intérêt en rapport avec sa communication
Mots-clés
Maladie de Crohn, fistules anales, anti-TNF alpha, cellules souches
Introduction
Définitions
Les LAP de la maladie de Crohn se définissent comme l’ensemble des lésions liées à la MC qui touchent le canal anal, le périnée, le bas rectum et la cloison recto-vaginale. Les lésions primaires correspondent à l’atteinte élémentaire de la maladie de Crohn, sous forme d’ulcération de la muqueuse du bas rectum ou du canal anal.
Ces lésions peuvent se compliquer de processus suppuratifs (fistules et abcès), de marisques et de sténoses. Les lésions non primaires sont dites « secondaires ».
Bien que les fistules compliquent souvent un ulcère creusant, il n’existe pas de lien chronologique prouvé entre lésion primaire et secondaire. En effet une lésion suppurative peut être inaugurale de la maladie et les ulcérations ne compliquent les fistules que dans 50 % des cas (1). Il est en revanche rare de découvrir la maladie au stade de sténose anale car elles apparaissent souvent après une phase d’activité inflammatoire prolongée.
Épidémiologie et conséquences des lésions ano-périnéales
On considère qu’un patient sur quatre porteur d’une maladie de Crohn développera une atteinte ano-périnéale au décours du suivi évolutif de sa maladie (2). Cependant, l’atteinte peut être inaugurale, voire précéder le diagnostic de plusieurs années (3). La maladie fistuleuse est considérée complexe dans 50 à 80 % des cas (4-6), rendant celle-ci plus difficile à traiter avec un risque de récidive dans 40 % des cas à 10 ans.
Douleurs et suintements sont les plaintes les plus fréquentes. La mise en place d’un séton est un facteur péjoratif des scores de qualité de vie (7).
Les études montrent une fréquence élevée de troubles de continence. Elle est significativement plus élevée chez les malades porteurs de maladie inflammatoire intestinale avec LAP (deux patients sur trois) que chez les malades sans LAP (un patient sur deux) selon une enquête menée sur plus de 1 000 patients (8). Selon ce même travail, 15 % des patients dans le groupe LAP sont porteurs de stomie.
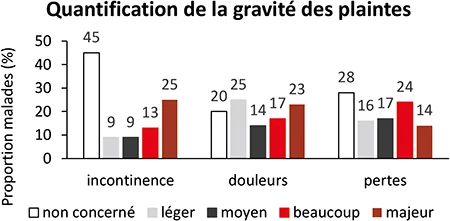
Ainsi, les LAP constituent un réel fardeau pour les patients d’autant plus qu’elles affectent la qualité de vie des malades dans toutes ses dimensions, y compris sexuelle, et réduisent le nombre de grossesses chez les patientes (9). Les trois quarts des malades porteur d’une maladie fistuleuse anopérinéale ont des manifestations dépressives et 13 % des idées suicidaires (10). (figure 1)

Figure 1 : Quantification des plaintes secondaires aux LAP, enquête portant sur 69 patients (7)
Classifications des LAP
La définition des LAP a donné lieu à la classification de Cardiff (dite UFS) qui permet de classer simplement les lésions selon leur type (Ulcération, Fistule, Sténose) et leur sévérité. Cette classification dans sa version simplifiée offre le principal avantage d’être très facile d’utilisation en routine. (tableau 1)
Tableau 1 : Classification UFS selon Hughes (11) simplifiée
| Ulcération | Fistule | Sténose |
|---|
| 0 | Absente | Absente | Absente |
| 1 | Superficielle | Fistule simple | Réversible (spasme, diaphragme ou induration lié aux phénomènes suppuratifs) |
| 2 | Creusante | Fistule complexe | Irréversible (sténose longue et fibreuse) |
Plusieurs classifications peuvent alors être utilisées. La classification de Parks (12) localise le trajet fistuleux principal par rapport à l’appareil sphinctérien. Cette classification est anatomique mais finalement relativement schématique et ne correspond pas toujours à la réalité clinique. Elle ne prend pas en compte les trajets secondaires ni les fistules en fer à cheval. La classification de Arnous (13) s’attache quant à elle à évaluer la hauteur du trajet fistuleux par rapport à l’appareil sphinctérien.
En pratique, on peut généralement retenir deux situations principales avec un impact thérapeutique et pronostic très différents et qui consistent à différencier les fistules selon leur caractère simple ou complexe.
Une fistule simple est caractérisée par un trajet unique, superficiel, trans-sphinctérien bas ou inter-sphinctérien bas, avec un seul orifice externe, non abcédée et sans lésion rectale active ou sténose anorectale. Celles-ci sont généralement accessibles à un geste chirurgical simple (fistulotomie directe).
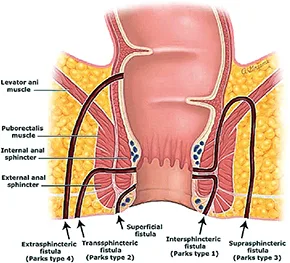
Toute fistule qui ne rentre pas dans ce cadre-là devient a fortiori complexe : fistules à trajets multiples ou ramifiés, fer à cheval, fistule en Y, fistules profondes, hautes (inter-sphinctérienne, trans-sphinctérienne, supra- ou extra-sphinctérienne, recto- ou ano-vaginale). La prise en charge chirurgicale de ces lésions est rendue plus souvent délicate. (figures 2A et 2B)

Figure 2 A : Classification des fistules selon Parks (12)

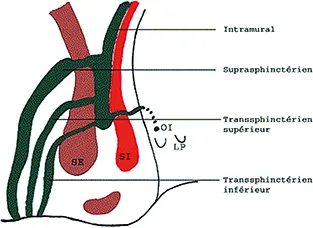
Figure 2 B : Classification des fistules selon Arnous (13)
Outils d’évaluation des lésions ano-périnéales
Quantification des symptômes
La quantification des plaintes exprimées par les malades peut être évaluée à l’aide du score PDAI (Perineal Disease Activity Index) (14). Il permet grâce à 5 paramètres cliniques simples de quantifier la maladie sur une échelle de 0 à 20. Ce score est simple et rapide à calculer en consultation, et permettra d’évaluer la réponse clinique au traitement. (tableau 2)
Tableau 2 : Quantification des plaintes selon le score PDAI (14)
| Suintement/écoulement |
|---|
| 0 = Aucun 1 = Minime suintement muqueux 2 = Suintement muqueux ou puriforme modéré 3 = Suintement important 4 = Écoulement fécal important |
| Douleur/limitation des activités |
|---|
| 0 = Aucune 1 = Inconfort modéré, pas de limitation des activités 2 = Inconfort moyen, limitation des activités 3 = Inconfort marqué, limitation partielle des activités 4 = Douleur importante, limitation importante |
| Limitation des activités sexuelles |
|---|
| 0 = Aucune 1 = Restriction légère 2 = Limitation modérée 3 = Limitation marquée 4 = Activité sexuelle impossible |
| Type d’atteinte périnéale |
|---|
| 0 = Aucune ou simples marisques 1 = Fissure ou coupure anale 2 = <3 fistules anales 3 = ≥3 fistules anales 4 = Ulcération atteignant le sphincter anal ou fistule avec important décollement cutané |
| Degré d’induration |
|---|
| 0 : Aucune 1 : Induration minime 2 : Induration modérée 3 : Induration importante 4 : Zone fluctuante/abcès |
Description des lésions
Par l’examen clinique
La complexité d’un trajet fistuleux peut être appréciée lors de l’examen proctologique. On évalue le nombre d’orifices externes et leur distance par rapport à la marge anale. Un trajet éloigné de l’orifice anal est plus souvent associé à un trajet dont le point de départ est haut situé. La palpation d’un trajet fistuleux sous forme d’un cordon partant de l’orifice externe en direction de l’anus témoigne généralement d’un trajet superficiel alors que l’induration de la sangle du releveur au toucher anorectal est plus en faveur d’un trajet profond.
Bien que l’examen sous anesthésie générale et la dissection chirurgicale du trajet fistuleux soient généralement suffisants à classifier les fistules, l’apport de l’imagerie est à l’heure actuelle devenu une aide incontournable pour aider le praticien dans son évaluation en particulier en préopératoire. Elle offre l’avantage de guider le chirurgien dans son geste chirurgical en particulier pour les trajets profonds.
Par échographie endo-anale
De réalisation rapide, elle peut être faite au décours de la consultation mais sera de réalisation difficile chez un patient douloureux voire impossible en présence d’une sténose. Elle peut être couplée à l’examen clinique sous anesthésie en cas de geste chirurgical.
Sa précision diagnostique pour les LAP de Crohn est évaluée entre 56 et 100 % avec, comparativement à l’IRM, une moins bonne définition des trajets fistuleux secondaires mais une meilleure détection des orifices internes (15,16).
Par Imagerie par Résonnance Magnétique (IRM)
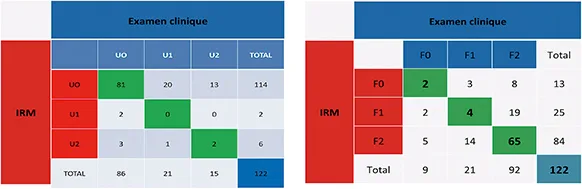
L’IRM permet de façon non invasive de bien visualiser les trajets fistuleux, leurs diverticules et les petits abcès profonds qui échappent parfois au chirurgien lors de son intervention. Une analyse comparative du classement des ulcérations et des fistules selon qu’il soit réalisé par un examen clinique ou lors d’une exploration IRM a montré que l’examen clinique est moins performant pour le diagnostic des fistules anales. Il sous-estime la complexité des fistules dans 25 % des cas et surestime les fistules simples dans 75 % des cas. Finalement, la concordance n’est présente que dans un peu plus de la moitié des cas. En ce qui concerne les ulcérations, 95 % des ulcérations superficielles et 87 % des ulcérations profondes n’ont pas été visualisées par l’IRM. Aucune sténose anale n’a été diagnostiquée par l’IRM (17). Ainsi, si l’IRM offre une meilleure sensibilité que l’examen clinique dans la description topographique des trajets fistuleux et notamment profonds, elle peut en revanche être mise en défaut pour les ulcérations souvent identifiées à tort comme des trajets superficiels ou inter sphinctériens.
Au final, la combinaison d’une IRM et d’un examen clinique sous anesthésie permet d’obtenir une sensibilité et une spécificité de l’ordre de 100 %. L’IRM est recommandée pour la prise en charge des lésions fistuleuses périnéales de Crohn par le consensus français et européen (18-19). (figures 3 et 4)

Figure 3 : Analyse comparative du classement de sévérité des ulcérations et des fistules anales de Crohn selon qu’il soit réalisé par un simple examen clinique ou lors d’une exploration IRM (17)

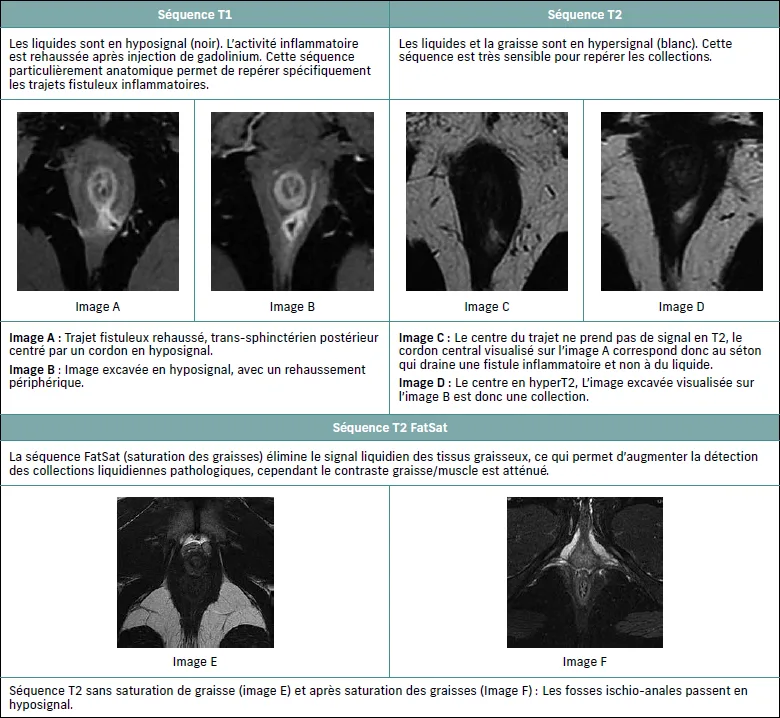
Figure 4 : Mémo pour la lecture de clichés d’IRM pelvienne
Quelles stratégies thérapeutiques « classiques » dans les LAP de Crohn à l’heure actuelle ?
La prise en charge doit s’envisager dans l’urgence en cas d’abcès, mais également à plus long terme avec pour objectif d’épargner la fonction sphinctérienne et de cicatriser la maladie périnéale.
La base du traitement, dans la majorité des cas, est une combinaison d’un traitement médical et chirurgical faisant appel à un travail de collaboration entre le gastro-entérologue, le proctologue et/ou le chirurgien.
Traitements des lésions ano-périnéales primaires : ulcérations
La prise en charge de ces lésions est mal codifiée mais est en règle générale médicale. Il faut éviter d’opérer une ulcération anale dans un contexte de maladie de Crohn, sauf dans le cas particulier de fissure « classique » chez un malade en rémission.
L’évolution des ulcérations anales étant souvent parallèle à celle de la maladie luminale, le traitement global de la maladie a souvent un effet favorable sur ce type de lésions ano-périnéales.
50 % des ulcérations superficielles guérissent spontanément (20) mais elles peuvent également s’aggraver et conduire à des sténoses, des fistules et des abcès, ce qui rend la décision thérapeutique médicale parfois difficile. Ainsi, en cas d’ulcérations sévères et menaçantes (lésions larges, creusantes, ou délabrantes), la décision est généralement plus facile et doit faire appel d’emblée à une biothérapie.
Traitements locaux
L’application de pommades cicatrisantes améliore souvent les symptômes mais n’est pas suffisante pour permettre une cicatrisation des lésions.
Les topiques à base de tacrolimus ont montré une amélioration des lésions sans obtenir toutefois une cicatrisation complète, de même que les antibiotiques (métronidazole en topique ou ovule) qui ne permettent généralement qu’une amélioration modérée avec un effet suspensif.
Parmi les traitements systémiques :
- Les corticoïdes et les salicylés sont inefficaces dans cette indication.
- L’azathioprine n’a pas été spécifiquement étudiée dans le traitement des LAP primaires, néanmoins, les thiopurines sont utilisées en traitement d’entretien à partir de données rétrospectives. Leur efficacité reste débattue et la cicatrisation est attendue dans moins de la moitié des cas.
- L’infliximab n’a pas été évalué prospectivement dans les LAP primaires de Crohn. Les données de cohortes rétrospectives montrent que les ulcérations cicatrisent lentement dans environ 1 cas sur deux à deux ans, mais le bénéfice d’un traitement anti-TNF alpha associé n’est pas prouvé (20).
Ainsi, bien que les biothérapies n’aient pas l’AMM dans l’indication des LAP non fistuleuses, les patients présentant des ulcérations sévères, symptomatiques et dont le risque de fistulisation semble maximal, doivent bénéficier malgré tout d’un traitement par anti-TNF alpha rapidement.
Traitements des lésions fistuleuses
Les traitements des fistules périnéales au cours de la maladie de Crohn sont multiples, médicaux et/ ou chirurgicaux. Aucun n’est parfaitement efficace et il existe toujours un risque de récidive de la maladie. En conséquence, il est important de préserver l’architecture de l’appareil sphinctérien en évitant les chirurgies mutilantes et répétées faisant courir un risque accru d’incontinence.
Dans le cas particulier des localisations ano-périnéales, les critères décisionnels ne reposent pas toujours sur des études contrôlées, mais sur la synthèse de consensus d’experts. Le consensus retenu est d’abord de drainer une suppuration si elle existe, puis de contrôler la maladie inflammatoire rapidement.
Traitement chirurgical
En présence d’un abcès, le premier geste thérapeutique doit être son évacuation sans délai afin de soulager le patient et d’éviter toute extension de la suppuration. Les antibiotiques (métronidazole, ciprofloxacine) peuvent être utilisés mais en aucun cas suffisants.
L’incision d’un abcès peut être effectuée sous anesthésie locale en cas d’abcès facilement accessible et peu profond. Il doit être réalisé sous anesthésie générale dans les autres cas. La fistule à l’origine de l’abcès doit être drainée sur séton non serré dans le même temps opératoire afin de limiter le risque de récidive rapide. (figure 5)
Le séton est laissé en place a minima jusqu’à disparition des phénomènes inflammatoires locaux. La récidive de l’abcès est fréquente à l’ablation du drain, c’est pourquoi un traitement de fond de la maladie doit être mis en place afin de contrôler la maladie luminale et périnéale.
Lorsque la fistule est simple et asymptomatique, aucun geste chirurgical n’est nécessaire. Le traitement médical peut être débuté sans drainage préalable en prenant de soin de surveiller l’apparition de signes inflammatoires locaux.

Figure 5 : Mise en place d’un séton de drainage, noué sans tension, dans une fistule anale
Traitements médicaux
Les antibiotiques seuls (métronidazole et ciprofloxacine) n’ont, qu’un effet suspensif temporaire sur les symptômes et leur utilisation prolongée peut être à l’origine d’effets secondaires (neuropathie périphérique, ruptures tendineuses). Les immunosuppresseurs seuls n’ont de leur côté pas prouvé leur efficacité (21).
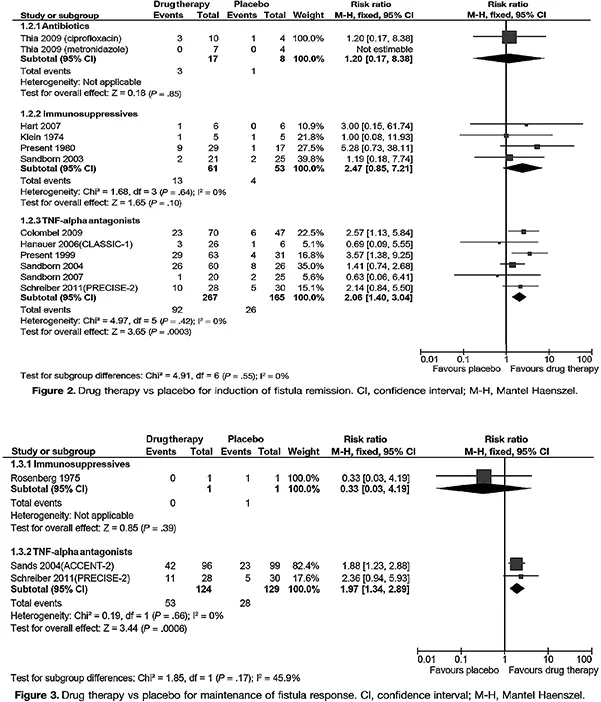
Le traitement de première intention repose alors sur les biothérapies (anti-TNF alpha) et en particulier l’infliximab car on dispose de quelques essais dédiés et d’analyse des sous-groupes de grands essais cliniques qui montrent avec un bon niveau de preuve que ces traitements permettent d’obtenir un meilleur tarissement des trajets fistuleux drainés que le placebo. Les effectifs restent faibles, mais ceux-ci sont regroupés dans une méta-analyse (21). Le bénéfice thérapeutique initial semble se maintenir à l’occasion du traitement d’entretien. Le bénéfice serait environ 2 fois supérieur au placebo, bien qu’un malade sur trois seulement soit cicatrisé à un an. (figure 6)

Figure 6 : Méta-analyse relatant l’efficacité des traitements médicaux des lésions fistuleuses de Crohn (21)
Peut-on optimiser la réponse ?
Combothérapie
Il n’y a pas eu d’essais randomisés dédiés comparant spécifiquement l’utilisation d’un traitement anti-TNF en association avec un traitement immunosuppresseur à une monothérapie anti-TNF.
Les analyses de sous-groupes des grands essais comparant l’infliximab en mono ou en combothérapie face au placebo dans la maladie de Crohn n’ont pas montré de différence entre ces deux régimes de traitement dans la cicatrisation des lésions fistuleuses de Crohn (22). Le faible effectif des sous-groupes peut aussi être source de manque de puissance statistique. Deux études rétrospectives ont enrôlé un plus grand nombre de patients et sur un suivi à plus long terme ont montré que la combothérapie était associé à un meilleur taux de fermeture des fistules (23,24).
Cette différence peut s’expliquer par l’effet connu des immunomodulateurs sur la réduction de l’immunogénicité et donc sur l’augmentation des taux résiduels d’IFX, et du fait que des taux plus élevés d’anti-TNF ont été associés à une meilleure réponse dans la maladie de Crohn.
En pratique, la combothérapie est actuellement le traitement le plus adapté aux patients présentant une maladie de Crohn périnéale. Cette pratique a été validée par la plupart des autres sociétés (25,26) y compris le consensus français (19), mais pas par l’ECCO (18).
Intérêt des dosages des taux résiduels d’anti-TNF
Plusieurs études rétrospectives et observationnelles ont identifié une association entre des niveaux sériques plus élevés d’infliximab et la réponse thérapeutique (27,28). Bien que le niveau seuil d’infliximabémie varie d’une étude à l’autre, il semble que la cible soit supérieure à celle qui est classiquement utilisée pour contrôler la maladie de Crohn luminale.

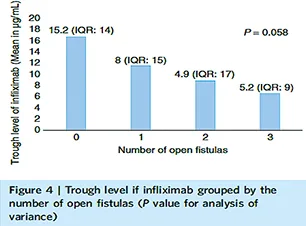
Figure 7 : L’infliximabémie est inversement proportionnelle au nombre d’orifices fistuleux (33)
Le dosage d’infliximab est significativement plus élevé dès la deuxième semaine de traitement chez les patients porteurs de maladie de Crohn périnéale en rémission à la semaine 14 (29) ; et le nombre d’orifices fistuleux est inversement proportionnel à l’infliximabémie (30). Le même type d’observation a été fait avec les dosages résiduels d’adalimumabémie (31). (figure 7)
Intuitivement, cela suggérerait que la surveillance des taux résiduels avec ajustements des doses chez les personnes ayant des taux résiduels bas pourrait améliorer les taux de guérison des fistules. Cependant cela n’a pas été évalué de manière prospective. Le seul essai ayant évalué prospectivement deux schémas d’induction d’IFX à 5 mg/kg et 10 mg/kg n’a pas montré de supériorité à la mise en place d’un schéma optimisé (32). Il existe également des travaux qui montrent qu’un taux résiduel bas peut simplement être le témoin d’une maladie plus active (effet de consommation).
Place des antibiotiques en adjuvant
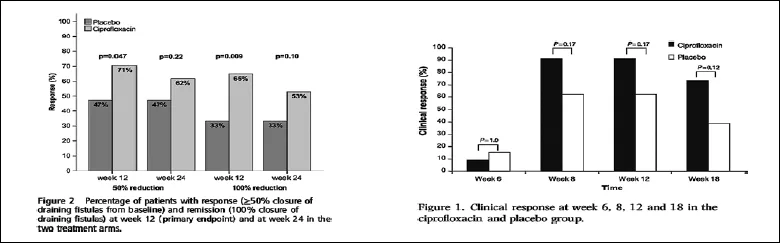
Trois essais ont évalué l’utilisation de l’antibiothérapie, principalement avec la ciprofloxacine, en association avec un traitement anti-TNF (ADA et IFX) pour la maladie de Crohn périanale. Tous ont montré une tendance à l’amélioration de la réponse clinique sur les fistules anales de Crohn à 18 et 24 semaines, bien qu’aucun de ces résultats n’ait été statistiquement significatif à la fin de la période d’étude (33-35). Ainsi, si un traitement combiné anti-TNF/antibiotique permet une amélioration dans 2/3 des cas lors de l’induction, cette différence n’est plus significative à long terme, bien qu’elle reste supérieure numériquement. Ces études n’ont peut-être pas été assez puissantes pour montrer une différence significative entre les groupes. En méta-analyse, l’induction de la réponse de la fistule (RR 1,58) et de la rémission (RR 1,94) est significativement supérieure avec les antibiotiques en association avec les anti-TNF par rapport au traitement anti-TNF seul (21).
L’utilisation d’antibiotiques dans ce contexte peut donc être proposée, en particulier lors du traitement initial de la maladie périanale avec un traitement anti-TNF, lorsque la suppuration est menaçante, compliquée ou fortement symptomatique. En revanche, l’utilisation prolongée des antibiotiques ne peut être recommandée pour des raisons évidentes de tolérance et d’écologie bactérienne. (figure 8)

Figure 8 : Résultats des essais conjuguant la ciprofloxacine avec l’ADA (33) à gauche et avec l’IFX (35) à droite
Existe-t-il une place pour les autres biothérapies dans les LAP de Crohn ?
Ustekinumab
Les données disponibles ont montré des signaux encourageants quant à l’utilisation de l’ustekinumab pour les maladies périnéales chez les patients en échec de traitement anti-TNF.
Les analyses post-hoc des grands essais contrôlés contre placebo (CERTIFI, UNITI) évaluant l’ustekinumab dans la maladie de Crohn ont révélé qu’il y avait une tendance à l’amélioration symptomatique de la fistule à la semaine 8 du traitement par l’ustekinumab par rapport au placebo (25 % vs. 14 %) puis à 80 % vs. 46 % à la semaine 44. Cependant les effectifs de l’analyse étaient faibles, avec seulement 26 patients dans les deux groupes, et les résultats n’étaient pas statistiquement significatifs.
Une étude de cohorte prospective, dans laquelle 99 % des 221 patients avaient déjà été exposés au moins à un traitement anti-TNF, a révélé que 36 % des patients étaient en rémission clinique complète de leur fistule à 24 semaines de traitement (36).
L’étude française observationnelle multicentrique Bio-LAP (37) menée par le GETAID à inclus 207 patients traités par ustekinumab avec LAP (active ou non) à l’initiation (99 % avaient également déjà été exposés à au moins un anti-TNF Alpha). Le succès clinique à 6 mois était défini par l’absence de poussée ano-périnéale nécessitant le recours à un traitement médical (topique, antibiotique) ou chirurgical. L’ustekinumab s’est avéré efficace dans 38 % des cas sur les LAP actives (148 patients), et le séton retiré dans 33 % des 88 patients porteurs à l’inclusion. Parmi les 59 patients avec LAP inactive à l’inclusion, 22 % ont récidivé leur maladie périnéale.
D’autres études rétrospectives sur l’utilisation de l’ustekinumab pour la maladie de Crohn périnéale ont été relatés dans une méta-analyse qui a révélé un taux de réponse partielle de 56 % et un taux de rémission complète de 17 % après 52 semaines de traitement (38).
Pour les patients peu répondeurs à l’ustekinumab, l’intensification du traitement a permis d’améliorer la réponse clinique dans une étude observationnelle (39). Cependant il n’existait pas de corrélation entre les taux sériques résiduels d’ustekinumab et la réponse clinique sur les patients porteurs de fistule anale issue de l’étude UNITI. L’analyse multivariée de l’étude Bio-LAP indiquait que l’absence d’optimisation du traitement était un facteur favorable au succès.
Un essai contrôlé et randomisé mené par le GETAID (USTAP) est en cours et permettra peut-être de préciser la place de l’ustekinumab dans cette indication afin de donner lieu à des recommandations.
Vedolizumab
Aucun essai contrôlé randomisé dédié n’a évalué l’efficacité du vedolizumab versus placebo dans la maladie de Crohn périnéale.
Une analyse post hoc de l’étude GEMINI 2 a comparé l’efficacité du vedolizumab d’entretien à un placebo pour la fermeture des fistules périnéales (40). 40 % avaient déjà reçu des anti-TNF alpha au préalable. L’étude a identifié une différence en faveur du vedolizumab à la semaine 14 (28 % contre 11 %) et 52 (31 % contre 11 %), mais la différence n’est pas significative, et aucune différence n’a été notée entre le traitement d’entretien administré toutes les 4 ou 8 semaines.
L’étude ENTERPRISE était un essai randomisé comparant deux schémas posologiques de vedolizumab pour le traitement de la maladie de Crohn périanale (41). 80 % de patients avaient déjà reçu un anti-TNF au préalable. Les patients ont soit reçu du vedolizumab d’induction standard de
300 mg aux semaines 0, 2 et 6, puis aux semaines 14 et 22, tandis que l’autre groupe a reçu le même schéma posologique plus une dose à la semaine 10. On déplore l’absence de groupe contrôle ou placebo dans le schéma de cette étude. On constate qu’à la semaine 30, 54 % des patients avaient une réponse clinique, tandis que 43 % avaient une fermeture complète des fistules. Il n’y avait aucune différence significative entre les deux groupes.
Dans le bras vedolizumab de l’étude française Bio-LAP portant sur 151 patients atteints de la maladie de Crohn périnéale (99 % des patients ayant déjà été traités par au moins un anti-TNF) a montré que 23 % des patients étaient en rémission après 6 mois de traitement, tandis que 67 % des patients ont arrêté le vedolizumab à 30 semaines de traitement en raison d’une maladie périnéale ou luminale non contrôlée (42). De plus, 31 % des patients atteints d’une maladie périanale qui ne présentaient aucun symptôme clinique au moment de l’initiation du vedolizumab ont développé des symptômes après le début du traitement. Un traitement immunomodulateur concomitant a été utilisé chez 44 % des patients de cette cohorte et il n’a pas été identifié comme un facteur prédictif du succès du traitement.
En conclusion, en cas d’échec d’un traitement médical optimal, combinant la chirurgie de drainage et incluant un anti-TNF à dose optimisé en combothérapie, compte tenu de l’absence d’autre alternative disponible, il est possible d’essayer une nouvelle biothérapie, bien que celles-ci n’aient pas obtenu l’AMM dans cette indication. Dans ce cas, le dossier sera idéalement discuté collégialement et on privilégiera en seconde ligne plutôt l’ustekinumab que le vedolizumab.
Fistule drainée, et après ?
Une fois le drainage de la fistule effectif (contrôle de la suppuration, rémission de l’inflammation locale et rémission luminale obtenues), le traitement radical de celle-ci est discuté.
Il faut s’efforcer de respecter au maximum l’architecture du sphincter anal afin de prévenir de troubles de continence fécale ultérieurs. Ainsi, la mise à plat du trajet fistuleux (fistulotomie) est généralement à éviter mais il peut se discuter en cas de fistule superficielle (43).
Pour les fistules plus profondes, peuvent être envisagées soit la simple abstention avec retrait du séton, soit une technique chirurgicale visant à obturer le trajet fistuleux (chirurgie dite « d’épargne sphinctérienne). De multiples techniques ont été proposées : obturation par colle ou plug, cautérisation du trajet par sonde laser ou sonde de radiofréquence, fermeture de l’orifice interne par lambeau rectal d’avancement, ligature du trajet fistuleux dans l’espace inter-sphinctérien (LIFT).
Les études visant à évaluer la place de ces traitements sont parcellaires avec des effectifs insuffisants souvent non contrôlés et des résultats décevants. C’est en particulier le cas pour les techniques d’obturation ou de cautérisation du trajet. On s’est longtemps demandé si obturer chirurgicalement une fistule en rémission, maintenue sous traitement anti-TNF d’entretien, était supérieur au simple retrait du séton.
L’essai randomisé PISA II a comparé le traitement médical seul (anti-TNF et retrait du séton) face à une stratégie de fermeture chirurgicale de l’orifice interne (Lambeau ou LIFT) (44). Le design de randomisation était particulier puisque 2/3 des patients avaient le choix du traitement et seulement 1/3 ont été réellement randomisés. Ce mode de randomisation a été justifié par les résultats de l’essai PISA I, interrompu face à un taux de réintervention trop important dans le groupe randomisé retrait simple du séton. Dans l’essai PISA II, le critère de jugement principal était la cicatrisation radiologique en IRM à 18 mois. La guérison radiologique était plus fréquente dans le groupe anti-TNF avec obturation chirurgicale : 12/38 (32 %) versus 5/56 (9 %) dans le groupe anti-TNF avec retrait simple du séton (p= 0,005). Cependant, la guérison clinique, définie par la fermeture de l’orifice externe sans écoulement, n’était pas différente entre les deux groupes : 26/38 (68 %) versus 29/56 (52 %) (p= 0,076).
Dans la pratique, on constate aujourd’hui une tendance à viser la fermeture du trajet fistuleux, mais le choix de la technique varie considérablement selon les centres et les habitudes du chirurgien. Les techniques visant à fermer l’orifice interne sont à privilégier.
Et en dernier recours ?
Dans certains cas de suppurations sévères et récalcitrantes à tous traitements, une stomie temporaire, visant à dériver les matières fécales pour permettre un assèchement et une cicatrisation des lésions, peut être proposée. Il est alors important de noter que la fermeture secondaire de la stomie est rarement possible. L’amputation abdomino-périnéale est devenue quant à elle exceptionnelle.
Traitement des marisques
Il s’agit de lésions, en général, persistantes et bénignes mais qui s’aggravent lors de poussées inflammatoires luminales de la maladie. Elles peuvent être asymptomatiques et régresser spontanément dans 40 % des cas.
Il faut le plus possible s’abstenir d’intervenir chirurgicalement, surtout devant des marisques inflammatoires, car l’exérèse de celles-ci peut aggraver les lésions ano-périnéales de maladie de Crohn (suppuration, rétrécissement, retard de cicatrisation…).
C’est seulement au stade cicatriciel (marisques fibreuses), lorsque la maladie est inactive et si les marisques sont volumineuses ou invalidantes, qu’un geste d’exérèse peut alors être discuté.
Traitement des sténoses anales
Deux types de sténoses sont à distinguer : les sténoses rectales basses souvent longues et les sténoses anales courtes (en diaphragme).
Les sténoses longues du bas rectum peuvent être l’expression d’une maladie inflammatoire active et doivent faire appel à un traitement médical (anti- TNF). Elles peuvent également être secondaires à une pathologie fistuleuse, qui nécessitera donc un traitement médico-chirurgical.
Dans les autres situations, le traitement fait appel le plus souvent à une dilatation anale (au doigt, à la bougie ou au ballon de dilatation) afin de lever les adhérences cicatricielles mais sans léser le sphincter interne chez ces patients à haut risque d’incontinence fécale à long terme.
Le traitement des sténoses combine souvent une prise en charge médicale et des séances de dilatation. En cas de récidive fréquente ou d’échec, aboutissant à une sténose serrée symptomatique et irréversible, une chirurgie non conservatrice pourra se discuter.
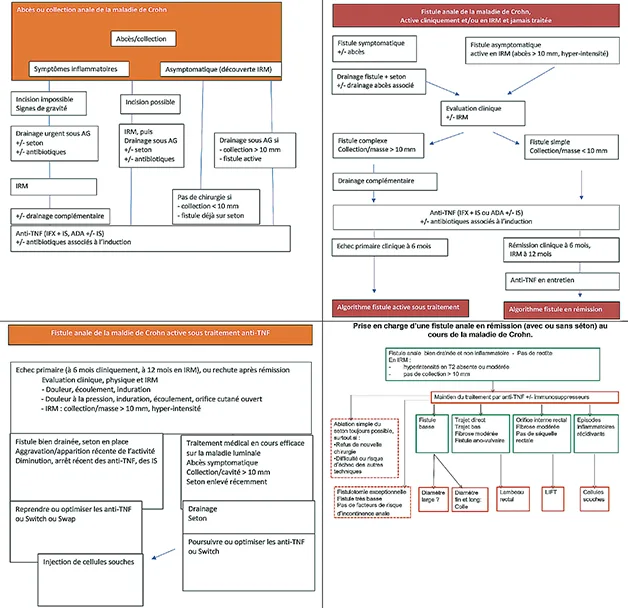
Arbres décisionnels du consensus français (SNFCP 2021)

Figure 9 : Arbres décisionnels édité par la Société Nationale Française de Colo-Proctologie (SNFCP) en 2021 pour le traitement des fistules périnéales dans le cadre d’une maladie de Crohn (Accord d’expert)
Quand et comment évaluer la réponse au traitement ?
Les critères d’une fistule en rémission ne fait à l’heure actuelle l’objet d’aucun consensus. Les études les plus anciennes prennent généralement comme critère de jugement principal, pour la rémission complète, la fermeture de l’orifice fistuleux et l’absence d’écoulement à la pression. La rémission partielle étant alors définie par la fermeture d’au moins 50 % des orifices. En pratique courante, on constate que la fermeture d’un orifice à un temps donné ne garantit pas de façon certaine sa fermeture à long terme. L’évaluation à un temps donné constitue donc un biais majeur dans l’interprétation des résultats de ces études.
Les objectifs de traitement ont évolué ces dernières années. Ils sont devenus plus stricts avec l’émergence de thérapies plus efficaces comme les anti-TNF mais également du fait d’une attention plus particulière portée à la qualité de vie des malades.
Ainsi des travaux ont été menés pour établir un consensus sur les cibles de traitement les plus appropriées.
Critères cliniques
Les cibles ont été réunies dans une revue systématique de la littérature issue d’entretien avec les patients (45). Celle-ci a identifié des critères de jugement relevant des « Patient Reported Outcomes » (incontinence, qualité de vie…) et des critères liés à l’activité de la maladie périanale (indice d’activité, nouvel abcès, récidive de fistule, nouvelle chirurgie, recours à une stomie). La réponse en IRM a paradoxalement été considérée comme secondaire dans cette étude, en partie en raison de son coût et de son accessibilité. Ces conclusions contrastent avec les directives devenues consensuelles dans la maladie de Crohn luminale, où la rémission endoscopique apparaît maintenant comme la cible.
Critères radiologiques
Il est maintenant établi que le caractère inflammatoire d’un trajet fistuleux peut persister en IRM malgré la fermeture de l’orifice externe (46). En effet, la cicatrisation en IRM peut être retardée de plusieurs mois (47).
Une étude observationnelle a suggéré que la disparition de l’aspect en hyperT2 et l’absence de rehaussement à l’injection étaient fortement corrélées à la rémission clinique chez les patients ayant eu une IRM 12 mois après le traitement (48).
D’autres études rétrospectives ont montré qu’une rémission profonde en IRM (disparition de l’hypersignal T2, du rehaussement à l’injection et de l’épaississement de la paroi rectale) semble être un facteur de bon pronostic à long terme (absence de récidive, de nouvelle chirurgie ou d’hospitalisation) (49,50).
Ces données ont été intégrées dans le score de Van Assche (51). Celui-ci permet de quantifier la sévérité de la maladie fistuleuse. Les principaux items recueillis lors de l’analyse IRM sont associés à une valeur de pondération numérique qui permet d’obtenir un score global de sévérité (de 0 et 22). Le recueil de ces informations et le calcul du score sont aujourd’hui recommandés, il permet alors de mesurer l’effet des traitements introduits. (tableau 3)
Tableau 3 : Score de Van Assche (51)
| Nombre de trajets |
|---|
| 0 – Aucun 1 – Simple direct 2 – Simple ramifié 3 – Multiple |
| Localisation du trajet principal de la suppuration |
|---|
| 1 – Intersphinctérien 2 – Transsphinctérien 3 – Supra sphinctérien |
| Extension maximale de la suppuration en profondeur |
|---|
| 1 – Sous lévatorienne 2 – Supra lévatorienne |
| Hyper signal du trajet fistuleux en séquence pondérée T2 |
|---|
| 0 – Absent 4 – Modéré 8 – Élevé |
| Collection de plus de 3 mm |
|---|
| 0 – Absente 4 – Présente |
| Epaisseur de la paroi rectale |
|---|
| 0 – Non 2 – Oui |
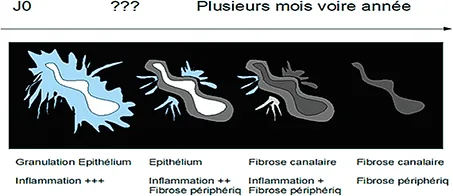
Ainsi, il apparaît aujourd’hui qu’au-delà de la simple réponse clinique, l’évaluation de la cicatrisation en IRM doit devenir la cible. Le timing de cette évaluation interviendra 6 à 12 mois après l’initiation de la prise en charge. (figure 10)

Figure 10 : Évolution du signal T2 en IRM d’une fistule
Nouveauté thérapeutique : la thérapie cellulaire
La thérapie cellulaire consiste à greffer des cellules vivantes humaines (dites « cellules souches ») afin de restaurer un tissu humain fragilisé par la maladie.
Une cellule souche est une cellule immature possédant la propriété spécifique de pouvoir s’auto-renouveler dans un environnement approprié et de se différencier en cellules matures avec des fonctions déterminées.
On distingue différents types de cellules souches :
- Les cellules souches totipotentes : présentes dans les 4 premiers jours après fécondation. Elles peuvent donner tous les types cellulaires, y compris les annexes embryonnaires et sont les seules à permettre le développement d’un organisme entier.
- Les cellules souches pluripotentes : présentes dans l’embryon de J5 à J14. Elles peuvent donner naissance à tous les types de cellules de l’organisme à partir des 3 feuillets : endodermique (poumons, intestins et foie), mésodermique (muscle, sang, os, cartilage) et ectodermique (neurones et peau) mais également aux gamètes (spermatozoïdes et ovocytes).
- Les cellules souches multipotentes : peuvent provenir du fœtus ou de l’adulte et sont présentes dans la plupart des tissus de l’organisme. Contrairement aux cellules souches pluripotentes, les cellules multipotentes ne peuvent se différencier qu’en un nombre restreint de types cellulaires. On distingue essentiellement les cellules souches mésenchymateuses et les cellules souches hématopoïétiques.
- Les cellules souches unipotentes : qui peuvent provenir comme les précédentes du fœtus et de l’adulte, n’engendrent que des cellules différenciées en seul type tissulaire.
Initialement, ce sont les cellules souches hématopoïétiques qui ont été utilisées dans la greffe de moelle osseuse. Actuellement, ce sont les cellules souches mésenchymateuses (du mésoderme ou tissu conjonctif) (CSM) multipotentes qui sont les plus communément utilisées. Elles sont retrouvées dans presque tous les tissus du corps et en particulier le stroma de la moelle osseuse, l’os, le périoste, le tissu adipeux et le muscle.
Selon le type de stimuli, elles ont la particularité de pouvoir se différencier en plusieurs types cellulaires dérivés du mésoderme (ostéoblastes, adipocytes, chondrocytes, stroma médullaire…). Certaines observations rapportent même une capacité de différentiation en cellules musculaires sarcomériques (squelettiques et cardiaques), en cellules endothéliales, voire même en cellules d’origine non mésodermique mais endodermique (comme les hépatocytes) ou neuro-ectodermique (comme les cellules neuronales).
Les CSM exercent différentes actions :
- Un effet anti-inflammatoire et immunomodulateur par l’intermédiaire de la sécrétion de molécules bioactives (interleukines, facteurs de croissance, prostaglandines, oxyde nitrique) qui agissent au contact des tissus et des cellules de l’hôte. Elles inhibent la fonction et prolifération des lymphocytes T effecteurs, des cellules dendritiques mais ont une action promotrice des lymphocytes T régulateurs.
- Un pouvoir de signalisation cellulaire par un mécanisme de plasticité, c’est-à-dire la capacité de migration d’un état différentié à un autre.
- Des propriétés prolifératives, anti-apoptotiques et pro-angiogéniques secondaires à la sécrétion de facteurs de croissance.
- Des effets antioxydants, antibactériens, antiviraux et anti-tumoraux.
Ces différents mécanismes expliquent l’effet des CSM sur la réparation des tissus endommagés.
D’où proviennent les cellules souches mésenchymateuses ?
Le prélèvement des CSM peut se réaliser sur le patient lui-même (CSM autologues) ou provenir de donneurs (CSM hétérologues ou allogéniques).
Malgré une tendance instinctive vers les cellules autologues pour des raisons d’histocompatibilité, il existe quelques contraintes liées à leur extraction, préparation et qualité.
Les CSM allogéniques se sont plus largement développés, avec des avantages pratiques en termes de faisabilité (traçabilité, stérilisation standardisée, standardisation du nombre des cellules et stockage dans des banques). De plus, la plupart des cellules souches n’expriment pas les molécules co-stimulatrices du CMH II et très peu du CMH I réduisant le risque de rejet immédiat ou d’immunisation secondaire. Au final, cette approche allogénique paraît la plus compatible avec la production pharmaceutique.
Résultats des études
Plusieurs essais de phase I et II et une étude de phase III (ADMIRE) sur l’efficacité des CSM dans les fistules de Crohn ont été menées.
L’analyse des essais de phase I et II montre une grande disparité en termes de type d’étude, du type et du nombre de cellules utilisées (autologues, allogéniques, FVS), du mode d’injection (intra et/ ou péri-fistuleux, en une ou plusieurs injections), des traitements médicaux et chirurgicaux associés, de la durée du suivi et des moyens d’évaluation. Le taux de guérison dans ces études variait de 46 à 90 %. Des effets secondaires ont été rapportés autour de 15 % (proctalgies, abcès ou fistules).
Les premières études de suivi après injection de cellules allogéniques ne montrent pas de réactions d’immunisation. Parmi tous ces essais cliniques, aucune preuve n’a été retenue d’un potentiel rôle pro-oncogénique.
L’étude ADMIRE de phase III contrôlée randomisée multicentrique en double aveugle a comparé l’injection de CSM d’origine adipocytaire versus placebo dans des fistules anopérinéales de la MC en échec du traitement médical. Il s’agissait de patients en rémission sur le plan luminal ou modérément actifs (score CDAI < 220), sans rectite, sténose rectale, fistule recto-vaginale ou stomie. Le critère de jugement principal combinait la rémission clinique (fermeture du/ des orifice(s) externe(s) attestée par l’absence de douleur ou d’écoulements à la pression) et radiologique (absence d’abcès de plus de 20 mm). Les résultats à S24 et à S52 étaient significativement en faveur des CSM (différentiel d’environ 15 %). Les résultats rétrospectifs à plus long terme se maintenaient dans 56 % des cas à un an et montraient la persistance d’une supériorité numérique de seulement 8 % en faveur des CSM.
L’étude ADMIRE a permis de donner l’AMM en 2019 aux CSM d’origine adipocytaire commercialisées sous le nom de darvadstrocel (Alofisel®, Takeda) dans le traitement des fistules anopérinéales complexes de la maladie de Crohn en échec d’une biothérapie.
Dans des études en vraie vie (52-54), les effectifs étaient faibles et les méthodes d’évaluation non standardisés mais les résultats semblaient prometteurs avec un bon profil de tolérance.
L’expérience française bi-centrique Paris-Rennes présentée aux JFHOD 2022 à propos de 46 patients suivis de manière prospective a montré un taux de réponse clinique de 74 % et radiologique de 88 %.
Les injections en pratique
Le coût du traitement dépasse les 50 000 euros et la conservation du produit à réception ne dépasse pas une vingtaine d’heures. Ainsi, la logistique doit donc être parfaitement rôdée afin de limiter toute perte. En pratique, un second patient dit « doublon » ou « back up » est prévu le même jour de l’injection en cas de déprogrammation du patient prévu initialement.
Un premier temps opératoire de curetage/ nettoyage du trajet fistuleux est préconisé dans les 2 à 3 semaines précédant l’injection.
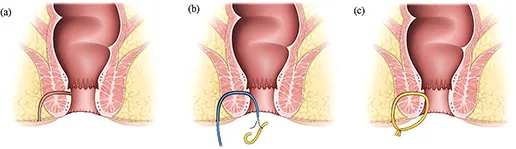
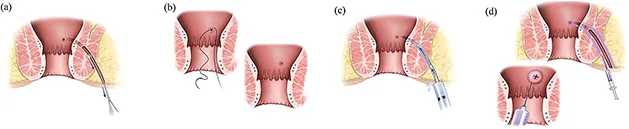
L’injection est réalisée lors du second temps opératoire. Une antibioprophylaxie per opératoire classique est préconisée. Après un second curetage du trajet, l’orifice interne est fermé (simple point ou lambeau rectal selon l’habitude du chirurgien). Les CSM sont injectés et répartis équitablement entre l’orifice interne et le trajet fistuleux. Un massage péri-orificiel permet de bien répartir le produit en fin de procédure. Aucun soin post-opératoire n’est à prévoir.
Conclusion
La prise en charge des LAP en 2022 reste difficile et nécessite souvent le recours à une équipe médico-chirurgicale coordonnée, entraînée et spécialisée. La préservation de l’appareil sphinctérien par des techniques chirurgicales d’épargne et l’optimisation du traitement médical restent l’objectif principal. L’apport de nouvelles thérapeutiques et une meilleure définition des objectifs thérapeutiques ouvrent des voies d’avenir.

Le trajet fistuleux est cureté et rincé (a), l’orifice interne est fermé (b) et l’étanchéité vérifiée (c) les CSM sont injectés en sous muqueux sous l’orifice interne et dans les parois le long du trajet fistuleux (d)
Bibliographie
- Wallenhorst T, Brochard C, Bretagne JF, Bouguen G, Siproudhis L. Crohn’s disease: is there any link between anal and luminal phenotypes? Int J Colorectal Dis. 2016;31(2):307-11.
- Schwartz DA, Loftus EV, Tremaine WJ, Panaccione R, Harmsen WS, Zinsmeister AR, et al. The natural history of fistulizing Crohn’s disease in Olmsted County, Minnesota. Gastroenterology. 1 avr 2002;122(4):875-80.
- Hellers G, Bergstrand O, Ewerth S, Holmström B. Occurrence and outcome after primary treatment of anal fistulae in Crohn’s disease. Gut. juin 1980;21(6):525-7.
- Molendijk I, Nuij VJAA, van der Meulen-de Jong AE, van der Woude CJ. Disappointing durable remission rates in complex Crohn’s disease fistula. Inflamm Bowel Dis. nov 2014;20(11):2022-8.
- Bell SJ, Williams AB, Wiesel P, Wilkinson K, Cohen RCG, Kamm MA. The clinical course of fistulating Crohn’s disease. Aliment Pharmacol Ther. 2003;17(9):1145-51.
- Eglinton TW, Barclay ML, Gearry RB, Frizelle FA. The spectrum of perianal Crohn’s disease in a population-based cohort. Dis Colon Rectum. juill 2012;55(7):773-7.
- Mahadev S, Young JM, Selby W, Solomon MJ. Quality of life in perianal Crohn’s disease: what do patients consider important? Dis Colon Rectum. mai 2011;54(5):579-85.
- Vollebregt PF, van Bodegraven AA, Markus-de Kwaadsteniet TML, van der Horst D, Felt-Bersma RJF. Impacts of perianal disease and faecal incontinence on quality of life and employment in 1092 patients with inflammatory bowel disease. Aliment Pharmacol Ther. mai 2018;47(9):1253-60.
- Grouin A, Brochard C, Siproudhis L, Lévêque J, Bretagne JF, Poulain P, et al. Perianal Crohn’s disease results in fewer pregnancies but is not exacerbated by vaginal delivery. Dig Liver Dis. 2015;47(12):1021-6.
- S M, Jm Y, W S, Mj S. Self-reported depressive symptoms and suicidal feelings in perianal Crohn’s disease. Colorectal Dis Off J Assoc Coloproctology G B Irel [Internet]. mars 2012 [cité 26 nov 2022];14(3). Disponible sur: https://pubmed.ncbi.nlm.nih.gov/21689304/
- Hughes LE. Clinical classification of perianal Crohn’s disease. Dis Colon Rectum. oct 1992;35(10):928-32.
- Parks AG, Gordon PH, Hardcastle JD. A classification of fistula-in-ano. Br J Surg. janv 1976;63(1):1-12.
- Arnous J, Denis J, Puymonbrun T. Les suppurations anales et périanales. À propos de 6 500 cas. Concours Med 1980 12 :1715-29.
- Irvine EJ. Usual therapy improves perianal Crohn’s disease as measured by a new disease activity index. McMaster IBD Study Group. J Clin Gastroenterol. janv 1995;20(1):27-32.
- Schwartz DA, Wiersema MJ, Dudiak KM, Fletcher JG, Clain JE, Tremaine WJ, et al. A comparison of endoscopic ultrasound, magnetic resonance imaging, and exam under anesthesia for evaluation of Crohn’s perianal fistulas. Gastroenterology. nov 2001;121(5):1064-72.
- Buchanan GN, Halligan S, Bartram CI, Williams AB, Tarroni D, Cohen CRG. Clinical examination, endosonography, and MR imaging in preoperative assessment of fistula in ano: comparison with outcome-based reference standard. Radiology. déc 2004;233(3):674-81.
- Garros A, Siproudhis L, Tchoundjeu B, Rohou T, Brochard C, Wallenhorst T, et al. Magnetic resonance imaging and clinical assessments for perianal Crohn’s disease: gain and limits. Dig Liver Dis Off J Ital Soc Gastroenterol Ital Assoc Study Liver. déc 2014;46(12):1072-6.
- Torres J, Bonovas S, Doherty G, Kucharzik T, Gisbert JP, Raine T, et al. ECCO Guidelines on Therapeutics in Crohn’s Disease: Medical Treatment. J Crohns Colitis. 1 janv 2020;14(1):4-22.
- Bouchard D, Abramowitz L, Bouguen G, Brochard C, Dabadie A, de Parades V, et al. Anoperineal lesions in Crohn’s disease: French recommendations for clinical practice. Tech Coloproctology. sept 2017;21(9):683-91.
- Wallenhorst T, Brochard C, Le Balch E, Bodere A, Garros A, Merlini-l’Heritier A, et al. Anal ulcerations in Crohn’s disease: Natural history in the era of biological therapy. Dig Liver Dis Off J Ital Soc Gastroenterol Ital Assoc Study Liver. nov 2017;49(11):1191-5.
- Lee MJ, Parker CE, Taylor SR, Guizzetti L, Feagan BG, Lobo AJ, et al. Efficacy of Medical Therapies for Fistulizing Crohn’s Disease: Systematic Review and Meta-analysis. Clin Gastroenterol Hepatol Off Clin Pract J Am Gastroenterol Assoc. déc 2018;16(12):1879-92.
- Jones JL, Kaplan GG, Peyrin-Biroulet L, Baidoo L, Devlin S, Melmed GY, et al. Effects of Concomitant Immunomodulator Therapy on Efficacy and Safety of Anti-Tumor Necrosis Factor Therapy for Crohn’s Disease: A Meta-analysis of Placebo-controlled Trials. Clin Gastroenterol Hepatol Off Clin Pract J Am Gastroenterol Assoc. déc 2015;13(13):2233-2240.e1-2; quiz e177-178.
- Zhu M, Xu X, Feng Q, Cui Z, Wang T, Yan Y, et al. Effectiveness of Infliximab on Deep Radiological Remission in Chinese Patients with Perianal Fistulizing Crohn’s Disease. Dig Dis Sci. mai 2021;66(5):1658-68.
- Bouguen G, Siproudhis L, Gizard E, Wallenhorst T, Billioud V, Bretagne JF, et al. Long-term Outcome of Perianal Fistulizing Crohn’s Disease Treated With Infliximab. Clin Gastroenterol Hepatol. 1 août 2013;11(8):975-981.e4.
- Lichtenstein GR, Loftus EV, Isaacs KL, Regueiro MD, Gerson LB, Sands BE. ACG Clinical Guideline: Management of Crohn’s Disease in Adults. Am J Gastroenterol. avr 2018;113(4):481-517.
- Steinhart AH, Panaccione R, Targownik L, Bressler B, Khanna R, Marshall JK, et al. Clinical Practice Guideline for the Medical Management of Perianal Fistulizing Crohn’s Disease: The Toronto Consensus. J Can Assoc Gastroenterol. déc 2018;1(4):141-54.
- Strik AS, Löwenberg M, Buskens CJ, B Gecse K, I Ponsioen C, Bemelman WA, et al. Higher anti-TNF serum levels are associated with perianal fistula closure in Crohn’s disease patients. Scand J Gastroenterol. avr 2019;54(4):453-8.
- Plevris N, Jenkinson PW, Arnott ID, Jones GR, Lees CW. Higher anti-tumor necrosis factor levels are associated with perianal fistula healing and fistula closure in Crohn’s disease. Eur J Gastroenterol Hepatol. janv 2020;32(1):32-7.
- Davidov Y, Ungar B, Bar-Yoseph H, Carter D, Haj-Natour O, Yavzori M, et al. Association of Induction Infliximab Levels With Clinical Response in Perianal Crohn’s Disease. J Crohns Colitis. 1 mai 2017;11(5):549-55.
- Yarur AJ, Kanagala V, Stein DJ, Czul F, Quintero MA, Agrawal D, et al. Higher infliximab trough levels are associated with perianal fistula healing in patients with Crohn’s disease. Aliment Pharmacol Ther. avr 2017;45(7):933-40.
- Gu B, Venkatesh K, Williams AJ, Ng W, Corte C, Gholamrezaei A, et al. Higher infliximab and adalimumab trough levels are associated with fistula healing in patients with fistulising perianal Crohn’s disease. World J Gastroenterol. 21 juin 2022;28(23):2597-608.
- Present DH, Rutgeerts P, Targan S, Hanauer SB, Mayer L, van Hogezand RA, et al. Infliximab for the treatment of fistulas in patients with Crohn’s disease. N Engl J Med. 6 mai 1999;340(18):1398-405.
- Dewint P, Hansen BE, Verhey E, Oldenburg B, Hommes DW, Pierik M, et al. Adalimumab combined with ciprofloxacin is superior to adalimumab monotherapy in perianal fistula closure in Crohn’s disease: a randomised, double-blind, placebo controlled trial (ADAFI). Gut. févr 2014;63(2):292-9.
- Colombel JF, Schwartz DA, Sandborn WJ, Kamm MA, D’Haens G, Rutgeerts P, et al. Adalimumab for the treatment of fistulas in patients with Crohn’s disease. Gut. juill 2009;58(7):940-8.
- West RL, van der Woude CJ, Hansen BE, Felt-Bersma RJF, van Tilburg AJP, Drapers J a. G, et al. Clinical and endosonographic effect of ciprofloxacin on the treatment of perianal fistulae in Crohn’s disease with infliximab: a double-blind placebo-controlled study. Aliment Pharmacol Ther. 2004;20(11-12):1329-36.
- Biemans VBC, van der Meulen – de Jong AE, van der Woude CJ, Löwenberg M, Dijkstra G, Oldenburg B, et al. Ustekinumab for Crohn’s Disease: Results of the ICC Registry, a Nationwide Prospective Observational Cohort Study. J Crohns Colitis. janv 2020;14(1):33-45.
- Chapuis-Biron C, Kirchgesner J, Pariente B, Bouhnik Y, Amiot A, Viennot S, et al. Ustekinumab for Perianal Crohn’s Disease: The BioLAP Multicenter Study From the GETAID. Am J Gastroenterol. nov 2020;115(11):1812-20.
- Attauabi M, Burisch J, Seidelin JB. Efficacy of ustekinumab for active perianal fistulizing Crohn’s disease: a systematic review and meta-analysis of the current literature. Scand J Gastroenterol. janv 2021;56(1):53-8.
- Glass J, Alsamman Y, Chittajallu P, Ahmed T, Fudman D. 26 USTEKINUMAB DOSE ESCALATION EFFECTIVE IN REAL-WORLD USE FOR LUMINAL AND PERIANAL CROHN’S DISEASE. Gastroenterology. 1 févr 2020;158(3):S123-4.
- Feagan BG, Schwartz D, Danese S, Rubin DT, Lissoos TW, Xu J, et al. Efficacy of Vedolizumab in Fistulising Crohn’s Disease: Exploratory Analyses of Data from GEMINI 2. J Crohns Colitis. avr 2018;12(5):621-6.
- Schwartz DA, Peyrin-Biroulet L, Lasch K, Adsul S, Danese S. Efficacy and Safety of 2 Vedolizumab Intravenous Regimens for Perianal Fistulizing Crohn’s Disease: ENTERPRISE Study. Clin Gastroenterol Hepatol. 1 mai 2022;20(5):1059-1067.e9.
- Chapuis-Biron C, Bourrier A, Nachury M, Nancey S, Bouhnik Y, Serrero M, et al. Vedolizumab for perianal Crohn’s disease: a multicentre cohort study in 151 patients. Aliment Pharmacol Ther. avr 2020;51(7):719-27.
- Herissay A, Siproudhis L, Le Balc’H E, L’Heritier AM, Dewitte M, Wallenhorst T, et al. Combined strategies following surgical drainage for perianal fistulizing Crohn’s disease: failure rates and prognostic factors. Colorectal Dis. janv 2021;23(1):159-68.
- Meima-van Praag EM, van Rijn KL, Wasmann KATGM, Snijder HJ, Stoker J, D’Haens GR, et al. Short-term anti-TNF therapy with surgical closure versus anti-TNF therapy in the treatment of perianal fistulas in Crohn’s disease (PISA-II): a patient preference randomised trial. Lancet Gastroenterol Hepatol. juill 2022;7(7):617-26.
- Sahnan K, Tozer PJ, Adegbola SO, Lee MJ, Heywood N, McNair AGK, et al. Developing a core outcome set for fistulising perianal Crohn’s disease. Gut. févr 2019;68(2):226-38.
- Bell SJ, Halligan S, Windsor ACJ, Williams AB, Wiesel P, Kamm MA. Response of fistulating Crohn’s disease to infliximab treatment assessed by magnetic resonance imaging. Aliment Pharmacol Ther. 2003;17(3):387-93.
- Tozer P, Ng SC, Siddiqui MR, Plamondon S, Burling D, Gupta A, et al. Long-term MRI-guided combined anti-TNF-α and thiopurine therapy for Crohn’s perianal fistulas. Inflamm Bowel Dis. oct 2012;18(10):1825-34.
- Savoye-Collet C, Savoye G, Koning E, Dacher JN, Lerebours E. Fistulizing perianal Crohn’s disease: contrast-enhanced magnetic resonance imaging assessment at 1 year on maintenance anti-TNF-alpha therapy. Inflamm Bowel Dis. août 2011;17(8):1751-8.
- Chambaz M, Verdalle-Cazes M, Desprez C, Thomassin L, Charpentier C, Grigioni S, et al. Deep remission on magnetic resonance imaging impacts outcomes of perianal fistulizing Crohn’s disease. Dig Liver Dis Off J Ital Soc Gastroenterol Ital Assoc Study Liver. mars 2019;51(3):358-63.
- Thomassin L, Armengol-Debeir L, Charpentier C, Bridoux V, Koning E, Savoye G, et al. Magnetic resonance imaging may predict deep remission in patients with perianal fistulizing Crohn’s disease. World J Gastroenterol. 21 juin 2017;23(23):4285-92.
- Van Assche G, Vanbeckevoort D, Bielen D, Coremans G, Aerden I, Noman M, et al. Magnetic resonance imaging of the effects of infliximab on perianal fistulizing Crohn’s disease. Am J Gastroenterol. févr 2003;98(2):332-9.
- Schwandner O. Stem cell injection for complex anal fistula in Crohn’s disease: A single-center experience. World J Gastroenterol. 28 juin 2021;27(24):3643-53.
- Cabalzar-Wondberg D, Turina M, Biedermann L, Rogler G, Schreiner P. Allogeneic expanded adipose-derived mesenchymal stem cell therapy for perianal fistulas in Crohn’s disease: A case series. Colorectal Dis Off J Assoc Coloproctology G B Irel. juin 2021;23(6):1444-50.
- Furukawa S, Mizushima T, Nakaya R, Shibata M, Yamaguchi T, Watanabe K, et al. Darvadstrocel for complex perianal fistulas in Japanese adults with Crohn’s disease: a phase 3 study. J Crohns Colitis. 23 sept 2022;jjac144.
Abréviations
LAP : Lésion ano-périnéales
MC : Maladie de Crohn
IFX : Infliximab
ADA : Adalimumab
TNF : Tumor Necrosis Factor
GETAID : Groupe d’étude thérapeutique des affections inflammatoires du tube digestif
CSM : Cellule Souches Mésenchymateuses