Liens d’intérêts
NOVONORDISK (invitation à des congrès)
Mots-clés
MASLD ; MASH ; Règles hygiéno-diététiques
Abréviations
AASLD : American Association for the Study of Liver Disease
CHC : carcinome hépatocellulaire
EASL : European Association for the Study of the Liver
EASD : European Association for the Study of Diabetes
EASO : European Association for the Study of Obesity
ESPEN : European Society for Clinical Nutrition and Metabolisme
FDA : Food and Drug Administration
MASLD (Metabolic dysfunction-Associated Steatotic Liver Disease) : hépatopathie stéatosique métabolique
MASH (Metabolic dysfunction-Associated SteatoHepatitis) : stéatohépatite métabolique
NAFLD (Non-Alcoholic Fatty Liver Disease) : stéatose hépatique non-alcoolique
NASH (Non-Alcoholic SteatoHepatitis) : stéatohépatite non alcoolique
Introduction
Les hépatopathies stéatosiques métaboliques, désormais connues sous le terme de Metabolic dysfunction-Associated Steatotic Liver Disease (MASLD) en remplacement de l’ancienne dénomination Non-Alcoholic Fatty Liver Disease (NAFLD), correspondent à l’expression hépatique du syndrome métabolique et se caractérisent par l’accumulation de graisse dans le foie, en dehors de toute consommation excessive d’alcool (1). La MASLD représente la première cause de maladie hépatique dans le monde avec une prévalence d’environ 30 % (2). Parmi ces patients, environ 25 % présentent une inflammation hépatique avec une souffrance hépatocytaire, appelée dorénavant MASH pour Metabolic dysfunction-Associated SteatoHepatitis en remplacement de l’ancienne dénomination Non Alcoholic Steatohepatitis (NASH). Cette inflammation favorise le développement d’une fibrose hépatique qui s’aggrave progressivement jusqu’au stade de cirrhose (3).
La MASLD est associée au diabète de type 2, aux dyslipidémies, à l’hypertension artérielle et à l’obésité. La prévalence mondiale de la MASLD est de 55,5 % chez les patients diabétiques de type 2 (4) et de 70 % chez les adultes en surpoids ou en situation d’obésité (5). Le diabète de type 2 et l’obésité (en particulier l’obésité androïde) sont les pathologies métaboliques avec le plus fort impact sur l’histoire naturelle de la MASLD, y compris la progression vers une fibrose avancée, une cirrhose et un carcinome hépatocellulaire qui y sont liés (3).
La MASLD est associée à un risque plus important de morbi-mortalité. Les causes de décès les plus fréquentes sont les maladies cardiovasculaires, les tumeurs malignes non hépatiques, et les pathologies du foie (6). Plus la fibrose est avancée (F2-F4), plus le risque de décès est important.
Hormis l’application de règles hygiéniques et diététiques permettant la perte de poids, il n’existe actuellement aucun traitement spécifique validé pour traiter la MASLD en France (3, 6, 7). Cependant, la recherche avance à grands pas et de nouvelles molécules très prometteuses apparaissent. Seule la MASLD sera traitée au cours de cet atelier de FMC. Il ne sera pas abordé les autres pathologies du spectre des pathologies stéatosiques hépatiques (alcooliques, atteinte mixte, secondaires aux traitements ou à la malabsorption…).
Physiopathologie de la MASLD
La MASLD est une pathologie complexe qui associe à la fois des facteurs environnementaux, génétiques et métaboliques (6). En effet, une alimentation déséquilibrée avec un microbiote altéré, associée à une sédentarité sur un terrain génétique prédisposant, peut induire une accumulation d’énergie stockée dans le foie et dans le tissu adipeux, responsables à terme d’une insulino-résistance et de troubles métaboliques (8). Quand les apports énergétiques dépassent les besoins métaboliques et les capacités d’élimination de l’organisme, les glucides entraînent la formation et l’accumulation de graisse intrahépatique par lipogénèse de novo. Ainsi le développement de la MASH semble dépendre du type de glucides et de lipides consommés (9). Les acides gras saturés et le fructose semblent avoir un impact plus important sur le foie. L’insulino-résistance présente à la fois dans les muscles, les tissus adipeux et le foie jouent un rôle majeur dans la physiopathologie de la MASLD. Par ailleurs, ces phénomènes induisent un stress cellulaire oxydatif, notamment au niveau du tissu adipeux avec une augmentation de la circulation des acides gras libres, responsable d’une inflammation systémique et d’une aggravation de l’insulino-résistance. Cette insulino-résistance est liée à une augmentation de la prévalence de la MASLD et de sa sévérité (6, 8).
Certains polymorphismes génétiques semblent associés à l’aggravation de la maladie hépatique et au développement du carcinome hépatocellulaire (CHC) dans la MASH (8, 10). Ainsi, certains polymorphismes, comme le polymorphisme I148M de PNPLA3, le variant E167K du gène TM6SF2, le variant rs641738 de MBOAT7 ou P446L de GCKR, seraient associés à une aggravation des lésions hépatiques ou une augmentation du risque cardiovasculaire, tandis que d’autres variants de gènes auraient plutôt un rôle protecteur comme pour HSD17B13 ou MARC1.
Des études de plus en plus nombreuses suggèrent également un rôle du microbiote intestinal (11). La dysbiose intestinale semble associée à la modulation des réponses immunitaires locales et à une altération de l’intégrité de la barrière intestinale (augmentation de sa perméabilité et diminution de la sécrétion de mucus) qui, à son tour, altère le métabolisme des acides biliaires secondaires et favorise la translocation des produits bactériens comme les lipopolysaccharides provenant de bactéries gram-négatives ou encore la production accrue de triméthylamine ou d’éthanol endogène. Ces modifications du microbiote seraient associées à la sévérité des lésions histologiques hépatiques chez les sujets ayant une MASLD (12).
La compréhension progressive de la physiopathologie de la MASH permet le développement de thérapies spécifiques. Les principaux leviers d’intervention susceptibles de prévenir ou de traiter la MASH comprennent, entre autres, une modification des apports alimentaires, une augmentation de l’activité physique, une amélioration de la sensibilité des adipocytes à l’insuline, une inhibition de la lipogenèse de novo, une augmentation du métabolisme oxydatif hépatique et une limitation de l’inflammation, de la mort cellulaire et de la fibrogénèse hépatique (3). Les analogues d’hormones peptidiques (FGF-19, FGF-21, du glucagon-like peptide-1, du GIP, du glucagon…) et les ligands des récepteurs nucléaires (ciblant les PPARa, PPARd, PPARg, les récepteurs b des hormones thyroïdiennes et les récepteurs X farnésoïde) sont également des cibles thérapeutiques prometteuses affectant de multiples voies métaboliques et ayant de possibles effets bénéfiques sur le foie.
Dépistage de la fibrose avancée
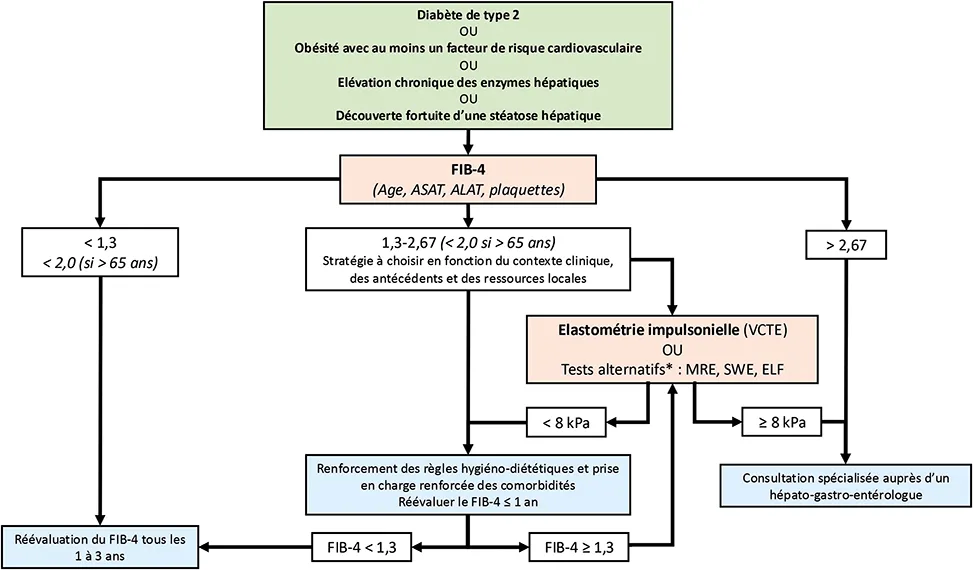
La sévérité de la fibrose hépatique représente le principal facteur pronostique dans la MASLD. Cette fibrose doit donc être dépistée et évaluée précocement et précisément notamment dans les populations à risque. Dans ses dernières recommandations (3), l’EASL, en association avec l’EASD et l’EASO, propose un algorithme de dépistage et d’évaluation de la fibrose avancée en utilisant les tests non invasifs, au sein des 3 principaux groupes à risques : les patients diabétiques de type 2, les patients en situation d’obésité avec au moins un facteur de risque cardiovasculaire et les patients avec une élévation chronique des enzymes hépatiques (figure 1). Cet algorithme séquentiel, relativement simple et facile à mettre en place en pratique clinique, peut aussi être appliqué en cas de découverte fortuite d’une stéatose hépatique. Il permet notamment de stratifier les individus dans des parcours de soins cliniques (par exemple, médecin généraliste, diabétologue, hépatologue…) en fonction de leur risque de développer des complications hépatiques. En effet, dans une étude multicentrique internationale, l’utilisation du FIB-4 puis du VCTE dans un algorithme séquentiel permettait de stratifier avec précision les patients atteints de MASLD en fonction de leur risque de complications hépatiques (13). Ces tests non invasifs sont des alternatives à la biopsie du foie, invasive et à risque, pour l’identification des patients nécessitant une prise en charge spécialisée.

Figure 1 : Algorithme d’évaluation non invasive du risque de fibrose avancée chez les patients présentant des facteurs de risque métabolique ou des signes de MASLD, selon les recommandations de l’EASL-EASD-EASO de 2024 (3). Cette stratégie vise à identifier les patients à risque de développer des complications hépatiques de la MASLD
ELF : Enhanced Liver Fibrosis ; FIB-4 : Fibrosis-4 Index ; MRE (Magnetic Resonance Elastography) : élastographie par résonance magnétique ; SWE (Shear Wave Elastography) : élastographie par ondes de cisaillement ; VCTE (Vibration-controlled transient elastography) : élastométrie impulsionnelle.
Par ailleurs, la présence d’une stéatohépatite hépatique est indirectement liée au pronostic car elle constitue le principal moteur de fibrogénèse hépatique. En effet, dans une cohorte d’histoire naturelle de 445 individus avec un suivi moyen de 4,9 ans entre les biopsies hépatiques appariées du NASH CRN, l’amélioration du score NAS au fil du temps était associée à la régression de la fibrose, tandis que l’aggravation du score NAS était associée à la progression de la fibrose (14). La résolution de la stéatohépatite paraît donc un facteur important à prendre en compte pour diminuer la fibrose hépatique. Cependant, bien que de nombreux projets de recherche prometteurs sont en cours, il n’existe à l’heure actuelle pas de tests non invasifs validés pour évaluer cette inflammation intrahépatique.
Prise en charge de la MASLD
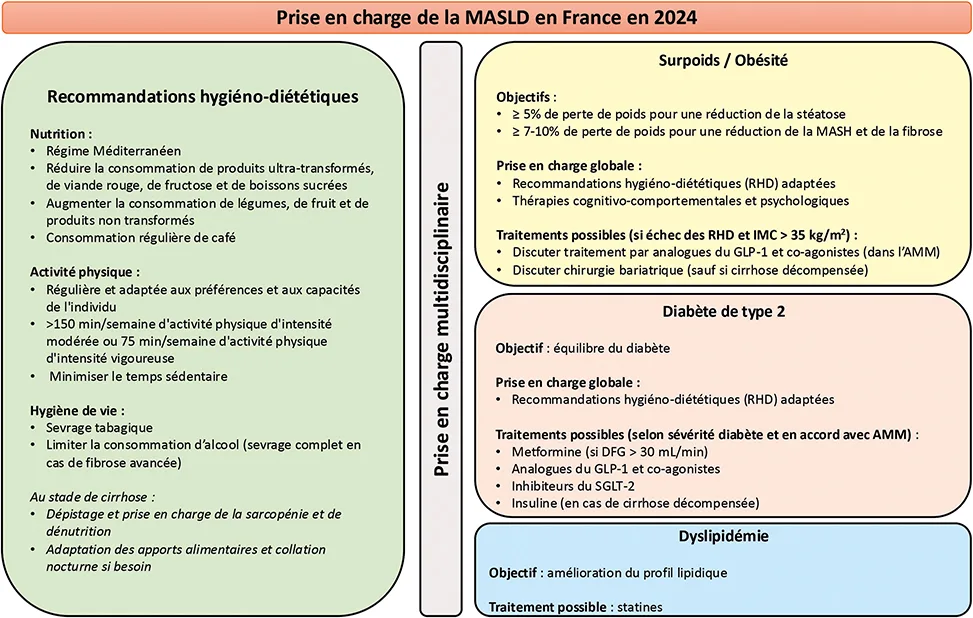
De par la complexité de la physiopathologie et les multiples comorbidités de la MASLD, sa prise en charge doit être multidisciplinaire et coordonnée, afin de couvrir toutes les composantes de la maladie (figure 2) (3, 6, 7). La régression de la fibrose étant associée à une diminution du risque de complications hépatiques, l’objectif en accord avec les recommandations des sociétés savantes d’hépatologie (EASL et AASLD) de diabétologie (EASD) et de nutrition (ESPEN et EASO), est de réduire à la fois l’activité de la maladie mais aussi la stéato-hépatite pour induire, si possible, une régression de cette fibrose hépatique. Pour ce faire, il est indispensable, en collaboration avec les diabétologues, les médecins nutritionnistes, les diététicien(ne)s, les psychologues, les kinésithérapeutes, les coaches d’APA d’améliorer les règles hygiéno-diététiques, d’optimiser les traitements des comorbidités et notamment du diabète de type 2, et d’envisager, si besoin pour les patients en situation d’obésité (≥ 35 kg/m2), un traitement spécifique ou une chirurgie bariatrique. Bien qu’aucun traitement n’ait pour l’instant d’AMM en France dans la MASLD, de nombreux essais cliniques sont ouverts et en cours d’inclusion.

Figure 2 : Prise en charge de la MASLD en France en 2024 (d’après les recommandations de l’EASL (3), de l’AASL (6) et de l’ESPEN (7))
Le choix recommandé des traitements pharmacologiques chez les personnes atteintes de MASLD/MASH, dépend des comorbidités et du stade de gravité de la maladie
GLP1 : agoniste du récepteur du peptide 1 de type glucagon ; AMM : autorisation de mise sur le marché ; RHD : règles hygiéno-diététiques ; SGLT-2 : sodium/glucose
co-transporteur 2 ; DFG : débit de filtration glomérulaire ; LDL : lipoprotéines de faible densité ; IMC : indice de masse corporelle ; HbA1c : hémoglobine glyquée.
Prise en charge hygiéno-diététique dans la MASLD
La modification des règles hygiéno-diététiques représente la pierre angulaire de la prise en charge de la MASLD. L’un des objectifs principaux est la perte de poids (3, 6, 7). Cette recommandation proposée à la fois par l’EASL-EASD-EASO, par l’AASLD et par l’ESPEN, fait suite aux résultats d’un essai interventionnel rigoureux avec des critères histologiques qui suggérait qu’une réduction du poids corporel de≥ 5 % est nécessaire pour réduire la stéatose, de 7-10 % pour améliorer l’inflammation, et de≥ 10 % pour améliorer la fibrose hépatique (15). Cette perte de poids doit être rigoureusement encadrée par une équipe multidisciplinaire (3, 6, 7). Cependant, peu de patients parviennent à atteindre ces objectifs et à maintenir une perte de poids au long cours. Un suivi adapté, régulier et au long cours, est indispensable pour maintenir la perte de poids dans le temps. Dans une étude de cohorte observationnelle, 32 % des patients atteints de MALSD qui étaient initialement en surpoids ou en situation d’obésité, ont perdu≥ 5 % de leur poids à un moment ou à un autre du suivi, mais seulement 25 % ont maintenu une perte de poids de≥ 5 % (16). Des essais contrôlés randomisés à plus long terme (à plus de 2 ans) sur les interventions liées au mode de vie, sont nécessaires pour mieux appréhender et adapter la prise en charge de ces patients.
L’alimentation joue donc un rôle central : une alimentation hypercalorique, trop riche en graisses saturées, en boissons sucrés, en viande rouge, en glucides raffinés ou en fructose, semble associée à une augmentation du risque de progression de la MASLD vers la MASH puis vers la cirrhose. Seul le régime méditerranéen, en limitant les produits ultra-transformés, la viande rouge et les boissons sucrés et en privilégiant une alimentation équilibrée riche en huile d’olive, fruits, légumes, fibres, poissons et céréales, semble réduire la stéatose, la MASH, la progression vers la fibrose et le risque de cancer hépatique. C’est actuellement le seul régime recommandé par les sociétés savantes (3, 6, 7). Il existe trop peu de données concernant l’efficacité d’autres régimes alimentaires pour les recommander pour le moment (régime cétogène, régime DASH, jeun intermittent ).
Concernant l’apport protéique, l’ESPEN recommande que les patients atteints de MASLD/MASH en situation de surpoids ou d’obésité et qui ne suivent pas un régime amincissant hypocalorique, doivent ingérer au moins 1 g/kg (poids corporel ajusté)/j de protéines (7). Ceux qui suivent un régime amincissant hypocalorique doivent, quant à eux, ingérer 1,2 g/kg (poids corporel ajusté)/j de protéines pour prévenir la perte de masse musculaire (7). Il faut particulièrement être attentif au risque de sarcopénie et de dénutrition au cours de la perte pondérale (7). L’ESPEN et l’AASL suggèrent un enrichissement de l’alimentation par des acides gras polyinsaturés de type Oméga-3, notamment en cas d’hypertriglycéridémie associée, pour améliorer les taux plasmatiques d’enzymes hépatiques et de triglycérides (6, 7). Pareillement, une consommation régulière de café d’au moins 3 tasses par jour, contenant de la caféine ou non, semble améliorer les lésions hépatiques, ralentir la progression de la fibrose et réduire les complications hépatiques (6).
Aucune donnée de la littérature ne permet actuellement de recommander une complémentation spécifique en prébiotiques, en probiotiques, en symbiotiques ou en micronutriments dans la MASLD (3, 7).
Concernant l’activité physique, l’EASL-EASD-EASO, l’ASSLD et l’ESPEN en accord avec l’OMS, recommandent une activité physique régulière et adaptée, d’intensité modérée d’au moins 150 minutes par semaine, ou forte d’au moins 75 minutes par semaine (3, 6, 7). Plusieurs études mettent en évidence une amélioration des lésions histologiques de la MASLD, proportionnellement à l’intensité de l’exercice physique. L’effet semble d’autant plus important quand l’activité physique est associée à des conseils diététiques.
Indications et modalités de la chirurgie bariatrique dans la MASLD
En cas d’échec des mesures hygiéno-diététiques et chez les patients éligibles, l’EASL-EASD-EASO, l’AASLD et l’ESPEN considèrent la chirurgie bariatrique comme une option thérapeutique sérieuse permettant d’obtenir une perte de poids durable allant jusqu’à 30 %, une amélioration de la fibrose hépatique, une rémission du diabète de type 2 et une diminution du risque d’évènements cardio-vasculaires et de la mortalité toutes causes confondues (3, 6, 7). L’étude multicentrique BRAVES, ouverte et randomisée, a démontré une résolution histologique de la MASH sans aggravation de la fibrose chez 55 % des patients ayant subi un pontage gastrique de type Roux-en-Y ou une sleeve-gastrectomy après un an de suivi, contre 15 % dans le groupe ayant modifié son mode de vie dans l’analyse intentionnelle (17). Dans cette étude, une amélioration de la fibrose≥ 1 stade sans aggravation de la MASH après 1 an a été obtenue chez 37 % des patients après un pontage gastrique de type Roux-en-Y et 39 % après une sleeve gastrectomie, contre 23 % après une modification du mode de vie. Par ailleurs, la chirurgie bariatrique améliore également le diabète de type 2 et diminue le risque de complications cardiovasculaires (3). L’absence de perte de poids substantielle après la chirurgie bariatrique semble associée à la persistance de la MASH. Bien que les procédures chirurgicales restrictives (sleeve-gastrectomie) entraînent une perte de poids un peu moins importante que les procédures malabsorptives (by-pass gastrique selon Roux en Y…), les 2 procédures sont recommandées de manière équivalente par l’ESPEN (7).
En France, la chirurgie bariatrique est recommandée par la Haute Autorité de Santé (HAS), en cas d’échec des règles hygiéno-diététiques et après discussion et validation collégiale au cours d’une RCP dédiée, chez les patients avec un IMC≥ 40 kg/m2 ou chez les patients avec un IMC entre 35 et 40 kg/m2 et une stéatohépatite métabolique (MASH) ou une fibrose hépatique (quel que soit le stade de la fibrose) (18). La stéatose isolée n’est pas une comorbidité retenue pour l’indication de chirurgie bariatrique. La chirurgie bariatrique peut être proposée en cas de cirrhose compensée CHILD- PUGH A, après une discussion au sein d’une équipe multidisciplinaire entraînée comprenant au moins un hépatologue car le risque de complication est très important (3, 18). Elle reste formellement contre-indiquée par toutes les sociétés savantes en cas de cirrhose décompensée (CHILD-PUGH B et C).
Par ailleurs, la chirurgie métabolique peut être proposée en France, selon la HAS, aux patients atteints de diabète de type 2 et qui présentent une obésité de grade I (IMC compris entre 30 et 35 kg/m2) lorsque les objectifs glycémiques individualisés ne sont pas atteints, malgré une prise en charge médicale, notamment diabétologique et nutritionnelle, incluant aussi une activité physique adaptée, bien conduite, selon les recommandations de bonne pratique actuelles, pendant au moins douze mois (19). Tout comme pour la chirurgie bariatrique, la décision doit être validée au cours d’une RCP dédiée comprenant au moins un diabétologue. Les contre-indications de la chirurgie bariatrique et de la chirurgie métabolique sont les mêmes (19).
Il existe encore trop peu de donnée pour recommander l’endoscopie bariatrique (3). Des études sont en cours pour évaluer l’efficacité et la sécurité de ces procédures endoscopiques au long cours dans la MASH (Etude ENDONASH – NCT04653311).
Thérapeutiques medicamenteuses dans la MASLD
En 2024, bien que plusieurs classes thérapeutiques semblent prometteuses et sont en cours d’évaluation en phase 3 (tableau 1), aucun médicament n’a encore obtenu d’Autorisation de Mise sur le Marché en France dans la MASLD.
Tableau 1 : Molécules actuellement évaluées en phase 3 (ou à venir) dans la MASLD
| Molécules | Mécanismes d’action | Phase 3 en cours de développement | Résultats de la phase 2 (phase 3 pour le RESMETIROM) |
| Enregis- trement de l’étude en phase 3 | Population étudiée en phase 3 | Population étudiée en phase 2 (enregis- trement de l’étude) | Résolution de la MASH sans aggravation de la fibrose | Amélioration de la fibrose (≥1 stade) sans aggravation de la MASH | Principaux effets notables | Principaux effets indésirables |
| RESMETIROM | Agoniste des récepteurs b-TRH | Phase 3 (NCT- 03900429) (1) | MASH F1b- F2-F3 | | Oui | Oui | Amélioration du LDL- cholestérol | Diarrhée, nausée |
| SEMAGLUTIDE | Agoniste des récepteurs au GLP-1 | Phase 3 (NCT- 04822181) | MASH F2- F3 | MASH F2- F3 (NCT- 02970942) (2) | Oui | Non | Perte de poids, Amélioration de l’insulino-résistance et des enzymes hépatiques | Nausée, constipation, anorexie, diarrhée, vomissement |
| SURVODUTIDE | Double agoniste des récepteurs au glucagon et au GLP-1 | Phase 3 (NCT- 06309992) | MASH F1- F2-F3 | MASH F1- F2-F3 (NCT- 04771273) (3) | Oui | Non | Perte de poids, Amélioration de la stéatose et des enzymes hépatiques | Nausée, diarrhée, vomissement, asthénie, tachycardie |
| TIRZEPATIDE | Double agoniste des récepteurs au GIP et au GLP-1 | NE | NE | MASH F2- F3 (NCT- 04166773) (4) | Oui | Oui | Perte de poids, Amélioration de la stéatose et des enzymes hépatiques | Nausée, diarrhée |
| LANIFIBRANOR | Agoniste Pan-PPAR | Phase 3 (NCT- 04849728) | MASH F2- F3 | MASH F1- F2-F3 (NCT- 03008070) (5) | Oui | Oui | Amélioration de la dyslipidémie (élévation du HDL-cholestérol et diminution des triglycérides), de l’insulino-résistance et des enzymes hépatiques | Prise de poids, nausée, diarrhée, œdèmes périphériques et anémie |
| EFRUXIFERMINE | Analogue du FGF-21 | Phase 3 (NCT- 06215716) | MASH F2- F3 | MASH F2- F3 (NCT- 04767529) (6) | Oui | Oui | Amélioration de la stéatose, de l’insulino- résistance, des enzymes hépatiques et du profil lipidique Meilleur contrôle glycémique | Diarrhée, nausée |
| PEGOZAFERMINE | Analogue du FGF-21 | Phase 3 (NCT- 06318169) | MASH F2- F3 | MASH F2- F3 (NCT- 04929483) (7) | Oui | Oui | Amélioration de la stéatose, du taux de triglycérides plasmatiques, et des enzymes hépatiques | Diarrhée, nausée, érythème au point d’injection |
| DENIFANSTAT | Inhibiteur de la FASN | Phase 3 (NCT- 06594523) | MASH F2- F3 | MASH F2- F3 (NCT- 04906421) (8) | Oui | Oui | Amélioration de la stéatose, des enzymes hépatiques Augmentation des triglycérides | Sècheresse oculaire, vertiges, alopécie |
NE : étude de phase 3 non enregistrée dans ClinicalTrials.gov au moment de la rédaction
1. Harrison SA, Bedossa P, Guy CD, Schattenberg JM, Loomba R, Taub R, et al. A Phase 3, Randomized, Controlled Trial of Resmetirom in NASH with Liver Fibrosis. N Engl J Med. 2024 Feb 8;390(6):497–509.
2. Newsome PN, Buchholtz K, Cusi K, Linder M, Okanoue T, Ratziu V, et al. A Placebo-Controlled Trial of Subcutaneous Semaglutide in Nonalcoholic Steatohepatitis. N Engl J Med. 2021 Mar 25;384(12):1113–24.
3. Sanyal AJ, Bedossa P, Fraessdorf M, Neff GW, Lawitz E, Bugianesi E, et al. A Phase 2 Randomized Trial of Survodutide in MASH and Fibrosis. N Engl J Med. 2024 Jul 25;391(4):311–9.
4. Loomba R, Hartman ML, Lawitz EJ, Vuppalanchi R, Boursier J, Bugianesi E, et al. Tirzepatide for Metabolic Dysfunction-Associated Steatohepatitis with Liver Fibrosis. N Engl J Med. 2024 Jul 25;391(4):299–310.
5. Francque SM, Bedossa P, Ratziu V, Anstee QM, Bugianesi E, Sanyal AJ, et al. A Randomized, Controlled Trial of the Pan-PPAR Agonist Lanifibranor in NASH. N Engl J Med. 2021 Oct 21;385(17):1547–58.
6. Harrison SA, Frias JP, Neff G, Abrams GA, Lucas KJ, Sanchez W, et al. Safety and efficacy of once-weekly efruxifermin versus placebo in non-alcoholic steatohepatitis (HARMONY): a multicentre, randomised, double-blind, placebo-controlled, phase 2b trial. Lancet Gastroenterol Hepatol. 2023 Dec;8(12):1080–93.
7. Loomba R, Sanyal AJ, Kowdley KV, Bhatt DL, Alkhouri N, Frias JP, et al. Randomized, Controlled Trial of the FGF21 Analogue Pegozafermin in NASH. N Engl J Med. 2023 Sep 14;389(11):998–1008.
8. Loomba R, Bedossa P, Grimmer K, Kemble G, Bruno Martins E, McCulloch W, et al. Denifanstat for the treatment of metabolic dysfunction-associated steatohepatitis: a multicentre, double-blind, randomised, placebo-controlled, phase 2b trial. Lancet Gastroenterol Hepatol. 2024 Dec;9(12):1090–100.
Tout d’abord, l’optimisation de la prise en charge et les traitements des comorbidités associées à la MASLD (diabète de type 2, hypertension artérielle, dyslipidémie ) est un préalable indispensable. Ainsi, en cas de dyslipidémie (notamment de LDL-cholestérol élevé), la prescription d’une statine est recommandée pour prévenir les complications cardiovasculaires (20). Cette prescription est possible et semble relativement bien tolérée en cas de MASLD (3, 6). Bien que les statines n’aient pas d’AMM spécifique dans la MASLD, plusieurs études cas-contrôle suggèrent que la prise de statines est associée à une réduction du risque de MASLD, de MASH et de fibrose hépatique, ainsi qu’à une diminution du risque de décompensation hépatique, de mortalité et de cancer hépatique chez les personnes atteintes de cirrhose (3). Il n’y a cependant aucune étude randomisée contrôlée permettant de recommander les statines comme un traitement spécifique de la MASLD.
La metformine ou les inhibiteurs du SGLT2, utilisés pour leurs indications respectives, à savoir le diabète de type 2, l’insuffisance cardiaque ou les maladies rénales chroniques, peuvent être utilisés en toute sécurité en cas de MASLD (3, 6). Plusieurs études cas-témoins avec des patients diabétiques de type 2 suggèrent une réduction modérée de la stéatose hépatique et des ALT avec l’empaglifozine (21) et la licoglifozine (22). Des études de phase 4 sont en cours pour évaluer les effets des inhibiteurs du SGLT-2 sur la MASLD chez des patients avec un diabète de type 2.
Pareillement, en accord avec les recommandations de l’EASL et les recommandations de prescriptions de l’ANSM, les analogues des récepteurs du GLP-1 (sémaglutide, liraglutide ) ou co-agonistes (tirzepatide…) peuvent être utilisés en toute sécurité en cas de diabète de type 2 ou d’obésité sévère (3, 6). Cependant, bien que plusieurs études suggèrent une amélioration des lésions histologiques de la MASLD chez les patients traités par analogue du GLP-1, ces traitements ne sont pas recommandés et autorisés comme traitement de la MASLD. Comme pour les inhibiteurs du SGLT2, des études cas-témoins ont suggéré que l’exposition aux analogues du GLP1 chez les personnes atteintes de diabète de type 2 ou d’obésité, est associée à une réduction des complications hépatiques (3). Une étude de phase 3 évaluant spécifiquement l’efficacité du semaglutide dans la MASH F2-F3 est en cours (tableau 1).
Concernant les thérapies spécifiques à la MASLD, seul le RESMETIROM a obtenu une l’autorisation de mise sur le marché par la Food and Drug Administration (FDA) aux États-Unis en mars 2024. Cet analogue oral des récepteurs béta-thyroïdiens (b-TRH) ne ciblant que le foie, est spécifiquement destiné à traiter les patients atteints de MASH avec fibrose hépatique modérée ou avancée (correspondant aux stades F2 et F3 de la maladie) associée à un régime alimentaire et à de l’exercice physique régulier et adapté (3). Les hormones thyroïdiennes réduisent la stéatose, inhibent la lipogenèse et limite la fibrogénèse hépatique. Dans un essai thérapeutique international contrôlé randomisé de phase 3 incluant 966 patients avec NASH (score NAS≥ 4) fibrosante (stades 1B, 2 et 3) prouvée par biopsie, les doses de 80 mg et de 100 mg de RESMETIROM ont été supérieures au placebo en ce qui concerne la résolution de la NASH et l’amélioration de la fibrose hépatique d’au moins un stade, sans différences significatives entre les groupes concernant les effets secondaires (23). Les enzymes hépatiques et les lipides sériques ont également été réduits de manière significative, tandis que les effets sur le contrôle de la glycémie et le poids corporel n’étaient pas significatifs. Bien que son efficacité semble démontrée, il n’y a actuellement pas suffisamment de données sur la durabilité des bénéfices histologiques, sur la prédiction individuelle de la réponse, sur les résultats liés au foie et sur la sécurité à long terme (3). Le traitement, nécessitant une évaluation et une autorisation par les Agences Européennes et Françaises du médicament, n’est pas encore disponible en France.
La vitamine E, vitamine liposoluble aux propriétés anti-oxydantes, anti-inflammatoires et anti-apoptotiques, réduirait la lipogénèse de novo et diminuerait la stéatose hépatique (24). Cependant, devant l’absence d’études solides de phase 3 permettant de démontrer son efficacité histologique sur la stéatohépatite et la fibrose hépatique et devant de potentiels des risques à long terme, l’EASL-EASD-EASO ne recommande pas la vitamine E comme traitement de la MASLD (3).
Les acides biliaires comme l’acide ursodesoxycholique (AUDC) ou l’acide obéticholique (OCA), malgré leurs effets hépato-protecteurs et antioxydants, n’ont pas encore apporté la preuve de leur efficacité dans la MASLD et présentent des effets indésirables invalidants voir sévères (prurit, asthénie…) (3). Des études sont encore en cours notamment avec l’acide 24-norursodesoxycholique (Étude de phase IIb – NCT05083390). De nombreuses molécules, comme les agonistes Pan-PPAR (lanifibranor ), les analogues du FGF-21 (pegozafermin…), les analogues du FGF-19 (aldafermin…), les inhibiteurs du récepteur de la chimiokine CCR2/5 (cenicriviroc…) sont en cours de développement et font l’objet d’étude de phases II ou III actuellement dans la MASH avec des résultats préliminaires intéressants et prometteurs.
À l’heure actuelle, il n’existe pas de marqueurs spécifiques de réponse thérapeutique. La réalisation de biopsie hépatique n’est pas souhaitable et n’est pas recommandé par l’EASL. Cependant, les tests non invasifs sont particulièrement intéressants pour le suivi car, dans plusieurs études de cohortes (25), leurs modifications dans le temps semblaient corréler au risque de complications. Certaines études suggéraient une amélioration de la stéatohépatite en cas de réduction du MRI-PDFF≥ 30 % ou d’une diminution du taux d’ALAT ≥ 17 UI/L. À ce titre, l’EASL-EASD-EASO et l’AASLD proposent d’utiliser l’amélioration des ALAT ou la réduction de la graisse intrahépatique mesurée par IRM comme marqueurs d’intérêt pour évaluer la réponse thérapeutique (3, 6). Des études sont encore nécessaires pour mieux monitorer la réponse aux traitements.
Conclusion
Les hépatopathies stéatosiques secondaires à un syndrome métabolique, notamment à un diabète de type 2 ou une obésité, sont fréquentes et potentiellement sévères. La physiopathologie complexe de cette atteinte hépatique, comprend à la fois un déséquilibre alimentaire associée à une sédentarité, à un microbiote altéré et à un terrain génétique prédisposant, qui peut induire une accumulation d’énergie stockée sous forme de graisse dans le foie et dans le tissu adipeux, responsables à terme d’une insulino-résistance et de troubles métaboliques. Une prise en charge nutritionnelle et une activité physique régulière et adaptée, permettant une perte de poids d’au moins 5 %, constituent la pierre angulaire de la prise en charge de la MALSD. L’optimisation de la prise en charge médicamenteuse ou non et des comorbidités (obésité, diabète de type 2, dyslipidémie ) est indispensable pour limiter le développement et la progression de la maladie. Avec des résultats significatifs sur la MASH et la fibrose hépatique, le resmetirom, analogue oral des récepteurs béta-thyroïdiens (b-TRH) autorisé par la FDA aux États-Unis depuis mars 2024 en cas de MASH avec fibrose F2 ou F3, est un traitement prometteur nécessitant une évaluation et une autorisation par les Agences Européennes et Françaises du médicament. De nombreuses autres molécules prometteuses sont en cours de développement dans des études de phase 2 et 3.
Remerciements : Je remercie le Professeur Jérôme BOURSIER (Service d’hépato-gastro-entérologie et oncologie médicale, CHU d’Angers) pour sa confiance, son soutien et ses précieux conseils.
Références
- Rinella ME, Lazarus JV, Ratziu V, Francque SM, Sanyal AJ, Kanwal F, et al. A multisociety Delphi consensus statement on new fatty liver disease nomenclature. J Hepatol. 2023 Dec;79(6):1542–56.
- Younossi ZM, Golabi P, Paik JM, Henry A, Van Dongen C, Henry The global epidemiology of nonalcoholic fatty liver disease (NAFLD) and nonalcoholic steatohepatitis (NASH): a systematic review. Hepatology. 2023 Apr 1;77(4):1335–47.
- European Association for the Study of the Liver (EASL), European Association for the Study of Diabetes (EASD), European Association for the Study of Obesity (EASO). EASL-EASD-EASO Clinical Practice Guidelines on the management of metabolic dysfunction-associated steatotic liver disease (MASLD). J Hepatol. 2024 Sep;81(3):492–542.
- Younossi ZM, Golabi P, de Avila L, Paik JM, Srishord M, Fukui N, et The global epidemiology of NAFLD and NASH in patients with type 2 diabetes: A systematic review and meta-analysis. J Hepatol. 2019 Oct;71(4):793–801.
- Riazi K, Azhari H, Charette JH, Underwood FE, King JA, Afshar EE, et The prevalence and incidence of NAFLD worldwide: a systematic review and meta-analysis. Lancet Gastroenterol Hepatol. 2022 Sep;7(9):851–61.
- Rinella ME, Neuschwander-Tetri BA, Siddiqui MS, Abdelmalek MF, Caldwell S, Barb D, et al. AASLD Practice Guidance on the clinical assessment and management of nonalcoholic fatty liver disease. 2023 May 1;77(5):1797–835.
- Bischoff SC, Ockenga J, Eshraghian A, Barazzoni R, Busetto L, Campmans-Kuijpers M, et Practical guideline on obesity care in patients with gastrointestinal and liver diseases – Joint ESPEN/UEG guideline. Clin Nutr. 2023 Jun;42(6):987–1024.
- Stefan N, Yki-Järvinen H, Neuschwander-Tetri BA. Metabolic dysfunction-associated steatotic liver disease: heterogeneous pathomechanisms and effectiveness of metabolism-based The Lancet Diabetes & Endocrinology [Internet]. 2024 Dec 13 [cited 2024 Dec 17]; Available from: https://www.sciencedirect.com/science/article/pii/S2213858724003188
- Yki-Järvinen H, Luukkonen PK, Hodson L, Moore Dietary carbohydrates and fats in nonalcoholic fatty liver disease. Nat Rev Gastroenterol Hepatol. 2021 Nov;18(11):770-86.
- Eslam M, Valenti L, Romeo Genetics and epigenetics of NAFLD and NASH: Clinical impact. J Hepatol. 2018 Feb;68(2):268–79.
- Aron-Wisnewsky J, Vigliotti C, Witjes J, Le P, Holleboom AG, Verheij J, et Gut microbiota and human NAFLD: disentangling microbial signatures from metabolic disorders. Nat Rev Gastroenterol Hepatol. 2020 May;17(5):279–97.
- Boursier J, Mueller O, Barret M, Machado M, Fizanne L, Araujo-Perez F, et The severity of nonalcoholic fatty liver disease is associated with gut dysbiosis and shift in the metabolic function of the gut microbiota. Hepatology. 2016 Mar;63(3):764–75.
- Boursier J, Hagström H, Ekstedt M, Moreau C, Bonacci M, Cure S, et Non-invasive tests accurately stratify patients with NAFLD based on their risk of liver-related events. J Hepatol. 2022 May;76(5):1013–20.
- Kleiner DE, Brunt EM, Wilson LA, Behling C, Guy C, Contos M, et Association of Histologic Disease Activity With Progression of Nonalcoholic Fatty Liver Disease. JAMA Netw Open. 2019 Oct 2;2(10):e1912565.
- Vilar-Gomez E, Martinez-Perez Y, Calzadilla-Bertot L, Torres-Gonzalez A, Gra-Oramas B, Gonzalez-Fabian L, et Weight Loss Through Lifestyle Modification Significantly Reduces Features of Nonalcoholic Steatohepatitis. Gastroenterology. 2015 Aug;149(2):367-378.e5; quiz e14-15.
- Malespin MH, Barritt AS, Watkins SE, Schoen C, Tincopa MA, Corbin KD, et al. Weight Loss and Weight Regain in Usual Clinical Practice: Results From the TARGET-NASH Observational Cohort. Clin Gastroenterol Hepatol. 2022 Oct;20(10):2393-2395.e4.
- Verrastro O, Panunzi S, Castagneto-Gissey L, De Gaetano A, Lembo E, Capristo E, et al. Bariatric-metabolic surgery versus lifestyle intervention plus best medical care in non-alcoholic steatohepatitis (BRAVES): a multicentre, open-label, randomised Lancet. 2023 May 27;401(10390):1786–97.
- Haute Autorité de Santé [Internet]. [cited 2024 Dec 17]. Obésité de l’adulte : prise en charge de 2e et 3e Available from: https://www.has-sante.fr/jcms/p_3346001/fr/obesite-de-l-adulte-prise-en-charge-de-2e-et-3e-niveaux
- Haute Autorité de Santé [Internet]. [cited 2024 Dec 17]. Chirurgie métabolique : traitement chirurgical du diabète de type 2 – Rapport d’évaluation. Available from: https://www.has-sante.fr/jcms/p_3303025/fr/chirurgie-metabolique-traitement-chirurgical-du-diabete-de-type-2-rapport-d-evaluation
- Athyros VG, Tziomalos K, Gossios TD, Griva T, Anagnostis P, Kargiotis K, et al. Safety and efficacy of long-term statin treatment for cardiovascular events in patients with coronary heart disease and abnormal liver tests in the Greek Atorvastatin and Coronary Heart Disease Evaluation (GREACE) Study: a post-hoc analysis. 2010 Dec 4;376(9756):1916–22.
- Kuchay MS, Krishan S, Mishra SK, Farooqui KJ, Singh MK, Wasir JS, et Effect of Empagliflozin on Liver Fat in Patients With Type 2 Diabetes and Nonalcoholic Fatty Liver Disease: A Randomized Controlled Trial (E-LIFT Trial). Diabetes Care. 2018 Aug;41(8):1801–8.
- Harrison SA, Manghi FP, Smith WB, Alpenidze D, Aizenberg D, Klarenbeek N, et al. Licogliflozin for nonalcoholic steatohepatitis: a randomized, double-blind, placebo-controlled, phase 2a study. Nat Med. 2022 Jul;28(7):1432–8.
- Harrison SA, Bedossa P, Guy CD, Schattenberg JM, Loomba R, Taub R, et A Phase 3, Randomized, Controlled Trial of Resmetirom in NASH with Liver Fibrosis. N Engl J Med. 2024 Feb 8;390(6):497–509.
- Sanyal AJ, Chalasani N, Kowdley KV, McCullough A, Diehl AM, Bass NM, et Pioglitazone, vitamin E, or placebo for nonalcoholic steatohepatitis. N Engl J Med. 2010 May 6;362(18):1675–85.
- Sanyal AJ, Anstee QM, Trauner M, Lawitz EJ, Abdelmalek MF, Ding D, et Cirrhosis regression is associated with improved clinical outcomes in patients with nonalcoholic steatohepatitis. Hepatology. 2022 May;75(5):1235–46.