Risques et avantages de la Combothérapie
POST’U 2018
MICI
Objectifs pédagogiques
- Connaître les indications de la combothérapie avec l’infliximab, l’adalimumab, le golimumab, le vedolizumab, l’ustekinumab
- Connaître les indications de la combothérapie dans la maladie de Crohn luminale et/ou fistulisante, et la RCH
- Connaître les risques à court et à long terme de la combothérapie
- Connaître la durée d’une combothérapie
- Quand et comment l’arrêter ?
Testez-vous
Nous vous invitons à tester vos connaissances sur l’ensemble des QCU tirés des exposés des différents POST'U. Les textes, diaporamas ainsi que les réponses aux QCM seront mis en ligne à l’issue des prochaines journées JFHOD.
Testez vos connaissances sur le sujet.
Les 5 points forts
- Chez un malade naïf d’immunomodulateur, l’efficacité de l’infliximab est meilleure quand il est associé d’emblée à l’azathioprine.
- Le bénéfice de la combothérapie avec l’adalimumab est moins bien établi qu’avec l’infliximab.
- La combothérapie augmente le risque d’infection opportuniste.
- Le risque de cancer sous combothérapie résulte de l’addition des risques néoplasiques propres de chacun des traitements associés.
- Le niveau de preuve pour associer systématiquement un immunosuppresseur au védolizumab ou à l’ustékinumab est faible, voire inexistant.
Liens d’intérêt
Conseils, interventions et transports auprès d’Abbvie, Ferring, HAC-pharma, Janssen, MSD, Pfizer, Takeda, Theradiag, Tillots.
Mots-clés : combothérapie, anti-TNF, immunosuppresseur.
Avec l’avènement de l’infliximab il y a près de 20 ans, la prise en charge des patients atteints de maladies inflammatoires chroniques de l’intestin (MICI) a été révolutionnée. Parmi les nombreuses questions soulevées par les anti-TNF depuis, celle de la combinaison avec un immunosuppresseur conventionnel, à savoir une thiopurine ou le méthotrexate, – ce qui correspond à la combothérapie – reste toujours très débattue. En effet, la combothérapie paraît plus efficace que la monothérapie par un immunosuppresseur ou un anti-TNF, mais elle expose à un risque accru d’effets indésirables. Nous verrons dans cette revue quelles sont les indications actuelles de la combothérapie avec les anti-TNF dans les MICI, ses limites et ses modalités pratiques. L’arrivée, ces dernières années, de nouvelles biothérapies dont les mécanismes d’action sont différents de celui des anti-TNF a conduit exactement au même questionnement sur la combothérapie. Étant donné les belles perspectives thérapeutiques à venir dans le domaine des MICI, il est probable que la controverse autour de la combothérapie née avec les anti-TNF ne se refermera pas avant longtemps.
Combothérapie avec les anti-TNF
Le bénéfice de la combothérapie est à la fois pharmacologique (addition, voire synergie des deux traitements) et immunologique. En effet, tous les anticorps monoclonaux ont un pouvoir immunogène qui peut conduire à la formation d’anticorps anti-médicament, ce qui a pour conséquences une perte de réponse et des réactions allergiques. Il a été observé, dès les premiers travaux avec l’infliximab, que les patients qui recevaient également un immunosuppresseur conventionnel développaient moins d’anticorps anti-médicament que ceux traités par monothérapie [1].
La supériorité de l’association entre un immunosuppresseur conventionnel, en l’occurrence le méthotrexate, et un anti-TNF par rapport à la monothérapie est démontrée depuis longtemps en rhumatologie, et ce quelle que soit la nature de l’anticorps monoclonal testé, autrement dit qu’il soit chimérique ou bien totalement humanisé [2]. Il a fallu plus de temps en gastroentérologie.
Il existe en pratique trois situations au cours des MICI qui peuvent conduire à la prescription d’un anti-TNF en association avec un immunosuppresseur :
- chez un malade naïf de tout immunomodulateur, n’ayant donc jamais reçu aucune molécule de ces deux classes thérapeutiques, qui est candidat à une combothérapie d’emblée,
- chez un malade déjà traité par un traitement immunosuppresseur classique et ne répondant pas suffisamment à celui-ci, où l’anti-TNF sera ajouté en combothérapie au traitement en cours,
- chez un malade initialement répondeur à un traitement anti-TNF en monothérapie ayant secondairement perdu la réponse en raison d’une immunisation, pour lequel un immunosuppresseur conventionnel sera ajouté dans l’objectif de restaurer la réponse.
Nous verrons qu’il existe peu d’études spécifiquement dédiées à chacune de ces situations pour ce qui est de la maladie de Crohn, encore moins pour ce qui est de la rectocolite hémorragique, et que toutes les combinaisons possibles entre les différents immunosuppresseurs et anti-TNF n’ont pas été testées dans la littérature.
Efficacité de la combinaison d’un immunosuppresseur avec l’infliximab
L’infliximab est la molécule pour laquelle le niveau de preuve est le plus élevé. Nous disposons de travaux de bonne qualité à la fois dans la maladie de Crohn et dans la rectocolite hémorragique. Il est important de rappeler tout d’abord que l’infliximab est un anticorps chimérique, humanisé à 75 %, qui occasionne la formation d’anticorps anti-médicament (ATI) chez plus de la moitié des malades traités et que cette production d’ATI est précoce, survenant dans 90 % des cas au cours de la première année de traitement [3].
Maladie de Crohn
Les résultats de l’essai SONIC ont constitué une avancée considérable dans la prise en charge chez des malades naïfs de tout immunomodulateur. Cet essai contrôlé randomisé avec double placebo a pour la première fois démontré que la combothérapie infliximab + azathioprine était bien plus efficace que chacun de ces deux traitements pris isolément [4]. L’essai SONIC a permis de faire un bond énorme chez des patients qui ont une maladie de diagnostic récent – médiane de 2,3 ans dans l’essai – entre le traitement par azathioprine en monothérapie qui avait encore le vent en poupe à cette époque et la combothérapie, faisant passer le taux de rémission sans corticoïdes à la semaine 26 de 30,6 % à 56,8 %, soit un gain de 26,2 % (p < 0,001) (Figure 1). Cette différence était même de 31,7 % lorsque l’analyse était restreinte aux malades qui avaient des lésions endoscopiques actives à l’inclusion (p < 0,001). Lorsque l’on comparait l’efficacité de la combothérapie à celle de la monothérapie par infliximab, la différence en termes de rémission sans corticoïdes à la semaine 26 restait significative dans la population globale de l’étude, mais n’était plus que de 12,4 % (p = 0,022). Elle n’était plus significative chez les malades ayant des lésions endoscopiques au départ (p = 0,12).
Figure 1. Essai randomisé comparant l’azathioprine en monothérapie à l’infliximab en monothérapie à la combothérapie azathioprine + infliximab en traitement de la maladie de Crohn : taux de patients en rémission clinique sans corticoïdes à la semaine 26 (4)
A : Dans la population globale des patients inclus dans l’essai SONIC (n = 508)
B : Chez les malades qui avaient des lésions endoscopiques actives à l’inclusion (n = 325)
AZA : azathioprine ; IFX : infliximab.
Selon des modalités similaires à l’essai SONIC, un essai contrôlé randomisé en double aveugle a comparé l’efficacité d’une association infliximab + méthotrexate à l’infliximab en monothérapie au cours de la maladie de Crohn chez des malades naïfs d’anti-TNF, mais tous les patients avaient, dans cet essai, une corticothérapie d’induction. À la semaine 50, il n’existait aucune différence entre les deux bras de traitement [5] (Figure 2).
Figure 2. Essai randomisé comparant l’association infliximab + méthotrexate à l’infliximab seul en traitement de la maladie de Crohn : taux d’échec à la semaine 50 (5)
MTX : méthotrexate ; IFX : infliximab.
S’agissant des patients déjà en échec d’un traitement immunosuppresseur conventionnel, et candidats à l’infliximab, les données disponibles sont de moins bonne qualité. Dans l’ensemble, l’analyse post hoc des essais contrôlés comme de nombreuses études observationnelles rétrospectives sont plutôt en faveur d’une supériorité de la combothérapie par rapport à la monothérapie par infliximab [6-8] (Figure 3). Le rapport des cotes (OR) calculé à partir des essais contrôlés sur le taux de rémission à 6 mois était de 1,79 (intervalle de confiance à 95 % (IC 95 %) : 1,08-3,01) en faveur de la combothérapie [9]. Cet avantage est probablement lié à l’effet préventif de l’immunosuppresseur sur la formation d’ATI, que ce soit avec l’azathioprine ou le méthotrexate. L’avis des experts est donc de plutôt privilégier la prescription de l’infliximab en combothérapie chez les malades en échec de traitement immunosuppresseur classique, à l’exception des patients à risque élevé d’effet indésirable [10].
Figure 3. Persistance du traitement anti-TNF au cours de la maladie de Crohn selon qu’il soit instauré en monothérapie (mono) ou en combothérapie (combo) (8)
ADA : adalimumab ; IFX : infliximab.
Chez les patients répondeurs à l’infliximab en monothérapie qui se sont secondairement immunisés et ont perdu de ce fait le bénéfice du traitement, la reprise d’un immunosuppresseur, que ce soit l’azathioprine ou le méthotrexate, peut restaurer le bénéfice du traitement anti-TNF, en faisant disparaître les anticorps anti-médicament ce qui permet de retrouver des taux plasmatiques adéquats [11], avec un délai médian de 5 mois.
Peu de travaux ont évalué l’efficacité de la combothérapie en traitement de la maladie de Crohn fistulisante, en particulier dans sa localisation ano-périnéale. Il existe quelques données qui suggèrent qu’une combothérapie serait plus efficace que l’infliximab en monothérapie. Ainsi, dans la cohorte rétrospective française Rennes-Nancy constituée de 156 patients traités par infliximab dans cette indication, la coprescription d’un immunosuppresseur était un facteur indépendant associé à la réponse à long terme (p = 0,02) [12].
Rectocolite hémorragique
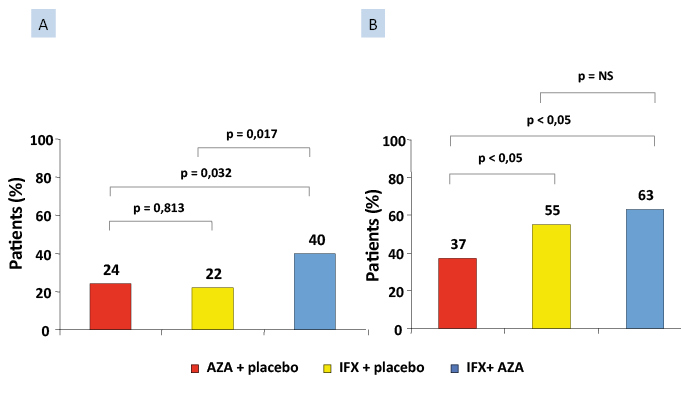
Un essai contrôlé randomisé avec double placebo similaire à l’essai SONIC a été mené chez 231 patients atteints de rectocolite hémorragique réfractaire [13]. Les patients ayant des poussées graves étaient exclus. Comme pour la maladie de Crohn, l’association infliximab et azathioprine était plus efficace que chacun de ces deux traitements en monothérapie selon le critère de jugement principal qui était la rémission clinique et endoscopique à la semaine 16 (Figure 4). Au niveau de la muqueuse, 63 % des malades traités en combothérapie étaient alors en rémission endoscopique, vs 55 % de ceux traités par infliximab en monothérapie (p = NS) et seulement 37 % de ceux traités par azathioprine seul (p < 0,05). Il faut néanmoins rappeler que cette étude était conçue pour un effectif de 600 malades, si bien qu’elle n’a pas la même force démonstrative que l’essai SONIC.
Figure 4. Essai randomisé comparant l’azathioprine en monothérapie à l’infliximab en monothérapie à la combothérapie azathioprine + infliximab en traitement de la rectocolite hémorragique (13)
A : taux de patients en rémission clinique et endoscopique sans corticoïdes à la semaine 16
B : taux de patients en rémission endoscopique à la semaine 16.
AZA : azathioprine ; IFX : infliximab.
Il existe aussi des séries rétrospectives qui ont évalué le bénéfice de la combothérapie avec l’infliximab au cours de la rectocolite hémorragique. La grande majorité des malades analysés étaient alors déjà en échec d’un traitement immunosuppresseur conventionnel [14]. En effet, la stratégie thérapeutique ascendante est de règle dans la rectocolite hémorragique et l’AMM des anti-TNF dans cette indication stipule qu’il faut un échec préalable des corticoïdes et des immunosuppresseurs. Si les données publiées demeurent assez hétérogènes, les avis d’experts recommandent comme pour la maladie de Crohn plutôt la combothérapie que la monothérapie par l’infliximab [10].
Pour la pratique
Quel que soit le type de MICI, la combothérapie infliximab et azathioprine est le traitement le plus efficace chez des malades naïfs d’anti-TNF. Chez les malades en échec des immunosuppresseurs à l’exception des malades à haut risque infectieux ou néoplasiques, il apparaît logique de débuter l’infliximab en combothérapie afin de prévenir la formation d’ATI. Comme nous verrons plus loin, l’objectif sera d’alléger le traitement dans un second temps.
Efficacité de la combinaison d’un immunosuppresseur avec l’adalimumab ou le golimumab
Les données publiées sur la combothérapie avec les anti-TNF sous-cutanés sont plus fragmentaires et concernent essentiellement l’adalimumab puisque le golimumab est plus récent et n’a été développé qu’en traitement de la rectocolite hémorragique.
Maladie de Crohn
Pendant longtemps les résultats de l’essai SONIC obtenus avec l’infliximab ont été extrapolés à l’adalimumab. Ce n’est que très récemment qu’un essai contrôlé randomisé a comparé la monothérapie par adalimumab à son association à l’azathioprine, à la dose de 25 à 100 mg/jour, chez des malades naïfs de tout immunomodulateur [15]. Cet essai multicentrique japonais appelé DIAMOND conduit en ouvert chez 176 patients est négatif selon le critère de jugement principal qui était la rémission clinique à la semaine 26 (Figure 5). Toutefois, le taux de réponse endoscopique à la semaine 26, définie par une réduction du score endoscopique simplifié (SES-CD) d’au moins 8 points ou par un score total inférieur à 5 points, était significativement plus élevé dans le groupe combothérapie que dans le groupe monothérapie (84,2 % et 63,8 % respectivement ; p = 0,02). Il n’existe pas d’étude dédiée avec le méthotrexate.
Figure 5. Essai randomisé comparant l’adalimumab en monothérapie à la combothérapie azathioprine + adalimumab (15)
A : taux de patients en rémission clinique sans corticoïdes à la semaine 26.
B : taux de patients en réponse endoscopique à la semaine 16.
ADA : adalimumab ; AZA : azathioprine.
Chez des patients qui sont déjà en échec d’un traitement immunosuppresseur, l’intérêt à poursuivre celui-ci lorsqu’un traitement par adalimumab est initié semble modeste. Ainsi, les analyses post hoc des données des essais randomisés n’ont pas identifié de supériorité de la combothérapie par rapport à l’adalimumab en monothérapie [9]. Selon une méta-analyse, le bénéfice clinique à 1 an à associer un immunosuppresseur conventionnel à l’adalimumab est faible, puisqu’il n’est observé que sur la réponse clinique et non sur la rémission [16]. Les séries rétrospectives menées sur des durées plus prolongées sont en revanche pour la plupart d’entre elles en faveur de la combothérapie [7]. Ainsi, dans la cohorte de l’Hôpital Saint-Antoine, dont la médiane de durée de traitement anti-TNF était de 39 mois, la proportion de patients en réponse clinique à 2 ans sous adalimumab en combothérapie était plus élevée qu’en monothérapie [8]. En outre, et comme avec l’infliximab, la durée du traitement par adalimumab était plus longue lorsqu’il était prescrit en combothérapie (Figure 3). C’est donc par analogie avec les études menées en rhumatologie [17], sur des arguments indirects en gastroentérologie et pour des raisons immunologiques, que l’avis des experts est de privilégier la combothérapie avec l’adalimumab chez les patients atteints de maladie de Crohn qui sont en échec de traitement immunosuppresseur classique [10].
Rectocolite hémorragique
Il n’y a aucune étude avec l’adalimumab ou le golimumab qui ont évalué le bénéfice à instaurer un anti-TNF en combothérapie d’emblée chez des malades naïfs de tout immunomodulateur.
Le bénéfice qu’il y a à poursuivre un immunosuppresseur inefficace lors de l’instauration d’un traitement par adalimumab ou golimumab a fait l’objet de très peu de travaux. Lorsque le niveau de preuve est aussi faible, les recommandations demeurent du niveau de l’avis d’expert et se basent sur l’extrapolation des études menées avec l’infliximab dans la rectocolite hémorragique, et avec l’adalimumab dans la maladie de Crohn pour plutôt conseiller la poursuite de l’immunosuppresseur [18].
Pour la pratique
L’avantage à associer un immunosuppresseur conventionnel à l’adalimumab ou au golimumab semble plus faible qu’avec l’infliximab, y compris chez des malades naïfs de tout immunomodulateur. Même si la combothérapie avec les anti-TNF sous-cutanés est recommandée par la plupart des avis d’experts, son bénéfice clinique n’est pas établi et apparaît avant tout immunologique.
Effets indésirables de la combinaison d’un immunosuppresseur avec un anti-TNF
La survenue d’effets secondaires avec une combothérapie est de facto plus fréquente qu’en cas de monothérapie puisque l’on va alors cumuler les effets indésirables spécifiques de chacune des deux molécules administrées (se référer aux fiches médicaments du GETAID pour le détail et la conduite à tenir devant les effets indésirables les plus fréquents – https://www.getaid.org). Par ailleurs, l’immunodépression prolongée due à la combinaison de deux immunomodulateurs puissants, mais aussi à la maladie elle-même et parfois au patient (comorbidités, âge) expose théoriquement à un risque infectieux et néoplasique accru.
Risque infectieux
Le risque infectieux lié à la combothérapie est avant tout celui d’une infection opportuniste, autrement dit une infection occasionnée par un micro organisme qui n’a pas ou peu d’effet pathogène en situation normale, mais qui est responsable d’une infection grave à la faveur d’une autre affection ou de son traitement [19]. Ce risque est non seulement lié aux traitements, mais aussi à l’âge, à la dénutrition, aux comorbidités et la sévérité de la MICI qui constituent des facteurs de risque indépendants et cumulatifs.
Selon l’European Crohn’s & Colitis Organisation (ECCO), les patients traités par une association d’immunomodulateurs, incluant aussi les corticoïdes systémiques, sont à risque d’infection opportuniste (recommandation de grade C) [20]. Il reste toutefois bien difficile d’apprécier très précisément le risque d’infection opportuniste sous combothérapie, car les données publiées sont jusqu’à présent rétrospectives, observationnelles et surtout déclaratives. Les principales études disponibles ayant évalué le risque d’infection sévère sont synthétisées dans le tableau I. Les résultats de la cohorte prospective européenne I-CARE qui est en cours de constitution seront donc très attendus.
| Étude | IS monothérapie OR (IC 95 %) | Anti-TNF monothérapie OR (IC 95 %) | Combothérapie OR (IC 95 %) |
|---|---|---|---|
| Toruner et al. | 3,40 (1,50-7,50) | 11,1 (0,80-148) | 1,60 (0,10-19) |
| Marehbian et al. | 3,63 (2,36-5,57) | 1,30 (0,40-4,25) | 6,18 (2,69-14,22) |
| Deepak et al. | 9,99 (1,28-78,16) | 1,95 (1,06-3,59) | 3,72 (1,82-7,59) |
| OR : odds ratio ; IC 95 % : intervalle de confiance à 95 %. | |||
Tableau I. Risque d’infection sévère selon le type de traitement de la MICI (d’après 10)
Le risque d’infection opportuniste existe quel que soit l’immunomodulateur prescrit, que ce soit un corticoïde, un immunosuppresseur conventionnel ou un anti-TNF, avec un OR compris entre 3,3 et 4,4 selon les molécules [21]. C’est en fait la combinaison de ces traitements qui va démultiplier le risque d’infection opportuniste comme cela a été observé dans l’étude cas-témoin de la Mayo Clinic.
La nature et surtout la sévérité de ces infections opportunistes est très variable puisque dans les études l’éventail s’étend d’infections bénignes comme des mycoses buccales ou gynécologiques à des récurrences herpétiques jusqu’à des infections systémiques mortelles. Il est en pratique très difficile de déterminer quelle est alors la part de l’anti-TNF et celle de l’immunosuppresseur. On admet généralement que l’anti-TNF va favoriser les infections à germe intracellulaire telles que la tuberculose ou la légionellose alors que les thiopurines augmentent le risque d’infection virale (virus du groupe herpes, papilloma virus).
En somme, il faut retenir avec un niveau de preuve scientifique faible que le risque d’infection opportuniste sous combothérapie est théoriquement plus élevé qu’en cas de monothérapie. Il est espéré que les études en cours nous permettront de mieux définir ce risque et plus particulièrement celui d’infection sévère qui sont celles qui sont redoutées par les malades et les prescripteurs.
Risque néoplasique
Avec l’infection, l’autre crainte à prescrire une combothérapie est de favoriser la survenue d’un cancer. Cette question difficile a fait l’objet de nombreuses études au cours des dernières années. Toutefois, il est impossible d’apprécier le risque néoplasique lié à la combothérapie sans avoir bien défini le risque néoplasique propre de chacun des immunomodulateurs qui la composent. Plusieurs études de cohorte, dont l’étude française CESAME, ont démontré que la prise de la prise de thiopurines favorisait la survenue de plusieurs types de cancers : lymphomes non hodgkiniens, cancers cutanés non mélanocytaires ou cancers des voies urinaires [22, 23]. Qui plus est, ces travaux ont permis de personnaliser le risque néoplasique associé aux thiopurines, en définissant les populations susceptibles de développer de tels cancers et à l’inverse celles qui avaient un risque identique de celui de la population générale. Jusqu’à présent aucun sur-risque de cancer associé à la prise de méthotrexate n’a été identifié. En ce qui concerne les anti-TNF pour lesquels nous avons un recul de 20 ans, il a été identifié une augmentation du risque de mélanome, avec un OR de 1,9 (IC 95 % : 1,0-3,7), dans une étude nord-américaine qui était dédiée aux MICI et basée sur 50 920 patients-années de traitement [23]. Tout récemment, une étude de l’ANSM effectuée à partir des données de l’Assurance maladie collectées entre 2009 et 2014 à partir de 187 362 patients atteints de MICI fait état d’un risque plus important de lymphome sous infliximab en monothérapie, avec un hazard ratio de 1,75 (IC 95 % : 1,15-3,03) [24] (Tableau II). Comme cela a été fait pour les immunosuppresseurs avec la cohorte CESAME, il reste à mieux définir quels seraient les sous-groupes de malades les plus à risque de cancers sous anti-TNF. Ici encore, les résultats de la cohorte I-CARE devraient être en mesure de répondre quant au risque néoplasique lié à chaque classe thérapeutique utilisée en traitement des MICI.
| Traitement | Ni thiopurine, ni infliximab | Thiopurine monothérapie | Infliximab monothérapie | Combothérapie |
|---|---|---|---|---|
| Patient/année | 522 487 | 111 113 | 60 736 | 11 514 |
| Lymphome : n HR (IC 95 %) |
166 | 56 2,02 (1,08-2,26) |
31 1,75 (1,15-3,03) |
13 4,83 (2,51-9,16) |
| HR : hasard ratio ; IC 95 % : intervalle de confiance à 95 %. | ||||
Tableau II. Données de l’Assurance maladie collectés entre 2009 et 2014 (187 362 patients avec un suivi médian de 4,9 ans) sur le risque de lymphome associé aux traitements des MICI [24].
Le risque néoplasique d’une combothérapie est donc au minimum l’addition de celui de chacun des deux immunomodulateurs associés comme cela a été observé dans les données de l’Assurance maladie [24, 25] (Tableau II). Toute la question est de savoir si l’association d’un immunosuppresseur, qui est le plus souvent une thiopurine au cours des MICI, à un anti-TNF exerce un effet synergique qui augmenterait leurs risques néoplasiques respectifs. Le problème du lymphome T hépato-splénique est à ce titre emblématique. C’est un évènement exceptionnel mais redoutable puisqu’il survient le plus souvent chez des hommes jeunes et que son pronostic est catastrophique. Parmi les cas observés chez des malades atteints de MICI, la plupart étaient traités par thiopurine et anti-TNF [26]. Toutefois, selon les données colligées par la Food and Drug Administration, ce risque est avant tout lié à la prise de thiopurines et n’est pas augmenté par la combothérapie [27]. En outre, comme la plupart de ces cas de lymphomes T hépato-spléniques étaient observés après les deux premières années de traitement par combothérapie, il semble prudent d’éviter de prolonger l’association thiopurine – anti-TNF au-delà si l’on veut réduire ce risque [28]. À ce jour, il n’y a pas d’élément pour affirmer que la combothérapie soit un facteur de risque indépendant associé un risque plus important de cancer cutané, que ce soit un carcinome ou un mélanome, ou gynécologique [25].
En miroir du risque néoplasique lié aux traitements des MICI que nous venons de détailler, il faut aussi prendre en compte l’effet positif de ces médicaments sur l’inflammation chronique que ce soit au niveau systémique, que l’on sait liée au risque d’accident vasculaire artériel, ou muqueux, qui est à l’origine du risque de cancers digestifs associés aux MICI. Au cours des années à venir, nous saurons mieux catégoriser les patients selon les risques liés à la MICI et à son traitement, de manière à personnaliser le traitement sur la base d’un rapport bénéfice-risque qui fait déjà l’objet de travaux de modélisation [29].
Autres risques :
Le risque allergique, qui concerne surtout l’infliximab, n’est non seulement pas augmenté en cas de combothérapie, mais diminué par rapport à l’anti-TNF en monothérapie puisque la co-prescription d’un immunosuppresseur conventionnel prévient la formation d’ATI qui sont à l’origine du phénomène.
Les manifestations paradoxales observés sous anti-TNF, qu’elles soient cutanées ou rhumatismales, semblent totalement indépendantes de la prescription associée d’un immunosuppresseur.
Pour la pratique
Le risque d’effets secondaires chez les patients traités en combothérapie est avant tout celui de chacune des molécules prescrites. La combinaison d’un immunosuppresseur et d’un anti-TNF semble légèrement augmenter le risque d’infection opportuniste et a un effet additif sur celui de cancer par rapport à la monothérapie. Des études sont en cours afin de mieux connaître ces risques et surtout d’identifier la typologie des malades qui sont les plus exposés.
Durée de la combothérapie entre un immunosuppresseur et un anti-TNF
L’instauration d’une combothérapie entre un immunosuppresseur et un anti-TNF a pour objectif de mettre en rémission clinique et si possible endoscopique un patient ayant une MICI en poussée. Ce n’est qu’une fois ce résultat obtenu que la question de l’allègement thérapeutique peut s’envisager.
Pourquoi discuter un allégement du traitement ?
D’un côté et comme nous venons de le voir, l’association entre un immunosuppresseur et un anti-TNF est la stratégie la plus efficace dans le traitement de la maladie de Crohn et de la rectocolite hémorragique. Ceci est lié à l’effet propre de chacun de ces deux traitements sur la maladie, de la synergie de l’association et de l’effet préventif des thiopurines ou du méthotrexate sur la formation d’anticorps anti-médicament, qui sont associés à la survenue de réactions allergiques et d’échappement thérapeutique. D’un autre côté, les risques de la combothérapie cumulent ceux des immunosuppresseurs et des anti-TNF et sont donc plus importants qu’en cas de monothérapie. Toute la question est donc de savoir à partir de quel moment les inconvénients de la combothérapie sont supérieurs à ses avantages. Hélas, aucun essai contrôlé sur la combothérapie n’a été mené au-delà de un an. C’est donc par la lecture d’études observationnelles rétrospectives, d’un niveau de preuve plus modeste, que l’on peut répondre.
Dans la perspective d’une désescalade thérapeutique, il faut également prendre en compte la sévérité d’une éventuelle rechute de la MICI et donc anticiper son traitement. À titre d’exemples, la reprise d’un traitement par thiopurine est à la fois efficace et bien tolérée alors que celle de l’infliximab, surtout quand la pause thérapeutique a été longue, expose à un risque de réaction d’hypersensibilité lors de la deuxième perfusion, et donc d’échec [30, 31].
Quand alléger le traitement ?
La formation d’anticorps anti-médicament est un phénomène précoce qui survient au cours des 6 à 12 premiers mois d’un traitement anti-TNF [3]. C’est pourquoi il est déconseillé d’alléger le traitement en interrompant l’immunosuppresseur avant d’avoir passé ce cap.
Après la première année de traitement, il semble que les malades traités en combothérapie aient une maladie mieux contrôlée que ceux recevant l’anti-TNF en monothérapie, en particulier en cas de maladie de Crohn ano-périnéale fistulisante (cf supra) [6-8, 12] (Figure 3).
Comment alléger le traitement ?
Les deux moyens pour alléger le traitement chez un malade en combothérapie sont la réduction de la dose ou l’interruption d’un des traitements en cours.
Selon une étude prospective récente de l’équipe de Saint-Étienne, il est possible de réduire de moitié la dose d’azathioprine chez un malade en combothérapie avec l’infliximab, sans conséquence clinique à un an, ni modification des taux résiduels de médicament [32]. La réduction de la dose d’anti-TNF est également possible chez un malade en rémission et dont les taux résiduels de médicament sont élevés [33].
La question de l’arrêt d’un des traitements chez un malade traité en combothérapie n’est envisageable qu’en cas de rémission clinique. L’obtention d’une rémission profonde, c’est-à-dire biologique (C-réactive protéine, calprotectine fécale), endoscopique, voire histologique – dans la rectocolite hémorragique uniquement – semble associée à une rémission plus durable et constitue la situation idéale pour envisager l’arrêt d’un des deux traitements. Toutes les options sont alors théoriquement possibles : arrêt de l’IS, arrêt de la biothérapie ou bien poursuite de la combothérapie. Les dosages pharmacologiques des médicaments semblent ici très utiles pour guider le choix du traitement à interrompre [34, 35]. Des essais randomisés comparant ces trois possibilités ont débuté. Dans l’avenir, il est possible que le traitement des MICI évolue vers des cycles de traitement, alternant des phases de traitements plus ou moins intensives quand la maladie est active et des périodes de pause où le traitement serait allégé en cas de rémission. Des études de cohorte sur de longues périodes sont en cours pour évaluer cette approche.
Combothérapie avec les autres biothérapies
L’arsenal thérapeutique contre les MICI s’est considérablement étoffé au cours des dernières années. Nous disposons désormais d’anticorps monoclonaux ciblant d’autres voies que celle du TNFa. Pour le moment dans notre pays, nous avons accès au védolizumab en traitement de la rectocolite hémorragique et à l’ustékinumab pour la maladie de Crohn. De nouveau, la question de la combothérapie avec ces biothérapies de nouvelle génération a été posée. Cependant, aucun essai thérapeutique n’a comparé à ce jour la combothérapie à la monothérapie avec ces traitements. Il est même probable qu’il n’y ait jamais d’étude en ce sens. C’est donc sur des éléments de preuve indirects que l’on peut apporter des éléments de réponse.
Combothérapie avec le védolizumab
Le védolizumab est un anticorps monoclonal ciblant l’intégrine a4b7 qui s’administre par voie intraveineuse et qui a démontré son efficacité en traitement de la maladie de Crohn et de la rectocolite hémorragique, si bien qu’il a obtenu une autorisation de mise sur le marché (AMM) dans ces deux indications après échec des anti-TNF en 2014. Depuis le début de l’année 2017, le remboursement de ce traitement n’est plus assuré dans la maladie de Crohn en France. Il est probable que le réexamen du dossier de ce médicament par les autorités permette dans un avenir proche qu’il soit de nouveau accessible en traitement des patients atteints de maladie de Crohn.
Dans les essais pivots de phase III, il n’a pas été observé d’avantage à associer un immunosuppresseur au védolizumab en traitement de la maladie de Crohn ou de la rectocolite hémorragique [36, 37].
Plusieurs études observationnelles ont été publiées depuis et ont cherché à identifier des facteurs associés à une meilleure efficacité de védolizumab. Il faut souligner que la plupart des malades évalués avaient déjà reçu des immunosuppresseurs et des anti-TNF. Les études concernant le védolizumab en traitement de la rectocolite hémorragique sont synthétisées dans le tableau III. Sur les 483 malades traités au total, aucune des séries publiées in extenso jusqu’à présent n’a mis en évidence un avantage à associer un immunosuppresseur, qui était alors très majoritairement l’azathioprine, au védolizumab en comparaison à la monothérapie.
| Auteur | Pays | Année | n sous IS / N ( %) | Effet |
|---|---|---|---|---|
| Shelton E et al. [42] | États-Unis | 2015 | 17/65 (27) | Aucun |
| Vivio EE et al. [43] | États-Unis | 2016 | 10/21 (48) | Aucun |
| Baumgart D et al. [44] | Allemagne | 2016 | 88/115 (77) | Aucun |
| Amiot A et al. [45] | France | 2016 | 26/121 (21) | Aucun |
| Kopylov U et al. [46] | Israël | 2017 | 16/69 (23) | Aucun |
| Eriksson C et al. [47] | Suède | 2017 | 42/92 (46) | Aucun |
| ND : non disponible. | ||||
Tableau III. Effet de l’association d’un immunosuppresseur (IS) avec le védolizumab sur son efficacité au cours de la rectocolite hémorragique dans les études observationnelles
Il n’y a donc pour le moment aucune donnée scientifique qui soutienne l’utilisation du védolizumab en combothérapie.
Combothérapie avec l’ustékinumab
L’ustékinumab est un anticorps monoclonal dirigé contre la sous-unité p40 commune aux interleukines 12 et 23 qui a été développé dans le psoriasis et a obtenu en 2017 une AMM pour le traitement de la maladie de Crohn réfractaire.
Dans les essais pivots de phase II et III ayant comparé l’ustékinumab au placebo chez des malades en échec des immunosuppresseurs conventionnels et souvent aussi des anti-TNF, la prise de thiopurines ou de méthotrexate à l’inclusion n’était pas associée à une meilleure efficacité [38, 39].
Plusieurs séries rétrospectives ont évalué la réponse à l’ustékinumab dans des cohortes de patients ayant une maladie de Crohn réfractaire aux immunosuppresseurs et aux anti-TNF. Les données des 488 malades inclus jusqu’à présent dans ces études observationnelles sont contradictoires (Tableau IV). La série française du GETAID a montré que les malades traités par immunosuppresseurs et ustékinumab avaient une meilleure réponse que ceux traités par ustékinumab en monothérapie (OR : 5,43 ; IC 95 % :1,14-25,77) [40]. À l’inverse, la série canadienne la plus récente, a observé que les malades traités en combothérapie avaient une moins bonne réponse à l’ustékinumab que ceux traités en monothérapie (OR : 0,37 ; IC 95 % : 0,15-0,89) [41].
| Auteur | Pays | Année | n sous IS / N ( %) | Effet |
|---|---|---|---|---|
| Kopylov U et al. [48] | Canada | 2014 | 4/38 (11) | Aucun |
| Wils P et al. [40] | France | 2016 | 18/122 (15) | Bénéfique |
| Harris KA et al. [49] | États-Unis | 2016 | 19/45 (65) | Aucun |
| Khorrami S et al. [50] | Espagne | 2016 | 42/116 (36) | Aucun |
| Ma C et al. [41] | Canada | 2017 | 73/167 (44) | Néfaste |
| ND : non disponible. | ||||
Tableau IV. Effet de l’association d’un immunosuppresseur (IS) avec l’ustékinumab sur son efficacité au cours de la maladie de Crohn hémorragique dans les études observationnelles
L’ensemble de ces données disponibles ne justifie pas l’usage de l’ustékinumab en combothérapie de manière systématique.
Conclusions, perspectives
La controverse autour de la monothérapie ou de la combothérapie née avec les anti-TNF n’est toujours pas résolue. Il y a un avantage incontestable à associer un immunosuppresseur à l’infliximab, en traitement induction chez des malades naïfs d’immunomodulateurs, que ce soit en traitement de la maladie de Crohn ou de la rectocolite hémorragique. En revanche, le bénéfice de la combothérapie chez des malades en échec d’immunosuppresseurs ou chez ceux traités par adalimumab et golimumab est incertain. C’est surtout pour éviter l’immunisation qu’il est conseillé d’associer un immunosuppresseur conventionnel à un anti-TNF. À ce jour, le niveau de preuve pour associer systématiquement un immunosuppresseur au védolizumab ou à l’ustékinumab est inexistant. Nous disposerons dans un avenir proche de nouvelles molécules pour traiter les MICI, à commencer par le tofacitinib qui devrait être disponible dans la rectocolite hémorragique dans la période à venir. L’élargissement des options thérapeutiques disponibles et donc des combinaisons entre les molécules devrait faire émerger de nouvelles problématiques. Il est possible que la combothérapie du futur associe deux biothérapies ensemble. Si l’impact économique d’une telle approche est prévisible, il faudra qu’elle fasse la preuve d’une grande efficacité et de son innocuité pour être diffusée.
Références
- Vermeire S, Noman M, Van Assche G, et al. Effectiveness of concomitant immunosuppressive therapy in suppressing the formation of antibodies to infliximab in Crohn’s disease. Gut. 2007;56:1226-31.
- Orme ME, Macgilchrist KS, Mitchell S, et al. Systematic review and network meta-analysis of combination and monotherapy treatments in disease-modifying antirheumatic drug-experienced patients with rheumatoid arthritis: analysis of American College of Rheumatology criteria scores 20, 50, and 70. Biologics. 2012;6:429-64.
- Ungar B, Chowers Y, Yavzori M, et al. The temporal evolution of antidrug antibodies in patients with inflammatory bowel disease treated with infliximab. Gut. 2014;63:1258-64.
- Colombel JF, Sandborn WJ, Reinisch W, et al. Infliximab, azathioprine, or combination therapy for Crohn’s disease. N Engl J Med 2010;362:1383-95.
- Feagan BG, McDonald JW, Panaccione R, et al. Methotrexate in combination with infliximab is no more effective than infliximab alone in patients with Crohn’s disease. Gastroenterology. 2014;146:681-88.
- Sokol H, Seksik P, Carrat F, et al. Usefulness of co-treatment with immunomodulators in patients with inflammatory bowel disease treated with scheduled infliximab maintenance therapy. Gut 2010;59:1363-8.
- Osterman MT, Haynes K, Delzell E, et al. Effectiveness and Safety of Immunomodulators With Anti-Tumor Necrosis Factor Therapy in Crohn’s Disease. Clin Gastroenterol Hepatol. 2015;13:1293-301
- Cosnes J, Sokol H, Bourrier A, et al. Adalimumab or infliximab as monotherapy, or in combination with an immunomodulator, in the treatment of Crohn’s disease. Aliment Pharmacol Ther. 2016;44:1102-113.
- Jones JL, Kaplan GG, Peyrin-Biroulet L, et al. Effects of Concomitant Immunomodulator Therapy on Efficacy and Safety of Anti-Tumor Necrosis Factor Therapy for Crohn’s Disease: A Meta-analysis of Placebo-controlled Trials. Clin Gastroenterol Hepatol. 2015;13:2233-40.
- Dulai PS, Siegel CA, Colombel JF, et al. Systematic review: Monotherapy with antitumour necrosis factor agents versus combination therapy with an immunosuppressive for IBD. Gut. 2014; 63: 1843-53.
- Ungar B, Kopylov U, Engel T, et al. Addition of an immunomodulator can reverse antibody formation and loss of response in patients treated with adalimumab. Aliment Pharmacol Ther. 2017;45:276-82.
- Bouguen G, Siproudhis L, Gizard E, et al. Long-term outcome of perianal fistulizing Crohn’s disease treated with infliximab. Clin Gastroenterol Hepatol 2013;11:75-981.
- Panaccione R, Ghosh S, Middleton S, et al. Combination therapy with infliximab and azathioprine is superior to monotherapy with either agent in ulcerative colitis. Gastroenterology. 2014;146:392-400.
- Filippi J, Laharie D, Michiels C, et al. Efficacy of sustained combination therapy for at least 6 months with thiopurines and infliximab in patients with ulcerative colitis in clinical remission: a retrospective multicenter French experience. J Crohns Colitis. 2015;9:252-8.
- Matsumoto T, Motoya S, Watanabe K, et al. Adalimumab Monotherapy and a Combination with Azathioprine for Crohn’s Disease: A Prospective, Randomized Trial. J Crohns Colitis. 2016;10:1259-66.
- Kopylov U, Al-Taweel T, Yaghoobi M, et al. Adalimumab monotherapy versus combination therapy with immunomodulators in patients with Crohn’s disease: a systematic review and meta-analysis. J Crohns Colitis. 2014;8:1632-41.
- Krieckaert CL, Nurmohamed MT, Wolbink GJ. Methotrexate reduces immunogenicity in adalimumab treated rheumatoid arthritis patients in a dose dependent manner. Ann Rheum Dis. 2012;71:1914-5.
- Dassopoulos T, Cohen RD, Scherl EJ, et al. Ulcerative Colitis Care Pathway. Gastroenterology. 2015;149:238-45.
-
Symmers WS. Opportunistic Infections. The Concept of ‘Opportunistic Infections’. Proc R Soc Med 1965;58:341-6.
- Rahier JF, Ben-Horin S, Chowers Y, et al. European evidence-based Consensus on the prevention, diagnosis and management of opportunistic infections in inflammatory bowel disease. J Crohns Colitis 2009;3:47-91.
-
Toruner M, Loftus EV, Jr., Harmsen WS, et al. Risk factors for opportunistic infections in patients with inflammatory bowel disease. Gastroenterology 2008;134:929-36.
- Beaugerie L, Brousse N, Bouvier AM, et al. Lymphoproliferative disorders in patients receiving thiopurines for inflammatory bowel disease: a prospective observational cohort study. Lancet 2009;374:1617-25.
-
Long MD, Martin CF, Pipkin CA, et al. Risk of melanoma and nonmelanoma skin cancer among patients with inflammatory bowel disease. Gastroenterology 2012;143:390-9.
- Lemaitre M, Kirchgesner J, Rudnichi A, et al. Association Between Use of Thiopurines or Tumor Necrosis Factor Antagonists Alone or in Combination and Risk of Lymphoma in Patients With Inflammatory Bowel Disease. JAMA 2017;318:1679-86.
- Magro F, Peyrin-Biroulet L, Sokol H, et al. Extra-intestinal malignancies in inflammatory bowel disease: results of the 3rd ECCO Pathogenesis Scientific Workshop (III). J Crohns Colitis. 2014;8:31-44.
- Mackey AC, Green L, Leptak C, Avigan M. Hepatosplenic T cell lymphoma associated with infliximab use in young patients treated for inflammatory bowel disease: update. J Pediatr Gastroenterol Nutr. 2009;48:386-8.
-
Deepak P, Sifuentes H, Sherid M, et al. T-cell non-Hodgkin’s lymphomas reported to the FDA AERS with tumor necrosis factor-alpha (TNF-) inhibitors: results of the REFURBISH study. Am J Gastroenterol 2013;108:99-105.
- Kotlyar DS, Osterman MT, Diamond RH, et al. A systematic review of factors that contribute to hepatosplenic T-cell lymphoma in patients with inflammatory bowel disease. Clin Gastroenterol Hepatol. 2011;9:36-41.
- Kirchgesner J, Beaugerie L, Carrat F, et al.Impact on Life Expectancy of Withdrawing Thiopurines in Patients with Crohn’s Disease in Sustained Clinical Remission: A Lifetime Risk-Benefit Analysis. PLoS One. 2016;11:e0157191.
- Treton X, Bouhnik Y, Mary J-Y, et al. Azathioprine withdrawal in patients with Crohn’s disease maintained on prolonged remission: a high risk of relapse. Clin Gastroenterol Hepatol 2009;7:80-5.
- Laharie D, Chanteloup E, Chabrun E, et al. The tolerance and efficacy of a postponed retreatment with infliximab in Crohn’s disease primary responders. Aliment Pharmacol Ther 2009;29:1240-8.
- Roblin X, Boschetti G, Williet N, et al. Azathioprine dose reduction in inflammatory bowel disease patients on combination therapy: an open-label, prospective and randomised clinical trial. Aliment Pharmacol Ther. 2017;46:142-9.
- Vande Casteele N, Ferrante M, Van Assche G, et al. Trough concentrations of infliximab guide dosing for patients with inflammatory bowel disease. Gastroenterology. 2015;148:1320-9
- Louis E, Mary J-Y, Vernier-Massouille G, et al. Maintenance of remission among patients with Crohn’s disease on antimetabolite therapy after infliximab therapy is stopped. Gastroenterology 2012;142:63-70.
- Drobne D, Bossuyt P, Breynaert C, et al. Withdrawal of immunomodulators after co-treatment does not reduce trough level of infliximab in patients with Crohn’s disease. Clin Gastroenterol Hepatol. 2015;13:514-21.
- Feagan BG, Rutgeerts P, Sands BE, et al. Vedolizumab as induction and maintenance therapy for ulcerative colitis. N Engl J Med. 2013;369:699-710.
- Sandborn WJ, Feagan BG, Rutgeerts P, et al. Vedolizumab as induction and maintenance therapy for Crohn’s disease. N Engl J Med. 2013;369:711-21.
- Sandborn WJ1, Gasink C, Gao LL, et al. Ustekinumab induction and maintenance therapy in refractory Crohn’s disease. N Engl J Med. 2012;367:1519-28.
- Feagan BG, Sandborn WJ, Gasink C, et al. Ustekinumab as Induction and Maintenance Therapy for Crohn’s Disease. N Engl J Med. 2016;375:1946-60.
- Wils P, Bouhnik Y, Michetti P, et al. Subcutaneous Ustekinumab Provides Clinical Benefit for Two-Thirds of Patients With Crohn’s Disease Refractory to Anti-Tumor Necrosis Factor Agents. Clin Gastroenterol Hepatol. 2016;14:242-50.
-
Ma C, Fedorak RN, Kaplan GG, et al. Long-term Maintenance of Clinical, Endoscopic, and Radiographic Response to Ustekinumab in Moderate-to-Severe Crohn’s Disease: Real-world Experience from a Multicenter Cohort Study. Inflamm Bowel Dis. 2017;23:833-9.
- Shelton E, Allegretti JR, Stevens B, et al. Efficacy of Vedolizumab as Induction Therapy in Refractory IBD Patients: A Multicenter Cohort. Inflamm Bowel Dis. 2015;21:2879-85.
- Vivio EE, Kanuri N, Gilbertsen JJ, et al. Vedolizumab Effectiveness and Safety Over the First Year of Use in an IBD Clinical Practice. J Crohns Colitis. 2016;10:402-9.
- Baumgart DC, Bokemeyer B, Drabik A, et al. Vedolizumab induction therapy for inflammatory bowel disease in clinical practice–a nationwide consecutive German cohort study. Aliment Pharmacol Ther. 2016;43:1090-102.
- Amiot A, Serrero M, Peyrin-Biroulet L, et al. One-year effectiveness and safety of vedolizumab therapy for inflammatory bowel disease: a prospective multicentre cohort study. Aliment Pharmacol Ther. 2017;46:310-21.
- Kopylov U, Ron Y, Avni-Biron I, et al. Efficacy and Safety of Vedolizumab for Induction of Remission in Inflammatory Bowel Disease-the Israeli Real-World Experience. Inflamm Bowel Dis. 2017;23:404-8.
- Eriksson C, Marsal J, Bergemalm D, et al. Long-term effectiveness of vedolizumab in inflammatory bowel disease: a national study based on the Swedish National Quality Registry for Inflammatory Bowel Disease (SWIBREG). Scand J Gastroenterol. 2017;52:722-9.
-
Kopylov U, Afif W, Cohen A, et al. Subcutaneous ustekinumab for the treatment of anti-TNF resistant Crohn’s disease – the McGill experience. J Crohns Colitis. 2014;8:1516-22.
-
Harris KA, Horst S, Gadani A, et al. Patients with Refractory Crohn’s Disease Successfully Treated with Ustekinumab. Inflamm Bowel Dis. 2016;22:397-401.
- Khorrami S, Ginard D, Marín-Jiménez I, et al. Ustekinumab for the Treatment of Refractory Crohn’s Disease: The Spanish Experience in a Large Multicentre Open-label Cohort. Inflamm Bowel Dis. 2016;22:1662-9.
FMC HGE : Organisme certifié Qualiopi pour la catégorie ACTIONS DE FORMATION