Objectifs pédagogiques
- Connaître les critères de qualité du bilan préopératoire
- Connaître la définition d’une tumeur résécable d’emblée, borderline ou localement avancée
- Connaître les indications et les modalités du traitement adjuvant
LIENS D’INTÉRÊT
Consultant expert : Merck, Baxter
Cours, formations : Celgene, Merk, Roche
Invitation à des congrès : Eumedica, BIOMUP, Servier
MOTS-CLÉS
Adénocarcinome du pancréas, chirurgie, chimiothérapie
ABRÉVIATIONS
ADKP : Adénocarcinome du pancréas TDM : Tomodensitométrie
AMS : Artère mésentérique supérieure
TC : Tronc cœliaque
AHC : Artère hépatique commune VMS : Veine mésentérique supérieure VP : Veine porte
En France, le taux incidence de l’adénocarcinome du pancréas (ADKP) est en augmentation continue depuis 1990 (+ 2,7 % par an chez l’homme et 3,8 % chez la femme entre 1990 et 2018), avec 14 000 nouveaux cas en 2017. Les progrès réalisés, ces dernières années, n’ont que peu modifié le pronostic de l’ADKP.
Le traitement de référence des formes résécables repose sur l’association de la chirurgie et d’une chimiothérapie adjuvante. La réalisation d’un traitement adjuvant permet d’améliorer la survie globale et sans récidive (1, 2).
Cependant au moment du diagnostic, la grande majorité des ADKP sont non résécables du fait de l’existence d’une extension métastatique (hépatique le plus souvent) et/ou d’une extension locorégionale (ganglionnaire et vasculaire) (3).
Le bilan d’imagerie a pour objectif d’éliminer une extension à distance et d’apprécier les rapports de la tumeur avec les structures vasculaires (Veine porte, veine mésentérique supérieure, artère mésentérique supérieure, artère hépatique, tronc cœliaque). Dans les formes non métastatiques, l’analyse précise des rapports vasculaires de la tumeur permet d’identifier les formes résécables pour lesquelles la chirurgie de première intention demeure le standard.
L’objectif de la chirurgie de l’ADKP est une exérèse R0 avec la morbi-mortalité la plus faible possible. La chimiothérapie adjuvante doit être réalisée chez tous les malades, indépendamment du statut N0/N+ et R0/R1 (2). Cependant celle-ci est souvent non réalisée en raison des suites des pancréatectomies (morbidité élevée, altération de l’état général).
Ce texte traite du bilan préopératoire, de la classification des ADKP non métastatiques en fonction des rapports vasculaires, des indications chirurgicales et du traitement adjuvant.
Une fois le diagnostic ADKP fait, le bilan préopératoire d’un ADKP comporte un bilan d’opérabilité et de résécabilité. Les objectifs de ce bilan sont d’éliminer les contre-indications opératoires :
Une fois les contre-indications éliminées, le bilan de résécabilité a pour objectif d’apprécier l’extension locorégionale (vais- seaux, organes adjacents) afin d’identifier les malades chez lesquels une résection R0 est possible.
Le bilan de résécabilité doit être récent, un délai supérieur à 3 ou 4 semaines entre l’examen et l’intervention augmente le risque de trouver une contre-indication à la résection lors de la laparotomie.4
La réalisation du bilan imagerie et son interprétation doivent être standardisées. L’évaluation définitive de la résécabilité doit être réalisée lors d’une réunion de concertation pluridisciplinaire en présence d’oncologues, radiologues et chirurgiens.
La tomodensitométrie (TDM) et l’IRM sont les deux examens de première intention pour le bilan diagnostique et d’extension. Leur efficacité pour évaluer la résécabilité est similaire (5, 6). La TDM, en raison d’une meilleure accessibilité, est l’examen le plus utilisé en France.
Si la lésion n’est pas visible au TDM (tumeur < 2 cm ou isodense au parenchyme pancréatique), l’IRM ou l’échoendoscopie peuvent être réalisées en deuxième intention.
L’IRM hépatique permet de détecter des métastases hépatiques chez 10 % des malades avec une TDM normale, permettant ainsi d’éviter une laparotomie inutile (7).
Les protocoles de TDM et IRM pour l’évaluation de la résécabilité des ADKP sont maintenant bien standardisés (5, 6). Le protocole de TDM recommandé est un examen biphasique par angioscanner multidetecteur :
Pour compléter l’acquisition d’images, le post-traitement va consister en l’optimisation des reconstructions MIP (Maximum Intensité Projection) pour l’étude vasculaire.
Le compte-rendu de la TDM doit être standardisé afin d’évaluer la résécabilité et de faciliter la décision thérapeutique (5). L’évaluation morphologique doit renseigner :
Enfin le compte-rendu morphologique doit comporter une conclusion faisant une synthèse du bilan morphologique.
Les ADKP du pancréas non métastatiques sont classés en fonction des rapports vasculaires identifiés à l’issue du bilan morpho- logique.
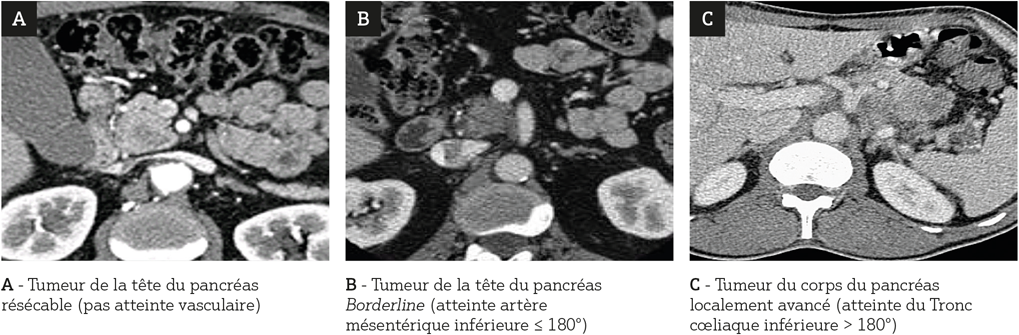
Figure 1
| Contact vasculaire (NCCN) | |||
| Résécable | Borderline | Localement avancé | |
| VMS/VP | Absent Ou < 180° sans irrégularité veineuse | < 180° avec irrégularité veineuse ≥ 180° | Thrombose Atteinte des veines jéjunales
|
| AMS | Absent | < 180° | ≥180° |
| AHC | Absent | Court reconstructible | Non reconstructible |
| TC | Absent | < 180° | ≥180° |
Figure 2 : Classification NCCN des adénocarcinomes du pancréas non métastatique
VMS/VP : veine mésentérique supérieure AMS : artère mésentérique supérieure TC : Tronc cœliaque
AHC : artère hépatique commune
Différentes classifications ont été proposées, actuellement celle qui est la plus utilisée est celle du NCCN (8) :
Un ADKP est jugé résécable en l’absence d’atteinte vasculaire (artérielle et veineuse) ou en présence d’une atteinte veineuse < 180°sans irrégularité du calibre veineux. Pour ce type de tumeurs une chirurgie de première intention doit être proposée (9, 10).
Un ADKP est classé borderline en présence :
Il s’agit dans ce cas de tumeurs potentiellement résécables mais avec un risque très élevé de résection R1. Les recommandations actuelles sont de proposer un traitement d’induction (Chimiothérapie +/- Radiochimiothérapie). Un nouveau bilan morphologique, réalisé à l’issue de ce traitement d’induction, permettra de juger de la réponse et de proposer une chirurgie aux patients répondeurs (9, 10).
Enfin un ADK du pancréas est classé localement avancé en présence :
Le traitement des ADKP localement avancés repose sur la chimiothérapie, la probabilité d’avoir une chirurgie secondaire est ici de l’ordre de 10 % (9, 10).
À noter que, pour un ADK du pancréas gauche, la présence d’une atteinte de la veine et/ou de l’artère spléniques, et ce quel que soit le degré d’envahissement, ne sont pas des critères de non-résécabilité. Ces patients sont candidats à une chirurgie de première intention.
Le traitement des ADKP résécables associe une exérèse chirurgicale à une chimiothérapie adjuvante. L’objectif de la chirurgie est une exérèse R0, avec une morbi-mortalité la plus faible possible pour permettre aux malades de recevoir la chimiothérapie adjuvante (9, 10).
La duodénopancréatectomie céphalique est l’intervention de référence des ADK de la tête du pancréas. Le curage ganglion- naire inclus les relais 5, 6, 8a, 12b1, 12b2, 12c, 13a, 13b, 14a, 14b, 17a, et 17b et doit comporter au minimum 15 ganglions (11).
Elle doit comporter la résection de la lame rétroporte mettant à nu le bord droit de l’artère mésentérique supérieure (9, 10). Pour les ADK du pancréas gauche, l’intervention recommandée est la splénopancréatectomie gauche. Le curage ganglionnaire inclus les relais 10,11,18 (9, 10).
L’encrage de la pièce opératoire est conseillé pour permettre une analyse anatomopathologique précise des limites chirurgicales (12).
La chirurgie demeure le seul traitement offrant une chance de guérison pour les malades ayant un adénocarcinome du pancréas résécable. Cependant la survie à 5 ans après chirurgie seule est d’environ 10 % (1, 2).
Une chimiothérapie adjuvante à base de gemcitabine ou de fluoropyridine améliore de manière significative la survie globale et sans récidive (1, 2).
Dans l’étude de phase III CONKO 001, les patients ont été randomisés pour recevoir de la gemcitabine (1 000 mg/m2 J1, J8, J14/4 sem. x 6) ou une simple surveillance. Cette étude concluait à une amélioration significative de la survie sans récidive (13,4 mois versus 6,9 mois, p < 0,001) et de la survie globale (22,8 versus 20,2 mois, p = 0,005) dans le groupe des malades ayant reçu la gemcitabine en adjuvant. Dans cette étude, le bénéfice de survie était présent dans tous les sous-groupes de malades, en particulier N0/N+ et R0/R1 (2).
L’essai ESPAC 3 a randomisé les patients entre 5-FU et AF [schéma de la Mayo clinic (6 cycles)] et gemcitabine (1 000 mg/m2 J1, J8, J14/4 sem. x 6). Le critère principal était la SG. La médiane de SG était de 23 mois dans le bras 5FU/AF et de 23,6 mois (95 % CI, 21,4-26,4) dans le bras gemcitabine (p = 0,39). Un événement indésirable grave était noté chez 14 % des patients du bras 5FU/AF versus 7,5 % ceux du bras gemcitabine (P < 0,001) (13).
L’essai ESPAC 4 a randomisé les patients entre gemcitabine (1 000 mg/m2 J1, J8, J14/4 sem. x 6) seule ou associée à de la capecitabine (1 660 mg/m² oral, pendant 21 jours suivi de 7 jours d’arrêt). Le critère principal était la survie globale. La médiane de survie globale était de 28 mois (95 % CI 23,5–31,5) dans le groupe gemcitabine plus capecitabine versus 25,5 mois (22,7–27,9) dans le groupe gemcitabine seule (hazard ratio 0,82 [95 % CI 0,68–0,98], p= 0·032) (14). Les résultats de cette étude ont été très critiqués en particulier en raison de l’absence de différence de survie sans récidive (15).
L’essai PRODIGE 24 a montré que comparé à la gemcitabine, le FOLFIRINOX modifié (pas de bolus et dose réduite d’iri- notecan) augmentait la médiane de survie sans récidive (21,6 versus 12,8 mois, HR : 0,58, p < 0,0001) et de survie globale (54,4 versus 35 mois. HR: 0,64, p = 0,003) chez les patients ayant un statut ECOG PS 0–1. Ce bénéfice de survie était retrouvé dans tous les sous-groupes de patients (16).
Enfin les résultats de l’essai APACT ont été présentés à l’ASCO en 2019, comparant la gemcitabine seule ou associée au nab-placitaxel (125 mg/m2 J1-8-15 / 28j). Le critère principal était la survie sans récidive. Cette étude est négative sur son critère principal, avec une médiane de survie sans récidive 19,4 vs 18,8 mois HR : 0,88 [0,729-1,063] p = 0,1824, respective- ment dans le bras avec et sans nab-placitaxel (17).
Après exérèse d’un ADKP, une chimiothérapie adjuvante est recommandée chez tous les malades.
Le FOLFIRINOX modifié est le nouveau standard thérapeutique pour les patients en bon état général (ECOG PS 0-1). Pour les malades avec un ECOG PS > 1, une chimiothérapie par gemcitabine ou fluoropyrimoidine est recommandée (9). Quelle que soit la chimiothérapie, la réalisation du traitement adjuvant complet est plus importante que le délai entre la chirurgie et le début de la chimiothérapie (dans les 3 mois) (18).
L’examen de première intention pour le bilan diagnostique et d’extension d’un ADKP est la TDM dont le protocole de réalisa- tion et l’interprétation doivent être standardisés. Chez les malades non métastatiques, l’analyse des rapports vasculaires permet de déterminer les tumeurs résécables, borderline et localement avancé. La chirurgie de première intention ne s’adresse qu’aux patients ayant une tumeur résécable à l’issue du bilan d’imagerie.
Après l’exérèse d’un ADKP, la chimiothérapie adjuvante doit être réalisée chez tous les malades car elle permet d’améliorer significativement la survie globale et sans récidive.
Toute reproduction ou réécriture, totale ou partielle, sans l’accord préalable écrit de la FMC HGE est interdite.
FMC HGE : Organisme certifié Qualiopi pour la catégorie ACTIONS DE FORMATION.