Objectifs pédagogiques
- Connaître les facteurs pronostiques lors du diagnostic et au cours du suivi
- Connaître leur impact sur la stratégie thérapeutique
- Savoir adapter la surveillance en fonction de ces facteurs
Consultance : Abbvie, BMS, Celltrion, Ferring, Galapagos, Janssen, Takeda
Présentations : Abbvie, BMS, Celltrion, FALK, Ferring, Galapagos, Janssen, Mylan, Pfizer, Takeda
Bourse de recherche : Abbvie, Celltrion, Ferring, Galapagos, Janssen, Fresenius Kabi
Maladie inflammatoire intestinale, complication, facteurs prédictif, monitoring étroit, suivi non invasif
Les maladie inflammatoires chroniques intestinales (MICI) sont des maladies chroniques qui, au fil de leur évolution, peuvent conduire à des lésions tissulaires irréversibles provoquant diverses complications, elles-mêmes entraînant une altération significative de la qualité de vie au long cours (1). La maladie de Crohn (MC) est une maladie transmurale associée à des phénomènes micro-inflammatoires persistants bien que le patient soit a- ou paucisymptomatique. Il existe donc une discordance entre les scores d’activité clinique et les scores endoscopiques qui pourrait conduire le clinicien à sous-estimer le potentiel évolutif de la maladie (2). L’utilisation d’outils non invasifs pour détecter ces phénomènes inflammatoires, de même que l’identification des patients à haut potentiel évolutif sont cruciaux pour une prise en charge pro-active visant à éviter l’apparition des complications. La rectocolite hémorragique (RCH) a longtemps été considérée comme une maladie à faible potentiel évolutif, probablement suite aux éléments suivants : une inflammation limitée à la muqueuse et la sous-muqueuse, une excellente réponse aux 5-aminosalicylés en première ligne, des taux élevés de cicatrisation muqueuse sous corticoïdes topiques et généraux lors des poussées et la possibilité ultime de recours à la chirurgie dans les cas réfractaires. Il a été démontré que la persistance d’une activité inflammatoire endoscopique à bas bruit (Mayo 1) et, plus récemment, d’une activité inflammatoire histologique, étaient associées à plus de rechutes (3), à une altération de la qualité de vie (4) et à des phénomènes de fibrose tissulaire induisant une perte de la compliance rectale associée à un syndrome rectal clinique chronique (5). La RCH doit, au même titre que la MC, faire l’objet d’un suivi régulier et d’une prise en charge thérapeutique personnalisée pour éviter les complications fonctionnelles au long cours.
Pour mettre en place une stratégie thérapeutique efficace, la connaissance de l’histoire naturelle des MICI est indispensable. La MC se présente initialement sur un mode purement inflammatoire dans 80 % des cas et seuls 20 % des patients présentent d’emblée une forme compliquée de sténose ou de fistule (figure 1) (6). Dans ces situations, l’instauration précoce d’un traitement biologique, le plus souvent l’association d’un anti-TNF et d’un immunosuppresseur, est recommandée (7). La prise en charge du patient présentant une forme inflammatoire est plus complexe. En effet, après 10 ans d’évolution, près de 50 % des patients développent des lésions sténosantes ou fistulisantes avec des délais d’apparition variables d’un patient à l’autre. L’identification de facteurs prédictifs au diagnostic et au cours du suivi d’une maladie compliquée précoce est indispensable pour une prise en charge appropriée. Les facteurs les plus pertinents sont évoqués dans les paragraphes suivants mais ils ne représentent pas une liste exhaustive (table 1).
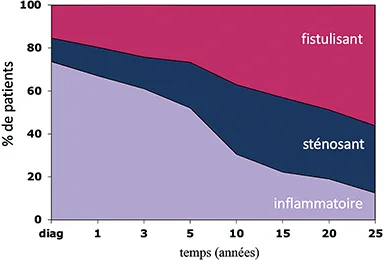
Figure 1 : Histoire naturelle de la MC
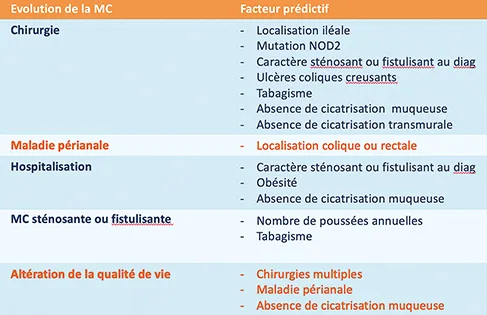
Table 1 : facteurs de risque de MC sévères
Plusieurs études, dont notamment le célèbre registre EPIMAD, ont démontré davantage de complications dans les formes pédiatriques de MC (8). En revanche, dans la population adulte, les données portant sur l’âge au diagnostic comme facteur de risque sont conflictuelles. Une cohorte de Saint- Antoine publiée en 2006 portant sur 1 223 patients atteints de MC (9) a démontré que 2 de ces 3 facteurs (un diagnostic avant l’âge de 40 ans, une maladie anale et une cure de corticoïdes au diagnostic) étaient des facteurs de risque d’évolution vers une maladie « instable » dans les 5 ans. Cette dernière était définie par la présence d’au moins un des facteurs suivants : plus de 2 cures de corticoïdes et/ ou corticodépendance, hospitalisation, symptômes digestifs chroniques liés à la MICI durant 12 mois cumulés, recours aux immunosuppresseurs, chirurgie intestinale ou périanale. Dans cette cohorte, 84 % des patients évoluaient vers une maladie instable au cours du suivi. Une étude similaire réalisée 2 ans plus tard au CHU de Liège sur une cohorte de 361 patients a validé la maladie anale et le recours aux corticoïdes comme facteurs de risque de maladie « instable » mais l’âge au diagnostic n’était plus retenu (10). Cette définition de la maladie « instable » est probablement trop large et peu discriminante vu le pourcentage élevé de patients évoluant péjorativement selon ces critères. Par contre, un diagnostic à un âge avancé a été validé à plusieurs reprises comme un facteur associé à une évolution non compliquée de la MC ou de la RCH. La cohorte EPIMAD a étudié les MICI du sujet âgé, définies par un diagnostic à l’âge de 60 ans ou plus (11). Une MC diagnostiquée au-delà de 60 ans présente un caractère inflammatoire dans 80 % des cas et le conserve, sans complication sténosante ni fistulisante, dans 70 % des cas après 15 ans de suivi, ce qui diffère de l’évolution des MC tous âges confondus (figure 2). Moins de 30 % nécessitent le recours aux immunosuppresseurs et seuls 10 % recevront des anti-TNF après 10 ans d’évolution. Dans la RCH, une étude de population norvégienne a démontré qu’un diagnostic avant l’âge de 50 ans était associé à un risque de colectomie diminué de 80 %. Par contre, l’association d’un diagnostic avant l’âge de 50 ans, d’une maladie pancolique et d’un syndrome inflammatoire au diagnostic était associée à un risque de colectomie multipliée par plus de 3 (12).
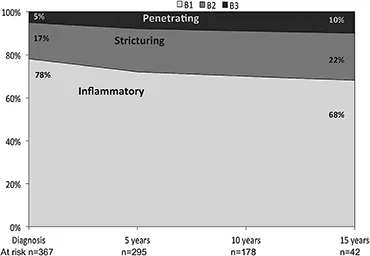
Figure 2 : Histoire naturelle de la MC du sujet âgé
L’obésité est un problème de santé publique comme en témoignent les 600 millions de personnes obèses de par le monde. Cette problématique concerne également les MICI avec 15 à 20 % d’obésité en Europe, ce qui est proche de la fréquence retrouvée dans la population générale (13). La présence d’une obésité, définie par un IMC >30, est un facteur qui pourrait être associé à une MICI plus sévère. Les adipocytes infiltrant le tissu adipeux sont impliqués dans la libération de taux élevés de cytokines pro-inflammatoires, appelés adipokines, de même qu’un déséquilibre du ratio entre les lymphocytes pro-inflammatoires Th17 et les lymphocytes T régulateurs (14). Cette population cellulaire, surreprésentée chez les patients obèses, pourrait contribuer à entretenir les phénomènes inflammatoires dans les MICI et, secondairement, mener plus fréquemment à des formes compliquées. Des études rétrospectives américaines n’ont pas démontré d’augmentation de l’utilisation de corticoïdes ni d’augmentation de risque chirurgical (15) dans la RCH. Par contre, ce sous-groupe de patient était hospitalisé plus fréquemment, ce qui représentait probablement le caractère plus « fragile » de cette population. Dans une autre étude rétrospective portant sur la MC, le nombre d’interventions chirurgicales et la nécessité d’escalade thérapeutique n’étaient pas influencées par le poids (16). À l’heure actuelle, il n’y a pas d’argument pour considérer que la population MICI obèse est sujette à davantage de complications et, de ce fait, ne nécessite pas une prise en charge plus « agressive » d’emblée.
Près de 100 gènes ont été associés à la présence de la MC et de la RCH, la plupart étant communs aux deux pathologies. Le premier gène associé à la MC est le gène NOD2, codant pour la protéine CARD15 (17). Il est présent chez 30 % des patients. Diverses études ont démontré une association entre une mutation NOD2 et la localisation iléale de la maladie. Par contre, l’association entre NOD2 et le phénotype sténosant ou fistulisant de la MC fait l’objet de résultats divergents. Une étude du CHU de Liège a démontré que la localisation iléale et l’activité de la maladie, définie par le nombre de rechutes annuelles, étaient indépendamment associés à une MC sténosante ou fistulisante mais pas la présence d’une mutation NOD2 (18). Certains anticorps dirigés contre des éléments bactériens sont associés à la MC (ASCA, anti-OmpC, anti-CBir, …). Bien que leur rôle reste flou, la présence de ces anticorps témoigne du rôle de l’immunité innée dans la physiopathologie des MICI. Une étude pédiatrique portant sur 536 patients atteints de MC a démontré, sur un suivi de 32 mois, que le risque de complications sténosantes et fistulisantes était associé directement au nombre d’anticorps présents avec une valeur prédictive positive de 8,8 % et, surtout, une valeur prédictive négative de 97 % (12). Bien qu’intellectuellement intéressante, cette étude ne présente pas d’application concrète dans la pratique clinique.
Le tabagisme actif est un facteur de risque bien établi dans la MC. Dans les études, il est systématiquement associé à des MC plus compliquées, sténosantes ou fistulisantes (10), et à des complications périanales. Dans le contexte spécifique post-opératoire, le tabagisme actif est associé à un risque significativement accru de récidives. La physiopathologie sous-jacente reste à l’heure actuelle mal comprise. Le tabagisme, à lui seul, ne doit pas induire une escalade thérapeutique non réfléchie mais doit s’intégrer à l’ensemble des autres éléments caractéristiques du patient et de la maladie. Dans la RCH, contrairement à certaines idées reçues, le tabagisme n’est pas associé à une forme moins sévère de la maladie. Une méta-analyse publiée en 2016 portant sur 16 études et plus de 2 000 patients n’a pas démontré un risque réduit de colectomie, de rechute, de maladie étendue ou de pochite chez les fumeurs par rapport aux non-fumeurs (19).
La maladie de Crohn peut toucher l’ensemble des segments du tube digestif. Au diagnostic, 30 % des patients présentent une localisation iléale isolée, 30 % une localisation colique isolée et 40 % une extension iléo-colique. Seuls 10 % des patients présentent une atteinte digestive haute. Au cours du temps, la localisation de la MC reste généralement stable avec seulement 10 à 15 % d’évolution vers une forme plus étendue (6). Comme expliqué précédemment, la localisation iléale est associée dans de nombreuses études à un risque accru d’évolution vers une forme sténosante ou fistulisante et à l’apparition plus rapide de ces complications (20), le corolaire étant un risque chirurgical augmenté à 10 ans. La présence d’une maladie anale est associée dans diverses études à un risque de plus de 50 % d’évolution vers une forme sténosante ou fistulisante à 10 ans contre 10 à 15 % des patients ne présentant pas de maladie anale. Les études parisiennes et liégeoises citées précédemment avaient également démontré qu’une localisation anale était associée à un risque augmenté de maladie « instable » à 5 ans (9,10). La présence d’une maladie anale est par ailleurs associée à une altération significative de la qualité de vie. La localisation rectale mérite une attention particulière. Elle est en effet associée à un risque accru de maladie anale, probablement suite à l’environnement inflammatoire qui en découle. De plus, en cas de lésions réfractaires au traitement médical, une résection chirurgicale n’est pas envisageable dans cette localisation de par son caractère délabrant imposant une stomie. Une localisation digestive haute, duodénale ou jéjunale, affecte 10 % des patients mais peut atteindre jusque 15 % dans des séries asiatiques (6). Cette localisation est presque systématiquement associée à une forme sténosante de la maladie entraînant un risque chirurgical augmenté par rapport aux patients ne présentant pas d’atteinte digestive haute. Cette localisation doit inciter à une prise en charge active et à un monitoring étroit vu le haut taux de complications. La sévérité des lésions coliques à l’endoscopie doit également être prise en considération. Une étude parisienne a démontré que les patients présentant des ulcérations creusantes et extensives (définie par une surface ulcérée de 10 % ou plus), présentaient un risque relatif de colectomie multiplié par 5 avec une probabilité de colectomie à 1, 3, et 8 ans de 20 %, 26 % et 42 % respectivement (21). Dans la RCH, l’extension de la maladie détermine le risque de colectomie. Dans cette maladie, le rectum est atteint isolément au diagnostic dans un tiers des cas, l’extension progresse jusqu’au côlon gauche dans un tiers des cas, et jusqu’au côlon droit dans un tiers à la moitié des cas (22). Contrairement à la MC, la localisation de la maladie peut évoluer au fil du temps. La maladie s’étend vers l’amont dans près d’un cas sur deux après 20 ans d’évolution. Cette extension vers l’amont est d’autant plus fréquente que les lésions initiales sont déjà étendues au-delà de la charnière rectosigmoïdienne. Une atteinte pancolique, sans intervalle de muqueuse saine, est observée dès la première coloscopie chez un quart des patients mais après 20 ans d’évolution touche près d’un patient sur 2. Une étude de population norvégienne a démontré un risque de colectomie à 10 ans de 19 % dans les formes étendues pancoliques contre 8 % dans les formes coliques gauches et 5 % dans les proctites (23).
Les facteurs de risque liés au patient ou à la localisation de la maladie sont importants à prendre en compte pour identifier les patients potentiellement à haut risque de complications chez qui un traitement plus « agressif » et un suivi rapproché doivent être mis en place. Néanmoins, ces facteurs sont larges et une sélection aveugle basée sur ceux-ci risquerait d’aboutir au surtraitement d’une proportion importante de patients. Ces facteurs sont par ailleurs fixés dès le départ et immuables au fil du temps, à l’exception du tabagisme. Des études ont démontré que le nombre de poussées de la maladie était pronostique d’une maladie instable au fil du temps. Il apparaît dès lors qu’une maladie bien contrôlée aura tendance à évoluer vers moins de complications. En tant que praticien, nous avons le pouvoir de débuter des traitements et de proposer des suivis appropriés à chaque patient dans le but d’assurer un contrôle optimal de la maladie et donc de changer son histoire naturelle. Le contrôle de la maladie peut être évalué à différents niveaux. La cicatrisation muqueuse est un concept bien établi et sera discuté. La cicatrisation transmurale et histologique sont des concepts émergents qui méritent d’être évoqués.
Le concept de cicatrisation muqueuse a émergé il y a une quinzaine d’années. Si, auparavant, la prise en charge médicale avait pour but le contrôle des symptômes et l’éviction des corticoïdes, un contrôle plus ambitieux a été suggéré dans le but de modifier l’histoire naturelle des MICI. La cicatrisation muqueuse peut être définie dans la maladie de Crohn par un score CDEIS <3 ou SES CD <5. De façon plus simple, on peut considérer, en pratique, que l’absence d’ulcération définit la cicatrisation muqueuse dans la MC (24). Dans la RCH, un score Mayo endoscopique de 0 (endoscopie normale) ou 1 (perte de la trame vasculaire, érythème), définit une cicatrisation muqueuse. Dans la MC tout comme dans la RCH, la cicatrisation muqueuse est associée à une diminution significative du risque de chirurgie au cours de la maladie (Figure 3). Elle est également associée à moins de rechutes (25) et à une normalisation de la qualité de vie (26). Grâce à l’avènement des anti-TNFs dans les années 2000, puis des nouvelles biothérapies, cet objectif est tout à fait réaliste chez la plupart des patients pour autant que le traitement ne soit pas débuté tardivement. En effet, des études démontrent que l’obtention d’une cicatrisation muqueuse dans les 2 ans suivant le diagnostic est associée à une rémission soutenue au fil du temps (27). Par ailleurs, dans la MC, les anti-TNFs sont moins efficaces s’ils sont positionnés plus de 2 ans après le diagnostic, cet effet étant encore plus marqué au-delà de 5 ans. Cette donnée n’est pas confirmée dans la RCH (28). Une étude récente belge et hollandaise vient de démontrer que le védolizumab débuté dans les 2 premières années du diagnostic d’une MC permet une cicatrisation à la fois clinique et endoscopique chez 47 % des patients contre 16 % si le traitement est débuté au-delà des 2 ans (29). L’obtention d’une cicatrisation muqueuse complète est parfois difficile, notamment dans les formes iléales et chez des patients en échec de plusieurs lignes de traitement. Des objectifs thérapeutiques raisonnables doivent être définis, en fonction du patient, de l’histoire de sa MICI et de la localisation des lésions. Les lésions iléales par exemple sont difficiles à cicatriser quel que soit le traitement choisi. Une étude de Leuven a démontré que l’obtention d’une cicatrisation muqueuse partielle, définie par une diminution de 50 % des lésions endoscopiques initiales, était associée à un risque chirurgical similaire par rapport au groupe de patients ne présentant plus aucun ulcère à l’endoscopie (30). À titre d’exemple, un patient âgé, ayant déjà bénéficié de 2 lignes de biothérapies, asymptomatique, et gardant quelques ulcères superficiels iléaux pourrait poursuivre dans la même voie thérapeutique tandis qu’un patient jeune, présentant des lésions coliques étendues (rectum inclus), devrait bénéficier de l’ensemble des possibilités thérapeutiques disponibles pour permettre une cicatrisation muqueuse, si possible complète. Une analyse personnalisée de la situation de chaque patient doit se faire au diagnostic mais aussi au fur et à mesure du suivi.
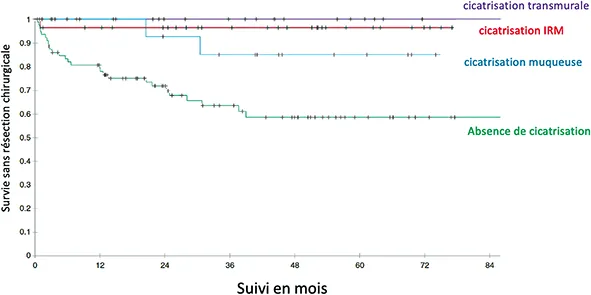
Figure 3 : Rôle de la cicatrisation muqueuse, de la cicatrisation à l’IRM
et de la combinaison des 2 (transmurale) dans le risque de chirurgie dans la MC
La maladie de Crohn étant une maladie transmurale, il semble logique de proposer une cicatrisation allant au-delà de la muqueuse. Les évolutions technologiques dans le domaine de l’imagerie médicale ont progressivement permis l’émergence de ce concept. C’est tout d’abord avec l’entéro-IRM que des outils de mesure de l’activité de la maladie ont été développés tels le MaRIA (Magnetic Resonance Index of Activity) (31) ou le score de Clermont (32). Des études ont démontré un risque plus faible d’hospitalisation, de chirurgie et d’escalade thérapeutique chez les patients présentant une cicatrisation transmurale par rapport à ceux présentant une cicatrisation muqueuse sans cicatrisation transmurale (33) (figure 3). Plus récemment, l’échographie intestinale a démontré une sensibilité et une spécificité similaires à l’IRM pour l’évaluation de l’activité et de l’extension de la MC iléale et colique (34). La cicatrisation transmurale, bien qu’intégrée comme objectif thérapeutique secondaire dans la plupart des études récentes dans la MC, n’est pas considérée à l’heure actuelle comme une cible thérapeutique formelle selon consensus STRIDE II (35).
Dans la RCH, des objectifs plus ambitieux tendent à se dégager. Tout d’abord, l’obtention d’une cicatrisation endoscopique définie par un Score Mayo 0 plutôt qu’on score Mayo ≤ 1 est associée à moins de rechute au cours du temps (3). Chez un patient en rémission clinique, le risque de rechute clinique est diminué de 2 à 3 fois en cas de rémission histologique par rapport à un patient gardant des signes d’activité histologique (36). Une inflammation histologique persistante au long cours est également associée à un risque de cancer colorectal augmenté de 5 fois (37). Bien que la cicatrisation histologique soit intégrée comme objectif thérapeutique secondaire dans la plupart des études récentes dans la RCH, il n’est pas recommandé à ce jour, d’intensifier ou d’introduire un traitement majeur en cas de persistance d’une activité histologique seule alors que le patient est en rémission clinique et endoscopique (35).
à l’exception de certaines situations spécifiques pour lesquelles le patient est exposé d’emblée à un risque maximal de complications (maladies compliquées d’emblée, maladies étendues, maladie périanale, lésions sévères diffuses), la plupart des patients présentent une maladie purement inflammatoire, souvent limitée en extension. Chez ces patients, le devenir de la maladie est difficile à prévoir. Il sera essentiellement déterminé par le choix de la prise en charge thérapeutique dans le but d’assurer un contrôle optimal de la MICI, basé sur une cicatrisation des lésions.
Quelle que soit l’attitude thérapeutique choisie (traitement maximal d’emblée ou plus progressif), c’est le suivi clinique qui sera déterminant afin d’optimiser le traitement le cas échéant. Cette stratégie est rendue possible par la disponibilité d’outils de monitoring précis et non invasifs. Selon les recommandations STRIDE 2, chaque patient avec une maladie de Crohn doit bénéficier d’un bilan morphologique complet au diagnostic avec coloscopie et IRM ainsi que d’un dosage de la CRP et de la calprotectine fécale (35) (figure 4). Le patient doit ensuite être évalué tous les 3 mois par un suivi clinique et des biomarqueurs. La réalisation d’une échographie intestinale a également été proposée récemment dans le contrôle serré des patients MICI. Elle est facile à pratiquer et bien acceptée du patient. Elle permet d’évaluer en temps réel la réponse initiale au traitement, tant dans la MC que dans la RCH (38,39). Elle doit être réalisée au diagnostic puis durant le suivi initial tous les 3 mois, au même titre que les biomarqueurs. Idéalement, le contrôle de la cicatrisation muqueuse par endoscopie doit être réalisé à un an, particulièrement chez les patients à risque. Chez les autres patients, cet examen peut être reporté à 2 ou 3 ans pour autant que les biomarqueurs et l’échographie intestinale se normalisent.
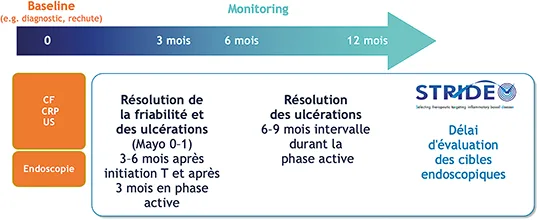
Figure 4 : Exemple de suivi des patients RCH ?
selon les recommandations STRIDE 2
Les facteurs de risque d’évolution péjorative des MICI doivent être connus en vue de proposer une attitude thérapeutique plus « agressive » d’emblée dans certaines situations. La présence d’une maladie étendue avec lésions sévères, d’une localisation jéjunale ou périanale et d’une complication sténosante ou fistulisante sont associées à un risque élevé de chirurgie, de complications et de mauvaise qualité de vie dans la MC. Dans la RCH,
une forme étendue, un âge jeune et un syndrome inflammatoire sont associés à un risque élevé de colectomie. La plupart des MICI ne présentent pas ces critères au diagnostic. C’est donc le contrôle étroit de la maladie via un suivi rapproché et l’utilisation de marqueurs/techniques non invasifs qui permettra une évolution favorable et l’éviction des complications.
MICI : maladie inflammatoires chroniques intestinales
MC : maladie de Crohn
RCH : rectocolite hémorragique
MaRIA : Magnetic Resonance Index of Activity
CDEIS : Crohn’s Disease Endoscopic Index score
SES CD : Simple Endoscopic Score for Crohn Disease
Toute reproduction ou réécriture, totale ou partielle, sans l’accord préalable écrit de la FMC HGE est interdite.
FMC HGE : Organisme certifié Qualiopi pour la catégorie ACTIONS DE FORMATION.