Liens d’intérêt
Consultance Olympus Medical ; Erbe ; Boston Scientific
Mots-clés
Tumeur sous-épithéliale, GIST, résection endoscopique
Caractérisation des lésions sous-muqueuses
Les lésions sous-muqueuses, mieux dénommées lésions sous-épithéliales proviennent de la muqueuse profonde, de la musculaire muqueuse, de la sous-muqueuse, ou de la musculaire propre de la paroi digestive. Le terme de tumeur sous-muqueuse (TSM) n’est donc pas tout à fait correct et devrait être réservé aux lésions originaires de la sous-muqueuse (1).
Ces lésions peuvent être responsables de symptômes tels que dysphagie, hémorragie digestive, anémie par carence martiale, nausées, vomissements ou douleurs abdominales en cas d’obstruction pylorique mais elles sont le plus souvent découvertes de façon fortuite lors de bilans endoscopiques (1/300 endoscopies). Leur fréquence apparaît plus élevée comme le démontrent des séries autopsiques où des MicroGISTs (<10 mm), et miniGISTs (10-20 mm) sont observées dans presque 20 % des cas (2).
Leur caractérisation endoscopique est peu spécifique puisqu’il s’agit le plus souvent de simples voussures pariétales recouvertes d’une muqueuse d’aspect normal. Elles peuvent présenter une ulcération à leur sommet responsable d’hémorragie, une ombilication ou dépression centrale suggestive de pancréas ectopique, ou un aspect jaunâtre suggestif de lipome. Leur consistance peut être évaluée par la pince à biopsie en position fermée, les tumeurs stromales étant dures au contact tandis que les lipomes se caractérisent par une déformabilité spécifique à 98 % (signe du coussin/ oreiller). Certaines caractéristiques sont suggestives d’une transformation maligne à savoir une lésion de grande taille, une croissance lors du suivi, où l’ulcération responsable d’hémorragie. Les techniques de chromoendoscopie ou de magnification endoscopique n’apportent pas d’élément diagnostique supplémentaire.
Ces lésions sont le plus souvent retrouvées dans l’estomac, ensuite dans l’œsophage puis dans le duodénum et le côlon. La localisation apporte déjà des éléments importants dans le diagnostic différentiel en particulier dans les tumeurs stromales puisqu’il s’agit le plus souvent de léiomyome dans l’œsophage et de tumeur stromale gastro-intestinale (GIST) dans l’estomac (3).
Diagnostic différentiel
Leur diagnostic différentiel comporte un large spectre de lésions qu’il faut d’abord différencier des compressions pariétales par un organe externe (aorte, kyste bronchogénique, adénopathie pour l’œsophage ; vésicule biliaire pour l’antre, rate pour la grosse tubérosité, boucle de l’artère splénique pour la face postérieure du corps gastrique, lobe gauche du foie pour la face antérieure du corps gastrique) ou par une pathologie comme une masse ganglionnaire, une tumeur bénigne ou maligne du foie ou un pseudokyste d’origine pancréatique. Il faut ensuite bien reconnaître les lésions vasculaires telles que des varices, ou kystiques telles les duplications œsophagiennes ou gastriques, les kystes bronchogéniques, ou les lymphangiomes. Le diagnostic différentiel est détaillé dans la table 1 et dépend principalement de la description et de l’orientation fournie par l’échoendoscopie. Celle-ci peut aisément distinguer les compressions extrinsèques, les lésions solides des lésions kystiques, et de préciser sa couche de naissance, son échogénicité, sa vascularisation, ses limites et sa taille (précision diagnostique >85 %). Certains critères échoendoscopiques sont suggestifs d’un caractère plus agressif ou de malignité, dont la taille (>3 cm), l’aspect hétérogène, la présence de composants kystiques ou des contours externes irréguliers.
| Type de TSM | Couche origine | Échogénicité | Taille (mm) | Limites | Localisation |
|---|
| Duplication | 3e/ externe | Anéchogène, doppler – | >20 | Nettes, parfois 5 couches | Toutes |
| Varices | 3e | Anéchogène, Doppler + | | Nettes, serpigineuses | Toutes |
| Lymphangiomes | 3e | Anéchgène avec septa internes, Doppler – | | Nettes | Toutes |
| Tum Cell Granuleuse Abrikossof | 2e, 3e | Hypoéchogène, plus échogène que muscle adjacent | <20 | Variables | Œsophage |
| Polype fibroide inflammatoire | 2e, 3e | Hypoéchogène, homogène, polypoide | 8-18 | Indistinctes | Antre> corps Intestin |
| Tumeurs Neuroendocrines | 2e, 3e | Hypoéchogène/intermédiaire hypo/ hyper | | Nettes | Estomac Intestin Rectum |
| Pancréas Ectopique | 2e à 4e | Hypoéchogène, texture hétérogène, avec kystes ou canal ou ombilication | <5-20 | Indistinctes | Antre Estomac Duodenum |
| Leiomyome | 2e à 4e | Hypoéchogène, idem muscle adjacent, moins que GIST. Homogène. Rarement multiloculé | variable | Nettes | Œsophage Estomac Intestin |
| GIST faible risque | 2e à 4e | Hypoéchogène, homogène, hypervasculaire | <30 | Nettes | Œsophage Estomac Intestin Rectum |
| GIST haut risque | 2e à 4e | Hypoéchogène, hétérogène, avec espaces kystiques ou foyers échogènes | >30 | Irrégulières | Eosophage Estomac Intestin Rectum |
| Lymphome | 2e à 4e | Hypoéchogène | variable | Irrégulières | Estomac Intestin |
| Schwanomme | 4e | Hypoéchogène, homogène, | | Nettes | Estomac |
| Tumeur Glomique | 3e/ 4e | Hypo/hyperechogène, hypervasculaire | variable | Nettes | Toutes |
| Endométriose | 4e/ 5e | Hypoéchogène, hétérogène, extension possible au septum rectovaginal | 20-50 | Irrégulières | Rectum Sigmoïde |
| Lipome | 3e | Hyperéchogène homogène | variable | Nettes | Toutes |
| Hyperplasie glandes Brunner | 2e, 3e | Iso/Hyperéchogène homogène, parfois canal interne | | Nettes | Bulbe duod |
| Métastases | toutes | Hypoéchogène | | Irrégulières | Toutes |
Table 1
Rôle de l’échoendoscopie
L’ESGE recommande l’échoendoscopie (EE) comme le meilleur outil pour préciser les caractéristiques des tumeurs sous-muqueuses (taille, localisation, couche d’origine, échogénicité, forme), mais l’échoendoscopie seule n’est pas capable de distinguer tous les types de tumeurs (Recommandation forte, preuves de qualité modérée) (4).
L’EE peut distinguer les TSM d’une compression extrinsèque (sensibilité de 92 %) et est capable de déterminer leur couche d’origine, leur taille, leur échogénicité et leurs marges. La précision rapportée pour l’identification de la couche d’origine des TSM dans une étude prospective et trois études rétrospectives était de 63 %-74,6 % ; cette précision était plus élevée (82,6 %-100 %) pour les TSM provenant de la couche sous-muqueuse (5).
Les caractéristiques de l’EE sont pathognomoniques pour les lipomes et les varices, et sous-optimales pour les autres types de TSM (précision de 43 % à 67 %). La précision de l’EE est de 77 % à 89 % pour le diagnostic des GIST, mais la précision du diagnostic différentiel des petites TSM gastriques par EE est faible et varie de 45,5 % à 48,0 % (6). La plupart des diagnostics erronés concernent des lésions hypoéchogènes provenant de la quatrième couche pariétale, et plus particulièrement des GIST de bas grade diagnostiquées à tort comme des léiomyomes. L’inhomogénéité, les spots hyperéchogènes, le halo marginal et une échogénicité plus élevée par rapport à la couche musculaire environnante apparaissent plus fréquemment dans les GIST que dans les léiomyomes ; deux de ces caractéristiques les distinguent avec une sensibilité de 89,1 % et une spécificité de 85,7 %.
L’ESGE suggère que l’échographie de contraste peut être utilisée pour la caractérisation des TSM dans le tube digestif supérieur et l’estimation du potentiel malin des GIST, mais elle ne peut pas remplacer l’acquisition tissulaire. De plus, l’ESGE suggère que les preuves sont insuffisantes pour recommander l’élastographie dans le diagnostic et la gestion des TSM.
L’échographie de contraste permet de visualiser la microvascularisation des TSM et améliore leur caractérisation, l’hyper rehaussement étant spécifique des GIST alors que l’hypo rehaussement est spécifique des TSM bénignes (7). Dans une méta-analyse évaluant la valeur de l’échoendoscopie avec contraste pour distinguer les GIST des autres TSM bénignes, avec un total de 187 patients, la sensibilité et la spécificité étaient respectivement de 89 % (95 %CI 82 %-93 %) et 82 % (95 %CI 66 %-92 %) (8).
En ce qui concerne la caractérisation des GIST, plusieurs études ont montré l’intérêt de l’échoendoscopie avec contraste pour différentier GIST de bas et de haut grade de malignité, la sensibilité allant de 63,6 % à 100 % et la spécificité de 63 % à 100 %, en particulier la présence de vaisseaux intra-tumoraux irréguliers, signe de tumeur stromale gastro-intestinale de haut grade de malignité (7-8).
Diagnostic histologique
L’ESGE suggère de recourir au diagnostic histologique pour toutes les tumeurs sous-muqueuses suggestives d’être une GIST, ou si elles ont une taille > 20 mm, ou présentent des critères à haut risque de malignité, ou nécessitent une résection chirurgicale ou un traitement oncologique (Recommandation faible, preuves de très faible qualité).
Il n’y a pas suffisamment de preuves dans la littérature pour suggérer que la ponction par EE est nécessaire pour toutes les TSM ou alors seulement pour celles de taille > 20 mm ou présentant des critères de haut risque (9). Les sociétés savantes d’oncologie européenne, japonaise et chinoise recommandent la résection chirurgicale lorsqu’une TSM est diagnostiquée immunohistologiquement comme une GIST, même si sa taille est inférieure à 20 mm (10-12). Par conséquent, un prélèvement de tissu pour une analyse immunohistochimique par EE ou une biopsie semble nécessaire pour un diagnostic définitif de GIST avant la chirurgie ou la chimiothérapie. En revanche, d’autres sociétés savantes recommandent que les petites GIST de < 20 mm puissent être suivies périodiquement par EE lorsqu’elles ne présentent pas de caractéristiques à haut risque (13). Dans les cas d’hémorragie grave, lorsqu’il n’y a pas de contre-indication à la résection, la biopsie doit être déconseillée et la résection doit être discutée par une équipe multidisciplinaire.
L’ESGE recommande indifféremment la biopsie à l’aiguille fine guidée par l’EE (EE-FNB) ou la biopsie assistée par incision muqueuse (MIAB) pour le diagnostic histologique des TSM de taille ≥ 20 mm (Recommandation forte, preuves de qualité modérée). L’ESGE suggère d’utiliser la MIAB (premier choix) ou l’EE-FNB (deuxième choix) pour le diagnostic tissulaire des SEL de taille < 20 mm (Recommandation faible, preuves de faible qualité).
La biopsie, à l’aide d’une pince, de la muqueuse recouvrant les TSM ne permet souvent pas d’obtenir du tissu tumoral pour l’évaluation pathologique. C’est pourquoi des techniques spéciales de biopsie ont été développées, telles que les méthodes «bite-on-bite», «jumbo» et «résection à l’anse». Des techniques plus récentes impliquent l’ouverture de la TSM par incision pour permettre des biopsies plus profondes de la tumeur (MIAB) (14). La technique MIAB a été évaluée dans le cadre d’une méta-analyse de 7 études montrant un rendement diagnostique global de 89 % (95 %CI 82,7 %-93,5 %). Aucune perforation n’a été observée et le taux d’hémorragie cliniquement significative était de 5 % (95 %CI 0,36 %-12,9 %) (15).
La MIAB a été comparée à l’EE avec ponction (FNA ou FNB) dans trois essais contrôlés randomisés (ECR), sans montrer de différence significative dans le taux de diagnostic histologique ou de complication, avec un avantage de la MIAB pour les tumeurs< 20 mm (plus difficiles à ponctionner par EE). La décision de réaliser une MIAB pour le diagnostic doit prendre en compte le risque de saignement et sa gestion, une durée de procédure plus longue que l’EE avec ponction et le fait qu’elle pourrait empêcher une résection endoscopique ultérieure par tunnélisation sous-muqueuse (16).
Les résultats des ponctions à l’aiguille fine (EE-FNA) sont restés médiocres dans le diagnostic des TSM avec des taux d’efficacité diagnostique inférieurs à 60 % (17). Les aiguilles FNB plus récentes, conçues pour obtenir des échantillons histologiques, n’ont été évaluées que récemment. Dans une méta-analyse de 10 études portant sur 669 patients (18), comparant FNB et FNA, FNB a surpassé FNA dans tous les résultats diagnostiques évalués : à savoir, le taux d’échantillons adéquats, le taux optimal de prélèvement de carottes histologiques, la précision diagnostique et le nombre de passages nécessaires pour obtenir des échantillons diagnostiques. La supériorité de l’EE-FNB a été corroborée par deux grandes études rétrospectives multicentriques récentes (19-20). Il n’y a pas d’étude comparant les différents modèles et tailles d’aiguilles de FNB, ou les aspects techniques de l’échantillonnage, le nombre optimal de passages de l’aiguille, ou l’utilisation d’une évaluation rapide ou macroscopique sur place (ROSE ou MOSE). En considérant la chirurgie comme le gold standard, la précision diagnostique de l’histologie obtenue par EE-FNB est élevée (83 %-100 %).
Surveillance
L’ESGE recommande de ne pas surveiller les léiomyomes asymptomatiques, les lipomes, les pancréas hétérotopiques, les tumeurs à cellules granuleuses, les schwannomes, et les tumeurs glomiques, si le diagnostic est établi (Recommandation forte, preuves de qualité modérée).
En effet ces lésions ne justifient aucun type de surveillance puisque le risque de malignité/ complication est anecdotique et qu’il n’y a aucune preuve que la surveillance apporte un quelconque bénéfice chez ces patients.
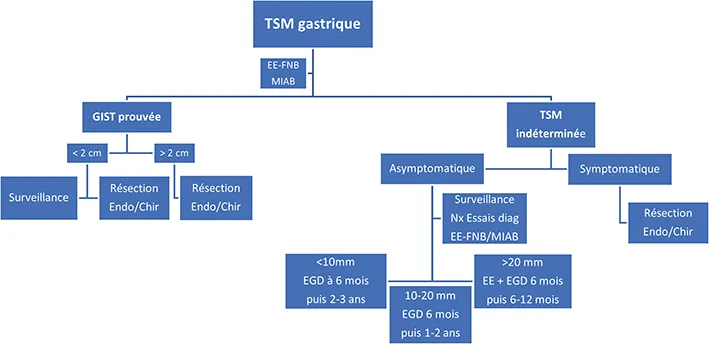
L’ESGE suggère que pour les GIST gastriques prouvées histologiquement, de taille < 20 mm, la surveillance ou la résection sont toutes deux des alternatives acceptables (Recommandation faible, preuves de très faible qualité). La stratégie est ici quelque peu controversée et nécessite d’être discutée avec le patient dans le contexte d’une réunion de concertation pluridisciplinaire dédiée, car le véritable potentiel du risque de malignité de ces lésions n’est connu qu’après la résection (figure 1). Néanmoins, la taille est un facteur de risque important et plusieurs études montrent que les GIST gastriques de moins de 20 mm ont un très faible risque de malignité et que la surveillance au lieu du traitement est une option sûre même pour les GIST de moins de 30 mm (en ne considérant la résection qu’en cas de croissance tumorale) (21), même si plusieurs sociétés (European Society for Medical Oncology [ESMO], Japan Society of Clinical Oncology [JSCO], Chinese Society of Clinical Oncology [CSCO]) recommandent la résection (10-12).

Figure 1 : Algorithme de prise en charge
Si l’on opte pour la surveillance des GIST prouvées, il faut être conscient de la faible compliance des patients au suivi à long terme (22). L’EE doit être recommandée comme la meilleure méthode de surveillance car il existe des caractéristiques à haut risque qui ne sont accessibles que par l’EE. Une surveillance par EE à 3-6 mois, puis à intervalles de 6-12 mois (pour les lésions de 20-30 mm), à 1-2 ans (pour les lésions de 10-20 mm) ou à 2-3 ans (pour les lésions de < 10 mm) pourrait être une bonne stratégie (même si aucune étude comparative ne permet de dire quelle est la meilleure stratégie de surveillance).
La situation est encore différente pour les tumeurs dont le diagnostic n’est pas (encore) établi (figure 1). L’ESGE suggère une surveillance des TSM œsophagiennes et gastriques asymptomatiques sans diagnostic précis, avec une EGD à 3-6 mois, puis à intervalles de 2-3 ans pour les lésions de taille < 10 mm et à intervalles de 1-2 ans pour les lésions de 10-20 mm. Pour les TSM asymptomatiques de taille > 20 mm qui ne sont pas réséquées, l’ESGE suggère une surveillance par EGD plus EE à 6 mois, puis à intervalles de 6 à 12 mois (Recommandation faible, preuves de très faible qualité).
Si le diagnostic est inconnu, la prise en charge dépendra de la localisation, et dans l’estomac, le diagnostic de GIST sera le plus souvent envisagé. Les lésions asymptomatiques, hypoéchogènes et bien délimitées (sans caractéristiques à haut risque à l’EE), d’une taille inférieure à 20 mm, et situées dans l’œsophage ou l’estomac présentent un très faible risque de malignité, et la surveillance semble probablement la meilleure option (23). Une étude rétrospective incluant 954 patients présentant ce type de lésion a montré que moins de 4 % de ces lésions avait augmenté de taille pendant la surveillance et qu’il n’y a pas eu de conséquences cliniques pour les patients (21). Une étude prospective multicentrique incluant 65 patients a suggéré que la surveillance de ce type de lésion (même de taille < 30 mm) est sûre, un seul patient ayant été orienté vers la chirurgie au cours du suivi (22). En ce qui concerne l’intervalle de surveillance, aucune étude n’a comparé différentes stratégies. La plupart des recommandations et avis d’experts suggèrent une EE et/ ou une EGD après 3 à 6 mois (pour confirmer la stabilité de la lésion), puis une EE ou une EGD chaque année ou tous les deux ans. Néanmoins, ces lésions comportent le risque d’être des GIST, avec un potentiel de malignité inhérent. Par conséquent, il pourrait être approprié de suivre la stratégie décrite ci-dessus pour les GIST connues pour lesquelles la décision de ne pas réséquer a été prise, avec des tentatives supplémentaires de diagnostic au moyen de l’EE-FNB. L’autre option est de procéder à une résection diagnostique pour obtenir un diagnostic précis (voir section Résection).
Résection
L’objectif de la résection endoscopique est de réaliser une résection curative R0, avec un taux de morbidité plus faible que la chirurgie, dans les lésions sans risque d’envahissement ganglionnaire. Les indications sont : le risque de malignité (GIST, et très rarement les tumeurs à cellules granuleuses) ; les symptômes tels que l’obstruction ou le saignement qui peuvent être associés à des léiomyomes, des schwannomes ou des lipomes ; et les lésions dans des endroits spécifiques chez les patients subissant une chirurgie bariatrique (4).
Le type de traitement et de suivi dépend du sous-type de tumeur, de la couche d’origine et de la localisation dans le tube digestif.
Œsophage
Les tumeurs à cellules granuleuses peuvent occasionnellement croître au cours du suivi, montrer une invasion dans la musculaire propre, ou être associées à une dysphagie, et dans ces cas, la résection endoscopique peut être envisagée. Les stratégies de traitement (EMR, ESD) dépendent de la taille et de la profondeur de l’infiltration de la paroi œsophagienne et également de l’expertise locale.
La majorité des tumeurs sous-muqueuses provenant de la musculeuse de l’œsophage sont des léiomyomes alors que les GIST sont très rares, représentant moins de 2 % des lésions. En cas de symptômes obstructifs, la résection endoscopique doit être mise en balance avec les risques et les avantages de l’énucléation thoracoscopique. En l’absence d’étude comparative, la taille et l’accès doivent déterminer la stratégie de traitement, avec une limite supérieure de taille de 35 mm pour l’approche endoscopique afin de permettre une ablation en bloc de la lésion (24). Dans l’œsophage, la dissection endoscopique avec tunnélisation (STER Submucosal tunneling endoscopic resection) type POEM est préférable. Une méta-analyse récente portant sur 701 patients présentant 728 lésions, dont 90 % dans l’œsophage ou le cardia, a montré des taux de résection en bloc, de résection R0 et d’événements indésirables de 86 % (95 % IC 75-93 %), 98 % (95 % IC 93-99 %) et 18 % (95 % IC 10-32 %), respectivement (25).
Estomac
L’ESGE suggère d’envisager la résection des GIST gastriques de moins de 20 mm prouvées histologiquement comme alternative à la surveillance. La décision de réséquer doit être discutée lors d’une réunion pluridisciplinaire. Le choix de la technique doit dépendre de la taille, de la localisation et de l’expertise locale (Recommandation faible, preuves de très faible qualité).
Les recommandations des sociétés scientifiques sont unanimes quant à l’indication de résection pour les GIST gastriques prouvées histologiquement et de taille supérieure à 2 cm, compte tenu de leur risque de malignité. En présence d’une indication de résection, l’ESGE suggère d’envisager l’excision endoscopique (soit la « Submucosal tunneling endoscopic resection » STER, « l’excavation sous-muqueuse endoscopique » ESE, ou l’EFTR) comme alternative à la chirurgie laparoscopique pour réséquer un GIST gastrique de taille < 35 mm et faisant saillie dans la lumière gastrique, avec une réunion multidisciplinaire préalable (Recommandation faible, preuves de très faible qualité) (4).
Les GIST de moins de 20 mm ont un faible risque de dégénérescence maligne et peuvent être suivies par endoscopie. Certains préconisent la résection endoscopique des GIST < 20 mm pour éviter la pénibilité d’un suivi répété par échoendoscopie pour des patients jeunes. Certains patients peuvent en effet préférer l’excision locale à un suivi répété à long terme. La limite supérieure de résécabilité endoscopique d’une GIST gastrique semble être de 40 mm, bien que des GIST de plus grande taille aient été retirés par voie endoscopique.
Les GIST non métastatiques de < 35 mm peuvent être excisées localement par EFTR (figure 2) ou par excision cunéiforme laparoscopique. Cette dernière est actuellement considérée comme le gold standard dans différentes recommandations internationales (26). La résection endoscopique des tumeurs sous-muqueuses originaires de la musculaire peut être divisée en techniques exposantes et non exposantes. Dans les techniques exposantes, la cavité intrapéritonéale est exposée au contenu luminal gastrique par une perforation iatrogène de la paroi gastrique qui est ensuite fermée. Les techniques de non-exposition ferment la perforation par tunnélisation sous-muqueuse (STER) (figure 3), ou avec une fermeture du défect muqueux par clippage préalable avec un dispositif de résection transmural type Ovesco. Il n’existe pas de comparaison directe randomisée entre les différentes méthodes de résection. Une méta-analyse récente portant sur 1 292 patients issus de 12 études principalement rétrospectives comparant la chirurgie laparoscopique à l’EFTR a montré des taux de complications, d’hospitalisation et de récidive similaires, avec une survie sans maladie à 5 ans similaire (27). Plus récemment des techniques hybrides associant laparoscopie et endoscopie (Lap-Endo cooperative surgery, LECS) montrent des avantages en terme de réduction des marges chirurgicales grâce à la visualisation endoscopique, avec une meilleure conservation anatomique et fonctionnelle de l’estomac.

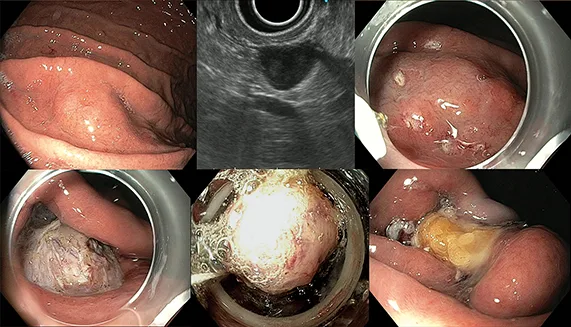
Figure 2 : Résection par FTRD d’une GIST gastrique de 15 mm
Tumeur sous-muqueuse peu bombante, connectée à la couche musculaire propre (4e couche), réséquée par technique hybride : ESD avec excavation puis EFTR à l’aide d’un clip OVESCO

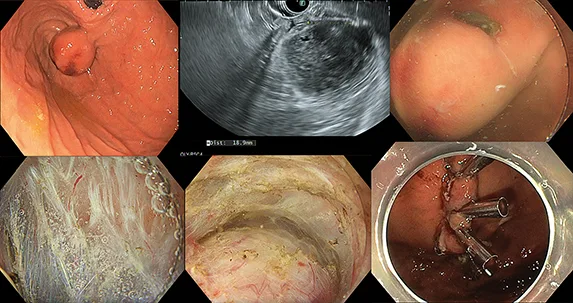
Figure 3 : Résection endoscopique d’une GIST gastrique hémorragique de 35 mm
Résection d’une tumeur sous-muqueuse hémorragique de 36 mm, sous-cardiale par technique STER (tunnélisation sous-muqueuse) sous eau en décubitus latéral gauche avec fermeture complète du défect musculaire limité et du défect muqueux par endoclips. La décision de résection endoscopique avait été prise en accord avec l’équipe chirurgicale du fait du caractère très protrusif de la lésion, stable sur le plan hémorragique sous IPP, de l’attache musculaire limitée à 15 mm, de la morbidité potentielle chirurgicale au niveau du cardia, et de l’accord de la patiente.
Une méta-analyse sur l’efficacité de la résection endoscopique des GIST de < 20 mm a montré un taux de résection R0 de 97 % (95 %CI 95 %-99 %), un taux de complication de 9 % (95 %CI 7 %-13 %), et un taux de récidive de 3 % (95 %CI 2 %-6 %) (28). Une autre méta-analyse sur les procédures STER gastriques pour des tumeurs sous-muqueuses a montré des résultats similaires, avec un taux de résection R0 de 97,9 % (95 %CI 93,6 %-99,3 %) (29).
Pour les tumeurs sous-muqueuses sans diagnostic histologique, l’ESGE suggère que, pour éviter un suivi inutile, la résection endoscopique soit une option pour les lésions gastriques de moins de 20 mm, après échec des tentatives d’obtention du diagnostic (Recommandation faible, preuves de très faible qualité).
Dans certains cas, il est en effet très difficile d’obtenir un diagnostic histologique, en raison de la petite taille de la lésion ou d’un accès difficile. Comme on suppose que 60 % des tumeurs sous-muqueuses provenant de la musculaire propre gastrique se révéleront être des GIST, cela conduit souvent à une surveillance biannuelle par échoendoscopie pour les lésions de taille < 20 mm. Il est connu que lorsqu’une stratégie de suivi est appliquée, les patients ont tendance à être perdus de vue après quelques séries d’investigations en raison d’une mauvaise compliance (22). Il n’existe pas de comparaison directe entre une stratégie de suivi avec résection en cas de croissance ou d’apparition de critères de malignité, et une stratégie d’excision diagnostique d’une tumeur d’histologie inconnue. L’alternative de la résection endoscopique au lieu du suivi doit être discutée avec le patient, au cas par cas.
Surveillance après résection
L’ESGE recommande de baser la stratégie de surveillance sur le type et le caractère complet de la résection. Après une résection curative d’une tumeur sous-muqueuse bénigne, aucun suivi n’est conseillé (Forte recommandation, preuves de faible qualité) (4).
Après une résection complète d’une GIST, la récidive locale n’est pas un problème (après une résection chirurgicale R0, les récidives sont principalement hépatiques ou péritonéales) et généralement, seules les méthodes d’imagerie (par ex. CT) sont recommandées pour la surveillance. Néanmoins, étant donné que l’histoire naturelle de cette tumeur après une résection endoscopique n’est pas clairement connue, une endoscopie 6 à 12 mois après la résection, puis après 2 à 3 ans, pourrait être une option pour la détection précoce d’une récidive locale qui pourrait être accessible à d’autres traitements (26).
L’ESGE suggère une nouvelle tentative de résection endoscopique ou chirurgicale après une résection non curative d’une GIST. Si cela n’est pas réalisable, la tumeur est considérée comme une tumeur localement avancée et sujette à une prise en charge oncologique (Recommandation faible, preuves de faible qualité).
Références
- 1. Nishida T, Kawai N, Yamaguchi S, et al. Submucosal tumors: Comprehensive guide for the diagnosis and therapy of gastrointestinal submucosal tumors. Dig Endosc 2013; 25: 479–489.
- Agaimy A, Wünsch PH, Hofstaedter F, et Minute gastric sclerosing stromal tumors (GIST tumorlets) are common in adults and frequently show c-KIT mutations. Am J Surg Pathol 2007; 31: 113–120.
- Casali PG, Abecassis N, Aro HT, et al. Gastrointestinal stromal tumours: ESMO-EURACAN clinical practice guidelines for diagnosis, treatment and follow-up. Ann Oncol 2018; 29: iv68–iv78.
- Deprez PH, Moons LMG, O’Toole D, Gincul R, Seicean A, Pimentel-Nunes P, et Endoscopic management of subepithelial lesions including neuroendocrine neoplasms: European Society of Gastrointestinal Endoscopy (ESGE) Guideline. Endoscopy. 2022 Apr;54(4):412-429. doi: 10.1055/ a-1751-5742. Epub 2022 Feb 18. PMID: 35180797.
- Rösch T, Kapfer B, Will U, et Accuracy of endoscopic ultrasonography in upper gastrointestinal submucosal lesions: a prospective multicenter study. Scand J Gastroenterol 2002; 37: 856–862.
- Karaca C, Turner BG, Cizginer S, et Accuracy of EUS in the evaluation of small gastric subepithelial lesions. Gastrointest Endosc 2010; 71: 722–727.
- Tang JY, Tao KG, Zhang LY, et al. Value of contrast-enhanced harmonic endoscopic ultrasonography in differentiating between gastrointestinal stromal tumors: A meta-analysis. J Dig Dis 2019; 20: 127–134. doi:10.1111/1751-2980.12710.
- Sakamoto H, Kitano M, Matsui S, et Estimation of malignant potential of GI stromal tumors by contrast-enhanced harmonic EUS (with videos). Gastrointest Endosc 2011; 73: 227–237.
- Akahoshi K, Oya M, Koga T, et Clinical usefulness of endoscopic ultrasound-guided fine needle aspiration for gastric subepithelial lesions smaller than 2 cm. J Gastrointestin Liver Dis 2014; 23: 405-412.
- ESMO/European Sarcoma Network Working Group. Gastrointestinal stromal tumours: ESMO clinical practice guidelines for diagnosis, treatment and follow-up. Ann Oncol 2014; 25 Suppl 3: iii21–26. doi:10.1093/annonc/mdu255.
- Nishida T, Hirota S, Yanagisawa A, et al. Clinical practice guidelines for gastrointestinal stromal tumor (GIST) in Japan: English Int J Clin Oncol 2008; 13: 416–430. doi:10.1007/s10147-008-0798-7.
- Li J, Ye Y, Wang J, et al. Chinese consensus guidelines for diagnosis and management of gastrointestinal stromal Chin J Cancer Res Chung-Kuo Yen Cheng Yen Chiu 2017; 29: 281–293. doi:10.21147/j.issn.1000-9604.2017.04.01.
- von Mehren M, Kane JM, Bui MM, et al. NCCN guidelines insights: Soft tissue sarcoma, version 2021. J Natl Compr Canc Netw 2020;18:1604–1612. doi: 10.6004/jnccn.2020.0058. PMID: 33285515.
- Dhaliwal A, Kolli S, Dhindsa BS, et Clinical efficacy and safety of mucosal incision-assisted biopsy for the diagnosis of upper gastrointestinal subepithelial tumors: A systematic review and meta-analysis. Ann Gastroenterol 2020; 33: 155–161. doi:10.20524/aog.2020.0460.
- Osoegawa T, Minoda Y, Ihara E, et Mucosal incision-assisted biopsy versus endoscopic ultrasound-guided fine-needle aspiration with a rapid on-site evaluation for gastric subepithelial lesions: A randomized cross-over study. Dig Endosc 2019; 31: 413–421.
- Sanaei O, Fernández-Esparrach G, De La Serna-Higuera C, et al. EUS-guided 22-gauge fine needle biopsy versus single-incision with needle knife for the diagnosis of upper gastrointestinal subepithelial lesions: a randomized controlled trial. Endosc Int Open 2020; 8: E266–E273.
- Zhang X-C, Li Q-L, Yu Y-F, et Diagnostic efficacy of endoscopic ultrasound-guided needle sampling for upper gastrointestinal subepithelial lesions: a meta-analysis. Surg Endosc 2016; 30: 2431–2441.
- Facciorusso A, Sunny SP, Del Prete V, et Comparison between fine-needle biopsy and fine-needle aspiration for EUS-guided sampling of subepithelial lesions: a meta-analysis. Gastrointest Endosc 2020; 91: 14-22.e2.
- Trindade AJ, Benias PC, Alshelleh M, et Fine-needle biopsy is superior to fine-needle aspiration of suspected gastrointestinal stromal tumors: a large multicenter study. Endosc Int Open 2019; 7: E931–E936.
- de Moura DTH, McCarty TR, Jirapinyo P, et al. EUS-guided fine-needle biopsy sampling versus FNA in the diagnosis of subepithelial lesions: a large multicenter study. Gastrointest Endosc 2020; 92: 108-119.e3.
- Song JH, Kim SG, Chung SJ, et Risk of progression for incidental small subepithelial tumors in the upper gastrointestinal tract. Endoscopy 2015; 47: 675–679. doi:10.1055/s-0034-1391967.
- Kushnir VM, Keswani RN, Hollander TG, et al. Compliance with surveillance recommendations for foregut subepithelial tumors is poor: results of a prospective multicenter study. Gastrointest Endosc 2015; 81: 1378–1384.
- Dumonceau J-M, Deprez PH, Jenssen C, et Indications, results, and clinical impact of endoscopic ultrasound (EUS)-guided sampling in gastroenterology: European Society of Gastrointestinal Endoscopy (ESGE) Clinical Guideline – Updated January 2017. Endoscopy 2017; 49: 695–714.
- Ye L-P, Zhang Y, Mao X-L, et Submucosal tunnelling endoscopic resection for the treatment of esophageal submucosal tumours originating from the muscularis propria layer: an analysis of 15 cases. Dig Liver Dis 2013; 45: 119–123.
- Peng W, Tan S, Huang S, et Efficacy and safety of submucosal tunneling endoscopic resection for upper gastrointestinal submucosal tumors with more than 1-year follow-up: a systematic review and meta-analysis. Scand J Gastroenterol 2019; 54: 397–406.
- Landi B, Blay J-Y, Bonvalot S, et al. Gastrointestinal stromal tumours (GISTs): French Intergroup clinical practice guidelines for diagnosis, treatments and follow-up (SNFGE, FFCD, GERCOR, UNICANCER, SFCD, SFED, SFRO). Dig Liver Dis 2019; 51: 1223–1231.
- Wang C, Gao Z, Shen K, et Safety and efficiency of endoscopic resection versus laparoscopic resection in gastric gastrointestinal stromal tumours: A systematic review and meta-analysis. Eur J Surg Oncol 2020; 46: 667–674.
- Zhang Q, Gao L-Q, Han Z-L, et Effectiveness and safety of endoscopic resection for gastric GISTs: a systematic review. Minim Invasive Ther Allied Technol 2018; 27: 127–137.
- Antonino G, Alberto M, Michele A, et Efficacy and safety of gastric exposed endoscopic full-thickness resection without laparoscopic assistance: a systematic review. Endosc Int Open 2020; 8: E1173–E1182.
Abréviations
EE : échoendoscopie
EFTR : endoscopic full-thickness resection
EGD : Eoso-gastro-duodénoscopie
EMR : endoscopic mucosal resection
ESD : endoscopic submucosal dissection
ESE : endoscopic submucosal excavation
ESGE : European Society of Gastrointestinal Endoscopy
FNA : fine-needle aspiration
FNB : fine-needle biopsy
GIST : gastrointestinal stromal tumor
MIAB : mucosal incision-assisted biopsy
STER : Submucosal tunneling endoscopic resection
TSM : Tumeur sous-muqueuse