Objectifs pédagogiques
- Connaître les manifestations proctologiques des hémopathies
- Savoir reconnaître les lésions anales métastatiques
- Savoir identifier les cancers rares de l’anus et connaître les principes de prise en charge
L’auteur déclare n’avoir aucun conflit d’intérêt avec sa présentation
Hémopathie – Métastase – Adénocarcinome – Mélanome – Carcinome basocellulaire
Non communiquées
On considère qu’environ 85 % des cancers de l’anus sont des carcinomes épidermoïdes. Les cancers non épidermoïdes de l’anus sont donc rares. De surcroît, ils recouvrent des pathologies très diverses. Dans cette mise au point, nous aborderons les hémopathies malignes, les métastases, les adénocarcinomes primitifs, les carcinomes basocellulaires, les mélanomes malins ainsi que les tumeurs mésenchymateuses et les tumeurs neuro- endocrines.
Les manifestations proctologiques des hémopathies malignes sont relativement fréquentes. Les hémopathies en cause sont diverses (tableau 1). Les patients atteints ont la particularité d’être souvent immuno-déprimés en raison de l’hémopathie elle-même, de l’hématotoxicité des divers traitements et/ou du contexte pathologique (infection par le VIH notamment ou maladie de Crohn sous traitement immuno-suppresseur) (1).
| ▪ Leucémies aiguës et chroniques |
| ▪ Lymphomes (le plus souvent non hodgkiniens) |
| ▪ Myélome multiple |
| ▪ Syndromes myélodysplasiques |
Tableau 1 : Principales hémopathies malignes pouvant se manifester par des signes proctologiques
Les lésions cliniques se caractérisent par leur polymorphisme et donc leurs nombreux diagnostics différentiels. En effet, il peut s’agir :
Il s’agit de localisations anales de l’hémopathie qui se présentent alors de façon diverse : ulcération, infiltration, masse… (figures 1 et 2) (1-4).
Leur présentation est également variable : abcès, fistule, cellulite… (1, 5-7). Elles sont fréquentes avec une prévalence oscillant entre 5 et 10 % (7-9). Elles seraient favorisées par un antécédent d’infection, une pathologie hémorroïdaire, une constipation et/ou une diarrhée persistante (7). Les germes en cause sont nombreux : cocci à Gram positif et négatif, anaérobies, Candida albicans… (8). Elles sont volontiers sévères avec un sur-risque de cellulite nécrosante et de septicémie (1, 5, 8, 10, 11).
Il peut s’agit de fissure, de pathologie hémorroïdaire, de condylomes, d’infection herpétique… (5, 7).
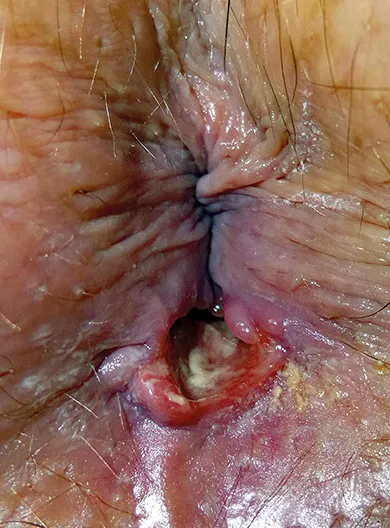
Figure n°1 : Atteinte anale d’une leucémie aiguë myélobastique
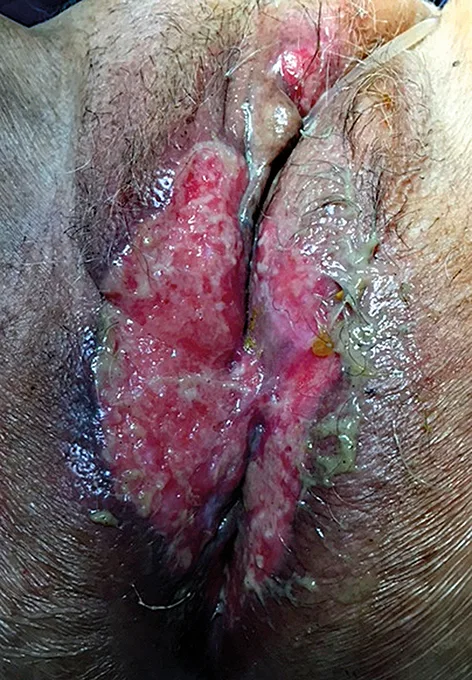
Figure n°2 : Atteinte ano-périnéale d’un lymphome (Coll.
Benoît Mory)
Le diagnostic des atteintes spécifiques repose sur l’histologie. Le diagnostic des autres lésions est clinique. Cependant, la présentation des suppurations peut être trompeuse en cas d’aplasie en raison de l’absence de pus franc (10). L’IRM peut être utile pour le bilan topographique des trajets fistuleux et des collections (12).
Le traitement de fond dépend habituellement du type d’hémopathie maligne et repose notamment sur la chimiothérapie, les anticorps monoclonaux et/ou la radiothérapie. En cas de suppuration, l’indication chirurgicale n’est pas facile à poser dans ce contexte de patients souvent fragiles en raison de l’âge, de l’immuno-dépression et/ou de la pancytopénie fréquente (5, 7, 10). Ceci étant dit, la chirurgie est souvent nécessaire en cas d’abcès (5), utile (10, 11) et relativement bien tolérée (9).
Les métastases anales sont exceptionnelles.
Elles peuvent se présenter sous la forme d’une masse anale ou péri-anale, cutanée et/ou muqueuse, bourgeonnante ou non, ulcérée ou non (Figure 3). Les cancers primitifs en cause concernent surtout le rectum et le côlon ainsi que le poumon, le sein, le rein et le pancréas. La dissémination se fait par voie hématogène (13-15).
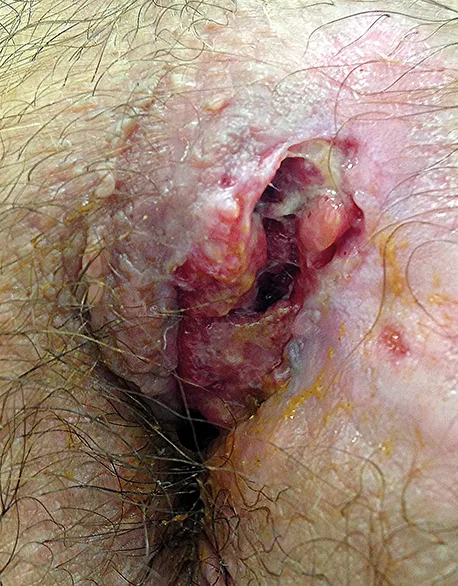
Figure n°3 : Métastase anale d’un adénocarcinome du sigmoïde
Les métastases anales peuvent aussi se présenter sous la forme d’une fistule. Cette forme a été largement décrite dans la littérature. Les cancers en cause sont pour l’essentiel ceux du rectum, du sigmoïde et du côlon gauche. La dissémination semble se faire par voie endoluminale, des cellules exfoliées venant s’implanter dans des zones d’effractions muqueuses pathologiques (fissure, fistule…) ou post-chirurgicales. Les patients sont en général des hommes dont l’âge moyen est de 60 ans (16-18).
La maladie de Paget anale dans sa forme secondaire est un cas particulier clinico-histologique. Sa présentation clinique est polymorphe sous la forme de plaques érythémateuses planes, plus ou moins étendues, parfois suintantes, ulcérées, hypertrophiques et/ou lichénifiées par endroits, voire infiltrées, au niveau de la marge et de la peau péri-anale (Figure 4). Les diagnostics différentiels sont nombreux (Tableau 2) et des prélèvements à visée histologique sont indispensables au moindre doute, notamment en cas de « dermatose chronique » rebelle aux divers topiques. Sur le plan histologique, il s’agit d’un adénocarcinome intra-épithélial avec de multiples cellules arrondies, de grande taille, dotées d’un cytoplasme pâle abondant PAS+ et d’un noyau volumineux anisocaryotique (cellules de Paget) (Figure 5). C’est une affection rare, avec moins de 200 cas publiés dans la littérature. La localisation anale et péri-anale de la maladie de Paget correspondrait à moins de 20 % de ses formes extra-mammaires mais en représenterait la localisation la plus fréquente. Elle résulterait soit de l’extension de contiguïté d’un carcinome du canal anal ou de la vulve, soit de la propagation à l’anus d’un cancer viscéral synchrone ou métachrone distant, notamment colo-rectal, uro-génital ou mammaire. Elle survient surtout après l’âge de 50 ans (19, 20).
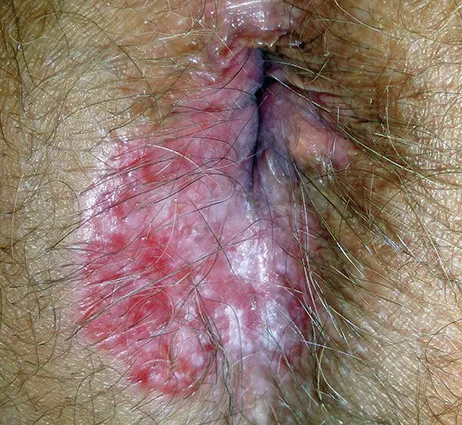
Figure n°4 : Maladie de Paget péri-anale secondaire
| ▪ Psoriasis |
| ▪ Eczéma |
| ▪ Maladie de Bowen |
| ▪ Lichen plan |
| ▪ Lichen scléreux |
| ▪ Carcinome basocellulaire |
| ▪ Dermites infectieuses (bactériennes, mycosiques, virales…) |
| ▪ Pemphigus bénin familial |
| ▪ Maladie de Crohn |
| ▪ Hidradénite suppurative |
Tableau 2 : Principaux diagnostics différentiels de la maladie de Paget
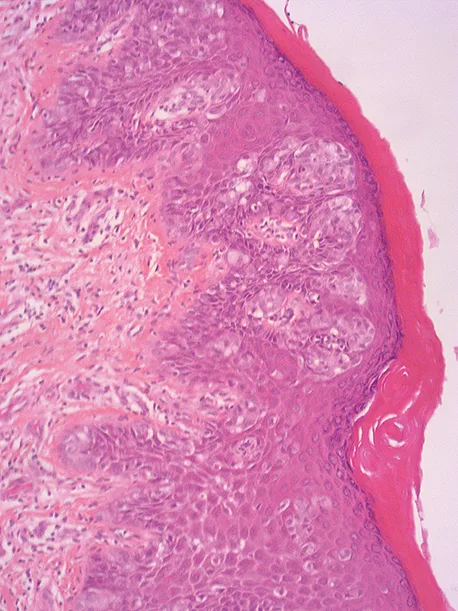
Figure n°5 : Aspect histologique d’une maladie de Paget
Dans tous les cas, les signes cliniques sont variables et non spécifiques : douleurs, prurit, saignements ou masse palpable.
Le diagnostic repose sur l’analyse histologique. L’étude immuno-histochimique (marqueurs CK7, CK20…) peut orienter vers l’origine secondaire et aider à évoquer le cancer primitif en cause.
Le traitement dépend de la tumeur primitive en cause, de son histologie, de l’extension par ailleurs. Il repose sur la chirurgie (amputation abdomino- périnéale notamment), la radiothérapie, la chimiothérapie, l’hormonothérapie, l’immunothérapie ou une combinaison de ces diverses approches. Le pronostic dépend du contexte. Il peut être meilleur en cas de maladie de Paget car l’évolution est en général plus lente, même si les récidives sont fréquentes et qu’il y a risque de cancer viscéral métachrone. À l’inverse, les métastases issues de cancers colo-rectaux semblent être plus agressives (16-20).
Les adénocarcinomes de l’anus représentent moins de 10 % des cancers de l’anus. En général, ils ne sont pas liés aux papillomavirus oncogènes. L’Organisation Mondiale de la Santé a proposé une classification des adénocarcinomes primitifs de l’anus (Tableau 3) (21). En pratique clinique, on voit surtout des adénocarcinomes de la muqueuse et/ou des glandes, les fistules dégénérées en adénocarcinome et la maladie de Paget primitive. Les adénocarcinomes de la muqueuse sont issus de l’épithélium glandulaire lieberkühnien de la partie haute du canal anal, voire d’îlots épithéliaux situés à distance, notamment dans la zone anale transitionnelle. Le phénotype peut être mucineux (anciennement colloïde muqueux) ou non mucineux. Les adénocarcinomes des glandes, non mucineux, sont issus des glandes de Hermann et Desfosses. L’âge moyen de ces patients est de 70 ans. La tumeur se présente le plus souvent sous la forme d’une masse plus ou moins ulcérée (Figure 6) (22, 23).
| ▪ Origine muqueuse : tumeurs provenant de la muqueuse luminale, siégeant souvent à la partie haute du canal anal (parfois difficile à distinguer d’un adénocarcinome du bas rectum) |
| ▪ Origine extra-muqueuse : tumeurs : – issues de glandes anales |
| ▪ Origine glandulaire ne correspondant pas aux deux catégories précédentes |
| ▪ Origine des annexes cutanées |
| ▪ Maladie de Paget primitive extra-mammaire |
Tableau 3 : Classification de l’Organisation Mondiale de la Santé des adénocarcinomes primitifs de l’anus
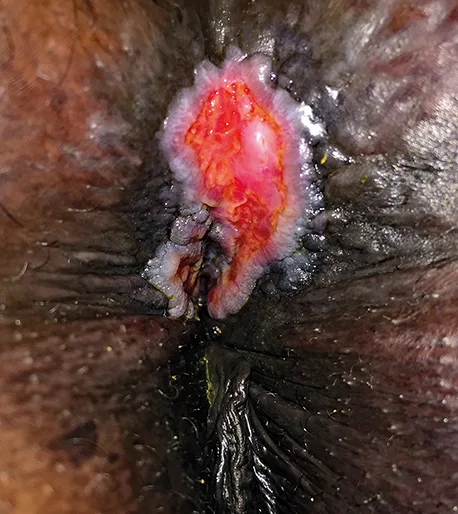
Figure n°6 : Adénocarcinome glandulaire primitif de l’anus (Coll. Eric Safa Far)
Les adénocarcinomes liés aux fistules anales (souvent mucineux) surviennent en cas de suppuration évoluant depuis plus de 10 ans, chez des patients de la cinquantaine, souvent atteints de maladie de Crohn. L’inflammation chronique semble en cause, possiblement favorisée par la prise de traitements immuno-suppresseurs. L’aspect clinique est souvent celui d’une fistule d’allure banale (Figure 7) (24-26).
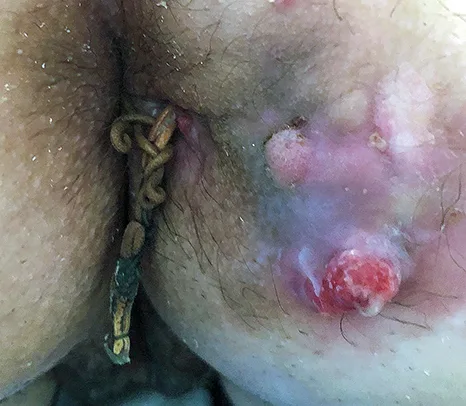
Figure n°7 : Fistule anale dégénérée en adénocarcinome d’une maladie de Crohn
La maladie de Paget a été précédemment évoquée. Dans le cas particulier, il s’agit de sa forme primitive (Figure 8). Les cellules de Paget semblent se développer à partir des cellules souches indifférenciées et pluripotentes de l’épiderme ou des annexes. La maladie de Paget primitive semble survenir plutôt après l’âge de 60 ans (19, 20).
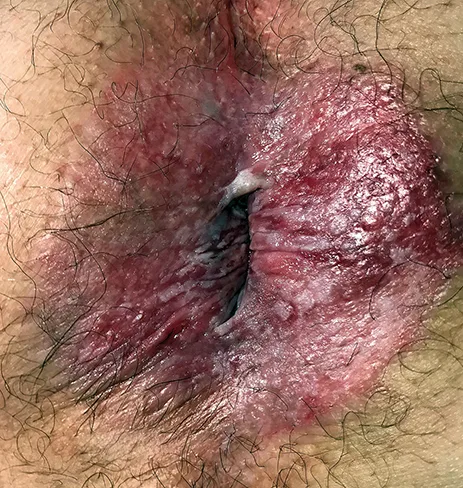
Figure n°8 : Maladie de Paget péri-anale primitive
Dans tous les cas, le diagnostic repose sur l’analyse histologique. L’immuno-histochimie (cytokératines) permet la recherche de l’épithélium d’origine.
En l’absence de grandes séries, le traitement n’est pas consensuel et il y a une grande variabilité dans la littérature. Le traitement par chimio- radiothérapie néo adjuvante suivi d’une chirurgie radicale d’amputation abdomino-périnéale semble être l’approche la plus efficace, donnant les meilleurs résultats en termes de survie (23, 27). Concernant la maladie de Paget, l’exérèse locale, parfois complétée par des plasties cutanées de recouvrement, est suffisante dans la plupart des cas (28). Cependant, elle n’est pas toujours possible lorsque les lésions sont étendues et/ou que le terrain se prête peu à une exérèse large. Certains proposent alors des applications d’imiquimod ou de 5-fluorouracil, voire de la photothérapie dynamique, mais les données publiées sont pauvres. Dans tous les cas, le suivi est impératif en raison du risque élevé de récidives (29, 30).
Le pronostic est mauvais. Il dépend bien sûr du terrain, de la taille, de l’extension et du degré de différenciation de la tumeur (31). Cependant, l’adénocarcinome primitif de l’anus est plus agressif que le carcinome épidermoïde de l’anus (32) et peut-être aussi que l’adénocarcinome du rectum (33). Le pronostic est également altéré en cas de fistule dégénérée dans le contexte d’une maladie de Crohn, sans doute en raison du diagnostic souvent tardif et de la prise de traitements immuno-suppresseurs (34). En revanche, le pronostic de la maladie de Paget primitive est meilleur, avec une survie globale et sans récidive d’environ 60 % à 5 ans, même si la localisation péri-anale semble avoir le moins bon pronostic des formes extra-mammaires de cette maladie (35).
Le mélanome malin est une tumeur issue des mélanocytes. Il représente environ 1 % des tumeurs anales. Cette localisation est au troisième rang après la peau et l’œil, mais elle représente moins de 3 % de la totalité des mélanomes malins.
Il est favorisé par l’exposition aux rayons ultraviolets au niveau de la peau mais ça n’est pas un facteur de risque au niveau ano-rectal (36). En revanche, le risque de mélanome est augmenté chez les patients atteints de MICI et traités par thiopurine et anti-TNF (37).
Le mélanome survient à tout âge avec un pic de fréquence à la sixième décennie, avec une prédominance féminine.
Les signes cliniques ne sont pas spécifiques : saignements, douleurs, sensation de tuméfaction, etc. À l’examen, le diagnostic peut être suspecté en cas de lésion pigmentée (Figure 9) mais une petite tumeur peut ressembler à une banale thrombose hémorroïdaire externe et induire en erreur. De même, il y a 20 à 30 % de formes achromiques qui sont trompeuses.
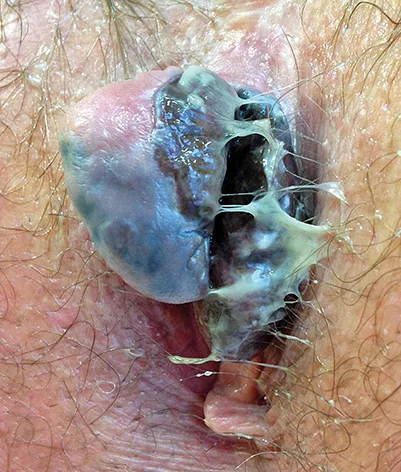
Figure n°9 : Mélanome malin de l’anus
En pratique, le diagnostic est donc souvent tardif. Le diagnostic formel repose sur l’histologie et l’immuno-histochimie. Le bilan d’extension par IRM pelvienne, scanner thoraco-abdomino-pelvien et TEP-scan permet de classer la tumeur (Tableau 4) (36).
| atteinte locale isolée |
| atteinte ganglionnaire loco-régionale |
| atteinte métastatique à distance (foie, poumons, os, cerveau…) |
Tableau 4 : Classification des mélanomes malins
Les principaux facteurs de mauvais pronostic sont indiqués dans le Tableau 5 (38).
| ▪ Longue durée des symptômes (plus de 3 mois) |
| ▪ Taille de la tumeur |
| ▪ Stade avancé de la tumeur |
| ▪ Atteinte des ganglions lymphatiques inguinaux |
| ▪ Mélanome achromique |
Tableau 5 : Principaux facteurs de mauvais pronostic d’un mélanome malin
Le traitement de première intention est, si possible, chirurgical. Cependant, il y a un débat non tranché entre l’exérèse locale et l’amputation abdomino-périnéale. Cette dernière est souvent envisagée car elle permet une exérèse loco-régionale complète mais sa pertinence est de plus en plus remise en question pour les raisons suivantes :
La radiothérapie adjuvante, avec ou sans chimiothérapie, n’a pas non plus démontré son intérêt formel en termes de survie. En revanche, la prise en charge du mélanome malin cutané a progressé au cours de la dernière décennie avec les nouvelles thérapies ciblées (inhibiteurs de BRAF et de MEK) et l’immunothérapie (ipilimumab, pembrolizumab, nivolumab…) qui semblent avoir un impact significatif sur la survie (40).
Le pronostic est souvent péjoratif, en raison de l’extension ganglionnaire et métastatique rapide et fréquente dès lors que la lésion mesure plus de 3 mm de diamètre, ce qui est le plus souvent le cas pour les mélanomes ano-rectaux. La survie sans récidive à 5 ans des formes opérées est de moins de 25 % (36, 38).
Le carcinome basocellulaire se développe à partir des cellules de la couche basale de l’épiderme. Il ne touche pas les muqueuses.
Son incidence augmente avec l’âge (âge moyen de 70 ans) avec une prédominance masculine. C’est une des tumeurs malignes les plus fréquentes de la peau et il siège le plus souvent au niveau du visage, du cou et du cuir chevelu. En revanche, la localisation anale ou péri-anale est exceptionnelle. Elle représente moins de 1 % de l’ensemble des carcinomes basocellulaires et environ 0,2 % de l’ensemble des cancers de l’anus avec environ 200 cas publiés, pour la plupart sous forme de cas cliniques.
Il est favorisé par l’exposition solaire prolongée. Un antécédent de radiothérapie, des antécédents familiaux, une immuno-suppression seraient également des facteurs de risque (41-44). De même, le risque de carcinome basocellulaire avant un diagnostic de RCH est plus élevé que chez les témoins non RCH et les traitements à base de thiopurine et d’anti-TNF augmenteraient le risque chez les patients atteints de MICI (37). En revanche, il ne semble pas y avoir de lien avec les papillomavirus oncogènes.
Les signes cliniques sont minimes, voire inexistants, en raison de la croissance lente et de l’absence de douleur. Le diagnostic est donc souvent fortuit.
La tumeur se présente sous la forme d’un nodule et/ou d’une papule, plus ou moins étendue en surface, souvent mal limité, parfois ulcéré, de couleur rosée ou grisâtre, voire pigmenté (Figure 10). Elle siège au niveau de la marge et de la peau péri-anale. L’extension canalaire est très rare. Les diagnostics différentiels sont nombreux (Tableau 6). L’aspect translucide perlé des bords et la présence de fines télangiectasies sont évocateurs. Il faut rechercher d’autres lésions concomitantes car elles seraient présentes chez 25 % des patients.
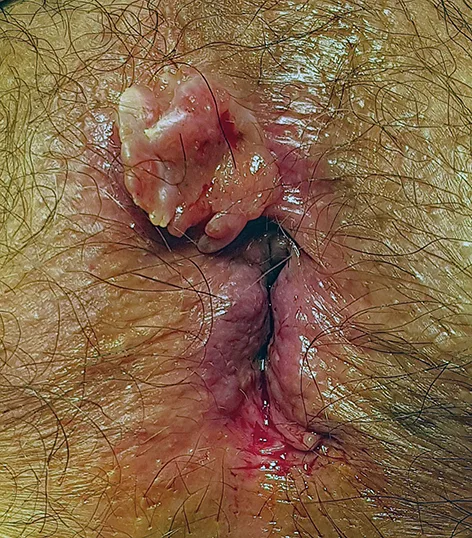
Figure n°10 : Carcinome basocellulaire de la marge anale
| ▪ Thrombose hémorroïdaire |
| ▪ Naevus |
| ▪ Mélanome |
| ▪ Carcinome épidermoïde |
| ▪ Adénocarcinome |
| ▪ Maladie de Bowen |
| ▪ Maladie de Paget |
| ▪ Kératose séborrhéique |
Tableau 6 : Principaux diagnostics différentiels du carcinome basocellulaire
Le diagnostic formel repose sur l’analyse histologique. L’immuno-histochimie est utile dans les cas difficiles, notamment de diagnostic différentiel avec le carcinome épidermoïde.
Le bilan d’extension est inutile car le carcinome basocellulaire a une malignité locale et son potentiel métastatique est extrêmement faible.
La chirurgie d’exérèse locale est le traitement de référence. La chirurgie plastique peut être utile en cas d’exérèse étendue. Les autres traitements relèvent de l’exception : radiothérapie, photothérapie dynamique, cryothérapie, coagulation, applications d’imiquimod ou de 5-fluorouracil, etc.
Les récidives sont rares. En revanche, la surveillance est conseillée en raison de la possible survenue de nouvelles lésions. Le pronostic est excellent dans la plupart des cas en raison de l’exceptionnel envahissement en profondeur (41-44).
Les tumeurs mésenchymateuses de l’anus sont exceptionnelles. La littérature est quasi exclusivement composée de cas cliniques (Tableau 7). Elles se présentent sous la forme d’une masse sous-cutanée et/ou sous-muqueuse, parfois ulcérée (Figure 11).
| ▪ GIST (Gastrointestinal Stromal Tumor) (45) |
| ▪ Léïomyome (46) |
| ▪ Schwannome (47) |
| ▪ Lymphangiome (48) |
| ▪ Lipome (49) |
| ▪ Neurofibrome (50) |
Tableau 7 : Principales tumeurs mésenchymateuses de l’anus publiées
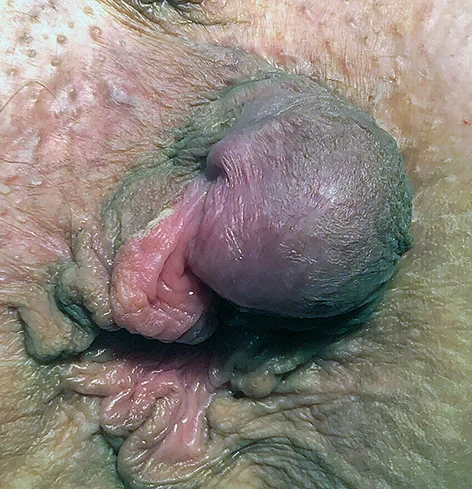
Figure n°11 : Léïomyome de la marge anale (Coll. Lucas Spindler)
Le diagnostic repose sur l’analyse histologique et immuno-histochimique pour différencier les tumeurs mésenchymateuses entre elles. L’imagerie est indispensable pour le bilan d’extension locale avant traitement (51).
Étant donné la rareté de la pathologie, il n’y a pas de standard de traitement. Il repose le plus souvent sur l’exérèse chirurgicale qui doit se faire sans effraction de la tumeur. Cette exérèse peut être purement locale ou élargie pouvant alors aller jusqu’à l’amputation abdomino-périnéale. Un traitement néoadjuvant par inhibiteurs de tyrosine kinase peut également être proposé afin de réduire le volume tumoral d’une GIST.
La surveillance est nécessaire en raison du risque de récidive locale. Le pronostic est meilleur en cas de tumeur de petite taille (< 2 cm) et d’un nombre de mitoses ≤ 5 par champ (52, 53).
Les tumeurs neuroendocrines de l’anus sont également exceptionnelles. Là encore, la littérature est pour l’essentiel constituée de cas cliniques (54-56). Il semblerait que leur incidence augmente, possiblement en raison de la généralisation du dépistage du cancer colo-rectal et une meilleure connaissance de la pathologie (57, 58).
Elles proviennent probablement des cellules neuroendocrines situées dans la muqueuse de type glandulaire du haut canal anal, voire dans la muqueuse transitionnelle. On distingue classiquement les tumeurs neuroendocrines bien différenciées et les carcinomes neuroendocrines peu différenciés (59).
Elles se présentent sous la forme d’une masse de taille variable, enfouie sous la peau et/ou la muqueuse (Figure 12).
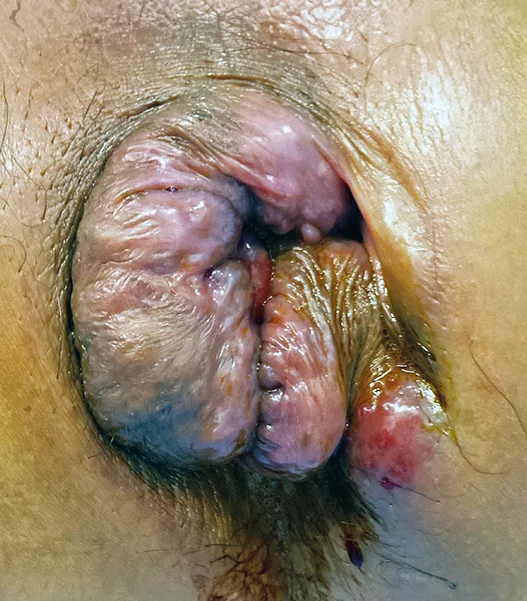
Figure n°12 : Tumeur neuro-endocrine de la marge anale (quadran antéro-droit) (Coll. Elise Pommaret)
Le diagnostic repose sur l’analyse histologique. Les colorations immuno-histochimiques sont utiles en cas de diagnostic différentiel avec les autres tumeurs malignes.
Elles sont le plus souvent localisées au moment du diagnostic et les formes métastatiques représentent moins de 15 % des cas (60). Le risque métastatique est plus élevé en cas de grande taille, d’envahissement de la musculeuse, d’invasion lympho-vasculaire et d’un taux élevé de mitoses. Le traitement est proposé par assimilation à celui des tumeurs à localisation rectale. Les lésions de moins de 1 cm de diamètre, sans aucun facteur de mauvais pronostic, peuvent être réséquées par exérèse chirurgicale simple ou par voie endoscopique. Les lésions de plus de 2 cm relèvent d’un bilan d’extension et d’une prise en charge chirurgicale carcinologique. La prise en charge des lésions entre 1 et 2 cm n’est pas consensuelle (60-62).
Le taux de survie global à 5 ans pour toutes les tumeurs carcinoïdes, quel que soit le site, est d’environ 70 % mais le pronostic serait meilleur au niveau ano-rectal (57).
L’auteur remercie le Dr Nadia Fathallah pour sa relecture du manuscrit, et le docteur Julien Adam, chef du service d’anatomo-pathologie de l’Hôpital Paris Saint-Joseph, pour ses précieux conseils.
Toute reproduction ou réécriture, totale ou partielle, sans l’accord préalable écrit de la FMC HGE est interdite.
FMC HGE : Organisme certifié Qualiopi pour la catégorie ACTIONS DE FORMATION.