Histoire naturelle de la maladie de Crohn
Objectifs pédagogiques
- Connaître l’évolution clinique des lésions et l’incidence des complications à long terme au cours de la maladie de Crohn
- Connaître les principaux facteurs prédictifs d’une évolution sévère de la maladie, notamment des risques de chirurgie délabrante
- Connaître l’impact des biothérapies et de l’usage précoce des immunosuppresseurs sur l’histoire naturelle de la maladie de Crohn
Introduction
L’histoire naturelle d’une maladie correspond à la description de son évolution au cours du temps, de son diagnostic jusqu’à la guérison ou la mort. Il s’agit d’une composante majeure de l’épidémiologie descriptive. Seules les études en population fournissent des données fiables sur l’histoire naturelle d’une maladie. C’est la raison pour laquelle nous n’aborderons pas ici les données provenant de centres experts tels les CHU en France, où les patients suivis ont une maladie plus sévère que dans les études de population. Différentes études en population ayant analysé l’histoire naturelle de la maladie de Crohn (MC) à travers le monde1, 2. Seuls les aspects concernant l’histoire naturelle de la MC chez l’adulte seront abordés ici.
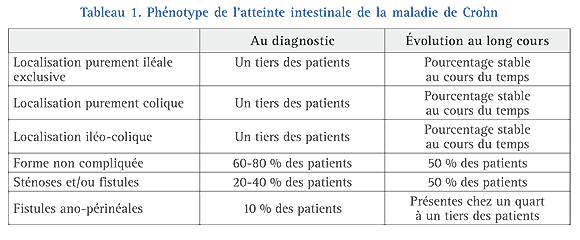
Phénotype de l’atteinte intestinale (Tableau 1)
Atteinte luminale et complications intestinales de la maladie de Crohn
La première étude à s’être intéressée à l’évolution de la localisation de la MC au cours du temps a repris les données de 103 patients diagnostiqués entre 1943 et 1982 dans le comté d’Olmsted, dans l’état du Minnesota aux États- Unis3. Lors du diagnostic initial, 35 % avaient une localisation iléale pure, 36 % avaient une localisation colique isolée, et 29 % avaient une localisation iléo-colique. Près de deux tiers des patients avaient une atteinte plus étendue au niveau du côlon et/ou de l’intestin grêle après un suivi médian de 8,5 ans.
Parmi les patients avec une MC diagnostiquée entre 1940 et 1993 (n = 226), un âge jeune au diagnostic et une atteinte iléale étaient associées au risque d’avoir une forme pénétrante. Contrairement au risque de complications (fistules, abcès, sténoses) qui augmentait au cours du temps, un changement dans la localisation de l’atteinte intestinale survenait chez seulement seuls 6,5 % des patients durant la même période de suivi.
En Europe, l’étude en population norvégienne IBSEN (Inflammatory Bowel South-Eastern Norway) a montré que parmi 200 patients avec une MC, 27 % avaient une iléite, 45 % une colite, 26 % une iléo-colite et 4 % avaient une atteinte du tube digestif supérieur au diagnostic4. Après 5 ans de suivi, ces chiffres étaient respectivement de 23 %, 37 %, 38 %et 6 %. Globalement, un changement dans la localisation de la maladie était observé chez 14 %des patients4. Dans une étude de population européenne multicentrique ayant inclus 358 patients avec une MC, 15 % avaient une iléite, 42 % une colite, 37 % une iléo-colite et 6 % avaient une atteinte du tube digestif supérieur au diagnostic5. Par ailleurs, 74 % des 358 patients avaient un phénotype purement inflammatoire, sans complications à type de fistules/abcès ou de sténoses au moment du diagnostic5.
Deux études en population ont analysé l’évolution au cours du temps des complications de la MC (sténoses, fistules/abcès). Parmi 200 patients norvégiens avec une MC, alors que 61 % avaient un phénotype purement inflammatoire au diagnostic, ce taux n’était plus que de 47 %après 5 années de suivi4. Dans le comté d’Olmsted, ce chiffre était de 80 % au diagnostic et de 50 % après 20 ans d’évolution6.
Atteinte ano-périnéale
En Suède, chez 507 patients avec une MC diagnostiquée entre 1955 et 1989, des fistules ano-périnéales ou ano-rectales sont survenues chez 37 % des patients au cours du suivi7. Plus récemment, en reprenant les cas de MC diagnostiqués entre 1990 et 2001 dans cette même région de Stockholm, des fistules ano-rectales étaient rapportées chez 14 % des patients avant ou après le diagnostic de MC8. Au Canada, la prévalence des fistules ano-périnéales était de 10 à 14 %9. Dans le comté d’Olsmted, l’incidence cumulée des fistules ano-périnéales était de 26 % après 20 ans d’évolution de la MC10. Deux études en population ont analysé l’évolution de ces fistules. En Suède, après un suivi moyen de 9,4 ans, une fistule sur deux avait complètement cicatrisé, 9 % des patients avaient une fistule toujours active, et 40 % avaient dû recourir à une procto-colectomie11. Plus récemment, chez 33 patients avec une MC compliquée de fistules anales et suivis dans le comté d’Olmsted, un patient sur deux a eu une chirurgie mineure, un patient sur quatre a pu être traité médicalement et un patient sur quatre a dû recourir à une coloproctectomie10. À noter que ces 2 études ont été menées alors que les immunosuppresseurs et les biothérapies étaient peu utilisés dans le traitement de la MC.
Évolution de la maladie (Tableau 2)
Activité de la maladie et taux de rechutes
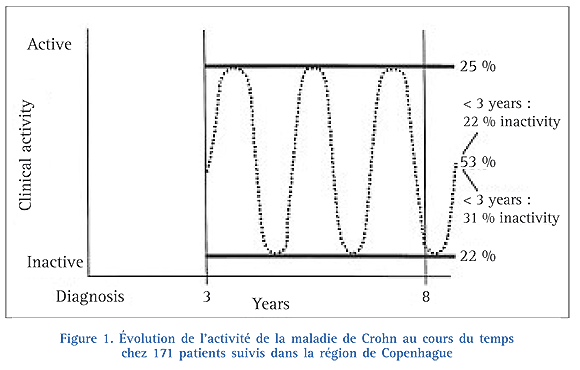
Parmi 103 patients avec une MC diagnostiquée entre 1940 et 1982 et suivis dans le comté d’Olsmted, 13 % avaient une MC active durant toute la période de suivi, 75 % avaient une alternance de poussées et de rémissions, et 10 % étaient en rémission clinique spontanée3. Grâce à un modèle de Markov utilisant les données provenant de cette même cohorte, les auteurs ont pu prédire l’évolution de la MC et démontrer qu’après le diagnostic, un patient passait 24 % de son temps en rémission clinique grâce à un traitement médical, 27 % de son temps avec une maladie peu active, 1 % du temps avec une forme sévère ayant bien répondu au traitement médical,4 %du temps avec une forme sévère dépendante d’un traitement médical, 1 % du temps était consacré aux interventions chirurgicales, et 41 % du temps en rémission clinique postchirurgie12. Deux études en population ont analysé l’activité de la maladie et le taux de rechutes au cours du temps. Chez 373 patients danois avec une MC diagnostiquée entre 1962 et 1987, la probabilité de ne pas présenter de poussée de la maladie était de 22 % 5 ans après le diagnostic pour chuter à 12 % après 10 ans d’évolution13. En considérant les 7 années suivant le diagnostic, 20 % des patients avaient une maladie active, 13 % d’entre eux n’avaient aucune poussée de la maladie, et 67 % des patients avaient une alternance de poussées entrecoupées de rémissions13 (Fig. 1). En Norvège, chez 177 patients avec une MC diagnostiquée entre 1990 et 1993 suivis sur une durée médiane de 124 mois, le taux cumulé de rechutes était de 53 % à un an et 90 % à 10 ans14. Dans une étude multicentrique européenne ayant inclus 358 patients avec une MC, seuls 27 % des patients n’avaient aucune poussée et n’avaient pas dû recourir à la chirurgie après un suivi médian de 123 mois5.
Globalement, il faut retenir que seuls 1 % des patients auront une maladie en permanence active, environ 10 % des patients seront en rémission prolongée spontanée, les autres patients ayant une évolution avec alternance de poussées et de rémissions.
Corticothérapie
Le traitement qui a été le mieux analysé dans les études en population sur la MC est la corticothérapie. Dans une étude danoise ayant inclus 196 patients avec une MC diagnostiquée entre 1979 et 1987, après un suivi médian de 3,4 ans, 56 % des patients avaient été exposés aux corticoïdes et 84 % d’entre eux avaient été traités pendant la première année suivant le diagnostic15. La durée médiane du traitement était de 84 jours (extrêmes : 5-229). Parmi les patients traités par corticoïdes, 48 % ont pu rentrer en rémission clinique, 32 %ont eu une réponse partielle, et 20 % étaient corticorésistants. À la fin du suivi, 44 % des patients avaient une réponse clinique soutenue, 36 % étaient corticodépendants et 20 % étaient réfractaires aux corticoïdes. Au total, 21 %des patients ont dû recourir à la chirurgie dont un quart des patients qui étaient corticodépendants et 59 % de ceux qui étaient corticorésistants15.
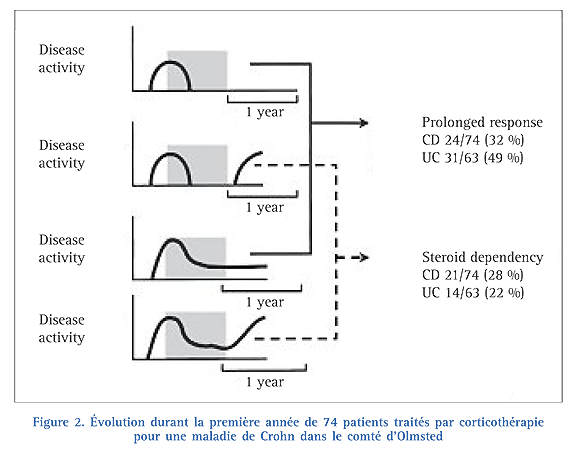
Dans le comté d’Olmsted, parmi 171 patients avec une MC, 43% ont reçu une corticothérapie dont 58 % ont eu une réponse complète, 26 % une réponse partielle, et 16 % étaient non répondeurs primaires après 30 jours de traitement16. À un an, 32 % avaient une réponse prolongée, 28 % étaient corticodépendants, et 38 % avaient dû recourir à la chirurgie16 (Fig. 2).
Hospitalisations
Au Danemark, pour les cas de MC diagnostiqués entre 1962 et 1987, 83 % des patients étaient hospitalisés au moins une fois durant la première année. Par la suite, 20 % des patients étaient hospitalisés chaque année13.
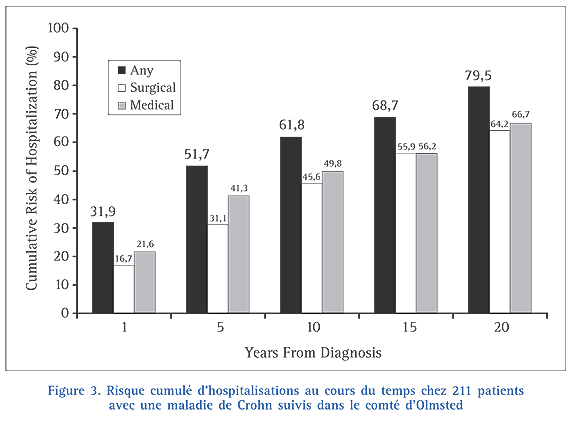
Au Canada, environ un quart des patients étaient hospitalisés au moins une fois entre 1994 et 200117. Seul1 % des patients étaient hospitalisés 3 fois dans la même année. Le taux d’hospitalisations a diminué de 29,2 pour 100 000 patients en 1994-1995 à 26,9 pour 100 000 patients pour l’année 2000-2001. La durée moyenne de séjour a également diminué de 10,3 jours en 1994-1995 à 9,1 jours en 2000-2001. Près d’une hospitalisation sur deux était en rapport avec une intervention chirurgicale17. Dans le comté d’Olmsted, (Fig. 3) parmi 211 patients avec une MC, 57 % étaient hospitalisés au moins une fois au cours du suivi1. L’incidence des hospitalisations était de 474 pour 1 000 patients-année, avec un taux maximal durant la première année suivant le diagnostic estimé à 474 pour 1 000 patients/année. La probabilité d’hospitalisations pour la MC était de 32 % à un an et de 62 % à 10 ans.
Chirurgie
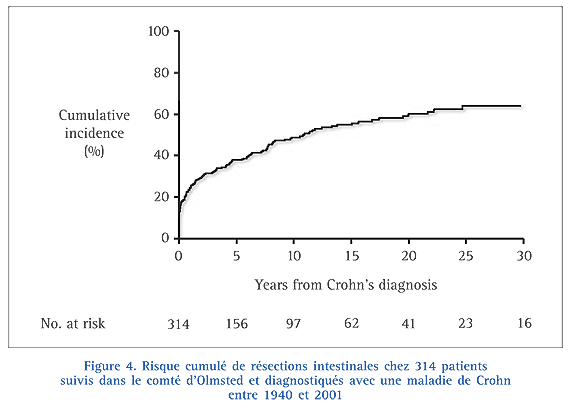
Dans le comté d’Olmsted, 41 % des patients avec une MC diagnostiquée entre 1935 et 1975 ont recourir à une intervention chirurgicale majeure après un suivi médian de 8,5 ans dont 67 %durant la première année18. Chez un patient sur 5, l’intervention était réalisée en urgence. Une récente mise à jour intégrant les cas de MC diagnostiqués jusqu’en 2001 a montré que l’incidence cumulée de première résection intestinale était de 24 % à un an et de 49 % à 10 ans (Fig. 4).
Le taux de recours à la chirurgie est donc resté stable depuis 1935.
Des données similaires ont été rapportées dans des études en population scandinaves. En Norvège, la probabilité de recourir à la chirurgie était de 14 % à un an et de 38 % à 10 ans. Au Danemark, ce chiffre était de 55 % à 10 ans. Dans une étude danoise plus récente reprenant les données de 209 patients avec une MC diagnostiquée entre 2003 et 2005, 12 % avaient une résection intestinale durant la première année20. Enfin, dans une étude de population multicentrique européenne, 40 % des patients ont eu une intervention chirurgicale durant les 10 premières années suivant le diagnostic.
Globalement, on peut retenir que la probabilité de recourir à la chirurgie est de 40-55 % à 10 ans. Le risque de recourir à une seconde intervention chirurgicale était de 16 % et 28 % respectivement un an et 10 ans après la première chirurgie1. Plus récemment, il a été montré que 9 % des patients devaient recourir à 2 interventions chirurgicales au minimum après 10 ans de suivi14. De façon similaire, au Danemark, 13 % des patients étaient opérés au minimum à 2 reprises.
Complications postopératoires
Dans une thèse de médecine ayant repris les cas de 856 MC diagnostiquées entre 1955 et 1974 dans la région de Stockholm, le taux de complications postopératoires majeures survenues dans les 30 jours ayant suivi la chirurgie était de 11 % ; 2 % des patients sont décédés de complications postopératoires21. Les mêmes chiffres ont été rapportés dans le comté d’Olmsted, avec 14 % de complications postopératoires majeures et 2 % de décès. Il n’existe pas de données récentes publiées à ce sujet dans les études en population18.
Récidive postopératoire
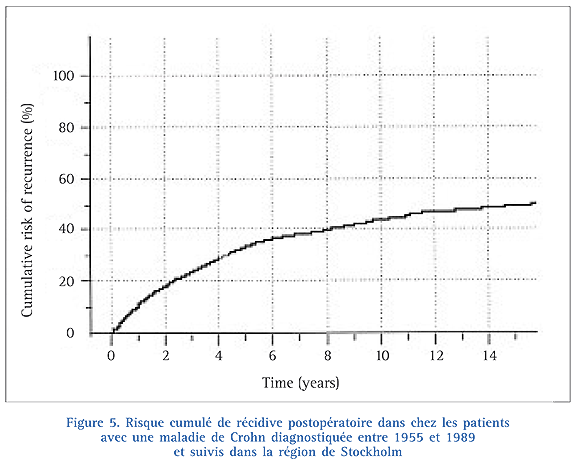
À Stockholm, la probabilité cumulée de récidive clinique postopératoire était de 30 % à 5 ans et de 50 % à 10 ans21. Ces résultats ont été récemment étendus à la période 1955-89, avec des chiffres stables de 33 % et 44 % à 5 et 10 ans (Fig. 5). Dans le comté d’Olmsted, le risque de récidive postopératoire était de 40 % à 5 ans, de 55 % à 10 ans et de 70 % après 20 ans ; la récidive était clinique, chirurgicale, endoscopique ou radiologique18. Dans cette étude, les auteurs ne distinguaient pas la récidive clinique de la récidive chirurgicale, endoscopique ou radiologique.
Facteurs prédictifs d’une évolution sévère (Tableau 3)
Critères cliniques
Dans le comté d’Olmsted, une localisation iléale et iléocolique au diagnostic était associée à un risque 5 à 7 fois plus élevé de développer des complications de la MC (sténoses, fistules, abcès) qu’une localisation purement colique6. En Norvège, un âge inférieur à 40 ans au diagnostic et la nécessité de recourir aux corticoïdes durant la première année étaient associés à un risque plus élevé de rechutes de la MC. Une localisation iléale terminale, la survenue de sténoses ou de fistules, et un âge inférieur à 40 ans au diagnostic étaient associés à un risque plus élevé de recourir à la chirurgie14. Dans une étude multicentrique européenne, une atteinte du tube digestif haut était associé à un risque plus élevé de poussées, contrairement à un âge au diagnostic supérieur à 40 ans ; une localisation colique de la MC était associée à un risque moindre de recourir à la chirurgie5. Enfin, récemment les critères que l’on appelle désormais « critères de Beaugerie » ont été répliqués dans l’étude de population du comté d’Olmsted.
Critères biologiques
Seule la protéine C-réactive (PCR) a été identifiée comme un facteur prédictif d’une évolution péjorative. Dans cette étude norvégienne, le risque de recours à la chirurgie à 5 ans était plus élevé chez les patients avec une localisation iléale de la MC et avec une PCR élevée, particulièrement chez ceux avec une PCR > 53 mg/L au diagnostic23.
Critères endoscopiques
En Norvège, 141 patients avec MC inclus dans l’étude IBSEN avaient une endoscopie au diagnostic puis environ un an plus tard24. Une cicatrisation muqueuse endoscopique était associée à un moindre recours à la corticothérapie après le diagnostic, mais les taux de rechutes, de chirurgie, et de complications de la MC étaient indépendants de l’activité endoscopique24. La valeur prédictive du score de Rutgeerts n’a pas analysée dans les études en population.
Complications extra-intestinales (Tableau 4)
Complications osseuses
Au Canada, l’incidence des fractures osseuses était de 86,2 pour 10 000 patients/année, soit une incidence annuelle de 0,9 % au cours de la MC25. Dans le comté d’Olmsted, l’incidence des fractures était de 155,7 pour 10 000 patients/année au cours de la MC26. Globalement, le risque de fracture osseuse est augmenté de 40 % chez les sujets avec une maladie inflammatoire chronique intestinale (MICI)2. Le risque d’ostéopénie et la densité minérale osseuse sont quant à eux comparables à la population générale. Les facteurs de risque de fractures osseuses étaient un âge élevé, le statut nutritionnel et à un moindre degré l’usage des corticoïdes2.
Thromboses
Globalement, le risque de thromboses artérielles au cours des MICI est similaire à celui observé dans la population générale27. Le risque de thromboses veineuses est, quant à lui, significativement augmenté au cours des MICI. Au Canada, les hospitalisations pour thrombose veineuse et/ou embolie pulmonaire étaient significativement plus élevées au cours des MICI que chez les sujets contrôlés, avec un risque globalement accru de 3 fois et aucune différence entre MC et rectocolite hémorragique27. Récemment, en utilisant la base de données « General Practice Research Database », Grainge et al. ont pu montrer que chez 13 756 patients avec une MICI le risque de thromboses veineuses était 3,5 fois plus élevé que dans la population générale. Ce risque était plus élevé lors des poussées de la maladie et, de manière plus surprenante, chez les patients avec une MICI suivis en ambulatoire par rapport à ceux hospitalisés28. Les facteurs de risque de thromboses veineuses au cours des MICI restant mal connus et semblent différer de ceux rapportés dans la population générale, avec notamment une absence de facteurs de risque génétiques2.
Maladies démyélinisantes
Deux études de population ont spécifiquement analysé l’association des maladies démyélinisantes aux MICI. Dans le comté d’Olmsted, 1 % des patients avec une MICI avaient également une sclérose en plaques, soit une prévalence 3,7 fois supérieure à celle attendue29. Dans le registre anglais General Practice Research Database (GPRD), l’incidence des atteintes démyélinisantes (sclérose en plaques, névrite optique, et autres types d’atteintes démyélinisantes) était significativement plus élevée au cours de la rectocolite hémorragique que chez les sujets contrôlés mais pas dans la MC ; en revanche, la prévalence de ces atteintes était plus élevée à la fois dans la MC (Odds Ratio (OR):1,5 ; IC à 95 % : 1,0-2,3) et la rectocolite hémorragique (OR :1,7 ; IC à 95 % : 1,3-2,4) que chez les contrôles.
Autres complications/ manifestations extra-intestinales
Les études en population ont confirmé les données provenant des centres experts concernant l’association de la cholangite sclérosante primitive, de la spondylarthrite ankylosante, de l’uvéite, du pyoderma gangrenosum, et de l’érythème noueux aux MICI2. Les études de population ont en revanche révélé que l’asthme, les atteintes bronchiques inflammatoires, le psoriasis, la péricardite, et la polyarthrite rhumatoïde étaient plus fréquents au cours de la MC2.
Néoplasies intestinales et extra-intestinales (Tableau 5)
Dysplasie colorectale
Deux études en population ont analysé la survenue des dysplasies colorectales au cours de la MC. Parmi 314 patients avec une MC diagnostiquée entre 1940 et 2001 et suivis dans le comté d’Olmsted, après un suivi médian de 10,8 ans, seul un cas de dysplasie de bas grade a été observé et 6 cas d’« adenomaassociated lesions or masses »31. L’incidence cumulée de la dysplasie colorectale était de 0,5 % à 5 ans31. Dans une étude multicentrique européenne, 2 cas de dysplasie colorectale ont été diagnostiqués parmi 365 patients avec MC après 10 ans de suivi, soit un taux de 0,5 %32.
Cancer colorectal et adénocarcinome du grêle
En 2006, Jess et al. ont rapporté un ratio standardisé d’incidence de 1,9 (IC à 95 % : 1,4-2,5) pour le cancer colorectal en incluant 6 études en population33. Concernant le risque de cancer du grêle, le ratio standardisé d’incidence était de 27,1 (IC à 95 % : 14,9-49,2)33. Dans une autre métaanalyse, lorsque seules les études en population étaient incluses dans l’analyse, le ratio standardisé d’incidence était de 1,4 (IC à 95 % : 0,9-2,1)34. Concernant le risque de cancer du grêle, le ratio standardisé d’incidence était de 21,1 (IC à 95 % : 10,2-43,8)34. Dans le comté d’Olmsted, le risque de cancer du grêle était encore plus élevé, avec un ratio standardisé d’incidence de 40,6 (IC à 95 % : 8,4-118)35. En Suède, parmi 21 788 patients hospitalisés avec une MC, le ratio standardisé d’incidence était de 13,8 (IC à 95 % : 10,4-18) pour le cancer du grêle et de 2,9 pour le cancer du côlon (IC à 95 % : 2,5-3,4)36.
Lymphome
Plusieurs études de population ont rapporté la fréquence du lymphome au cours des MICI, avec des résultats souvent discordants qui s’expliquent en partie par un effectif de taille souvent insuffisante. Dans une première métaanalyse, il existait une légère augmentation du risque de lymphome chez les patients atteints de MC, avec un ratio standardisé d’incidence de 1,5 (IC à 95 % : 1,1-2)34, alors qu’un risque similaire à celui de la population générale était rapporté dans une métaanalyse plus récente37.
Autres cancers extra-intestinaux
Le risque de cancers extra-intestinaux variait selon les études en population, avec des résultats souvent discordants qui s’expliquent une nouvelle fois en partie par un effectif de taille souvent insuffisante2. Une métaanalyse ayant inclus 8 études en population et 17 052 patients avec une MICI a montré qu’il existait un risque accru de cancers du tractus digestif haut (ratio standardisé d’incidence: 2,9 ; IC 95 %: 1,7-5), de cancers bronchiques (ratio standardisé d’incidence :1,8 ; 1,2-2,8), de cancers de la vessie (ratio standardisé d’incidence :2,0 ; 1,1-3,6), et de cancers cutanés (ratio standardisé d’incidence : 2,4 ; 1,4-3,9)37.
Mortalité (Tableau 5)
Une métaanalyse a montré une augmentation légère mais significative de la mortalité chez les patients avec une MC inclus dans les études en population, avec un ratio standardisé de mortalité de 1,39 (1,3-1,5)38. Cette surmortalité était principalement liée à une augmentation du risque de cancers bronchiques, de maladies gastro- intestinales, de maladies génitourinaires, et de maladie pulmonaire obstructive chronique38.
Impact des traitements sur l’histoire naturelle de la maladie de Crohn
L’impact des traitements que sont les thiopurines (azathioprine, 6-mercaptopurine) et les anti-Tumor Necrosis Factor (TNF) sur l’évolution de la MC reste mal connu. Récemment, une étude de population ayant repris les données de 341 patients avec une MC diagnostiquée dans la région de Cardiff entre 1986 et 2003 a montré que la probabilité de recourir à la chirurgie à 5 ans avait baissé de 59 % pour les patients diagnostiqués avec une MC entre 1986 et 1991 à 25 % pour ceux diagnostiqués entre 1998 et 200339. En analyse multivariée, un usage de l’azathioprine durant la première année suivant le diagnostic était un facteur de risque indépendant de moindre recours à la chirurgie39. Concernant les anti-TNF, peu de données sont disponibles sur le taux de chirurgie chez les patients avec MC inclus dans des études en population. Une seule étude scandinave a retrouvé un taux de chirurgie abdominal majeure égal à 17 %(33/191) chez des patients avec MC ayant reçu en moyenne 2,6 perfusions d’infliximab entre 1999 et 200140. La seule étude à avoir analysé à ce jour l’impact de l’azathioprine et des anti-TNF sur le risque de chirurgie dans la MC provient du CHU de Nancy41. Dans cette étude, qui est par définition une étude provenant d’un centre expert et pas une étude en population, 26 % des 296 patients diagnostiqués avec une MC entre 2000 et 2008 ont dû recourir à une intervention chirurgicale au cours du suivi dont la durée médiane était de 57 mois41. En analyse multivariée, une durée d’exposition aux anti-TNF inférieure à 16 mois (Hazard Ratio : 3,86 ; IC à 95 % : 1,77-8,45) et une durée de traitement par azathioprine inférieure à 1,5 mois (Hazard Ratio : 2,0 ; IC à 95 % : 1,2-3,34) étaient associées à un risque plus élevé de recours à la chirurgie41. De telles données ne sont pas encore disponibles dans les études en population. L’impact des thiopurines et des anti- TNF sur l’évolution de la MC fistulisante n’a jamais été analysé dans les études en population.
Conclusion
Ces données montrent que la MC est une maladie chronique, invalidante, et destructrice. Seuls 10 % des patients ont une rémission clinique prolongée en l’absence de traitement médical. Actuellement, encore un patient sur 2 doit recourir à une chirurgie abdominale majeure. Il n’existe toujours pas de données sur l’impact des biothérapies sur l’histoire naturelle de la MC. De même, les facteurs prédictifs d’une évolution péjorative restent mal connus. Une meilleure compréhension de l’histoire naturelle de cette maladie devrait permettre d’améliorer la prise en charge de ces patients en identifiant ceux qui pourraient bénéficier d’un traitement médical agressif (traitement par anti-TNF en association ou non à des immunosuppresseurs) et précoce (traitement débuté avant la survenue de complications de la MC que sont les sténoses, les fistules et les abcès).
Références
- Peyrin-Biroulet L, Loftus EV, Jr., Colombel JF, Sandborn WJ. The natural history of adult Crohn’s disease in population-based cohorts. Am J Gastroenterol 2010;105:289-97.
- Peyrin-Biroulet L, Loftus EV, Jr., Colombel JF, Sandborn WJ. Longterm complications, extraintestinal manifestations, and mortality in adult Crohn’s disease in population-based cohorts. Inflamm Bowel Dis 2010; 17:471-8.
- Gollop JH, Phillips SF, Melton LJ, 3rd, Zinsmeister AR. Epidemiologic aspects of Crohn’s disease: a population based study in Olmsted County, Minnesota, 1943-1982. Gut 1988;29:49-56.
- Henriksen M, Jahnsen J, Lygren I, Aadland E, Schulz T, Vatn MH, Moum B. Clinical course in Crohn’s disease: results of a five-year population- based follow-up study (the IBSEN study). Scand J Gastroenterol 2007;42:602-10.
- Wolters FL, Russel MG, Sijbrandij J, Ambergen T, Odes S, Riis L, Langholz E, Politi P, Qasim A, Koutroubakis I, Tsianos E, Vermeire S, Freitas J, van Zeijl G, Hoie O, Bernklev T, Beltrami M, Rodriguez D, Stockbrugger RW, Moum B. Phenotype at diagnosis predicts recurrence rates in Crohn’s disease. Gut 2006;55:1124-30.
- Thia KT, Sandborn WJ, Harmsen WS, Zinsmeister AR, Loftus EV, Jr. Risk factors associated with progression to intestinal complications of Crohn’s disease in a population-based cohort. Gastroenterology 2010;139:1147-55.
- Lapidus A, Bernell O, Hellers G, Lofberg R. Clinical course of colorectal Crohn’s disease: a 35-year follow-up study of 507 patients. Gastroenterology 1998;114:1151-60.
- Lapidus A. Crohn’s disease in Stockholm County during 1990-2001: an epidemiological update. World J Gastroenterol 2006;12:75-81.
- Tang LY, Rawsthorne P, Bernstein CN. Are perineal and luminal fistulas associated in Crohn’s disease? A population- based study. Clin Gastroenterol Hepatol 2006;4:1130-4.
- Schwartz DA, Loftus EV, Jr., Tremaine WJ, Panaccione R, Harmsen WS, Zinsmeister AR, Sandborn WJ. The natural history of fistulizing Crohn’s disease in Olmsted County, Minnesota. Gastroenterology 2002;122:875-80.
- Hellers G, Bergstrand O, Ewerth S, Holmstrom B. Occurrence and outcome after primary treatment of anal fistulae in Crohn’s disease. Gut 1980;21:525-7.
- Silverstein MD, Loftus EV, Sandborn WJ, Tremaine WJ, Feagan BG, Nietert PJ, Harmsen WS, Zinsmeister AR. Clinical course and costs of care for Crohn’s disease: Markov model analysis of a population-based cohort. Gastroenterology 1999;117:49-57.
- Munkholm P, Langholz E, Davidsen M, Binder V. Disease activity courses in a regional cohort of Crohn’s disease patients. Scand J Gastroenterol 1995;30:699-706.
- Solberg IC, Vatn MH, Hoie O, Stray N, Sauar J, Jahnsen J, Moum B, Lygren I. Clinical course in Crohn’s disease: results of a Norwegian populationbased ten-year follow-up study. Clin Gastroenterol Hepatol 2007;5:1430-8.
- Munkholm P, Langholz E, Davidsen M, Binder V. Frequency of glucocorticoid resistance and dependency in Crohn’s disease. Gut 1994;35:360-2.
- Faubion WA, Jr., Loftus EV, Jr., Harmsen WS, Zinsmeister AR, Sandborn WJ. The natural history of corticosteroid therapy for inflammatory bowel disease: a populationbased study. Gastroenterology 2001;121:255-60.
- Bernstein CN, Nabalamba A. Hospitalization, surgery, and readmission rates of IBD in Canada: a population- based study. AmJGastroenterol 2006;101:110-8.
- Agrez MV, Valente RM, Pierce W, Melton LJ, 3rd, van Heerden JA, Beart RW, Jr. Surgical history of Crohn’s disease in a well-defined population. Mayo Clin Proc 1982;57:747-52.
- Binder V, Hendriksen C, Kreiner S. Prognosis in Crohn’s disease–based on results from a regional patient group from the county of Copenhagen. Gut 1985;26:146-50.
- Vind I, Riis L, Jess T, Knudsen E, Pedersen N, Elkjaer M, Bak Andersen I, Wewer V, Norregaard P, Moesgaard F, Bendtsen F, Munkholm P. Increasing incidences of inflammatory bowel disease and decreasing surgery rates in Copenhagen City and County, 2003-2005: a population-based study from the Danish Crohn colitis database. Am J Gastroenterol 2006;101: 1274-82.
- Hellers G. Crohn’s disease in Stockholm county 1955-1974. A study of epidemiology, results of surgical treatment and long-term prognosis. Acta Chir Scand Suppl 1979;490:1-84.
- Bernell O, Lapidus A, Hellers G. Risk factors for surgery and postoperative recurrence in Crohn’s disease. Ann Surg 2000;231:38-45.
- Henriksen M, Jahnsen J, Lygren I, Stray N, Sauar J, Vatn MH, Moum B. C-reactive protein: a predictive factor and marker of inflammation in inflammatory bowel disease. Results from a prospective population-based study. Gut 2008;57:1518-23.
- Froslie KF, Jahnsen J, Moum BA, Vatn MH. Mucosal healing in inflammatory bowel disease: results from a Norwegian population-based cohort. Gastroenterology 2007;133:412-22.
- Bernstein CN, Blanchard JF, Leslie W, Wajda A, Yu BN. The incidence of fracture among patients with inflammatory bowel disease. A populationbased cohort study. Ann Intern Med 2000;133:795-9.
- Loftus EV, Jr., Crowson CS, Sandborn WJ, Tremaine WJ, O’Fallon WM, Melton LJ, 3rd. Long-term fracture risk in patients with Crohn’s disease: a population-based study in Olmsted County, Minnesota. Gastroenterology 2002;123:468-75.
- Bernstein CN, Wajda A, Blanchard JF. The incidence of arterial thromboembolic diseases in inflammatory bowel disease: a population-based study. Clin Gastroenterol Hepatol 2008;6:41-5.
- Grainge MJ, West J, Card TR. Venous thromboembolism during active disease and remission in inflammatory bowel disease: a cohort study. Lancet 2010;375:657-63.
- Kimura K, Hunter SF, Thollander MS, Loftus EV, Jr., Melton LJ, 3rd, O’Brien PC, Rodriguez M, Phillips SF. Concurrence of inflammatory bowel disease and multiple sclerosis. Mayo Clin Proc 2000;75:802-6.
- Gupta G, Gelfand JM, Lewis JD. Increased risk for demyelinating diseases in patients with inflammatory bowel disease. Gastroenterology 2005;129:819-26.
- Jess T, Loftus EV, Jr., Velayos FS, Harmsen WS, Zinsmeister AR, Smyrk TC, Tremaine WJ, Melton LJ, 3rd, Munkholm P, Sandborn WJ. Incidence and prognosis of colorectal dysplasia in inflammatory bowel disease: a population-based study from Olmsted County, Minnesota. Inflamm Bowel Dis 2006;12:669-76.
- Katsanos KH, Vermeire S, Christodoulou DK, Riis L, Wolters F, Odes S, Freitas J, Hoie O, Beltrami M, Fornaciari G, Clofent J, Bodini P, Vatn M, Nunes PB, Moum B, Munkholm P, Limonard C, Stockbrugger R, Rutgeerts P, Tsianos EV. Dysplasia and cancer in inflammatory bowel disease 10 years after diagnosis: results of a population-based European collaborative follow-up study. Digestion 2007; 75:113-21.
- Jess T, Gamborg M, Matzen P, Munkholm P, Sorensen TI. Increased risk of intestinal cancer in Crohn’s disease: a meta-analysis of population- based cohort studies. Am J Gastroenterol 2005;100:2724-9.
- von Roon AC, Reese G, Teare J, Constantinides V, Darzi AW, Tekkis PP. The risk of cancer in patients with Crohn’s disease. Dis Colon Rectum 2007;50:839-55.
- Jess T, Loftus EV, Jr., Velayos FS, Harmsen WS, Zinsmeister AR, Smyrk TC, Schleck CD, Tremaine WJ, Melton LJ, 3rd, Munkholm P, Sandborn WJ. Risk of intestinal cancer in inflammatory bowel disease: a population-based study from olmsted county, Minnesota. Gastroenterology 2006;130:1039-46.
- Hemminki K, Li X, Sundquist J, Sundquist K. Cancer risks in Crohn disease patients. Ann Oncol 2009;20:574-80.
- Pedersen N, Duricova D, Elkjaer M, Gamborg M, Munkholm P, Jess T. Risk of extra-intestinal cancer in inflammatory bowel disease: meta-analysis of population-based cohort studies. Am J Gastroenterol 2010;105:1480-7.
- Duricova D, Pedersen N, Elkjaer M, Gamborg M, Munkholm P, Jess T. Overall and cause-specific mortality in Crohn’s disease: a meta-analysis of population-based studies. Inflamm Bowel Dis 2010;16:347-53.
- Ramadas AV, Gunesh S, Thomas GA, Williams GT, Hawthorne AB. Natural history of Crohn’s disease in a population- based cohort from Cardiff (1986-2003): a study of changes in medical treatment and surgical resection rates. Gut 2010;59:1200-6.
- Ljung T, Karlen P, Schmidt D, Hellstrom PM, Lapidus A, Janczewska I, Sjoqvist U, Lofberg R. Infliximab in inflammatory bowel disease: clinical outcome in a population based cohort from Stockholm County. Gut 2004;53:849-53.
- Peyrin-Biroulet L, Oussalah A, Williet N, Pillot C, Bresler L, Bigard MA. Impact of azathioprine and tumour necrosis factor antagonists on the need for surgery in newly diagnosed Crohn’s disease. Gut 2011 (In Press).
Les 5 points forts
- À long terme, un patient sur deux aura une complication de la maladie de Crohn à type de sténose, fistule et/ou abcès.
- 1 % des patients aura une maladie en permanence active, 10%des patients seront en rémission prolongée spontanée (en l’absence de traitement médical d’entretien) et près de 90% des patients auront une évolution faite d’alternance de poussées et de rémission.
- Un patient sur deux sera hospitalisé pour une complication et un patient sur deux sera opéré pour sa maladie de Crohn après 10 ans d’évolution.
- Un âge inférieur à 40 ans au diagnostic, la nécessité de recourir à une corticothérapie pour traiter la première poussée, une atteinte ano-périnéale, et un taux élevé de protéine C-réactive au diagnostic sont des facteurs pronostiques d’une évolution péjorative.
- La mortalité est légèrement augmentée au cours de la maladie de Crohn.
FMC HGE : Organisme certifié Qualiopi pour la catégorie ACTIONS DE FORMATION
FMC HGE : Organisme certifié Qualiopi pour la catégorie ACTIONS DE FORMATION