Liens d’intérêt
Aucun lien d’intérêt n’a été déclaré par l’auteur
Mots-clés
Lithogénèse ; Acide ursodésoxycholique ; Syndrome LPAC
Introduction
La lithiase biliaire est devenue un problème majeur de santé publique, notamment dans les pays développés où elle affecte jusqu’à 20 % de la population générale. Elle est actuellement la pathologie gastro-intestinale la plus pourvoyeuse d’hospitalisations (4 % de la population occidentale).
Une nouvelle cause de lithiase biliaire, principalement intrahépatique a été révélée en 2006 : le syndrome LPAC. Depuis cette date, la compréhension de la physiopathologie de la lithiase biliaire a beaucoup progressé et fait intervenir maintenant des anomalies génétiques, environnementales, locales, hormonales même métaboliques.
Sa prise en charge médicale est devenue multidisciplinaire et fait appel aux dernières avancées radiologiques, endoscopiques et chirurgicales.
Pour bien comprendre et prendre en charge la lithiase biliaire, il est important de bien préciser certaines définitions.
Définitions
La lithiase biliaire : La lithiase biliaire correspond à la présence d’un ou plusieurs calculs dans les voies biliaires ; c’est-à-dire dans la vésicule biliaire (VB), dans la voie biliaire principale (VBP) et/ ou dans les voies biliaires intrahépatiques (VBIH). Qu’il y ait 1 seul calcul ou 1 000 calculs, nous parlons toujours de la « lithiase biliaire » au singulier.
Le calcul biliaire : Il correspond à l’élément solide et mobile présent de façon anormale dans les voies biliaires. Il peut être de nature, de taille, de localisation et de traduction clinique variable :
- Il peut mesurer de 1 mm à plus de 4 cm,
- Il est constitué principalement de cholestérol (dans 95 % des cas), de bilirubine (5 % des cas) ou d’un mélange des deux,
- Il peut être de localisation vésiculaire, canalaire, intra et/ ou extra-hépatique,
- Il peut être asymptomatique, symptomatique (colique hépatique) ou compliqué (cholécystite, pancréatite ou angiocholite).
La maladie lithiasique biliaire : Elle regroupe toutes les manifestations cliniques ou biologiques dont la cause est la présence d’une lithiase biliaire.
Pour parler de maladie lithiasique biliaire, il faut, soit que des symptômes ou complications lui soient rapportés ; soit que la localisation de ces calculs soit atypique et menaçante, notamment dans la VBP ou dans les VBIH.
La boue biliaire (ou « sludge ») : La boue biliaire n’est pas une lithiase. Elle n’est pas non plus une cause de calcul car elle survient presque physiologiquement dans toute situation de stase biliaire (nutrition parentérale). Elle contribue, en revanche, fortement à la formation de calculs.
Physiologie de la bile / lithogénèse
Physiologie de la bile
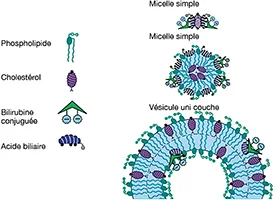
La bile est un mélange complexe de substances théoriquement non miscibles : de l’eau, des sels biliaires, de la bilirubine conjuguée et des lipides (cholestérol) (figures 1 et 2).

Figure 1

Figure 2
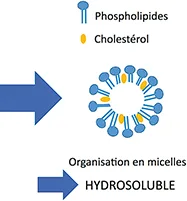
La principale difficulté pour la stabilité chimique de ce liquide est la solubilisation du cholestérol (qui est un lipide) dans le milieu aqueux de la bile. Cela est rendu possible grâce à la présence des phospholipides qui permettent la formation de micelles hydrosolubles contenant les molécules incompatibles entres elles (figure 2). Les acides biliaires y contribuent également mais à une moindre mesure.
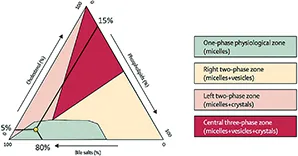
La stabilité de ce mélange est donc obtenue grâce à des concentrations précises de cholestérol, de sels biliaires et de phospholipides mais aussi à une mobilité constante de ce mélange (motricité de la vésicule et cycle entéro-hépatique) (figure 3).

Figure 3 : Diagramme ternaire de Small (Portincasa et al. Lancet 2006)
Physiopathologie de la lithiase
Lithiase cholestérolique
Dans certaines conditions, ces micelles de cholestérol peuvent fusionner entre elles et donner naissance à des vésicules à une couche puis des vésicules à multiples couches autour desquelles le cholestérol va cristalliser. Ce phénomène s’appelle la nucléation car c’est autour de ce petit noyau que va croître le calcul de cholestérol (figure 1).
La paroi de la vésicule biliaire interfère également avec ce mélange en déshydratant la bile par résorption d’eau et en sécrétant une mucine le long de ses parois qui favorisera la croissance du calcul.
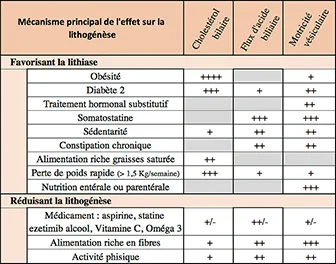
Les facteurs d’instabilité de ce mélange sont principalement la sursaturation de la bile en cholestérol (HDL notamment), une diminution de sécrétion des sels biliaires, l’appauvrissement de la bile en phospholipides et l’immobilité de la vésicule biliaire (tableau 1).

Tableau 1
Le lieu de formation de la lithiase biliaire cholestérolique est donc la vésicule biliaire, qui concentre tous les facteurs favorisants à la nucléation et à la croissance du ou des calculs.
La présence d’un calcul ailleurs dans les voies biliaires (en dehors du cas particulier du calcul brun) est donc le fruit d’une migration incomplète ou l’existence d’anomalies morphologiques des voies biliaires responsables d’une stase biliaire extra vésiculaire (maladie de Caroli principalement).
Autres calculs
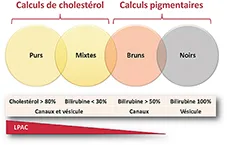
Il existe 2 autres types de calculs dont la physiopathologie diffère ; le calcul pigmentaire et le calcul brun (figure 4).

Figure 4
Le calcul pigmentaire (ou calcul noir) est lié à l’augmentation de la sécrétion de bilirubine non conjuguée observée dans toutes les formes d’hémolyse chronique.
Le calcul brun est constitué de bilirubine de calcium issue de l’action de déconjugaison de la bilirubine par les béta-glucuronidases bactériennes, observée principalement dans les lésions ou infections chroniques des voies biliaires ; ce pourquoi on les trouve rarement dans la vésicule biliaire.
Le syndrome LPAC
Il existe une entité particulière de la maladie lithiasique responsable d’une lithogénèse directement dans les VBIH saines : le syndrome LPAC (Low Phospholipid Associated Cholelitiasis).
Comme son nom l’indique, la cause en est un déficit de phospholipides dans la bile entrainant la nucléation et la croissance de calcul directement dans les voies biliaires saines, indépendamment du taux de cholestérol biliaire et de l’immobilité de la vésicule.
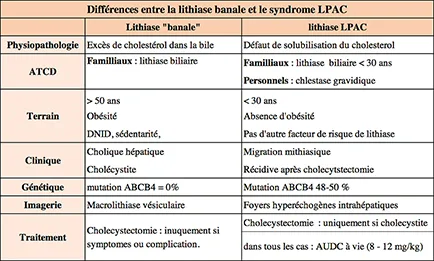
Ce qui distingue également le syndrome LPAC de la lithiase cholestérolique classique est le terrain : femme jeune (entre 15 et 30 ans pour la plupart), sans surpoids ni autre facteur favorisant et n’ayant pas de calcul dans la vésicule ou n’ayant plus de vésicule biliaire. Sa traduction clinique est faite de fréquents épisodes de douleur d’allure biliaire (tableau 4), parfois associés à un tableau biologique de migration lithiasique, voire même de pancréatite et qui récidivent après cholécystectomie (tableau 2).

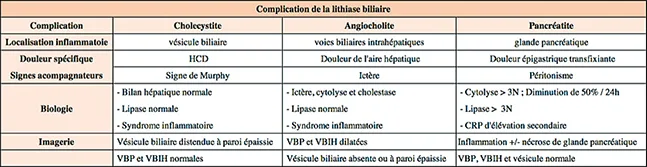
Tableau 2

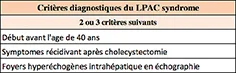
Tableau 3

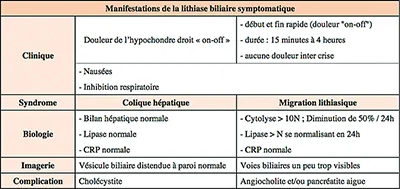
Tableau 4
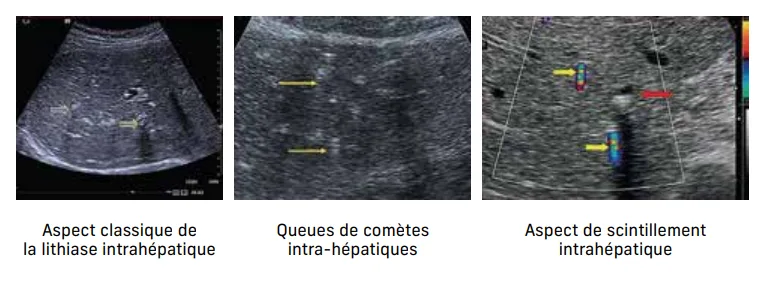
Le diagnostic du LPAC repose sur des critères cliniques et anamnestiques précis (tableau 3), mais surtout sur la mise en évidence d’images échographiques spécifiques intrahépatiques : queues comètes, écho de répétition… (figure 5).

Figure 5
Bien que des mutations du gène ABCB4 codant pour la protéine MDR3 (transporteur principal de la phospholipide dans la bile) soient identifiées depuis 2006, ces dernières ne participent pas au diagnostic car elles ne sont présentées que dans 50 % des cas.
Le diagnostic est donc rendu difficile par la faible diffusion des critères diagnostiques et par l’expérience particulière que doivent acquérir les radiologues pour l’identifier… ainsi, l’errance diagnostique peut dépasser 8 ans (figure 5).
Le syndrome LPAC est pourtant beaucoup plus fréquent qu’on ne le pense : il ne représente que 1 % de tous les cas de lithiase biliaire, mais si on s’intéresse aux patients de moins de 30 ans, sans surpoids et ayant présenté des manifestations biliaires de tous types : on arrive à une prévalence de 50 % !
Épidémiologie
Sur notre planète, il existe une grande variabilité ethnique et géographique de la lithiase biliaire liée notamment à la prévalence élevée de certaines parasitoses (Asie) ou maladies hémolytiques (Afrique) ou de variantes génétiques (Amérindiens) dans certaines régions du globe.
Dans les pays occidentaux, les facteurs de risque de survenue la lithiase cholestérolique sont connus de longue date : sexe féminin (x 3), obésité (x 2) et âge avancé. On observe en effet une prévalence de 20 % pour la population française de plus de 65 ans.
Certaines situations physiologiques ou pathologiques sont aussi considérées comme favorisant la lithogénèse : la grossesse, la perte de poids rapide et la nutrition entérale ou parentérale prolongée.
D’autres facteurs favorisants, moins connus, ont récemment été identifiés : l’insulinorésistance et le diabète de type 2, la diminution du HDL cholestérol, la carence en vitamine C, le traitement au long cours par somatostatine, l’alimentation occidentale de type « fastfood », la sédentarité, la constipation chronique et certaines formes de l’apoliproprotéines E.
Le rôle protecteur des statines et de l’alcool est évoqué mais de façon discutable.
Tous ces facteurs de risques associent une ou plusieurs actions positives ou négatives sur la saturation de la bile en cholestérol (comme, par exemple, les œstrogènes et la progestérone), sur le cycle entéro-hépatique des acides biliaires ou sur la mobilité de la vésicule biliaire (tableau 1).

Tableau 5
Manifestations cliniques
Définitions et incidences
La lithiase biliaire peut se révéler dans 3 situations cliniques différentes : la lithiase asymptomatique de découverte fortuite, la lithiase symptomatique douloureuse ou bien encore la lithiase compliquée nécessitant une hospitalisation.
La lithiase est le plus souvent asymptomatique (80 % des cas), ce qui ne l’empêche pas d’être associée à des symptômes digestifs qui ne lui sont pas rapportables : dyspepsie, RGO, ballonnement et flatulence… Ces derniers sont souvent à l’origine de la prescription de l’examen morphologique ayant mis en évidence la lithiase mais leur prévalence y est identique à celle observée dans la population générale ; ces symptômes ne sont donc pas spécifiques.
La lithiase devient symptomatique lorsqu’elle entraîne des manifestations cliniques assez stéréotypées mais qui ne mettent pas en jeu le pronostic vital : il s’agit de la colique hépatique et du syndrome de migration lithiasique.
La lithiase peut également être responsable d’une complication mettant en jeu le pronostic vital et obliger à un acte invasif en urgence : il s’agit de la cholécystite, de l’angiocholite et de la pancréatite.
Le risque qu’une lithiase asymptomatique devienne symptomatique est de 2 à 4 % par an tout en restant limité à 20 % de la population lithiasique au bout de 20 ans.
Le risque que cette même lithiase asymptomatique entraîne directement une complication sans être précédée de symptômes n’est que de 0,1 à 0,3 % par an.
Le risque de survenue de cette même complication est donc bien plus important lorsque cette lithiase est déjà symptomatique ; ce risque est multiplié par 10 pour atteindre 3 à 4 % par an.
À l’inverse, 80 % des patients hospitalisés pour complication biliaire avaient déjà présenté des symptômes biliaires.
Lithiase symptomatique
La colique hépatique et la migration sont les principales manifestions cliniques de la lithiase biliaire. Elles sont cliniquement proches et ne se différencient que par la normalité ou la modification du bilan biologique hépatique.
La colique hépatique : elle est la conséquence d’une mise sous tension de la vésicule biliaire suite à l’obstruction temporaire et suraiguë du canal cystique par un calcul ou de la boue biliaire. Elle se caractérise par une douleur très facilement identifiable : crise de douleur biliaire (cf. tableau 4) très intense, située à l’hypochondre droit ou l’épigastre, d’une durée allant de 10 minutes à 3 heures, marquée par un début et une fin brutale (« douleur ON/OFF »). Cette douleur est parfois associée à une nausée, une inhibition transitoire de la respiration profonde et une irradiation scapulaire.
La crise se répète dans 50 % des cas avec un rythme irrégulier, plutôt en post prandial tardif, mais laisse habituellement un intervalle libre de symptôme entre chaque crise.
Dans le cas de la colique hépatique, le calcul restant bloqué dans la vésicule, celui-ci n’entraîne pas d’obstruction de la VBP et n’est donc pas associé à une modification du bilan biologique hépatique ce qui caractérise plutôt le tableau de migration lithiasique.
Migration lithiasique : il s’agit du passage transitoire d’un calcul, habituellement de petite taille, dans la VBP, le plus souvent à l’occasion d’une contraction de la vésicule biliaire. Ce calcul se retrouve entraîné jusqu’à la papille où il reste coincé obstruant ainsi le flux de bile (800 ml/j). Il s’en suit alors une augmentation rapide de la pression dans l’arbre biliaire entraînant d’une part une douleur de colique hépatique mais également une forte cytolyse. Au bout de quelques minutes à quelques heures, la pression biliaire devient suffisante pour expulser le calcul. La pression se normalise ainsi brutalement, la douleur disparaît soudainement et les transaminases diminuent au rythme de leur ½ vie plasmatique soit -50 % en 24 heures (tableau 4).
Complications de la lithiase biliaire
Les principales complications de la lithiase biliaire sont la cholécystite, l’angiocholite et la pancréatite.
La cholécystite est la plus fréquente des complications biliaires et survient chez 10 % des patients ayant présenté au moins 1 colique hépatique. Elle correspond à une inflammation suraiguë de la vésicule biliaire et fait suite à une obstruction prolongée (plus de 5 heures) du canal cystique. Cette obstruction devient alors permanente du fait du simple œdème inflammatoire de celui-ci.
Le principal symptôme, outre la douleur biliaire devenue permanente, est le signe de MURPHY qui est une défense localisée à la région vésiculaire responsable d’une inhibition respiratoire brutale à la palpation de l’hypochondre droit (avec la main ou la sonde d’échographie).
On retrouve également les nausées, les vomissements et une fièvre inconstante.
La pancréatite aiguë biliaire se distingue des autres causes de pancréatite par le terrain de survenue et par l’existence d’une cytolyse initiale > 3N se normalisant ensuite rapidement, qui témoigne de l’obstruction temporaire du canal biliaire. Les lésions sont plus souvent caudales et l’évolution vers une forme grave est plus fréquente (la cytolyse initiale fait partie des critères de gravité de RANSON).
Cette cytolyse transitoire peut d’ailleurs manquer lors de la prise en charge tardive de la pancréatite.
L’angiocholite est l’infection des voies biliaires intrahépatiques en amont d’un obstacle. Elle peut s’associer à la pancréatite, ce qui en fait un critère supplémentaire de gravité de mortalité. Elle se traduit par un ictère fébrile persistant, associé à une cholestase, une cytolyse et par une dilatation de la voie biliaire principale en imagerie (tableau 2).
Diagnostic paraclinique
La radiologie offre 3 techniques d’imageries différentes qui peuvent diagnostiquer la lithiase biliaire et ses complications.
Le diagnostic de lithiase vésiculaire repose avant tout sur l’échographie transpariétale. La lithiase y apparaît comme des foyers hyperéchogènes et mobiles dans le fond de la vésicule biliaire associés à des cônes d’ombre hypo échogènes. Cet examen peut également mettre en évidence un épaississement de la paroi vésiculaire en cas de cholécystite ou une dilatation de la VBP en cas de migration dans la VBP.
Sa sensibilité est de 94 % et sa spécificité quasi parfaite.
Elle demeure cependant dépendante de l’expérience de l’opérateur (notamment dans le LPAC) et de ses conditions de réalisation (absence de jeûne ou présences de gaz digestifs).
Lorsque la présence d’une lithiase reste fortement suspectée malgré une vésicule paraissant alithiasique en échographie standard, l’écho endoscopie devient alors le 2e examen de référence car plus sensible (98 %), notamment pour les petits calculs vésiculaires mais surtout pour les localisations atypiques (VBP ou VBIH).
Dans le cadre d’un LPAC syndrome l’aspect échographique des microcristaux de cholestérol ont un aspect très différent (figure 5). L’échographie transpariétale et l’écho-endoscopie nécessitent à la fois une expertise de l’opérateur et un ciblage de l’examen sur cette hypothèse diagnostique ; sans quoi, sa sensibilité devient minime.
L’IRM, et notamment la bili IRM, est également un examen dont la performance s’approche de celle de l’écho-endoscopie pour ce qui est de ses localisations cholédociennes et vésiculaires, notamment lorsque la VBP est dilatée. La bili IRM a donc sa place après l’échographie initiale si une écho-endoscopie n’est pas réalisable dans l’immédiat.
Dans le cadre de la lithiase intrahépatique, notamment dans le syndrome LPAC, la bili IRM est très peu performante en dehors des cas de macro- calculs qui ne représentent que 10 % des cas. Le génotypage du gène MDR3 n’étant présent que de 50 % des cas, celui-ci n’est pas nécessaire pour poser le diagnostic.
Cependant, sa réalisation est importante car elle permet d’éliminer les rares diagnostics différentiels du syndrome LPAC que sont les anomalies macroscopiques du calibre des voies biliaires (CSP et maladie de Caroli) qui sont également pourvoyeuses de lithiases biliaires intrahépatiques.
Le scanner abdominal a une très mauvaise sensibilité pour le diagnostic de lithiase biliaire. Son seul intérêt réside dans l’évaluation de la gravité de la pancréatite biliaire (à la 72e heure).
Traitement
Bien qu’un traitement quotidien et prolongé par AUDC soit connu pour limiter la lithogénèse cholestérolique, et même parfois de faire disparaître les calculs déjà formés, son indication en traitement préventif ou curatif n’est pas recommandée, hormis dans quelques rares situations.
Le traitement de la lithiase biliaire est principalement chirurgical et/ ou endoscopique.
Prévention primaire de la lithiase biliaire
Parmi les nombreuses situations médicales favorisant la formation de lithiase biliaire, seules 2 sont reconnues comme pouvant justifier préventif d’un traitement pharmacologie (avec un niveau de preuve très faible) : l’amaigrissement rapide après chirurgie bariatrique (500 mg par jour d’AUDC jusqu’à stabilisation du poids) et le traitement au long cours par les analogues de la somatostatine.
Dans les autres situations tels que l’obésité, le diabète de type 2, le traitement hormonal substitutif de la ménopause, la nutrition parentérale, aucun traitement pharmacologique n’est à proposer.
Lorsqu’une lithiase biliaire est découverte de façon fortuite dans la vésicule biliaire, aucun geste chirurgical ou médical n’est indiqué pour la faire disparaître pour prévenir d’une quelconque manifestation clinique ou complication. Il en va de même lorsqu’une chirurgie limitant l’accès endoscopique à la VBP est réalisée ; le traitement chirurgical d’une éventuelle cholécystite secondaire reste aisé et ne justifie pas le sur-risque d’une cholécystectomie systématique préventive associée au geste de dérivation digestive.
Prévention de la complication de la lithiase biliaire
Lorsqu’une lithiase biliaire devient symptomatique ou se complique, une cholécystectomie est alors clairement indiquée afin de limiter le risque de récidive.
Lorsqu’il existe un calcul de la VBP principale, une extraction de celui-ci est nécessaire, soit par voie endoscopique (avant ou après le geste chirurgical), soit chirurgicalement par cholédocotomie pendant la cholécystectomie.
Bien qu’après l’extraction d’un calcul de la VBP, une récidive soit observée dans 5 à 20 % des cas, aucun traitement pharmacologique n’est indiqué, car ces récidives restent le plus souvent accessibles à une extraction endoscopique. De plus aucune étude, ou essai contrôlé, n’a pu montrer une efficacité de l’AUDC en termes de prévention de la récidive.
En revanche, lorsque la lithiase n’est pas vésiculaire mais intrahépatique ou cholédocienne, le risque de complication est majeur et une prise en charge thérapeutique doit être envisagée.
Lorsque le calcul intrahépatique est unique, une extraction endoscopique ou une hépatectomie doit être discutée en fonction de la localisation de ce dernier.
Lorsque la lithiase intra-hépatique est faite de nombreux calculs, comme dans le LPAC syndrome mais également dans la maladie de Caroli, un traitement médical par AUDC est nécessaire. La dose est alors de 8 à 12 mg/kg/j au long cours.
Bibliographie
- Lammert F, Acalovschi M, Ercolani G, et EASL Clinical Practice Guidelines on the prevention, diagnosis and treatment of gallstones. European Association for the Study of the Liver (EASL) ; J Hepatol. 2016 vol. 65 : 146-181
- Pariente A, Erlinger S, Lithiase biliaire et obésité : épidémiologie, physiopathologie, manifestations clinqiues et prévention. Hépato Gastro ; 24 : 18-25.
- Dong C, Condat B, Picon-Coste M, et al. Low-phospholipid-associated cholelithiasis syndrome: Prevalence, clinical features, and J Hepatol 2021 vol3 100201.
- Condat B, Zanditenas D, Barbu V, et al. Prevalence of low phospholipid-associated cholelithiasis in young female Dig Liver Dis. 2013 Nov;45(11):915-9.
- Recommandations de pratique cliniques de la Prise en charge de la lithiase biliaire (2010).
- Bartoli E, Capon Du cristal au calcul biliaire. Act.Med.Int. Gastroenterologie (16) 2002 ; 38-42.
Abréviations
VB : Vésicule biliaire
VBP : Voie biliaire principale
VBIH : Voies biliaires intrahépatiques
AUDC : Acide Urso Désoxy Cholique
LPAC: Low Phospholipid Associated Cholelithiasis
IRM : Imagerie par résonance magnétique