Résection des adénocarcinomes pancréatiques : les limites du raisonnable
Objectifs pédagogiques
- Quel bilan morphologique préopératoire ?
- Connaître les critères préopératoires théoriques d’inextirpabilité et leurs limites
- Comment les interpréter après un traitement néoadjuvant
- Connaître les différentes techniques opératoires et l’incidence du bilan préthérapeutique dans le choix
Introduction
Le diagnostic de l’adénocarcinome céphalique repose sur un faisceau d’arguments cliniques, morphologiques et biologiques ; lorsque ces arguments convergent, la preuve histologique avant la résection pancréatique n’est pas exigée [1-4]. La biopsie par voie échoendoscopique est utile en cas de doute diagnostique car elle peut permettre d’éviter une laparotomie et a fortiori une résection, inutiles comme par exemple dans les pancréatites « auto-immunes » ou chroniques [4]. En pratique, les contre-indications formelles à un geste d’exérèse à visée curative admises par tous sont :
- la présence d’une carcinose péritonéale ou de métastases hépatiques ;
- l’envahissement d’une ou plusieurs adénopathies lombo-aortiques ;
- un envahissement du tronc coeliaque, de l’artère hépatique ou de l’artère mésentérique supérieure ;
- une thrombose de l’axe veineux mésentérico-portal associée à un cavernome portal. En revanche, lorsque l’axe veineux est perméable, l’envahissement veineux n’est qu’une contre-indication relative à une exérèse « d’emblée », sous réserve de critères précis permettant d’espérer une résection curative de type R0 [1-4].
Nous ne discuterons pas ici la valeur « diagnostique » des examens morphologiques, mais leur contribution à la décision de résection (« résécabilité ») chez un malade opérable (ie en l’absence de contre-indication d’ordre anesthésique).
Un bilan morphologique préopératoire de qualité doit limiter le nombre des laparotomies exploratrices et le nombre des interventions palliatives ; cependant, il doit avoir une très grande spécificité concernant l’envahissement vasculaire (parfois au prix d’une perte relative de sensibilité) pour ne pas classer comme non résécable un patient qui pourrait bénéficier d’une résection, ce qui aboutirait à une perte de chance.
Quel bilan morphologique ?
La tomodensitométrie (TDM) en mode spiralé multicoupe est l’examen de référenc
e L’avènement de la TDM en mode spiralé (ou hélicoïdal) a rendu caduques les études comparant les examens morphologiques qui faisaient référence à la TDM en mode incrémental (acquisition tranche par tranche) [5, 6]. Deux revues systématiques de la littérature publiées en 2005 et 2006 ont montré que la TDM spiralée (acquisition en mode hélicoïdal), en coupes fines (2 ou3mm), avec injection vasculaire et acquisition à la phase artérielle puis portale, était l’examen le plus performant pour apprécier la résécabilité des adénocarcinomes pancréatiques [7, 8]. La qualité de l’examen a une grande importance. Après l’apparition, en 1992, du scanner à acquisition spiralée, la révolution technologique que constitue la multiplication des détecteurs (scanner multibarrette ou multidétecteur ou matriciel ; mode multicoupe) a ouvert de nouvelles possibilités de caractérisation et d’étude des rapports anatomiques vasculaires par la vitesse d’acquisition des images et la finesse des reconstructions. La résolution spatiale est excellente. L’acquisition volumique permet une représentation dans les différents plans de l’espace.
La TDM en mode hélicoïdal s’avère surtout efficace pour affirmer la « non résécabilité vasculaire » du fait de sa grande spécificité. Les performances de la TDM en mode hélicoïdal pour le diagnostic d’envahissement vasculaire sont bien documentées et concordantes ; elles montrent :
- une spécificité de 89 à 100 % ;
- une sensibilité de 80 à 91 % ;
- une précision globale de 89 à 93 % et,
- des performances meilleures pour l’envahissement artériel que pour l’envahissement veineux [5, 6].
Les travaux qui ont évalué les performances des scanners multicoupes de première génération (4 coupes par rotation) ou de dernière génération (16 coupes et au-delà) montrent :
- une spécificité de 82 à 100 % ;
- une sensibilité de 83 à 100 % et,
- une valeur prédictive négative d’envahissement vasculaire de 99 à 100 % [5, 6].
L’utilisation de reconstructions multiplanaires coronales et sagittales améliore la précision globale de la TDM multicoupe dans l’évaluation de l’extension vasculaire ; les coupes axiales et les reconstructions volumiques multiplanaires (MPVR) rendent plus facilement visibles les « encoches latérales » et les sténoses modérées de l’axe veineux mésentérico-portal [6-8]. Lorsqu’il existe un simple contact avec l’axe veineux, la TDM ne peut affirmer l’envahissement histologique mais, comme nous le verrons plus loin, il ne s’agit pas d’une contreindication opératoire. Enfin, étant donné la variabilité interobservateur, une relecture de l’examen TDM dans un centre expert est souhaitable, et si la TDM ne répond pas aux exigences d’un examen pancréatique, l’examen doit être renouvelé [5].
En pratique, la TDM en mode hélicoïdal multicoupe est l’examen de référence pour le diagnostic d’envahissement vasculaire [6]. Dans ces conditions, la probabilité pour que l’exploration peropératoire modifie l’indication de résection reste alors de l’ordre de 10 à 15 % ; il s’agit le plus souvent de petites métastases hépatiques, et plus rarement d’une carcinose péritonéale ou d’un envahissement ganglionnaire aorticocave.
Autres examens
L’échographie, qui est réalisée le plus souvent en première intention, peut dépister d’emblée des métastases hépatiques ; cependant, sauf « expérience particulière », elle n’apporte rien au bilan morphologique de résécabilité [5].
Pour le diagnostic de l’envahissement vasculaire, il n’est pas démontré que la précision de l’échoendoscopie soit supérieure à celle de la TDM spiralée ; ses performances brutes sont supérieures à celles de la TDM pour le diagnostic de l’envahissement ganglionnaire, mais l’impact de cette différence est mal chiffré [7]. La sensibilité globale de l’échoendoscopie pour le diagnostic d’envahissement vasculaire est de l’ordre de 70 % [9, 10] ; aujourd’hui, l’échoendoscopie n’est plus considérée comme l’examen le plus performant pour le bilan d’extension vasculaire d’un adénocarcinome du pancréas. Ainsi, en présence d’une tumeur clairement résécable sur les données d’une TDM spiralée de qualité, l’intérêt de l’échoendoscopie systématique n’est pas démontré sauf pour le diagnostic des petites tumeurs car la sensibilité de l’échoendoscopie (> 95 %) est alors nettement supérieure à celle de la TDM spiralée (80 %) [7, 8] qui méconnaît 20 à 30 % des cancers du pancréas de diamètre inférieur ou égal à 20 mm ; la sensibilité de l’échoendoscopie est indépendante de la taille de la tumeur. En pratique, l’échoendoscopie doit être réalisée :
- en cas de tumeur = 20 mm ;
- en cas de doute diagnostique pour permettre la biopsie de la tumeur ;
- dans les cas où une adénopathie distale, dont l’envahissement peut modifier la stratégie thérapeutique, peut être biopsiée [9, 10].
L’IRM a l’avantage de permettre une étude parenchymateuse, vasculaire et canalaire au cours du même examen, mais sa résolution spatiale reste inférieure à celle de la TDM spiralée [5-7]. Toutes les études qui avaient suggéré une supériorité de l’IRM sur la TDM pour le bilan d’extension local comportaient des biais importants (TDM non optimale) [5]. L’IRM est performante dans la recherche et surtout la caractérisation des métastases hépatiques ; elle est indiquée lorsqu’il existe un doute sur la nature d’une ou de plusieurs lésions hépatiques ; d’ailleurs, il est possible que l’utilisation de l’IRM avec séquences de « diffusion » et injection de nouveaux produits de contraste puisse augmenter le nombre des métastases hépatiques découvertes avant l’intervention ; ces techniques d’imagerie sont en cours d’évaluation [11].
Le PET-scan n’est pas utile au bilan de résécabilité. Il reste peu utilisé pour la détection de métastases à distance malgré une sensibilité comprise entre 61 et 100%, et une spécificité comprise entre 67 et 100%; il pourrait être utile à l’évaluation de la réponse après traitement néoadjuvant, lorsqu’une résection « secondaire » est envisagée (cf. infra) [5, 12].
L’artériographie coelio-mésentérique n’est pas utile au bilan de résécabilité. Elle a été quasiment abandonnée en raison des performances de la TDM hélicoïdale multicoupe qui permet, grâce à la qualité de ses reconstructions multiplanaires, de reconnaître les variations anatomiques de la distribution artérielle et les sténoses du tronc coeliaque par un ligament arqué ou, plus rarement, par un athérome qui peuvent modifier la stratégie préopératoire (stenting) ou peropératoire (section d’un ligament arqué) avant duodénopancréatectomie céphalique. L’artériographie peut avoir encore une place pour l’exploration hémodynamique des sténoses néoplasiques du tronc coeliaque en cas d’adénocarcinome du pancréas gauche, lorsqu’une résection vasculaire emportant le tronc coeliaque est programmée. Il s’agit d’une indication exceptionnelle, mais la résection du tronc coeliaque implique une revascularisation hépatique qui peut être assurée naturellement à contre-courant, par l’artère gastroduodénale (inversion du flux de l’artère gastroduodénale), ce qui témoigne de la collatéralité entre les territoires coeliaque et mésentérique supérieur.
L’exploration par laparoscopie n’a pas d’intérêt démontré pour la mise en évidence d’une extension locorégionale, vasculaire ou ganglionnaire. En revanche, la contribution de l’exploration laparoscopique au bilan de résécabilité est différente dans les adénocarcinomes du pancréas céphaliques et ceux du corps et de la queue du pancréas.
L’exploration par laparoscopie a été évaluée directement ou plus souvent indirectement dans les cancers céphaliques, pour le diagnostic de métastases hépatiques ou péritonéales non visibles en imagerie [13, 14]. La probabilité pour que l’exploration peropératoire contre-indique la résection est inférieure à 15 % lorsqu’un adénocarcinome céphalique est jugé clairement résécable sur l’imagerie, et il existe des faux négatifs (métastases non vues en laparoscopie et diagnostiquées lors de la laparotomie). Elle pourrait être indiquée lorsqu’il existe un doute sur l’extension locorégionale car la probabilité pour que l’exploration peropératoire contre-indique la résection est alors de 25 % [13], et chez les patients qui ont un risque élevé de métastases (taux de CA 19-9 sérique > 100 UI /mL ou 150 UI/mL en l’absence de cholestase, tumeur de diamètre > 3 cm de diamètre) car, en cas de maladie métastatique, un geste palliatif endoscopique est préférable à un geste chirurgical [1-3].
L’exploration par laparoscopie n’est donc pas recommandée en cas de localisation céphalique. En revanche, dans les adénocarcinomes du pancréas gauche, l’exploration systématique par laparoscopie est recommandée [2] : en effet, la probabilité pour que l’exploration peropératoire contre-indique la résection est de l’ordre de 30 %. La cause la plus fréquente de non résécabilité est la présence demétastases hépatiques ou péritonéales non vues en imagerie.
Avant toute résection, l’exploration par laparotomie intéresse le foie, le péritoine et les axes vasculaires. L’exploration ganglionnaire rétropéritonéale nécessite un décollement duodénopancréatique. L’existence de métastases ganglionnaires inter-aortico-caves constitue une contre-indication à la résection [1-3, 14], mais l’intérêt d’un curage « premier » ou même d’un « picking » ganglionnaire systématique n’a pas été évalué de façon prospective. En revanche, toute adénopathie macroscopiquement suspecte dans ce territoire doit être biopsiée, analysée en histologie extemporanée, et doit faire contre-indiquer l’exérèse si elle s’avère métastatique : en effet, dans ces cas, les médianes de survie après résection ne dépassent pas un an.

Qu’est-ce qu’un adénocarcinome pancréatique clairement résécable ?
Objectifs pédagogiques
- Connaître les critères préopératoires théoriques d’inextirpabilité ;
- Comment les interpréter après un traitement néoadjuvant.
En l’absence de métastases (viscérales ou ganglionnaires distales) et de carcinose péritonéale, l’irrésécabilité des adénocarcinomes pancréatiques est essentiellement liée à l’envahissement vasculaire ; nous verrons qu’il est corrélé à l’envahissement de la « marge rétropéritonéale ». Qu’il s’agisse de localisations céphaliques ou corporéocaudales, les signes formels d’envahissement vasculaire par un adénocarcinome du pancréas en TDM sont :
- l’occlusion ou la thrombose ;
- une diminution de calibre du vaisseau (sténose) ;
- l’englobement tissulaire circonférentiel (sur 360°) du vaisseau, même en l’absence de diminution de calibre.
Les deux premiers signes sont observés essentiellement en cas d’envahissement veineux et le troisième dans les envahissements artériels. Ces signes s’accompagnent classiquement d’une contiguïté entre la tumeur pancréatique et les anomalies vasculaires.
L’espace graisseux périartériel (artère mésentérique supérieure, tronc coeliaque, artère hépatique commune) et l’axe veineux mésentérico-portal sont les deux éléments anatomiques qui doivent faire l’objet d’une étude approfondie pour évaluer la résécabilité.
Disparition de l’espace graisseux périartériel
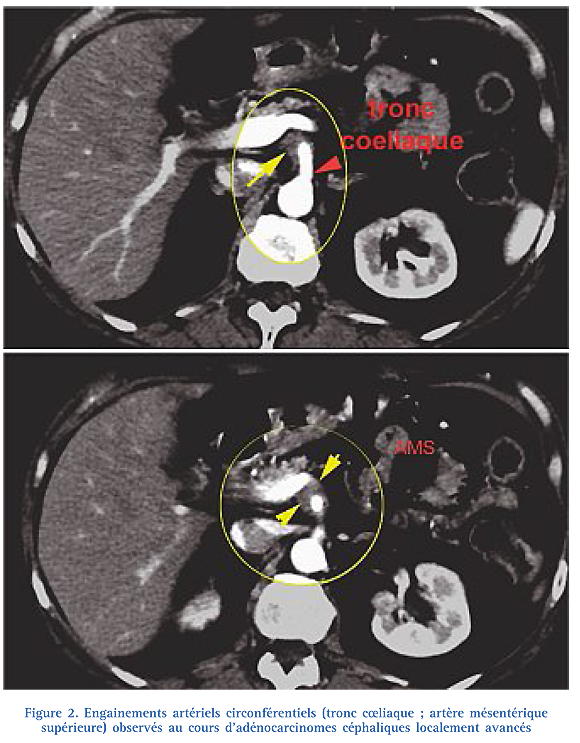
La disparition de l’espace graisseux périartériel (Fig. 1) traduit un « contact » de la tumeur avec l’axe artériel (« abutment » des auteurs anglo-saxons) et, à un stade plus avancé, un « engainement » plus ou moins étendu sur la circonférence et la longueur de l’axe vasculaire (Fig. 2) ;
- en cas de contact, ou d’engainement < 180°, la tumeur doit être considérée comme « à la limite de la résécabilité » (« borderline »), car même si la résection est techniquement réalisable, le risque d’une résection R1, voire R2, est très élevé ;
- en cas « d’engainement » de plus de 180°, la tumeur doit être considérée comme localement avancée et toute tentative de résection « primaire » (ie avant tout traitement médical) est contre-indiquée ; l’engainement circonférentiel n’entraîne pas obligatoirement une réduction du calibre artériel.
En résumé, l’atteinte artérielle est une contre-indication à la résection d’emblée.
Il est rare que ces anomalies périvasculaires soient isolées ou siègent à distance de la masse pancréatique ; dans ce cas, le diagnostic différentiel avec une pancréatite compliquée devient très difficile et repose sur les données de la ponction si une masse est visible, et sur l’aspect évolutif en imagerie dans le cas contraire [5].
Il existe un piège concernant l’engainement artériel, très spécifique de l’envahissement néoplasique : il perd sa valeur prédictive en cas de poussées de pancréatite aiguë. Certaines tumeurs intracanalaires papillaires et mucineuses (TIPMP) peuvent être associées à un « pseudo-engainement vasculaire » lié aux poussées de pancréatites ; cette densification de la graisse périartérielle, qui donne un aspect de pseudo-épaississement (« thickening ») de la paroi artérielle et qui peut être circonférentielle, ne doit pas faire récuser à tort une indication opératoire. Vuillerme et al. ont montré, dans une série récente évaluant 46 patients opérés de TIPMP dégénérées, que la valeur prédictive positive de la TDM pour la « non résécabilité » des TIPMP malignes, était seulement de 17 % [15].
Perméabilité et altérations « pariétales » de l’axe veineux
La perméabilité et les altérations « pariétales » de l’axe veineux peuvent modifier l’indication opératoire. L’analyse précise de la circonférence de l’axe veineux et de la longueur de l’atteinte vasculaire permet de classer l’extension vasculaire [42] (Fig. 3) : l’envahissement veineux s’effectue typiquement en trois phases : contiguïté, sténose puis occlusion. Une sténose localisée de l’axe veineux au contact de la tumeur est un signe d’envahissement plus spécifique que l’existence d’une simple contiguïté, même hémicirconférentielle. Il est rare que l’atteinte veineuse soit atypique dans les adénocarcinomes canalaires ; cependant, il peut s’agir d’un envahissement endoluminal en contact avec la tumeur, comme on l’observe dans certaines tumeurs endocrines du pancréas. Cet aspect est surtout visible au niveau de la confluence portale ; il ne doit pas remettre en cause le diagnostic d’adénocarcinome si le reste de la sémiologie TDM est en faveur de ce diagnostic [5].
- Les signes formels d’envahissement sont la sténose ou la thrombose veineuse (Fig. 4). Il s’agit alors de tumeurs localement avancées. La thrombose de l’axe veineux est habituellement associée à une atteinte de l’axe artériel. En cas de thrombose, les signes indirects d’envahissement veineux sont liés au développement d’une circulation collatérale et d’une hypertension portale segmentaire. Une dilatation de la veine gastroépiploïque et une circulation collatérale périgastrique peuvent traduire un envahissement de la veine splénique (cancers du pancréas gauche). Une dilatation des arcades pancréatiques et une circulation collatérale péripancréatique peuvent traduire un envahissement de la veine mésentérique supérieure (cancers céphaliques). Dans les formes très évoluées, un cavernome portal revascularise la veine porte sous-hilaire (Fig. 4).
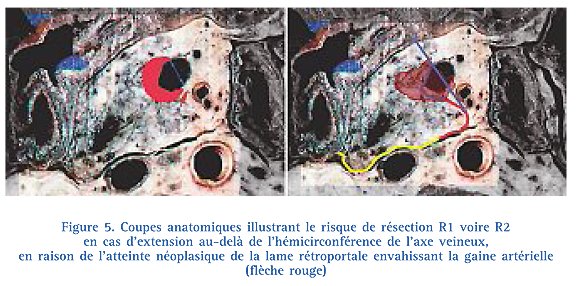
- Un engainement veineux de plus de 180° est un signe quasi formel d’envahissement, en l’absence de sténose [2, 3, 16-19] ; dans ces cas, la tumeur vient souvent au contact de l’artère mésentérique supérieure, la lame rétroportale est le plus souvent envahie et la marge de résection rétropéritonéale est positive (Fig. 5). Il s’agit alors de tumeurs « à la limite de la résécabilité » (synonymes dans la littérature, « potentiellement résécables », « borderline »).
- Par contre, l’existence isolée d’un contact inférieur à 180° entre la tumeur et l’axe veineux ne permet en aucun cas de prédire son envahissement avec une spécificité suffisante. Il ne s’agit pas d’une contreindication à la résection. D’ailleurs, 20 à 30 % des veines réséquées dans ce cas de figure ne présentent pas d’envahissement histologique mais seulement des lésions inflammatoires [2].
En résumé, l’existence d’un contact tumeur – axe veineux < 180° n’est pas une contre-indication à la résection. Au-delà, le risque d’une résection R1 voire R2 paraît prohibitif. Mieux vaut alors recourir à un traitement néoadjuvant qui sera suivi d’une réévaluation permettant parfois une résection « secondaire » (cf. infra) [16-19].
Dans certains centres spécialisés, une sténose très courte (< 2 cm) et peu serrée ne constitue pas une contreindication absolue à un geste d’exérèse, à condition que l’atteinte veineuse ne s’étende pas au niveau de la convergence des veines jéjunales (ce qui s’observe surtout dans les tumeurs du crochet pancréatique) [18]. Cependant, en cas d’envahissement veineux circonférentiel et a fortiori en présence d’un cavernome, la résection est habituellement contre-indiquée en raison des difficultés techniques (le cavernome rend l’abord du pancréas hémorragique), du fréquent envahissement de la lame rétroportale et/ou de la racine du mésentère empêchant la réalisation d’une exérèse R0 [2, 3, 20]. Dans l’étude d’Ishikawa et al. [21], aucun patient ayant une résection pancréatique avec un envahissement dépassant l’hémicirconférence de la veine porte ou 1,2 cm de longueur n’a survécu au-delà de 18 mois.
L’enquête multicentrique française, réalisée à l’occasion du 112e Congrès français de chirurgie, a montré sur une très large série de patients (435 résections veineuses chez 1 670 malades) que la TDM avait une valeur prédictive sur la survie et que les résections segmentaires étendues sur plus de 2 cm de longueur avaient un mauvais pronostic [20] :
- lorsque, sur la TDM, l’engainement veineux était supérieur à une simple encoche latérale, il n’y avait pas de survivant à 3 ans après résection ;
- en cas de résection veineuse segmentaire > 2 cm, la survie à 3 ans était divisée par 2 (20 % versus 43 %) et l’analyse multivariée des facteurs pronostiques montrait que le risque de décès était multiplié par 2,17 (HR : 2,17 ; IC :1,42-3,32) ;
- par contre, les résections R0 N0 avaient la même survie que les résections céphaliques sans résection veineuse.
Les contre-indications « vasculaires »
Pour les adénocarcinomes céphaliques
En cas d’envahissement artériel, une duodénopancréatectomie céphalique avec résection artérielle expose à une morbidité et une mortalité (atteignant plus de 30 %) postopératoires prohibitives pour la majorité des équipes expertes ; les résultats carcinologiques sont très décevants [20]. En revanche, un envahissement latéral de l’axe veineux n’est pas une contre-indication à l’exérèse, sous réserve de l’absence d’envahissement de la lame rétroportale au contact de l’artère mésentérique supérieure ou du tronc coeliaque [2, 3, 20].
Pour les adénocarcinomes du pancréas gauche
L’extension à l’artère mésentérique supérieure est une contre-indication à l’exérèse. En revanche, l’extension néoplasique aux vaisseaux spléniques n’est pas une contre-indication à la résection [2, 3]. Les envahissements du confluent veineux mésentéricoportal et du tronc coeliaque peuvent être techniquement accessibles à une résection dont l’intérêt carcinologique reste discuté [20, 22]. Chez quelques malades très sélectionnés (statut clinique, CA 199, au mieux réponse à un traitement néoadjuvant), et après un traitement « médical d’induction », la résection du tronc coeliaque et de l’artère hépatique propre peut être envisagée ; le foie est alors « revascularisé » par le flux « inversé » de l’artère gastro-duodénale.
Les critères préopératoires théoriques d’inextirpabilité sont résumés dans le Tableau II (voir aussi l’annexe).
Leur interprétation après un traitement néoadjuvant est difficile, surtout lorsque le traitement a comporté une irradiation. En dehors d’une réponse tumorale évidente, l’interprétation radiologique des engainements vasculaires est complexe, l’échoendoscopie n’est pas contributive et la valeur prédictive du PET-scan n’est pas évaluée ; c’est alors l’absence d’évolutivité de la maladie, le statut clinique et la diminution, ou mieux la normalisation du taux de CA 19-9, qui conduisent à une laparotomie exploratrice. En pratique, le problème majeur est celui de l’extension artérielle et ce sont les biopsies chirurgicales des gaines artérielles qui, lorsqu’elles sont négatives, permettent d’indiquer une résection [16, 17].
Techniques opératoires – Impact du bilan morphologique sur le choix de ces techniques
Objectif pédagogique
- Connaître les différentes techniques opératoires et l’impact du bilan morphologique sur le choix de ces techniques
Les recommandations qui concernent les techniques opératoires reposent sur des niveaux de preuve qui sont faibles [2, 3]. Cependant, lorsqu’une exérèse est indiquée, elle doit répondre à des impératifs que les recommandations récentes de la Société française de chirurgie digestive et l’Association de chirurgie hépatobiliaire et de transplantation hépatique ont publié sous le label de l’INCA et l’HAS [2, 3]. Nous envisagerons les techniques « conventionnelles » et les modifications techniques qui peuvent résulter du bilan morphologique préopératoire, le préalable indispensable à toute résection étant l’analyse des données de l’imagerie.
Adénocarcinomes céphaliques
La technique « conventionnelle »
Dans la majorité des cas, la tumeur est à distance des vaisseaux mésentériques et une duodénopancréatectomie céphalique pour cancer peut être R0 en respectant les points suivants [2, 3] (Fig. 6) :
- la section de la voie biliaire principale doit être réalisée le plus haut possible, sous le confluent biliaire supérieur et la dissection doit « squelettiser » l’artère hépatique et la veine porte pédiculaire dans le but de réséquer la totalité des ganglions lymphatiques de premier relais situés dans le pédicule hépatique ;
- la section pancréatique doit porter sur l’isthme et la tranche de section doit être confiée de façon systématique à un examen histologique extemporané ; en effet, il existe dans 10 à 20 % des cas des foyers néoplasiques (cancers infiltrants, néoplasies intraépithéliales ou tumeurs intracanalaires mucineuses et papillaires du pancréas – TIPMP méconnues) qui imposent une recoupe avec examen extemporané de la nouvelle tranche de section ;
- la dissection vasculaire doit comporter une dissection et une mobilisation circonférentielle de l’axe veineux mésentéricoportal et une mise à nu de l’hémicirconférence droite de l’artère mésentérique supérieure, ce qui permet l’exérèse complète de la « lame rétroportale » ou « pancréas rétrovasculaire ». En effet, la marge la plus importante sur le plan pronostique est la marge « postérieure » ou « rétropéritonéale », qui correspond au tissu pancréatique qui forme le lit de l’axe veineux puis qui vient au contact du tissu celluleux qui entoure le bord droit de l’artère mésentérique supérieure et s’étend jusqu’au plexus coeliaque droit (Fig. 1) [23] ;
- une lymphadénectomie « régionale » est recommandée ; elle doit emporter les ganglions péripancréatiques antérieurs et postérieurs, hépatiques propres et communs, pédiculaires hépatiques, et situés au bord droit du tronc coeliaque et de l’artère mésentérique supérieure : ce sont les relais ganglionnaires définis comme relais « N1 » par la classification TNM-UICC 2002 [24]. La lymphadénectomie « étendue » qui emporte tous les relais coeliaques, ceux situés au bord gauche de l’artère mésentérique supérieure, et les ganglions aortico-caves n’est pas recommandée ; elle augmente la morbidité postopératoire et n’améliore pas la survie (4 essais randomisés négatifs) [25, 28] ; – la conservation pylorique est une option (4 essais randomisés) [66, 69] car elle ne modifie ni la morbimortalité ni le pronostic carcinologique (le taux d’envahissement des ganglions péripyloriques est faible [15 à 25 %] et cet envahissement est très rarement isolé), mais une antrectomie est recommandée si la localisation de la tumeur à la partie haute de la tête expose à une résection R1 en cas de conservation pylorique.
Le bilan morphologique peut modifier la technique opératoire
- Le contrôle premier de l’artère mésentérique supérieure [2, 3], avant toute section digestive ou pancréatique, est recommandé (Fig. 7) :
- en cas de doute sur l’envahissement de la lame rétroportale, car il évite la constatation d’une exérèse palliative en fin de procédure ;
- en cas de résection veineuse « prévisible » sur la tomodensitométrie, et/ou en cas de « suspicion » macroscopique d’extension tumorale à la paroi veineuse, car il facilite la résection « monobloc » en « pédiculisant » la pièce de résection sur le segment veineux envahi (Fig. 7). En cas d’envahissement veineux, le risque que l’exérèse soit R1 est majoré en raison de la fréquence de l’extension néoplasique à la lame rétroportale, malgré l’élargissement de l’exérèse à l’axe veineux. L’abord premier de l’artère mésentérique supérieure permet d’ouvrir la gaine artérielle et de réaliser si besoin une biopsie avec examen histologique extemporané, ce qui pourrait diminuer le taux des exérèses palliatives.
- Une dissection « plus poussée » de la veine mésentérique supérieure doit être envisagée lorsqu’il existe une suspicion d’extension au mésocôlon droit. L’élargissement de l’exérèse aux organes adjacents au cours de la duodénopancréatectomie céphalique concerne essentiellement le côlon droit en raison de l’envahissement du mésocôlon ; dans ce cas, il existe un risque de résection R1 au niveau de la racine du mésentère et l’élargissement « monobloc » nécessite alors une dissection « plus poussée » de la veine mésentérique supérieure [2, 3].
En résumé, les modifications techniques sont liées aux élargissements recommandés. Il est recommandé d’élargir en monobloc la duodénopancréatectomie céphalique :
- à l’axe veineux mésentérico-porte, lorsque l’extension néoplasique est limitée à moins de son hémicirconférence droite car l’élargissement peut permettre une résection curative (R0), avec une mortalité et une morbidité postopératoires comparables et des survies prolongées (cf. ante) ;
- au mésocôlon et/ou au côlon droit, en cas d’envahissement du mésocôlon.
Pièce opératoire
La pièce opératoire doit être orientée par le chirurgien avec un repérage des limites de résection et d’un éventuel envahissement vasculaire, et un encrage des marges de résection, au minimum la lame rétroportale. Le taux des résections R1 varie considérablement dans la littérature selon qu’un examen histopathologique « standardisé » est réalisé ou non (15 à 80 % !) [23, 29] ; or le caractère curatif (R0) des résections chirurgicales des adénocarcinomes pancréatiques est le premier facteur pronostique et, en cas de résection R0, le statut ganglionnaire devient le premier facteur pronostique [20]. Nous n’envisagerons pas ici les facteurs pronostiques, mais l’examen histologique d’au moins 10 ganglions est nécessaire pour déterminer le stade de la maladie ; le ratio du nombre de ganglions envahis sur le nombre de ganglions examinés est considéré aujourd’hui comme un facteur pronostique majeur [30], ce que confirme les données du rapport de l’Association française de chirurgie 2010 [20].
Adénocarcinomes du pancréas gauche
Technique « conventionnelle »
La technique conventionnelle est une résection pancréatique gauche et splénique conduite de droite à gauche ; une spléno-pancréatectomie gauche pour cancer peut être R0 en respectant les points suivants [2, 3] :
- l’abord premier des vaisseaux spléniques sur l’axe médian et leur ligature proximale ;
- la section pancréatique isthmique doit se faire en regard du bord droit de l’axe veineux, à proximité de l’artère gastro-duodénale ; l’intérêt d’un examen histologique extemporanée de la tranche de section n’est pas évalué, d’autant plus que l’existence d’une tranche tumorale constitue une indication théorique à une totalisation de la pancréatectomie ;
- la dissection vasculaire, outre l’abord des vaisseaux spléniques, doit « squelettiser » l’artère hépatique et l’axe veineux mésentéricoportal et mettre à nu les bords gauches de l’artère mésentérique supérieure et du tronc coeliaque qui constituent les limites de la résection ;
- la dissection « centrifuge » dans le plan d’accolement du mésogastre postérieur, au contact du fascia périrénal gauche, ou au contact du rein ou de la surrénale si la tumeur semble infiltrer le fascia, doit permettre la résection du tissu cellulograisseux rétropancréatique ;
- une lymphadénectomie « régionale » est recommandée ; elle doit emporter les relais ganglionnaires péripancréatiques antérieurs et postérieurs, hépatiques communs, situés au bord gauche de l’artère mésentérique supérieure et du tronc coeliaque et ceux situés dans l’épiploon gastrosplénique : ce sont les relais ganglionnaires définis comme relais « N1 » par la classification TNM-UICC 2002 [24]. Une lymphadénectomie « étendue », emportant les relais ganglionnaires précédents, les relais coeliaques droits, ceux situés au bord droit de l’artère mésentérique supérieure, et les ganglions aortico-caves jusqu’à l’origine de l’artère mésentérique inférieure, ne semble pas utile [2, 3].
Le bilan morphologique peut modifier la technique opératoire
C’est le cas, comme à droite, lorsqu’il montre un envahissement vasculaire ou viscéral susceptible d’être réséqué… mais là aussi c’est une découverte opératoire qui peut obliger à modifier la technique opératoire. Les résections veineuses sont plus rares qu’à droite et les élargissements viscéraux sont plus fréquents.
- Les atteintes vasculaires pouvant faire l’objet d’une résection sont rares, qu’il s’agisse d’une extension veineuse au confluent splénomésaraïque ou d’une extension artérielle au tronc coeliaque (cf. ante) : elles peuvent faire discuter une exérèse chez un patient à faible risque opératoire, à la condition que ces résections vasculaires permettent une exérèse R0. À titre d’exemple, dans le Rapport de l’Association française de chirurgie 2010 [20], moins de 8 % des résections veineuses étaient réalisées au cours d’exérèses pancréatiques gauches (33/435 ; soit 12 % des 271 résections pancréatiques gauches colligées). Les résections artérielles concernent moins de 5 % des malades.
- En revanche, 30%des exérèses pour cancer pancréatique gauche sont élargies de nécessité à un ou plusieurs organes de voisinage (côlon gauche, estomac, angle duodénojéjunal, rein et surrénale gauches) [2, 3, 20]. Cet élargissement est justifié lorsqu’il permet une résection R0, car s’il majore la morbidité postopératoire, la mortalité n’est pas plus élevée qu’en cas d’exérèse non élargie. L’élargissement doit être réalisé en « monobloc » avec une marge suffisante (ce qui n’implique pas obligatoirement le sacrifice total de l’organe envahi : la « gastrectomie longitudinale » en est un bon exemple.
En résumé, les modifications techniques sont liées, comme pour les exérèses céphaliques, aux élargissements vasculaires ou viscéraux.
Pièce opératoire
Comme pour les exérèses céphaliques, le caractère curatif (R0) des résections et l’extension ganglionnaire sont les premiers facteurs pronostiques [20]. La préparation de la pièce opératoire doit suivre les mêmes règles ; la pièce doit être orientée par le chirurgien pour que les limites de la résection soient clairement identifiables. Comme pour la marge rétropéritonéale, les marges « latérales » (ou « circonférentielles ») doivent être encrées. En cas d’élargissement, la zone à étudier doit être repérée sur la pièce et il est souhaitable de prélever les groupes ganglionnaires « centraux » pour les distinguer de l’envahissement péritumoral.
Conclusions : les limites du raisonnable
La tomodensitométrie en mode spiralé multicoupe est aujourd’hui l’examen de référence pour le bilan morphologique qui permet de juger de la résécabilité d’un adénocarcinome pancréatique. En l’absence d’extension métastatique, ce sont les rapports vasculaires de la tumeur qui permettent de distinguer les cancers clairement résécables des formes avancées. Pour les cancers céphaliques, l’envahissement de l’artère mésentérique supérieure et/ou du tronc coeliaque et/ou de l’artère hépatique, est une contreindication à l’exérèse (au moins d’emblée) ; à gauche, l’envahissement de l’artère mésentérique supérieure est une contre-indication à l’exérèse alors que l’exérèse du tronc coeliaque peut être exceptionnellement indiquée ; par contre, les vaisseaux spléniques sont emportés par l’exérèse conventionnelle. L’envahissement veineux mésentérico-portal est une contre indication « relative » : en effet, lorsque l’extension ne dépasse pas l’hémicirconférence de l’axe et que les convergences veineuses mésentériques sont « libres », une exérèse R0 peut offrir des chances de survie prolongée ; les exérèses veineuses sont schématiquement beaucoup plus fréquentes au cours des exérèses céphaliques. Les élargissements viscéraux au cours des exérèses pancréatiques peuvent être justifiés s’ils permettent une résection R0 ; à droite, ils concernent le mésocôlon ou le côlon droit, mais à gauche les exérèses viscérales sont plus fréquentes.
Références
- Cancer du pancréas (Thésaurus National de Cancérologie Digestive) http://www.snfge.asso.fr/01-Bibliotheque/0D-Pratiques-cliniques/referentiels.asp
- Recommandations de pratiques chirurgicales 2009 – (SFCD / ACHBT labellisées INCa-HAS) Pancréas : A Sauvanet, JR Delpero. http://www. snfge.asso.fr/01-Bibliotheque/0D-Pratiques- cliniques/Reco_hors_HAS/ recos_chir_sfcd_long.pdf
- Slim K. Cancérologie digestive : pratiques chirurgicales. J Chir 2009;146 (Suppl. 2):S11-S80.
- Delpero JR. Quand ne pas biopsier une masse solide du pancréas ? Association nationale française de formation continue en hépato-gastroentérologie. In : Post’U. Springer Éd., 104-12 http://www.snfge.asso.fr/01-Bibliotheque/0B-ConferencesFlash/2009/267/indexConf.asp
- Zins M. Adénocarcinome pancréatique : bilan d’extension. Traité de pancréatologie clinique, Levy P, Ruszniewski P, Sauvanet A. Flammarion Medecine-Sciences, Paris, 2005. 168-77.
- Hidalgo M. Pancreatic Cancer. N Engl J Med 2010;362:1605-17.
- Bipat S, Phoa S, van Delden O, et al. Ultrasonography, Computed Tomography and Magnetic Resonance Imaging for Diagnosis and determining Resectability of Pancreatic Adenocarcinoma: a Metaanalysis. J Comput Assist Tomogr 2005;29: 438-45.
- Michl P, Pauls S, Gress TM. Evidence based diagnosis and staging of pancreatic cancer. Best Pract Res Clin Gastroenterol 2006;20:227-51.
- Puli SR, Singh S, Hagedorn CH, Reddy J, Olyaee M. Diagnostic accuracy of EUS for vascular invasion in pancreatic and periampullary cancers: a metaanalysis and systematic review. Gastrointest Endosc 2007;65:788-97.
- Dewitt J, Devereaux BM, Lehman GA, et al. Comparison of endoscopic ultrasound and computed tomography for the preoperative evaluation of pancreatic cancer: a systematic review. Clin Gastroenterol Hepatol 2006;4:717-25.
- Hirokawa Y, Isoda H, Okada T, Arizono S, Shimada K, Yamamoto A, et al. Improved detection of hepatic metastases from pancreatic cancer using periodically rotated overlapping parallel lines with enhanced reconstruction (PROPELLER) technique after SPIO administration. Invest Radiol 2010;45:158-64.
- Wakabayashi H, Nishiyama Y, Otani T, et al. Role of 18F-fluorodeoxyglucose positron emission tomography imaging in surgery for pancreatic cancer. World J Gastroenterol 2008;14:64-9.
- Maire F, Sauvanet A, Trivin F, et al. Staging of pancreatic head adenocarcinoma with spiral CT and endoscopic ultrasonography: an indirect evaluation of the usefulness of laparoscopy. Pancreatology 2004;4:436-40.
- Pancreatic Section of the British Society of Gastroenterology, Pancreatic Society of Great Britain and Ireland, Association of Upper Gastrointestinal Surgeons of Great Britain and Ireland, Royal College of Pathologists, Special Interest Group for Gastro- Intestinal Radiology. Guidelines for the management of patients with pancreatic cancer periampullary and ampullary carcinomas. Gut 2005;54:v1-v16.
- Vullierme MP, Giraud-Cohen M, Hammel P, et al. Malignant intraductal papillary mucinous neoplasm of the pancreas: in situ versus invasive carcinoma surgical resectability. Radiology 2007;245:483-90.
- Sa Cunha A, Rault A, Laurent C, et al. Surgical resection after radiochemotherapy in patients with unresectable adenocarcinoma of the pancreas. J Am Coll Surg 2005;201:359-65.
- Turrini O, Viret F, Moureau-Zabotto L, Guiramand J, et al. Neoadjuvant chemoradiation and pancreaticoduodenectomy for initially locally advanced head pancreatic adenocarcinoma. Eur J Surg Oncol 2009;35:1306-11.
- Evans DB, Farnell MB, Lillemoe KD, Vollmer C Jr, Strasberg SM, Schulick RD. Surgical Treatment of Resectable and Borderline Resectable Pancreas Cancer: Expert Consensus Statement. Ann Surg Oncol 2009;16:1736-44.
- Chun YS, Milestone BN, Watson JC, Cohen SJ, et al. Defining venous involvement in borderline resectable pancreatic cancer. Ann Surg Oncol 2010;17:2832-8.
- Delpero JR, Paye F, Bachellier P. Cancer du Pancréas. Monographies de l’association Française de Chirurgie. Arnette, Wolters Kluwer France, 2010.
- Ishikawa O, Ohigashi H, Imaoka S, et al. Preoperative indications for extended pancreatectomy for locally advanced pancreas cancer involving the portal vein. Ann Surg 1992;215:231-6.
- Hirano S, Kondo S, Hara T, et al. Distal pancreatectomy with en bloc celiac axis resection for locally advanced pancreatic body cancer: long-term results. Ann Surg 2007;246:46-51.
- Delpero JR, Turrini O. Adénocarcinomes pancréatiques céphaliques : une étude critique du taux des marges de résection positives. Bull Cancer 2008;95:1193-8.
- AJCC Cancer Staging Manual, Sixth Edition, Exocrine pancreas, 2002: 157-64.
- Pedrazzoli S, Di Carlo V, Dionigi R, et al. Standard versus extended lymphadenectomy associated with pancreaticoduodenectomy in the surgical treatment of adenocarcinoma of the head of pancreas. A multicenter, prospective, randomized study. Ann Surg 1998;228:508-17.
- Nimura Y, Nagino M, Kato H, et al. Regional versus extended lymph node dissection in radical pancreatoduodenectomy for pancreatic cancer. A multicenter, randomized controlled trial (abstract). J Intern HPB Ass 2004;6 (Suppl I):2.
- Farnell MB, Pearson RK, Sarr MG, et al. A prospective randomized trial comparing standard pancreatoduodenectomy with pancreatoduodenectomy with extended lymphadenectomy in resectable pancreatic head adenocarcinoma. Surgery 2005;138:628-30.
- Riall TS, Cameron JL, Lillemoe KD, et al. Pancreaticoduodenectomy with or without distal gastrectomy and extended retroperitoneal lymphadenectomy for periampullary adenocarcinoma—part 3: update on 5-year survival. J Gastrointest Surg 2005;9:1191-1204.
- Chang DK, Johns AL, Merrett ND, et al. Margin Clearance and Outcome in Resected Pancreatic Cancer. J Clin Oncol 2009;27:2855-62.
- Bhatti I, Peacock O, Awan AK, Semeraro D, Larvin M, Hall RI. Lymph Node Ratio versus Number of Affected Lymph Nodes as Predictors of Survival f o r R e s e c t e d Pa n c r e a t i c Adenocarcinoma. World J Surg 2010;34:768-75.
Les 5 points forts
- Le but du bilan morphologique est de limiter les indications de chirurgie exploratrice ou palliative.
- La TDM spiralée en coupes fines (2 ou 3 mm) avec acquisition à la phase artérielle puis portale est l’examen de référence pour apprécier la résécabilité des ADKP.
- L’échoendoscopie ne doit plus être systématique dans le bilan de résécabilité.
- L’envahissement veineux n’est pas toujours une contre-indication à la résection (< 180°) ; l’envahissement artériel reste une contre-indication, tout au moins à une résection primaire.
- La réévaluation par imagerie de l’engainement artériel après traitement néoadjuvant par radiochimiothérapie est difficile.
FMC HGE : Organisme certifié Qualiopi pour la catégorie ACTIONS DE FORMATION
FMC HGE : Organisme certifié Qualiopi pour la catégorie ACTIONS DE FORMATION